基于同时封装靶物质并合成具有氧化还原活性MOFs的制法的制作方法
本发明属于合成技术领域,具体涉及一种基于同时封装靶物质并合成具有氧化还原活性MOFs的制法。
背景技术:
金属有机框架材料(MOFs)是一类由金属离子(簇)与有机桥联配体连接而成的具有纳米孔穴的超分子晶体材料。有着很多优异特点:比表面积超大,孔径和拓扑结构可以调控,热稳定性、化学稳定性很好,因此,金属有机框架材料比其他材料有着广阔的发展前景。可以调控的孔径以及拓扑结构使得金属有机框架材料在生物、化学传感方面有着广阔的应用前景,此外,人们已经研究了金属有机框架材料在催化剂、气体储存、吸附与分离、药物缓释等诸多方面的应用。
因为电化学传感技术具有灵敏度高、环境友好、检测快速、易于操作等特点,因而使用范围十分广阔。利用MOFs材料构建电化学传感可进一步改善电化学传感器的检测灵敏度和特异性,提高其分析的精确性。
目标识别是传感器的要素之一,MOFs材料在传感方面具有天然优势。MOFs材料的拓扑结构、节点金属离子的选择、连接体有机配体的尺寸和形状以及框架的组成方式等因素都会影响MOFs的孔结构和孔尺寸。利用孔的结构和尺寸对所需的物质进行定性选择,是MOFs的一个十分重要的性能,也是把MOFs材料应用到传感领域的一个最吸引人的特点。尺寸小于MOFs孔结构的原子或分子才可以被吸附进孔中进行检测,而孔内的结构和基团可与目标物存在相互作用(如静电相互作用、氢键、π-π、共价键等),从而进一步提高选择性。根据前文所提到的MOFs材料独特的孔结构和大的比表面积,鉴于这些特点,所以MOFs可以高效吸附富集目标物,从而提高检测灵敏度。
虽然大部分MOFs材料不具有电传导能力,但其独特的孔结构和化学可调节性使得MOFs材料在电化学传感领域有着非常广阔的应用前景。通过改变有机配体、金属离子或直接向金属有机框架材料中导入氧化还原活性的物质制备新型的具有氧化还原活性及良好电传导能力的孔结构稳定的MOFs材料,并通过物理沉积、自组装、电解沉积等方法构建MOFs薄膜电化学传感界面及传感器件。研究具有氧化还原活性及良好电传导能力的MOFs材料传感界面的构造、孔结构、界面上生物分子识别、富集以及电化学信号转换等科学问题,使得电化学传感器的选择性提高,检测限降低,检测范围变宽;利用其生物相容性,构筑对底物具有生物识别性和生物酶催化功能的生物界面,研究生物传感器中所涉及的生物分子在界面上的电子氧化还原转移基本行为。
但是,现有的方法一般是通过浸渍的方式向金属有机框架中导入氧化还原活性物质,需要先合成MOFs,再将靶物质溶解在有机溶剂中通过共价键将靶物质修饰在MOFs上。此方法的弊端如下:1、实验过程复杂且成本高,并且产生大量废弃物;2、此方法中MOFs的孔尺寸较小且是固定的,难以封装大分子的靶物质,使得靶物质聚集在MOFs材料的表面,降低了靶物质的负载量;3、MOFs材料中靶物质的负载电力能力降低。
技术实现要素:
本发明的一个目的是为了克服现有技术中的MOFs材料不具有电传导能力的缺陷,提供一种基于同时封装靶物质并合成具有氧化还原活性MOFs的制法。
本发明的另一个目的是提供上述制法制备得到的金属有机框架复合材料,该金属有机框架为靶分子修饰的ZIF-8,具有电传导的特性,解决了现有技术中的金属有机框架不具有电传导能力的弊端。
本发明的第三个目的是提供一种修饰电极,该修饰电极为上述MOFs材料修饰的电极,该修饰电极可以对多巴胺进行准确、灵敏地检测,具有更好的检测灵敏度和准确性。
本发明的第四个目的是提供一种三电极体系。
本发明的第五个目的是提供上述修饰电极在检测多巴胺中的应用。
为了解决以上技术问题,本发明的技术方案为:
基于同时封装靶物质并合成具有氧化还原活性MOFs的制法,包括如下步骤:
在硝酸锌水溶液中加入靶物质和2-甲基咪唑水溶液,进行反应,得到的沉淀物即为目标产物。
发明人经过研究发现,虽然大部分MOFs材料不具有电传导能力,但其独特的孔结构和化学可调节性使得MOFs材料在电化学传感领域有着非常广阔的应用前景,通过直接导入氧化还原活性的物质制备新型的具有氧化还原活性及良好电传导能力的孔结构稳定的MOFs材料,从而制备出高效的电化学传感器。亚甲基兰、甲基橙或金属纳米颗粒是电活性物质,通过一锅法制备了亚甲基兰、甲基橙或金属纳米颗粒修饰的ZIF-8,亚甲基兰、甲基橙或金属纳米颗粒增大了ZIF-8的孔结构,从而提供了一个快递的电子转移渠道,使MOFs具有很好的电催化活性和电传导性能,目标物可通过MOFs孔道扩散与嵌入其中的金属颗粒接触,然后发生相互作用,产生信号变化,保证MOFs独特的性能结构的同时赋予其电化学活性。
本发明制备得到的金属有机框架复合材料对于目标物的氧化还原反应具有更好的电催化能力。MOFs电子传导率低,电催化能力差,而将具有电催化活性的靶物质封装到MOFs中形成复合材料,增大了MOFs的孔结构,从而提供了一个快速转移电子的渠道,提高了MOFs复合材料的电传导能力和电催化活性。
优选的,所述靶物质为亚甲基兰、甲基橙或金属纳米颗粒。
优选的,在硝酸锌水溶液中加入亚甲基兰溶液中,混合均匀后再加入2-甲基咪唑。
优选的,所述的硝酸锌与2-甲基咪唑的摩尔比为1:30-40。
优选的,所述硝酸锌水溶液的浓度为0.2-0.3g/ml。
优选的,所述2-甲基咪唑的浓度为0.1-0.3g/ml。
优选的,反应的温度为20-30℃,反应的时间为10-20min。进一步优选为,反应的温度为25℃,反应的时间为10-20min。
优选的,对所述沉淀物洗涤后,在75-85℃下真空干燥,干燥的时间为10-14h。
在80℃左右下真空干燥,不会破坏ZIF-8骨架的结构,还会提高干燥效率,节省干燥时间。
进一步优选的,对沉淀物进行洗涤使用的洗涤液为水和乙醇的混合溶液。本发明中使用乙醇和水作为有机溶剂,选择水和乙醇的混合溶液作为洗涤液,保证不引入其他杂质。
更进一步优选的,所述洗涤液中,水和乙醇的体积比为1:0.8-1.2。
上述制法制备得到的金属有机框架复合材料,包括金属有机框架ZIF-8和封装在金属有机框架内部的靶物质,所述靶物质为亚甲基兰、甲基橙或金属纳米颗粒。靶物质具有氧化还原活性和电传导能力。
基于同时封装靶物质并合成具有氧化还原活性MOFs的制法,有如下优点:1、此实验过程快速简便,易操作。2、靶物质有效地被包裹在MOFs中,从而可以控制MOFs的孔尺寸,增大MOFs的孔尺寸。3、此方法制得的MOFs材料电传导能力显著增强。
ZIF-8骨架结构由金属Zn离子与甲基咪唑酯中的N原子相连形成的ZnN4四面体结构单元构成,拓扑结构与方钠石(sodalite,SOD)类似,每个单元晶胞包含2个SOD笼,SOD笼直径为1.16nm,每个SOD笼通过6个Zn原子组成的六元环笼口相连,六元环笼口直径为0.34nm。
一种由上述金属有机框架复合材料修饰的修饰电极。
一种三电极系统,包括电化学工作站和与其连接的辅助电极、工作电极和参比电极,其中,所述工作电极为上述修饰电极。
上述修饰电极的制备方法,包括如下步骤:
将上述金属有机框架分散到水中形成分散液,然后将分散液滴加到电极表面,干燥后得到亚甲基蓝@MOFs修饰电极。
优选的,所述分散液中金属有机框架的浓度为0.8-1.2mg/ml。
上述修饰电极在检测多巴胺、槲皮素、芦丁中的应用。
本发明的有益效果为:
选用亚甲基兰、甲基橙以及金属纳米颗粒作为靶物质,通过一锅法在合成MOFs的同时将靶物质封装在内,得到亚甲基兰、甲基橙或金属纳米颗粒修饰的ZIF-8,克服现有的MOFs材料不具有电传导能力的缺陷。
本发明的合成方法简单、快速、成本低,制备产物可对多巴胺、槲皮素、芦丁等物质进行准确、灵敏、简便、快捷的探测,为生物检测、化学分析等领域的研究提供了一种新的发展方向。
附图说明
图1为实施例中基于同时封装靶分子并合成具有氧化还原活性MOFs的一锅法制法的过程示意图;
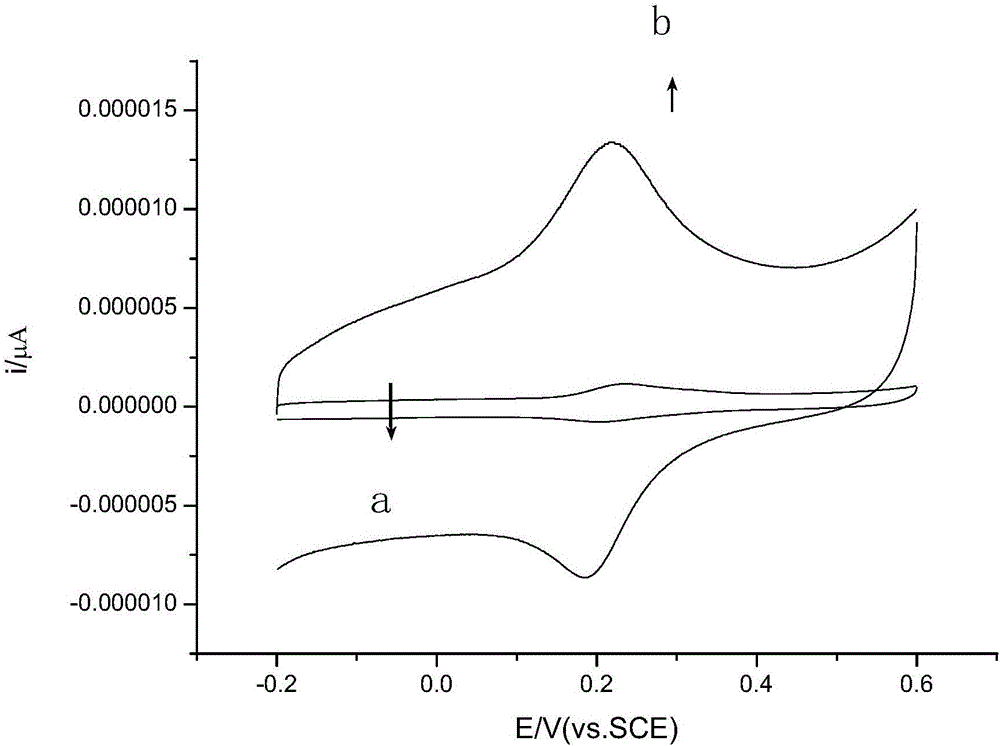
图2为实施例1中,多巴胺在裸电极和在亚甲基蓝修饰的MOFs修饰电极上响应的CV曲线对比图,其中,a为裸电极,b为亚甲基蓝修饰的MOFs修饰电极;
图3为实施例1中,多巴胺在不同pH值中的响应循环伏安曲线,a为pH=7,b为pH=8,c为pH=6,d为pH=5;
图4为实施例1中,多巴胺在不同的扫描速度下的循环伏安曲线,沿箭头方向从下到上依次为a-y,a-y依次表示多巴胺在扫速为10mv,20mv,30mv,40mv,50mv,60mv,70mv,80mv,90mv,100mv,110mv,120mv,130mv,140mv,150mv,160mv,170mv,180mv,190mv,200mv,210mv,220mv,230mv,240mv,250mv的CV曲线;
图5为实施例1中,亚甲基蓝修饰的ZIF-8修饰电极在不同浓度的DA溶液中循环伏安曲线,沿箭头方向,从下往上为a-j,a-j代表的DA溶液浓度依次为1×10-8mol/L,1×10-7mol/L,5×10-7mol/L,1×10-6mol/L,5×10-6mol/L,1×10-5mol/L,5×10-5mol/L,1×10-4mol/L,1×10-3mol/L。
具体实施方式
下面结合附图和具体实施例对本发明进行详细说明。
下面各试验中用到的物质和设备来源如下:
Zn(NO3)2·6H2O,分析纯,购自阿拉丁;
亚甲基蓝,分析纯,购自阿拉丁;
甲基橙,分析纯,购自阿拉丁;
槲皮素,分析纯,购自阿拉丁;
铜纳米颗粒,购自阿拉丁;
芦丁,分析纯,购自阿拉丁;
2-甲基咪唑分析纯,购自阿拉丁;
多巴胺,分析纯,购自阿拉丁;
磷酸盐,分析纯,购自国药集团化学试剂有限公司;
二次蒸馏水,自制。
磁力搅拌器,型号78-1),购自丹瑞仪器;
真空干燥箱,型号EB-71L,购自上海辰华仪器有限公司;
电化学工作站型号CHI650,购自上海辰华仪器有限公司。
实施例1
基于同时封装靶分子并合成具有氧化还原活性MOFs的一锅法制法的过程参见图1,详细的制备步骤如下:首先,将0.2g(0.66mmol)的Zn(NO3)2·6H2O溶解在0.8g(800μl)的二次水水中。用去离子水配制10mg/ml的亚甲基蓝的溶液,然后,将4ml的亚甲基兰原液滴加到Zn(NO3)2水溶液中,均匀用力搅拌一分钟后,将含有2g(24.36mmol)2-甲基咪唑和8g二次水的10g溶液滴加到上述溶液中。将反应混合物放在磁力搅拌器上搅拌15分钟。通过离心分离收集沉淀物并且用水和乙醇(1:1)的混合溶液至少洗涤三次后,放在真空干燥箱80℃下干燥12小时。
制备Nafion/亚甲基蓝@MOFs/GCE:将亚甲基蓝@MOFs溶解到二次水中形成 1mg/ml的分散溶液,在超声波清洗器中超声2h,得到分散良好的亚甲基蓝@MOFs溶液。取6μl上述亚甲基蓝@MOFs分散液滴加到电极表面,干燥,得到亚甲基蓝@MOFs修饰电极(亚甲基蓝@MOFs/GCE)。用亚甲基蓝@MOFs/GCE和裸GCE分别对多巴胺进行CV检测,多巴胺在裸电极(曲线a)和在亚甲基蓝修饰的MOFs修饰电极(曲线b)上的CV图,通过观察CV扫描图,可以得到亚甲基蓝修饰的MOFs的修饰电极的检测灵敏度和准确性均比裸电极好,参见图2。
组装三电极体系,将辅助电极、参比电极和工作电极与电化学工作站连接,工作电极为上面制备得到的亚甲基蓝@MOFs/GCE。此处的参比电极可以为饱和甘汞电极、Ag/AgCl电极或标准氢电极(SHE或NHE)。辅助电极为铂黑电极或在介质中保持惰性的金属材料,如Ag、Ni、W、Pb等。
下面试验中的三电极体系的辅助电极为铂黑电极,参比电极为饱和甘汞电极。
分别配置pH=5,6,7,8的PBS缓冲溶液,随后将确定质量(0.0019g)的多巴胺溶解在不同pH的PBS溶液(本文中的PBS溶液均为磷酸盐缓冲液)中,随后转移到100ml容量瓶中定容。把三电极体系插在不同pH的PBS缓冲溶液中,以200mv/s的速度扫描,将扫描电压区间设置为-0.2-0.6V的条件下,通过观察扫描图可以得知,在pH为5-6时,得到的伏安循环图形状数据最好,参见图3,图中,a为pH=7,b为pH=8,c为pH=6,d为pH=5。
分别配置pH为5.68的PBS缓冲溶液,随后将确定质量(0.0019g)的多巴胺溶解在PBS中,随后转移到100ml容量瓶中定容。把三电极系统插在PBS缓冲溶液中,以不同的扫描速度扫描,将扫描电压区间设置为-0.2-0.6V的条件下,通过观察上图可以得知,在扫描速度为200mv/s时,得到的伏安循环图形状数据最好,参见图4,图中,按箭头方向的扫描电压依次为10mv,20mv,30mv,40mv,50mv,60mv,70mv,80mv,90mv,100mv,110mv,120mv,130mv,140mv,150mv,160mv,170mv,180mv,190mv,200mv,210mv,220mv,230mv,240mv,250mv。
配置pH为5.68的PBS溶液,称取1×10-4mol的DA(多巴胺)用PBS溶解,随后转移到100ml容量瓶中,配置成1×10-3mol/L的溶液,随后从其中取25ml,再用PBS稀释到100ml容量瓶中,配置成5×10-4mol/L的溶液。按照上述方法,依次配置1×10-3mol/L,1×10-4mol/L,5×10-5mol/L,1×10-5mol/L,5×10-6mol/L,1×10-6mol/L,5×10-7mol/L,1×10-7mol/L,1×10-8mol/L的DA溶液,设置扫描速度为200mv/s,扫描电压区间-0.2-0.6v然后分别测试其伏安曲线,参见图5,图中,伏安曲线从上往下依次对应的DA溶液浓度为5×10-4mol/L,1×10-4mol/L,1×10-3mol/L,5×10-5mol/L,1×10-5mol/L,5×10-6mol/L,1×10-6mol/L,5×10-7mol/L,1×10-7mol/L,1×10-8mol/L。由图5可以看出,随着浓度的增大,响应电流依次增大。
实施例2
基于同时封装靶分子并合成具有氧化还原活性MOFs的一锅法制法的过程参见图1,详细的制备步骤如下:首先,将0.2g(0.66mmol)的Zn(NO3)2·6H2O溶解在0.8g(800μl)的二次水水中。用去离子水配制10mg/ml的甲基橙溶液,然后,将4ml的甲基橙原液滴加到Zn(NO3)2水溶液中,均匀用力搅拌一分钟后,将含有2g(24.36mmol)2-甲基咪唑和8g二次水的10g溶液滴加到上述溶液中。将反应混合物放在磁力搅拌器上搅拌15分钟。通过离心分离收集沉淀物并且用水和乙醇(1:1)的混合溶液至少洗涤三次后,放在真空干燥箱80℃下干燥12小时。
制备Nafion/甲基橙@MOFs/GCE:将甲基橙@MOFs溶解到二次水中形成 1mg/ml的分散溶液,在超声波清洗器中超声2h,得到分散良好的甲基橙@MOFs溶液。取6μl上述甲基橙@MOFs分散液滴加到电极表面,干燥,得到甲基橙@MOFs修饰电极(甲基橙@MOFs/GCE)。
甲基橙@MOFs修饰电极,可以用于检测槲皮素。
组装三电极体系,将辅助电极、参比电极和工作电极与电化学工作站连接,工作电极为上面制备得到的甲基橙@MOFs/GCE。此处的参比电极可以为饱和甘汞电极、Ag/AgCl电极或标准氢电极(SHE或NHE)。辅助电极为铂黑电极或在介质中保持惰性的金属材料,如Ag、Ni、W、Pb等。
下面试验中的三电极体系的辅助电极为铂黑电极,参比电极为饱和甘汞电极。
分别配置pH=5,6,7,8的PBS缓冲溶液,随后将确定质量(0.0038g)的槲皮素溶解在不同pH的PBS溶液(本文中的PBS溶液均为磷酸盐缓冲液)中,随后转移到100ml容量瓶中定容。把三电极体系插在不同pH的PBS缓冲溶液中,以200mv/s的速度扫描,将扫描电压区间设置为-0.2-0.6V的条件下,通过观察扫描图可以得知,在pH为5时,得到的伏安循环图形状数据最好。
分别配置pH为5的PBS缓冲溶液,随后将确定质量(0.0038g)的槲皮素溶解在PBS中,随后转移到100ml容量瓶中定容。把三电极系统插在PBS缓冲溶液中,以不同的扫描速度扫描,将扫描电压区间设置为-0.2-0.6V的条件下,扫描速度为200mv/s时,得到的伏安循环图形状数据最好。
配置pH为5的PBS溶液,称取1×10-4mol的槲皮素用PBS溶解,随后转移到100ml容量瓶中,配置成1×10-3mol/L的溶液,随后从其中取25ml,再用PBS稀释到100ml容量瓶中,配置成5×10-4mol/L的溶液。按照上述方法,依次配置1×10-3mol/L,1×10-4mol/L,5×10-5mol/L,1×10-5mol/L,5×10-6mol/L,1×10-6mol/L,5×10-7mol/L,1×10-7mol/L,1×10-8mol/L的DA溶液,设置扫描速度为200mv/s,扫描电压区间-0.2-0.6v然后分别测试其伏安曲线。
实施例3
基于同时封装靶分子并合成具有氧化还原活性MOFs的一锅法制法的过程参见图1,详细的制备步骤如下:首先,将0.2g(0.66mmol)的Zn(NO3)2·6H2O溶解在0.8g(800μl)的二次水水中。用去离子水配制10mg/ml的铜纳米颗粒悬浮液,然后,将4ml的金属纳米颗粒悬浮液滴加到Zn(NO3)2水溶液中,均匀用力搅拌一分钟后,将含有2g(24.36mmol)2-甲基咪唑和8g二次水的10g溶液滴加到上述溶液中。将反应混合物放在磁力搅拌器上搅拌15分钟。通过离心分离收集沉淀物并且用水和乙醇(1:1)的混合溶液至少洗涤三次后,放在真空干燥箱80℃下干燥12小时。
制备Nafion/金属纳米颗粒@MOFs/GCE:将金属纳米颗粒@MOFs溶解到二次水中形成1mg/ml的分散溶液,在超声波清洗器中超声2h,得到分散良好的金属纳米颗粒@MOFs溶液。取6μl上述金属纳米颗粒@MOFs分散液滴加到电极表面,干燥,得到金属纳米颗粒@MOFs修饰电极(金属纳米颗粒@MOFs/GCE)。
金属纳米颗粒@MOFs修饰电极,可以用于检测芦丁。
组装三电极体系,将辅助电极、参比电极和工作电极与电化学工作站连接,工作电极为上面制备得到的金属纳米颗粒@MOFs/GCE。此处的参比电极可以为饱和甘汞电极、Ag/AgCl电极或标准氢电极(SHE或NHE)。辅助电极为铂黑电极或在介质中保持惰性的金属材料,如Ag、Ni、W、Pb等。
下面试验中的三电极体系的辅助电极为铂黑电极,参比电极为饱和甘汞电极。
分别配置pH=6,7,8,9的PBS缓冲溶液,随后将确定质量(0.0075g)的芦丁溶解在不同pH的PBS溶液(本文中的PBS溶液均为磷酸盐缓冲液)中,随后转移到100ml容量瓶中定容。把三电极体系插在不同pH的PBS缓冲溶液中,以200mv/s的速度扫描,将扫描电压区间设置为-0.2-0.6V的条件下,在pH为8时,得到的伏安循环图形状数据最好。
分别配置pH为8的PBS缓冲溶液,随后将确定质量(0.0075g)的芦丁溶解在PBS中,随后转移到100ml容量瓶中定容。把三电极系统插在PBS缓冲溶液中,以不同的扫描速度扫描,将扫描电压区间设置为-0.2-0.6V的条件下,在扫描速度为200mv/s时,得到的伏安循环图形状数据最好。
配置pH为8的PBS溶液,称取1×10-4mol的芦丁用PBS溶解,随后转移到100ml容量瓶中,配置成1×10-3mol/L的溶液,随后从其中取25ml,再用PBS稀释到100ml容量瓶中,配置成5×10-4mol/L的溶液。按照上述方法,依次配置1×10-3mol/L,1×10-4mol/L,5×10-5mol/L,1×10-5mol/L,5×10-6mol/L,1×10-6mol/L,5×10-7mol/L,1×10-7mol/L,1×10-8mol/L的DA溶液,设置扫描速度为200mv/s,扫描电压区间-0.2-0.6v然后分别测试其伏安曲线。
上述虽然结合附图对本发明的具体实施方式进行了描述,但并非对发明保护范围的限制,所属领域技术人员应该明白,在本发明的技术方案的基础上,本领域技术人员不需要付出创造性劳动即可做出的各种修改或变形仍在本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!