定量检测CCL17基因表达的引物和探针及其应用的制作方法
本发明涉及生物技术领域,尤其涉及一种定量检测CCL17基因表达的引物和探针及其应用。
背景技术:
rCCL17【chemokine(C-C motif)ligand 17】基因是位于16号染色体q臂的Cys-Cys(CC)基因簇中的一种。CC细胞因子的特点是两个毗邻的半胱氨酸,可以分泌蛋白参与免疫调节和炎性过程。该基因编码的趋化因子对T淋巴细胞有趋化作用,而非单核细胞或粒细胞。该基因的产物的受体是CCR4和CCR8,这一趋化因子对T细胞在胸腺的发育、成熟T细胞的活化有重要作用。
已发现恶性霍奇金淋巴瘤的特征性细胞高表达CCL17,且分泌到血清中。CCL17与恶性细胞、调节性T细胞和Th2细胞表达的趋化因子受体CCR4相结合。高CCL17水平与免疫调节细胞因子和趋化因子共同作用于炎性的霍奇金淋巴瘤微环境,促进肿瘤的发生、维持和进展。血清CCL17水平可预测霍奇金淋巴瘤的治疗结局;CCL17水平与经典霍奇金淋巴瘤的肿瘤负荷有关,而且治疗后的CCL17的变化与患者的治疗反应相关。欧洲霍奇金研究组的大型霍奇金淋巴瘤临床试验研究发现治疗前CCL17(TARC)水平与已有的临床危险因素有关,而且可以预测治疗反应。此外,CCL17(TARC)水平也参与了一个新的预测治疗反应的多变量模型。这些数据显示该趋化因子可作为霍奇金淋巴瘤的生物标记物。该研究中血清CCL17的水平采用双抗夹心ELISA(R&D systems)。这些结果显示,血清CCL17可作为经典霍奇金淋巴瘤的生物标记物。
此外,血清CCL17水平升高也与进展性黑色素瘤患者树突状细胞免疫治疗后的无进展生存期相关。也有报道,CCL17与过敏性皮炎,哮喘、荨麻疹,系统性红斑狼疮等过敏及免疫性疾病相关。
技术实现要素:
本发明的一个目的是提供一种试剂盒。
本发明提供的试剂盒,包括DNA分子甲,所述DNA分子甲由引物对甲和探针甲组成;
所述引物对甲由序列表中序列1所示的单链DNA分子和序列2所示的单链DNA分子组成;
所述探针甲为序列表中序列3所示的单链DNA分子。
上述试剂盒的功能为如下1)-3)中任一种:
1)辅助诊断肿瘤患者;
2)辅助鉴定肿瘤细胞系;
3)定量检测CCL17基因的表达量。
上述试剂盒中,所述试剂盒还包括含有CCL17基因或其片段的阳性对照质粒。
上述试剂盒中,所述阳性对照质粒为含有序列表中序列7所示的CCL17基因片段的重组质粒。
上述试剂盒中,所述阳性对照质粒为将pMD18-T载体与序列表中序列7所示的CCL17基因片段连接得到的重组质粒。
上述试剂盒中,所述序列表中序列1所示的单链DNA分子、所述序列表中序列2所示的单链DNA分子、所述探针甲的摩尔比为40:40:25。
上述试剂盒中,所述肿瘤为淋巴肿瘤或白血病;
所述肿瘤患者为淋巴肿瘤患者或白血病患者;
所述白血病患者具体为急性淋巴细胞白血病患者,为急性淋巴细胞白血病初诊患者或难治复发患者。
所述淋巴肿瘤具体为伯基特淋巴瘤、套细胞淋巴瘤、组织细胞淋巴瘤;
伯基特淋巴瘤细胞系为Raji;
套细胞淋巴瘤细胞系为Marver;
组织细胞淋巴瘤细胞系为U937;
人淋巴瘤细胞系为Romas;
所述白血病为急性淋巴细胞白血病(ALL)、慢性粒细胞白血病急变或急性髓性白血病(AML);急性淋巴细胞白血病细胞系为BV173、NALM-6、Romas、SUP-B15、Molt4、Jurkat或6T-CEM;慢性粒细胞白血病急变细胞系为MEG-1或K562;急性髓性白血病细胞系为HL60或NB4。
上述试剂盒还包括DNA分子乙,所述DNA分子乙由引物对乙和探针乙组成,
所述引物对乙由序列表中序列4所示的单链DNA分子和序列5所示的单链DNA分子组成;
所述探针乙为序列表中序列6所示的单链DNA分子。
上述试剂盒还包括内参对照质粒,所述内参对照质粒为含有序列表中序列8所示的ABL1基因片段的重组质粒。
上述试剂盒中,所述阳性对照质粒为将pMD18-T载体与序列表中序列8所示的ABL1基因片段连接得到的重组质粒。
上述试剂盒中,所述DNA分子乙中,所述序列表中序列4所示的单链DNA分子、所述序列表中序列5所示的单链DNA分子、所述探针乙的摩尔比为40:40:25。
上述DNA分子甲在制备试剂盒中的应用也是本发明保护的范围。
上述DNA分子甲和上述阳性对照质粒在制备试剂盒中的应用也是本发明保护的范围。
上述试剂盒的功能为如下1)-3)中任一种:
1)辅助诊断肿瘤患者;
2)辅助鉴定肿瘤细胞系;
3)定量检测CCL17基因的表达量;
所述肿瘤患者为淋巴肿瘤患者或白血病患者;
所述白血病患者具体为急性淋巴细胞白血病患者,为急性淋巴细胞白血病初诊患者或难治复发患者。
所述淋巴肿瘤具体为伯基特淋巴瘤、套细胞淋巴瘤、组织细胞淋巴瘤;
伯基特淋巴瘤细胞系为Raji;
套细胞淋巴瘤细胞系为Marver;
组织细胞淋巴瘤细胞系为U937;
人淋巴瘤细胞系为Romas;
所述白血病为急性淋巴细胞白血病(ALL)、慢性粒细胞白血病急变或急性髓性白血病(AML);急性淋巴细胞白血病细胞系为BV173、NALM-6、Romas、SUP-B15、Molt4、Jurkat或6T-CEM;慢性粒细胞白血病急变细胞系为MEG-1或K562;急性髓性白血病细胞系为HL60或NB4。
检测CCL17基因的表达的物质在制备检测辅助诊断肿瘤患者试剂盒或辅助鉴定肿瘤细胞系试剂盒中的应用也是本发明保护的范围;
所述肿瘤具体为淋巴肿瘤或白血病。
上述检测CCL17基因表达的物质为第一个目的提供的试剂盒。
本发明设计了定量检测CCL17基因表达的引物和探针,建立了实时荧光定量检测CCL17的方法,可以用于定量检测CCL17基因表达水平,并发现定量检测CCL17在ALL患者中的表达水平具有临床意义,从而用于肿瘤细胞系的辅助鉴定或肿瘤患者的辅助诊断,将在医学检测领域发挥重要的作用。
附图说明
图1为阳性对照质粒的RQ-PCR荧光标准曲线。
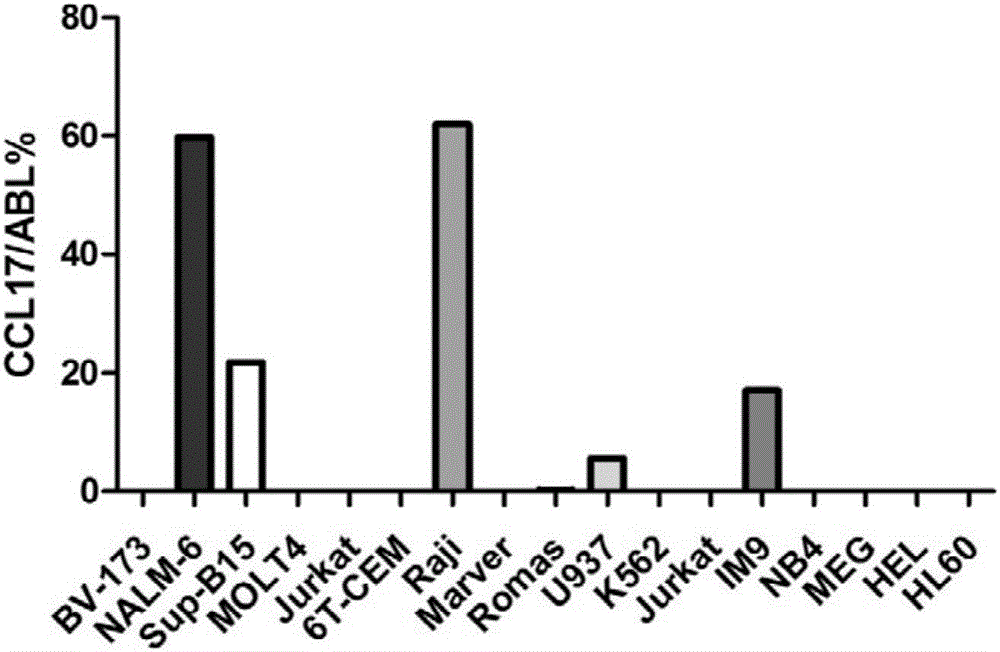
图2为引物和探针检测细胞系的结果。
图3为引物和探针检测急性淋巴细胞白血病患者的结果。
具体实施方式
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实施例1、检测CCL17表达的特异引物和探针设计
针对CCL17基因(NCBI基因库序列号:NM_002987.2,提交时间是2013.12.15,序列7)的设计特异性引物对甲(由上游引物CCL17-FP和下游引物CCL17-RP组成,扩增产物为82bp)和探针甲(探针CCL17-probe):
上游引物CCL17-FP(序列1):5’-CAGGGATGCCATCGTTTTTG-3’;
下游引物CCL17-RP(序列2):5’-AACTGCATTCTTCACTCTCTTGTTGT-3’;
探针CCL17-probe:
FAM-CAGGGCCATCTGTTCGGACCCC-BHQ(序列3)。
针对ABL1基因(内参基因;NCBI基因库序列号:NM_005157)设计的特异性引物对乙(由上游引物ABL1-F和下游引物ABL1-R组成,扩增产物为124bp)和探针乙(探针ABL1-T-probe):
上游引物ABL1-F(序列表的序列4):5’-TGGAGATAACACTCTAAGCATAACTAAAGGT-3’;
下游引物ABL1-R(序列表的序列5):5’-GATGTAGTTGCTTGGGACCCA-3’;
探针ABL1-T-probe(5’→3’):
FAM-CCATTTTTGGTTTGGGCTTCACACCATT–TAMRA(核苷酸序列为序列表的序列6)。
分别合成特异性引物对甲、探针甲、特异性引物对乙和探针乙。
实施例2、引物和探针检测阳性对照质粒的灵敏度检测
一、相关质粒的制备
1、阳性对照质粒(含有CCL17基因片段的质粒)的制备
阳性对照质粒为将序列表中序列7所示的CCL17基因插入pMD18-T质粒的ECOR V酶切位点间得到的载体。
2、内参对照质粒(含有ABL基因片段的质粒)的制备
内参对照质粒为将ABL基因插入pMD18-T质粒的ECOR V酶切位点间得到的载体。
3、阴性对照质粒
pMD18-T质粒。
二、检测阳性对照质粒的灵敏度检测
将上述一得到的阳性对照质粒用灭菌双蒸注射用水进行10倍梯度稀释得到各个稀释液(每微升分别含有106、105、104、103、102、101、100个拷贝的CCL17基因片段);将上述一得到的内参对照质粒用灭菌双蒸注射用水进行10倍梯度稀释得到各个稀释液(每微升分别含有106、105、104、103、102、101、100个拷贝的ABL基因片段);通过测定吸光度值计算CCL17基因片段或ABL基因片段的拷贝数)。
将各个阳性对照质粒稀释液采用实施例1得到的特异性引物对甲和探针甲在荧光实时定量PCR仪(美国ABI公司7500-FAST型)上进行RQ-PCR。将各个内参对照质粒采用实施例1得到的特异性引物对乙和探针乙在荧光实时定量PCR仪(美国ABI公司7500-FAST型)上进行RQ-PCR。
PCR反应体系(10μl):上游引物0.4μM,下游引物0.4μM,探针0.25μM,2×TaqMan通用PCR公共体系5μl(ABI公司,美国),质粒1μl;其余为去离子水。
PCR反应条件:50℃2min,1个循环;95℃10min,1个循环;95℃15s,60℃1min,50个循环。
内参对照质粒RQ-PCR荧光标准曲线(阈值为0.082)函数为log10ABL1=(Ct-38.47)/-3.22,相关系数均达到0.99以上,检测内参基因的灵敏度达10个拷贝。
阳性对照质粒的RQ-PCR荧光标准曲线见图1(阈值为0.082),函数为log10CCL17=(Ct-37.453)/-3.37,相关系数均达到0.99以上,检测CCL17基因片段的灵敏度至少为10个拷贝。
实施例3、检测细胞系及肿瘤患者
一、试剂盒的组装
试剂盒由如下组件组成:实施例1制备的针对CCL17基因的特异性引物对甲和探针甲、针对ABL1基因的特异性引物对乙和探针乙;实施例2制备的阳性对照质粒和内参对照质粒。
二、应用步骤一的试剂盒检测细胞系
分别检测各个细胞系中的CCL17基因的表达水平。每个细胞系样本皆重复检测3次。步骤如下:
1、提取各个细胞的总RNA,反转录为cDNA。
2、以cDNA为模板,用特异性引物对甲和探针甲在荧光实时定量PCR仪(美国ABI公司7500-FAST型)上进行RQ-PCR;以cDNA为模板,用特异性引物对乙和探针乙在荧光实时定量PCR仪(美国ABI公司7500-FAST型)上进行RQ-PCR。分析每批RQ-PCR结果时阈值均固定为阈值为0.082。
PCR反应体系和PCR反应条件同实施例2。分别用阳性对照质粒和内参对照质粒制作标准曲线。对照标准曲线得到各细胞系中CCL17基因和ABL1基因的拷贝数。以CCL17基因的拷贝数与ABL1基因的拷贝数的比值表示CCL17基因的相对表达水平(%)。
结果见表1和图2,CCL17在部分急性B淋巴细胞系(SUP-B15、NALM-6以及Romas)中表达,在急性B淋巴细胞白血病细胞系BV173及MOLT4不表达,在组织细胞性淋巴瘤细胞系U937,多发性骨髓瘤细胞系IM9有一定程度表达,在伯基特淋巴瘤Raji细胞中高表达,而在套细胞淋巴瘤细胞系Marver,急性髓系白血病细胞系HL60,NB4及慢性粒细胞白血病急变细胞系K562及MEG-01,急性红白血病细胞系HEL及套细胞淋巴瘤细胞系MAVER,急性T淋巴细胞系MOLT4,Jurkat,6T-CEM不表达。
所述白血病为急性淋巴细胞白血病、慢性粒细胞白血病急变或急性髓性白血病;急性淋巴细胞白血病细胞系为SUP-B15、Molt4、Jurkat、6T-CEM;慢性粒细胞白血病急变细胞系为MEG-1或K562;急性髓性白血病细胞系为HL60或NB4。
表1血液肿瘤细胞系中CCL17基因的表达水平
三、应用步骤一的试剂盒检测急性淋巴白血病患者
分别选取若干急性淋巴细胞白血病患者(包括189例B-ALL初诊患者、102例B-ALL缓解患者、21例难治复发B-ALL患者),16例T-ALL初诊患者,70例AML初诊患者及43例健康正常人。
1、用TRIzol试剂盒(购自美国Invitrogen公司)并参照试剂盒说明书在无菌条件下提取各个志愿者的骨髓标本的RNA(或外周血标本的RNA也可),反转录为cDNA。
2、以cDNA为模板,用特异性引物对甲和探针甲在荧光实时定量PCR仪(美国ABI公司7500-FAST型)上进行RQ-PCR;以cDNA为模板,用特异性引物对乙和探针乙在荧光实时定量PCR仪(美国ABI公司7500-FAST型)上进行RQ-PCR。分析每批RQ-PCR结果时阈值均固定为阈值为0.082。
PCR反应体系和PCR反应条件同实施例2。
分别用阳性对照质粒和内参对照质粒制作标准曲线。对照标准曲线得到各患者中CCL17基因和ABL1基因的拷贝数。以CCL17基因的拷贝数与ABL1基因的拷贝数的比值表示CCL17基因的相对表达水平(%)。
结果见图3所示,可以看出,在43例健康人组成的正常组中CCL17低表达,中位值0.05%(范围0%~6.87%);189例B-ALL初诊患者组中CCL17中位值为0.23%(范围0%~69000%);189例缓解B-ALL患者组中CCL17中位值0.02%(范围0%~3339%);21例难治复发B-ALL患者组CCL17中位值为0.68%(范围0.003%~13490%)。统计结果显示,与正常组相比,初诊B-ALL组的CCL17表达水平显著增高(P=0.0007);
与初诊B-ALL组相比,缓解B-ALL组的CCL17表达水平显著下降(P〈0.0001)。B-ALL初诊组、难治复发组相比无统计学差异(P=0.34)。正常组与B-ALL缓解组相比无统计学差异。正常组与初诊AML组及初诊T-ALL组相比较,无统计学差异(P值分别为0.27和0.54)。因此,可以确定,检测CCL17表达的引物和探针可以用来辅助鉴定待测患者是否患有急性淋巴白血病或待测癌细胞是否为淋巴肿瘤细胞或其他血液系统肿瘤细胞。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种快速区分prv中国型、欧美型及疫苗株的双色荧光检测方法、引物及探针的制作方法
- 实时荧光pcr技术定量检测myd88基因l265p突变的方法、引物和探针的制作方法
- 用于定性检测白血病融合基因的引物、探针、试剂盒及方法
- 在体外检测或/及定量乙型肝炎病毒的方法及其所使用的引物、探针的制作方法
- 用于检测多种呼吸道病毒的pcr引物组、探针组及试剂盒的制作方法
- 一种检测人类met基因14外显子剪接突变的引物、探针及试剂盒的制作方法
- 使用重叠引物和熔解探针检测单核苷酸多态性的制作方法
- 用于检测多种呼吸道病毒的pcr引物组、探针组及试剂盒的制作方法
- 一种检测人类met基因14外显子剪接突变的引物、探针及试剂盒的制作方法
- 使用重叠引物和熔解探针检测单核苷酸多态性的制作方法
- 一种木瑚菌属食用菌鉴别用分子标记及引物和探针的制造方法与工艺
- 一组用于驴源性的实时荧光PCR检测的特异性引物和探针的制造方法与工艺
- 一组用于鸡源性实时荧光PCR检测的特异性引物和探针的制造方法与工艺
- 一种快速检测异鳞蛇鲭和棘鳞蛇鲭源性成分的方法与制造工艺
- 一种检测食管癌相关标志物的探针组合及其试剂盒的制造方法与工艺
- 一种检测皮肤癌相关标志物的探针组合及其试剂盒的制造方法与工艺
- 一种检测骨髓瘤相关标志物的探针组合及其试剂盒的制造方法与工艺
- 一种用于检测样品中牛凸隆病毒的荧光RT-PCR引物、探针和试剂盒及检测方法与制造工艺
- CYP2C19基因多态性检测引物、探针及试剂盒的制造方法与工艺
- 检测CYP2C9和VKORC1基因多态性的引物、探针和试剂盒的制造方法与工艺