一种氟氢可的松醋酸酯的制备方法与流程
发明领域
本发明属于医药化学领域,具体涉及氟氢可的松醋酸酯制备方法。
背景技术:
氟氢可的松醋酸酯,又名醋酸氟氢可的松,9α-氟皮质醇醋酸酯,9α-氟醋酸氢化可的松等,其化学名为:11β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯,市售剂型分为片剂和软膏。本品为肾上腺皮质激素类药,属中效皮质类固醇,有抗炎、抗过敏作用,能抑制结缔组织的增生,降低毛细血管和细胞膜的通透性,减少炎性渗出,抑制组胺及其他炎症介质的形成和释放。主要用于肾上腺皮质功能减退症的替代治疗,并可外用于过敏性皮炎、接触性皮炎、脂溢性皮炎、湿疹等皮肤病。
在氟氢可的松醋酸酯的合成方法中,其中关键的合成步骤是对化合物9β,11β-环氧-17α-羟基孕甾-4-烯-3,20-二酮-21-醋酸酯进行氟化开环。根据文献,常用的氟化试剂有无水氟化氢[fried,j.;sabo,e.f.,j.am.chem.soc.1957,79,1130.]和52~55%氟化氢水溶液[us2894007],前者使用无水氟化氢气体,操作不便,腐蚀性高,毒性大,对设备要求较高;后者使用氟化氢水溶液,并且需要在反应中使用到强酸如高氯酸,反应副产物较多,不易控制,因此使用上述工艺进行工业化生产面临诸多的问题。
本发明针对现有技术中的制备方法的缺陷进行了改进与优化。与现有技术中的方法相比,本发明的制备方法不仅总产率有显著的提高,而且操作安全简易,试剂用量少,后处理方便,适合工业生产。
技术实现要素:
本发明的目的在于,提供一种低毒性、低腐蚀性、后处理简单、试剂用量少的氟氢可的松醋酸酯的制备方法。
氟氢可的松醋酸酯的结构式如式(i)所示:
所用起始物料为9β,11β-环氧-17α-羟基孕甾-4-烯-3,20-二酮-21-醋酸酯,结构如式(ⅱ)所示:
本发明提供一种氟氢可的松醋酸酯的制备方法,该方法包括:将9β,11β-环氧-17α-羟基孕甾-4-烯-3,20-二酮-21-醋酸酯与氟化试剂进行开环反应,其中所述氟化试剂为氟化氢的有机胺盐或有机胺溶液。
本发明所述的氟化试剂选自三乙胺三氟化氢盐和氢氟酸吡啶溶液,优选选自70%的氢氟酸吡啶溶液。
本发明所述的开环反应在有机溶剂下进行,所述有机溶剂选自吡啶、二氯甲烷、三氯甲烷、乙酸乙酯中的一种或多种。开环反应的温度为0~30℃,进一步优选为0~10℃。
在开环反应结束后,用水进行萃取提纯,萃取所得的有机相经浓缩后进行重结晶,所述重结晶所用溶剂为二氯甲烷、乙酸乙酯、乙醇、丙酮中的一种或多种,进一步优选为二氯甲烷或乙酸乙酯。
本发明重点改良了关键工艺步骤环氧化合物开环氟化的试剂及条件,以氟化氢的有机胺盐或氟化氢的溶液代替高毒性、高腐蚀性的氟化氢气体,操作安全方便,氟化试剂用量少,适合工业生产。
与us2894007使用到的氟化氢水溶液相比,本发明的技术方案具有如下效果:不需要使用氟化氢水溶液和强酸,减少反应液对反应设备及装置的高腐蚀性;us2894007使用的氟化氢投料量非常巨大,起始物与氟化氢的投料摩尔比为1:50~300,而本发明在1:20即可取得非常好的收率;us2894007反应结束后反应后的目标产品在反应液中的含量为50~65%,而本发明的含量可高达70%。
下列实施例对本发明的方法进一步的说明,但不限制本发明的范围。
附图说明
图1为氟氢可的松醋酸酯的核磁氢谱谱图
图2为氟氢可的松醋酸酯的核磁碳谱谱图
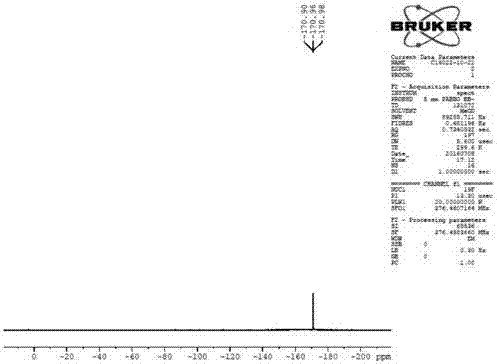
图3为氟氢可的松醋酸酯的核磁氟谱谱图
具体实施方式
11β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的制备合成路线如下:
其含量和有关物质参照2010版的中国药典方法进行检测。
实施例111β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的制备
将化合物1(1g,2.49mmol)溶于二氯甲烷20ml,降温至0~10℃,加入40%氢氟酸水溶液5ml和60%高氯酸水溶液5ml。在0~10℃下,反应2小时。反应结束后,加入水50ml,用二氯甲烷50ml×2萃取水相两次,合并二氯甲烷相,用水洗至中性,无水硫酸钠干燥后,减压浓缩得泡沫状固体,经柱层析纯化得氟氢可的松醋酸酯。
实施例211β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的制备
将化合物1(1g,2.49mmol)溶于二氯甲烷20ml,降温至0~10℃,加入50%氢氟酸水溶液5ml和60%高氯酸水溶液5ml。在0~10℃下,反应2小时。反应结束后,加入水50ml,用二氯甲烷50ml×2萃取水相两次,合并二氯甲烷相,用水洗至中性,无水硫酸钠干燥后,减压浓缩得泡沫状固体,经柱层析纯化得氟氢可的松醋酸酯。
实施例311β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的制备
将化合物1(1g,2.49mmol)溶于二氯甲烷20ml,降温至0~10℃,加入三氟化氢三乙胺(1ml,约8.6mmol)。在0~10℃下,反应2小时。反应结束后,加入水5ml,用二氯甲烷5ml×2萃取水相两次,合并二氯甲烷相,用水洗至中性,无水硫酸钠干燥后,减压浓缩得泡沫状固体,经柱层析纯化得氟氢可的松醋酸酯。
实施例411β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的制备
将化合物1(1g,2.49mmol)溶于二氯甲烷20ml,降温至0~10℃,加入70%吡啶氢氟酸(1ml,含hf约39mmol)。在0~10℃下,反应2小时。反应结束后,加入水50ml,用二氯甲烷50ml×2萃取水相两次,合并二氯甲烷相,用水洗至中性,无水硫酸钠干燥后,减压浓大部分溶剂,有固体析出,过滤,干燥,得氟氢可的松醋酸酯固体。
实施例511β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的制备
将化合物1(0.2g,0.50mmol)悬浮于70%吡啶氢氟酸0.45ml(含hf约17mmol)中。在0~10℃下,反应2小时。反应结束后,加入水5ml,用二氯甲烷10ml×2萃取水相两次,合并二氯甲烷相,用水洗至中性,无水硫酸钠干燥后,减压浓大部分溶剂,有固体析出,过滤,干燥,得氟氢可的松醋酸酯固体。
实施例611β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的制备
将化合物1(2g,5.0mmol)溶于二氯甲烷20ml,降温至0~10℃,加入70%吡啶氢氟酸(2.6ml,含hf约100mmol)。在0~10℃下,反应2小时。反应结束后,加入水50ml,用二氯甲烷50ml×2萃取水相两次,合并二氯甲烷相,用水洗至中性,无水硫酸钠干燥后,减压浓大部分溶剂,经柱层析纯化得氟氢可的松醋酸酯,得类白色氟氢可的松醋酸酯固体1.0g,收率47.8%,hplc纯度为97.5%
实施例711β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的制备
将化合物1(2g,5.0mmol)溶于二氯甲烷20ml,降温至20~30℃,加入70%吡啶氢氟酸(4.0ml,含hf约150mmol)。在0~10℃下,反应2小时。反应结束后,加入水50ml,用二氯甲烷50ml×2萃取水相两次,合并二氯甲烷相,用水洗至中性,无水硫酸钠干燥后,减压浓大部分溶剂,有固体析出,过滤,干燥,得类白色氟氢可的松醋酸酯固体1.2g,收率57.4%,hplc纯度为98.3%。
实施例811β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的制备
将化合物1(20g,49.8mmol)溶于二氯甲烷200ml,降温至0~10℃,加入70%吡啶氢氟酸26ml(含hf约1mol)。在0~10℃下,反应1小时。反应结束后(反应液中约含目标产品收率70%),加入水50ml,用二氯甲烷50ml×2萃取水相两次,合并二氯甲烷相,用水洗至中性,减压浓大部分溶剂,有固体析出,过滤,干燥,得类白色氟氢可的松醋酸酯11.0g,收率52.4%,hplc纯度98.2%,相关核磁数据见图1-3。
实施例911β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的重结晶
将氟氢可的松醋酸酯粗品(0.5g,1.18mmol)悬浮于乙酸乙酯30ml,加热至回流,溶清后,自然冷却至室温,有白色固体析出,过滤,干燥得氟氢可的松醋酸酯0.25g,收率50.0%。
实施例1011β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的重结晶
将氟氢可的松醋酸酯粗品(0.5g,1.18mmol)悬浮于丙酮5ml,加热至回流,溶清后,自然冷却至室温,有白色固体析出,过滤,干燥得氟氢可的松醋酸酯0.20g,收率40.0%。
实施例1111β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的重结晶
将氟氢可的松醋酸酯粗品(0.5g,1.18mmol)悬浮于乙醇5ml,加热至回流,溶清后,自然冷却至室温,有白色固体析出,过滤,干燥得氟氢可的松醋酸酯0.15g,收率30.0%。
实施例1211β,17α,21-三羟基-9α-氟孕甾-4-烯-3,20-二酮-21-醋酸酯的重结晶
将氟氢可的松醋酸酯粗品(0.8g,1.19mmol)悬浮于二氯甲烷50ml,加热至回流,溶清后,自然冷却至室温,有白色固体析出,过滤,干燥得氟氢可的松醋酸酯0.6g,收率75.0%。
尽管以上已经对本发明作了详细描述,但是本领域技术人员理解,在不偏离本发明的精神和范围的前提下可以对本发明进行各种修改和改变。本发明的权利范围并不限于上文所作的详细描述,而应归属于权利要求书。
- 还没有人留言评论。精彩留言会获得点赞!