一种氧氟沙星‑血蓝蛋白包被原及其制备方法和检测试纸卡与流程
本发明属于生物医药和医学检验技术领域,尤其涉及一种氧氟沙星-血蓝蛋白包被原及其制备方法和检测试纸卡。
背景技术:
氧氟沙星(Ofloxacin,OFL)是第三代氟喹诺酮类药物,又名氟嗪酸,是由日本第一制药株式会社于1980年开发的一种抗生素,因为分子的基本结构中引入了疏水性的氟原子及亲水性的哌嗪环,使其抗菌活性得到了增强,与早期喹诺酮类药物相比,其细菌耐药性也大大降低了。这类药物通过抑制细菌的DNA旋转酶和拓扑异构酶Ⅳ,抑制细菌DNA复制、转录和修复过程,具有抗菌谱广、高效、低毒、组织穿透力强的特点,是继磺胺类药物之后人类在合成抗菌药物方面最重要的突破之一,其抗菌作用是磺胺类药物的近千倍,可与第三代头孢类抗菌药物相媲美。目前,OFL已成为兽医临床和水产养殖中最重要的抗感染药物之一,被大量用于治疗、预防和促生长,甚至作为饲料添加剂使用。然而此类氟喹诺酮类药物对人体有一定毒副作用,包括胃肠道、中枢神经系统的不良反应、心脏毒性、致病菌产生耐药性和潜在致癌性等,其在牲畜体内的残留会对环境及人体健康造成严重伤害。
氧氟沙星药物残留检测的传统方法有微生物学法,高效液相色谱法(HPLC),液质联用法(LC-MS)和液相色谱-串联质谱法(LC-MS/MS)等方法。这些方法灵敏度高、特异性强,但样品前处理繁琐,需要专业的技术人员和昂贵的仪器设备,不适合大批量的市场监测要求。免疫学检测方法建立在抗体对抗原的分子识别上,具有抗原抗体的亲合力高、检测快速、经济实用,能够实现对生物液体的小体积、大通量检测的优点。但是根据现有技术中,杜付彬等人报道氧氟沙星人工抗原的合成及鉴定方法,具体采用碳二亚胺法和混合酸酐法合成氧氟沙星免疫原和包被原,但是制备的氧氟沙星免疫原并未免疫小鼠,因此,无法估算单克隆抗体的特异性;再如,公告号为CN100418982C的专利公开了一种氧氟沙星的偶联物及其制备方法,采用碳二亚胺法制备的氧氟沙星的偶联物免疫白兔,抗血清的最低检测限为1ppb(1μg/L)。因此,现有技术需要更低的检测限的氧氟沙星检测试剂盒。
技术实现要素:
有鉴于此,本发明的目的在于一种氧氟沙星-血蓝蛋白包被原及其制备方法,使制备得到的氧氟沙星-血蓝蛋白包被原具有较高的反应原性和偶联率高的特点。
本发明另一个目的是提供一种氧氟沙星检测试纸卡,使所述试纸卡具有检测速度快、特异性强、灵敏度高、结果准确的特点。
为了实现上述发明目的,本发明提供以下技术方案:
本发明提供了一种氧氟沙星-血蓝蛋白包被原,具有式I所示结构:
表示所述包被原中偶联的血蓝蛋白。
本发明提供了一种氧氟沙星-血蓝蛋白包被原的制备方法,包括以下步骤:
1)将氨基戊酸和氧氟沙星在缓冲溶液体系中进行脱水缩合反应,将得到的反应液依次进行萃取和反萃取,得到碳链延伸的氧氟沙星半抗原;
2)将所述步骤1)得到的碳链延伸的氧氟沙星半抗原溶于N,N-二甲基甲酰胺,得到碳链延伸的氧氟沙星半抗原溶液;将氯甲酸异丁酯与所述碳链延伸的氧氟沙星半抗原溶液混合,搅拌反应,得到活化的氧氟沙星半抗原;
3)将血蓝蛋白和磷酸缓冲液混合,调节混合液的pH值至9.0~10,在振荡条件下反应,得到血蓝蛋白;
4)将所述步骤3)中得到的活化的血蓝蛋白溶解于含有N,N-二甲基甲酰胺的磷酸盐缓冲溶液中,得到活化的血蓝蛋白溶液;
5)将所述步骤2)得到的活化的氧氟沙星半抗原滴加到所述步骤4)得到的血蓝蛋白溶液中,在振荡条件下反应,得到具有式I所示结构的氧氟沙星-血蓝蛋白包被原:
所述步骤1)~2)与步骤3)之间没有时间顺序的限制。
优选的,所述步骤1)中氨基戊酸溶液的pH值为10.0~12.0;所述氨基戊酸溶液的质量浓度为20~40mg/ml。
优选的,所述步骤1)中氧氟沙星溶液的质量浓度为15~30mg/ml;
所述氧氟沙星溶液中的溶剂为摩尔浓度为0.01~0.02mol/L、pH值为7.4的PBS溶液。
优选的,所述步骤1)中萃取用萃取剂为乙酸乙酯;所述洗涤的洗涤液为质量浓度为0.09~0.18mg/ml的盐酸溶液;所述反萃取用反萃剂为质量浓度为2.1~4.2mg/ml的碳酸氢钠溶液。
优选的,所述步骤3)中碳链延伸的氧氟沙星半抗原、N,N-二甲基甲酰胺和氯甲酸异丁酯的摩尔比为3~10:1。
优选的,所述步骤3)中振荡的转速为50~200r/min,所述步骤3)中反应的温度为30~37℃
优选的,所述步骤4)中血蓝蛋白与N,N-二甲基甲酰胺的摩尔比为3~10:1。
优选的,所述步骤5)中氧氟沙星半抗原与血蓝蛋白的摩尔比为5~10:1。
优选的,所述步骤5)中振荡的转速为50~200r/min;所述振荡的温度为30~37℃。
本发明还提供了一种检测氧氟沙星用试纸卡,包括卡壳、底板、样品垫、金标垫、检测和吸水区,所述检测区设有检测线T和质控线C,其特征在于,所述检测线T位置包被有氧氟沙星-血蓝蛋白包被原,所述质控线C位置包被有兔抗IgG,所述金标垫附着有金标记的氧氟沙星单克隆抗体;
所述金标记的氧氟沙星单克隆抗体是由所述的细胞株分泌得到。
优选的,所述氧氟沙星包被原的包被浓度为0.05~0.1μg/ml。
优选的,所述氧氟沙星单克隆抗体的质量浓度为0.01~0.02mg/ml。
本发明提供的一种氧氟沙星-血蓝蛋白包被原,具有式I所示结构。所述的氧氟沙星-血蓝蛋白免疫原在氧氟沙星的羧基上进行C链衍生化,使羧基伸长,使抗原决定簇暴露在外,制成的包被原具有较强的反应原性。
本发明提供的一种氧氟沙星-血蓝蛋白包被原的制备方法,氧氟沙星上羧基进行C链衍生化,同时血蓝蛋白进行活化,再利用酸酐偶合法合成包被原,制备出的免疫原具有偶联率高、反应原性强的特点。
本发明提供的单克隆抗体具有特异性强、灵敏度高的单克隆抗体。
本发明提供的一种检测氧氟沙星用试纸卡,包括卡壳,底板,样品垫,金标垫,检测区和吸水区,所述检测区设有检测线T和质控线C,所述检测线T位置包被有氧氟沙星-血蓝蛋白包被原,所述质控线C位置包被有兔抗IgG,所述金标垫附着有金标记的氧氟沙星单克隆抗体。本发明将上述制备得到的氧氟沙星单克隆抗体与氧氟沙星包被原制备成的试纸卡,具有检测速度快,灵敏度高,且满足快速检测的要求,所述试纸卡的检测限可达0.06ng/ml。
进一步的,卡壳的使用可以延长检测结果观察时间,试纸卡稳定性好。本试纸卡样品吸收垫将检测溶液完全吸收,使之与偶联垫上金标抗体充分反应,可以有效减少误差率;还可以防止外界杂质干扰,影响金标抗体与检测抗原的结合;成本低、投资少。使用本发明试纸卡,不需要另配复杂的仪器设备和昂贵的试剂,现场检测一步到位,成本低廉,见效快;易于大范围推广应用。本试纸卡操作简单,适合不同类别的人员使用,如实验室检测、海关检疫、卫生监督、规模养殖及个体生产等,具有广阔的市场前景和较大的经济效益和社会效益。
附图说明
图1为实施例1中氧氟沙星-血蓝蛋白包被原合成反应合成路线图;
图2为实施例3中左氧氟沙星免疫抗原合成路线图;
图3为实施例5中氧氟沙星特异性免疫学检测试纸卡的结构示意图;
图4为实施例5中氧氟沙星特异性免疫学检测试纸卡中试纸条的侧视图;
图5为实施例5中氧氟沙星特异性免疫学检测试纸卡中试纸条的俯视图。
具体实施方式
本发明提供了一种氧氟沙星-血蓝蛋白包被原,具有式I所示结构:
表示所述包被原中偶联的血蓝蛋白。
本发明提供了一种氧氟沙星-血蓝蛋白包被原的制备方法,包括以下步骤:
1)将氨基戊酸和氧氟沙星在缓冲溶液体系中进行脱水缩合反应,将得到的反应液依次进行萃取和反萃取,得到碳链延伸的氧氟沙星半抗原;
2)将所述步骤1)得到的碳链延伸的氧氟沙星半抗原溶于N,N-二甲基甲酰胺,得到碳链延伸的氧氟沙星半抗原溶液;将氯甲酸异丁酯与所述碳链延伸的氧氟沙星半抗原溶液混合,搅拌反应,得到活化的氧氟沙星半抗原;
3)将血蓝蛋白和磷酸缓冲液混合,调节混合液的pH值至9.0~10,在振荡条件下反应,得到血蓝蛋白;
4)将所述步骤3)中得到的活化的血蓝蛋白溶解于含有N,N-二甲基甲酰胺的磷酸盐缓冲溶液中,得到活化的血蓝蛋白溶液;
5)将所述步骤2)得到的活化的氧氟沙星半抗原滴加到所述步骤4)得到的血蓝蛋白溶液中,在振荡条件下反应,得到具有式I所示结构的氧氟沙星-血蓝蛋白包被原:
所述步骤1)~2)与步骤3)之间没有时间顺序的限制。
本发明将氨基戊酸溶液和氧氟沙星溶液进行脱水缩合反应,得到脱水缩合反应液。本发明中,所述氨基戊酸溶液的质量浓度优选为20~40mg/ml,更优选为24mg/ml。所述氨基戊酸溶液的溶剂为水。所述氨基戊酸溶液的pH值优选为10.0~12.0,更优选为11.0。所述氨基戊酸溶液的pH值优选采用质量浓度为0.1%的氢氧化钠溶液调整,调整后的氨基戊酸溶液冰浴搅拌,所述冰浴搅拌的目的是逐渐降低反应溶液至4℃,进行氨基戊酸和氧氟沙星的脱水缩合反应。所述冰浴的方法没有特殊限制采用本领域技术人员所熟知的冰浴的技术方案即可。
本发明中,所述氧氟沙星溶液的质量浓度优选为15~30mg/ml,更优选为22mg/ml。所述氧氟沙星溶液的溶剂优选为摩尔浓度为0.01~0.02mol/L、pH值为7.4的PBS溶液。
在本发明中,所述脱水缩合反应具体方法优选为:在搅拌状态下将所述氧氟沙星溶液逐滴加入氨基戊酸溶液中,在搅拌条件下进行脱水缩合反应。本发明中,所述搅拌的转速优选为50~200r/min,更优选为100r/min;所述脱水缩合反应的时间优选为2~3h;所述脱水缩合反应的温度优选为30~37℃。所述逐滴加入的每滴液体的体积为0.02ml。所述逐滴加入的每滴液体的速度为50滴/min。所述逐滴加入能够使氧氟沙星溶液与氨基戊酸溶液充分发生脱水缩合反应,提高氧氟沙星(OFL)羧基C链延伸化的比例。
脱水缩合反应后,本发明将得到的反应液进行萃取,本发明对所述萃取的具体操作没有特殊限制,采用本领域技术人员所熟知的萃取的技术方案即可。在本发明中,所述萃取用萃取剂优选为乙酸乙酯。萃取剂的用量为2~5ml。所述萃取的目的是去除不溶解的大颗粒杂质分子,其反应产物进入有机相。
所述萃取后,得到水相和有机相。本发明优选将所述萃取后有机相进行洗涤。本发明对所述洗涤的方法没有特殊限制,采用本领域技术人员所熟知的洗涤的技术方案即可。在本发明中,所述洗涤用洗涤液优选为盐酸溶液。所述盐酸溶液的质量浓度优选为0.09~0.18mg/ml更优选为0.15mg/ml。所述洗涤的次数优选2~5次,更优选3次。
得到有机相后,本发明将所述有机相进行反萃取,反萃取后得到的水相含有反应产物,即碳链延伸的氧氟沙星半抗原。在本发明中,所述反萃取用反萃剂优选为碳酸氢钠溶液。所述碳酸氢钠溶液的质量浓度优选为2.1~4.2mg/ml,更优选为3.15mg/ml。所述反萃取的目的是将反应产物重新溶解在水相中。反萃剂的用量为3~6ml。
得到碳链延伸的氧氟沙星半抗原后,本发明将所述碳链延伸的氧氟沙星半抗原溶于N,N-二甲基甲酰胺,得到碳链延伸的氧氟沙星半抗原溶液;将氯甲酸异丁酯与所述碳链延伸的氧氟沙星半抗原溶液混合,搅拌反应,得到活化的氧氟沙星半抗原;
本发明中,所述碳链延伸的氧氟沙星半抗原与N,N-二甲基甲酰胺的摩尔比优选为3~10:1,更优选为5:1。
本发明中,所述搅拌反应优选在磁力搅拌的条件下进行。所述磁力搅拌的转速优选为50~200r/min,更优选为100r/min。本发明中,所述搅拌反应的温度优选为30~37℃,更优选为35℃。实现避光反应是用锡伯纸将试剂瓶进行严密包装,阻止光线进入。
本发明将血蓝蛋白和磷酸缓冲液混合,调节混合液的pH值至9.0~10,进行振荡,得到溶解的血蓝蛋白。
本发明中,所述血蓝蛋白(KLH)的质量和磷酸缓冲液的体积比优选为(40~60)mg:(2~5)ml,更优选为45mg:3ml。
本发明中,所述pH值优选采用NaHCO3溶液调节。所述NaHCO3溶液的质量浓度优选为2.1~4.2mg/ml,更优选为3.15mg/ml。所述pH值优选调整至9.6。
本发明中,所述振荡条件的转速优选为50~200r/min,更优选为100r/min。所述反应的时间优选为3~5h,更优选为4h。所述振荡的目的是加速血蓝蛋白的完全溶解。
将血蓝蛋白溶解后,本发明将溶解的血蓝蛋白溶与含有N,N-二甲基甲酰胺的磷酸盐缓冲溶液混合,得到血蓝蛋白溶液。本发明中,所述血蓝蛋白与N,N-二甲基甲酰胺的摩尔比为3~10:1,更优选为5:1。
得到活化的氧氟沙星半抗原和血蓝蛋白溶液后,本发明将所述活化的氧氟沙星半抗原滴加到所述KLH溶液中,在振荡条件下脱水缩合反应,得到具有式I所示结构的氧氟沙星-血蓝蛋白(氧氟沙星-KLH)包被原:
本发明中,所述滴加的速率30~100滴/min。
本发明中,所述振荡的转速优选为50~200r/min,更优选为100r/min;所述振荡的温度优选为30~37℃,更优选为35℃。所述反应的时间优选为3~5h,更优选为4h。所述反应的温度优选为30~37℃。
本发明还提供了一种检测氧氟沙星用试纸卡,包括卡壳,底板,样品垫,金标垫,检测区和吸水区,所述检测区设有检测线T和质控线C,所述检测线T位置包被有氧氟沙星-血蓝蛋白包被原,所述质控线C位置包被有兔抗IgG,所述金标垫附着有金标记的氧氟沙星单克隆抗体。
本发明中,所述兔抗IgG的包被浓度为0.2~0.5mg/ml,更优选为0.3mg/ml。本发明对所述兔抗IgG的来源没有特殊限制,采用本领域技术人员所熟知的兔抗IgG即可。
本发明中,所述氧氟沙星-血蓝蛋白包被原的包被浓度优选为0.05~0.1μg/ml,更优选为0.08μg/ml。
本发明中,所述检测区的材料优选为硝酸纤维素膜。所述硝酸纤维素膜的来源没有特殊限制,采用本领域技术人员所熟知的硝酸纤维素膜即可。
本发明中,所述金标记的氧氟沙星单克隆抗体在金标垫上的浓度优选为0.01~0.02mg/ml,更优选为0.015mg/ml。
本发明中,所述氧氟沙星单克隆抗体由所述左氧氟沙星免疫原免疫小鼠筛选得到产抗氧氟沙星的单克隆抗体的细胞株,对所述细胞株进行培养,收集氧氟沙星单克隆抗体。
本发明中,所述左氧氟沙星免疫原为左氧氟沙星-牛血清白蛋白完全抗原。所述左氧氟沙星-牛血清白蛋白完全抗原的制备方法没有特殊限制,采用本领域技术人员所熟知的左氧氟沙星-牛血清白蛋白完全抗原的制备方法即可。本发明实施例中所述左氧氟沙星-牛血清白蛋白完全抗原是采用碳乙二胺法合成。
本发明中,所述氧氟沙星单克隆抗体的收集方法优选包括以下步骤:
当培养的细胞株的浓度达到107/ml以上时,向液体石蜡处理过的母鼠腹腔内注射单克隆细胞,培养10~12d;
培养完成后,抽取母鼠腹水,用饱和硫酸胺法纯化抗氧氟沙星单克隆抗体,得到抗氧氟沙星单克隆抗体。
本发明中,所述注射单克隆细胞的数量优选为107~109/只,更优选为108/只。
本发明中,所述金标记的氧氟沙星单克隆抗体的制备方法没有特殊限制采用本领域技术人员所熟知的制备方法即可。
本发明中,所述金标垫的材料优选为玻璃纤维或聚酯膜。所述玻璃纤维和聚酯膜的来源没有特殊限制,采用本领域技术人员所熟知的玻璃纤维和聚酯膜即可。
本发明中,所述吸水区的材料优选采用吸水纸。所述吸水纸的厚度优选为0.35mm。所述吸水纸的来源没有特殊限制,采用本领域技术人员所熟知的吸水纸即可。
本发明中,所述样品垫优选进行预处理。所述预处理的方法优选为用样品垫处理液浸泡后烘干,得到处理后的样品垫。所述样品垫处理液包括以下重量百分比的组分:含质量浓度3~8%的BSA,质量浓度为1~3%的蔗糖,质量浓度为0.5%~1%的NaCl和质量浓度为0.03%~0.0%8的NaN3的PBS缓冲液,更优选为含质量浓度为5%的BSA,质量浓度为2%的蔗糖,质量浓度为0.8%的NaCl和质量浓度为0.05%的NaN3的PBS缓冲液。本发明中,所述样品垫的材料优选为玻璃纤维。所述玻璃纤维的来源没有特殊限制,采用本领域技术人员所熟知的玻璃纤维即可。
本发明中,所述检测氧氟沙星用试纸卡的制备方法优选包括以下步骤:所述检测线和质控线的划线,所述的结合垫的制备,所述的样品垫的制备和所述试纸卡的组装。
所述检测线和质控线的包被方法优选采用喷点仪包被。所述包被的具体步骤为:将硝酸纤维素膜置于喷点仪平台上,氧氟沙星-血蓝蛋白包被原溶液放于A池,兔抗IgG溶液放于B池,在喷点仪作用下将包被抗原和二抗分别点射于硝酸纤维素膜上,形成检测线(T线)和质控线(C线)。室温自然干燥后,将其浸入封闭液中30min,37℃烘干后,加入干燥剂,4℃密封保存。
所述封闭液优选为质量浓度为1%的BSA的PBS缓冲液,所述的PBS缓冲液的pH值优选为7.4。
本发明中,所述的金标垫的制备方法,优选包括以下步骤:
将玻璃纤维棉放入含有BSA、蔗糖、NaCl和NaN3的PBS处理液处理,烘干,然后将金标抗体灌注已处理好的玻璃纤维棉上,真空冷冻干3~5h,即为金标垫。
本发明中,所述BSA溶液的质量浓度优选为4~6%,更优选为5%。
本发明中,所述蔗糖的质量浓度优选为1~3%,更优选为2%。
本发明中,所述NaCl的质量浓度优选为0.6~1.0%,更优选为0.8%。
本发明中,所述NaN3的质量浓度为0.03~0.07%,更优选为0.05%。
本发明中,所述处理的时间优选为15~30min,更优选为20min。
本发明中,所述烘干的温度优选为35~40℃,更优选为37℃。
本发明中,所述的样品垫的制备方法,优选包括以下步骤:
玻璃纤维棉要用含质量浓度为2%的BSA,质量浓度为1%的蔗糖,质量浓度为0.5%的硼酸钠和质量浓度为0.1%的NaN3的PBS处理后,干燥备用,即为样品垫。
本发明中,所述的试纸卡的组装,优选包括以下步骤:
在底板上,按照样品垫、结合垫、NC膜、吸收垫依次组装在一起,形成组装板;
将所述组装板切割成试纸条。
本发明中,所述样品垫、结合垫、NC膜、吸收垫之间的重叠区域优选5~6mm。
本发明优选将试纸条封装于带有加样孔和观察窗的特制的塑料盒体中,即为氧氟沙星特异性免疫学检测试纸卡。
本发明中,所述一种检测氧氟沙星用试纸卡的使用方法没有特殊限制,采用本领域技术人员所熟知的试纸卡使用方法即可。
本发明中,所述检测氧氟沙星用试纸卡的检测结果判定方法具体为:
试纸卡以红色印迹线“|”或“‖”作为检测线的阳性和阴性标记,即在硝酸纤维素膜上质控线(C线)显示一条红色“|”印迹时,表示被检测样品溶液呈阳性;若硝酸纤维素膜上质控线(C线)和检测线(T线)同时出现两条红色“‖”印迹时,表示样品溶液呈阴性。本发明提供的试纸卡的检测限可达0.06ng/ml。
下面结合实施例对本发明提供的一种氧氟沙星免疫原及其制备方法和检测试纸卡进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
实施例1
氧氟沙星检测抗原的合成,合成反应如附图1所示。
氧氟沙星羧基C链延伸化:称取2mmol氨基戊酸加入三角烧瓶中,然后用2ml氢氧化钠溶液调节pH值,冰浴搅拌;用含50%DMF的甲醇溶解氧氟沙星,搅拌状态下逐滴加入氨基戊酸-氢氧化钠溶液中,磁力搅拌反应2h;用乙酸乙酯萃取,稀盐酸洗涤,再用碳酸氢钠溶液反萃取,制得OFL半抗原。
所述的氧氟沙星-血蓝蛋白(OFL-KLH)检测抗原通过混合酸酐偶联方法实现:称取20mg OFL半抗原溶解在2ml DMF中,加入10μL三乙胺,4℃冰浴条件下反应1h。然后加入30μL氯甲酸异丁酯,继续搅拌反应1h。将30mg的KLH溶于2ml碳酸盐缓冲溶液中(CBS,0.05mol/L,pH 9.6),并加入2ml DMF搅拌反应0.5h。冰浴、搅拌条件下将OFL反应产物逐滴加入KLH溶液中,加完后在4℃下振荡反应6h。反应液装入透析袋,CBS缓冲液4℃透析5d,6h换液1次,离心取上清,得OFL-KLH检测抗原,-20℃冻存。
实施例2
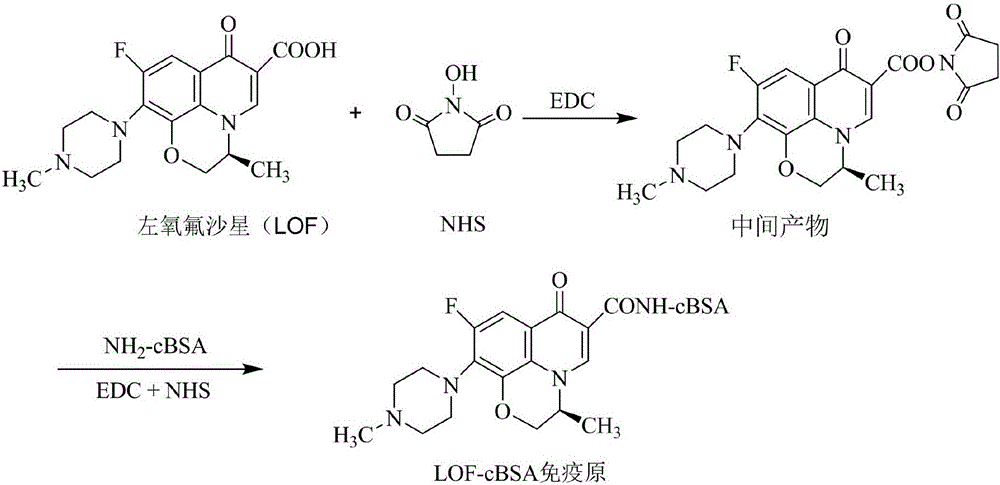
左氧氟沙星(LOF)免疫原的合成;合成反应如附图2所示。
(1)BSA活化:糖基化修饰法,在偏碱性环境中使葡萄糖上的醛基与蛋白质上的羧基偶联,封闭羧基,提高BSA上偶联氨基的数量。具体过程如下:称取66mg牛血清白蛋白(BSA)和1mg葡萄糖溶于PBS缓冲液中,用NaHCO3调节pH值至9.5,40℃摇床反应2h,制得活化的cBSA。
(3)免疫原的合成:采用碳二亚胺两步法合成LOF免疫原。取LOF半抗原19.3mg,用2.3ml N,N-二甲基甲酰胺(DMF)搅拌溶解后,加入N-羟基琥珀酰亚胺(NHS)14.4mg和1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDC.HCl)51.2mg,溶解后室温条件下避光,摇床振荡反应24h,称A液。将活化的cBSA溶解于含50%DMF的PBS磷酸盐缓冲溶液中,称B液。将A液逐滴缓慢加入到B液中,并不断震荡,加完后继续反应3h,获得LOF-cBSA免疫原。反应结束后将反应液装入透析袋,用PBS缓冲液透析6d,每天换液3次。紫外扫描透析液无小分子吸收峰时分装于安瓿瓶中,–20℃保存。
实施例3
抗氧氟沙星单克隆抗体的制备;
1、所述的抗氧氟沙星特异性单克隆抗体由左氧氟沙星-牛血清白蛋白(LOF-cBSA)偶联物免疫Balb/C小鼠制备而来,由以下步骤实现:
(1)小鼠免疫:用LOF-cBSA免疫8-10周龄雌性Balb/C小鼠5只,剂量为60μg/只,体积为0.2ml。首免用PBS稀释的免疫原与等体积FCA完全乳化,以后每隔3w加强免疫一次,换用FIA乳化。免疫5次后断尾采血分离血清,用间接ELISA和间接竞争ELISA(ciELISA)筛选效价高,抑制效果好的小鼠作为融合备用鼠。融合前3d超免小鼠,尾静脉和腹腔各注射60μg免疫原。
(2)细胞融合:融合前4-5d用含有8-氮鸟嘌呤的完全培养基(含15%FBS的RPMI-1640)传代培养NS0细胞;前1d用HAT培养滋养细胞;融合时眶下窦采血,脱颈致死小鼠。无菌取脾脏制备脾细胞,在PEG-1500作用下与NS0细胞融合(细胞数量比约为10:1),将融合后的细胞悬液加入到已铺有滋养细胞的96孔细胞板中,HAT培养。
(3)单克隆细胞株的筛选:融合后10-14d用间接ELISA和ciELISA筛选强阳性、抑制率高、生长状态好的杂交瘤细胞株,用有限稀释法进行3次亚克隆。然后用氟喹诺酮类药物标准品溶液筛选灵敏度高、特异性强的单克隆源细胞株,共取得7株。其中,L2H4D2细胞株灵敏度最高,特异性最强,除与氧氟沙星和左氧氟沙星100%交叉反应外,与其它氟喹诺酮类药物无交叉反应,其抗体特异性结果见表1。
表1 L2H4D2细胞株抗体特异性
(4)单克隆抗体的生产:将L2H4D2细胞株转移到24孔细胞板及50ml细胞瓶中扩大培养。筛选的杂交瘤细胞浓度达到约107/ml时,向10d前经液体石蜡处理过的经产母鼠腹腔内注射单克隆细胞108/只。10~12d后抽取腹水,饱和硫酸胺法纯化抗OFL特异性单克隆抗体,进行胶体金标记。
实施例4
试纸卡灵敏度检测对比实验
利用杂交瘤细胞株L2H4D2分泌的单克隆抗体,进行胶体金标记,同时采用混合酸酐法合成的包被抗原OFL-KLH,以及本实验室EDC法合成的包被抗原OFL-OVA进行对比实验,在PBS缓冲液(0.01mol/L,pH 7.4)中进行试纸卡添加检测实验,两种包被原的试纸卡制备方法和检测条件完全相同。
结果表明:混合酸酐法合成的包被抗原OFL-KLH制备的试纸卡,检测灵敏度为0.06ng/ml,而EDC法合成的包被抗原OFL-OVA制备的试纸卡,检测灵敏度为0.5ng/ml。
实施例5
金标抗体的制备方法
胶体金标记氧氟沙星特异性单克隆抗体(氧氟沙星mAb)制备,由以下步骤实现:
(1)胶体金溶液的制备:取超纯水溶解的0.01%氯金酸溶液100ml,置电炉加热至沸腾,3min后边搅拌,边迅速加入1%的柠檬酸三钠溶液2ml。继续加热,溶液颜色由无色转为浅黄色,最后变为橙红色时停止加热。冷却后用超纯水恢复至原体积,进行透射电镜扫描,鉴定胶体金质量及颗粒大小。胶体金悬液中加入最终质量浓度为0.05%的叠氮钠(NaN3),4℃冰箱中保存备用。
(2)抗体预处理:高浓度的抗体长时间冷冻保存会发生不同程度的聚集,这些聚集物会影响标记的稳定性。因此标记前,将抗氧氟沙星特异性单克隆抗体10000r/min,4℃条件下离心30min,弃沉淀,上清液用0.01mol/L PBS稀释成1mg/ml。
(3)待标mAb实际用量的确定:酶标板用每孔50μl双蒸水铺底,纵排加入倍比稀释的氧氟沙星mAb,每孔50μl,设空白对照(BC)。用0.1mol/L K2CO3调节胶体金溶液至pH 9.0,加入到酶标板中,每孔50μl混匀。室温孵育15min后,加入10%NaCl溶液100μl,混匀,静置。对照孔与mAb量不足以稳定金溶胶的各孔呈现由红变蓝的聚沉现象,而mAb量达到或超过最低稳定量的各孔仍保持红色不变。选择不聚沉时mAb的最低量,在此基础上增加20%,即为待标氧氟沙星mAb的实际用量。
(4)金标抗体的制备:将事先确定的最佳标记氧氟沙星mAb的实际用量与胶体金偶联,常温搅拌30min,5000r/min离心20min,弃上清后,加入10%BSA硼酸钠溶液,使BSA终浓度为1%作为稳定剂。金标抗体溶液10000r/min离心30min,弃上清,用20mmol/L的硼酸盐稀释液(含1%BSA和0.1%叠氮钠)将金标抗体恢复至原体积的1/10,放置在4℃冰箱备用。
实施例6
试纸卡的生产和组装。
硝酸纤维素膜(NC膜)的制备方法,将硝酸纤维素膜置于X-only单向喷点仪平台上,检测抗原放于A池,RaMIgG放于B池,展平压紧,开机后将氧氟沙星-KLH检测抗原和二抗分别点射于硝酸纤维素膜上,形成检测线(T线)和质控线(C线)。室温自然干燥后,将其浸入封闭液(质量浓度为1%的BSA的PBS缓冲液,pH 7.4)中30min,37℃烘干后,加入干燥剂,4℃密封保存。
结合垫的制备方法,将玻璃纤维棉裁成4mm宽的细条,放入含质量浓度为5%的BSA,质量浓度为2%的蔗糖,质量浓度为0.8%的NaCl和质量浓度为0.05%的NaN3的PBS处理液中20min,37℃恒温烘干,然后将金标抗体灌注已处理好的玻璃纤维棉上,真空冻干4h,即为结合垫。
样品垫的制备方法,玻璃纤维棉要用含质量浓度为2%的BSA,质量浓度为1%的蔗糖,质量浓度为0.5%的硼酸钠和质量浓度为0.1%的NaN3的PBS处理后,干燥备用,即为样品垫。
试纸卡的组装,在支持板(PVC板)上,将NC膜、结合垫、样品垫、吸收垫和胶膜等按一定工艺组装在一起,用CM4000切割机制成4mm宽的试纸条。然后,按一定工艺将试纸条封装于带有加样孔和观察窗的特制的塑料盒体中,即为本发明的氧氟沙星特异性免疫学检测试纸卡,试纸卡的图片见附图3~5,其中1为卡壳,2为检测区,3为底板,4为样品垫,5为金标垫,6为硝酸纤维素膜,7为吸水垫,8为点样孔,9为观察窗,10为质控线(C线),11为检测线(T线),12为胶膜,13为标记线。
实施例7
本发明的氧氟沙星特异性免疫学检测试纸卡样品前处理过程:
(1)牛奶样品:采集新鲜牛奶2ml放于10ml离心管中,以1000r/min离心10min,拨去上层脂肪层,吸取上层清液,用PBS稀释10倍后,直接上样检测。
(2)鸡蛋样品:去除蛋壳,取蛋液2g于10ml离心管中,加入配制好的PBS缓冲液(pH 7.4)与甲醇的混合液(V:V=1:1)充分匀浆,涡旋1min,后振荡10min,以5000r/min离心10min,取上清液于洁净离心管中,置于4度冰箱中保存,备检。
(3)鸡肉样品:将鸡肉组织样品切碎、研磨后称取5g样本于20ml离心管中,再加入乙腈5ml,于旋涡仪涡动10min,6000r/min离心5min;取1ml上清液,加入4ml的样品稀释液振荡摇匀1min;取100ml用于样品分析。
将处理后的样品溶液用滴管滴入试纸卡加样孔内3-4滴,3-5min即可观察结果。
试纸卡以红色印迹线“|”或“‖”作为检测线的阳性和阴性标记,即在硝酸纤维素膜上质控线(C线)显示一条红色“|”印迹时,表示被检测样品溶液呈阳性;若硝酸纤维素膜上质控线(C线)和检测线(T线)同时出现两条红色“‖”印迹时,表示样品溶液呈阴性。样品的浓度为0.06ng/ml时,检测线隐约出线。
由以上实施例可知,本发明提供的试纸卡,通过制备具有强免疫性的免疫原免疫动物筛选得到具有高亲和力的抗氧氟沙星特异性单克隆抗体,所述单克隆抗体与包被原制备而成。因此,快速检测试纸卡灵敏度高、特异性强,其检测限可达0.06ng/ml。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!