一种基于数字PCR平台的miRNA‑21的检测试剂盒及其应用的制作方法
本发明属于生物
技术领域:
,具体涉及一种基于数字PCR平台的miRNA-21的检测试剂盒及其应用。
背景技术:
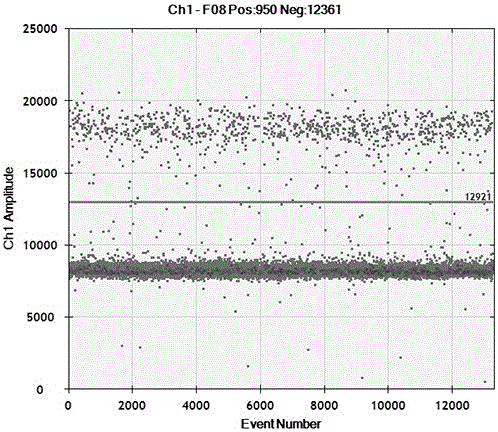
:MicroRNA(miRNA)是真核生物中广泛存在的一种长约22个核苷酸的非编码小RNA分子,其对细胞发育、分化、增殖和凋亡至关重要,调控并影响了整个生命活动的过程。近几年的研究表明,miRNA可作为新一代的肿瘤标志物,在癌症诊断、预后中具有重要的应用前景和意义。大量研究已证实,miRNA-21-5p(miRNA-21)可用作一种肿瘤标志物,在乳腺癌、肝癌、肺癌、结肠癌、胃癌、前列腺癌、胰腺癌、神经胶质瘤等多种癌症组织中上调表达。并且在肝癌、肺癌、结肠癌、胃癌等等癌症病人的血清或血浆样本中,也可检测出游离miRNA-21的明显上调表达,因此其对于肿瘤的早期诊断和预后具有重要的意义。由于在人体例如血浆、血清、尿液等体液中的miRNA分子含量普遍较低,需要一种非常灵敏和特异的检测方法。微滴式数字PCR(DropletDigitalTMPCR)被称为第三代PCR技术,由于其在微量检测技术上的重大创新和突破,目前已成为液体活检中认知度最高的技术手段,相比目前传统常用的荧光定量PCR方法更加灵敏和准确。但是目前还没有一种方便快捷的基于数字PCR平台的miRNA-21检测的试剂盒。技术实现要素:本发明的目的在于克服现有技术的缺点,提供一种基于数字PCR平台的miRNA-21的检测试剂盒及其应用。本发明的目的通过以下技术方案来实现:一种基于数字PCR平台的miRNA-21的检测试剂盒,包括检测miRNA-21的反转录引物、检测引物、质控品反转录引物和检测质控品引物;其中,所述反转录引物的核苷酸序列如SEQIDNO.1所示,具体为:5’-GTCGTATCCAGTGCGAGCCGTTGAGACCGCAAGTGCACTGGATACGACTCAACATC-3’;所述检测引物的上游引物核苷酸序列如SEQIDNO.2所示,具体为:5’-GCCGCTAGCTTATCAGACTGAT-3’,检测引物的下游引物核苷酸序列如SEQIDNO.3所示,具体为:5’-ATCCAGTGCGAGCCGTTG-3’;所述质控品反转录引物的核苷酸序列如SEQIDNO.4所示,具体为:5’-GTCGTATCCAGTGCGAGCCGTTGAGACCGCAAGTGCACTGGATACGACCAAGCTGA-3’;所述检测质控品引物的上游引物核苷酸序列如SEQIDNO.5所示,具体为:5’-GCCGTCACCGGGTGTAAAT-3’,检测质控品引物的下游引物核苷酸序列如SEQIDNO.6所示,具体为:5’-ATCCAGTGCGAGCCGTTG-3’。作为优选方案,所述试剂盒由反转录缓冲液、反转录酶、PCR缓冲液、超纯水、阳性对照品、质控品、质控品反转录缓冲液和质控品PCR缓冲液组成;其中,所述反转录缓冲液包括dNTPs、RTBuffer、RNaseinhibitor、反转录引物和超纯水;所述PCR缓冲液包括PCRBuffer、检测引物和超纯水;所述阳性对照品为合成的人源miRNA-21序列;所述质控品为合成的线虫来源的cel-miRNA-39;所述质控品反转录缓冲液包括dNTPs、RTBuffer、RNaseinhibitor、质控品反转录引物和超纯水;所述质控品PCR缓冲液包括PCRBuffer、检测质控品引物和超纯水。作为优选方案,所述阳性对照品的核苷酸序列如SEQIDNO.7所示,具体为:5’-UAGCUUAUCAGACUGAUGUUGA-3’。作为优选方案,所述质控品的核苷酸序列如SEQIDNO.8所示,具体为:5’-UCACCGGGUGUAAAUCAGCUUG-3’。上述的试剂盒在基于数字PCR平台检测miRNA-21中的应用。本发明具有以下优点:本发明试剂盒提供的反转录缓冲液和PCR缓冲液不但在组分上进行了优化有利于长期稳定保存,同时可将加样工作量简化至最小,以减少加样时可能出现的失误或误差,有利于得到稳定可靠的检测结果;本发明试剂盒选择用人血清或血浆为样本,保存方便,检测非侵入性,可减少病人痛苦;本发明试剂盒基于数字PCR平台,在检测血清或血浆中微量核酸时,灵敏度和准确性要高于目前其他技术平台。附图说明图1为本发明试剂盒检测待测样品血浆中miRNA-21含量的数字PCR结果图;图2为本发明试剂盒检测质控品中miRNA-21含量的数字PCR结果图;图3为本发明试剂盒检测阳性对照组中miRNA-21含量的数字PCR结果图;图4为本发明试剂盒检测阴性对照组中miRNA-21含量的数字PCR结果图。具体实施方式下面结合附图及实施例对本发明做进一步的描述,本发明的保护范围不局限于以下所述。实施例1:一种基于数字PCR平台的miRNA-21的检测试剂盒所述试剂盒由9ul的反转录缓冲液、2ul的反转录酶、17ul的PCR缓冲液、20ul超纯水、2ul阳性对照品、10ul质控品、9ul的质控品反转录缓冲液和17ul的质控品PCR缓冲液组成;其中,所述反转录缓冲液包括100mMdNTPs(withdTTP)0.15ul、10×RTBuffer1.5ul、10mg/mlRNaseinhibitor0.2ul、10uM反转录引物1ul和超纯水6.15ul;2ul的反转录酶为分装自ABI公司的MultiScribeTMReverseTranscriptase,50U/μL;反转录引物的核苷酸序列如SEQIDNO.1所示,具体为:5’-GTCGTATCCAGTGCGAGCCGTTGAGACCGCAAGTGCACTGGATACGACTCAACATC-3’;所述PCR缓冲液包括2×PCRBuffer10ul(分装自Bio-rad公司的ddPCRTMEvaGreenSupermix)、检测引物和超纯水6ul,所述检测引物包括10uM检测上游引物0.5ul和10uM检测下游引物0.5ul;所述检测引物的上游引物核苷酸序列如SEQIDNO.2所示,具体为:5’-GCCGCTAGCTTATCAGACTGAT-3’,检测引物的下游引物核苷酸序列如SEQIDNO.3所示,具体为:5’-ATCCAGTGCGAGCCGTTG-3’;所述阳性对照品为合成的人源104copies/ulmiRNA-21序列;所述阳性对照品的核苷酸序列如SEQIDNO.7所示,具体为:5’-UAGCUUAUCAGACUGAUGUUGA-3’;所述质控品为合成的线虫来源4×104copies/ul的cel-miRNA-39,所述质控品的核苷酸序列如SEQIDNO.8所示,具体为:5’-UCACCGGGUGUAAAUCAGCUUG-3’;所述质控品反转录缓冲液包括100mMdNTPs(withdTTP)0.15ul、10×RTBuffer1.5ul、10mg/mlRNaseinhibitor0.2ul、10uM质控品反转录引物1ul和超纯水6.15ul;所述质控品PCR缓冲液包括2×PCRBuffer10ul(分装自Bio-rad公司的ddPCRTMEvaGreenSupermix)、检测质控品引物和超纯水6ul,所述检测质控品引物包括10uM检测质控品上游引物0.5ul和10uM检测质控品下游引物0.5ul,所述检测质控品引物的上游引物核苷酸序列如SEQIDNO.5所示,具体为:5’-GCCGTCACCGGGTGTAAAT-3’,检测质控品引物的下游引物核苷酸序列如SEQIDNO.6所示,具体为:5’-ATCCAGTGCGAGCCGTTG-3’。实施例2:检测健康人血浆中的miRNA-21的表达水平1、样本采集及处理使用Streck无创采血管采集健康人血液5ml一份。将血液转移至新的15ml离心管中,4℃2000g离心10min,吸取上层血浆至一新的15ml离心管中。再将血浆4℃4000g离心20min,吸取上层血浆至一新的15ml离心管中。吸取200ul上层血浆使用QIAGEN的miRNeasySerum/PlasmaKit按照操作说明书进行总RNA的提取,注意在提取过程时,样品经QIAzolLysisReagent处理后,加入本发明试剂盒提供的10ul质控品,最后提取得到40ul的总RNA样品。其中,质控品的使用方法为:在使用试剂盒提取待测血浆或血清样本总RNA(包括总microRNA)时,在加入裂解液类试剂裂解样品后,加入本试剂盒提供的10ul质控品,随后完成后续的提取步骤。检测质控品时的反转录和PCR步骤分别使用本试剂盒提供的质控品反转录缓冲液和质控品PCR缓冲液,反应体系和反应条件与普通待测样本一致。待所有反应完成后,用Bio-Rad的QX200TM微滴式数字PCR仪进行结果读取。质控品检测结果计算:假设提取后总RNA样品体积为BμL,Bio-radQX200数字PCR检测结果为Ccopies/μL,则质控品的浓度(Xcopies/μL)按以下公式进行计算:公式:X拷贝数/μL=(C×20×15/3×B/2)/A=(60×B×C)/A实验有效性要求:质控品检测结果应满足:3×104~4×104copies/ul,否则实验无效。2、实验检测将提取的总RNA样品进行反转录和PCR实验操作后,反转录的反应体系如表1所示,反应条件如表2所示,PCR实验操作miRNA-21检测反应体系如表3所示,miRNA-21检测反应条件如表4所示,待所有反应完成后,使用Bio-radQX200TM微滴式数字PCR仪进行结果读取。包括有待测样本,如图1所示,质控品,如图2所示,阳性对照组,如图3所示,和阴性对照组,如图4所示。其中,阳性对照和阴性对照的使用方法为:在使用本试剂盒检测待测样本时,也使用本试剂盒提供的阳性对照品和超纯水来分别用作实验的阳性对照和阴性对照,进行反转录和PCR反应。除了反转录体系中加入的RNA样品替换为2ul的阳性对照品或超纯水,其余反应体系和反应条件与待测样本一致。待所有反应完成后,用Bio-Rad的QX200TM微滴式数字PCR仪进行结果读取。实验有效性要求:1.阳性对照读取结果应满足:180~200copies/ul,否则实验无效。2.阴性对照读取结果应满足:0copies/ul,否则实验无效。表1:miRNA-21反转录反应体系成分体积反转录缓冲液9ul反转录酶1ulRNA样品(总量5~50ng)2ul超纯水3ul共计15ul表2:miRNA-21反转录反应条件步骤时间温度130min16℃230min42℃35min85℃4Forever4℃表3:miRNA-21检测反应体系成分体积PCR缓冲液17ul反转录样品3ul共计20ul表4:miRNA-21检测反应条件3、实验结果每组反应最终检测的微滴数在14000~22000之间,均大于10000,表示结果有效可靠。检测结果显示A组miRNA-21浓度为22.2copies/ul,B组为159copies/ul,C组为192copies/ul,D组为0copies/ul。经计算,待测健康人血浆样本中miRNA-21的原浓度为(60×40×22.2)/200=226.4copies/ul,质控品的浓度为5×40×159=3.18×104copies/ul,且阳性对照和阴性对照的直接检测结果符合本试剂盒要求,因此本次检测有效。SEQUENCELISTING<110>成都仕康美生物科技有限公司<120>一种基于数字PCR平台的miRNA-21的检测试剂盒及其应用<130>2016<160>8<170>PatentInversion3.5<210>1<211>56<212>DNA<213>人工序列<400>1gtcgtatccagtgcgagccgttgagaccgcaagtgcactggatacgactcaacatc56<210>2<211>22<212>DNA<213>人工序列<400>2gccgctagcttatcagactgat22<210>3<211>18<212>DNA<213>人工序列<400>3atccagtgcgagccgttg18<210>4<211>56<212>DNA<213>人工序列<400>4gtcgtatccagtgcgagccgttgagaccgcaagtgcactggatacgaccaagctga56<210>5<211>19<212>DNA<213>人工序列<400>5gccgtcaccgggtgtaaat19<210>6<211>18<212>DNA<213>人工序列<400>6atccagtgcgagccgttg18<210>7<211>22<212>RNA<213>人工序列<400>7uagcuuaucagacugauguuga22<210>8<211>22<212>RNA<213>人工序列<400>8ucaccggguguaaaucagcuug22当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1