一株鼠抗猪PD‑1单克隆抗体及其应用的制作方法
本发明涉及一株鼠抗猪pd-1单克隆抗体及其应用,属于抗体工程技术领域。
背景技术:
程序性死亡因子-1(programmeddeath-1,pd-1)属于b7家族成员,它是50kda~55kda左右的i型跨膜蛋白分子,诱导性表达于活化的t细胞、b细胞、nk细胞、nkt细胞、单核细胞和树突状细胞。现已发现,pd-1有pd-l1和pd-l2两个配体。pd-l1广泛表达于t细胞、b细胞、树突状细胞、巨噬细胞、血管内皮细胞以及多种肿瘤细胞。pd-l2则诱导性表达于树突状细胞、巨噬细胞、髓源性肥大细胞和生发中心b细胞。pd-1/pd-l是一对重要的负性协同刺激分子,pd-1所介导的负性协同刺激信号能导致t细胞的凋亡和功能耗竭,在t细胞成熟过程的阴性和阳性选择中发挥重要作用。近年来研究表明,pd-1/pd-l抑制途径在自身免疫性疾病的发生发展以及慢性病毒感染中均发挥了重要作用。采用阻断型抗体干预pd-1/pd-l信号可有效提高机体抗慢性病毒感染免疫力;相反,可通过增强pd-1负性信号来缓解自身免疫反应和抑制器官移植排斥反应。因此,制备鼠抗猪pd-1单克隆抗体具有重要的理论研究和实际应用价值。
技术实现要素:
为了解决上述问题,本发明的目的是提供一株鼠抗猪pd-1单克隆抗体及其应用,该单克隆抗体能够和猪pd-1蛋白特异性结合。
为了实现上述目的,本发明所采用的技术方案是:
一株鼠抗猪pd-1单克隆抗体,所述的单克隆抗体由保藏编号为cctccno:c2016196的杂交瘤细胞株2b5分泌,所述的杂交瘤细胞株2b5保藏于中国典型培养物保藏中心,保藏地址为中国武汉武汉大学,保藏日期为2016年11月30日。
所述的单克隆抗体为lgg1类免疫球蛋白。
一种所述的鼠抗猪pd-1单克隆抗体在制备检测猪pd-1蛋白试剂中的应用。
所述的单克隆抗体在制备猪pd-1蛋白诊断试剂或辅助诊断试剂中的应用。
所述的诊断试剂包括免疫组织化学检测试剂或血清免疫检测试剂。
所述的血清免疫检测试剂为酶联免疫吸附检测试剂。
一种包含所述的单克隆抗体的药物组合物。
本发明的有益效果:
本发明以诱导表达纯化后的猪pd-1胞外区蛋白为免疫原,有效地激发小鼠机体对靶分子的特异性免疫应答。运用elisa方法对杂交瘤进行筛选,筛选出的上清液为阳性的生长孔内常会有两个以上的杂交瘤细胞集落,有的集落可能不分泌抗体,或分泌的不是所需抗体,因此,要利用克隆培养方法及时将其分开。最常用的杂交瘤克隆培养法是有限稀释法和软琼脂培养法。本发明中,采用有限稀释法对杂交瘤细胞进行克隆培养,最终获得1株可稳定分泌鼠抗猪pd-1的单克隆抗体的杂交瘤细胞株,其单抗为igg1类免疫球蛋白,非其他亚型;且该株单抗具有良好的效价。通过elisa试验鉴定,结果呈阳性反应,初步证明该株单抗是抗pd-1胞外区蛋白的,再用交叉试验证明该株单抗与pet32a载体蛋白和无关蛋白无交叉反应,进一步证明所筛出的杂交瘤是特异的,用western-blot鉴定阳性杂交瘤分泌单克隆抗体与重组蛋白发生特异性反应,最后用流式细胞术检测证实杂交瘤分泌单克隆抗体可以与外周血单核细胞(pbmc)上pd-1蛋白有效结合。
本发明成功研制了特异性鼠抗猪pd-1单克隆抗体,并对mab的免疫学特性进行初步分析。该mab的获得为进一步从蛋白水平检测疾病状态下pd-1分子的表达变化奠定了基础。
附图说明
图1为western-blot试验鉴定单克隆抗体的特异性结果,图中,m:marker;1:pd-1蛋白;2:rosetta上清;3:pet-32a(+)空载体蛋白。
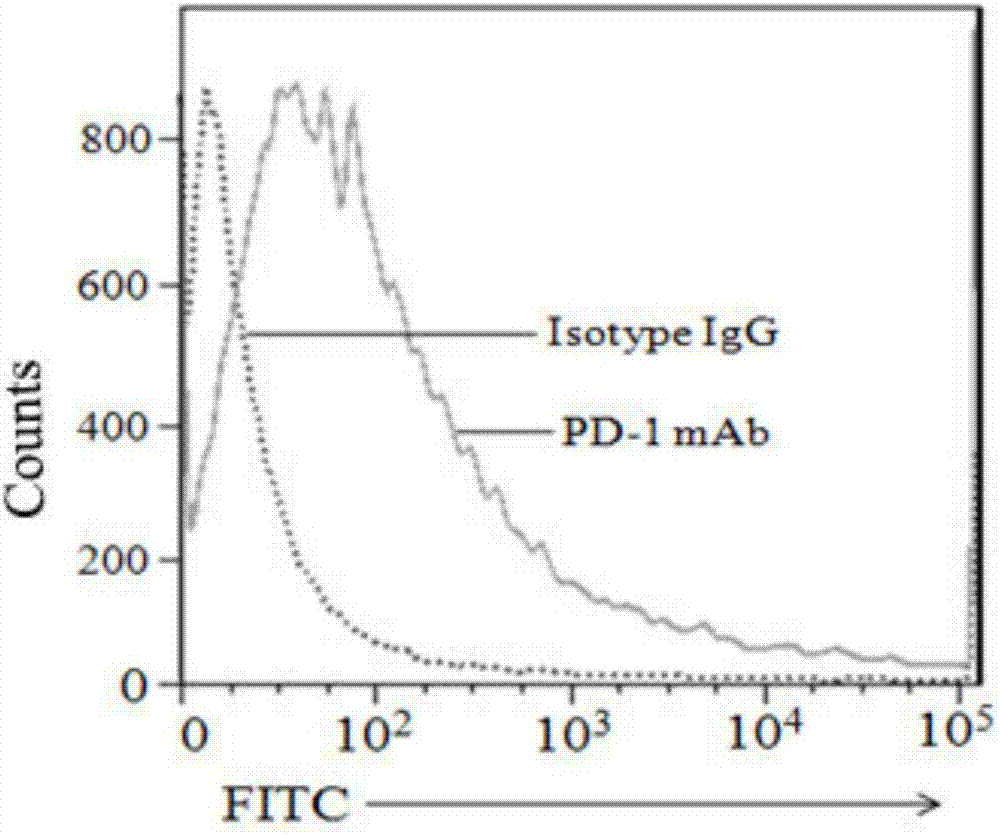
图2为流式细胞术检测单抗与猪pbmc上pd-1蛋白的结合情况。
具体实施方式
以下结合具体实施例来进一步说明发明内容,没有特殊说明的情况下,所采用的操作手段、验证方法等都是本领域技术人员的常规技术手段,具体可参考《分子克隆实验指南》及其它常规实验方法。本发明只是突出了技术方案的创新点,故现有技术不在此做进一步的说明。
实验材料
小鼠骨髓瘤细胞ns0由本实验室冻存;6~8周龄balb/c小鼠购自上海斯莱克实验动物有限公司,在本实验室动物房饲养。1640培养基、hat和ht培养基购自美国gibco公司;胎牛血清购自杭州四季青生物有限公司;弗氏完全佐剂、弗氏不完全佐剂和可溶性单组分tmb底物溶液购自美国sigma公司;聚乙二醇(peg)1500购自美国roche公司;hrp标记羊抗鼠igg购自美国invitrogen公司;tween-20购自广州鼎国生物技术有限公司;鼠igg亚型鉴定试剂盒购自美国roche公司;细胞培养板、细胞冻存管购自上海微科生化试剂有限公司;其它试剂均为国产分析纯试剂。
gnk溶液:称取kcl0.4g、nacl8g、na2hpo4·12h2o3.56g、nah2po4·h2o0.69g、酚红0.01g、葡萄糖2g,加双蒸水(ddw)定容至1000ml,调节ph值至7.2,115℃高压灭菌,4℃保存备用。
实施例1鼠抗猪pd-1单抗的制备
1、免疫原的制备
根据genbank中猪pd-1的基因序列及原核表达载体多克隆酶切位点,设计其胞外区引物,以猪外周血单个核细胞(pbmc)的cdna为模板,应用pcr技术扩增pd-1胞外区片段,并与pmd18-t-simple载体连接,构建pmd-pd-1重组质粒,转化至dh5α中通过菌液pcr筛选阳性克隆并测序,利用限制性内切酶ecori和xhoi分别对阳性重组质粒pmd-pd-1及原核表达载体pet-32a(+)进行双酶切并回收,利用t4dna连接酶连接回收的酶切目的片段及载体片段,构建pet-32a-pd-1原核表达载体,连接产物转化至dh5α中,经鉴定正确后转化至宿主菌rosetta(de3)进行诱导表达。应用sds-page分析重组蛋白的表达情况,western-blot鉴定重组蛋白的抗原特异性。然后采用镍柱对重组目的蛋白进行分离纯化,用纯化的蛋白加入等体积的完全弗氏佐剂或不完全弗氏佐剂,在匀浆机上进行乳化,分别制成完全佐剂抗原和不完全佐剂抗原。其中,涉及的具体步骤有:
1.1含有pet-32a-pd-1原核表达载体的宿主菌rosetta(de3)的诱导表达
将含有重组表达质粒pet-32a-pd-1的菌种rosetta(de3)于含amp(100μg/ml)lb液体培养基中,37℃过夜扩大培养。取上述培养菌按体积比1:100接种于新鲜的相应的2×yt培养液,37℃培养至od600值为0.5,加入iptg至终浓度为0.5mmol/l,以诱导目的蛋白的表达,于37℃继续培养4h,将诱导的产物5000rpm、4℃离心10min后,收集菌体,按体积比1:20加pbs重悬菌体,加入溶菌酶至终浓度为100μg/ml,30℃水浴30min;超声破碎15min,8000rpm、4℃离心20min后收集沉淀,用适量2m尿素洗涤液重悬放冰上10min,8000rpm、4℃离心20min,重复洗4-5次,最后用8m尿素溶解包涵体,8000rpm、4℃离心20min,收集上清置-80℃保存备用。
表达产物的sds-page分析:12%分离胶(质量分数),约15.0ml,各组分见表1。将各组分混合均匀后,将分离胶溶液立即加入已安装好的玻璃制胶平板中,至距离玻璃板顶端约1.5cm,然后在分离胶溶液上轻轻覆盖约1.0cm的水层,以防止空气中的氧气对凝胶聚合的抑制作用。室温静置约30min,待凝胶聚合完全后,倒掉覆盖的水层,用水冲洗凝胶上部几次后用滤纸尽可能吸干凝胶顶端的水。
表112%分离胶的配制
配制5%浓缩胶(质量分数),约6.1ml,各组分见表2。将各组分混合均匀后,将浓缩胶溶液立即加入至玻璃板内,液面与玻板上沿齐平,立即将梳子轻轻插入玻板之间,尽可能避免产生气泡。约30min浓缩胶聚合完全后,小心拔出梳子。加入适量1×tris-gly电泳缓冲液,上样前用电泳缓冲液冲洗梳子孔,小心加入处理后的样品。浓缩胶阶段电压为80v,待溴酚蓝进入分离胶时升电压至120v,直至溴酚蓝前沿迁移至凝胶底部。电泳完毕后,小心剥离凝胶,加入适量的考马斯亮蓝r-250染色液缓慢振摇染色2h,取出凝胶在水中漂洗数次,再用考马斯亮蓝脱色液脱色3h,其间需更换脱色3次。待蛋白条带清晰后,观察结果,用凝胶成像系统拍照并保存。结果显示,表达产物的相对分子质量为33kda,与预期重组蛋白的相对分子质量一致。
表25%浓缩胶的配制
表达产物的western-blot分析:目的蛋白经sds-page电泳后,切下需要转膜的部分。分别将凝胶、海绵垫和pvdf膜(在甲醇浸泡1~2min)预先在电转移缓冲液中平衡30~60min。然后按照从上到下依次为海绵垫、凝胶、pvdf膜、海绵垫的顺序依次放好,特别是在把凝胶放到pvdf膜上时要尽量避免气泡的产生,最后用手轻轻压紧排除各层之间的气泡,以消除气泡的产生。放好半干转移器上盖,连接至电泳仪,正负极依次接好,在25v条件下转膜30~45min。将电转移结束后的凝胶放入考马斯亮蓝r-250染色液中染色,以检查转移效果。
转移完毕后取下pvdf膜,进行如下操作:
封闭:将pvdf膜放入大小适当的玻璃平皿中,并做好标记,然后用tbst洗涤,用质量分数5%脱脂奶粉-tbst室温封闭过夜;
洗膜i:弃去封闭液,用tbst慢摇洗膜三次,每次5min~10min;
加一抗:将6×his单克隆抗体(工作浓度2μg/ml)和羊抗人pd-1单克隆抗体(工作浓度0.4μg/ml)分别用1%脱脂奶粉-tbst稀释后加入,37℃慢摇2h;
洗膜ⅱ:弃去一抗,用tbst慢摇洗膜三次,每次5min~10min;
加二抗:将辣根过氧化物酶标记羊抗鼠(二抗)用1%脱脂奶粉-tbst稀释(1:1000)后加入,37℃缓慢振摇60min;
洗膜ⅲ:弃去二抗,用tbst缓慢振摇洗膜三次,每次5min~10min;
显色:参照aec显色试剂盒中的说明书配制显色液,将pvdf膜置于显色液中,待出现特异性反应条带后,立即用双蒸水冲洗以终止反应,拍照记录结果。
western-blot结果显示,该重组蛋白能与6×his单克隆抗体和羊抗人pd-1抗体所识别,证明pd-1胞外区基因片段在原核表达系统中获得正确表达,且具有良好的反应原性。
1.2pet-32a-pd-1重组目的蛋白的纯化
依照proteinpure-ni-ntaresin亲和柱的操作手册,进行蛋白纯化,具体步骤如下:
平衡:用5~10倍体积的平衡缓冲液平衡层析柱。对于结合能力强的his标签重组蛋白或提高其特异性结合,平衡液中可加入低浓度咪唑(10mm~20mm)。
上样:样品缓冲液应尽可能与平衡缓冲液一致。为了避免堵塞层析柱样品已提前过滤或离心。
洗涤:用5~10倍柱体积的平衡缓冲液洗涤层析柱,收集流出液。
洗脱:可采不同浓度的咪唑洗脱目的蛋白。
然后对收集洗脱的目的蛋白进行sds-page鉴定后,使用梯度透析法对鉴定的纯化蛋白进行浓缩和脱盐,具体步骤为:于处理好的透析袋中加入适当的含目的蛋白的洗脱液,用夹子夹好后依次放入8mol/l、6mol/l、4mol/l、2mol/l、1mol/l、0.5mol/l的尿素溶液中,每个梯度4℃透析3h,最后透析到pbs溶液中。经硅胶适当浓缩后,收集重组目的蛋白溶液并测量目的蛋白的浓度。
2、动物免疫
选择3只6周龄左右的雌性balb/c小鼠,采用颈背部皮下多点注射法进行免疫,50μg/只,每只200μl的剂量。用弗氏完全佐剂乳化的抗原进行首次免疫,皮下多点注射;然后用弗氏不完全佐剂乳化的抗原分别进行二次免疫和三次免疫,每次间隔14d,三次免疫10天后,用间接elisa测抗体效价,当抗体效价达到1:1600后即可进行融合,细胞融合前3~5d进行加强免疫,尾静脉或腹腔注射25μg不加佐剂的抗原。
结果显示,首次免疫后3只balb/c鼠的血清抗体效价分别为3.2×103、3.2×103和6.4×103;三次免疫后效价分别为2.56×104、2.56×104和5.12×104(见表3)。
表3免疫balb/c鼠的血清效价
3、ns0骨髓瘤细胞的复苏与培养
在融合前一周,复苏骨髓瘤细胞ns0,置于37℃,5%co2培养箱中培养过夜,次日换液。融合当天,用吸管轻轻吹取处于对数生长期的ns0细胞,收集至离心管中,1000r/min离心10min,弃去上清液,用gnk溶液洗涤一次后将细胞重新悬浮,细胞计数,调整细胞密度为106个/ml,放培养箱中备用。
4、饲养细胞的制备
融合前1d制备饲养细胞。取昆明鼠1只致死,75%酒精消毒体表,无菌手术剪刀打开小鼠的腹部皮肤,暴露腹膜。然后用5ml注射器将5ml预冷的hat培养基打入小鼠腹腔,轻轻压挤腹部,重新吸出注入的液体,收取小鼠腹腔巨噬细胞。用hat培养基稀释至40ml,100μl/孔添加到4块96孔细胞培养板中,置37℃、5%co2培养箱中培养。
5、细胞融合
在40℃水浴中预热gnk溶液、50%(质量分数)peg溶液;用于融合的小鼠采血并分离血清,然后致死浸泡到酒精中;收集ns0细胞于50ml离心管中,1000r/min离心10min,弃上清,用gnk溶液洗一次;依次剪开小鼠皮肤、腹膜,暴露腹腔,取脾脏放置于尼龙纱布上研碎,并用gnk溶液洗下去,收集脾细胞于50ml离心管中,1000r/min离心10min,弃上清;将脾细胞与ns0骨髓瘤细胞混合于50ml离心管中(脾细胞数约为2.6×108个,所用ns0细胞大约是3瓶80%的10mlns0细胞,脾细胞:ns0细胞个数约为10:1),加gnk溶液至40ml,1000r/min离心10min,弃上清,打散细胞团;将此融合管移入40℃水浴中,用1ml吸管将预热的50%peg(ph8.0)滴加到融合管中,边加边轻轻摇动融合管,1min内加完,并继续在水浴中缓缓摇动融合管1.5min。立即缓慢滴加40℃预热的gnk溶液15ml。加入步骤为:1ml/30s,3ml/30s,11ml/30s。然后慢慢补加gnk溶液至40ml,37℃水浴静置5min,1000r/min离心10min,弃上清。打散细胞团,加40mlhat培养基吹打混匀,加到含饲养细胞的96孔细胞培养板上,每孔100μl,置37℃5%co2培养箱中培养。
6、融合细胞的培养
融合后的细胞置于co2培养箱中培养,次日检查有无污染,如发现污染立即滴加1%的naoh。一般3~4d可见小克隆;7d时于出现克隆的孔内半量换液;10d左右可以吸取少量上清用于筛选,并补加等量的hat培养基;14d左右对所筛选的阳性孔可半量更换ht培养基,同时对筛选阳性孔的细胞转至24孔培养板中扩大培养,准备克隆化,在筛选过程中将hat培养基逐渐更换为1640完全培养基。
7、阳性杂交瘤细胞的筛选
用5μg/ml纯化重组pd-1胞外区蛋白包板,50μl/孔,通过间接elisa对融合的杂交瘤细胞培养上清液进行初次筛选,对筛选的强阳性克隆孔进行第二次特异性筛选,用载体蛋白、正常大肠杆菌上清以及其它无关蛋白进行包板检测,其检测方法与第一次相同,同时设立对照组,对筛选的特异性较强的阳性孔转至24孔培养板中扩大培养,准备克隆化。
具体筛选步骤如下:用5μg/ml的蛋白包被,50μl/孔,4℃包被过夜,次日用pbst洗板,然后用5%脱脂牛奶(pbst溶解)于37℃封闭2h,弃上清,用封闭液1:1稀释待检测克隆孔上清(一抗),每孔50μl为宜。同时做阳性、阴性对照、空白对照和无克隆孔上清对照,37℃孵育30min,弃上清,pbst洗涤5次,加二抗,二抗1:1000倍稀释,50μl/孔,37℃孵育30min,弃上清,用pbst洗5次,然后加入tmb显色剂,显色5~10min,测od450值。
8、阳性杂交瘤细胞的克隆
当阳性克隆的细胞孔长至80%时进行有限稀释,有限稀释前一天制备饲养细胞。取出少许细胞悬液进行计数,采用有限稀释法对阳性孔的细胞进行克隆化。其步骤如下:
用10μl台盼蓝和10μl细胞悬液于pcr管中等比例混合后,在显微镜下进行活细胞计数,公式:细胞数/ml=n/4×103×10×稀释倍数(n为显微镜下四角4个大方格的活细胞总数),计算每毫升细胞悬液所含的活细胞数,然后取适量的细胞悬液,用1640培养基稀释到10ml,并且要含有2×103个活细胞(稀释度i),用稀释度i的细胞悬液铺板半块96孔板,100μl/孔,20个细胞/孔;取1ml稀释度i的细胞悬液加9ml1640完全培养基(稀释度ⅱ),用稀释度ⅱ的细胞悬液铺板另半块96孔板,100μl/孔,2个细胞/孔;取3ml稀释度ⅱ的细胞悬液加7ml1640完全培养基(稀释度ⅲ),用稀释度ⅲ的细胞悬液铺一块96孔板,100μl/孔,0.6个细胞/孔;将上述培养板置于co2培养箱中培养,培养7d后,对单克隆孔进行标记并半量换液,当单克隆长至孔底的1/10时,进行效价检测和特异性检测,筛选出特异性较高和阳性较强的细胞进行重复克隆;同时每次将克隆剩余细胞转入24孔细胞培养板培养(并在原孔中补加另一批培养基,以防二者同时污染或细胞死亡),继而转入6孔板或细胞中进行扩大培养,并及时冻存;经过多次克隆操作,直至所有克隆的细胞孔检测阳性率为100%时,即可确定已获得分泌单克隆抗体的杂交瘤细胞株;获得稳定分泌抗体的杂交瘤细胞株后,及时进行扩大培养并冻存。
9、腹水的制备、纯化
将8~12周龄雌性balb/c小鼠腹腔注射0.5ml液体石蜡致敏。7d后腹腔注射杂交瘤细胞,细胞注射量为5×106个/只,接种细胞后每天观察小鼠腹部,待小鼠腹部明显膨大,用无菌注射器吸出腹水,3000r/min离心20min,取上清分装、标记,-20℃保存备用。应用igg类单克隆抗体纯化试剂盒提取纯化单抗,按照北京百奥莱博科技有限公司提供的该纯化试剂盒使用说明书步骤操作。
实施例2鼠抗猪pd-1单抗特异性鉴定
1、间接elisa鉴定单克隆抗体的特异性
经3次亚克隆,获得1株分泌特异性单抗的杂交瘤细胞,杂交瘤细胞株命名为2b5。分别用获得的猪pd-1蛋白、鸡pd-1蛋白、rosetta(de3)上清与pet-32a(+)空载体蛋白(包被浓度均为5μg/ml)包被酶标板,50μl/孔。加入待检单抗上清,50μl/孔(1:200稀释),37℃孵育30min,pbst洗板3次。加入1∶1000倍稀释的hrp标记的山羊抗鼠igg二抗50μl,置于37℃温箱孵育30min,pbst洗涤3次,加入50μltmb显色液,作用5-10min,用2mol/lh2so4终止反应,读取各检测孔od450数值,各孔od450值以p/n>2.1为阳性判定标准(结果见表4)。结果表明,该株单抗能与重组猪pd-1蛋白反应而不与pet32a(+)空载体蛋白和无关蛋白反应,具有良好的特异性
表4单抗特异性鉴定结果
2、western-blot试验鉴定单克隆抗体的特异性
重组pd-1胞外区目的蛋白经sds-page电泳后,切下需要转膜的部分。分别将凝胶、海绵垫和pvdf膜(在甲醇浸泡1~2min)预先在电转移缓冲液中平衡30~60min。然后按照从上到下依次为海绵垫、凝胶、pvdf膜、海绵垫的顺序依次放好,特别是在把凝胶放到pvdf膜上时要尽量避免气泡的产生,最后用手轻轻压紧排除各层之间的气泡,以消除气泡的产生。放好半干转移器上盖,连接至电泳仪,正负极依次接好,在25v条件下转膜30~45min。当电转移结束后的凝胶放入考马斯亮蓝r-250染色液中染色,以检查转移效果。
转移完毕后取下pvdf膜,将pvdf膜用tbst洗涤,用5%脱脂奶粉-tbst室温封闭过夜;弃去封闭液,用tbst慢摇洗膜三次,每次5~10min;加入一抗:将杂交瘤细胞2b5培养上清用1%脱脂奶粉-tbst稀释(1∶100)后将pvdf膜覆盖,37℃慢摇2h;弃去一抗,pbst慢摇洗膜3次,每次5-10min;加入hrp标记的山羊抗鼠igg二抗(1∶1000稀释),37℃缓慢振摇1h;弃二抗,用tbst缓慢振摇洗膜三次,每次5min~10min;按照aec显色试剂盒的说明书配制显色液,将pvdf膜置于显色液中,待出现特异性反应条带后,立即用双蒸水冲洗以终止反应,拍照记录结果。同时设置rosetta上清和pet-32a(+)空载体蛋白对照组(结果见图1)。结果表明,该株单抗与猪pd-1蛋白发生特异性反应,并出现特异条带,但不与对照组rosetta上清与pet-32a(+)空载体蛋白反应,无条带出现。
实施例3鼠抗猪pd-1单抗生物学特性鉴定
1、单克隆抗体效价的检测
将收集的杂交瘤细胞培养上清按1:1、1:21、1:22、1:23、1:24、1:25、1:26、1:27、1:28、1:29、1:210、1:211、1:212、1:213稀释,杂交瘤细胞注射小鼠腹腔后取得的腹水按1∶100、1∶200、1∶400、1∶800、1∶1600、1∶3200、1∶6400、1∶12800、1∶25600、1∶51200、1∶102400、1∶204800稀释后,将重组pd-1胞外区蛋白包板,通过间接elisa法测定其od450值,分检测杂交瘤细胞上清及腹水效价。用免疫前小鼠血清做平行阴性对照试验,以与重组pd-1胞外区蛋白靶抗原发生反应的单克隆抗体的最大稀释度即为其效价,各孔od450值以p/n≥2.1为阳性。结果表明,细胞上清的效价为1:212;腹水的效价为1:2.048×105。
2、单克隆抗体亚型鉴定
采用ig亚类鉴定试剂盒法鉴定上述单克隆抗体的ig亚类,操作步骤严格按说明书进行。结果表明杂交瘤细胞株2b5分泌的单抗为igg1类免疫球蛋白,非其他亚型。
3、杂交瘤细胞株分泌单抗的稳定性鉴定
收集体外连续传代的杂交瘤细胞株上清,用间接elisa法测定其效价,冻存细胞,间隔1个月后复苏冻存的细胞,检测其培养上清液中的抗体效价,连续检测3个月,以此评价该分泌抗体的稳定性。结果表明,克隆纯化的杂交瘤细胞于液氮冻存3个月后复苏,经多次传代仍能够稳定分泌高效价抗体,抗体效价可达1∶212。
4、单克隆抗体的流式细胞术检测
参照外周血淋巴细胞分离液的说明书分离猪外周血淋巴细胞,具体步骤如下:
(1)从猪前腔静脉采集抗凝血5ml(抗凝剂为10%柠檬酸钠,全血与抗凝剂比例为10:1),抗凝血与等量pbs轻轻混匀;
(2)取4ml淋巴细胞分离液于12ml玻璃离心管中,将上述混匀血6ml沿管壁慢慢加入离心管中(注:动作要轻,不能混匀),水平离心,2000rpm,室温离心20min;
(3)用毛细管吸取血浆层与分离液之间的白色细胞薄层,移入新的12ml玻璃离心管中,加入2~5倍体积pbs,轻轻悬浮细胞,1000rpm,室温离心10min,弃上清,加入10mlpbs,轻轻悬浮细胞,重复离心一次,弃上清;
(4)观察白细胞中红细胞量,适当加入1~2ml红细胞裂解液,冰上裂解红细胞5min,加入10mlpbs,1000rpm,室温离心10min,弃上清,加入0.5mlpbs悬浮细胞,使其分散为单个细胞悬液,细胞计数后备用。
取1×106个pbmcs加入终浓度为10μg/ml的抗pd-1的单克隆抗体中,反应体系为100μl,鼠igg1为同型抗体对照,37℃作用1h,用pbs洗涤3次,加入fitc标记的羊抗鼠igg(1:500倍稀释),37℃作用1h,用pbs洗涤3次,用1mlpbs悬浮细胞,流式细胞术检测(结果见图2)。图2结果显示,单克隆抗体的荧光强度比同型抗体对照的荧光强度明显增强,说明制备的单抗可以很好的结合pbmc上的pd-1蛋白。
- 还没有人留言评论。精彩留言会获得点赞!