一种降解硫酸半乳聚糖并分析其寡糖结构的方法与流程
本发明属于医药化学
技术领域:
,具体涉及一种降解硫酸半乳聚糖并分析其寡糖结构的方法。
背景技术:
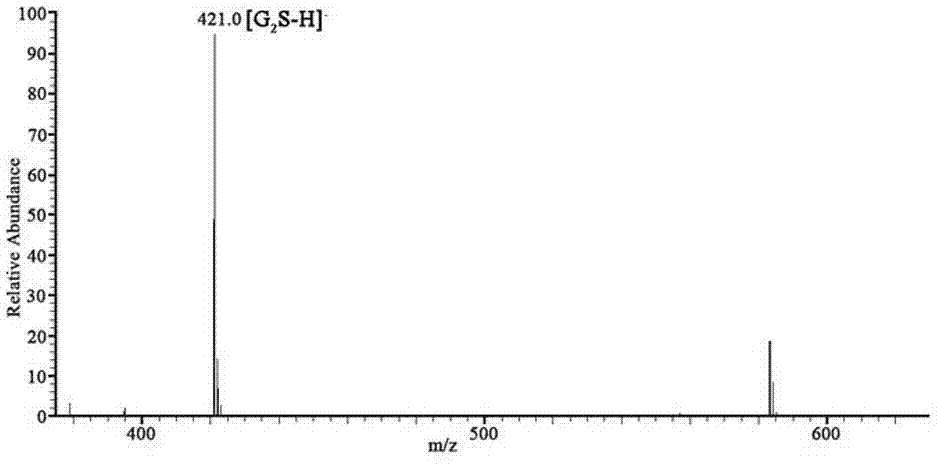
:半乳聚糖为海洋红藻、绿藻的常见多糖种类,含量丰富,常具有抗凝血、抗肿瘤、免疫调节等多种生物学活性,安全性高,在医药和食品领域具有非常广阔的应用前景。但是半乳聚糖的单糖残基连接方式多样,结构复杂,难以阐明其详细结构。目前,半乳聚糖的结构研究方法多采用多糖甲基化反应、核磁共振等方法。其中,甲基化反应存在多糖甲基化不完全、甲基化图谱复杂等缺点。核磁共振方法得出的多糖图谱常出现信号重叠、难以归属全部信号等缺点。将多糖制备为寡糖,减小多糖的分子量,并且降低了多糖结构的复杂性,有利于其结构分析,而且可以采用质谱法分析寡糖结构。质谱法具有灵敏度高、需要样品量很少、分析速度快、并且能够提供分子量和大量的寡糖结构信息。技术实现要素:本发明针对半乳聚糖结构研究困难的问题,提供了一种降解硫酸半乳聚糖获得其寡糖的方法,并采用质谱法对寡糖结构进行分析,获得了寡糖的精确结构,克服了现有技术在分析多糖结构时的缺点。本发明是通过以下技术方案来实现的,一种降解硫酸半乳聚糖并分析其寡糖结构的方法,其特征在于,包括以下步骤:a.将半乳聚糖溶于浓度为0.05mol/l的三氟乙酸溶液中,使多糖的质量百分浓度为1%,在50-70℃下反应1-2h;b.反应结束后,加入1-4mol/l氢氧化钠溶液中和至ph为7,然后加入85%以上乙醇使其沉淀,离心收集上清部分,浓缩、脱盐、冻干,即得寡糖混合物;c.采用bio-gelp4凝胶柱对寡糖混合物进行分离纯化,流动相为0.2mol/lnh4co3溶液,流速为0.3ml/min,获得不同聚合度的半乳寡糖;d.采用负离子模式的电喷雾质谱对半乳寡糖进行分析,以n2为载气,流速为250l/h和15l/h,在二级质谱中,需要锥孔电压80ev,氩气作为碰撞气体,同时为了得到最佳序列信息,碰撞能量保持在20-50ev,寡糖样品溶于乙腈和水的体积比为1:1的溶液中,浓度达到10-20pmol/μl,注射10μl进行质谱分析。作为优选,一种降解硫酸半乳聚糖并分析其寡糖结构的方法,包括以下步骤:a.将半乳聚糖溶于浓度为0.05mol/l的三氟乙酸溶液中,使多糖的质量百分浓度为1%,在60℃下反应1.5h;b.反应结束后,加入2mol/l氢氧化钠溶液中和至ph为7,然后加入85%以上乙醇使其沉淀,离心收集上清部分,浓缩、脱盐、冻干,即得寡糖混合物;c.采用bio-gelp4凝胶柱对寡糖混合物进行分离纯化,流动相为0.2mol/lnh4co3溶液,流速为0.3ml/min,获得不同聚合度的半乳寡糖;d.采用负离子模式的电喷雾质谱对半乳寡糖进行分析,以n2为载气,流速为250l/h和15l/h,在二级质谱中,需要锥孔电压80ev,氩气作为碰撞气体,同时为了得到最佳序列信息,碰撞能量保持在20-50ev,寡糖样品溶于乙腈和水的体积比为1:1的溶液中,浓度达到10-20pmol/μl,注射10μl进行质谱分析。进一步的,所述的步骤b中,脱盐过程采用sephadexg10凝胶柱脱盐。进一步的,所述的步骤c,采用bio-gelp4凝胶柱对寡糖混合物进行分离纯化,流动相为0.2mol/lnh4co3溶液,流速为0.3ml/min,硫酸苯酚法检测,按峰合并收集样品,经bio-gelp4凝胶柱进行二次纯化,获得不同聚合度的半乳寡糖。本发明的有益之处在于,(1)本发明采用的酸降解法经济实惠、简单易行,仅引入一种无机盐杂质,易于除去;(2)本发明采用的质谱分析法需要样品量少、耗时短、能准确的分析半乳糖的连接方式和取代位置等结构信息。附图说明图1是寡糖混合物的红外光谱图;图2是寡糖f1的负离子es-ms质谱图;图3是寡糖f1的es-cid-ms/ms二级质谱图;图4是寡糖f1的质谱断裂示意图;图5是寡糖f1的核磁共振氢谱图;图6是寡糖f1的核磁共振碳谱图。具体实施方式为了使本发明的技术方案能更清晰地表示出来,下面结合实施例对本发明作进一步说明。一、半乳聚糖的降解将5g硫酸半乳聚糖(本发明所用的半乳聚糖为松藻来源的冷水提粗多糖经凝胶柱分离纯化得到的纯品多糖组分,重均分子量约为31kda)溶于500ml浓度为0.05mol/l的三氟乙酸溶液中,使多糖的质量百分浓度为1%,在60℃下反应1.5h。反应结束后,冷却至室温,加入2mol/l氢氧化钠溶液中和至ph为7,然后加入4倍体积95%乙醇使其沉淀,4℃下静置过夜。6000r·min-1离心10min,收集上清部分,蒸发浓缩,经sephadexg10凝胶柱脱盐,冻干,即得寡糖混合物。采用bio-gelp4凝胶柱对寡糖混合物进行分离纯化,流动相为0.2mol/lnh4co3溶液,流速为0.3ml/min,每管收集3ml,硫酸苯酚法检测,按峰合并收集样品,经bio-gelp4凝胶柱进行二次纯化,获得不同聚合度的半乳寡糖f1-f5。所得寡糖运用ir、es-ms技术对其结构进行表征(如图1、2所示)。从图1中可以看出,1254cm-1附近的强峰是s=o对称伸缩振动吸收峰,843cm-1处的吸收峰为c-o-s伸缩振动峰,这两个信号为硫酸基取代的特征吸收峰。927cm-1左右处为β-d-吡喃半乳糖的特征吸收峰;1604cm-1处为丙酮酸的羧基的非对称吸收峰。寡糖混合物的红外光谱图与母体半乳聚糖极为相似,说明本发明的酸降解方法可以有效地断裂糖苷键而不破坏半乳聚糖的基本化学结构。从图2中可以看出,m/z421.0为单硫酸化半乳二糖[m-h]-峰,与单硫酸化半乳二糖的理论分子量422相符,推断f1的组成为g2s(g:galactose;s:sulfateester)。依次对寡糖组分f2-f5的es-ms质谱图进行分析,寡糖组分f1-f5的负离子es-ms归属如表1所示。表1寡糖组分f1-f5的负离子es-ms归属寡糖组分质荷比(电荷)聚合度(dp)片段归属f1421.0(-1)2[g2s-h]-f2745.1(-1)4[g4s-h]-f3491.0(-1)2[g2sp-h]-f4366.0(-2)3[g3s2p-2h]2-447.0(-2)4[g4s2p-2h]2-528.0(-2)5[g5s2p-2h]2-609.1(-2)6[g6s2p-2h]2-f5324.3(-3)4[g4s3p-3h]3-378.3(-3)5[g5s3p-3h]3-432.4(-3)6[g6s3p-3h]3-486.4(-3)7[g7s3p-3h]3-540.4(-3)8[g8s3p-3h]3-644.1(-2)6[g6s2p2-2h]2-注:g:galactose;s:sulfateester;p:pyruvate二、半乳寡糖的结构分析采用负离子模式的电喷雾质谱(es-ms)对半乳寡糖进行分析,以n2为载气,流速为250l/h和15l/h。在二级质谱(cid-ms/ms)中,需要锥孔电压80ev,氩气作为碰撞气体,同时为了得到最佳序列信息,碰撞能量保持在20-50ev。寡糖样品溶于乙腈和水的体积比为1:1的溶液中,浓度达到10-20pmol/μl,注射10μl进行质谱分析。从图3中可以看出,m/z241和m/z259为环间断裂离子b1和c1;361、331和301为环内断裂产生的0,4a2、1,4a2和2,4a2离子碎片,这些离子峰的出现是由于二糖丢失了分子量为60、90、120的碎片,但是没有丢失分子量为30的碎片,说明还原末端残基是1-3连接方式。并且有文献报道,0,2a碎片离子的形成,得力于c-3位游离羟基的存在,以此来辅助c2-c3化学键的断裂,在此二糖的断裂中没有出现0,2a2离子,也能证明半乳糖以1→3连接方式存在。m/z199和139归属为0,2a1和2,4a1离子,也是由环内断裂产生,证明硫酸基位于第一个糖环的c-4位。具体结构及断裂方式如图4所示,所以寡糖f1(g2s)结构为β-d-galp-(4so4)-(1→3)-d-galp。采用核磁共振技术对f1的质谱分析结果进行验证,如图5、6所示,寡糖f1的碳氢信号归属如表2所示。表2寡糖f1的碳氢信号归属a:→3)-α-d-galp-oh,b:β-d-galp-(4so4)-(1→,c:→3)-β-d-galp-oh本发明提供了一种酸降解半乳聚糖的方法,获得了不同聚合度的寡糖组分,并采用负离子模式的电喷雾质谱及二级质谱对寡糖结构进行研究,具有需要样品量少、耗时短、结果准确等优点,大大简化了多糖结构分析中的困难。本发明的技术方案也可用于其它多糖的结构研究。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1