人JAK2V617F基因突变检测试剂盒的制作方法
本发明涉及基因工程技术领域,具体涉及一种人JAK2V617F基因突变检测试剂盒。
背景技术:
真性红细胞增多症(PV)是一种造血干细胞克隆性疾病,临床以红细胞数及容量显著增多为特点,出现多血质及高黏滞血症所致的表现,常伴脾大。PV起病隐袭,进展缓慢,晚期可发生各种转化。本病在人群中的发病率约为2.8/10万,较常见于男性(大约是1.4∶1),诊断时的平均年龄是60岁,范围为15到90岁,但儿童罕见,5%的病人发病时不足40岁。
真性红细胞增多症属骨髓增殖性疾病范畴,为典型骨髓增殖性肿瘤中的一种。骨髓增殖性肿瘤(Myeloproliferative neoplasms,MPNs)是指骨髓组织持续增殖而引起的一组疾病,常表现为造血干细胞的一系或多系细胞恶性增生。根据增生的细胞系的不同,MPNs又可分为典型MPNs和非典型MPNs。典型MPNs包括真性红细胞增多症(Polycythemia vera,PV)、原发性血小板增多症(Essential thrombocythemia,ET)、原发性骨髓纤维化(Primary myelofibrosis,PMF)和慢性髓系白血病(Chronic myeloid leukemia,CML),它们之间关系密切,具有相似的临床特征并常可相互转化或合并存在。
早在上个世纪60年代,CML的发病机制就已经明确,即CML患者体内存在费城染色体,因此CML又称费城染色体阳性MPNs。目前,国内外各大医院也正是通过检测患者是否存在费城染色体进行CML的诊断。直到2005年4月,科学家们在费城染色体阴性MPNs发病机理的研究方面取得了实质性的突破。研究结果表明:近97%的PV患者、约50%的ET患者和50%左右的PMF患者存在JAK2V617F的突变,随后的JAK2V617F转基因小鼠模型和骨髓移植小鼠模型证明了JAK2V617F突变是导致MPNs的主要原因,揭示了MPNs发病的分子机制。
目前,对于MPNs的诊断,国内绝大多数医院仍采用常规的诊断方法,即根据主要诊断指标(红细胞容量、动脉血氧饱和度、脾脏肿大情况等)再结合次要诊断指标(白细胞增多、中性粒细胞碱性磷酸酶活性、血清VB12含量等)进行诊断,诊断项目繁多,费用较高。而且传统的诊断方法经常不能确诊和导致误诊,延误了患者的治疗,给患者本人及其家属带来了极大的痛苦和负担。由于通过检测JAK2V617F来确诊MPNs具有充分的科学依据,在2008年,世界卫生组织(WHO)已经将检测JAK2V617F作为PV、ET和PMF的一项主要的诊断指标。
综上所述,本发明拟提供一种检测人JAK2V617F基因突变的试剂盒,使MPNs疾病,尤其是PV疾病的诊断更加准确、便捷和快速。
技术实现要素:
本发明提供的检测人JAK2V617F基因突变的试剂盒将基因的提取和突变检测有机整合至一个试剂盒中,简化了实验的操作步骤,提高了实验的效率。
本发明采取的技术方案如下:
人JAK2V617F基因突变检测试剂盒,包括A盒和B盒,A盒包括磁珠BC、裂解液BL、洗涤液BW1和洗脱液CE;B盒包括预混液I、预混液II、阳性标准品、阴性标准品、超纯水、15mg/mL的蛋白酶K溶液、DNALoading Buffer和DNA Marker。
优选的,所述预混液I制备步骤包括:将20μM的JAK3引物(SEQ ID NO.2所示)和20μM的JAK4引物(SEQ ID NO.3所示)等体积混合,然后将混合引物与2×Taq PCR MIX Loading Dye-free按体积比2∶55的比例混匀即得。
优选的,所述预混液II制备步骤包括:按照终浓度为5μM J2f引物(SEQ ID NO.4所示)、5μM J2r引物(SEQ ID NO.5所示)、10μM J2nf引物(SEQ ID NO.6所示)和40μM J2mr引物(SEQ ID NO.1所示)的量配制巢式PCR引物,然后将巢式PCR引物与2×Taq PCR MIX Loading Dye-free按体积比2∶55的比例配制,混匀即得。
优选的,所述蛋白酶K溶液为将蛋白酶K溶解于Tris-HCl、CaCl2和甘油三者的混合溶液中获得;所述Tris-HCl浓度为10mM,pH值7.5,CaCl2浓度为20mM,甘油质量分数为50%。
优选的,所述阴性标准品制备步骤包括:将pKS-JAK2质粒1μL加入到100μL E.coli DH5α感受态细胞溶液中,混合均匀,42℃水浴热激90s,冰浴冷却至0℃,加入800μL LB液体培养基,37℃轻微振荡复苏1h,取100μL培养物涂含100μg/mL Amp的LB固体平板,37℃培养12~14小时;挑单菌落振荡过夜培养,提取质粒DNA,用超纯水将质粒DNA稀释到10ng/μL,即为阴性标准品。
优选的,所述阳性标准品的制备步骤包括:将pKS-JAK2V617F质粒1μL加入到100μL E.coli DH5α感受态细胞溶液中,混合均匀,42℃水浴热激90s,冰浴冷却至0℃,加入800μL LB液体培养基,37℃轻微振荡复苏1h,取100μl培养物涂含100μg/mL Amp的LB固体平板,37℃培养12~14小时;挑单菌落振荡过夜培养,提取质粒,用超纯水将质粒DNA稀释到10ng/μL,并按1:9的体积比与阴性标准品混合均匀即得阳性标准品。
优选的,所述试剂盒中各样品的量为:
本发明课题组应用等位基因特异性PCR(Allele-specific PCR,ASP)及DNA序列分析法,分析检测了从吉林大学中日联谊医院随机收集的血液样本中JAK2V617F基因突变的情况。截止2005年底,在3935例非MPNs患者中,检测出39例患者存在JAK2V617F基因突变,阳性率近1%,远远高于PV等MPNs在人群中的发病率。而且血常规结果显示,这些阳性患者均未达到MPNs的诊断标准,但是统计学分析显示,阳性人群的白细胞和血小板数量明显高于阴性人群。接下来,课题组又对2613例心脑血管疾病患者进行了JAK2V617F基因突变的筛查,发现JAK2V617F基因突变阳性44例,阳性率为1.68%。这预示着JAK2V617F基因不仅与血液细胞的异常发育有关,甚至还可能与人类其他重大疾病直接相关。因此,JAK2V617F基因突变检测试剂盒不仅可以用于MPNs,尤其用于PV的诊断,而且在心脑血管疾病等重大疾病的早期诊断、辅助诊断以及提早预防等方面均可发挥重要作用,具有广阔的市场应用前景。
本发明的有益效果在于:
1)本试剂盒集基因组DNA提取和基因突变检测于一体,增加了操作的连续性,降低了由于采用不同方法提取得到的基因组DNA质量的不稳定性,显著增加了检测的成功率;
2)本试剂盒的检测限可达1%,因此,对于MPNs,尤其是对于PV疾病的早期诊断和治疗具有重要的指导意义;
3)本试剂盒操作方便,耗时短,全程检测仅需3个小时,依照使用说明书,普通技术人员均可操作,而且结果判定容易、准确,只要出现与对照相符的条带即可下结论;
4)本试剂盒所需设备简单,只需要普通的PCR仪及成像设备即可,使用范围更加广泛,适用于医疗条件不发达或欠发达地区;
5)本试剂盒检测原理明确,增强了MPNs诊断的科学性,可有效地帮助医生进行确诊;
6)检测成本降低,患者无需做过多的、不必要的辅助检查,只要做一些常规检查再进行该项基因突变检测即可确诊,减轻或避免了因确诊给患者身体带来的二次伤害,同时减轻了患者的经济负担。
附图说明
图1为本发明所述试剂盒检测限实验结果;
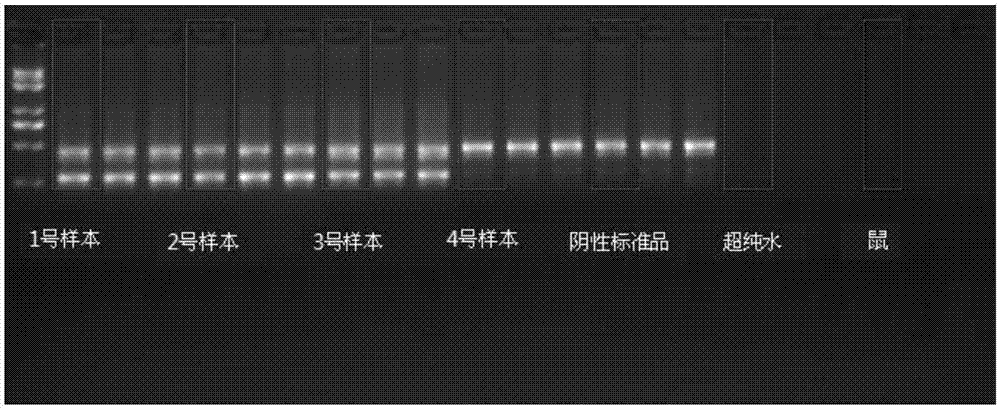
图2为本发明所述试剂盒特异性实验结果;
图3为本发明所述试剂盒可重复性实验结果。
具体实施方式
下面将对本发明技术方案的实施例进行详细的描述。以下实施例仅用于更加清楚地说明本发明的技术方案,因此只作为示例,而不能以此来限制本发明的保护范围。
下述试剂均为购买商品,其厂商为:
2×Taq PCR MIX Loading Dye-free,购自GenStar;6×DNA loading buffer,购自GenStar;2K Plus DNA Marker,购自TransGen;蛋白酶K,购自Roche;引物JAK3和JAK4,购自Invitrogen;磁珠BC、裂解液BL、洗涤液BW1、洗脱液CE购自长春市志昂生物科技有限公司。
JAK2基因Genbank登录号3717,基因突变位置为93526位上的G突变为T(即V617位点)。JAK2基因93253位至93774位的基因片段序列(包括V617位点)如SEQ ID NO.7所示。
实施例1
人JAK2V617F基因突变检测试剂盒,包括A盒和B盒,A盒试剂有:磁珠BC、裂解液BL、洗涤液BW1、洗脱液CE;B盒试剂有:MIX I、MIX II、阳性标准品、阴性标准品、超纯水、蛋白酶K、DNA Loading Buffer、DNA Marker。该试剂盒的规格有但不限于20次、50次和100次,各试剂装量见表1。
表1试剂装量
阴性标准品制备:将pKS-JAK2质粒1μL加入到100μLE.coli DH5α感受态细胞溶液中,混合均匀,42℃水浴热激90s,冰浴冷却至0℃,加入800μL LB液体培养基,37℃轻微振荡(<200rpm)复苏1h,取100μL培养物涂LB固体平板(含100μg/mL Amp),37℃培养12~14小时;挑单菌落振荡过夜培养,提取质粒DNA。用超纯水将质粒DNA稀释到10ng/μL,即为阴性标准品。
阳性标准品制备:将pKS-JAK2V617F质粒1μL加入到100μL E.coli DH5α感受态细胞溶液中,混合均匀,42℃水浴热激90s,冰浴冷却至0℃,加入800μL LB液体培养基,37℃轻微振荡(<200rpm)复苏1h,取100μl培养物涂LB固体平板(含100μg/mL Amp),37℃培养12~14小时;挑单菌落振荡过夜培养,提取质粒,用超纯水将质粒DNA稀释到10ng/μL,并按1∶9的比例与上述制得的阴性标准品混合均匀即得阳性标准品。
采用DNA测序的方法确定标准品的均一性,阴性标准品测序结果为应为100%的野生型JAK2,阳性标准品测序结果应为100%的JAK2V617F突变型。MIX I的制备:取引物JAK3(20μM,SEQ ID NO.2)和JAK4(20μM,SEQ ID NO.3)等体积混合制备成JAK3/4,将JAK3/4与2×Taq PCR MIX Loading Dye-free以2∶55的比例混匀即得MIX I。
MIX II的制备:按照终浓度为5μM J2f引物(SEQ ID NO.4)、5μM J2r引物(SEQ ID NO.5)、10μM J2nf引物(SEQ ID NO.6)和40μM J2mr引物(SEQ ID NO.1)配制巢式PCR引物MIX 60,将MIX 60与2×Taq PCR MIX Loading Dye-free以2∶55的比例配制,混匀即得MIX II。
蛋白酶K溶液的制备:称取一定量的蛋白酶K,溶于pH 7.5的10mM Tris-HCl、20mM CaCl2和50%甘油的贮存缓冲液中,制成蛋白酶K的浓度为15mg/mL的蛋白酶K溶液。
需要说明的是,MIX I、MIX II、阳性标准品、阴性标准品、超纯水、蛋白酶K、DNA Loading Buffer、DNA Marker、洗脱液CE应为清澈透明液体,无沉淀、无悬浮物、无絮状物。
裂解液BL、洗涤液BW1如有固体析出,应置于50℃温浴中,固体溶解并充分混匀后应为清澈透明液体,无沉淀、无悬浮物、无絮状物。
实施例2
试剂盒检测JAK2V617F基因突变的方法,具体如下:
1、血液基因组DNA的提取
1)取20μL蛋白酶K,加入1.5mL离心管中,注意蛋白酶K要加到离心管底部。将全血样品充分混匀后,取200μL加入离心管中,再加入200μL裂解液。涡旋振荡混匀,70℃消化15分钟,期间可涡旋振荡1次。
需要注意的是,请保证蛋白酶K、样品和裂解液按顺序加入,不要于裂解液中直接加入蛋白酶K。另外,全血样品于-20℃以下可长期保存,如于2~8℃保存,保存时间请勿超过10天。如果全血样品保存时间过长,可通过适当延长消化时间(例如20分钟)以改善提取效果。
2)孵育结束后瞬时离心,然后于每个样品中加入480μL无水乙醇及60μL磁珠,涡旋振荡混匀后于室温静置10分钟进行DNA吸附,期间可涡旋振荡2~3次。室温吸附后,涡旋振荡混匀,将离心管置于磁力架上,磁吸1分钟或至溶液澄清。小心地将离心管内液体完全吸弃,注意不要触碰磁珠。
需要注意的是,磁珠使用前需充分振荡混匀后立刻吸取,但连续振荡时间不宜超过30秒,可多次短时振荡。磁珠使用前后均可于磁力架上存放。如实验条件允许,室温静置也可改为在翻转摇匀仪上翻转10分钟(50rpm)进行DNA吸附。实验过程中除磁吸步骤外,其它步骤均不要将离心管置于磁力架上。每次将离心管置于磁力架上磁吸前应涡旋振荡均匀。吸弃步骤应注意不要触碰磁珠。
3)加入700μL已加入乙醇的洗涤液BW1,盖上离心管管盖,涡旋振荡混匀20秒,放回磁力架上。在离心管不离开磁力架的情况下,反复颠倒磁力架,将离心管管盖洗净,磁吸1分钟或至溶液澄清。先吸弃管盖中的液体,然后吸弃所有液体。
4)加入800μL已加入乙醇的洗涤液BW2,按照步骤3的方法洗涤1次。
5)加入800μL体积分数80%的乙醇溶液,按照步骤3的方法洗涤1次。
6)将离心管置于磁力架上,室温开盖干燥5~10分钟。
需要注意的是,干燥过程中请注意观察磁珠干燥状态,如磁珠仍可以流动或者表面发亮,表明磁珠未充分干燥,需继续干燥,待干燥至磁珠表面无光泽或磁珠颜色由棕色变为浅棕色,表明磁珠已干燥充分。注意请不要使磁珠过分干燥(磁珠颜色由棕色变为浅黄色),过分干燥会影响DNA的洗脱效率。
7)加入50~100μL洗脱液,涡旋振荡混匀后于70℃温浴10分钟。再次涡旋振荡混匀磁珠,于磁力架上磁吸1分钟后吸取上清,进行后续实验,或于-20℃保存待用。
需注意的是,吸液时注意不要触碰磁珠,要慢速吸取,不要把磁珠带出。若吸取时有磁珠带出,应把液体吹回至离心管中重新吸取。
2、PCR检测JAK2V617F突变
1)首轮PCR
分别吸取血液基因组DNA、阳性对照品、阴性标准品各1μL,加入到装有预混液MIX I的PCR管中,按照如下反应条件进行PCR:94℃3min;94℃30s,61℃20s,72℃30s,共35个循环;72℃5min;4℃储存备用;
2)巢式PCR
吸取首轮PCR产物1μL,加入到装有预混液MIX II的PCR管中,按照如下反应条件进行PCR:94℃3min;94℃30s,60℃20s,72℃30s,共30个循环;72℃5min。
PCR产物在3%琼脂糖凝胶中120V电压进行电泳30分钟,观察结果。
3、结果判定:
若样品PCR产物条带与阳性对照品一致,即可判定该样品为JAK2V617F突变阳性;若样品PCR产物条带与阴性标准品一致,即可判定该样品为正常样品。
实施例3
试剂盒检测限的确定
实验步骤如下:
1)取试剂盒中阴性标准品99μL与阳性标准品1μL混合,配制成JAK2V617F突变DNA为1%的样本;
2)用移液器吸取9.6μL超纯水和11.4μL MIX I加入到PCR管中,然后加入1μL突变率为1%的样本,混合均匀,平行配制10份;
3)用移液器吸取9.6μL超纯水和11.4μL MIX I加入到PCR管中,然后加入1μL超纯水,混合均匀,作为空白对照;
4)将PCR管置于PCR仪中,按照如下反应条件进行PCR:94℃预变性2min;主循环:94℃变性20s,61℃退火20s,72℃延伸30s;30个循环后,72℃延伸5min;
5)将步骤4)中得到的首轮PCR产物用超纯水稀释15倍,用移液器吸取已稀释的首轮产物各1μL(包括空白对照),分别加入到装有11.4μL MIX II和9.6μL超纯水的PCR管中,混合均匀;
6)将PCR管置于PCR仪中,按照如下反应条件进行PCR:94℃预变性1min;主循环:94℃变性20s,62℃退火20s,72℃延伸30s;25个循环后,72℃延伸5min;
7)称取1.8g的琼脂糖,加入7.5mL超纯水和65mL 1xTAE配制成3%的琼脂糖凝胶;
8)于琼脂糖凝胶的上样孔中分别加入3μL的DNA Marker以及步骤6)中得到的11个PCR产物,电泳30分钟后观察结果。
结果如图1所示,图中,空白样品是指首轮PCR以超纯水为模板的对照样品;M样品是指DNA标准分子量;1-10号样品为以含有1%JAK2V617F的DNA为模板的10个平行样品。若电泳结果出现P条带即可判定本试剂盒的检测限为1%。最终确定,试剂盒的检测限可达到1%,即样本中有1%的JAK2基因发生V617F突变就能检测出来。
实施例4
试剂盒的特异性检测
实验步骤如下:
1)首轮PCR
吸取JAK2V617F突变阳性患者血液基因组DNA 1μL,加入到装有预混液MIX I的PCR管中,按照如下反应条件进行PCR:94℃预变性3min;94℃变性30s,61℃退火20s,72℃延伸30s,共35个循环;72℃延伸5min。
2)巢式PCR
吸取首轮PCR产物1μL,加入到装有预混液MIX II的PCR管中,按照如下反应条件进行PCR:94℃3min;94℃预变性30s,60℃退火20s,72℃延伸30s,共30个循环;72℃延伸5min。
其中1、2、3号样本为从吉林大学第一医院获得的JAK2V617F突变阳性患者的外周血样本;4号样本为从医院获得的正常人外周血样本;鼠:小鼠外周血样本;超纯水:电导率为18.2MΩ.cm的纯净水。
从图2中可以看出,不含任何物种DNA的超纯水样本没有出现任何条带,说明本试剂盒具有物质特异性,即PCR的模板必须是DNA而非像超纯水类的其它物质。由于本试剂盒使用的引物是根据人类基因组DNA序列设计,因此,所有来自人源的样本(无论是否存在突变)和阴性标准品进行PCR后均扩增出了相应的条带,而来自鼠源的样本没有得到任何条带,说明引物设计是成功的,试剂盒是具有种属特异性的。
实施例5
试剂盒重复性检测
取吉林大学第一医院获得的用荧光定量PCR的检测方法确定为JAK2V617F突变阳性患者的血液样本作为阳性参考品,符合率:采用本发明所述试剂盒对4份阳性参考品进行测定,检测结果全部为阳性。
取小鼠外周血基因组DNA和超纯水作为阴性参考品,符合率:采用本发明所述试剂盒对2份阴性参考品进行检测,检测结果没有任何条带,结果全部为阴性。
分别取2个浓度水平的JAK2V617F阳性和阴性DNA参考品,使用同一批次试剂盒对阳性和阴性样本各重复检测10次,检测结果见图3,图3中A图中各列样品如下:M:DNA Marker;1-10:稀释后的阳性样本(0.2ng/μL)平行10个;11-20:稀释后的阳性样本(5ng/μL)平行10个。图3中B图各列样品如下:M:DNA Marker;1-10:稀释后的阴性样本(0.1ng/μL)平行10个;11-20:稀释后的阴性样本(3.7ng/μL)平行10个。由图3所示结果可知,本试剂盒具有良好的实验可重复性。
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围,其均应涵盖在本发明的权利要求和说明书的范围当中。
〈110〉申请人:吉林省锐吉尔生物科技有限公司
〈120〉人JAK2V617F基因突变检测试剂盒
〈160〉7
〈210〉1
〈211〉21
〈212〉DNA
〈213〉人工序列
〈220〉
〈223〉J2mr引物
〈400〉1
cttactctcg tctccacaga a 21
〈210〉2
〈211〉26
〈212〉DNA
〈213〉人工序列
〈220〉
〈223〉JAK3引物
〈400〉2
ttccaggctt acacaggggt ttcctc 26
〈210〉3
〈211〉26
〈212〉DNA
〈213〉人工序列
〈220〉
〈223〉JAK4引物
〈400〉3
ctataatact ctattgtttg ggcatt 26
〈210〉4
〈211〉25
〈212〉DNA
〈213〉人工序列
〈220〉
〈223〉J2f引物
〈400〉4
gttgatggca gttgcaggtc catat 25
〈210〉5
〈211〉19
〈212〉DNA
〈213〉人工序列
〈220〉
〈223〉J2r引物
〈400〉5
tttaacttca ttgctttcc 19
〈210〉6
〈211〉23
〈212〉DNA
〈213〉人工序列
〈220〉
〈223〉J2nf引物
〈400〉6
ggttttaaat tatggagtat gtg 23
〈210〉7
〈211〉522
〈212〉DNA
〈213〉智人(HOMO SAPIENS)
〈220〉
〈223〉JAK2基因93253位至93774位的基因片段序列(包括V617位点)
〈400〉7
ttccaggctt acacaggggt ttcctcagaa cgttgatggc agttgcaggt ccatataaag 60
ggaccaaagc acattgtatc ctcatctata gtcatgctga aagtaggaga aagtgcatct 120
ttattatggc agagagaatt ttctgaacta tttatggaca acagtcaaac aacaattctt 180
tgtacttttt tttttcctta gtctttcttt gaagcagcaa gtatgatgag caagctttct 240
cacaagcatt tggttttaaa ttatggagta tgtgtctgtg gagacgagag taagtaaaac 300
tacaggcttt ctaatgcctt tctcagagca tctgtttttg tttatataga aaattcagtt 360
tcaggatcac agctaggtgt cagtgtaaac tataatttaa caggagttaa gtatttttga 420
aactgaaaac actgtaggac tattcagtta tatcttgtga aaaaggaaag caatgaagtt 480
aaaagtagaa ggttacaatg cccaaacaat agagtattat ag 522
- 还没有人留言评论。精彩留言会获得点赞!