天山雪莲种子中的倍半萜内酯类化合物及其制备方法与流程
本发明为植物化学领域,具体为中药有效成分的提取、分离与制备工艺领域,尤其涉及从雪莲种子中提取、分离具有药理活性的一个新的倍半萜内酯类化合物。
背景技术:
天山雪莲(saussureainvolucrata)系菊科(asteraceae)风毛菊属(saussurea)植物,是新疆的著名特产,又称新疆雪莲,全草入药。雪莲分布于我国新疆天山和昆仑山一带,生长在雪线以上。其国外分布很少,资料表明,仅在俄罗斯、哈萨克斯坦和蒙古有分布。天山雪莲又名雪莲花,学荷花,是维吾尔族医常用药材(名为“塔格依力斯”)。天山雪莲在医药应用上已有数百年的历史,中国传统中医理论认为雪莲性温,味微苦,入肝、脾、肾三经,具有散寒除湿、活血通经、强筋助阳、抗炎、镇痛、收缩子宫等功能。民间用于治疗风湿性关节炎、肩周炎等疾病、妇女小腹冷痛、闭经、胎衣不下、麻疹不透、肺寒咳嗽、阳萎等症,在治疗跌打损伤、雪盲和牙痛方面也有使用。现代药理学证明雪莲具有抗肿瘤、清除自由基、抗感染和免疫调节等作用。从已有文献来看,新疆雪莲中化学成分种类比较丰富(黄酮、萜类、香豆素和植物甾醇等)并且具有很好的药理活性(抗炎镇痛、抗癌、解痉降压、终止妊娠和抗染色体损伤等)。天山雪莲(saussureainvolucrata)种子在零摄氏度发芽,3~5℃生长,幼苗能经受-20℃的严寒。在生长期不到两个月的环境里,高度却能超过其他植物的五到七倍。它虽然要五年才能开花,但实际生长天数只有八个月。独特的生物学特征可能造就了结构新颖的次生代谢产物。另外,通过文献调研,目前对新疆雪莲种子的化学成分和药理作用进行报道的文献还较少。因此对于新疆雪莲种子进行化学成分及其生物活性的研究对于雪莲药用价值的开发具有极高的学术价值和非常重要的科学意义,不仅可对雪莲种子的化学成分研究其有效成分及药理功效奠定了良好的基础,也为同类产品进一步开发再利用,提高商品技术附加值提供理论与技术支持。
技术实现要素:
本发明的目的在于,提供一种天山雪莲种子中的倍半萜内酯类化合物及其制备方法,该化合物以天山雪莲种子药材为原料,用有机溶剂提取和萃取后,通过硅胶柱层析法、葡聚糖凝胶lh-20柱层析法、反相ods柱层析、制备型高效液相色谱的三种或四种方式进行分离,采取薄层层析法检测分析,得到天山雪莲种子中的倍半萜内酯类化合物,化学名称为(3s,3ar,4s,6ar,8r,9as,9br)-4,8-二羟基-3-甲基-6,9-二甲基二氢薁基[4,5-b]呋喃-2(9bh-酮)。
本发明所述的一种天山雪莲种子中的倍半萜内酯化合物,该化合物的结构式(ⅰ)为:
其中:化合物(ⅰ)被命名为雪莲內酯d,其化学名称为(3s,3ar,4s,6ar,8r,9as,9br)-4,8-二羟基-3-甲基-6,9-二甲基二氢薁基[4,5-b]呋喃-2(9bh-酮)。
所述天山雪莲种子中倍半萜内酯化合物的制备方法,按下列步骤进行:
a、以天山雪莲种子为原料,粉碎后,用3-10倍体积浓度的75-95%乙醇、无水乙醇或甲醇进行室温下冷浸提取,或温度20-70℃加热回流提取,提取液经减压浓缩后得到粗提物;
b、将步骤a得到的粗提物用蒸馏水分散,用石油醚进行萃取3-5次后,水层用三氯甲烷或二氯甲烷萃取3-5次,将萃取液浓缩,得到萃取物浸膏;
c、将步骤b得到的萃取物浸膏经正相硅胶柱层析分离,经过葡聚糖凝胶lh-20柱层析或反相ods柱层析纯化后,再用高效液相色谱进行纯化,即得到倍半萜内酯类化合物,为雪莲內酯d。
步骤c中所用正相硅胶柱层析法为常压或加压柱层析,所用洗脱剂为二氯甲烷或三氯甲烷和甲醇的混合溶剂,采用梯度洗脱。
步骤c中葡聚糖凝胶lh-20柱层析法的洗脱剂为体积比1:1的甲醇:三氯甲烷或甲醇:二氯甲烷等度洗脱,或体积浓度10-60%的甲醇-水梯度洗脱。
步骤c中反相柱ods柱层析采用体积浓度10-90%的甲醇-水或乙腈-水梯度洗脱。
步骤c中高效液相色谱进行分离,洗脱剂为体积浓度10-90%的甲醇-水溶液或体积浓度10-60%的乙腈-水溶液,采用梯度洗脱。
附图说明
图1为本发明化合物的核磁共振氢谱谱图;
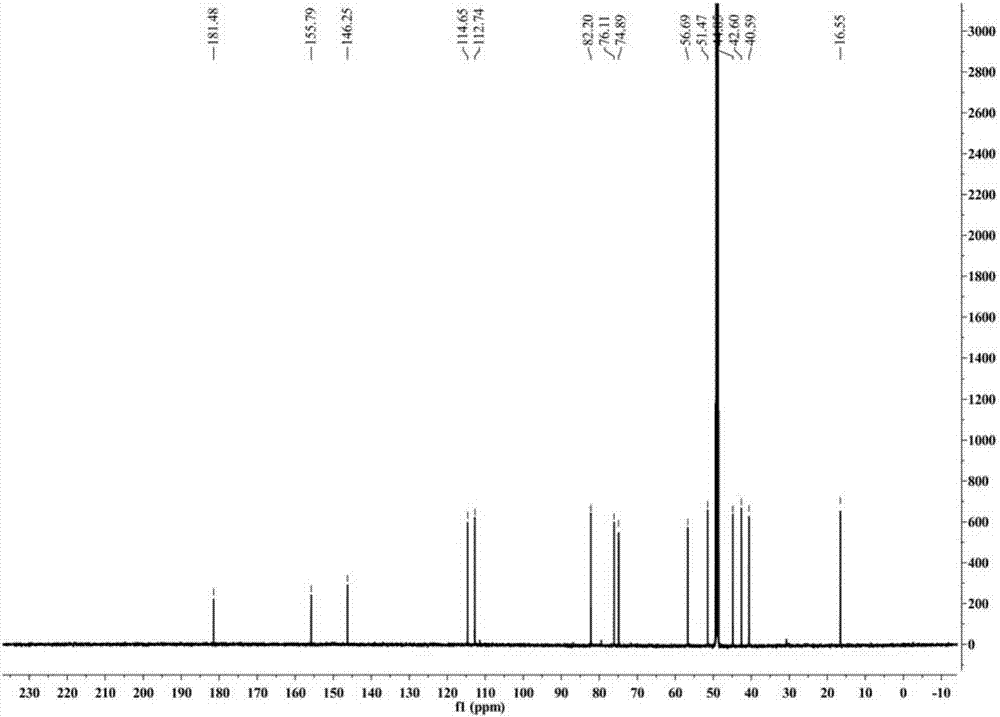
图2为本发明化合物的核磁共振碳谱谱图;
图3为本发明化合物的高分辨质谱图。
具体实施方式
实施例1
a、取天山雪莲种子3kg,粉碎后,用5倍体积浓度的95%乙醇水溶液回流提取,温度20℃,将提取液经减压浓缩后得到粗提物;
b、将步骤a得到的粗提物用蒸馏水分散,用石油醚进行萃取5次后,水层用三氯甲烷萃取3次,将三氯甲烷萃取液浓缩,得到萃取物浸膏;
c、将步骤b得到的三氯甲烷萃取物浸膏用常压正相硅胶柱层析分离,按体积比100:1-0:100的三氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行硅胶薄层层析(tlc)跟踪分析,合并相同流分,最终得到5个流分a-e;将流分e再次利用常压正相硅胶柱层析进行分离,依次用体积比为30:1-0:1的正己烷-三氯甲烷和体积比为20:1-0:1的三氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行tlc跟踪分析,合并相同流分,最终得到12个组分ea-el;将ej流分用葡聚糖凝胶lh-20凝胶柱层析纯化,以体积比为1:1的三氯甲烷-甲醇进行纯化,得到ej1-34流分,依次收集洗脱液在室温浓缩后,进行tlc跟踪分析合并流份ej12-13;将合并流份ej12-13采用制备型高效色谱[反相柱(c185μm10×250mm)]进行纯化,以浓度为32%的乙腈-水溶液等度洗脱,得到化合物名称为(3s,3ar,4s,6ar,8r,9as,9br)-4,8-二羟基-3-甲基-6,9-二甲基二氢薁基[4,5-b]呋喃-2(9bh-酮),(1.8mg),(3.0ml/min,210nm,tr=23min),命名为雪莲內酯d。
实施例2
a、取天山雪莲种子3kg,粉碎后,用3倍体积浓度的75%乙醇水溶液回流提取,温度50℃,提取液经减压浓缩后得到粗提物;
b、将步骤a得到的粗提物用蒸馏水分散,用石油醚进行萃取5次后,水层用三氯甲烷萃取3次,将三氯甲烷萃取液浓缩,得到萃取物浸膏;
c、将步骤b得到的三氯甲烷萃取物浸膏用常压正相硅胶柱层析分离,按体积比100:1-0:100的三氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行硅胶薄层层析(tlc)跟踪分析,合并相同流分,最终得到5个流分a-e;将流分e用加压硅胶柱层析进行分离,依次用体积比为30:1-0:1的正己烷-三氯甲烷和体积比为20:1-0:1三氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行tlc跟踪分析,合并相同流分,最终得到12个组分ea-el;将ej流分用葡聚糖凝胶lh-20凝胶柱层析纯化,以体积比为1:1的二氯甲烷-甲醇进行纯化,得到ej1-34流分,依次收集洗脱液在室温浓缩后,进行tlc跟踪分析合并流份ej12-13;将合并流份ej12-13采用制备型高效色谱[反相柱(c185μm10×250mm)]进行纯化,以浓度为49%的甲醇-水溶液等度洗脱,得到化合物名称为(3s,3ar,4s,6ar,8r,9as,9br)-4,8-二羟基-3-甲基-6,9-二甲基二氢薁基[4,5-b]呋喃-2(9bh-酮),(1.8mg),(3.0ml/min,210nm,tr=18min),命名为雪莲內酯d。
实施例3
a、取天山雪莲种子3kg,粉碎后,用3倍体积的无水乙醇回流提取,温度70℃,提取液经减压浓缩后得到粗提物;
b、将步骤a得到的粗提物用蒸馏水分散,用石油醚进行萃取5次后,水层用三氯甲烷萃取3次,将三氯甲烷萃取液浓缩,得到萃取物浸膏;
c、将步骤b得到的三氯甲烷萃取物浸膏用常压正相硅胶柱层析分离,按体积比100:1-0:100的三氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行硅胶薄层层析(tlc)跟踪分析,合并相同流分,最终得到5个流分a-e;将流分e用常压正相硅胶柱层析进行分离,依次用体积比为30:1-0:1的正己烷-三氯甲烷和体积比为20:1-0:1的三氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行tlc跟踪分析,合并相同流分,最终得到12个组分ea-el;将ej流分用采用反相ods柱层析进行纯化,以浓度为10-90%的甲醇-水溶液梯度洗脱,依次收集洗脱液在室温浓缩后,进行tlc跟踪分析合并流份ej12-13,将合并流份ej12-13,采用制备型高效色谱[反相柱(c185μm10×250mm)]进行纯化,以浓度为32%的乙腈-水溶液等度洗脱,得到化合物名称为(3s,3ar,4s,6ar,8r,9as,9br)-4,8-二羟基-3-甲基-6,9-二甲基二氢薁基[4,5-b]呋喃-2(9bh-酮),(1.8mg),(3.0ml/min,210nm,tr=23min),命名为雪莲內酯d。
实施例4
a、取天山雪莲种子3kg,粉碎后,用5倍体积无水甲醇回流提取,温度30℃,提取液经减压浓缩后得到粗提物;
b、将步骤a得到的粗提物用蒸馏水分散,用石油醚进行萃取5次,水层依次加入三氯甲烷萃取3次,将三氯甲烷萃取液浓缩,得到萃取物浸膏;
c、将步骤b得到的三氯甲烷萃取物浸膏用常压正相硅胶柱层析分离,按体积比100:1-0:100的三氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行硅胶薄层层析(tlc)跟踪分析,合并相同流分,最终得到5个流分a-e;将流分e用加压正相硅胶柱层析进行分离,依次用体积比为30:1-0:1的正己烷-三氯甲烷和体积比为20:1-0:1的三氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行tlc跟踪分析,合并相同流分,最终得到12个组分ea-el;将ej流分用采用反相ods柱层析进行纯化,以浓度为10-90%的乙腈-水溶液梯度洗脱,依次收集洗脱液在室温浓缩后,进行tlc跟踪分析合并流份ej12-13,将合并流份ej12-13采用制备型高效色谱[反相柱(c185μm10×250mm)]进行纯化,以浓度为32%的乙腈-水溶液等度洗脱,得到化合物名称为(3s,3ar,4s,6ar,8r,9as,9br)-4,8-二羟基-3-甲基-6,9-二甲基二氢薁基[4,5-b]呋喃-2(9bh-酮),(1.8mg),(3.0ml/min,210nm,tr=23min),命名为雪莲內酯d。
实施例5
a、取天山雪莲种子3kg,粉碎后,用3倍体积浓度的75%乙醇水溶液室温下冷浸提取,提取液经减压浓缩后得到粗提物;
b、将步骤a得到的粗提物用蒸馏水分散,用石油醚进行萃取5次后,水层用二氯甲烷萃取3次,将二氯甲烷萃取液浓缩,得到萃取物浸膏;
c、将步骤b得到的二氯甲烷萃取物浸膏用正相硅胶柱层析分离,按体积比100:1-0:100的二氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行硅胶薄层层析(tlc)跟踪分析,合并相同流分,最终得到5个流分a-e;将流分e用正相硅胶柱层析进行分离,依次用体积比为30:1-0:1的正己烷-二氯甲烷和体积比为20:1-0:1的二氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行tlc跟踪分析,合并相同流分,最终得到12个组分ea-el;将ej流分用葡聚糖凝胶lh-20柱层析纯化,以甲醇等度洗脱依次收集洗脱液在室温浓缩后,得到流分ej1-34,进行tlc跟踪分析合并流分ej12-13,将合并流份ej12-13采用制备型高效色谱[反相柱(c185μm10×250mm)]进行纯化,以浓度为32%的乙腈-水溶液等度洗脱,得到化合物名称为(3s,3ar,4s,6ar,8r,9as,9br)-4,8-二羟基-3-甲基-6,9-二甲基二氢薁基[4,5-b]呋喃-2(9bh-酮),(1.8mg),(3.0ml/min,210nm,tr=23min),命名为雪莲內酯d。
实施例6
a、取天山雪莲种子3kg,粉碎后,用3倍体积浓度的无水甲醇室温下冷浸提取,提取液经减压浓缩后得到粗提物;
b、将步骤a得到的粗提物用蒸馏水分散,用石油醚进行萃取5次后,水层用三氯甲烷萃取3次,将三氯甲烷萃取液浓缩,得到萃取物浸膏;
c、将步骤b得到的三氯甲烷萃取物浸膏用常压正相硅胶柱层析分离,按体积比100:1-0:100的三氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行硅胶薄层层析(tlc)跟踪分析,合并相同流分,最终得到5个流分a-e;将流分e用加压正相硅胶柱层析进行分离,依次用体积比为30:1-0:1的正己烷-二氯甲烷和体积比为20:1-0:1的二氯甲烷-甲醇进行梯度洗脱,依次收集洗脱液减压浓缩后,进行tlc跟踪分析,合并相同流分,最终得到12个组分ea-el;将ej流分用葡聚糖凝胶lh-20柱层析纯化,用甲醇等度洗脱进行纯化,得到ej1-34流分,依次收集洗脱液在室温浓缩后,进行tlc跟踪分析合并流分ej12-13,将合并流份ej12-13采用制备型高效色谱[反相柱(c185μm10×250mm)]进行纯化,以浓度为49%的甲醇-水溶液等度洗脱,得到化合物名称为(3s,3ar,4s,6ar,8r,9as,9br)-4,8-二羟基-3-甲基-6,9-二甲基二氢薁基[4,5-b]呋喃-2(9bh-酮),(1.8mg),(3.0ml/min,210nm,tr=18min),命名为雪莲內酯d。
实施例7
将实施例1-6任意一种天山雪莲种子中的倍半萜内酯类化合物采用薄层层析法检测分析,采用高分辨质谱、一维和二维核磁共振谱等现代波谱手段鉴定其结构,其结果为:化合物名称为(3s,3ar,4s,6ar,8r,9as,9br)-4,8-二羟基-3-甲基-6,9-二甲基二氢薁基[4,5-b]呋喃-2(9bh-酮),为无色针状晶体,薄层板喷浓硫酸-香草醛(2%)显色剂溶液显深紫色;测定其在温度20℃时,甲醇溶液中浓度为1.0mg/ml浓度下的旋光度为-15;hr-esi-ms(m/z)给出的准分子离子峰为[m+h]-287.1257(计算值为287.1254),确定其分子式为c15h20o4。1hnmr(600mhz)和13cnmr(150mhz)数据见表1:
表1
根据核磁共振氢谱、碳谱及二维谱数据确定天山雪莲种子中倍半萜内酯类化合物的结构为(3s,3ar,4s,6ar,8r,9as,9br)-4,8-二羟基-3-甲基-6,9-二甲基二氢薁基[4,5-b]呋喃-2(9bh-酮)。
- 还没有人留言评论。精彩留言会获得点赞!