一种亚型Ph‑likeALL的检测试剂盒及其检测方法与流程
本发明涉及分子生物学领域,具体涉及一种亚型ph-likeall的检测试剂盒及其检测方法。
背景技术:
急性淋巴细胞白血病(简称all)是儿童最常见的肿瘤,发病率随年龄的增长而降低,目前重现性染色体改变是all的重要标志,包括染色体重组、结构改变等。多年来,临床通过结合上述染色体变异特征,对all进行危险分层治疗,使得all的治疗效果得到了很大得改善,其中儿童all的5年生存率提高到了85%,然而仍有部分患者治疗预后差,all的复发难治性使得该病依然是儿童及成人主要的致死疾病之一。
随着全基因组测序、基因表达谱芯片等生物技术在all疾病研究中的大量运用,临床对于all有了更多的认识,其中由欧美研究人员发现的一类特殊的all亚型ph-likeall(又称bcr-abl1likeall)是近年来重要的临床发现之一,对于all的危险分层及治疗提供了新的参考依据。
ph-likeall,是根据基因表达谱鉴定的一组疾病,其基因表达谱与bcr-abl1阳性all相似,但不表达bcr-abl1,所以称之为bcr-abl1-likeall,又称为ph-likeall。此类all主要见于急性前体b细胞淋巴细胞白血病(bcp-all),一般缺少bcp-all中典型的基因及染色体变异(etv6-runx1、e2a-pbx1、erg和mll重排、超二倍体等)且经常会伴有高风险临床特征。研究发现,ph-likeall约占sr(标危)和hr(高危)儿童b-all的15%,在青年all中约为27.4%。与bcr-abl1阳性all相似,ph-likeall患者预后差,常规化疗效果不佳,易复发。目前,国内外市场上没有一款产品专门用于检测ph-likeall。
技术实现要素:
本发明所要解决的技术问题是,克服以上现有技术的缺陷,提供一种亚型ph-likeall的检测试剂盒及其检测方法,能够全面准确地检测ph-likeall。
本发明的技术方案是:一种亚型ph-likeall的检测试剂盒,包括12组荧光探针和复染液;12组所述荧光探针分别为abl1,abl2,csf1r,pdgfrb,crlf2,jak2,epor,il2rb,ntrk3,ptk2b,tslp和tyk2;所述复染液由以下重量份数的组分组成:革兰氏染色液5~7份,生理盐水1~3份,纤维素0.2~0.6份,荧光素0.5~0.7份,磷酸一铵0.1~0.3份。
绝大部分ph-likeall患者有染色体重排或其他的遗传改变,可激活细胞因子受体或激酶信号。重排基因包括abl1,abl2,crlf2,csf1r,epor,jak2,ntrk3,pdgfrb,ptk2b,il2rb,tslp和tyk2。abl1,abl2,csf1r,jak2表达和pdgfrb融合基因导致细胞因子独立性扩增和磷酸化stat5激活。将上述重排基因进行标记得到荧光探针,与复染液制成试剂盒。
复染液在变性杂交后添加,其效果在复染及观察过程中体现。复染液采用革兰氏染色液为主要成分,荧光素增加荧光效果,添加生理盐水可保持荧光探针的标记显色效果;纤维素促进细胞的均匀分散,磷酸一铵则加快异常细胞的融合过程,细胞均匀分散的过程中,异常细胞相互间快速地融合。总之各组分相互有效地配合可以准确快速的观察样本是否有异性。
所述革兰氏染色液由以下重量份数的组分组成:结晶紫2~3份,草酸铵0.06~0.1份,蒸馏水500~600份,碘1~3份,碘化钾1~3份,乙醇120~150份,番红0.2~0.3份。
所述荧光探针的规格均为20人份,每组荧光探针的数量均为1管。所述荧光探针的3’号位均标记为橙色,所述荧光探针的5’号位均标记为绿色。所述复染液的规格为3只1ml。
一种基于所述亚型ph-likeall的检测试剂盒的检测方法,包括以下步骤:1)对样本进行肝素化处理制成骨髓涂片,将骨髓涂片进行预处理,制成涂片;2)将荧光探针用水溶解,并加入杂交液,得到探针溶液;3)将探针溶液滴加到涂片的杂交区域,进行变性杂交;4)滴加复染液到涂片的杂交区域,扫描并观察结果。添加复染液可以准确地观察到样本是否有异性,fish正常细胞显示为2橙色、2绿色,fish异常细胞显示1橙色、1绿色和一橙绿融合。
优选地,所述肝素化处理采用下列重量份数制成的涂层液:肝素5~10份,聚氨酯70~80份,羟丙基纤维素3~7份,水80~100份。采用该配方的涂层液,无毒,生物相容性好,使用中对细胞影响小,无细胞毒性;肝素溶于水,避免有机溶剂,降低成本;羟丙基纤维素亦可溶于水,促进样本均匀快速的肝素化。
进一步优选地,所述肝素化处理方法为:加热所述涂层液到40~50℃,然后真空条件下向样本喷涂。
优选地,所述步骤1)还可以对样本滴加edta—醋酸钠制成骨髓涂片。
优选地,所述杂交液由以下重量份数的物质组成:十二烷基磺酸钠5~10份,柠檬酸缓冲液20~50份,尿素30~50份。
优选地,所述骨髓涂片的预处理包括如下步骤:a)将涂片60~70℃预热5~10min,用浸蜡脱蜡透明液脱蜡2次每次10~20min,用无水乙醇脱水2次每次3~5min;所述浸蜡脱蜡透明液为异构烷烃型;b)依次在85%乙醇、70%乙醇、纯化水中梯度复水,各0.5~2min,吸去残余溶液;c)放在已经预热到75~85℃的预处理液中保温20~40min,取出在纯化水中浸泡1~2min,吸去残余溶液;d)取40~60mg胃蛋白酶干粉溶解在已预热至36~38℃的酶缓冲液中,浸入消化20~30min;e)在纯化水中浸泡1~2min,依次在85%乙醇、70%乙醇、纯化水中梯度脱水,各0.5~2min,干燥备用。所述步骤c)中所述预处理液为0.9~1.1mol/l的硫氰酸钠溶液。所述酶缓冲液为0.01mol/l的稀盐酸,室温下的ph值为2.0±0.2。
本发明的有益效果是:
1)本试剂盒检测囊括了目前已知的所有针对性用药的ph-likeall类型,经探针溶液与样本变性杂交后,滴加复染液,能够全面准确地检测ph-likeall;
2)荧光探针具有很强的特异性,只结合特定位点的染色体,特异性强;
3)采用荧光原位杂交技术,荧光信号在显微镜下一目了然,灵敏度很高;
4)该检测试剂盒具有简单、快速、成本低、灵敏度高、特异性强、检测全面等优点,获得骨髓细胞后可迅速处理成涂片,一般可在2-5天内出结果;
5)使用该试剂盒进行全面的检测,可以为临床指导用药提供有利依据。
附图说明
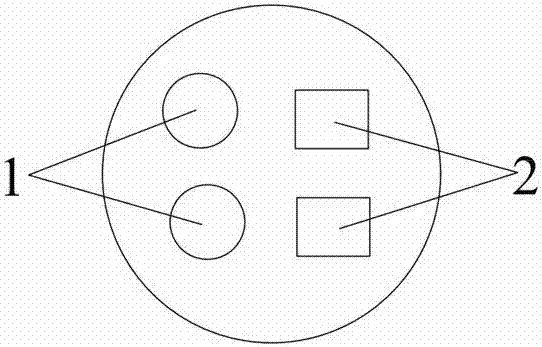
图1为fish正常细胞示意图,1、橙色,2、绿色。
图2为fish异常细胞,1、橙色,2、绿色,3、融合。
具体实施方式
下面用具体实施例对本发明做进一步详细说明,但本发明不仅局限于以下具体实施例。
以下所提供的实施例并非用以限制本发明所涵盖的范围,所描述的步骤也不是用以限制其执行顺序。本领域技术人员结合现有公知常识对本发明做显而易见的改进,亦落入本发明要求的保护范围之内。
实施例一
一种亚型ph-likeall的检测试剂盒,包括12组荧光探针和复染液;12组所述荧光探针分别为abl1,abl2,csf1r,pdgfrb,crlf2,jak2,epor,il2rb,ntrk3,ptk2b,tslp和tyk2;所述复染液由以下重量份数的组分组成:革兰氏染色液5份,生理盐水1份,纤维素0.2份,荧光素0.5份,磷酸一铵0.1份。
一种基于上述亚型ph-likeall的检测试剂盒的检测方法,包括下列步骤:
1)对样本进行肝素化处理制成骨髓涂片,将骨髓涂片进行预处理,制成涂片;所述肝素化处理方法为:加热所述涂层液到40℃,然后真空条件下向样本喷涂;所述肝素化处理采用下列重量份数制成的涂层液:肝素5份,聚氨酯70份,羟丙基纤维素3份,水80份;所述涂层液的剂量为20u/kg。
2)将荧光探针用水溶解,并加入杂交液,得到探针溶液;所述杂交液由以下重量份数的物质组成:十二烷基磺酸钠5份,柠檬酸缓冲液20份,尿素30份;
3)将探针溶液滴加到涂片的杂交区域,进行变性杂交;
4)滴加复染液到涂片的杂交区域,盖上盖玻片,置-25℃暗处复染30分钟,扫描并观察结果。
使用物镜对样本进行扫描,确定样本是否有异质性。fish正常细胞显示为2橙色、2绿色,fish异常细胞显示1橙色、1绿色和1橙绿融合。
所述骨髓涂片的预处理包括如下步骤:
1)60℃预热10min,用浸蜡脱蜡透明液脱蜡2次每次20min,用无水乙醇脱水2次每次5min,所述浸蜡脱蜡透明液为异构烷烃型;
2)依次在85%乙醇、70%乙醇、纯化水中梯度复水,各2min,吸去残余溶液;
3)放在已经预热到75℃的预处理液中保温40min,取出在纯化水中浸泡2min,吸去残余溶液;所述预处理液为0.9mol/l的硫氰酸钠溶液;
4)取40mg胃蛋白酶干粉溶解在已预热至36℃的酶缓冲液中,浸入消化20min;所述酶缓冲液为0.01mol/l的稀盐酸,室温下的ph值为2;
5)在纯化水中浸泡2min,依次在85%乙醇、70%乙醇、纯化水中梯度脱水,各2min,干燥备用。
实施例二
一种亚型ph-likeall的检测试剂盒,包括12组荧光探针和复染液;12组所述荧光探针分别为abl1,abl2,csf1r,pdgfrb,crlf2,jak2,epor,il2rb,ntrk3,ptk2b,tslp和tyk2;所述复染液由以下重量份数的组分组成:革兰氏染色液7份,生理盐水3份,纤维素0.6份,荧光素0.7份,磷酸一铵0.3份。
一种基于上述亚型ph-likeall的检测试剂盒的检测方法,包括下列步骤:
1)对样本进行肝素化处理制成骨髓涂片,将骨髓涂片进行预处理,制成涂片;所述肝素化处理方法为:加热所述涂层液到50℃,然后真空条件下向样本喷涂;所述肝素化处理采用下列重量份数制成的涂层液:肝素10份,聚氨酯80份,羟丙基纤维素7份,水100份;所述涂层液的剂量为40u/kg。
2)将荧光探针用水溶解,并加入杂交液,得到探针溶液;所述杂交液由以下重量份数的物质组成:十二烷基磺酸钠10份,柠檬酸缓冲液50份,尿素50份;
3)将探针溶液滴加到涂片的杂交区域,进行变性杂交;
4)滴加复染液到涂片的杂交区域,盖上盖玻片,置-15℃暗处复染40分钟,扫描并观察结果。
使用物镜对样本进行扫描,确定样本是否有异质性。fish正常细胞显示为2橙色、2绿色,fish异常细胞显示1橙色、1绿色和1橙绿融合。
所述骨髓涂片的预处理包括如下步骤:
1)70℃预热5min,用浸蜡脱蜡透明液脱蜡2次每次15min,用无水乙醇脱水2次每次5min,所述浸蜡脱蜡透明液为异构烷烃型;
2)依次在85%乙醇、70%乙醇、纯化水中梯度复水,各1min,吸去残余溶液;
3)放在已经预热到85℃的预处理液中保温20min,取出在纯化水中浸泡2min,吸去残余溶液;所述预处理液为1.1mol/l的硫氰酸钠溶液;
4)取60mg胃蛋白酶干粉溶解在已预热至38℃的酶缓冲液中,浸入消化30min;所述酶缓冲液为0.01mol/l的稀盐酸,室温下的ph值为2.2;
5)在纯化水中浸泡2min,依次在85%乙醇、70%乙醇、纯化水中梯度脱水,各2min,干燥备用。
实施例三
一种亚型ph-likeall的检测试剂盒,包括12组荧光探针和复染液;12组所述荧光探针分别为abl1,abl2,csf1r,pdgfrb,crlf2,jak2,epor,il2rb,ntrk3,ptk2b,tslp和tyk2;所述复染液由以下重量份数的组分组成:革兰氏染色液6份,生理盐水2份,纤维素0.4份,荧光素0.6份,磷酸一铵0.2份。
一种基于上述亚型ph-likeall的检测试剂盒的检测方法,包括下列步骤:
1)对样本进行肝素化处理制成骨髓涂片,将骨髓涂片进行预处理,制成涂片;所述肝素化处理方法为:加热所述涂层液到45℃,然后真空条件下向样本喷涂;所述肝素化处理采用下列重量份数制成的涂层液:肝素8份,聚氨酯75份,羟丙基纤维素5份,水90份;所述涂层液的剂量为30u/kg。
2)将荧光探针用水溶解,并加入杂交液,得到探针溶液;所述杂交液由以下重量份数的物质组成:十二烷基磺酸钠8份,柠檬酸缓冲液35份,尿素40份;
3)将探针溶液滴加到涂片的杂交区域,进行变性杂交;
4)滴加复染液到涂片的杂交区域,盖上盖玻片,置-20℃暗处复染30分钟,扫描并观察结果。
使用物镜对样本进行扫描,确定样本是否有异质性。fish正常细胞显示为2橙色、2绿色,fish异常细胞显示1橙色、1绿色和1橙绿融合。
所述骨髓涂片的预处理包括如下步骤:
1)65℃预热8min,用浸蜡脱蜡透明液脱蜡2次每次15min,用无水乙醇脱水2次每次4min,所述浸蜡脱蜡透明液为异构烷烃型;
2)依次在85%乙醇、70%乙醇、纯化水中梯度复水,各1min,吸去残余溶液;
3)放在已经预热到80℃的预处理液中保温30min,取出在纯化水中浸泡2min,吸去残余溶液;所述预处理液为1mol/l的硫氰酸钠溶液;
4)取50mg胃蛋白酶干粉溶解在已预热至37℃的酶缓冲液中,浸入消化25min;所述酶缓冲液为0.01mol/l的稀盐酸,室温下的ph值为2.0;
5)在纯化水中浸泡2min,依次在85%乙醇、70%乙醇、纯化水中梯度脱水,各1min,干燥备用。
实施例四
一种亚型ph-likeall的检测试剂盒,包括12组荧光探针和复染液;12组所述荧光探针分别为abl1,abl2,csf1r,pdgfrb,crlf2,jak2,epor,il2rb,ntrk3,ptk2b,tslp和tyk2;所述复染液由以下重量份数的组分组成:革兰氏染色液6份,生理盐水2份,纤维素0.4份,荧光素0.6份,磷酸一铵0.2份。
一种基于上述亚型ph-likeall的检测试剂盒的检测方法,包括下列步骤:
1)对样本edta—醋酸钠制成骨髓涂片,将骨髓涂片进行预处理,制成涂片;所述肝素化处理方法为:加热所述涂层液到45℃,然后真空条件下向样本喷涂;所述肝素化处理采用下列重量份数制成的涂层液:肝素8份,聚氨酯75份,羟丙基纤维素5份,水90份;所述涂层液的剂量为30u/kg。
2)将荧光探针用水溶解,并加入杂交液,得到探针溶液;所述杂交液由以下重量份数的物质组成:十二烷基磺酸钠8份,柠檬酸缓冲液35份,尿素40份;
3)将探针溶液滴加到涂片的杂交区域,进行变性杂交;
4)滴加复染液到涂片的杂交区域,盖上盖玻片,置-20℃暗处复染40分钟,扫描并观察结果。
使用物镜对样本进行扫描,确定样本是否有异质性。fish正常细胞显示为2橙色、2绿色,fish异常细胞显示1橙色、1绿色和1橙绿融合。
所述骨髓涂片的预处理包括如下步骤:
1)65℃预热8min,用浸蜡脱蜡透明液脱蜡2次每次15min,用无水乙醇脱水2次每次4min,所述浸蜡脱蜡透明液为异构烷烃型;
2)依次在85%乙醇、70%乙醇、纯化水中梯度复水,各1min,吸去残余溶液;
3)放在已经预热到80℃的预处理液中保温30min,取出在纯化水中浸泡1min,吸去残余溶液;所述预处理液为1mol/l的硫氰酸钠溶液;
4)取50mg胃蛋白酶干粉溶解在已预热至37℃的酶缓冲液中,浸入消化25min;所述酶缓冲液为0.01mol/l的稀盐酸,室温下的ph值为2.0;
5)在纯化水中浸泡2min,依次在85%乙醇、70%乙醇、纯化水中梯度脱水,各1min,干燥备用。
- 还没有人留言评论。精彩留言会获得点赞!
- 禽流感病毒H5N1亚型Re-5株阳性血清和阴性血清标准物质及制备方法
- 5亚型Na<sup>+</sup>/H<sup>+</sup>交换泵(NHE5)抑制剂在改善记忆保持(memory retention)中的用途的制作方法
- Hiv-1亚型间(c/b’)基因组和其用途的制作方法
- 一种基于rt-lamp技术的h3亚型流感快速检测分型方法
- Hiv-1亚型间(c/b’)基因组和其用途的制作方法
- PCV2、PRV与SIV H9亚型多重SYBR Green Ⅰ实时荧光PCR引物及其检测方法
- 一株hiv-1 crf01_ae亚型毒株及其应用的制作方法
- CSFV、PRRSV、PCV2与SIV H9亚型多重SYBR Green Ⅰ实时荧光PCR引物及其检测方法
- PRRSV、SIV H9亚型与PCV2多重SYBR Green Ⅰ实时荧光PCR引物及其检测方法
- 一种含hiv-1 crf01-ae亚型rt基因的杂交免疫缺陷质粒、病毒及应用的制作方法