用于无创产前检测胎儿非整倍体染色体的参考品的制作方法
本发明涉及基因检测领域,具体涉及用于无创产前检测胎儿非整倍体染色体的参考品。
背景技术:
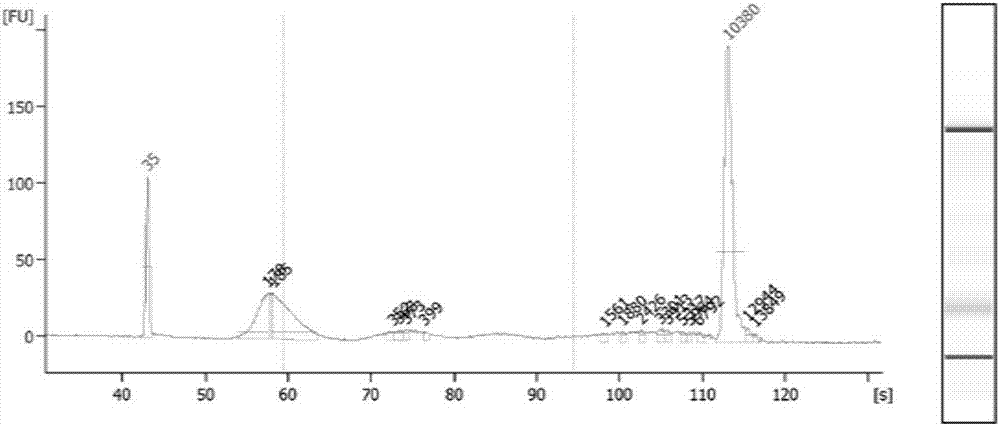
:提高生殖健康水平及防控重大出生缺陷是我国重大需求。随着二胎政策放开,将有更多的高龄孕妇,如何精确、简便、快速、有效的对其进行产前检测,控制好出生缺陷,始终是摆在我国相关政府部门和临床检验实验室面前的一道难题。尽早进行产前筛查和诊断是应对出生缺陷的最有效的应对措施。目前羊膜腔穿刺、绒毛活检、脐血抽取等传统产前诊断技术,存在侵入性取材方式本身不可克服的固有缺陷,对胎儿和孕妇都存在相当程度的危险性。血清学筛查和超声等无创性产前检测方法灵敏度和准确性欠佳。建立安全、准确的产前诊断体系,不仅是减少先天性遗传病儿出生、提高人口质量的根本途径,也是有利于国计民生的重大课题。因此发展新的无创性产前检测技术不仅具有重要的临床意义,也是当前产前诊断领域发展的主导方向之一。基于二代测序技术检测胎儿游离脱氧核糖核酸进行唐氏综合症无创产前筛查是本领域重要进展。利用二代测序技术对母体外周血浆中游离dna进行测序,并将测序结果进行生物信息分析,得到胎儿的遗传信息,从而判断胎儿是否患21三体综合征(唐氏综合征)、18三体综合征(爱德华氏综合征)、13三体综合征(帕陶氏综合征)三大染色体疾病。多项研究结果显示,无创产前检测技术是一种有效的筛查胎儿染色体非整倍体的方法,准确性可达99%以上,与目前临床上所用的母体血清筛查实验相比,无创产前检测具有准确率高,假阳性率低的特点。而且该方法相对比较安全,可以有效避免胎儿宫内感染及流产、减轻孕妇心理负担。无创产前检测技术的临床应用,可以显著的减少侵入性产前诊断在临床上的应用,提高侵入性产前诊断阳性检出率。因此,无创产前检测技术具有较高的临床应用价值。但目前该技术的发展受到参考品获取方面的限制,目前针对无创产前检测技术没有参考品,市场上买不到可用的参考品,从而严重制约了相关产品研发和现有产品的质量控制,因此,本发明提供了一种用于无创产前检测胎儿非整倍体染色体的参考品,用于无创产前检测相关产品的研发和质量控制。技术实现要素:本发明的目的是提供一种用于无创产前检测胎儿非整倍体染色体的参考品。在一种实施方式中,本发明提供一种用于无创产前检测胎儿非整倍体染色体的参考品,所述参考品包括:来源于正常染色体倍型的母体的组织或培养的细胞系基因组的第一片段化核酸,和来源于非整倍体染色体阳性的胎儿的组织或培养的细胞系基因组的第二片段化核酸,所述第一片段化核酸与第二片段化核酸有遗传相关性;所述第一片段化核酸和所述第二片段化核酸的长度是150-200个碱基对;由于孕周10-16周的孕妇血浆游离dna中胎儿游离dna的比例一般为5-30%,所以本发明中所述第一片段化核酸的量占所述参考品总核酸量的至少70%,和所述第二片段化核酸的量占所述参考品总核酸量的5-30%。第一片段化核酸的量例如是80%、90%、95%、97%。这种细胞系包括来源于corriellinstitute或americantypeculturecollection(atcc)的细胞系,例如来源于corriellinstitute的ag09387(来自母亲,正常染色体倍型)。无创产前检测参考品的第二片段化核酸来源于细胞系,例如来源于21号染色体三体的细胞系。这种细胞系包括来源于corriellinstitute或americantypeculturecollection(atcc)的细胞系,例如来源于corriellinstitute的ag09394(来自孩子,t21三体,其母亲的细胞为ag09387)。在一种实施方式中,非整倍体染色体是单倍体、部分单倍体、三倍体、部分三倍体、四倍体或五倍体。在一种实施方式中,非整倍体染色体是21号染色体三倍体、18号染色体三倍体或13号染色体三倍体。在一种实施方式中,第一片段化核酸来源于母体的外周血的淋巴细胞。在一种实施方式中,第二片段化核酸来源于胎儿的胎盘组织。在一种实施方式中,第一片段化核酸和/或所述第二片段化核酸通过超声方法进行片段化或者通过酶切方法进行片段化获得。在一种实施方式中,酶切方法中使用的酶是仅降解核小体连接区的核酸酶。在一种实施方式中,核酸酶是微球菌核酸酶。在一种实施方式中,参考品是21号染色体三倍体的参考品。在一种实施方式中,第一片段来源于培养的ag09387细胞系,和第一片段来源于培养的ag09394细胞系。本发明的参考品制备简单,定量准确,易于质控,充分模拟实际临床样本,具有重要应用前景。附图说明为了更清楚地说明本申请实施例中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本申请中记载的一些实施例,对于本领域普通技术人员来说,在不付出创造性劳动的前提下,还可以根据这些附图获得其它的附图。图1是孕妇外周血游离dna的片段分布图;图2是通过超声人工制备的来源于组织细胞的dna的片段分布图;和图3是通过超声人工制备的来源于细胞系的dna片段分布图。具体实施方式为了使本领域
技术领域:
人员更好地理解本申请中的技术方案,下面将结合下面结合实施例对本发明作进一步说明,显然,所描述的实施例仅仅是本申请一部分实施例,而不是全部的实施例。基于本申请中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都应当属于本申请保护的范围。实施例1通过组织和血液来源的基因组dna制备阳性参考品样本选择:样本1是t21三体综合征(唐氏综合征)阳性男性胎儿的胎盘组织样本,选择男性胎儿的原因是利于定量检测混合核酸的掺入比例;样本2是母体样本,即该胎儿母亲的外周血,两个样本有遗传相关性,用于模拟母体外周血来源的游离dna的组成。样本3是怀孕女性的血浆样本,用于提供血浆游离dna。dna提取:使用基因组提取试剂盒(dp304,天根生化科技北京有限公司)根据说明书提取样本1(胎盘组织样本)的基因组dna。对样本2(外周血)首先裂解红细胞,然后将分离到的白细胞用基因组提取试剂盒(dp304,天根生化科技北京有限公司)根据说明书提取其基因组dna。使用病毒核酸提取系统(thermofisher,37011d)对样本3(怀孕女性的血浆样本)进行血浆游离核酸提取,操作步骤按照系统说明书进行。提取的核酸于-20℃保存,长期保存于-80℃。dna片段化:通过超声方法把上述提取的基因组dna进行片段化。使用covaris离心管(afafiberscrew-cap,covaris)用超声仪m220(covaris)对50μl基因组dna进行超声片段化,根据仪器说明书设置超声时间为375秒,以获得预期核酸片段长度为150-200bp的片段。片段化核酸用dna纯化试剂盒根据说明书进行纯化(d4032,zymo)。并用ampurexp磁珠进行选择性回收核酸片段,回收片段大小在160-200bp的dna片段。通过qubit3.0(thermo)进行核酸定量,然后按照胎儿dna:母体dna的比例为1:10的比例将样本1和样本2来源的片段化dna混合(由于孕周10-16周的孕妇血浆游离dna中胎儿游离dna的比例一般为5-30%,所以本次实验中掺入比例是胎儿dna:母体dna为1:10),得到t21三体综合征(唐氏综合征)阳性参考品样本,然后通过bioanalyzer2100(agilent)电泳来检测片段化dna。电泳如图2所示。与样本3提取的游离dna片段大小一致(图1)。通过数字pcr测定胎儿dna含量:对上述片段化核酸混合物用伯乐数字pcr系统(qx200)定量其中胎儿dna浓度比例。获得精确定量胎儿dna比例的片段化核酸混合物作为阳性参考品。pcr反应体系配制如下:体系包括1×dropletpcrsupermix(bio-rad);用于扩增y染色体上sry基因的上游引物及下游引物,扩增上游引物sry-f序列为seqidno.1:5'-tggcgattaagtcaaattcgc-3',扩增下游引物sry-r序列为seqidno.2:5'-ccccctagtaccctgacaatgtatt-3'(生工生物工程(上海)股份有限公司合成),引物终浓度为900nm;sry特异的探针序列为seqidno.3:5'-tgtcgcactctccttgtttttgaca-3'(theromofisher公司合成),羧基端用fam标记,羟基端用无荧光的猝灭基团nfq修饰,探针终浓度为250nm;参照基因选择1号染色体上的eif2c1基因,其扩增上游引物e1f2c1-f序列为seqidno.4:5'-gttcggctttcaccagtct-3',扩增下游引物e1f2c1-r序列为seqidno.5:5'-ctccatagctctccccactc-3'(生工生物工程(上海)股份有限公司合成),引物终浓度为900nm;特异的探针序列probe2为seqidno.6:5’-cgccctgccatgtggaagat-3’,羧基端用vic标记,羟基端用无荧光的猝灭基团nfq修饰,探针终浓度为250nm。上述获得的核酸混合物和提取的游离dna用qubit定量后,在体系中加入1ng作为模板,最后补加去离子水至终体积为20μl。微液滴生成:首先打开qx200液滴生成仪电源,预热30分钟;然后按上述配制的20μl反应体系振荡混匀,离心除气泡,将微液滴生成芯片放入卡槽中,在芯片最下面一排8个孔中各加入70μl微滴生成油,中间一排8个孔加入反应体系,盖上胶垫,然后将以上卡槽平稳放置于微滴生成仪中,启动液滴生成。芯片的最上面一排孔用于收集液滴。液滴生成反应结束后,将收集的微液滴转移到96孔板中,然后进行pcr反应,反应程序为:95℃10min;95℃20sec,60℃1min,40cycle;98℃10min;4℃hold;ramp2℃/s。微液滴检测:将完成pcr的96孔板放入qx200微液滴读取仪中,打开quantasoft软件,先进行flushsystem。然后对96孔板中样品信息进行设定,主要是提供实验名称、类型、检测体系以及探针荧光标记信息等,然后运行检测程序,结束后结果自动保存和分析。检测结果如表1所示,来源于组织细胞和其母体外周血细胞的片段化dna混合物中胎儿dna的含量为10.7%,与预期结果相符合,可作为t21阳性参考品。实施例2通过培养细胞来源的基因组dna制备阳性参考品样本选择:样本4是t21三体阳性细胞系ag09394(男性),样本5是其对应的母亲的细胞系为ag09387。用rpmi1640培养基,含2mm左旋谷酰胺,15%胎牛血清进行细胞培养,向t25组织培养瓶中加入10-20ml培养基(竖直放置培养),37℃,co2浓度5%培养箱培养。保持培养基中细胞浓度不低于200,000个细胞/ml。间隔3-4天应更换新鲜培养基。培养上限密度为一百万个细胞/ml,对培养后细胞进行计数,然后对1×108细胞用基因组提取试剂盒(dp304,天根生化科技北京有限公司)根据说明书提取样本4和样本5的细胞基因组dna。dna片段化:按照实施例1中的方法对dna进行片段化和磁珠纯化,然后通过qubit3.0(thermo)进行核酸定量,并按照ag09394dna:ag09387dna的比例为1:10的比例将样本4和样本5来源的片段化dna混合,得到t21阳性参考品样本,然后通过bioanalyzer2100(agilent)电泳来检测片段化dna。电泳如图3所示。与样本3提取的游离dna片段大小一致(图1)。同样,按照实施例1中的方法对片段化核酸进行ddpcr定量。来源于细胞系制备的片段化dna混合物中胎儿dna的含量为10.4%,与预期结果相符合,可作为t21阳性参考品。表1是通过数字pcr定量的胎儿dna占核酸总量的比例结果实施例3通过无创产前dna检测试剂对t21阳性参考品进行检测为了验证制备的无创产前检测胎儿非整倍体染色体的阳性参考品是否可以满足无创产前检测的需求,本次实验利用无创产前二代测序试剂盒(博奥生物)对其进行测试。测试样本为实施例1和实施例2中的血浆游离dna和两个片段化dna混合物。首先,根据说明书进行文库构建,然后利用qpcr测试文库浓度,其中文库浓度结果如表2所示,从表2中的数据可以说明建库浓度3个样本没有差异,其建库结果达到测试预期。然后对文库进行测序分析,按照正常sop操作分别完成对上述3例样本的测序,测序结果表明,3例样本均为t21阳性,与预期结果相符。结果表明,本发明的片段化dna混合物可作为无创产前检测用的阳性参考品。表2通过无创产前检测试剂盒对本发明的参考品的检测结果序号样本名称文库浓度(nm/μl)1样本3提取的游离dna25.762样本1和样本2提取的dna超声破碎的核酸混合物44.733样本4和样本5提取的dna超声破碎的核酸混合物46.47应该理解到披露的本发明不仅仅限于描述的特定的方法、方案和物质,因为这些均可变化。还应理解这里所用的术语仅仅是为了描述特定的实施方式方案的目的,而不是意欲限制本发明的范围,本发明的范围仅受限于所附的权利要求。本领域的技术人员还将认识到,或者能够确认使用不超过常规实验,在本文中所述的本发明的具体的实施方案的许多等价物。这些等价物也包含在所附的权利要求中。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1