再生柞蚕丝素蛋白溶液及其制备方法与流程
本发明涉及一种天然高分子溶液及其制备方法,具体涉及一种再生柞蚕丝素蛋白溶液及其制备方法。
背景技术:
生物医用材料是当前生命科学和材料科学共同的前沿研究热点之一。目前已经开发应用于组织工程等生物医学领域的可降解高分子材料很多,但这些材料的原创性研究工作大多属于国外并在我国申请了多项专利。因此积极寻找合适的原料,研制具有我国自主知识产权的生物材料,对于减小我国组织工程支架等生物材料对国外的依赖性,培育新的高新技术产业和实现国民经济的可持续发展具有重要意义。柞蚕丝(tussahsilk;antheraeapernyi)是以柞蚕茧为原料缫制而成的天然蚕丝纤维,是我国的宝贵资源。我国年产柞蚕茧3~4万吨,占世界柞蚕茧总产量的90%以上,这是世界稀有我国特有的宝贵资源,但目前柞蚕丝主要用作普通的纺织原料,所体现出的经济价值十分有限。除作低价值纺织原料以外,将柞蚕丝用作生物医学材料的需求越来越强烈,比如用作酶固定载体、细胞培养基质、伤口敷料、人工皮肤、组织工程支架等。
从六十年代至今,国内外学者对柞蚕丝素蛋白的氨基酸组成、分子结构、物理性能等进行了较多的研究。与家蚕丝相比,柞蚕丝具有更强的吸湿性、耐热性、耐酸碱性,其氨基酸组成也有所不同:柞蚕丝素蛋白主要氨基酸含量顺序为丙氨酸(ala)>甘氨酸(gly)>丝氨酸(ser)>酪氨酸(tyr),且含有丰富的天冬氨酸(asp)和精氨酸(arg),因此含有精氨酸-甘氨酸-天冬氨酸(rgd)三肽序列。rgd序列作为细胞膜整合素受体与细胞外配体相结合的识别位点,介导细胞与细胞外基质及细胞之间的相互作用,能够促进细胞对支架的黏附。这些优异的特性赋予柞蚕丝素蛋白在组织工程支架等生物材料领域得天独厚的优势和广泛的应用前景。
天然柞蚕丝因为形态单一(纤维状)和结晶度较高难降解而限制了其应用。已知有很多盐溶液可以溶解天然桑蚕丝,如氯化钙(cacl2)、氯化镁(mgcl2)、溴化锂(libr)等,从而可以轻易制得桑蚕丝素蛋白(b丝素蛋白)溶液。然而由于极强的分子间作用,柞蚕丝比桑蚕丝更难溶解,一般溶解桑蚕丝的体系很难溶解柞蚕丝。强酸和强碱都会使柞蚕丝素蛋白发生剧烈水解,分子量大大降低,如经过盐酸、磷酸和硫酸溶解后的分子量大约在200-5000d,所以通常只是用强酸和强碱来制取丝素肽和丝素粉,极大限制其应用。
近年来出现的微波水解法制得的分子量在2000-3000d之间,该分子量的柞蚕丝素蛋白依然不能满足医用材料的要求,因此需要探索其他溶解方法来获得较大分子量的柞蚕丝素蛋白,从而能够满足对柞蚕丝素蛋白溶液再次成型加工及成品物理机械性能的要求。目前可以获得柞蚕丝素蛋白溶液的方法主要有两种:第一种方法是直接从成熟柞蚕后部丝腺中提取液态柞蚕丝素蛋白,该方法操作步骤简单,但仅适用于小量制备柞蚕丝素蛋白溶液及进行相关研究,无法工业化;另外一种方法是用中性盐溶解的方法获得再生柞蚕丝素蛋白溶液,目前可以溶解柞蚕丝的中性盐主要是硝酸钙和硫氰酸锂(liscn),虽然该方法可以提高柞蚕丝素蛋白溶液的获取量,但溶解效率低、工艺复杂,更重要的是会严重破坏柞蚕丝原有的多级结构,使得再生柞蚕丝素蛋白材料性能较差,难以满足应用要求。
技术实现要素:
针对现有技术的不足,本发明解决的技术问题是提供一种再生柞蚕丝素蛋白溶液及其制备方法,由该方法得到的柞蚕丝素蛋白保留其本身的原有多级原纤结构。
为解决上述技术问题,本发明的技术方案是这样实现的:
一种再生柞蚕丝素蛋白溶液的制备方法,包括如下步骤:
(1)对柞蚕丝进行除杂、脱胶、超声波处理,得到前处理柞蚕丝;
(2)将前处理柞蚕丝置于含甲酸的三氟乙酸水溶液中,制备混合液,常温下搅拌溶解,得到再生柞蚕丝素蛋白有机溶液;
(3)将再生柞蚕丝素蛋白有机溶液置于去离子水中透析,得到再生柞蚕丝素蛋白溶液。
上述技术方案中,所述超生波处理的功率为1~10kw,时间为30~50分钟;优选的,所述超生波处理的功率为3~6kw,时间为35~40分钟。
上述技术方案中,所述三氟乙酸水溶液的质量浓度为80~90%;优选的,所述三氟乙酸水溶液的质量浓度为85~88%。
上述技术方案中,所述混合液中,甲酸的质量为三氟乙酸的3~5%。
上述技术方案中,所述混合液中,前处理柞蚕丝的浓度(蚕丝溶解浓度)为5wt%~10wt%;优选的蚕丝溶解浓度为7~8wt%。
上述技术方案中,所述搅拌溶解的时间为5~20分钟。
上述技术方案中,所述透析的温度为4~10℃,透析的时间为3~5天。
本发明还公开了一种再生柞蚕丝素蛋白材料及其制备方法,包括如下步骤:
(1)对柞蚕丝进行除杂、脱胶、超声波处理,得到前处理柞蚕丝;
(2)将前处理柞蚕丝置于含甲酸的三氟乙酸水溶液中,制备混合液,常温下搅拌溶解,得到再生柞蚕丝素蛋白有机溶液;
(3)将再生柞蚕丝素蛋白有机溶液置于去离子水中透析,得到再生柞蚕丝素蛋白水溶液;
(4)将再生柞蚕丝素蛋白水溶液制备得到再生柞蚕丝素蛋白材料。
上述技术方案中,所述再生柞蚕丝素蛋白材料包括再生柞蚕丝素蛋白膜、再生柞蚕丝素蛋白凝胶。
本发明实质上是采用三氟乙酸为溶剂,添加少量甲酸,在常温下直接快速溶解柞蚕丝,然后经透析去除有机溶剂,得到再生柞蚕丝素蛋白水溶液,以纳米纤维为主要结构;制备成再生丝素材料,具有良好的力学性能。
与已有技术相比较,本发明的优点如下:
本发明公开的制备方法使用超声波前处理工艺,疏松了蚕丝内部的紧密结构,有利于溶剂渗透加速了蚕丝的溶解,并且有利于调控溶剂对丝蛋白的溶解程度。
本发明公开的再生柞蚕丝素蛋白溶液及其制备方法,仅采用有机溶剂,避免高浓度中性盐在高温条件下对蚕丝的严重降解,并且通过有机溶剂的混合配比实现调控蚕丝蛋白溶解程度的目的。
本发明公开的再生柞蚕丝素蛋白溶液与以往柞蚕丝素蛋白溶液相比,显著特征是以柞蚕丝素蛋白纳米原纤为主要单元,该纳米原纤为天然柞蚕丝本身具有,而非再生过程中通过自组装形成,是天然柞蚕丝素蛋白纳米原纤。
本发明公开的再生柞蚕丝素蛋白溶液首次仅以有机溶剂为溶解液,常温搅拌即可实现产品制备,该制备方法工艺简单,得到的溶液无盐、有机溶剂残留,为纯柞蚕丝素蛋白溶液。
附图说明
图1是本发明实施例一制得溶液中丝素蛋白形态的扫描电镜图;
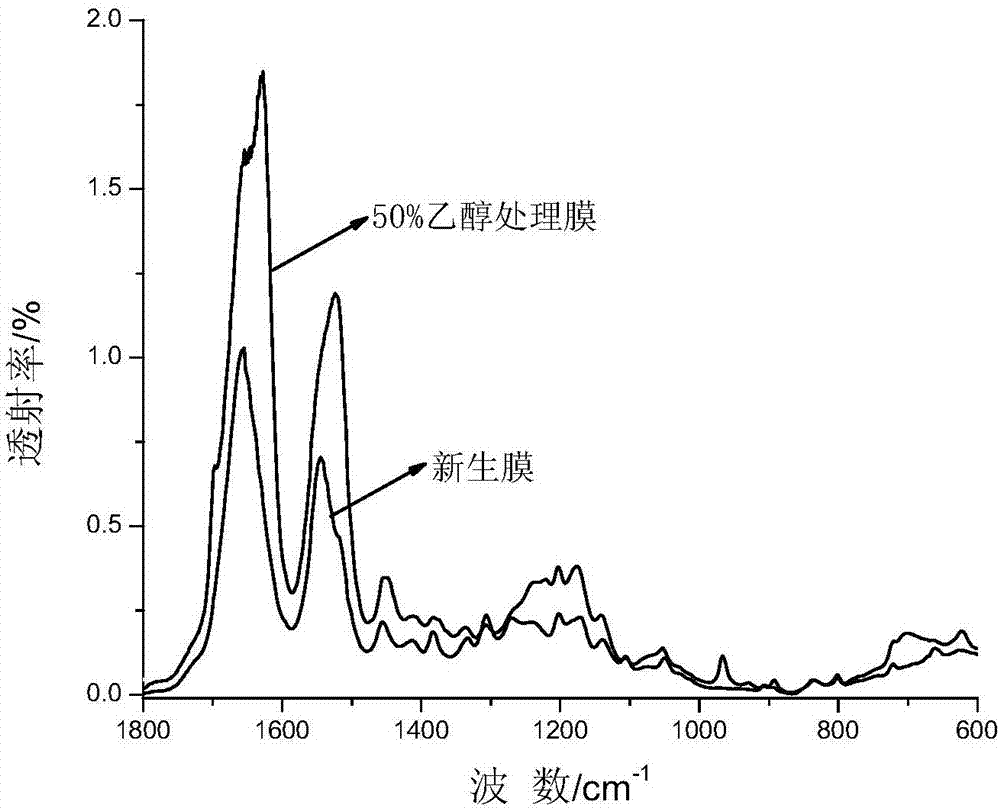
图2是本发明实施例一制得的再生丝素蛋白膜处理前后的红外谱图;
图3是本发明实施例二制得溶液中丝素蛋白形态的扫描电镜图。
具体实施方式
下面对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域技术人员在没有做出创造性劳动前提下所获得所有其他实施例,都属于本发明保护的范围。
实施例一
天然柞蚕丝用质量分数0.5wt%的碳酸氢钠溶液煮沸60min,去离子水充分洗涤晾干后获得脱胶蚕丝。将脱胶蚕丝置于烧杯中,加入去离子水,然后进行超声处理,超声波功率5kw,超声波处理时间40分钟。室温下,将脱胶蚕丝置于含有3%甲酸(三氟乙酸质量为基数)的86wt%三氟乙酸水溶液中,蚕丝质量分数7%,磁力搅拌10min后获得再生丝素蛋白三氟乙酸溶液。然后将溶液注入透析袋中,置于流动去离子水中透析3d,透析温度10℃,得到纯化的再生柞蚕丝素蛋白纳米纤维水溶液。该溶液中丝素蛋白为纳米纤维状,纤维长度为0.1-15µm,直径0.01-1µm(如图1所示),丝素蛋白分子量分布范围150~300kda。再生丝素蛋白溶液注入聚乙烯皿中,自然干燥即得到再生柞蚕丝素蛋白膜,蛋白质结构为无定形结构,经乙醇水溶液处理后转化为β-折叠结晶结构(如图2所示),该膜力学性能优异,断裂强度98mpa,断裂伸长率6.5%;经过凝胶化处理,可得到生物相容性良好的再生柞蚕丝素蛋白凝胶;湿态压缩模量为96mpa;可应用在制备组织工程支架中。
对比例一:
参见实施例一的工艺,其中不含甲酸,丝素蛋白分子量分布范围50~70kda;再生柞蚕丝素蛋白膜的断裂强度46mpa,断裂伸长率3.5%;再生柞蚕丝素蛋白凝胶的湿态压缩模量为36mpa。
实施例二:
天然柞蚕丝用质量分数0.05wt%的碳酸氢钠溶液煮沸60min,然后去离子水充分洗涤,重复三次晾干后获得脱胶蚕丝。将脱胶蚕丝置于烧杯中,加入去离子水,然后进行超声处理,超声波功率3kw,超声波处理时间35分钟。室温下,将脱胶蚕丝置于含有5%甲酸(三氟乙酸质量为基数)的85wt%三氟乙酸水溶液中,蚕丝质量分数8%,磁力搅拌5min后获得再生丝素蛋白有机溶液。然后将溶液注入透析袋中,置于流动去离子水中透析5d,透析温度4℃,得到纯化的再生柞蚕丝素蛋白纳米纤维水溶液。该溶液中丝素蛋白为纳米纤维状,如图3所示,丝素蛋白分子量分布范围140~200kda;自然干燥即得到再生柞蚕丝素蛋白膜,断裂强度95mpa,断裂伸长率6.1%;经过凝胶化处理,可得到生物相容性良好的再生柞蚕丝素蛋白凝胶;湿态压缩模量为94mpa;可应用在制备组织工程支架中。
对比例二:
参见实施例二的工艺,其中不含甲酸,丝素蛋白分子量分布范围40~65kda;再生柞蚕丝素蛋白膜的断裂强度40mpa,断裂伸长率3.2%;再生柞蚕丝素蛋白凝胶的湿态压缩模量为38mpa。
实施例三:
天然柞蚕丝用质量分数0.25wt%的碳酸氢钠溶液煮沸60min,然后去离子水充分洗涤,重复三次晾干后获得脱胶蚕丝。将脱胶蚕丝置于烧杯中,加入去离子水,然后进行超声处理,超声波功率6kw,超声波处理时间35分钟。室温下,将脱胶蚕丝置于含有4%甲酸(三氟乙酸质量为基数)的88wt%三氟乙酸水溶液中,蚕丝质量分数7%,磁力搅拌20min后获得再生丝素蛋白有机溶液。然后将溶液注入透析袋中,置于流动去离子水中透析3d,透析温度4℃,得到纯化的再生柞蚕丝素蛋白纳米纤维水溶液,丝素蛋白分子量分布范围110~180kda;自然干燥即得到再生柞蚕丝素蛋白膜,蛋白质结构为无定形结构,经乙醇水溶液处理后转化为β-折叠结晶结构,断裂强度89mpa,断裂伸长率6.1%;经过凝胶化处理,可得到生物相容性良好的再生柞蚕丝素蛋白凝胶;湿态压缩模量为95mpa;可应用在制备组织工程支架中。
对比例三:
参见实施例三的工艺,其中不采用超声波处理,丝素蛋白分子量分布范围90~120kda;再生柞蚕丝素蛋白膜的断裂强度68mpa,断裂伸长率5.5%;再生柞蚕丝素蛋白凝胶的湿态压缩模量为82mpa。
实施例四:
天然柞蚕丝用质量分数0.5wt%的碳酸氢钠溶液煮沸60min,然后去离子水充分洗涤,重复三次晾干后获得脱胶蚕丝。将脱胶蚕丝置于烧杯中,加入去离子水,然后进行超声处理,超声波功率1kw,超声波处理时间50分钟。室温下,将脱胶蚕丝置于含有4%甲酸(三氟乙酸质量为基数)的80wt%三氟乙酸水溶液中,蚕丝质量分数5%,磁力搅拌15min后获得再生丝素蛋白有机溶液。然后将溶液注入透析袋中,置于流动去离子水中透析5d,透析温度10℃,得到纯化的再生柞蚕丝素蛋白纳米纤维水溶液,丝素蛋白分子量分布范围160~320kda;自然干燥即得到再生柞蚕丝素蛋白膜,蛋白质结构为无定形结构,经乙醇水溶液处理后转化为β-折叠结晶结构,断裂强度78mpa,断裂伸长率5.5%;经过凝胶化处理,可得到生物相容性良好的再生柞蚕丝素蛋白凝胶;湿态压缩模量为82mpa;可应用在制备组织工程支架中。
对比例四:
参见实施例四的工艺,其中甲酸用量为8%,丝素蛋白分子量分布范围8~10kda;再生柞蚕丝素蛋白膜的断裂强度40mpa,断裂伸长率2.9%;再生柞蚕丝素蛋白凝胶的湿态压缩模量为31mpa。
实施例五:
天然柞蚕丝用质量分数0.25wt%的碳酸钠溶液煮沸60min,然后去离子水充分洗涤,重复两次晾干后获得脱胶蚕丝。将脱胶蚕丝置于烧杯中,加入去离子水,然后进行超声处理,超声波功率10kw,超声波处理时间30分钟。室温下,将脱胶蚕丝置于含有4%甲酸(三氟乙酸质量为基数)的90wt%三氟乙酸水溶液中,蚕丝质量分数5%,磁力搅拌10min后获得再生丝素蛋白有机溶液。然后将溶液注入透析袋中,置于流动去离子水中透析3d,透析温度4℃,得到纯化再生柞蚕丝素蛋白纳米纤维水溶液,丝素蛋白分子量分布范围130~200kda;自然干燥即得到再生柞蚕丝素蛋白膜,蛋白质结构为无定形结构,经乙醇水溶液处理后转化为β-折叠结晶结构,断裂强度75mpa,断裂伸长率5.6%;经过凝胶化处理,可得到生物相容性良好的再生柞蚕丝素蛋白凝胶;湿态压缩模量为83mpa;可应用在制备组织工程支架中。
对比例五:
参见实施例五的工艺,其中超声波功率20kw,丝素蛋白分子量分布范围30~80kda;再生柞蚕丝素蛋白膜的断裂强度58mpa,断裂伸长率4.5%;再生柞蚕丝素蛋白凝胶的湿态压缩模量为49mpa。
实施例六:
天然柞蚕丝用质量分数0.5wt%的碳酸钠溶液煮沸60min,去离子水充分洗涤晾干后获得脱胶蚕丝。将脱胶蚕丝置于烧杯中,加入去离子水,然后进行超声处理,超声波功率6kw,超声波处理时间50分钟。室温下,将脱胶蚕丝置于含有4%甲酸(三氟乙酸质量为基数)的85wt%三氟乙酸水溶液中,蚕丝质量分数10%,磁力搅拌10min后获得再生丝素蛋白有机溶液。然后将溶液注入透析袋中,置于流动去离子水中透析3d,透析温度4℃,得到纯化的再生柞蚕丝素蛋白纳米纤维水溶液,丝素蛋白分子量分布范围160~300kda;自然干燥即得到再生柞蚕丝素蛋白膜,蛋白质结构为无定形结构,经乙醇水溶液处理后转化为β-折叠结晶结构,断裂强度72mpa,断裂伸长率5.5%;经过凝胶化处理,可得到生物相容性良好的再生柞蚕丝素蛋白凝胶;湿态压缩模量为81mpa;可应用在制备组织工程支架中。
对比例六:
参见实施例六的工艺,其中采用90%的甲酸溶解,不采用三氟乙酸,丝素蛋白分子量分布范围6~8kda;再生柞蚕丝素蛋白膜的断裂强度28mpa,断裂伸长率2.5%;再生柞蚕丝素蛋白凝胶的湿态压缩模量为29mpa。
- 还没有人留言评论。精彩留言会获得点赞!