一种氨基甲壳素及其制备方法和应用与流程
本发明涉及农药行业,可应用于农药领域,具体涉及一种氨基甲壳素的制备方法和应用。
背景技术:
甲壳素(chitin)是仅次于纤维素的第二大多糖,它存在于虾、蟹、或者一些微生物和真菌的细胞壁。其独特的性质,生物降解性,生物相容性和无毒性使其广泛的应用于医药、食品、农业、日化、环保等方面。
近年来,甲壳素及其衍生物对细菌和真菌等微生物群体的抗菌活性受到很大的关注。甲壳素的大多数生物活性归因于其游离氨基。多糖骨架上的(乙酰基)氨基无疑在展现各种独特性质方面起关键作用。实现这一点的最常见方法是将含胺侧链与多糖主链连接,许多研究人员已经修饰了中性多糖以纳入氨基。然而,由于甲壳素具有强氢键联网络结构和高度结晶性,所以甲壳素的化学改性是困难的。
技术实现要素:
为解决上述技术问题,为解决上述技术问题,本发明提供了一种氨基甲壳素及其制备方法和应用。先以甲壳素为原料,加入对甲苯磺酰氯制备出磺酰化甲壳素,再将磺酰化甲壳素与叠氮化钠反应,得到叠氮化甲壳素,随后将叠氮基团还原得到氨基甲壳素。
具体技术方案如下:
一种氨基甲壳素,所述氨基甲壳素结构式如下:
其中聚合度n的平均取值范围为300~900。
所述氨基甲壳素可应用于农药领域。
氨基甲壳素的制备方法,以甲壳素、氢氧化钠、对甲苯磺酰氯的氯仿溶液、叠氮化钠、二甲基亚砜、三苯基膦为原料,先以甲壳素为原料,加入对甲苯磺酰氯制备出磺酰化甲壳素,再将磺酰化甲壳素与叠氮化钠反应,得到叠氮化甲壳素,随后将叠氮基团还原得到氨基甲壳素,包括如下步骤:
(1)磺酰化甲壳素的制备:取一定量的甲壳素分散于氢氧化钠溶液中,进行减压操作3~5小时,依次加入相应比例冰、对甲苯磺酰氯的氯仿溶液,于0℃反应1~3小时,室温下继续反应1~3小时,然后加入水中进行沉淀、抽滤并洗涤至中性得到滤饼,即得磺酰化甲壳素;
(2)叠氮化甲壳素的制备:取一定量上述磺酰化甲壳素与相应比例叠氮化钠,溶于二甲基亚砜中,于80~100℃反应4~6小时,然后加入乙酸乙酯进行沉淀、抽滤得到滤饼,即得叠氮化甲壳素;
(3)氨基甲壳素的制备:取一定量上述叠氮化甲壳素与相应比例三苯基膦,加入一定量的n’n-二甲基甲酰胺,在室温反应12~24h,然后加入乙醇进行沉淀、抽滤得到滤饼,即得氨基甲壳素。
上述步骤(1)所述甲壳素、氢氧化钠、冰、对甲苯磺酰氯、氯仿、用量为:1g甲壳素、用20~50ml的42%氢氧化钠溶液、10~50g冰、3~15g对甲苯磺酰氯、10~50ml氯仿;
上述步骤(2)所述磺酰化甲壳素、二甲基亚砜、叠氮化钠用量为:1g磺酰化甲壳素、20~50ml的二甲基亚砜、0.4~2g叠氮化钠;
上述步骤(3)所述叠氮化甲壳素、n’n-二甲基甲酰胺、三苯基膦用量为:1g叠氮化甲壳素、用40~100ml的n’n-二甲基甲酰胺、1~5g三苯基膦。
上述步骤(1)所述的减压操作为:将分散于氢氧化钠溶液中的甲壳素装入反应瓶,将反应瓶接到旋蒸蒸发仪上,打开水泵抽气,降低压力,反应瓶常温旋转。
本方法的优点是:
(1)甲壳素具有强氢键与高度结晶性,因此,甲壳素的化学改性通常是困难的。由于与相邻重复单元的分子内氢键和相邻的乙酰胺基团的空间位阻,c3-oh(3号碳的羟基)具有较低的反应性,如果c3-oh(3号碳的羟基)发生反应,那么活性高的c6-oh(6号碳的羟基)必然会发生反应,两个位置均发生取代,取代度高即主链上活性官能团更多,抗菌效果更高,本发明选用甲苯磺酰化来制备甲壳素衍生物,因为甲苯磺酰基是一个良好的亲电基团和离去基团,所以使用-oh基团的磺酰化得到中间体磺酰化甲壳素,方便后续反应。
甲壳素通过在碱溶液中减压的方式,先使甲壳素构型由
然后加入叠氮化钠,使磺酰基离去得到叠氮化甲壳素,最后还原叠氮基团,将氨基引入到甲壳素中,增加了糖骨架上氨基的含量,首次合成了抗菌能力较强的氨基甲壳素,抗菌活性测定结果表明氨基甲壳素的抗菌活性明显高于甲壳素、对某些真菌,其抑菌活性接近阳性对照(两性霉素)。
(2)通常抗菌药物都是水溶性的,不溶于水的糖衍生物抗菌效果都不好,但是研究表明本发明合成的产物虽然不溶于水,但是具有很好的抗菌活性,可以广泛应用于农药领域。
附图说明
图1为甲壳素的红外光谱图;
图2为本发明实施例1制备的磺酰化甲壳素的红外光谱图;
图3为本发明实施例1制备的叠氮化甲壳素的红外光谱图;
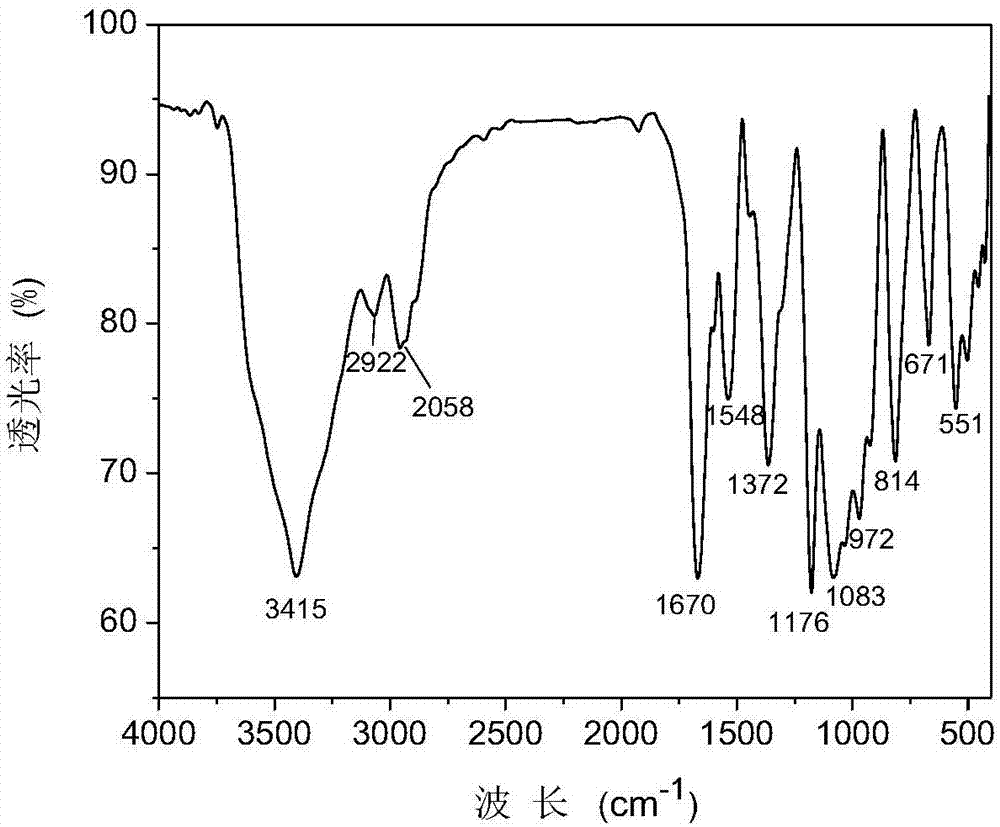
图4为本发明实施例1制备的氨基甲壳素的红外光谱图。
具体实施方式
下面结合实施例对本发明进行详细说明,但本发明的保护范围不受实施例所限。
实施例1:
(1)磺酰化甲壳素的制备:取1.0g甲壳素分散于20ml42%的氢氧化钠溶液中,减压5小时,加入20g冰、对甲苯磺酰氯的氯仿溶液(5g对甲苯磺酰氯溶于10ml氯仿),于0℃反应2小时,室温下继续反应2小时,然后加入水中进行沉淀、抽滤并洗涤至中性得到滤饼,即得磺酰化甲壳素;
(2)叠氮化甲壳素的制备:取2.5g磺酰化甲壳素,倒入50mldmso(二甲基亚砜),再加入1.6g叠氮化钠,于90℃反应6小时,然后加入乙酸乙酯中进行沉淀、抽滤得到滤饼,即得叠氮化甲壳素;
(3)氨基甲壳素的制备:取0.63g叠氮化甲壳素,倒入40mldmf(n,n-二甲基甲酰胺)与1.83g三苯基膦在室温反应12小时,然后加入乙醇中进行沉淀、抽滤得到滤饼,即得氨基甲壳素。
实施例2:
(1)磺酰化甲壳素的制备:取1.0g甲壳素分散于30ml42%的氢氧化钠溶液中,减压3小时,加入30g冰、对甲苯磺酰氯的氯仿溶液(8g对甲苯磺酰氯溶于20ml氯仿),于0℃反应1.5小时,室温下继续反应1.5小时,然后加入水中进行沉淀、抽滤并洗涤至中性得到滤饼,即得磺酰化甲壳素;
(2)叠氮化甲壳素的制备:取2.5g磺酰化甲壳素,倒入60mldmso(二甲基亚砜),再加入2.6g叠氮化钠,于80℃反应6小时,然后加入乙酸乙酯中进行沉淀、抽滤得到滤饼,即得叠氮化甲壳素;
(3)氨基甲壳素的制备:取0.63g叠氮化甲壳素,倒入50mldmf(n,n-二甲基甲酰胺)与2.1g三苯基膦在室温反应12小时,然后加入乙醇中进行沉淀、抽滤得到滤饼,即得氨基甲壳素。
实施例3:
(1)磺酰化甲壳素的制备:取1.0g甲壳素分散于40ml42%的氢氧化钠溶液中,减压4小时,加入40g冰、对甲苯磺酰氯的氯仿溶液(12g对甲苯磺酰氯溶于30ml氯仿),于0℃反应2.5小时,室温下继续反应2.5小时,然后加入水中进行沉淀、抽滤并洗涤至中性得到滤饼,即得磺酰化甲壳素;
(2)叠氮化甲壳素的制备:取2.5g磺酰化甲壳素,倒入70mldmso(二甲基亚砜),再加入3.6g叠氮化钠,于100℃反应4小时,然后加入乙酸乙酯中进行沉淀、抽滤得到滤饼,即得叠氮化甲壳素;
(3)氨基甲壳素的制备:取0.63g叠氮化甲壳素,倒入60mldmf(n,n-二甲基甲酰胺)与2.4g三苯基膦在室温反应18小时,然后加入乙醇中进行沉淀、抽滤得到滤饼,即得氨基甲壳素。
实施例4:
(1)磺酰化甲壳素的制备:取1.0g甲壳素分散于50ml42%的氢氧化钠溶液中,减压4小时,加入50g冰、对甲苯磺酰氯的氯仿溶液(15g对甲苯磺酰氯溶于40ml氯仿),于0℃反应3小时,室温下继续反应3小时,然后加入水中进行沉淀、抽滤并洗涤至中性得到滤饼,即得磺酰化甲壳素;
(2)叠氮化甲壳素的制备:取2.5g磺酰化甲壳素,倒入80mldmso(二甲基亚砜),再加入3.6g叠氮化钠,于95℃反应5小时,然后加入乙酸乙酯中进行沉淀、抽滤得到滤饼,即得叠氮化甲壳素;
(3)氨基甲壳素的制备:取0.63g叠氮化甲壳素,倒入60mldmf(n,n-二甲基甲酰胺)与2.8g三苯基膦在室温反应24小时,然后加入乙醇中进行沉淀、抽滤得到滤饼,即得氨基甲壳素。
图1为甲壳素的红外光谱图,图2为本发明实施例1制备的磺酰化甲壳素的红外光谱图,由图可见,与甲壳素原料相比,2058cm-1处为甲基的振动吸收峰,1776cm-1处的吸收峰为磺酰基的峰,814cm-1处的吸收峰为苯环的吸收峰。以上分析数据,证明磺酰化甲壳素合成成功。
图3为本发明实施例1制备的叠氮化甲壳素的红外光谱图,由图3与图2对比可见,2112cm-1处为叠氮的振动吸收峰,1776cm-1处的吸收峰消失,证明叠氮化甲壳素合成成功。
图4为本发明实施例1制备的氨基甲壳素的红外光谱图,由图4与图3对比可见,2112cm-1处的吸收峰消失,证明氨基甲壳素合成成功。
抗菌能力的测定:分别测定两性霉素(阳性对照),甲壳素和氨基甲壳素的抑菌能力。将实施例1中实验用甲壳素和氨基甲壳素真空冷冻干燥至恒重后。以等量的两性霉素b为阳性对照,以无菌水代替样品作为空白对照。将培养基摇匀倒入直径为9cm的培养皿中,待其完全凝固后,取真菌菌液涂抹均匀,然后在培养基上打4个孔(直径为5mm),将样品(两性霉素b,甲壳素,氨基甲壳素和水)填入孔中。在27℃下培养48h,测量菌落的抑制直径,全部实验重复一次。甲壳素和氨基甲壳素的抑菌能力如表1所示。
表1甲壳素和氨基甲壳素的抑菌直径
实验结果表明,本发明所合成的氨基甲壳素与甲壳素的抑菌能力如表1所示,将氨基引入到甲壳素中,得到抗菌能力较强的氨基甲壳素,且氨基甲壳素的抗菌能力强于甲壳素,对特定真菌,其抗菌能力强于对照两性霉素。基于上述结果,我们推测氨基甲壳素的抗菌活性主要源自甲壳素骨架上的氨基。
- 还没有人留言评论。精彩留言会获得点赞!