检测SMAD4基因V354L位点突变的试剂盒的制作方法
本发明涉及一种检测smad4基因v354l位点突变的试剂盒,属于生物技术和医学技术领域。
背景技术:
smad4是一种抑癌基因,常见于胰腺癌和结肠癌。转化生长因子β(tgf-β)调节着细胞生长、分化以及多种生理、病理过程,tgf-β与smad4构成的信号通路与肿瘤的发生机制密切相关,smad4在该信号通路中发挥着核心作用。相关研究发现,smad4基因的缺失或突变与肿瘤细胞的侵袭、淋巴结转移以及肿瘤血管形成密切相关。smad4基因的缺失还可以促进肺癌的发生与发展,当smad4基因被敲除后,肺癌细胞对dna拓扑异构酶抑制剂的敏感性增强。
taqman探针是一种荧光检测技术,用含有特异序列的荧光标记探针来检测pcr产物,taqman探针的出现使得定量pcr技术的特异性有了很大提高。该特异性的荧光探针在两条引物之间与模板特异性地结合。在探针的5’端标记有荧光报告基团如fam、vic等,在探针的3’端标记荧光淬灭基团。当探针完整时,仪器检测不到荧光信号,因为报告基团发射的荧光信号会会被淬灭基团吸收;在pcr扩增过程中,taqdna聚合酶会酶切降解与模板相结合的探针,导致3’端淬灭基团与5’端报告基团分离,仪器就可以检测到荧光信号。
目前发明一种能够快速检测患者smad4基因v354l(c.1060g>c)位点突变的方法,进而有助于指导非小细胞肺癌患者辅助性化疗方案的选择,成为急需解决的问题。
技术实现要素:
本发明针对现有技术在检测smad4基因v354l(c.1060g>c)位点突变时所表现出的缺点,提供一种准确、快速、廉价的检测smad4基因v354l(c.1060g>c)位点突变的试剂盒。
发明概述
发明人采用二代高通量测序技术检测到smad4基因v354l(c.1060g>c)突变位点,并通过统计学方法分析发现了接受辅助性化疗的肺癌患者的预后与smad4基因v354l(c.1060g>c)位点突变密切相关。在所有检测到smad4基因v354l(c.1060g>c)位点突变的iiboriiia期非小细胞肺癌患者中,接受卡铂联合多西他赛的辅助性化疗方案相比于卡铂联合长春瑞滨,患者的无病生存期(dfs)以及总生存期(os)显著延长。然而在所有smad4基因该位点没有发生突变的iiboriiia期非小细胞肺癌患者中,卡铂联合多西他赛方案或者卡铂联合长春瑞滨方案,对患者预后的影响无统计学差异。根据上述发现,发明人根据实时荧光定量pcr检测方法,设计出一种检测smad4基因v354l(c.1060g>c)位点突变的试剂盒,该试剂盒能够准确、快速地检测smad4基因该位点的突变,并且操作较为简便,成本相对廉价。
发明详述
检测smad4基因v354l位点突变的试剂盒,包括:
检测smad4基因v354l(c.1060g>c)位点突变的特异性引物,所述特异性引物的上游核苷酸序列如seqidno.1所示,下游核苷酸序列如seqidno.2所示。
根据本发明优选的,上述试剂盒,还包括:
特异性识别smad4基因v354l(c.1060g>c)突变位点的taqman探针,所述taqman探针的野生型序列如seqidno.3所述,突变型taqman探针序列如seqidno.4所示;
根据本发明优选的,上述试剂盒,还包括:
缓冲液,dntps,taqdna聚合酶,mgcl2和dna提取试剂盒。
根据本发明优选的,上述试剂盒,反应在20μl体系中进行,各成分反应浓度如下:
引物0.2μm、taqman探针0.1μm、dntps0.25mm、taqdna聚合酶0.025u/μl、mgcl21.5mm、dna提取试剂盒提取到的模板dna<250ng。
根据本发明优选的,所述野生型taqman探针的5′端连接vic荧光标记;突变型taqman探针的5′端连接fam荧光标记。
有益效果
1、本发明首次发现了smad4基因v354l(c.1060g>c)位点突变与接受辅助性化疗的非小细胞肺癌患者的预后密切相关,并根据该发现设计出检测smad4基因v354l(c.1060g>c)位点突变的试剂盒,有助于为非小细胞肺癌患者术后的辅助性化疗提供个体化指导;
2、本发明所述的试剂盒采用实时荧光定量pcr技术,在检测smad4基因v354(c.1060g>c)位点突变上,相比现有二代高通量测序技术,该试剂盒具有操作简单、时间短、价格低廉的特点,并且该试剂盒实用范围广,所检测的dna可以提取自新鲜组织、外周血以及石蜡切片样本。
附图说明
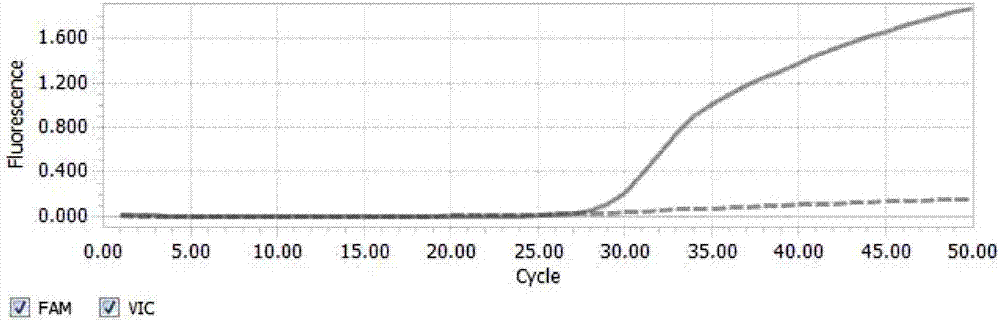
图1是用本发明所述试剂盒检测smad4基因v354l(c.1060g>c)位点野生型的检测结果;
图中:虚线为vic荧光基团在野生型探针5′端上所发荧光;
图2是用本发明所述试剂盒检测smad4基因v354l(c.1060g>c)位点突变型的检测结果;
图中:实线为fam荧光基团在突变型探针5′端上所发荧光。
具体实施方式
下面结合实施例对本发明的技术方案做进一步阐述,但本发明所保护范围不限于此。
实施例中dna提取试剂盒包括:genereadtmdnaffpekit购自qiagen公司;tianampgenomicdnakit购自tiangen公司。
taqdna聚合酶等其他试剂均购自大连宝生物公司。
实施例1
发明人采用二代高通量测序技术检测到smad4基因v354l(c.1060g>c)突变位点,并通过统计学方法分析发现了接受辅助性化疗的肺癌患者的预后与smad4基因v354l(c.1060g>c)位点突变密切相关。在所有smad4基因该位点没有发生突变的iiboriiia期非小细胞肺癌患者中,卡铂联合多西他赛方案或者卡铂联合长春瑞滨方案,对患者预后的影响无统计学差异。但是在所有检测到smad4基因v354l(c.1060g>c)位点突变的iiboriiia期非小细胞肺癌患者中,接受卡铂联合多西他赛的辅助性化疗方案相比于卡铂联合长春瑞滨,患者的无病生存期(dfs)以及总生存期(os)显著延长。
具体研究过程如下:
入组病例:发明人回顾性地调查了从2010年2月至2012年7月在山大二院就诊的非小细胞肺癌患者,根据入组标准,最终确定一批iiboriiia期非小细胞肺癌入组本研究,入组肺癌患者均有明确的临床病理特征和完整的术后随访信息,且所有患者术后均接受了辅助性化疗,方案为卡铂联合多西他赛或者长春瑞滨。
研究方法:采用二代高通量测序技术对上述肿瘤组织进行基因测序,步骤包括:
①应用dna提取试剂盒genereadtmdnaffpekit从石蜡切片标本中提取dna并进行定量;②根据提取的dna建立ionampliseqtm文库;
③进行ionpgmtmhi-qtm测序及数据分析。
研究结果:在33.3%的病人中检测到了smad4基因v354l(c.1060g>c)位点突变,发明人通过kaplan-meier分析法发现:在所有检测到smad4基因v354l(c.1060g>c)位点突变的iiboriiia期非小细胞肺癌患者中,接受卡铂联合多西他赛的辅助性化疗方案相比于卡铂联合长春瑞滨,患者的无病生存期(dfs)以及总生存期(os)显著延长;然而在所有smad4基因该位点没有发生突变的iiboriiia期非小细胞肺癌患者中,卡铂联合多西他赛方案或者卡铂联合长春瑞滨方案,对患者预后的影响无统计学差异。
研究结论:在检测到smad4基因v354l(c.1060g>c)位点突变的肺癌患者中,接受卡铂联合多西他赛化疗方案的患者表现出了更好的预后。通过对smad4基因该位点的检测,可以为非小细胞肺癌患者辅助性化疗方案的选择提供更加有效合理的指导。
根据上述发现,进行特异性引物设计,引物设计原则如下所示:
①在核酸系列保守区内设计引物,引物序列长度一般为18~25bp之间;②引物的3’端至少要有4个碱基是完全保守的;③所设计引物中的碱基要保证随机分配,tm值在58~60℃之间;④引物中不能存在连续4个互补的碱基;⑤引物3′端不可修饰,但引物5′端可以修饰;⑥引物的3’端最好不为g或/和c,且不应有2个g或/和c出现在引物3’端的5个碱基中。
taqman探针设计原则如下所示:
①探针的设计应在核酸序列保守区内,并具有特异性;②所设计的探针尽量缩短,长度一般在10~30碱基之间;③要保证探针序列中的碱基随机分布;④探针序列中不能含有连续4个互补的碱基;⑤探针序列内碱基g的数量不能比碱基c的数量多,且碱基g+c含量应控制在40%~60%之间;⑥探针5'端的第一个碱基不能是g;⑦在探针5′端连接荧光发光基团,3′端连接荧光猝灭基团。
根据上述原则进行引物设计:
1、在cosmic数据库中找到包含smad4基因v354l(c.1060g>c)突变位点的cdna序列,长度为20-30bp;
2、通过blast确定该cdna序列在dna上所对应的外显子序列;
3、根据该外显子序列,通过genomebrower确定与之对应的完整dna序列(包括外显子和内含子),如下所示:g为突变位点
4、使用引物和探针设计软件primerexpress3.0.1确定上游引物序列如seqidno.1所示,下游引物序列如seqidno.2所示;野生型taqman探针的序列如seqidno.3所示,突变型taqman探针的序列如seqidno.4所示。
实施例2
检测smad4基因v354l(c.1060g>c)位点突变的试剂盒,包括:
检测smad4基因v354l(c.1060g>c)突变位点特异引物,所述特异引物的上游引物核苷酸序列如seqidno.1所示,所述特异引物的下游引物核苷酸序列如seqidno.2所示;
特异性识别smad4基因v354l(c.1060g>c)位点突变的taqman探针,如seqidno.3所述,vic荧光标记连接在野生型taqman探针的5′端;如seqidno.4所示,fam荧光标记连接在突变型taqman探针的5′端。
缓冲液,taqdna聚合酶,dntps,mgcl2和dna提取试剂盒;
各成分反应浓度如下:
引物0.2μm、taqman探针0.1μm、taqdna聚合酶0.025u/μl、dntps0.25mm、mgcl21.5mm、dna提取试剂盒提取到的模板dna10~50ng。
实施例3
应用实施例2所述检测smad4基因v354l(c.1060g>c)位点突变的试剂盒检测10例非小细胞肺癌石蜡切片样本中smad4基因该位点的突变情况。
使用dna提取试剂盒genereadtmdnaffpekit(qiagen)分别从10例石蜡切片样本中提取模板dna;
pcr反应在20μl体系中进行,pcr的反应条件为:
使用罗氏lc96实时荧光pcr仪进行pcr反应,94℃预变性180sec,然后按照94℃变性5sec,60℃退火和延伸30sec,进行50个循环。
经检测,有7例检测结果如图1所示,smad4基因v354l(c.1060g>c)位点为野生型;有3例检测结果如图2所示,smad4基因v354l(c.1060g>c)位点为突变型。
采用二代高通量测序技术分别对上述10例石蜡切片标本进行基因检测,所得10例样本smad4基因该位点的检测结果与应用本发明所述试剂盒检测结果完全一致。
实施例4
应用实施例2所述检测smad4基因v354l(c.1060g>c)位点突变的试剂盒检测10例非小细胞肺癌新鲜癌组织中rb1基因c.2039t>c位点的突变。
应用dna提取试剂盒tianampgenomicdnakit(tiangen)分别从10例新鲜癌组织中提取模板dna;
pcr反应条件、各组分反应时终浓度以及结果判定同实施例1。
7例样本中smad4基因v354l(c.1060g>c)位点为野生型,如图1所示;3例样本中smad4基因v354l(c.1060g>c)位点为突变型,如图2所示。
采用二代高通量测序技术分别对10例新鲜癌组织标本进行基因检测,所得10例样本smad4基因该位点的检测结果与应用本发明所述试剂盒检测结果完全一致。
实施例5
应用实施例2所述检测smad4基因v354l(c.1060g>c)位点突变的试剂盒检测10例非小细胞肺癌患者外周血中smad4基因v354l(c.1060g>c)位点突变。
应用dna提取试剂盒tianampgenomicdnakit(tiangen)分别从10例血液标本中提取模板dna;
pcr反应条件、各组分反应时终浓度以及结果判定同实施例1。
8例样本中smad4基因v354l(c.1060g>c)位点为野生型,如图1所示;2例样本中smad4基因v354l(c.1060g>c)位点为突变型,如图2所示。
采用二代高通量测序技术分别对10例血液标本进行基因检测,所得10例样本smad4基因该位点的检测结果与应用本发明所述试剂盒检测结果完全一致。
实施例6
选取了2011年1月至2012年1月之间的非小细胞肺癌患者的石蜡切片标本32例,所选病例都接受了术后辅助性化疗(卡铂联合多西他赛或长春瑞滨),并且有完整的术后随访信息。
应用实施例2所述检测smad4基因v354l(c.1060g>c)位点的试剂盒检测32例非小细胞肺癌石蜡切片样本中smad4基因该位点的突变情况。
使用dna提取试剂盒genereadtmdnaffpekit(qiagen)分别从32例石蜡切片标本中提取模板dna;
pcr反应条件、各组分反应时终浓度以及结果判定同实施例1。
结果发现其中15例存在smad4基因v354l(c.1060g>c)位点突变。发明人进一步通过kaplan-meier分析法发现:存在smad4基因v354l(c.1060g>c)位点突变的肺癌病人,接受卡铂联合多西他赛化疗方案相比卡铂联合长春瑞滨化疗方案能显著延长无病生存期(dfs)和总生存期(os)。从而证明了检测smad4基因v354l(c.1060g>c)位点突变的试剂盒具有为非小细胞肺癌患者辅助性化疗方案提供个体化指导的应用价值。
以上所述实施例仅为本发明优选的具体实施方案,并不用来限制本发明,凡是在本发明精神和原则之内,所作的任何修改、等同替换以及改进等,均应包含在本发明的保护范围之内。
sequencelisting
<110>山东大学第二医院
<120>检测smad4基因v354l位点突变的试剂盒
<160>4
<170>patentinversion3.5
<210>1
<211>24
<212>dna
<213>人工合成
<400>1
cttcaagctgccctattgttactg24
<210>2
<211>21
<212>dna
<213>人工合成
<400>2
caaaagcgatctcctccagaa21
<210>3
<211>17
<212>dna
<213>人工合成
<400>3
tgatggatacgtggacc17
<210>4
<211>17
<212>dna
<213>人工合成
<400>4
tgatggatacctggacc17
- 还没有人留言评论。精彩留言会获得点赞!