在单管反应中同时检测多个高危型人乳头瘤病毒的试剂盒的制作方法
本发明属于体外诊断领域,具体涉及一种在单管反应中同时检测多个高危型人乳头瘤病毒的试剂盒。
背景技术:
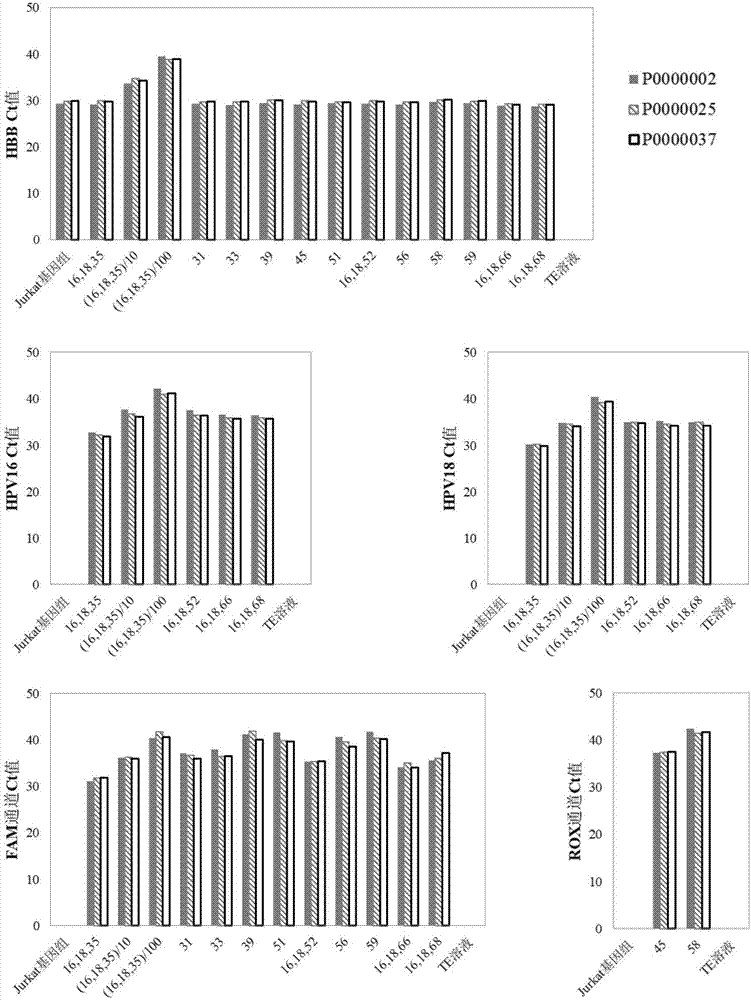
:人乳头瘤病毒(humanpapillomavirus,hpv)是一种嗜上皮性双链dna球形病毒,属于乳头瘤病毒科,主要感染皮肤和粘膜组织。hpv感染可引起疣、良性肿瘤和癌症。目前已有证据显示hpv感染可以导致包括宫颈癌、阴道癌、阴茎癌、肛门癌、口咽癌等多种癌症。据国际人乳头瘤病毒参考中心(internationalhumanpapillomavirusreferencecenter)的最新统计,目前共发现超过200种hpv基因型。然而并不是所有的hpv基因型均可以诱发癌症。低危型hpv的感染可以诱发生长在生殖器官附近皮肤和粘膜上的人类寻常疣、尖锐湿疣以及生长在粘膜上的乳头状瘤等良性病变,只有为数不多的高危型hpv的感染可能致癌。目前了解最深入的hpv致癌的范例是女性宫颈癌。也正是因为在这方面的先驱性工作,德国科学家haraldzurhausen于2008年获得诺贝尔生理学和医学奖。宫颈癌是发生在女性子宫下段宫颈处的恶性肿瘤,是女性中第4位高发恶性肿瘤,占妇女癌症死亡率的第4位。据国际卫生组织(who)的国际癌症研究中心(iarc)报道,2012年全球宫颈癌新发病例为52.8万例,约有26.6万妇女死于宫颈癌。几乎所有宫颈癌的发生都是高危型hpv的持续感染导致的,而且从最初感染到癌症的发生需要经历5到10年的时间。因此,利用以高危型hpv的遗传物质dna作为检测对象的hpv分子诊断技术来进行宫颈癌筛查,可以提前发现病因,有效地对宫颈癌进行早期预防,从而降低发病率和死亡率。与醋酸目测检查、巴氏涂片和液基细胞学等传统宫颈癌筛查手段相比,hpv分子诊断具有灵敏度高且不依赖病理医生的主观判断的优势。因此,hpv分子诊断已经成为当前发达国家宫颈癌筛查的首选方法。hpv分子诊断技术最大的一个挑战是在保证检测灵敏度的同时有效地将高危型hpv与低危型hpv区分开来,以避免因误诊而造成的过度诊断和过度治疗以及由此对患者产生的不必要的精神压力。如前所述,目前发现的hpv基因型已经超过200种,而根据who/iarc等权威机构的研究成果,其中只有14种基因型被定义为可以诱发宫颈癌的高危型,即hpv16、18、31、33、35、39、45、51、52、56、58、59、66和68。此外,即使是14种高危型hpv中也并不是每一种基因型都具有相同的致癌能力。hpv16和18是其中危害最大的两个基因型,二者分别导致55%和15%的宫颈癌病例。因此,能够对hpv16和18进行分型的高危型hpv分子诊断技术对于hpv检测阳性患者的分流具有独到的优势。再有,并不是所有宫颈部位感染了高危型hpv的患者就一定会罹患宫颈癌,大部分此类感染为一过性感染,即人体自身的免疫功能可以在6到24个月内有效地将其清除。高危型hpv能否被免疫系统清除的决定因素是多方面的,既包括患者免疫系统清除感染的能力,也包括所感染hpv的病毒载量。多年来的流行病学研究显示高危型hpv感染存在一个临床阈值。病毒载量低于这一阈值的高危型hpv感染往往是一过性感染,很少会诱发宫颈癌;而病毒载量高于这一阈值的感染诱发宫颈癌的几率将大大升高。因此,用于宫颈癌早期筛查的高危型hpv分子诊断技术还应该具有一定的定量能力以区分低载量的一过性感染和可能最终诱发宫颈癌的高载量感染。目前针对hpv核酸的检测方法主要有杂交捕获法、pcr-反向点杂交法、液态芯片法和荧光定量pcr法等。针对上述用于宫颈癌早期筛查的高危型hpv分子诊断技术的特点以及其它方面的性能指标,下表中概括了这几种方法的主要优缺点:由上表可以看出,从方法学角度考虑,目前最能满足宫颈癌早期筛查要求的检测手段是荧光定量pcr技术。该技术的灵敏度和特异性均高于杂交捕获法而与pcr-反向点杂交法和液态芯片法相当。荧光定量pcr法还可以对检测对象在很大跨度范围内进行精确定量,而利用pcr终产物与固定于薄膜或微球上的探针杂交实现靶序列检测的pcr-反向点杂交法和液态芯片法则不能定量。但是,在现有技术中,采用荧光定量pcr技术进行hpv核酸检测,需要针对每一种hpv基因型提供一个特异性探针、一个正向引物和一个反向引物,在单管反应中同时检测多个hpv基因型时,若干组特异性探针、正向引物和反向引物势必会引起更多的非特异性结合,这在一定程度上影响了检测的灵敏度和精准度。技术实现要素:针对现有技术中的不足之处,本发明旨在提供一种高灵敏度、高特异性的可以在一管荧光定量pcr反应中同时检测hpv16、18、31、33、35、39、45、51、52、56、58、59、66和68共14种hpv基因型的试剂盒。为实现上述目的,本发明的技术方案如下:一种在单管反应中同时检测多个高危型人乳头瘤病毒的试剂盒,其至少包括有分别对应hpv16、18、31、33、35、39、45、51、52、56、58、59、66和68这14个基因型的特异性探针seqidno.1-14;以及综合对应该14个基因型且数量少于14对的正向引物和反向引物。优选的是,所述的在单管反应中同时检测多个高危型人乳头瘤病毒的试剂盒,其中,综合对应14个基因型的正向引物数量为6个,分别为:seqidno.15-20。优选的是,所述的在单管反应中同时检测多个高危型人乳头瘤病毒的试剂盒,其中,综合对应14个基因型的反向引物数量为6个,分别为:seqidno.21-26。优选的是,所述的在单管反应中同时检测多个高危型人乳头瘤病毒的试剂盒,其中,试剂盒还包括有用于与作为人体细胞内质控的血红蛋白β基因互补配对的特异性探针seqidno.27。优选的是,所述的在单管反应中同时检测多个高危型人乳头瘤病毒的试剂盒,其中,试剂盒还包括有用于与作为人体细胞内质控的血红蛋白β基因互补配对的正向引物seqidno.28和反向引物seqidno.29。本发明的有益效果是:本发明通过对现有hpv核酸检测试剂盒配方的改进,使得本申请的技术方案可以仅使用6个正向引物和6个反向引物就能够在单管反应中同时实现高灵敏度、高特异性地检测14种高危型人乳头瘤病毒。6个正向引物和6个反向引物中的每一个引物并不是只单独作用于14种高危型hpv中的一种,而是同时贡献于多个hpv基因型,而6个正向引物和6个反向引物作为一个整体,恰好满足了同时贡献扩增14种高危型hpv的需求。附图说明图1为本发明荧光定量pcr反应检测不同hpv基因型的浓度梯度标准品所得的扩增曲线图(以hpv16、18、33和51四个基因型为例);hpv16和18的浓度梯度区间为10~107拷贝/反应;hpv33和51的浓度梯度区间为100~108拷贝/反应;每个浓度梯度的检测反应包含3个技术重复。图2为3个不同批次的本发明试剂盒对同一组标准品的检测结果对比图;其中,p0000002、p0000025和p0000037为批次编号。具体实施方式下面结合附图对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。下面列出本案一实施例的在单管反应中同时检测多个高危型人乳头瘤病毒的试剂盒,其至少包括有分别对应hpv16、18、31、33、35、39、45、51、52、56、58、59、66和68这14个基因型的特异性探针seqidno.1-14;以及综合对应该14个基因型且数量少于14对的正向引物和反向引物。其中,综合对应14个基因型的正向引物数量为6个,分别为:seqidno.15-20。其中,综合对应14个基因型的反向引物数量为6个,分别为:seqidno.21-26。其中,试剂盒还包括有用于与作为人体细胞内质控的血红蛋白β基因(hbb)互补配对的特异性探针seqidno.27。其中,试剂盒还包括有用于与作为人体细胞内质控的血红蛋白β基因互补配对的正向引物seqidno.28和反向引物seqidno.29。当然,试剂盒中还优选包括完成荧光定量pcr反应所需的助剂,例如:pcr缓冲液、4种dntp混合液、热启动聚合酶等等。表1示出具体引物和探针的序列:表1表1中,hpv16探针(seqidno.1)使用的荧光基团为joe;hpv18探针(seqidno.2)使用的荧光基团为cy5;hpv31、33、35、39、51、52、56、59、66和68这10个探针(seqidno.3、4、5、6、8、9、10、12、13和14)使用的荧光基团为fam;hpv45和58(seqidno.7和11)两个探针使用的荧光基团为rox;seqidno.27所使用的荧光基团为tamra。此外,seqidno.3、10、12和13是根据申请号为201710184261.7的专利《高信噪比多探针pcrtaqman探针及其应用》设计的可以显著降低荧光定量pcr背景信号的特殊探针。这类特殊探针的淬灭基团不在寡聚核苷酸的3’端,而是在序列中间的某个胸腺嘧啶核苷酸(t)上,而其3’端则由磷酸基团、氨基或其它封闭碱基封闭。上述4个探针序列中小写的“t”代表带有淬灭基团的t核苷酸,而3’端则由c3linker封闭。表2提供一具体实施例的包括上述所有引物和探针、可以同时检测全部14种hpv基因型、用于单管多重荧光定量pcr的pcr反应液。该反应液配方见表2:表2名称反应终浓度浓度单位无mg2+离子pcr缓冲液1xmg2+4mm4种dntp混合液0.2mmseqidno.10.07μmseqidno.20.05μmseqidno.30.065μmseqidno.40.06μmseqidno.50.05μmseqidno.60.065μmseqidno.70.1μmseqidno.80.07μmseqidno.90.05μmseqidno.100.2μmseqidno.110.1μmseqidno.120.09μmseqidno.130.05μmseqidno.140.05μmseqidno.150.9μmseqidno.160.2μmseqidno.170.2μmseqidno.180.2μmseqidno.190.2μmseqidno.200.2μmseqidno.210.4μmseqidno.220.25μmseqidno.230.25μmseqidno.240.2μmseqidno.250.2μmseqidno.260.2μmseqidno.270.05μmseqidno.280.2μmseqidno.290.2μm热启动聚合酶(taq)0.12u/μl为了验证本发明试剂盒的技术性能,本团队制备了14个分别包含上述14个hpv基因型的dna靶序列的质粒,并与人体基因组dna混合来制备不同组份及不同浓度的标准品。向标准品中加入人体基因组dna的目的在于模拟临床样本中必然存在的人体dna。这些标准品中的人体基因组dna由来源于t细胞白血病患者的jurkat培养细胞纯化而得。实施例1:为了验证本发明试剂盒能够在大跨度浓度范围内定量检测不同hpv基因型,本案制备了不同hpv基因型的10倍稀释的浓度梯度标准品。使用本发明试剂盒进行荧光定量pcr反应所得结果如表3和图1所示,这说明在106浓度跨度范围内,本发明pcr反应可以定量检测相应hpv基因型。表3.试剂盒检测14种hpv基因型浓度梯度标准品所得结果(ct值)注:“/”代表未检测。由于hpv16和18是致癌能力最强、危害最大的两个基因型,本案特意将本发明荧光定量pcr反应针对这两个基因型的灵敏度设计并调试得高于其它12种基因型。实施例2:为了验证本发明试剂盒配方的稳定性,本案先后使用3套不同批次的原材料试剂制备了3个不同批次的试剂盒,并用所得试剂盒对同一组标准品进行检测。所得结果显示3批试剂盒的检测结果非常相近(表4和图2)。表4.三个不同批次的本发明试剂盒检测同一组标准品所得结果总结。注:“\”代表无扩增曲线。实施例3:以参与宫颈癌筛查的93名女性为检测对象,本案完成了试剂盒与德国凯杰公司(qiagen)出品的carehpv核酸检测试剂盒的对比实验。carehpv试剂盒可以检测相同的14种hpv基因型,但不能将hpv16和18与其它12种基因型区别开来,而只能给出阴性或阳性的检测结果。由医院完成宫颈脱落细胞的采样,每名患者采两个样。该医院检验科按照carehpv试剂盒说明书完成对其中一套93例样本的检测。另一套93例样本采用本案的技术方案完成检测:首先完成样本中dna的提取;而后使用本发明试剂盒对纯化后的dna进行检测。该对比实验结果显示两个试剂盒的检测结果一致率达到95.7%(表5)。对于两个试剂盒检测结果均为阳性以及两个试剂盒检测结果不一致的14个案例的进一步研究显示,本发明试剂盒对不同hpv基因型具有更好的特异性(表6):1、carehpv试剂盒对第13号患者的检测结果为阳性,而本发明试剂盒的检测结果为阴性;尽管琼脂糖凝胶电泳中能够看到hpv特异性的pcr反应条带,但测序结果显示其为hpv70,一个低危hpv基因型。这一结果表明carehpv试剂盒的检测结果属于由非特异性反应造成的假阳性。2、carehpv试剂盒对第79、84和103号患者的检测结果为阳性,而本发明试剂盒的检测结果为阴性;并且琼脂糖凝胶电泳中看不到hpv特异性的pcr反应条带。这一结果也与carehpv试剂盒的检测结果属于由非特异性反应造成的假阳性吻合。表5.本发明试剂盒与carehpv试剂盒以临床样本为对象的对比实验结果。表6.两个试剂盒检测结果均为阳性和检测结果不一致案例的进一步分析结果。尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。编号名称序列两端修饰中间修饰seqidno.1hpv16探针ttatgtgctgccatatctacttcagaaact5'-joe,3'-bhq1无seqidno.2hpv18探针ctacacagtctcctgtacctg5'-cy5,3'-bhq2无seqidno.3hpv31探针gtgctgcaattgcaaacagtgatactac5'-fam,3'-c3linker/ibhq1dt/seqidno.4hpv33探针ctttatgcacacaagtaactagtgac5'-fam,3'-bhq1无seqidno.5hpv35探针ctgctgtgtcttctagtgacag5'-fam,3'-bhq1无seqidno.6hpv39探针ctatagagtcttccataccttctac5'-fam,3'-bhq1无seqidno.7hpv45探针cctgtgccaagtacatatgaccc5'-rox,3'-bhq2无seqidno.8hpv51探针ctgcggtttccccaac5'-fam,3'-bhq1无seqidno.9hpv52探针actttatgtgctgaggttaaaaagg5'-fam,3'-bhq1无seqidno.10hpv56探针ctgctacagaacagttaagtaaatatg5'-fam,3'-c3linker/ibhq1dt/seqidno.11hpv58探针tatgcactgaagtaactaaggaagg5'-rox,3'-bhq2无seqidno.12hpv59探针ctacttcttctattcctaatgtatacac5'-fam,3'-c3linker/ibhq1dt/seqidno.13hpv66探针ctaaatatgatgcccgtgaaatcaatc5'-fam,3'-c3linker/ibhq1dt/seqidno.14hpv68探针ctgaatcagctgtaccaaatatttatg5'-fam,3'-bhq1无seqidno.15正向引物1tggtagatactacacgcagtac无无seqidno.16正向引物2ttgtttgttactgtagttgatac无无seqidno.17正向引物3cagctttttattacctgtgttg无无seqidno.18正向引物4cagttgtttgtcacagttgtgg无无seqidno.19正向引物5caattgtttttaacagttgtag无无seqidno.20正向引物6caattatttcttactgttgtgg无无seqidno.21反向引物1gcacagttgaaaaataaactgtaa无无seqidno.22反向引物2gcacaattgaaaaataaattgtaaa无无seqidno.23反向引物3gcataactgaaatataaattgtaaa无无seqidno.24反向引物4cataattgaaaaataaattgcaattc无无seqidno.25反向引物5caaactgtagttcatattcctccac无无seqidno.26反向引物6caactgaaatataaattgcaaatc无无seqidno.27hbb探针gctcctgggagtagattg5'-tamra,3'-bhq2无seqidno.28hbb正向引物ccagaagagccaaggacaggtacg无无seqidno.29hbb反向引物tttgaggttgctagtgaacacag无无当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1