一种高纯度的米尔贝肟中间体(II)制备方法与流程
本发明涉及一种高纯度米尔贝肟中间体(ⅱ)分离纯化方法,属于抗体内外寄生虫类药物分离纯化技术领域。
背景技术:
米尔贝霉素(milbemycin)于1967年由日本sankyo公司的青木(aoki)等人从筛选的链霉菌streptomyceshygroscopicussubsp.aureoiacrimosus的发酵液中发现的一类十六元大环内脂化合物,对各种螨虫、农业害虫以及园艺害虫(如鳞翅目的蚜虫、幼虫)都有很好的防治效果,并且对宠物犬类和猫类的致命寄生虫病(如犬恶丝虫病)等均有良好的治疗效果。
米尔贝肟(milbemycinoxime)是米尔贝霉素a3和a4在c5位的羟基变成肟基的衍生物,它们是一类大环内酯类抗体内外寄生虫类药物,是一种主要用做治疗犬类的抗虫药,米尔贝肟对治疗和预防大部分比较常见寄生虫疾病都有极好的效果,通常用来预防和治疗由线虫、恶丝虫病等引发的猫、狗等疾病。米尔贝肟首次在国内开始应用是在1997年由台湾诺华公司推出的商品名为倍脉心(成分为milbemycinoxime)的抗虫药,作为犬科动物和猫科动物预防肠内寄生虫和其它寄生虫的内服药,正是由于其对哺乳动物体内外寄生虫都具有很好的驱杀作用,并且对一些阿维菌素敏感的犬类几乎无任何毒副作用,使得其应用价值和研究前景越来越受到世界的广泛重视。
米尔贝肟中间体(ⅱ)是米尔贝霉素a3和a4在c5位的羟基变成酮基的衍生物。高纯度的米尔贝肟中间体(ⅱ)可用于米尔贝肟生产过程中中间体的检测,以确保产品的合格性。目前国内尚未有高纯度的米尔贝肟中间体发明专利,并且通常高纯度的米尔贝肟中间体(ⅱ)是实验室通过制备柱进行分离纯化制备,该工艺所用的设备昂贵,生产量低。本发明方法分离纯度高,成本低、产品收率高,可实现工业化生产。
技术实现要素:
本发明提供了一种高纯度米尔贝肟中间体(ⅱ)的分离纯化法,将链霉素发酵产生的发酵液经固液分离,浸取后得到米尔贝霉素(i)溶液,经氧化反应得到的米尔贝肟中间体(ⅱ)溶液,经过浓缩溶解、硅胶层析分离,得到的洗脱液经过浓缩、结晶、抽滤干燥得到的米尔贝肟中间体(ⅱ)纯度在97%以上。该方法分离纯度高,成本低、产品收率高。
一种高纯度米尔贝肟中间体(ⅱ)的分离纯化法,其特征在于步骤如下:
(1)用于硅胶层析的样品米尔贝肟中间体(ⅱ)溶液纯度≥65.0%。
(2)米尔贝肟中间体(ⅱ)溶液浓缩,控制浓缩罐温度40-50℃,真空度≤-0.09mpa,直至所有米尔贝肟中间体(ⅱ)溶液浓缩至冷凝器下视镜无液体流出。
(3)溶解:浓缩结束后往浓缩罐中加入产品量2~3倍重量的90~95%正庚
烷-丙酮/正己烷-丙酮/正庚烷-二氯甲烷溶液。
(4)干法装硅胶层析柱,将溶解液湿法上柱。
(5)洗脱:用流动相浓度为90~98%正庚烷-丙酮/正己烷-丙酮/正庚烷-二氯甲烷溶液对硅胶柱进行洗脱。
(6)洗脱结束后,将合格的洗脱液真空浓缩,控制浓缩罐温度40-50℃,
真空度≤-0.09mpa,直至所有米尔贝肟中间体(ⅱ)溶液浓缩至冷凝器下视镜无液体流出。
(7)浓缩结束后,往浓缩罐中加入产品量3~4倍重量的90~95%正庚烷-
丙酮/正庚烷-乙腈/正庚烷-三氯甲烷溶液,搅拌升温至60~65℃溶解至澄清,降温至10~20℃,保温结晶2小时以上。
(8)抽滤后进行干燥,干燥温度50~60°c,真空≤-0.085mpa,干燥8~12小时后得到纯度≥97%的米尔贝肟中间体(ⅱ)。
本方法使用硅胶柱价格相对低,操作简单,该方法稳定可靠,易于工业化,提高了产品的纯度、质量和收率。
附图说明
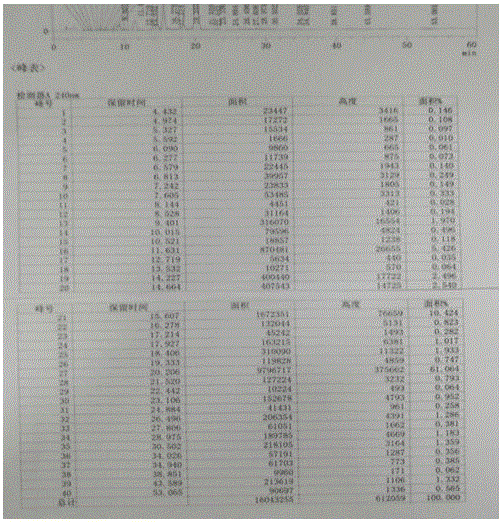
图1是实施例1层析前的米尔贝肟中间体(ⅱ)的液相色谱图。
图2是实施例1所分离纯化后的米尔贝肟中间体(ⅱ)的液相色谱图。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。
实施例1
将链霉素发酵产生的发酵液经固液分离,浸取后得到米尔贝霉素溶液,经氧化反应(常规反应)得到的米尔贝肟中间体(ⅱ)溶液,将该溶液浓缩,控制浓缩罐温度40-50℃,真空度≤-0.09mpa,直至所有米尔贝肟中间体(ⅱ)溶液浓缩至冷凝器下视镜无液体流出。浓缩结束后往浓缩罐中加入产品量2.5倍重量的93%正庚烷-丙酮溶液溶解,得到米尔贝肟中间体(ⅱ)溶解液11.91kg,取样检测含量21.4%,纯度71.7%,共2.55kg(液相色谱图见图1)。
上柱:将上述溶液抽至不锈钢反应釜内,用物料泵将米尔贝肟中间体(ⅱ)溶解液全部打入层析柱中。
洗脱:上柱结束后,用浓度为95%正庚烷-丙酮溶液对硅胶柱进行洗脱,将检测合格洗脱液合并在一起进行洗脱液浓缩。
洗脱液浓缩:洗脱结束后,将合格的洗脱液真空浓缩,控制浓缩罐温度40-50℃,真空度≤-0.09mpa,直至所有米尔贝肟中间体(ⅱ)溶液浓缩至冷凝器下视镜无液体流出。
结晶:浓缩结束后,往浓缩罐中加入7.68kg的92%正庚烷-丙酮溶液,搅拌升温至60~65℃溶解至澄清,降温至10~20℃保温结晶3小时。
干燥:将结晶液用过滤器过滤,将湿品放入干燥机减压干燥,干燥温度50~60℃,真空≤-0.085mpa,干燥12小时后出粉,最终的得到1.86kg米尔贝肟中间体(ⅱ),经液相色谱检测纯度为98.6%,收率72.9%(液相色谱图见图2)。
实施例2
将链霉素发酵产生的发酵液经固液分离,浸取后得到米尔贝霉素溶液,经氧化反应(常规反应)得到的米尔贝肟中间体(ⅱ)溶液,将该溶液浓缩,控制浓缩罐温度40-50℃,真空度≤-0.09mpa,直至所有米尔贝肟中间体(ⅱ)溶液浓缩至冷凝器下视镜无液体流出。浓缩结束后往浓缩罐中加入产品量2.2倍重量的95%正己烷-丙酮溶液溶解,得到米尔贝肟中间体(ⅱ)溶解液9.70kg,取样检测含量22.4%,纯度70.3%,共2.17kg。
上柱:将上述溶液抽至不锈钢反应釜内,用物料泵将米尔贝肟中间体(ⅱ)溶解液全部打入层析柱中。
洗脱:上柱结束后,用浓度为96%正己烷-丙酮溶液对硅胶柱进行洗脱,将检测合格洗脱液合并在一起进行洗脱液浓缩。
洗脱液浓缩:洗脱结束后,将合格的洗脱液真空浓缩,控制浓缩罐温度40-50℃,真空度≤-0.09mpa,直至所有米尔贝肟中间体(ⅱ)溶液浓缩至冷凝器下视镜无液体流出。
结晶:浓缩结束后,往浓缩罐中加入7.81kg的93%正己烷-丙酮溶液,搅拌升温至60~65℃溶解至澄清,降温至10~20℃保温结晶3小时。
干燥:将结晶液用过滤器过滤,将湿品放入干燥机减压干燥,干燥温度50~60℃,真空≤-0.085mpa,干燥12小时后出粉,最终的得到1.54kg米尔贝肟中间体(ⅱ),经液相色谱检测纯度为98.1%,收率71.0%。
实施例3
将链霉素发酵产生的发酵液经固液分离,浸取后得到米尔贝霉素溶液,经氧化反应(常规反应)得到的米尔贝肟中间体(ⅱ)溶液,将该溶液浓缩,控制浓缩罐温度40-50℃,真空度≤-0.09mpa,直至所有米尔贝肟中间体(ⅱ)溶液浓缩至冷凝器下视镜无液体流出。浓缩结束后往浓缩罐中加入产品量2.4倍重量的92%正庚烷-丙酮溶液溶解,得到米尔贝肟中间体(ⅱ)溶解液11.6kg,取样检测含量22.1%,纯度70.3%,共2.56kg。
上柱:将上述溶液抽至不锈钢反应釜内,用物料泵将米尔贝肟中间体(ⅱ)溶解液全部打入层析柱中。
洗脱:上柱结束后,用浓度为95%正庚烷-丙酮溶液对硅胶柱进行洗脱,将检测合格洗脱液合并在一起进行洗脱液浓缩。
洗脱液浓缩:洗脱结束后,将合格的洗脱液真空浓缩,控制浓缩罐温度40-50℃,真空度≤-0.09mpa,直至所有米尔贝肟中间体(ⅱ)溶液浓缩至冷凝器下视镜无液体流出。
结晶:浓缩结束后,往浓缩罐中加入8.52kg的94%正庚烷-丙酮溶液,搅拌升温至60~65℃溶解至澄清,降温至10~20℃保温结晶3小时。
干燥:将结晶液用过滤器过滤,将湿品放入干燥机减压干燥,干燥温度50~60℃,真空≤-0.085mpa,干燥12小时后出粉,最终的得到1.84kg米尔贝肟中间体(ⅱ),经液相色谱检测纯度为97.9%,收率71.9%。
上述具体实施方式不以任何形式限制本发明的技术方案,凡是采用等同替换或等效变换的方式所获得的技术方案均落在本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!