微流控PCR芯片的制作方法
本实用新型涉及生物分子检测技术领域,特别涉及一种微流控PCR芯片。
背景技术:
聚合酶链式反应(PCR)已经成为分子诊断领域的新标准,PCR方法是从分子水平上通过针对于基因序列的特异性引物探针的设计实现检测,与免疫方法相比,PCR方法可以大大提高检测的准确性和灵敏性。微流控技术是在微米尺度对流体进行操作的一项全新的分析技术,相比于常规的分析方法,其具有高通量、自动化、集成化和低成本等优势。
目前,微流控技术和PCR技术的结合越来越获得关注,借助于微流控易于实现高通量筛选的优势,PCR技术能够应用于分子标记物的大规模筛选和诊断等领域。现有的分子诊断方面的高通量筛选技术主要包括分子杂交(DNA芯片技术)、多重PCR技术和液相芯片技术等。分子杂交技术需要预先对靶标基因进行扩增,然后扩增产物与互补探针序列进行杂交后才可检测结果,加之其也要进行冲洗和温浴,操作步骤繁琐。多重PCR技术需要对不同的靶标基因进行荧光探针编码,不仅需要高分辨率的光学系统,同时多靶标同时反应,引物和探针设计要求高,而且容易造成交叉反应。液相芯片技术不仅需要复杂的荧光编码微球制备和共价偶联技术,同时也需要复杂的操作步骤,其仪器昂贵,使得普通用户难以接受。
技术实现要素:
有鉴于此,本实用新型旨在提出一种微流控PCR芯片,以可提供一种适于高通量PCR检测使用的PCR芯片。
为达到上述目的,本实用新型的技术方案是这样实现的:
一种微流控PCR芯片,其包括:
基底部,所述基底部包括具有热传递性的基底,平铺于所述基底顶部的疏水层,以及以微阵列方式布置于所述疏水层上的多个亲水单元;
腔室部,所述腔室部与所述基底固连,以围构形成位于各所述亲水单元上方的反应腔室;
密封盖,所述密封盖具有透光性、并连接于所述腔室部的顶部,以构成对所述反应腔室的密封;
加气口,所述加气口位于所述密封盖或所述腔室部其一上,以与外部有压气源连通,而于所述反应腔室内注入气体。
进一步的,于各所述亲水单元至少其一处沉积有呈干燥状的包括有引物的试剂。
进一步的,所述试剂通过喷墨打印机点样于所述亲水单元处,并经干燥处理而成干燥状。
进一步的,所述干燥处理方式包括有真空冷冻干燥或常温自然干燥。
进一步的,所述真空冷冻干燥的温度为-85~-75℃,真空度为0.008~0.012Mpa。
进一步的,所述基底为亲水性材质,所述亲水单元由镂空所述疏水层、而暴露于所述疏水层外的所述基底构成。
进一步的,所述基底的材料包括玻璃或硅片。
进一步的,所述疏水层的材料包括氟硅烷或六甲基二硅胺。
进一步的,各所述亲水单元处的所述基底的表面为光滑平面或刻蚀形成的微阱阵列。
进一步的,所述刻蚀方式包括湿法刻蚀或干法刻蚀。
进一步的,所述基底部通过以下的步骤制备而成:
步骤s1、提供基底;
步骤s2、于所述基底上形成疏水层;
步骤s3、于所述疏水层上形成光刻胶层,并通过光刻方式于所述光刻胶层上形成呈微阵列布置的多个镂空状的图案;
步骤s4、通过等离子体机轰击,去除各所述图案区域的疏水层,使所述图案区域的基底暴露于外,而形成所述亲水单元;
步骤s5、剥离所述光刻胶层。
进一步的,于所述步骤s5之前还包括:
步骤s50、于所述亲水单元的基底表面刻蚀形成微阱阵列。
进一步的,步骤s2中为将所述基底与所述疏水层材料一同放入加热箱,恒温保持,而于所述基底表面反应生成所述疏水层。
进一步的,所述步骤s3中具体包括:
步骤s31、于所述疏水层上旋涂光刻胶,并烘干形成光刻胶层;
步骤s32、于光刻机中,在掩膜版下对所述光刻胶层进行UV曝光处理;
步骤s33、放入显影液中进行显影处理,于光刻胶层形成所述图案;
步骤s34、烘干固化。
进一步的,所述腔室部由透光性材料制成。
进一步的,所述密封盖及所述腔室部的材料包括PP、PET或PC。
进一步的,所述基底与所述腔室部经胶黏剂粘接相连。
进一步的,所述胶黏剂包括环氧树脂胶或紫外固化胶。
同时,本实用新型也提出了应用该微流控PCR芯片的微流控PCR检测系统,该检测系统包括:
如上所述的微流控PCR芯片;
加样装置,所述加样装置用于在所述亲水单元处投加待检测样品,于所投加的待检测样品上方形成密封油层,以及由所述加气口向所述反应腔室内注入气体;
热循环装置,所述热循环装置用于对所述基底进行加热,以使所述待检测样品进行热循环扩增;
荧光采集装置,所述荧光采集装置用于对热循环扩增后的所述待检测样品进行荧光信号采集,并可将采集信号向外输出。
进一步的,所述加样装置包括:
固定框架,所述固定框架用于装载所述微流控PCR芯片;
制动杆,滑动设置于所述固定框架上;
样品导流槽,设置于所述制动杆上,所述样品导流槽具有顶部开口的储液腔,并于所述样品导流槽的底部设有与所述储液腔贯通的呈狭缝状的出口;
密封油导流槽,设置于所述制动杆上,且具有与所述样品导流槽相同的结构;
驱动机构,设置于所述固定框架与所述制动杆之间,以驱使所述制动杆带动所述样品导流槽及所述密封油导流槽形成相对于所述微流控PCR芯片的滑动;
控制机构,所述控制机构与所述驱动机构连接,以控制所述驱动机构动作;
加气接口,所述加气接口为分别与外部气源相连的多个,且各所述加气接口分别与所述加气口及所述样品导流槽和密封油导流槽的顶部开口相通,以向所述反应腔室及所述样品导流槽和密封油导流槽内注入气体。
进一步的,所述驱动机构包括导轨,以及与所述制动杆传动连接的、驱使所述制动杆沿所述导轨滑动的步进电机。
进一步的,注入所述反应腔室内的气体压力大于0.1MPa。
进一步的,注入所述反应腔室内的气体为惰性气体或空气。
进一步的,在与所述样品导流槽和密封油导流槽的顶部开口相连的所述加气接口处设有压力调节阀件。
进一步的,所述热循环装置包括:
支撑架,用于承载所述微流控PCR芯片;
薄膜加热器,设于所述支撑架上,并与所述微流控PCR芯片的所述基底抵接;
电源控制机构,与外部电源及所述薄膜加热片电连接,以控制向所述薄膜加热片的供电。
进一步的,所述荧光采集装置包括:
光源;
第一滤光片,位于所述光源的出射光方向上,而对所述光源的出射光进行过滤;
二向色镜,位于所述光源的出射光方向上,以构成所述光源出射光向所述微流控PCR芯片的照射,以及所述微流控PCR芯片中的所述待检测样品所发荧光向外的出射;
图像采集单元,位于所述荧光的出射方向上,以对所述荧光进行采集,并可将采集信号向外输出;
第二滤光片,位于所述荧光的出射方向上,且置于所述图像采集单元的前侧,以对出射的所述荧光进行过滤。
进一步的,所述光源为激光光源,所述图像采集单元为CMOS传感器。
相对于现有技术,本实用新型具有以下优势:
本实用新型的微流控PCR芯片通过于疏水层上的呈微阵列的亲水单元的布置,能够实现高通量筛选检测,并可将不同指标(特异性引物和探针)固定在基底特定的反应位置,从而可通过空间进行分辨,不需进行多色荧光编码的光谱分辨,能够简化检测分辨方式。
同时,本实用新型中通过疏水层及亲水单元的设置,在样品投加时,通过疏水层和亲水单元的亲疏水作用,能够在各亲水单元处自动形成独立的静态样品液滴,从而可便于待检测样品的投加操作。
此外,本实用新型中通过反应腔室的密封以及加气口的设置,检测时可通过注入气体以使反应腔室内气体压力大于水的饱和蒸气压,而保持高压状态,以此可在PCR加热反应过程中抑制水分的蒸发,也可显著降低各样品液滴的体积。由此,可使得检测使用的试剂的消耗量减少,也可在单位面积上集成更多的PCR反应单元,而能够提高PCR检测指标的数量和并行度,使得检测设备集成度高,以有助于检测成本的降低。
而且本实用新型中通过降低单个样品液滴的体积,还可显著提高待测样品的浓度,可有利于PCR热循环扩增反应的进行,可提高PCR芯片的灵敏度,而能够大大缩短反应时间,以在较短时间内即可检测到阳性信号,提升检测效率。
综上所述,本实用新型的微流控PCR芯片能够实现高通量筛选检测,可简化PCR检测分辨方式,便于待检测样品的投加操作,且能够利于热循环扩增反应的进行,有助于提升检测效果,且检测试剂消耗量少,可使得设备集成度高、测试成本降低,而有着很好的实用性。
附图说明
构成本实用新型的一部分的附图用来提供对本实用新型的进一步理解,本实用新型的示意性实施例及其说明用于解释本实用新型,并不构成对本实用新型的不当限定。在附图中:
图1为本实用新型实施例所述的微流控PCR芯片的结构示意图;
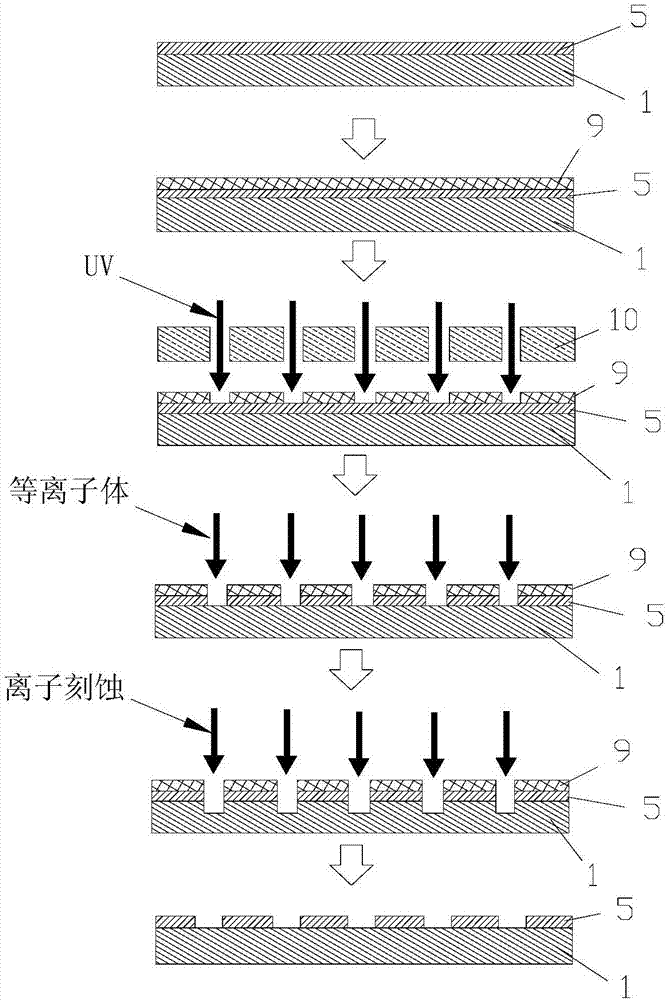
图2为本实用新型实施例所述的基底部的制备流程图;
图3为本实用新型实施例所述的加样装置的结构示意图;
图4为本实用新型实施例所述的样品导流槽的结构示意图;
图5为本实用新型实施例所述的微流控PCR芯片投加待检测样品及密封油后的结构示意图;
图6为本实用新型实施例所述的微流控PCR检测系统的工作示意图;
附图标记说明:
1-基底,2-腔室部,3-密封盖,4-加气口,5-疏水层,6-亲水单元,7-反应腔室,8-胶黏剂,9-光刻胶层,10-掩膜版,11-样品导流槽,12-密封油导流槽,13-制动杆,14-固定框架,15-导轨,16-步进电机,17-样品液滴,18-密封油层,19-支撑架,20-薄膜加热器,21-光源,22-图像采集单元,23-第一滤光片,24-二向色镜,25-第二滤光片,100-芯片,111-储液腔,112-顶部开口,113-出口。
具体实施方式
需要说明的是,在不冲突的情况下,本实用新型中的实施例及实施例中的特征可以相互组合。
下面将参考附图并结合实施例来详细说明本实用新型。
本实施例涉及一种微流控PCR芯片,其整体上包括基底部、腔室部及密封盖和加气口,且如图1中所示的,其中,基底部包括具有热传递性的基底1,平铺设置于基底1顶部的疏水层5,以及以微阵列方式布置在疏水层5上的多个亲水单元6。腔室部2与基底1固连而围构形成有位于各亲水单元6上方的反应腔室7,密封盖7连接于腔室部2的顶部,以构成对该反应腔室7的密封,且密封盖7为透光性的。加气口4则位于密封盖3上,且其用于与外部有压气源连通,而向反应腔室7内注入气体。
基于如上的整体结构,具体上,本实施例中基底1采用亲水性材质制成,优选的,构成基底1的材料可为亲水性的玻璃或硅片,而本实施例中形成疏水层5的材料则可为氟硅烷或六甲基二硅胺。此外,作为一种优选的结构形式,本实施例中可通过镂空该疏水层5,从而由疏水层5的镂空位置处的暴露于疏水层5之外的具有亲水性的基底1构成位于疏水层5上的微阵列排布的亲水单元6,此时各亲水单元6均呈现为一凹坑结构。
本实施例中对于由基底1直接构成的亲水单元6而言,进一步的,在具体应用中可使得各亲水单元6处的基底1的表面为光滑平面,而除了为光滑平面,也可通过刻蚀处理而使得暴露于外的基底1的表面形成微阱阵列,此时的刻蚀处理采用现有的湿法刻蚀或干法刻蚀手段均可。
本实施例中如上结构的基底部在实际制备时,其可如图2中所示的,此时以基底1采用硅片,疏水层5材料采用氟硅烷为例,首先选取准备好作为基底1的硅片,然后将硅片和氟硅烷一同放入加热箱内,在80℃温度下保持一个小时,使得氟硅烷变成蒸汽而与硅片表面反应以形成疏水层5。
在形成疏水层5后,接着,再于疏水层5上旋涂光刻胶,并在110℃下烘干一分钟从而形成光刻胶层9,然后将形成有光刻胶层9的硅片放入光刻机中,在掩膜版10下对光刻胶层9进行UV曝光处理,曝光处理后便将硅片再放入显影液中进行显影处理,此时便可在光刻胶层9上形成呈微阵列布置的多个镂空状的图案,且该图案具体可为圆形、矩形或其它形状。微阵列排布的图案形成后,再将硅片放置于等离子体机下进行轰击,去除各图案区域的暴露于光刻胶层9外的氟硅烷形成的疏水层5,使得各图案区域的硅片暴露于外部,这样便形成了由基底1构成的亲水单元6。
在各图案区域的硅片暴露后,本实施例仍可图2中所示的还可采用湿法刻蚀或干法刻蚀的方式在暴露于外的硅片的表面离子刻蚀形成微阱阵列。当然,若需要使得亲水单元6处的基底1的表面为光滑平面,也可去除离子刻蚀这一步骤,在等离子体轰击后便进行光刻胶层9的剥离。
而在形成各亲水单元6之后,接着,还需要将硅片通过丙酮进行冲洗,以剥离剩余的光刻胶层9,然后在光刻胶层9去除后,再利用异丙酮和去离子水依次对硅片进行清洗,并在100℃下对硅片进行烘干即可。
本实施例中,与基底1相连的腔室部2也为采用透光性的材料制成,且腔室部2与同具有透光性的密封盖3均可采用如PP、PET或PC等聚合物塑料经注塑工艺加工制得。而在基底1与腔室部2之间的连接方式上,本实施例中两者可通过胶黏剂8粘结在一起,且该胶黏剂8具体可采用环氧树脂胶或是紫外固化胶。
本实施例中,密封盖3可通过卡接的方式连接于腔室部2的顶端,设置于密封盖3上的加气口4具体可采用鲁尔接口或其它现有气路接口结构,以可通过气管与外部气源连接。此外,除了将加气口4设置于密封盖3上,当然在不影响检测的前提下,也可将加气口4布置于腔室部2的侧部或是底部。
本实施例的微流控PCR芯片中,进一步的,在其使用时,于所形成的各亲水单元6中,在至少一个亲水单元6处还沉积形成有包括有引物的呈干燥状的试剂。该试剂在检测时,一般均为由引物及探针构成,而在于亲水单元6处布置时,试剂可通过喷墨打印机点样于亲水单元6处的基底1表面,然后根据试剂的类型,再经过真空冷冻干燥或是常温自然干燥的方式,使得试剂干燥便可。其中,对于真空冷冻干燥方式而言,本实施例中其操作条件为温度在-85~-75℃,例如可为-80℃,真空度为0.008~0.012Mpa,例如可为0.01MPa。
在沉积包括引物及探针的试剂后,本实施例的微流控PCR芯片即可进行待检测样品投加,并热循环扩增,而进行PCR检测作业。本实施例的微流控PCR芯片用于PCR检测的具体内容将在下文中结合于微流控PCR检测系统的介绍一起进行说明。
本实施例的微流控PCR检测系统整体上包括有如上所述的微流控PCR芯片,还包括用于上述微流控PCR芯片中的亲水单元6处投加待检测样品,且于所投加的待检测样品上方形成密封油层,以及由加气口4向反应腔室7内注入气体的加样装置,用于对微流控PCR芯片中的基底1进行加热,以使待检测样品进行热循环扩增的热循环装置,以及用于对热循环扩增后的待检测样品进行荧光信号采集,并可将采集的信号向外输出的荧光采集装置。
具体结构上,如图3所示为本实施例加样装置的一种示例性结构,其包括固定框架14,固定框架14为一平台结构,以用于装载需进行待检测样品投加的微流控PCR芯片(简称芯片),芯片100可通过形成于固定框架14上的凹槽结构,而定位在固定框架14上。在固定框架14上设置有滑动布置的制动杆13,制动杆13上则设置有分别用于投加待检测样品的样品导流槽11和用于投加密封油的密封油导流槽12,而在制动杆13与固定框架14之间则还设置有用于驱使制动杆13带动两个导流槽相对于芯片100滑动的驱动机构,该驱动机构也与一控制机构相连,以由控制机构对驱动机构的动作进行控制。
本实施例中上述的驱动机构具体包括固定于固定框架14上的两个并排布置于芯片100两相对侧的导轨15,以及通过步进电机16驱使滑动于该两个导轨15上的另一导轨15,该导轨15与其下方的两个导轨15垂直布置,制动杆13即位于该导轨15上,且制动杆13也通过1一步进电机16的驱使,而能够实现制动杆13及两个导流槽沿这一导轨15的滑动,步进电机16驱使下的沿导轨15滑动的形式可参考现有结构。由此,通过各导轨15及步进电机16的设置,便能够实现两个导流槽相对于芯片100在二维方向上的于任意位置处的移动。
本实施例的样品导流槽11的一种示例性结构如图4中所示,其具有一中空的储液腔111,样品导流槽11的顶部设置有与储液腔111连通的顶部开口112,在样品导流槽11的底部则设置有与储液腔111相贯通、且呈细长的狭缝状的出口113。通过该狭缝状的出口113的设置,可使得注入储液腔111内的待检测样品借助于表面张力作用而于出口113处形成悬浮在样品导流槽11底端的悬滴。
此时,通过调整样品导流槽11在制动杆13上的固定位置,而使得位于样品导流槽11底端的悬滴与芯片100中的基底1表面接触,且在通过步进电机16驱使,而使得样品导流槽11沿芯片100滑动的过程中,随着样品导流槽11的缓慢移动(速度在0.01mm/s~100mm/s之间),由于疏水层5的疏水性和亲水单元6处的基底1的亲水性所带来的对待检测样品吸引力上的差异,待检测样品便会被分裂开而固定于具有亲水性的亲水单元6处,由此可在芯片100上形成独立的样品液滴。
本实施例中密封油导流槽12的结构与样品导流槽11相同,且其在密封油的投加上也与上述的待检测样品投加过程相同。不过,在此需要说明的是,为了保证待检测样品以及密封油的持续性投加,本实施例中在导流槽随制动杆移动的过程中,也需要通过顶部开口112向储液腔111内注入一定压力的气体,以此使得待检测样品或密封油能够平稳的流出,而于导流槽底端形成悬滴。
本实施例的与驱动机构连接的控制机构具体可采用现有的单片机或PLC,以及位置、位移传感器等电气控制部件即可。而本实施例的加样装置则还包括有多个分别与外部气源相连的加气接口,上述向储液腔111内注气即通过该加气接口和顶部开口12的连接实现,同时,该加气接口也用于和芯片100上的加气口4连接,以向芯片100的反应腔室7中注入气体。
其中,该加气接口具体由与气体管路连接的现有气路接头构成即可,而本实施例中通过加气接口向反应腔室7内注入的气体可为惰性气体或空气,其注入后的反应腔室7内的气体压力应不小于0.1MPa。此外,为了对注入样品导流槽11及密封油导流槽12内的气体压力进行调节控制,以使得待检测样品和密封油实现平稳的流出,在与样品导流槽11或密封油导流槽12相连的各加气接口处也设置有压力调节阀件,该压力调节阀件可采用现有气路阀体结构,并优选为具有压力变送器的电控阀体,以达到闭环调节效果。
本实施例的芯片100通过加样装置投加待检测样品及密封油后的状态可如图5中所示,此时于各亲水单元6处形成了独立的由待检测样品构成的样品液滴17,密封油覆盖于疏水层5及各样品液滴17上,形成了可阻隔水分挥发的密封油层18。而在密封油层18之上的反应腔室7内,通过加气口4注入压力不小于0.1MPa的气体后,还可进一步的防止样品液滴17中的水分在热循环装置加热过程中击穿密封油层18挥发。
本实施例中如图6中所示的,热循环装置具体包括用于承载芯片100的支撑架19,以及设置于支撑架19上的薄膜加热器20,支撑架19也为一平台结构,芯片100在放置于支撑架19上后基底1与薄膜加热器20相抵接,而薄膜加热器20则与电源控制机构电连接,该电源控制机构同时也与外部电源电连接,以可向薄膜加热器供电使其对基底1进行加热,而使得样品液滴17中的待检测样品进行热循环扩增反应。此外,本实施例的电源控制机构亦可通过设置温度变送器实现对加热温度的控制。
仍如图6中所示的,本实施例的荧光采集装置包括光源21,以及位于光源21出射光方向上的第一滤光片23和二向色镜24,第一滤光片23对光源21发出的光进行过滤,二向色镜24则对光源21的出射光进行反射,以使光源21的出射光照射于芯片100上,而使样品液滴17处产生荧光。而本实施例的荧光采集装置还包括位于样品液滴17所发出的荧光出射方向上的第一滤光片25和图像采集单元22。
本实施例中第二滤光片25用于对出射的荧光进行过滤,图像采集单元22具体可采用现有的CMOS传感器,而作为一种优选,光源21则可采用激光光源。
本实施例的微流控PCR检测系统在进行检测时,作为其中的一个应用示例,首先制备如实施例一中的芯片100,制备中可在各亲水单元6处随机进行试剂的沉积,然后于样品导流槽11内注入待检测样品,于密封油导流槽12内注入密封油,再控制压力调节阀件使得各导流槽底端产生悬滴,并使得悬滴和基底1表面接触。接着,在步进电机16的驱动下,使制动杆13带动两个导流槽缓慢移动,样品导流槽11形成亲水单元6处的独立的样品液滴17,密封油导流槽12则随后形成覆盖布置的密封油层18。
然后,连接密封盖3,并通过加气口4向芯片100的反应腔室7中注入惰性气体或空气,便可将芯片100放置于支撑架19上,以通过薄膜加热器20加热进行热循环扩增反应,反应完成后便可通过荧光采集装置进行荧光采集。此时,通过采集的荧光图像可发现在沉积有试剂的亲水单元6处荧光强度会增强,形成阳性的反应位点,而没有沉积试剂的亲水单元6处则为阴性位点。
以上所述仅为本实用新型的较佳实施例而已,并不用以限制本实用新型,凡在本实用新型的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本实用新型的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!