救助嵌合抗原受体系统的制作方法
本申请根据35u.s.c.§119(e)要求2016年6月29日提交的美国临时申请第62/356,335号和2016年4月14日提交的美国临时申请第62/322,634号的益处,所述申请中的每一个以全文引用的方式并入本文中。
关于序列表的陈述
以文本格式代替纸本拷贝提供与本申请相关的序列表,并且在此以引用的方式并入本说明书中。含有序列表的文本文件的名称为blbd_068_02wo_st25.txt。文本文件为42kb,创建于2017年4月14日,并与说明书的提交同时,经由efs网电子提交。
本发明涉及用于治疗癌症的改善的组合物和方法。更明确地说,本发明涉及细胞免疫疗法组合物和使用所述细胞免疫疗法组合物治疗癌症的方法。
背景技术:
癌症为全世界范围内重大的健康问题。基于2008-2010的速率,40.76%当今出生的男性和女性将在其一生的某个时间诊断患有某种形式的癌症。相比于女性的15.30%,20.37%的男性将在其50岁与70岁之间罹患癌症。在2010年1月1日,美国约有13,027,914名具有癌症病史的男性和女性存活-6,078,974名男性和6,948,940名女性。据估计,在2013年美国将有1,660,290名男性和女性(854,790男性和805,500女性)诊断患有癌症且全国将有580,350名男性和女性死于癌症。howlader等人2013。
尽管已在检测、预防和治疗癌症方面取得进展,但通用的成功疗法策略尚未实现。各种形式的癌症治疗的应答为混合的。治疗癌症的传统方法包括化学疗法和放射疗法,其由于有毒副作用而效用有限。利用治疗抗体进行免疫疗法也成效有限,这部分归因于不良的药物动力学特征曲线,抗体被血清蛋白酶和肾小球处的过滤快速消除,以及进入到肿瘤部位的渗透有限和标靶抗原对肿瘤细胞的表达水平有限。尝试使用表达嵌合抗原受体(chimericantigenreceptor;car)的经基因修饰细胞也成效有限,这归因于cart细胞不良的体内膨胀、输液之后细胞的快速消失、令人失望的临床活性和复发性或难治性癌症。
技术实现要素:
本发明一般提供用于产生t细胞疗法的改善载体和其使用方法。更明确地说,本发明提供救助car、可二聚救助受体和其在治疗、预防或改善癌症,以及在特定的优选实施例中复发性或难治性癌症中的用途。
在各种实施例中,提供救助嵌合抗原受体(chimericantigenreceptor;car),其包含:胞外抗原结合域;多聚化域;跨膜域;一个或多个胞内共刺激信号传导域;和/或初级信号传导域。
在各种实施例中,提供救助嵌合抗原受体(car),其包含:胞外抗原结合域;跨膜域;多聚化域;一个或多个胞内共刺激信号传导域;和/或初级信号传导域。
在特定实施例中,救助car进一步包含胞外抗原结合域,所述胞外抗原结合域包含抗体或其抗原结合片段。
在一些实施例中,救助car进一步包含选自由以下组成的组的抗体或抗原结合片段:camelig、ignar、fab片段、fab'片段、f(ab)'2片段、f(ab)'3片段、fv、单链fv抗体(“scfv”)、双scfv、(scfv)2、微型抗体、双功能抗体、三功能抗体、四功能抗体、二硫化物稳定的fv蛋白(“dsfv”)和单域抗体(sdab,纳米抗体)。
在额外实施例中,抗体或抗原结合片段为scfv。
在某些实施例中,胞外抗原结合域结合选自由以下组成的组的抗原:α叶酸受体、5t4、αvβ6整合素、bcma、b7-h3、b7-h6、caix、cd16、cd19、cd20、cd22、cd30、cd33、cd37、cd44、cd44v6、cd44v7/8、cd70、cd79a、cd79b、cd123、cd138、cd171、cea、cspg4、egfr、包括erbb2(her2)的egfr家族、egfrviii、egp2、egp40、epcam、epha2、epcam、fap、胎儿achr、frα、gd2、gd3、磷脂酰肌醇蛋白聚糖-3(gpc3)、hla-a1+mage1、hla-a2+mage1、hla-a3+mage1、hla-a1+ny-eso-1、hla-a2+ny-eso-1、hla-a3+ny-eso-1、il-11rα、il-13rα2、lambda、lewis-y、kappa、间皮素、muc1、muc16、ncam、nkg2d配体、ny-eso-1、prame、psca、psma、ror1、ssx、存活素、tag72、tems、vegfr2和wt-1。
在特定实施例中,救助car进一步包含胞外抗原结合域,其结合选自由以下组成的组的抗原:bcma、cd19、cspg4、psca、ror1和tag72。
在特定实施例中,救助car进一步包含胞外抗原结合域,其结合选自由以下组成的组的抗原:bcma、cd19、cd20、cd22、cd23、cd33、cd37、cd52、cd80和hla-dr。
在某些实施例中,胞外抗原结合域结合bcma或cd19。
在一些实施例中,胞外抗原结合域结合在癌细胞上表达的抗原。
在额外实施例中,胞外抗原结合域结合在实体癌细胞上表达的抗原。
在一些实施例中,胞外抗原结合域结合在液体癌细胞上表达的抗原。
在特定实施例中,救助car进一步包含胞外抗原结合域,其结合在恶性b细胞上表达的抗原。
在另外的实施例中,胞外抗原结合域结合在恶性浆细胞上表达的抗原。
在特定实施例中,救助car进一步包含选自由以下组成的组的多聚化域:fkbp多肽、frb多肽、钙调神经磷酸酶多肽、亲环素多肽、细菌性dhfr多肽、pyl1多肽、abi1多肽、gib1多肽、gai多肽和其变异体。
在特定实施例中,救助car进一步包含选自由以下组成的组的多聚化域:fkbp多肽、frb多肽和其变异体。
在额外实施例中,多聚化域选自由以下组成的组:fkbp12多肽和frbt2098l多肽。
在一些实施例中,跨膜域从选自由以下组成的组的多肽分离:t细胞受体的α或β链、cdδ、cd3ε、cdγ、cd3ζ、cd4、cd5、cd8α、cd9、cd16、cd22、cd27、cd28、cd33、cd37、cd45、cd64、cd71、cd80、cd86、cd134、cd137、cd152、cd154、amn和pd1。
在特定实施例中,救助car进一步包含跨膜域,所述跨膜域从选自由以下组成的组的多肽分离:cd8α;cd4、cd45、pd1和cd152。
在某些实施例中,跨膜域从cd8α分离。
在某些实施例中,一个或多个共刺激信号传导域和/或初级信号传导域包含免疫受体酪氨酸活化基元(immunoreceptortyrosineactivationmotif;itam)。
在特定实施例中,救助car进一步包含一个或多个共刺激信号传导域,所述一个或多个共刺激信号传导域从选自由以下组成的组的共刺激分子分离:tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9、tlr10、card11、cd2、cd7、cd27、cd28、cd30、cd40、cd54(icam)、cd83、cd134(ox40)、cd137(4-1bb)、cd278(icos)、dap10、lat、nkd2c、slp76、trim和zap70。
在一些实施例中,一个或多个共刺激信号传导域从选自由以下组成的组的共刺激分子分离:cd28、cd134、cd137和cd278。
在额外实施例中,一个或多个共刺激信号传导域从cd137分离。
在额外实施例中,初级信号传导域从选自由以下组成的组的多肽分离:fcrγ、fcrβ、cd3γ、cd3δ、cd3ε、cd3ζ、cd22、cd79a、cd79b和cd66d。
在特定实施例中,初级信号传导域从cd3ζ分离。
在一些实施例中,救助car进一步包含铰链区多肽。
在特定实施例中,铰链区多肽包含cd8α的铰链区。
在一些实施例中,救助car进一步包含间隔区。
在特定实施例中,救助car进一步包含信号肽。
在另外的实施例中,信号肽包含igg1重链信号多肽、cd8α信号多肽或人类gm-csf受体α信号多肽。
在各种实施例中,提供救助car,其包含信号肽、抗bcmascfv、连接子、frb(t82l)多聚化域、cd8α铰链和跨膜域、4-1bb共刺激域和cd3ζ初级信号传导域。
在各种实施例中,提供救助car,其包含阐述于seqidno:2中的氨基酸序列。
在各种实施例中,提供可二聚救助受体,其包含:抗原结合域;和多聚化域。
在不同其它实施例中,提供可二聚救助受体,其包含:a)抗原结合域;多聚化域;和锚定域。
在各种特定实施例中,提供可二聚救助受体,其基本上由以下组成:抗原结合域;连接子;和多聚化域。
在各种某些实施例中,提供可二聚救助受体,其基本上由以下组成:信号肽;抗原结合域;连接子;和多聚化域。
在各种其它实施例中,提供可二聚救助受体,其基本上由以下组成:抗原结合域;连接子;多聚化域;铰链域;和锚定域。
在各种其它实施例中,提供可二聚救助受体,其基本上由以下组成:信号肽;抗原结合域;连接子;多聚化域;铰链域;和锚定域。
在额外实施例中,抗原结合域包含抗体或其抗原结合片段。
在特定实施例中,抗体或抗原结合片段选自由以下组成的组:camelig、ignar、fab片段、fab'片段、f(ab)'2片段、f(ab)'3片段、fv、单链fv抗体(“scfv”)、双scfv、(scfv)2、微型抗体、双功能抗体、三功能抗体、四功能抗体、二硫化物稳定的fv蛋白(“dsfv”)和单域抗体(sdab,纳米抗体)。
在一些实施例中,抗体或抗原结合片段为scfv。
在额外实施例中,抗原结合域结合选自由以下组成的组的抗原:α叶酸受体、5t4、αvβ6整合素、bcma、b7-h3、b7-h6、caix、cd16、cd19、cd20、cd22、cd30、cd33、cd37、cd44、cd44v6、cd44v7/8、cd70、cd79a、cd79b、cd123、cd138、cd171、cea、cspg4、egfr、包括erbb2(her2)的egfr家族、egfrviii、egp2、egp40、epcam、epha2、epcam、fap、胎儿achr、frα、gd2、gd3、磷脂酰肌醇蛋白聚糖-3(gpc3)、hla-a1+mage1、hla-a2+mage1、hla-a3+mage1、hla-a1+ny-eso-1、hla-a2+ny-eso-1、hla-a3+ny-eso-1、il-11rα、il-13rα2、lambda、lewis-y、kappa、间皮素、muc1、muc16、ncam、nkg2d配体、ny-eso-1、prame、psca、psma、ror1、ssx、存活素、tag72、tems、vegfr2和wt-1。
在某些实施例中,抗原结合域结合选自由以下组成的组的抗原:bcma、cd19、cspg4、psca、ror1和tag72。
在特定实施例中,抗原结合域结合选自由以下组成的组的抗原:bcma、cd19、cd20、cd22、cd23、cd33、cd37、cd52、cd80和hla-dr。
在一些实施例中,抗原结合域结合bcma或cd19。
在一些实施例中,抗原结合域结合在癌细胞上表达的抗原。
在另外的实施例中,抗原结合域结合在实体癌细胞上表达的抗原。
在特定实施例中,抗原结合域结合在液体癌细胞上表达的抗原。
在某些实施例中,抗原结合域结合在恶性b细胞上表达的抗原。
在特定实施例中,抗原结合域结合在恶性浆细胞上表达的抗原。
在特定实施例中,多聚化域选自由以下组成的组:fkbp多肽、frb多肽、钙调神经磷酸酶多肽、亲环素多肽、细菌性dhfr多肽、pyl1多肽、abi1多肽、gib1多肽、gai多肽和其变异体。
在一些实施例中,多聚化域选自由以下组成的组:fkbp多肽、frb多肽和其变异体。
在另外的实施例中,多聚化域选自由以下组成的组:fkbp12多肽和frbt2098l多肽。
在额外实施例中,铰链域选自基本上由以下组成的组:cd4铰链、cd8α铰链、pd-1铰链和cd152铰链。
在特定实施例中,锚定域选自由以下组成的组:gpi分子和跨膜域。
在额外实施例中,锚定域包含选自由以下组成的组的多肽的跨膜区:t细胞受体的α或β链、cdδ、cd3ε、cdγ、cd3ζ、cd4、cd5、cd8α、cd9、cd16、cd22、cd27、cd28、cd33、cd37、cd45、cd64、cd71、cd80、cd86、cd134、cd137、cd152、cd154、amn和pd1。
在各种实施例中,提供可二聚救助受体,其包含信号肽、抗cd19scfv、连接子和fkbp12多聚化域。
在各种实施例中,提供可二聚救助受体,其包含信号肽、抗cd19scfv、连接子和结合至桥接因子的fkbp12多聚化域。
在各种实施例中,提供可二聚救助受体,其包含阐述于seqidno:3-5中的任一个中的多肽序列。
在各种实施例中,提供可二聚救助受体,其包含结合至桥接因子的阐述于seqidno:3-5中的任一个中的多肽序列。
在各种实施例中,提供编码本文中所涵盖的救助car的多核苷酸。
在特定实施例中,提供编码本文中所涵盖的可二聚救助受体的多核苷酸。
在各种实施例中,提供编码本文中所涵盖的多核苷酸的载体。
在某些实施例中,载体为表达载体。
在特定实施例中,载体为游离型载体。
在特定实施例中,载体为病毒载体。
在一些实施例中,载体为逆转录病毒载体。
在另外的实施例中,载体为慢病毒载体。
在特定实施例中,慢病毒载体选自基本上由以下组成的组:人类免疫缺陷病毒1(humanimmunodeficiencyvirus1;hiv-1);人类免疫缺陷病毒2(humanimmunodeficiencyvirus2;hiv-2)、维斯纳-梅迪病毒(visna-maedivirus;vmv)病毒;山羊关节炎-脑炎病毒(caprinearthritis-encephalitisvirus;caev);马传染性贫血病毒(equineinfectiousanemiavirus;eiav);猫免疫缺陷病毒(felineimmunodeficiencyvirus;fiv);牛免疫缺陷病毒(bovineimmunedeficiencyvirus;biv);和猿猴免疫缺陷病毒(simianimmunodeficiencyvirus;siv)。
在某些实施例中,载体包含左(5')逆转录病毒ltr、psi(ψ)包装信号、中央多嘌呤段/dna瓣(cppt/flap)、逆转录病毒导出元件;可操作地连接于本文中所涵盖的多核苷酸的启动子;和右(3')逆转录病毒ltr。
在额外实施例中,5'ltr的启动子被异源启动子置换。
在特定实施例中,异源启动子为巨细胞病毒(cmv)启动子、劳氏肉瘤病毒(rsv)启动子或猴病毒40(sv40)启动子。
在额外实施例中,3'ltr为自我失活(sin)ltr。
在各种实施例中,提供一种细胞,其包含本文中所涵盖的救助car、可二聚救助受体、多核苷酸和/或载体。
在各种实施例中,提供一种细胞,其包含本文中所涵盖的救助car和可二聚救助受体。
在各种实施例中,提供一种细胞,其包含本文中所涵盖的一种或多种多核苷酸。
在各种实施例中,提供一种细胞,其包含本文中所涵盖的一种或多种载体。
在一些实施例中,细胞为造血细胞。
在另外的实施例中,细胞为免疫效应细胞。
在特定实施例中,细胞为cd3+、cd4+、cd8+或其组合。
在某些实施例中,细胞为t细胞。
在额外实施例中,细胞为细胞毒性t淋巴细胞(cytotoxictlymphocyte;ctl)、肿瘤浸润淋巴细胞(tumorinfiltratinglymphocyte;til)或辅助t细胞。
在一些实施例中,细胞来源为外周血液单核细胞、骨髓、淋巴结组织、脐带血、胸腺组织、来自感染部位的组织、腹水、胸腔积液、脾组织或肿瘤。
在各种实施例中,提供一种组合物,其包含本文中所涵盖的救助car、可二聚救助受体、多核苷酸、载体和/或细胞。
在各种实施例中,提供一种组合物,其包含生理学上可接受的赋形剂和本文中所涵盖的救助car、可二聚救助受体、多核苷酸、载体和/或细胞。
在各种实施例中,提供救助car系统,其包含:包含结合第一抗原的救助car的cart细胞;结合第二抗原的可二聚救助受体;和桥接因子。在各种实施例中,提供救助car系统,其包含:包含结合第一抗原的救助car的cart细胞;和结合至桥接因子的可二聚救助受体。
在各种实施例中,提供救助car系统,其包含:包含结合第一抗原的救助car的cart细胞和结合第二抗原的可二聚救助受体;以及桥接因子。
在另外的实施例中,可二聚救助受体由可操作地连接于诱导型启动子的多核苷酸编码。
在特定实施例中,第一抗原不同于第二抗原。
在某些实施例中,第一抗原和第二抗原选自由以下组成的组:bcma、cd19、cd20、cd22、cd23、cd33、cd37、cd52、cd80和hla-dr。
在特定实施例中,第一抗原和第二抗原选自由bcma或cd19组成的组。
在额外实施例中,第一抗原为bcma且第二抗原为cd19。
在一些实施例中,第一抗原为cd19且第二抗原为bcma。
在某些实施例中,救助car多聚化域和可二聚救助受体多聚化域为选自以下的对:fkbp和frb、fkbp和钙调神经磷酸酶、fkbp和亲环素、fkbp和细菌性dhfr、钙调神经磷酸酶和亲环素、pyl1和abi1、或gib1和gai或其变异体。
在特定实施例中,救助car多聚化域包含fkbp多肽或其变异体,且可二聚救助受体多聚化域包含frb多肽或其变异体。
在一些实施例中,救助car多聚化域包含frb多肽或其变异体,且可二聚救助受体多聚化域包含fkbp多肽或其变异体。
在另外的实施例中,桥接因子为ap21967、西罗莫司(sirolimus)、依维莫司(everolimus)、诺瓦莫司(novolimus)、吡美莫司(pimecrolimus)、地磷莫司(ridaforolimus)、他克莫司(tacrolimus)、坦罗莫司(temsirolimus)、优米莫司(umirolimus)或佐他莫司(zotarolimus)。
在特定实施例中,救助car包含对bcma具有特异性的scfv、frbt2098l多聚化域、跨膜域、4-1bb的共刺激域和cd3ζ的初级信号传导域;可二聚救助受体包含对cd19具有特异性的scfv、fkbp12多聚化域,和任选地锚定域;且桥接因子为ap21967。
在额外实施例中,救助car包含对bcma具有特异性的scfv、fkbp12多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的初级信号传导域;可二聚救助受体包含对cd19具有特异性的scfv、frbt2098l多聚化域,和任选地锚定域;且桥接因子为ap21967。
在一些实施例中,救助car包含对cd19具有特异性的scfv、frbt2098l多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的初级信号传导域;可二聚救助受体包含对bcma具有特异性的scfv、fkbp12多聚化域,和任选地锚定域;且桥接因子为ap21967。
在特定实施例中,救助car包含对cd19具有特异性的scfv、fkbp12多聚化域、跨膜域、4-1bb的共刺激域和cd3ζ的初级信号传导域;可二聚救助受体包含对bcma具有特异性的scfv、frbt2098l多聚化域,和任选地锚定域;且桥接因子为ap21967。
在某些实施例中,救助car包含对bcma具有特异性的scfv、frb多聚化域、跨膜域、4-1bb的共刺激域和cd3ζ的初级信号传导域;可二聚救助受体包含对cd19具有特异性的scfv、fkbp12多聚化域,和任选地锚定域;且桥接因子为雷帕霉素(rapamycin)、坦罗莫司或依维莫司。
在一些实施例中,救助car包含对bcma具有特异性的scfv、fkbp12多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的初级信号传导域;可二聚救助受体包含对cd19具有特异性的scfv、frb多聚化域,和任选地锚定域;且桥接因子为雷帕霉素、坦罗莫司或依维莫司。
在某些实施例中,救助car包含对cd19具有特异性的scfv、frb多聚化域、跨膜域、4-1bb的共刺激域和cd3ζ的初级信号传导域;可二聚救助受体包含对bcma具有特异性的scfv和fkbp12多聚化域,和任选地锚定域;且桥接因子为雷帕霉素、坦罗莫司或依维莫司。
在另外的实施例中,救助car包含对cd19具有特异性的scfv、fkbp12多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的初级信号传导域;可二聚救助受体包含对bcma具有特异性的scfv和frb多聚化域,和任选地锚定域;且桥接因子为雷帕霉素、坦罗莫司或依维莫司。
在各种实施例中,提供一种用于减少受试者中的复发性/难治性癌细胞的数目的方法,其包含向所述受试者施用:有效量的可二聚救助受体,其中受试者先前已被施用包含救助car的免疫效应细胞;和有效量的桥接因子,其结合可二聚救助受体和救助car的多聚化域。
在各种实施例中,提供一种用于减少受试者中的复发性/难治性癌细胞的数目的方法,其包含向所述受试者施用:有效量的结合至桥接因子的可二聚救助受体,其中受试者先前已被施用包含救助car的免疫效应细胞。
在各种实施例中,提供一种用于减少受试者中的复发性/难治性癌细胞的数目的方法,其包含向所述受试者施用:有效量的包含可二聚救助受体的救助cart细胞;用以诱导可二聚救助受体的表达的诱导剂;和有效量的桥接因子,其结合可二聚救助受体和救助car的多聚化域。
在各种实施例中,提供一种治疗有需要的受试者中的癌症的方法,其包含向所述受试者施用:有效量的可二聚救助受体,其中受试者先前已被施用包含救助car的免疫效应细胞;和有效量的桥接因子,其结合可二聚救助受体和救助car的多聚化域。
在各种实施例中,提供一种治疗有需要的受试者中的癌症的方法,其包含向所述受试者施用:有效量的结合至桥接因子的可二聚救助受体,其中受试者先前已被施用包含救助car的免疫效应细胞。
在各种实施例中,提供一种治疗有需要的受试者中的癌症的方法,其包含向所述受试者施用:有效量的包含可二聚救助受体的救助cart细胞;用以诱导可二聚救助受体的表达的诱导剂;和有效量的桥接因子,其结合可二聚救助受体和救助car的多聚化域。
在额外实施例中,癌症为实体癌。
在特定实施例中,癌症选自由以下组成的组:肾上腺癌、肾上腺皮质癌、肛门癌、阑尾癌、星形细胞瘤、非典型畸胎样/横纹肌样肿瘤、基底细胞癌、胆管癌、膀胱癌、骨癌、脑癌/cns癌、乳癌、支气管肿瘤、心脏肿瘤、子宫颈癌、胆管癌、软骨肉瘤、脊索瘤、结肠癌、结肠直肠癌、颅咽管瘤、乳腺管原位癌(dcis)、子宫内膜癌、室管膜瘤、食道癌、鼻腔神经胶质瘤、尤因氏肉瘤、颅外生殖细胞肿瘤、性腺外生殖细胞肿瘤、眼癌、输卵管癌、纤维组织细胞肉瘤、纤维肉瘤、胆囊癌、胃癌、胃肠道类癌瘤、胃肠道间质瘤(gastrointestinalstromaltumor;gist)、生殖细胞肿瘤、神经胶质瘤、神经胶母细胞瘤、头颈癌、成血管细胞瘤、肝细胞癌、下咽癌、眼内黑素瘤、卡波西肉瘤、肾癌、喉癌、平滑肌肉瘤、唇癌、脂肪肉瘤、肝癌、肺癌、非小细胞肺癌、肺类癌瘤、恶性间皮瘤、髓性癌、神经管胚细胞瘤、脑膜瘤、黑素瘤、梅克尔细胞癌、中线消化道癌(midlinetractcarcinoma)、嘴癌、粘液肉瘤、骨髓发育不良综合征、骨髓增生赘瘤、鼻腔和副鼻窦癌、鼻咽癌、神经母细胞瘤、少突神经胶质瘤、口腔癌(oralcancer)、口腔癌(oralcavitycancer)、口咽癌、骨肉瘤、卵巢癌、胰脏癌、胰脏胰岛细胞瘤、乳头状癌、副神经节瘤、副甲状腺癌、阴茎癌、咽癌、嗜铬细胞瘤、松果体瘤、垂体肿瘤、胸膜肺母细胞瘤、原发性腹膜癌、前列腺癌、直肠癌、视网膜母细胞瘤、肾细胞癌、肾盂和输尿管癌、横纹肌肉瘤、唾液腺癌、皮脂腺癌、皮肤癌、软组织肉瘤、鳞状细胞癌、小细胞肺癌、小肠癌、胃癌、汗腺癌、滑膜瘤、睾丸癌、喉癌、胸腺癌、甲状腺癌、尿道癌、子宫癌、子宫肉瘤、阴道癌、血管癌、外阴癌和肾母细胞瘤。
在另外的实施例中,癌症选自由以下组成的组:肝癌、胰脏癌、肺癌、乳癌、膀胱癌、脑癌、骨癌、甲状腺癌、肾癌和皮肤癌。
在额外实施例中,癌症为液体癌或血液癌。
在特定实施例中,恶性血液肿瘤为b细胞恶性肿瘤。
在一些实施例中,b细胞恶性肿瘤选自由以下组成的组:白血病、淋巴瘤和多发性骨髓瘤。
在某些实施例中,b细胞恶性肿瘤选自由以下组成的组:急性淋巴细胞性白血病(acutelymphocyticleukemia;all)、急性骨髓性白血病(acutemyeloidleukemia;aml)、骨髓母细胞白血病、前髓细胞白血病、骨髓单核细胞性白血病、单核细胞性白血病、红白血病、毛细胞白血病(hairycellleukemia;hcl)、慢性淋巴细胞性白血病(chroniclymphocyticleukemia;cll)、和慢性骨髓白血病(chronicmyeloidleukemia;cml)、慢性骨髓单核细胞性白血病(chronicmyelomonocyticleukemia;cmml)和真性红细胞增多症、霍奇金淋巴瘤、结节性淋巴细胞为主型的霍奇金淋巴瘤、伯基特淋巴瘤、小淋巴细胞性淋巴瘤(smalllymphocyticlymphoma;sll)、弥漫性大b细胞淋巴瘤、滤泡性淋巴瘤、成免疫细胞性大细胞淋巴瘤、前体b成淋巴细胞性淋巴瘤、套细胞淋巴瘤、边缘区淋巴瘤、蕈样真菌病、多形性大细胞淋巴瘤、塞扎莱综合征、前体t成淋巴细胞性淋巴瘤、多发性骨髓瘤、明显多发性骨髓瘤、郁积性多发性骨髓瘤、浆细胞白血病、非分泌性骨髓瘤、igd骨髓瘤、骨硬化性骨髓瘤、骨骼的孤立性浆细胞瘤,和髓外浆细胞瘤。
在特定实施例中,b细胞恶性肿瘤为多发性骨髓瘤。
在各种实施例中,提供一种用于改善受试者中与癌症相关的一种或多种症状的方法,其包含向所述受试者施用:有效量的可二聚救助受体,其中受试者先前已被施用包含救助car的免疫效应细胞;和有效量的桥接因子,其结合可二聚救助受体和救助car的多聚化域。
在各种实施例中,提供一种用于改善受试者中与癌症相关的一种或多种症状的方法,其包含向所述受试者施用:有效量的结合至桥接因子的可二聚救助受体,其中受试者先前已被施用包含救助car的免疫效应细胞。
在各种实施例中,提供一种用于改善受试者中与癌症相关的一种或多种症状的方法,其包含向所述受试者施用:有效量的包含可二聚救助受体的救助cart细胞;用以诱导可二聚救助受体的表达的诱导剂;和有效量的桥接因子,其结合可二聚救助受体和救助car的多聚化域。
在特定实施例中,所改善的一种或多种症状选自由以下组成的组:虚弱、疲劳、呼吸急促、容易瘀伤和出血、频繁感染、淋巴结肿大、腹胀或腹痛、骨头或关节疼痛、骨折、非计划体重减轻、食欲不振、盗汗、持续性轻度发热和排尿减少。
附图说明
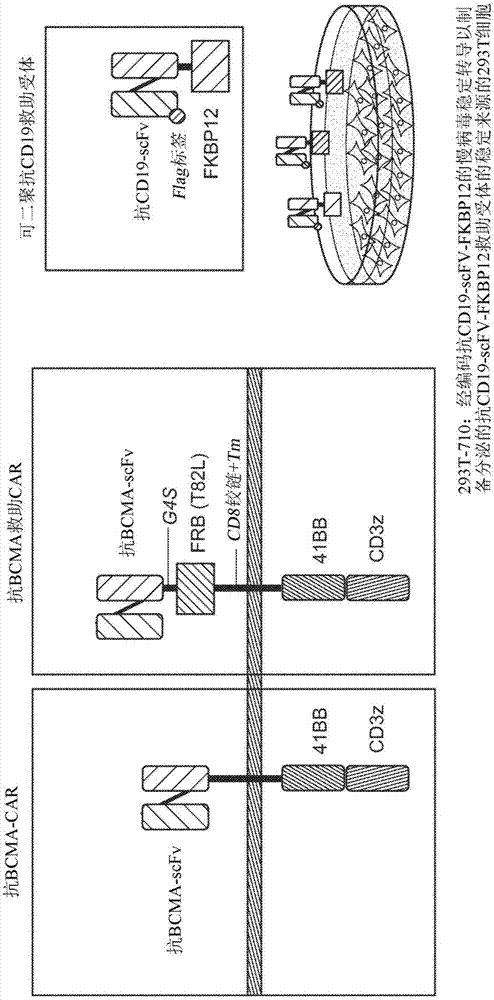
图1展示相比于救助car系统cart细胞(左图)的草图。救助car系统包含救助car(中央图)和可二聚救助受体(右上图)。右下图展示经工程改造以表达分泌的可二聚救助受体的293t细胞系。
图2a展示细胞毒性分析的结果。抗bcmacart细胞和抗bcma救助cart细胞与k562-bcma(+)和k562-bcma(-)细胞以5:1的e:t比值共同培养24小时。共同培养物用媒剂或ap21967处理。
图2b展示干扰素γ(ifnγ)释放分析的结果。抗bcmacart细胞和抗bcma救助cart细胞与k562bcma(+)细胞以1:1的e:t比值共同培养24小时。共同培养物用媒剂或ap21967处理。
图3a展示救助car系统的草图。抗bcma救助car和可二聚抗cd19救助受体在桥接因子ap21967存在下杂二聚。
图3b展示细胞毒性分析的结果。抗bcma救助cart细胞与nalm-6-cd19(+)细胞和k562cd19(-)细胞以2:1的e:t比值共同培养24小时。共同培养物用媒剂或100nmap21967以及用0μl、10μl或30μl含有可二聚抗cd19救助受体的293t-710细胞上清液处理。
图3c展示干扰素γ(ifnγ)释放分析的结果。抗bcma救助cart细胞与nalm-6-cd19(+)细胞以1:1的e:t比值共同培养24小时。共同培养物用100nmap21967和0μl或100μl含有可二聚抗cd19救助受体的293t-710细胞上清液处理。
图4a展示可二聚抗cd19救助受体的纯化方案。
图4b展示纯化的可二聚抗cd19救助受体预装载有配体。
图5展示细胞毒性分析的结果。在存在或不存在250ng预装载可二聚抗cd19救助受体下,在具有或不具有100nmap21967下,抗bcmacart细胞或抗bcma救助cart细胞与nalm-6-cd19(+)细胞和k562cd19(-)细胞以2:1e:t比值共同培养24hr。
图6展示预装载的可二聚抗cd19救助受体的滴定分析的结果。抗bcma救助cart细胞与nalm-6-cd19(+)细胞和k562cd19(-)细胞以2:1e:t比值在减少量(125ng、62.5ng、31.3ng、15.6ng、7.8ng、3.9ng、2.0ng)的预装载可二聚抗cd19救助受体下共同培养24hr。
图7展示细胞因子释放分析的结果。抗bcma救助cart细胞或未转导的t细胞与cd19阳性nalm-6细胞以1:1e:t比值在减少量(125ng、62.5ng、31.3ng、15.6ng、7.8ng、3.9ng、2.0ng)的预装载可二聚抗cd19救助受体下共同培养24hr。测量il-2、il-4、il-17a、tnf和ifnγ量。
图8a展示抗bcmadaric和可二聚抗cd19救助受体系统的草图。
图8b展示可用抗cd19救助受体将经抗bcmatdaric细胞重导引于表达cd19的nalm-6细胞。
图8c展示当在抗cd19救助受体存在下与cd19表达nalm-6细胞共同培养时,抗bcmatdaric细胞仅分泌可检测水平的ifnγ。
具体实施方式
序列标识符的简要说明
seqidno:1阐述抗bcmacar的多肽序列。
seqidno:2阐述抗bcma救助car的多肽序列。
seqidno:3阐述二聚救助受体的多肽序列。
seqidno:4阐述二聚救助受体-t2a荧光报告子的多肽序列。
seqidno:5阐述二聚救助受体-t2a荧光报告子的多肽序列。
seqidno:6阐述抗bcmadaric的多肽序列。
seqidno:7-17阐述各种连接子的氨基酸序列。
seqidno:18-42阐述蛋白酶裂解位点和自我裂解多肽裂解位点的氨基酸序列。
a.概述
癌症常常是表达不同水平的各种抗原的细胞的异源库。一般来说,免疫疗法最初经选择以靶向抗原,所述抗原在大多数癌细胞上表达且基本缺乏在正常细胞上的表达。有效的靶向免疫疗法将杀灭大部分表达标靶抗原的癌细胞,从而实现部分或完全缓解。然而,因为大多数癌症本质上为异源的,所以不表达或表达低水平靶向抗原的剩余癌细胞得以存活或可能会产生初始免疫疗法未有效靶向的癌细胞。
仍限制cart细胞疗法的功效的一个主要障碍为“抗原阴性”癌症的复发。举例来说,尽管抗cd19cart细胞疗法最初导致复发性和难治性急性all的缓解速率令人印象深刻,但cd19阴性白血病胚细胞的复发在约10-20%的病例中出现。抗原阴性复发的速率令人警惕地高表示到目前为止cart免疫疗法的弱点仍未解决。不希望受任何具体的理论所束缚,本发明人已通过以下方式解决所述问题:重新工程改造car使得其可重新靶向实际上无限数目的在复发性或难治性抗原阴性癌细胞上表达的其它抗原。因此,本文中所涵盖的组合物和方法表示cart细胞免疫疗法的重要进展。
在各种实施例中,提供救助嵌合抗原受体(car)。救助car可包含一个或多个抗原结合域、多聚化域、跨膜域和一个或多个胞内信号传导域。在一些实施例中,car可通过将多聚化域并入car中适用于救助car。多聚化域可细胞内或细胞外安置。
在各种实施例中,提供可二聚救助受体。可二聚救助car受体可包含一个或多个抗原结合域和多聚化域,和任选地连接子域、铰链域和/或锚定域中的一种或多种。
在不同其它实施例中,提供救助car系统。救助car系统可包含救助cart细胞、可二聚救助受体和桥接因子。桥接因子结合救助car和可二聚救助受体的多聚化域,这导致官能性car信号传导复合物的形成。
在一些实施例中,救助cart细胞进一步包含诱导性可二聚救助受体。
在特定实施例中,提供一种用于纯化预负载桥接因子的可二聚救助受体的方法。
除非明确相反地指出,否则特定实施例的实践将采用在所属领域的技术范围内的化学、生物化学、有机化学、分子生物学、微生物学、重组dna技术、遗传学、免疫学以及细胞生物学的常规方法,其中许多方法出于说明的目的在下文有描述。在文献中全面解释了这些技术。参看例如sambrook等人,《分子克隆实验指南(molecularcloning:alaboratorymanual)》(第3版,2001);sambrook等人,《分子克隆实验指南》(第2版,1989);maniatis等人,《分子克隆实验指南》(1982);ausubel等人,《最新分子生物学实验方法汇编(currentprotocolsinmolecularbiology)》(约翰·威利父子出版公司(johnwileyandsons),2008年7月更新);《精编分子生物学实验指南(shortprotocolsinmolecularbiology)》,来自《最新分子生物学实验方法汇编》的方法概要,格林出版联合公司和威利跨学科(greenepub.associatesandwiley-interscience);glover,《dna克隆实用方法(dnacloning:apracticalapproach)》,第i卷和第ii卷(irl出版社,牛津(oxford),1985);anand,《复杂基因组分析技术(techniquesfortheanalysisofcomplexgenomes)》,(学术出版社(academicpress),纽约(newyork),1992);《转录与翻译(transcriptionandtranslation)》(b.hames和s.higgins编,1984);perbal,《分子克隆实践指南(apracticalguidetomolecularcloning)》(1984);harlow和lane,《抗体(antibodies)》,(冷泉港实验室出版社(coldspringharborlaboratorypress),冷泉港,纽约,1998);《免疫学最新方案(currentprotocolsinimmunology)》q.e.coligan,a.m.kruisbeek,d.h.margulies,e.m.shevach和w.strober编,1991);《免疫学年度综述(annualreviewofimmunology)》;以及如《免疫学进展(advancesinimmunology)》的杂志中的专论。
b.定义
除非另有定义,否则本文使用的所有技术和科学术语都具有与本发明所属领域的普通技术人员通常所了解相同的含义。虽然可以在实践或测试特定实施例时使用与本文中所描述的方法和材料类似或等同的任何方法和材料,但是本文中描述组合物、方法和材料的优选实施例。为了本公开的目的,下文定义以下术语。
本文使用的冠词“一(a/an)”指的是冠词的语法对象中的一个或超过一个(即至少一个或一个或多个)。举例来说,“一元件”意指一个元件或一个或多个元件。
替代方案(例如“或”)的使用应理解为意指替代方案中的一个、两个或其任何组合。
术语“和/或”应理解为意指替代方案中的一个或两个。
如本文所使用,术语“约”或“大约”是指数量、水平、数值、数目、频率、百分比、尺度、尺寸、量、重量或长度与参考数量、水平、数值、数目、频率、百分比、尺度、尺寸、量、重量或长度相比,变化多达15%、10%、9%、8%、7%、6%、5%、4%、3%、2%或1%。在一个实施例中,术语“约”或“大约”是指数量、水平、数值、数目、频率、百分比、尺度、尺寸、量、重量或长度的范围,所述范围为参考数量、水平、数值、数目、频率、百分比、尺度、尺寸、量、重量或长度的±15%、±10%、±9%、±8%、±7%、±6%、±5%、±4%、±3%、±2%或±1%。
在本说明书通篇中,除非上下文另外要求,否则措辞“包含(comprise/comprises/comprising)”应理解成暗示包括所陈述的步骤或要素或步骤或要素的群组,但不排除任何其它步骤或要素或步骤或要素的群组。“由……组成”打算包括并且限于短语“由……组成”之后的任何事物。因此,短语“由……组成”指示所列要素为需要或必需的,并且不能存在其它要素。“基本上由……组成”打算包括短语后所列的任何要素,并且限于不干扰或影响本发明中规定的所列要素的活性或作用的其它要素。因此,短语“基本上由……组成”表示所列要素是必不可少的或必选的,而且不能存在显著影响所列要素的活性或作用的其它要素。
贯穿本说明书提及“一个实施例”、“一实施例”、“特定实施例”、“相关实施例”、“某一实施例”、“额外实施例”或“另一实施例”或其组合是指结合实施例描述的特定特征、结构或特征包括于至少一个实施例中。因此,贯穿本说明书中的各处出现的前述短语不一定全部指代同一实施例。此外,在一个或多个实施例中,特定特性、结构或特征可以任何合适方式组合。还应理解,在一个实施例中对一个特征的正面叙述用作在一特定实施例中排除所述特征的基础。
“抗原(ag)”是指可刺激动物中抗体产生或t细胞应答的化合物、组合物或物质,其包括注入或吸入动物中的组合物(如包括癌症特异性蛋白质的组合物)。示例性抗原包括但不限于脂质、碳水化合物、多糖、糖蛋白、肽或核酸。抗原与特异性体液或细胞免疫产物反应,所述产物包括由异源抗原(如所公开的抗原)诱导的那些。
“标靶抗原”或“所关注的标靶抗原”为本文中所涵盖的结合域经设计以结合的抗原。在特定实施例中,标靶抗原选自由以下组成的组:α叶酸受体、5t4、αvβ6整合素、bcma、b7-h3、b7-h6、caix、cd16、cd19、cd20、cd22、cd30、cd33、cd37、cd44、cd44v6、cd44v7/8、cd70、cd79a、cd79b、cd123、cd138、cd171、cea、cspg4、egfr、包括erbb2(her2)的egfr家族、egfrviii、egp2、egp40、epcam、epha2、epcam、fap、胎儿achr、frα、gd2、gd3、磷脂酰肌醇蛋白聚糖-3(gpc3)、hla-a1+mage1、hla-a2+mage1、hla-a3+mage1、hla-a1+ny-eso-1、hla-a2+ny-eso-1、hla-a3+ny-eso-1、il-11rα、il-13rα2、lambda、lewis-y、kappa、间皮素、muc1、muc16、ncam、nkg2d配体、ny-eso-1、prame、psca、psma、ror1、ssx、存活素、tag72、tems、vegfr2和wt-1。
在一个实施例中,抗原为mhc-肽复合物,如i类mhc-肽复合物或ii类mhc-肽复合物。
如本文所用,术语“结合域”、“胞外域”、“抗原结合域”、“胞外结合域”、“胞外抗原结合域”、“抗原特异性结合域”和“胞外抗原特异性结合域”可互换地使用并提供能够特异性结合于所关注的标靶抗原的多肽。结合域可来源于天然、合成、半合成或重组来源。
如本文所用的术语“特异性结合亲和力”或“特异性结合(specificallybinds/specificallybound/specificbinding)”或“特异性靶向”描述抗体或其抗原结合片段以大于背景结合的结合亲和力结合于标靶抗原。如果结合域以例如大于或等于约105m-1的亲和力或ka(即,单位为1/m的特定结合相互作用的平衡缔合常数)与抗原结合或缔合,那么结合域“特异性结合”于标靶抗原。在某些实施例中,结合域(或其融合蛋白)以大于或等于约106m-1、107m-1、108m-1、109m-1、1010m-1、1011m-1、1012m-1或1013m-1的ka结合于标靶。“高亲和力”结合域(或其单链融合蛋白)是指具有至少107m-1、至少108m-1、至少109m-1、至少1010m-1、至少1011m-1、至少1012m-1、至少1013m-1或更高的ka的那些结合域。
或者,亲和力可定义为单元为m的特定结合相互作用的平衡解离常数(kd)(例如10-5m至10-13m或更小)。结合域多肽的亲和力可易于使用常规技术测定,例如通过竞争性酶联免疫吸附分析(enzyme-linkedimmunosorbentassay;elisa),或通过结合缔合,或使用标记配体的位移分析,或使用表面等离子体共振装置,如可获自新泽西州皮斯卡塔韦biacore公司的biacoret100,或光学生物传感器技术,如可分别获自康宁和珀金埃尔默的epic系统或enspire(此外,参见例如scatchard等人(1949)《纽约科学院年报(ann.n.y.acad.sci.)》51:660;和美国专利第5,283,173号;第5,468,614号或等效物)。
在一个实施例中,特异性结合的亲和力比背景结合大约2倍、比背景结合大约5倍、比背景结合大约10倍、比背景结合大约20倍、比背景结合大约50倍、比背景结合大约100倍、或比背景结合大约1000倍或更多。
“抗体”是指结合剂,其为多肽,至少包含特异性地识别和结合抗原的抗原决定基的轻链或重链免疫球蛋白可变区,所述多肽如脂质、碳水化合物、多糖、糖蛋白、肽或含有抗原决定簇的核酸,如免疫细胞识别的那些。
“抗原决定基”或“抗原决定簇”是指与结合剂结合的抗原的区域。
抗体包括其抗原结合片段,如camelig、ignar、fab片段、fab'片段、f(ab)'2片段、f(ab)'3片段、fv、单链fv蛋白(“scfv”)、双scfv、(scfv)2、微型抗体、双功能抗体、三功能抗体、四功能抗体、二硫化物稳定的fv蛋白(“dsfv”)和单域抗体(sdab,纳米抗体)以及负责抗原结合的全长抗体的部分。术语还包括基因工程改造形式,如嵌合抗体(例如人类化鼠抗体)、异结合抗体(例如双特异性抗体)和其抗原结合片段。还参见《皮尔斯目录与手册(piercecatalogandhandbook)》,1994-1995(piercechemicalco.,rockford,il);kuby,j.,《免疫学(immunology)》,第3版,w.h.freeman&co.,newyork,1997。
如熟练人员将理解和如本文中其它地方所描述,完全抗体包含两个重链和两个轻链。每个重链由可变区和第一、第二和第三恒定区组成,而每个轻链由可变区和恒定区组成。哺乳动物重链分类为α、δ、ε、γ和μ。哺乳动物轻链分类为λ或κ。包含α、δ、ε、γ和μ重链的免疫球蛋白分类为免疫球蛋白(ig)a、igd、ige、igg和igm。完全抗体形成“y”形状。y的干由结合在一起的两个重链的第二和第三恒定区(对于ige和igm,第四恒定区)组成且二硫键(链间)形成于铰链中。重链γ、α和δ具有由三个串联(呈直线)ig域构成的恒定区,和用于增加的柔性的铰链区;重链μ和ε具有由四个免疫球蛋白域构成的恒定区。第二和第三恒定区分别称为“ch2域”和“ch3域”。y的每个臂包括结合于单个轻链的可变区和恒定区的单个重链的可变区和第一恒定区。轻链和重链的可变区负责抗原结合。
轻链和重链可变区含有间杂有三个高变区(也称为“互补决定区”或“cdr”)的“构架”区。cdr可通过常规方法定义或鉴别,如通过根据kabat等人(wu,tt和kabat,
e.a.,《实验医学杂志(jexpmed.)》132(2):211-50,(1970);borden,p.和kabate.a.,pnas,84:2440-2443(1987)的序列;(参见kabat等人,《免疫学感兴趣的蛋白质的序列(sequencesofproteinsofimmunologicalinterest)》,美国卫生与公众服务部,1991,其以引用的方式并入本文中),或通过根据chothia等人(chothia,c.和lesk,a.m.,《分子生物学杂志(jmol.biol.)》,196(4):901-917(1987),chothia,c.等人,《自然(nature)》,342:877-883(1989))的结构。
用于预测轻链cdr的规则的说明性实例包括:cdr-l1约在残基24处开始,前面是cys,为约10-17个残基,且之后为trp(通常为trp-tyr-gln,以及trp-leu-gln、trp-phe-gln、trp-tyr-leu);cdr-l2在cdr-l1末端之后约16个残基处开始,一般前面是ile-tyr,以及val-tyr、ile-lys、ile-phe,且为7个残基;且cdr-l3在cdr-l2末端之后约33个残基处开始,前面是cys,为7-11个残基,且之后为phe-gly-xxx-gly(seqidno:44)(xxx为任何氨基酸)。
用于预测重链cdr的规则的说明性实例包括:cdr-h1约在残基26处开始,前面是cys-xxx-xxx-xxx(seqidno:45),为10-12个残基且之后为trp(通常为trp-val,以及trp-ile、trp-ala);cdr-h2在cdr-h1末端之后约15个残基处开始,一般前面是leu-glu-trp-ile-gly(seqidno:46),或多种变异体,为16-19个残基,且之后为lys/arg-leu/ile/val/phe/thr/ala-thr/ser/ile/ala;且cdr-h3在cdr-h2末端之后约33个残基处开始,前面是cys-xxx-xxx(seqidno:45)(通常为cys-ala-arg),为3至25个残基,且之后为trp-gly-xxx-gly(seqidno:47)。
在一个实施例中,轻链cdr和重链cdr根据卡巴特方法测定。
在一个实施例中,轻链cdr以及重链cdr2和cdr3根据卡巴特方法测定,且重链cdr1根据abm方法测定,所述abm方法包含在卡巴特和科西亚方法之间,参见例如whiteleggn&reesar,《蛋白质工程(proteineng.)》2000年12月;13(12):819-24和《分子生物学方法(methodsmolbiol.)》2004;248:51-91。用于预测cdr的程序公开可用,例如abysis(www.bioinf.org.uk/abysis/)。
不同轻链或重链的构架区的序列在物种(如人类)内具有相对保存性。抗体的构架区(其是成分轻链和重链的组合构架区)用于在三维空间中定位和对准cdr。cdr主要负责与抗原的抗原决定基结合。每个链的cdr通常称为cdr1、cdr2和cdr3,从n端开始依序编号,并且也通常通过具体cdr所位于的链鉴别。因此,位于抗体的重链的可变域的cdr称为cdrh1、cdrh2和cdrh3,而位于抗体的轻链的可变域的cdr称为cdrl1、cdrl2和cdrl3。具有不同特异性(即针对不同抗原的组合位点)的抗体具有不同cdr。尽管抗体与抗体之间的cdr不同,但cdr内仅有限数目的氨基酸位置直接涉及抗原结合。cdr内的这些位置称为特异性决定残基(sdr)。
“vl”或“vl”的提及是指免疫球蛋白轻链的可变区,其包括抗体、fv、scfv、dsfv、fab或如本文中所公开的其它抗体片段的可变区。
“vh”或“vh”的参考是指免疫球蛋白重链的可变区,其包括抗体、fv、scfv、dsfv、fab或如本文中所公开的其它抗体片段的可变区。
“单克隆抗体”是由b淋巴细胞的单一克隆或由其中已转染单一抗体的轻链和重链基因的细胞产生的抗体。单克隆抗体通过所属领域的技术人员已知的方法制得,例如通过由骨髓瘤细胞与免疫脾细胞的融合体制备形成抗体的杂交细胞。单克隆抗体包括人类化单克隆抗体。
“嵌合抗体”具有来自一个物种(如人类)的构架残基和来自另一物种(如小鼠)的cdr(一般赋予抗原结合)。在特定的优选实施例中,抗原特异性结合域为嵌合抗体或其抗原结合片段。
在特定实施例中,抗体为人类抗体(如人类单克隆抗体)或其特异性结合于标靶抗原的抗原结合片段。人类抗体可通过组合选自具有如上文所述的已知人类恒定域序列的人源噬菌体呈现文库的fv克隆可变域序列构建。或者,人类单克隆抗体可通过融合瘤方法制备。用于产生人类单克隆抗体的人类骨髓瘤和小鼠-人类杂交骨髓瘤细胞系已例如通过kozbor《免疫学杂志(j.immunol.)》,133:3001(1984);brodeur等人,《单克隆抗体产生技术和应用(monoclonalantibodyproductiontechniquesandapplications)》,第51-63页(marceldekker,inc.,newyork,1987);和boerner等人,《免疫学杂志(j.immunol.)》,147:86(1991)描述。另外,可以使用转殖基因动物(例如小鼠)在无内源性免疫球蛋白产生存在下产生人类抗体的完整谱。参见例如jakobovits等人,《美国国家科学院院刊(pnasusa)》,90:2551(1993);jakobovits等人,《自然》,362:255(1993);bruggermann等人,《免疫学年会(yearinimmunol.)》,7:33(1993)。还可以使用基因混编从非人类,例如啮齿动物抗体衍生人类抗体,其中人类抗体具有与起始非人类抗体相似的亲和力和特异性。参见1993年4月1日公开的pctwo93/06213。不同于通过cdr接枝进行的非人类抗体的传统人类化,此技术提供完全人类抗体,其不具有非人类来源的fr或cdr残基。
“人类化”抗体是包括人类构架区和一个或多个来自非人类(例如小鼠、大鼠或合成)免疫球蛋白的cdr的免疫球蛋白。提供cdr的非人类免疫球蛋白称为“供体”,并且提供构架的人类免疫球蛋白称为“受体”。在一个实施例中,所有cdr都来自人类化免疫球蛋白中的供体免疫球蛋白。恒定区不必存在,但如果存在,那么它们必须与人类免疫球蛋白恒定区大体上一致,即至少约85-90%,如约95%或更多一致。因此,人类化免疫球蛋白的所有部分(可能cdr除外)与天然人类免疫球蛋白序列的相应部分大体上一致。人类化或其它单克隆抗体可以具有其它保守性氨基酸取代,其对抗原结合或其它免疫球蛋白功能基本无影响。人类化抗体可借助于基因工程改造构建(参见例如美国专利第5,585,089号)。
如本文所用的“camelig”或“camelidvhh”是指重链抗体的已知最小抗原结合单位(koch-nolte等人,《美国实验生物学学会联合会杂志(fasebj.)》,21:3490-3498(2007))。“重链抗体”或“camelid抗体”是指含有两个vh域和不含轻链的抗体(riechmannl.等人,《免疫学方法杂志(j.immunol.methods)》231:25-38(1999);wo94/04678;wo94/25591;美国专利第6,005,079号)。
“免疫球蛋白新抗原受体”的“ignar”是指来自鲨鱼免疫系统全部的抗体的类别,所述抗体由一个可变新抗原受体(vnar)域和五个恒定新抗原受体(cnar)域的均二聚体组成。ignar表示一些基于免疫球蛋白的已知最小蛋白质骨架且高度稳定并具有有效的结合特征。固有稳定性可归因于(i)基础的ig骨架,其相比于发现于鼠类抗体中的常规的抗体vh和vl域呈现大量的带电和暴露亲水性表面的残基;和(ii)互补决定区(cdr)环中的稳定的结构特点,所述互补决定区(cdr)环包括环间二硫桥键和环内氢键的模式。
木瓜蛋白酶消化抗体产生两个相同的抗原结合片段,称为“fab”片段,各自具有单一抗原结合位点;和剩余的“fc”片段,其名字反映了其容易结晶的能力。胃蛋白酶处理产生f(ab')2片段,所述片段具有两个抗原组合位点且仍然能够交联抗原。
“fv”为含有完全抗原结合位点的最小抗体片段。在一个实施例中,双链fv物种由一个重链可变域与一个轻链可变域经由非共价紧密缔合而成的二聚体组成。在单链fv(scfv)物种中,一个重链可变域与一个轻链可变域可以通过柔性肽连接子共价连接,因此轻链和重链可以类似于双链fv物种的“二聚”结构缔合。在这一配置中,每个可变域的三个高变区(hvr)相互作用以界定vh-vl二聚体的表面上的抗原结合位点。六个hvr共同地对抗体赋予抗原结合特异性。然而,尽管单个可变域(或仅包含三个对抗原具有特异性的hvr的fv的一半)能够识别并结合抗原,但亲和力低于整个结合位点。
fab片段含有重链和轻链可变域且还含有轻链的恒定域和重链的第一恒定域(ch1)。fab'片段与fab片段不同之处在于,重链ch1域的羧基端增添了几个残基,包括一个或多个来自抗体铰链区的半胱氨酸。fab'-sh是本文关于fab'的名称,其中恒定域的半胱氨酸残基载有游离硫醇基。f(ab′)2抗体片段最初产生为在其之间具有铰链半胱氨酸的fab'片段对。抗体片段的其它化学偶联也是已知的。
术语“双功能抗体”是指具有两个抗原结合位点的抗体片段,所述片段包含连接到同一多肽链(vh-vl)中的轻链可变域(vl)的重链可变域(vh)。通过使用过短以使得同一链上的两个域之间不能配对的连接子,迫使所述域与另一条链的互补域配对,并且产生两个抗原结合位点。双功能抗体可为二价或双特异性的。双功能抗体更充分地描述于例如ep404,097;wo1993/01161;hudson等人,《自然医学(nat.med.)》9:129-134(2003);和hollinger等人,《美国国家科学院院刊》90:6444-6448(1993)。三功能抗体和四功能抗体也描述于hudson等人,《自然医学》9:129-134(2003)中。
“单域抗体”或“sdab”或“纳米抗体”是指由抗体重链的可变区(vh域)或抗体轻链的可变区(vl域)组成的抗体片段(holt,l.等人,《生物技术趋势(trendsinbiotechnology)》,21(11):484-490)。
“单链fv”或“scfv”抗体片段包含抗体的vh和vl域,其中这些域存在于单多肽链中且以任一取向(例如vl-vh或vh-vl)存在。一般来说,scfv多肽还在vh域与vl域之间包含多肽连接子,由此使scfv能够形成抗原结合所希望的结构。关于scfv的综述,参看例如pluckthün,《单克隆抗体的药理学(thepharmacologyofmonoclonalantibodies)》,第113卷,rosenburg和moore编,(springer-verlag,纽约(newyork),1994),第269-315页。
单链抗体可以从对所需标靶具有特异性的融合瘤的v区基因克隆。这类杂交瘤的产生已变得常规。可用于克隆可变区重链(vh)和可变区轻链(vl)的技术已描述于例如orlandi等人,pnas,1989;86:3833-3837。
“连接子”是指为实现分子的合适间隔和构形所增添的各种多肽域(例如vh与vl域之间)之间的多个氨基酸残基。在特定实施例中,连接子为可变区连接序列。“可变区连接序列”为氨基酸序列,其连接vh和vl域且提供与两个子结合域的相互作用相容的间隔功能,使得所得多肽保留对与包含相同轻链和重链可变区的抗体相同的靶分子的特异性结合亲和力。在特定实施例中,连接子分离一个或多个重链或轻链可变域、铰链域、多聚化域、跨膜域、共刺激域和/或初级信号传导域。
适用于本文中所涵盖的特定实施例的连接子的所说明实例包括但不限于以下氨基酸序列:ggg;dgggs(seqidno:7);tgekp(seqidno:8)(参见例如liu等人,pnas5525-5530(1997));ggrr(seqidno:9)(pomerantz等人1995,见上文);(ggggs)n,其中n=1、2、3、4或5(seqidno:10)(kim等人,pnas93,1156-1160(1996.));egkssgsgseskvd(seqidno:11)(chaudhary等人,1990,《美国国家科学院院刊(proc.natl.acad.sci.u.s.a.)》87:1066-1070);kesgsvsseqlaqfrsld(seqidno:12)(bird等人,1988,《科学(science)》242:423-426)、ggrrgggs(seqidno:13);lrqrdgerp(seqidno:14);lrqkdgggserp(seqidno:15);lrqkd(gggs)2erp(seqidno:16)。或者,柔性连接子可使用能够自身建模dna-结合位点和肽(desjarlais&berg,pnas90:2256-2260(1993),pnas91:11099-11103(1994))的电脑程式或通过噬菌体呈现方法合理设计。在一个实施例中,连接子包含以下氨基酸序列:gstsgsgkpgsgegstkg(seqidno:17)(cooper等人,《血液(blood)》,101(4):1637-1644(2003))。
“间隔子域”是指分离两个域的多肽。在一个实施例中,间隔子域将抗原结合域移动远离效应细胞表面以能够实现适当的细胞/细胞接触、抗原结合和活化(patel等人,《基因疗法(genetherapy)》,1999;6:412-419)。在特定实施例中,间隔子域分离一个或多个重链或轻链可变域、多聚化域、跨膜域、共刺激域和/或初级信号传导域。间隔子域可来源于天然、合成、半合成或重组来源。在某些实施例中,间隔子域为免疫球蛋白的一部分,所述免疫球蛋白包括但不限于一个或多个重链恒定区,例如ch2和ch3。间隔子域可包括天然存在的免疫球蛋白铰链区或改变的免疫球蛋白铰链区的氨基酸序列。
“铰链域”是指多肽,其在远离效应细胞表面定位抗原结合域以能够实现适当的细胞/细胞接触、抗原结合和活化方面起重要作用。在特定实施例中,多肽可在结合域与多聚化域之间、结合域与跨膜域(tm)之间、或多聚化域与跨膜域之间包含一个或多个铰链域。铰链域可来源于天然、合成、半合成或重组来源。铰链域可包括天然存在的免疫球蛋白铰链区或改变的免疫球蛋白铰链区的氨基酸序列。
“改变的铰链区”是指(a)具有至多30%氨基酸变化(例如至多25%、20%、15%、10%或5%氨基酸取代或缺失)的天然存在的铰链区;(b)具有至多30%氨基酸变化(例如至多25%、20%、15%、10%或5%氨基酸取代或缺失)的长度为至少10个氨基酸(例如至少12、13、14或15个氨基酸)的天然存在的铰链区的一部分;或(c)包含核心铰链区的天然存在的铰链区的一部分(其长度可为4、5、6、7、8、9、10、11、12、13、14或15个,或至少4、5、6、7、8、9、10、11、12、13、14或15个氨基酸)。在某些实施例中,天然存在的免疫球蛋白铰链区中的一个或多个半胱氨酸残基可被一个或多个其它氨基酸残基(例如一个或多个丝氨酸残基)取代。改变的免疫球蛋白铰链区或者或另外可以具有被另一氨基酸残基(例如丝氨酸残基)取代的野生型免疫球蛋白铰链区的脯氨酸残基。
如本文所用的“多聚化域”是指优选地直接或经由桥接分子与另一不同多肽相互作用或缔合的多肽,其中不同多聚化域的相互作用实质上有助于或有效促进多聚化(即,二聚体、三聚体或多部分复合物的形成,所述多部分复合物可为均二聚体、杂二聚体、均三聚体、异三聚体、均多聚体、异质多聚体)。多聚化域可来源于天然、合成、半合成或重组来源。
适用于本文中所涵盖的特定实施例的多聚化域的说明性实例包括fkbp多肽、frb多肽、钙调神经磷酸酶多肽、亲环素多肽、细菌性dhfr多肽、pyl1多肽、abi1多肽、gib1多肽、gai多肽和其变异体。
“桥接因子”是指与两个或更多个多聚化域缔合且安置在两个或更多个多聚化域之间的分子。在特定实施例中,多聚化域仅在桥接因子存在下实质上有助于或有效促进多肽复合物的形成。在特定实施例中,多聚化域在无桥接因子存在下不会有助于或有效促进多肽复合物的形成。适用于本文中所涵盖的特定实施例的桥接因子的说明性实例包括但不限于雷帕霉素(rapamycin)(西罗莫司(sirolimus))或其雷帕霉素类似物、库马霉素(coumermycin)或其衍生物、赤霉素或其衍生物、脱落酸(aba)或其衍生物、甲氨蝶呤或其衍生物、环孢菌素a或其衍生物、fkcsa或其衍生物、fkbp(slf)或其衍生物的甲氧苄氨嘧啶(tmp)-合成配体、或其任何组合。
雷帕霉素类似物(rapamycinanalogs;rapalogs)包括但不限于美国专利第6,649,595号中所公开那些,该等雷帕霉素类似物结构以全文引用的方式并入本文中。在某些实施例中,桥接因子为相比于雷帕霉素免疫抑制效果显著降低的雷帕霉素类似物。在一优选实施例中,雷帕霉素类似物为ap21967衍生物(又称为c-16-(s)-7-甲基吲哚雷帕霉素,ic50=10nm,化学修饰的非免疫抑制雷帕霉素类似物)。
“显著降低的免疫抑制效果”是指如临床上或在具有人类免疫抑制活性的合适体外(例如t细胞增殖的抑制)或体内替代物中所测量,雷帕霉素类似物的免疫抑制效果为针对等摩尔量的雷帕霉素所观测或预期的免疫抑制效果的至少小于0.1至0.005倍。在一个实施例中,“显著降低的免疫抑制效果”是指雷帕霉素类似物在此类体外分析中的ec50值比在同一分析中针对雷帕霉素所观测到的ec50值大至少10至250倍。雷帕霉素类似物的其它说明性实例包括但不限于ap21967、依维莫司、诺瓦莫司(novolimus)、吡美莫司、地磷莫司、他克莫司、坦罗莫司、优米莫司和佐他莫司。
如本文所用,“锚定域”是指促进可二聚救助受体系栓、锚定或缔合至细胞表面的氨基酸序列或其它分子。示例性锚定域包括具有在细胞膜中稳定的结构的氨基酸序列或促进糖脂(又称为糖基磷脂酰肌醇或gpi)添加的氨基酸序列,或类似物。借助于背景,gpi分子通过转酰氨基作用反应翻译后附接至蛋白质标靶,这导致羧基端gpi信号序列裂解(参见例如white等人,《细胞科学杂志(j.cellsci.)》113:721,2000)以及已经合成的gpi锚定分子同时转移至新近形成的羧基端氨基酸(参见示例性gpi锚的www.ncbi.nlm.nih.gov/books/nbk20711,该等gpi锚以全文引用的方式合并)。在某些实施例中,锚定域为疏水性域(例如跨膜域)或gpi信号序列。在一些实施例中,编码本文中所涵盖的多肽的核酸分子包含锚定域,任选地其中锚定域为gpi分子。
“跨膜域”为将多肽锚定至细胞质膜的域。tm域可来源于天然、合成、半合成或重组来源。
“胞内信号传导域”是指多肽,其参与通过在免疫效应细胞上表达的受体将标靶抗原有效结合的信息转导至免疫效应细胞内部以引发效应细胞功能(例如活化、细胞因子产生、增殖和细胞毒性活性),所述信息包括细胞毒性因子的释放,或抗原结合至在免疫效应细胞上表达的受体所引起的其它细胞应答。
术语“效应功能”是指免疫效应细胞的专用功能。t细胞的效应功能例如可为溶细胞活性或帮助或活性,包括细胞因子的分泌。因此,术语“胞内信号传导域”是指转导效应功能信号且导引细胞执行专用功能的蛋白质的部分。尽管通常可采用整个胞内信号传导域,但在许多情况下不必使用整个域。就使用胞内信号传导域的截短部分来说,可使用这类截短部分代替整个域,只要其转导效应功能信号即可。术语胞内信号传导域意欲包括足以转导效应功能信号的胞内信号传导域的任何截短部分。
众所周知,仅经由tcr产生的信号不足以完全活化t细胞且还需要二次或共刺激信号。因此,可以称t细胞活化通过两个不同类别的胞内信号转导域介导:经由tcr(例如tcr/cd3复合物)起始抗原依赖性初级活化的初级信号传导域和以不依赖抗原的方式起作用以提供二次或共刺激信号的共刺激信号传导域。
“初级信号传导域”是指以刺激方式或以抑制方式调节tcr复合物的初级活化的信号传导域。以刺激方式起作用的初级信号传导域可含有信号传导基元,所述信号传导基元称为基于免疫受体酪氨酸的活化基元或itam。适用于特定实施例的含有初级信号传导域的itam的说明性实例包括但不限于来源于fcrγ、fcrβ、cd3γ、cd3δ、cd3ε、cd3ζ、cd22、cd79a、cd79b和cd66d的那些。
如本文所用,术语“共刺激信号传导域”或“共刺激域”是指共刺激分子的胞内信号传导域。共刺激分子是除抗原受体或fc受体以外的细胞表面分子,其在结合于抗原时提供t淋巴细胞的有效活化和功能所需的第二信号。可分离共刺激域的这类共刺激分子的说明性实例包括但不限于:tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9、tlr10、card11、cd2、cd7、cd27、cd28、cd30、cd40、cd54(icam)、cd83、cd134(ox40)、cd137(4-1bb)、cd278(icos)、dap10、lat、nkd2c、slp76、trim和zap70。
如本文所用,术语“癌症”大体上涉及异常细胞不受控制地分裂且可侵入邻近组织的一类疾病或病状。
如本文所用,术语“恶性肿瘤”是指一种癌症,其中肿瘤细胞群组呈现以下中的一种或多种:不受控生长(即,超过正常限度的分裂)、侵入(即,浸入和破坏相邻组织)和癌转移(即,经由淋巴或血液扩散至身体中的其它位置)。如本文所用,术语“转移”是指癌症从身体的一个部分扩散到另一部分。由已扩散的细胞所形成的肿瘤称为“转移瘤”或“癌转移”。转移瘤含有与原始肿瘤(原发瘤)中的那些细胞相似的细胞。
如本文所用,术语“良性”或“非恶性”是指肿瘤可生长至较大但不扩散到身体的其它部分。良性肿瘤自我限制且通常不入侵或转移。
“癌细胞”是指癌症生长或组织的单独细胞。癌细胞包括实体癌和液体癌两者。“肿瘤”或“肿瘤细胞”一般指代由细胞的异常生长所形成的肿胀或病变,其可为良性的、癌前的或恶性的。大多数癌症形成肿瘤,但液体癌,例如白血病不必形成肿瘤。对于形成肿瘤的那些癌症,术语癌症(细胞)和肿瘤(细胞)可互换地使用。个体中肿瘤的量是“肿瘤负荷”,其可以肿瘤的数目、体积或重量形式测量。
术语“复发”是指在改善或缓解一段时间后,诊断到癌症恢复,或癌症恢复的征象和症状。
“缓解”也称为“临床缓解”且包括部分和完全缓解。在部分缓解中,癌症的一些但并非全部征象和症状消失。在完全缓解中,癌症的全部征象和症状消失,但癌症仍可能存在于身体中。
“难治性”是指癌症对使用特定治疗剂的疗法具有抵抗性或对其无应答。癌症可从治疗开始难治(即,对初始暴露于治疗剂无应答),或历经第一治疗时段过程或在后续治疗时段期间,由于对治疗剂产生抗性而难治。
“抗原阴性”是指细胞不表达抗原或表达可忽略量的抗原,所述抗原不可检测。在一个实施例中,抗原阴性细胞不结合针对抗原的受体。在一个实施例中,抗原阴性细胞不显著结合针对抗原的受体。
如本文所用,术语“患者”是指可用本文中所涵盖的组合物和方法治疗的已诊断患有特定疾病、病症或病状的受试者。
如本文所用,“治疗(treatment/treating)”包括对疾病或病理学病况的症状或病变的任何有益或理想作用,并且甚至可以包括所治疗疾病或病况的一个或多个可测量标记的最小降低。治疗可以任选地涉及疾病或病况的减少,或延迟疾病或病况的进展,例如延迟肿瘤生长。“治疗”不一定表示疾病或病况或其相关症状完全根除或治愈。
如本文所用,“预防(prevent)”和类似词语(例如“prevented”、“preventing”等)指示用于预防、抑制或降低疾病或病况出现或复发的可能性的方法。还指的是延迟疾病或病况发作或复发或延迟疾病或病况的症状出现或复发。如本文所用,“预防”和类似词语还包括在疾病或病况发作或复发之前降低疾病或病况的强度、影响、症状和/或负荷。
如本文中所使用,短语“改善……的至少一种症状”是指减少受试者正在治疗的疾病或病况的一种或多种症状。在特定实施例中,所治疗的疾病或病况为癌症,其中所改善的一种或多种症状包括但不限于虚弱、疲劳、呼吸急促、容易瘀伤和出血、频繁感染、淋巴结肿大、腹胀或腹痛(由于腹部器官增大)、骨头或关节疼痛、骨折、非计划体重减轻、食欲不振、盗汗、持续性轻度发热和排尿减少(由于肾功能损伤)。
“提高”或“促进”、或“增加”或“扩增”通常是指本文所涵盖的组合物相较于由媒剂或对照分子/组合物引起的应答能够产生、引发或引起更大生理应答(即,下游作用)。可测量的生理应答可以尤其包括t细胞扩增、活化、存留的增加和/或癌细胞杀伤能力的增加,从本领域中的理解和本文中的描述显而易见。“增加”或“提高”量通常为“统计显著”量,且可包括相比于媒剂或对照组合物所产生的应答1.1、1.2、1.5、2、3、4、5、6、7、8、9、10、15、20、30或更多倍(例如500、1000倍)(包括两者之间且大于1的全部整数与小数点,例如1.5、1.6、1.7、1.8等)的增加。
“减小”或“降低”或“减轻”或“减少”或“减弱”通常是指本文所涵盖的组合物相较于由媒剂或对照分子/组合物引起的应答能够产生、引发或引起更小生理应答(即,下游作用)。“降低”或“减少”量通常为“统计显著”量,且可包括相比于媒剂、对照组合物所产生的应答,或在特定细胞谱系中的应答,1.1、1.2、1.5、2、3、4、5、6、7、8、9、10、15、20、30或更多倍(例如500、1000倍)(包括两者之间且大于1的全部整数与小数点,例如1.5、1.6、1.7、1.8等)的减少。
“维持(maintain)”或“保持”或“维持(maintenance)”或“无变化”或“无实质性变化”或“无实质性减小”通常是指本文所涵盖的组合物相较于由媒剂、对照分子/组合物引起的应答或特定细胞谱系中的应答能够在细胞中产生、引发或引起大体上类似或相当的生理应答(即,下游作用)。相当的应答是与参考应答并无显著不同或可测量不同的应答。
c.救助嵌合抗原受体
在各种实施例中,提供经基因工程改造的受体,其重导引免疫效应细胞对表达标靶抗原的癌细胞的细胞毒性。这些经基因工程改造的受体在本文中称为救助嵌合抗原受体(car)。救助car是组合对所需抗原的基于抗体的特异性与t细胞受体活化胞内域以产生展现抗原特异性细胞免疫活性的嵌合蛋白的分子。救助car还含有多聚化域,所述多聚化域允许抗原特异性car经重导引至另一抗原。如本文所用,术语“嵌合”描述由来自不同来源的不同蛋白质或dna部分构成。包含救助car的t细胞称为cart细胞,其表达救助car或救助cart细胞。
在特定实施例中,救助car包含结合标靶抗原的胞外域(也称为结合域或抗原特异性结合域)、多聚化域、跨膜域和一个或多个胞内信号转导域。在其它特定实施例中,救助car包含胞外抗原特异性结合域、跨膜域、多聚化域和一个或多个胞内信号传导域。救助car的抗原结合域与靶细胞表面上的标靶抗原的接合导致救助car的群聚且将活化刺激传递至含救助car的细胞。救助car的主要特征是其能够重导引免疫效应细胞特异性,进而触发增殖、细胞因子产生、吞噬作用或可以不依赖主要组织相容性的方式介导表达标靶抗原的细胞的细胞死亡的分子的产生,采用单克隆抗体、可溶性配体或细胞特异性共受体的细胞特异性靶向能力。
在各种实施例中,本文中所涵盖的救助car提供对癌症,任选地对救助car所靶向的初始抗原具有抗原阴性的复发性或难治性癌症的增加的靶向灵活性和重新靶向性。
在特定实施例中,救助car包含:胞外抗原结合域;多聚化域;跨膜域;一个或多个胞内共刺激信号传导域;和/或初级信号传导域。
在特定实施例中,救助car包含:胞外抗原结合域;跨膜域;多聚化域;一个或多个胞内共刺激信号传导域;和/或初级信号传导域。
在特定实施例中,救助car包含:胞外结合域,其包含抗体或其抗原结合片段;一个或多个间隔子域和/或连接子;多聚化域、一个或多个铰链域、跨膜域包括;一个或多个胞内共刺激信号传导域;和初级信号传导域。
在特定实施例中涵盖的救助car包含选自由以下组成的组的抗原结合域:camelig、ignar、fab片段、fab'片段、f(ab)'2片段、f(ab)'3片段、fv、单链fv抗体(“scfv”)、双scfv、(scfv)2、微型抗体、双功能抗体、三功能抗体、四功能抗体、二硫化物稳定的fv蛋白(“dsfv”)和单域抗体(sdab,纳米抗体)。在一些优选实施例中,抗原结合域为scfv或单域抗体。
在特定实施例中,抗原结合域结合选自由以下组成的组的标靶抗原:α叶酸受体、5t4、αvβ6整合素、bcma、b7-h3、b7-h6、caix、cd16、cd19、cd20、cd22、cd30、cd33、cd37、cd44、cd44v6、cd44v7/8、cd70、cd79a、cd79b、cd123、cd138、cd171、cea、cspg4、egfr、包括erbb2(her2)的egfr家族、egfrviii、egp2、egp40、epcam、epha2、epcam、fap、胎儿achr、frα、gd2、gd3、磷脂酰肌醇蛋白聚糖-3(gpc3)、hla-a1+mage1、hla-a2+mage1、hla-a3+mage1、hla-a1+ny-eso-1、hla-a2+ny-eso-1、hla-a3+ny-eso-1、il-11rα、il-13rα2、lambda、lewis-y、kappa、间皮素、muc1、muc16、ncam、nkg2d配体、ny-eso-1、prame、psca、psma、ror1、ssx、存活素、tag72、tems、vegfr2和wt-1。
在特定实施例中,标靶抗原选自由以下组成的组:bcma、cd19、cspg4、psca、ror1和tag72。
在特定实施例中,标靶抗原选自由以下组成的组:bcma、cd19、cd20、cd22、cd23、cd33、cd37、cd52、cd80和hla-dr。
特定实施例中所涵盖的car在救助car的各个域之间包含一个或多个连接子或间隔子多肽从而在一些情况下提供救助car域的合适间隔和构形。在特定实施例中,连接子安置在救助car的抗原结合域中的scfv的重链可变域与轻链可变域之间。在特定实施例中,连接子为(ggggs)n连接子,其中n=1、2、3、4或5(seqidno:10)。
在某些实施例中,救助car包含间隔子域,所述间隔子域含有igg1、igg4或igd的ch2和ch3域。
在特定实施例中救助car还可以含有铰链域。适用于本文所述的救助car的说明性铰链域包括来源于1型膜蛋白(如cd8α和cd4)的胞外区的铰链区,其可为来自这些分子的野生型铰链区或可改变。在另一实施例中,铰链域包含cd8α铰链区。在一个实施例中,铰链为pd-1铰链或cd152铰链。
在特定实施例中,救助car包含一个或多个多聚化域。在特定实施例中,多聚化域为胞外的。多聚化域可安置在抗原结合域与跨膜域之间、抗原结合域与铰链域之间、或铰链域与跨膜域之间。适用于本文中所涵盖的特定实施例的多聚化域的说明性实例包括fkbp多肽、frb多肽、钙调神经磷酸酶多肽、亲环素多肽、细菌性dhfr多肽、pyl1多肽、abi1多肽、gib1多肽、gai多肽和其变异体。
在一个实施例中,多聚化域选自由以下组成的组:fkbp多肽、frb多肽和其变异体。
在一个实施例中,多聚化域选自由以下组成的组:fkbp12多肽和frbt2098l多肽。
在特定实施例中,救助car包含tm域,所述tm域可来源于(即至少包含以下各者的跨膜区):t细胞受体的α或β链、cdδ、cd3ε、cdγ、cd3ζ、cd4、cd5、cd8α、cd9、cd16、cd22、cd27、cd28、cd33、cd37、cd45、cd64、cd71、cd80、cd86、cd134、cd137、cd152、cd154、amn和pd1。在一特定实施例中,tm域为合成的且主要包含疏水性残基,如亮氨酸和缬氨酸。
在一个实施例中,救助car包含来源于pd1、cd152或cd8α的tm域。在另一实施例中,救助car包含来源于pd1、cd152或cd8α以及长度优选地在1、2、3、4、5、6、7、8、9或10个氨基酸之间的短寡肽或多肽连接子的tm域,所述连接子连接救助car的tm域和胞内信号传导域。基于甘氨酸-丝氨酸的连接子提供尤其适合的连接子。
本文中涵盖的救助car包含一个或多个胞内信号传导域。在一个实施例中,救助car包含一个或多个共刺激胞内信号传导域和/或初级信号传导域。在一个实施例中,胞内信号传导域包含免疫受体酪氨酸活化基元(itam)。
适用于特定实施例的含有itam的初级信号传导域的说明性实例包括来源于fcrγ、fcrβ、cd3γ、cd3δ、cd3ε、cd3ζ、cd22、cd79a、cd79b和cd66d的那些。在特定的优选实施例中,救助car包含cd3ζ初级信号传导域和一个或多个共刺激信号传导域。胞内初级信号传导域和共刺激信号传导域可按任何次序串列连接至跨膜域的羧基端。
这类共刺激分子的说明性实例包括tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9、tlr10、card11、cd2、cd7、cd27、cd28、cd30、cd40、cd54(icam)、cd83、cd134(ox40)、cd137(4-1bb)、cd278(icos)、dap10、lat、nkd2c、slp76、trim和zap70。在一个实施例中,救助car包含一个或多个共刺激信号传导域,所述共刺激信号传导域选自由以下组成的组:cd28、cd137和cd134。在一个实施例中,救助car包含一个或多个共刺激信号传导域,所述共刺激信号传导域选自由以下组成的组:cd28、cd137和cd134以及cd3ζ初级信号传导域。
d.可二聚救助受体
在各种实施例中,本文中所涵盖的救助car已经工程改造以重导引免疫效应细胞对复发性或难治性癌细胞的细胞毒性。重导引或重新靶向cart细胞(救助cart细胞)对复发性或难治性癌细胞的分子在本文中称为可二聚救助受体。可二聚救助受体是分子,其组合对在复发性或难治性癌细胞上表达的抗原的基于抗体的特异性与在桥接因子存在下与救助car的多聚化域相互作用的多聚化域。在桥接因子存在下,可二聚救助受体接合救助car分子以重新起始对复发性或难治性癌细胞的免疫效应细胞活性。不希望受任何具体的理论所束缚,预期针对初始癌症抗原的cart细胞疗法将导致缓解。然而,如果癌症恢复和缺乏表达或表达极少初始癌症抗原,那么选择靶向在复发性或难治性癌细胞上表达的抗原的可二聚救助受体以重新起始对癌症的免疫效应细胞活性。
在各种实施例中,向已进行cart细胞疗法的受试者施用可二聚救助受体多肽。
在各种实施例中,向已进行cart细胞疗法的受试者施用预装载有桥接因子的可二聚救助受体多肽。
在各种实施例中,救助cart细胞包含可操作地连接于编码可二聚救助受体的多核苷酸的诱导型启动子。
在特定实施例中,可二聚救助受体包含结合桥接因子。
在特定实施例中,可二聚救助受体包含抗原结合域和多聚化域。
在特定实施例中,可二聚救助受体包含抗原结合域、多聚化域和锚定域。
在特定实施例中,可二聚救助受体包含抗原结合域、多聚化域、铰链域和锚定域。
在特定实施例中,可二聚救助受体基本上由信号肽、抗原结合域、连接子域和多聚化域组成。
在特定实施例中,可二聚救助受体基本上由信号肽、抗原结合域、连接子域、多聚化域、铰链域和锚定域组成。
在特定实施例中,可二聚救助受体基本上由抗原结合域、连接子域和多聚化域组成。。
在特定实施例中,可二聚救助受体基本上由抗原结合域、连接子域、多聚化域、铰链域和锚定域组成。
在特定实施例中涵盖的可二聚救助受体包含抗体或其抗原结合片段。在特定实施例中,抗体或抗原结合片段选自由以下组成的组:camelig、ignar、fab片段、fab'片段、f(ab)'2片段、f(ab)'3片段、fv、单链fv抗体(“scfv”)、双scfv、(scfv)2、微型抗体、双功能抗体、三功能抗体、四功能抗体、二硫化物稳定的fv蛋白(“dsfv”)和单域抗体(sdab,纳米抗体)。在一个优选实施例中,可二聚救助受体包含scfv抗原结合域。
在特定实施例中,可二聚救助受体包含抗原结合域,所述抗原结合域结合选自由以下组成的组的抗原:α叶酸受体、5t4、αvβ6整合素、bcma、b7-h3、b7-h6、caix、cd16、cd19、cd20、cd22、cd30、cd33、cd37、cd44、cd44v6、cd44v7/8、cd70、cd79a、cd79b、cd123、cd138、cd171、cea、cspg4、egfr、包括erbb2(her2)的egfr家族、egfrviii、egp2、egp40、epcam、epha2、epcam、fap、胎儿achr、frα、gd2、gd3、磷脂酰肌醇蛋白聚糖-3(gpc3)、hla-a1+mage1、hla-a2+mage1、hla-a3+mage1、hla-a1+ny-eso-1、hla-a2+ny-eso-1、hla-a3+ny-eso-1、il-11rα、il-13rα2、lambda、lewis-y、kappa、间皮素、muc1、muc16、ncam、nkg2d配体、ny-eso-1、prame、psca、psma、ror1、ssx、存活素、tag72、tems、vegfr2和wt-1。
在一个实施例中,抗原选自由以下组成的组:bcma、cd19、cspg4、psca、ror1和tag72;或选自由以下组成的组:bcma、cd19、cd20、cd22、cd23、cd33、cd37、cd52、cd80和hla-dr。
在特定实施例中,可二聚救助受体包含一个或多个连接子。连接子可安置在抗原结合域的重链可变区与轻链可变区与之间和/或抗原结合域与多聚化域之间。在一个实施例中,连接子为(ggggs)n连接子,其中n=1、2、3、4或5(seqidno:10)。
在一个实施例中,可二聚救助受体包含选自由以下组成的组的多聚化域:fkbp多肽、frb多肽、钙调神经磷酸酶多肽、亲环素多肽、细菌性dhfr多肽、pyl1多肽、abi1多肽、gib1多肽、gai多肽和其变异体。
在一个实施例中,多聚化域包含fkbp多肽、frb多肽或其变异体。
在一个实施例中,多聚化域包含fkbp12多肽或frbt2098l多肽。
在特定实施例中,可二聚救助受体包含铰链域。在一个实施例中,铰链域选自基本上由以下组成的组:cd4铰链、cd8α铰链、pd-1铰链和cd152铰链。
在特定实施例中,可二聚救助受体包含tm域,所述tm域可来源于(即至少包含以下各者的跨膜区):t细胞受体的α或β链、cdδ、cd3ε、cdγ、cd3ζ、cd4、cd5、cd8α、cd9、cd16、cd22、cd27、cd28、cd33、cd37、cd45、cd64、cd71、cd80、cd86、cd134、cd137、cd152、cd154、amn和pd1。在一特定实施例中,tm域为合成的且主要包含疏水性残基,如亮氨酸和缬氨酸。
在特定实施例中,可二聚救助受体包含gpi锚定分子。
e.救助car系统
复发性或难治性癌症是困扰细胞免疫疗法领域的普遍问题。本文中所涵盖的救助car系统提供用于治疗复发性/难治性癌症,尤其不再表达最初靶向的抗原(初始标靶抗原)的那些癌症的高效解决方案。举例来说,用抗cd19cart细胞治疗cd19表达白血病的患者最初可能展示改善和癌症消退,但最终白血病可能恢复,缺乏cd19表达。这种情况呈现出严重的问题,因为存在于患者中的cart细胞对cd19具有特异性且因此,复发性或难治性cd19阴性癌细胞对免疫系统不可见并将在无其它治疗性干预下不受限制地生长。救助car系统提供呈其它靶向受体形式的干涉,所述靶向受体在本文中称为可二聚救助受体。
在各种实施例中,向受试者提供救助car系统以便治疗癌症,以及在某些优选实施例中复发性或难治性癌症。救助car系统包含cart细胞,所述cart细胞包含针对在癌细胞上表达的第一抗原的救助car;针对在癌细胞上表达的第二抗原的可二聚救助受体;和桥接因子。
在各种实施例中,可向受试者提供或施用预装载或结合于桥接因子的可二聚救助受体。
在不同其它实施例中,在向受试者提供或施用时可二聚救助受体未预装载或结合于桥接因子。
不希望受任何具体的理论所束缚,预期一旦复发性/难治性癌症癌症在已用cart细胞治疗的受试者中显示自身,所述cart细胞表达针对在复发性/难治性癌症上不再表达,或不再显著表达的第一抗原的救助car,就向受试者施用针对在复发性或难治性癌细胞上表达或显著表达的第二抗原的可二聚救助受体。进一步向受试者施用桥接因子,所述桥接因子结合救助car的多聚化域和可二聚救助受体的多聚化域;进而促进救助car与救助受体之间的缔合。此缔合重新接合car信号传导路径且促进对表达第二抗原的复发性/难治性癌细胞的免疫效应细胞活性。
在特定实施例中,救助car系统包含:cart细胞(救助cart细胞),其包含结合第一抗原的car;结合第二抗原的可二聚救助受体;和桥接因子,其结合救助car和可二聚救助受体以形成对表达第二抗原的癌细胞的功能活性救助car。
在一个实施例中,向受试者施用可二聚救助受体。
在一个实施例中,救助cart细胞包含核酸,所述核酸包含诱导型启动子和编码可二聚救助受体的多核苷酸。
在一些实施例中,救助car和可二聚救助受体经设计以结合同一抗原上的不同抗原决定基。
在优选实施例中,第一抗原不同于第二抗原。
在特定实施例中,第一抗原和第二抗原独立地选自由以下组成的组:α叶酸受体、5t4、αvβ6整合素、bcma、b7-h3、b7-h6、caix、cd16、cd19、cd20、cd22、cd30、cd33、cd37、cd44、cd44v6、cd44v7/8、cd70、cd79a、cd79b、cd123、cd138、cd171、cea、cspg4、egfr、包括erbb2(her2)的egfr家族、egfrviii、egp2、egp40、epcam、epha2、epcam、fap、胎儿achr、frα、gd2、gd3、磷脂酰肌醇蛋白聚糖-3(gpc3)、hla-a1+mage1、hla-a2+mage1、hla-a3+mage1、hla-a1+ny-eso-1、hla-a2+ny-eso-1、hla-a3+ny-eso-1、il-11rα、il-13rα2、lambda、lewis-y、kappa、间皮素、muc1、muc16、ncam、nkg2d配体、ny-eso-1、prame、psca、psma、ror1、ssx、存活素、tag72、tems、vegfr2和wt-1。
在一个实施例中,救助car系统靶向b细胞恶性肿瘤。
在特定实施例中涵盖的救助car系统包含:cart细胞,其包含靶向选自由以下组成的组的第一抗原的救助car:bcma、cd19、cd20、cd22、cd23、cd33、cd37、cd52、cd80和hla-dr;和可二聚救助受体,其靶向选自由以下组成的组的第二抗原:bcma、cd19、cd20、cd22、cd23、cd33、cd37、cd52、cd80和hla-dr。
在特定实施例中,救助car系统包含:cart细胞,其包含靶向bcma的救助car;和可二聚救助受体,其靶向选自由以下组成的组的第二抗原:cd19、cd20、cd22、cd23、cd33、cd37、cd52、cd80和hla-dr。
在某些实施例中,救助car系统包含:cart细胞,其包含靶向cd19的救助car;和可二聚救助受体,其靶向选自由以下组成的组的第二抗原:bcma、cd20、cd22、cd23、cd33、cd37、cd52、cd80和hla-dr。
在一个实施例中,救助car系统包含:cart细胞,其包含靶向bcma的救助car;和靶向cd19的可二聚救助受体。
在另一实施例中,救助car系统包含:cart细胞,其包含靶向cd19的救助car;和靶向bcma的可二聚救助受体。
救助car系统为灵活性癌症靶向系统,其中对一种标靶抗原具有初始特异性的救助car经共同选择以经由救助car和可二聚救助受体中的多聚化域的桥接因子介导的缔合识别第二标靶抗原。
在各种实施例中,救助car多聚化域和可二聚救助受体多聚化域是选自以下的对:fkbp和frb、fkbp和钙调神经磷酸酶、fkbp和亲环素、fkbp和细菌性dhfr、钙调神经磷酸酶和亲环素、pyl1和abi1、或gib1和gai或其变异体。
在一个实施例中,救助car多聚化域包含fkbp多肽或其变异体,且可二聚救助受体多聚化域包含frb多肽或其变异体。
在一个实施例中,救助car多聚化域包含frb多肽或其变异体,且可二聚救助受体多聚化域包含fkbp多肽或其变异体。
在一个实施例中,桥接因子为ap21967、西罗莫司、依维莫司、诺瓦莫司、吡美莫司、地磷莫司、他克莫司、坦罗莫司、优米莫司或佐他莫司。
在一特定实施例中,救助car系统包含:cart细胞,其包含救助car,所述救助car具有对bcma具有特异性的scfv、frbt2098l多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的itam或初级信号传导域;和可二聚救助受体,其具有对cd19具有特异性的scfv、fkbp12多聚化域,和任选地锚定域,其中桥接因子为ap21967。
在一个实施例中,救助car系统包含:cart细胞,其包含救助car,所述救助car具有对cd19具有特异性的scfv、frbt2098l多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的itam或初级信号传导域;和可二聚救助受体,其具有对bcma具有特异性的scfv、fkbp12多聚化域,和任选地锚定域,其中桥接因子为ap21967。
在一特定实施例中,救助car系统包含:cart细胞,其包含救助car,所述救助car具有对bcma具有特异性的scfv、fkbp12多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的itam或初级信号传导域;和可二聚救助受体,其具有对cd19具有特异性的scfv、frbt2098l多聚化域,和任选地锚定域,其中桥接因子为ap21967。
在一个实施例中,救助car系统包含:cart细胞,其包含救助car,所述救助car具有对cd19具有特异性的scfv、fkbp12多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的itam或初级信号传导域;和可二聚救助受体,其具有对bcma具有特异性的scfv、frbt2098l多聚化域,和任选地锚定域,其中桥接因子为ap21967。
在另一实施例中,救助car系统包含:cart细胞,其包含救助car,所述救助car具有对bcma具有特异性的scfv、frb多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的itam或初级信号传导域;和可二聚救助受体,其具有对cd19具有特异性的scfv、fkbp12多聚化域,和任选地锚定域,其中桥接因子为雷帕霉素、坦罗莫司或依维莫司。
在另一实施例中,救助car系统包含:cart细胞,其包含救助car,所述救助car具有对cd19具有特异性的scfv、frb多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的itam或初级信号传导域;和可二聚救助受体,其具有对bcma具有特异性的scfv、fkbp12多聚化域,和任选地锚定域,其中桥接因子为雷帕霉素、坦罗莫司或依维莫司。
在另一实施例中,救助car系统包含:cart细胞,其包含救助car,所述救助car具有对bcma具有特异性的scfv、fkbp12多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的itam或初级信号传导域;和可二聚救助受体,其具有对cd19具有特异性的scfv、frb多聚化域,和任选地锚定域,其中桥接因子为雷帕霉素、坦罗莫司或依维莫司。
在另一实施例中,救助car系统包含:cart细胞,其包含救助car,所述救助car具有对cd19具有特异性的scfv、fkbp12多聚化域、跨膜域、4-1bb的共刺激域,和cd3ζ的itam或初级信号传导域;和可二聚救助受体,其具有对bcma具有特异性的scfv、frb多聚化域,和任选地锚定域,其中桥接因子为雷帕霉素、坦罗莫司或依维莫司。
f.多肽
本文中涵盖各种多肽,其包括但不限于救助car多肽、可二聚救助受体多肽和其片段、细胞和包含其的组合物、以及表达多肽的载体。
除非相反地指示且根据常规含义,即作为氨基酸的序列,“多肽”、“多肽片段”、“肽”和“蛋白质”可互换地使用。多肽可合成或以重组方式制得。多肽不限于特定长度,例如其可包含全长蛋白质序列或全长蛋白质的片段,且可包括多肽的翻译后修饰,例如糖基化、乙酰化、磷酸化等,以及所属领域中已知的天然存在的和非天然存在的其它修饰。在各种实施例中,多肽在蛋白质的n末端处包含信号(前导)序列,其共同翻译或翻译后导引蛋白质的转移。适用于本文中所涵盖的多肽的合适的信号序列的说明性实例包括但不限于igg1重链信号多肽、cd8α信号多肽或人类gm-csf受体α信号多肽。多肽可使用多种熟知重组和/或合成技术中的任一种制备。本文中所涵盖的多肽专门涵盖具有本文中所涵盖的救助car或可二聚救助受体的一个或多个氨基酸的缺失、添加和/或取代的序列。
如本文所使用,“经分离的肽”或“经分离的多肽”等是指从细胞环境和与细胞的其它组分的缔合体外分离和/或纯化肽或多肽分子,即,不与体内物质明显缔合。类似地,“经分离细胞”是指已从体内组织或器官获得并基本上不含胞外基质的细胞。
多肽包括“多肽变异体”。多肽变异体与天然存在的多肽的不同之处可在于一个或多个取代、缺失、添加和/或插入。这类变异体可天然存在或可例如通过修饰上文多肽序列中的一种或多种来合成地产生。举例来说,在特定实施例中,可能需要通过引入一个或多个取代、缺失、添加和/或插入多肽来改善多肽的结合亲和力和/或其它生物特性。在特定实施例中,多肽包括与本文中所涵盖的参考序列中的任一种具有至少约65%、66%、67%、68%、69%、70%、71%、72%、73%、74%、75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、86%、97%、98%或99%氨基酸一致性的多肽,通常其中变异体维持参考序列的至少一种生物活性。
多肽包括“多肽片段”。多肽片段是指多肽,其可为具有天然产生或以重组方式制得的多肽的氨基末端缺失、羧基末端缺失和/或内部缺失或取代的单体或多聚体。在某些实施例中,多肽片段可包含至少5到约500个氨基酸长的氨基酸链。应了解,在某些实施例中,片段长度为至少5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、55、60、65、70、75、80、85、90、95、100、110、150、200、250、300、350、400或450个氨基酸。特别有用的多肽片段包括官能性域,其包括抗原结合域或抗体片段。
多肽还可以与连接子或其它序列框内融合或结合以易于合成、纯化或鉴别多肽(例如聚his),或促进多肽与固体支撑物的结合。
如上文所述,多肽可以不同方式改变,包括氨基酸取代、缺失、截短和插入。用于这类操控的方法在所属领域中一般已知。举例来说,参考多肽的氨基酸序列变异体可以通过dna中的突变制备。突变诱发和核苷酸序列改变的方法在所属领域中众所周知。参看例如kunkel(1985,《美国国家科学院院刊(proc.natl.acad.sci.usa.)》82:488-492);kunkel等人(1987,《酶学方法(methodsinenzymol)》,154:367-382);美国专利第4,873,192号;watson,j.d.等人(《基因分子生物学(molecularbiologyofthegene)》,第四版,加利福尼亚州门洛帕克的本杰明-卡明斯公司(benjamin/cummings,menlopark,calif.),1987)以及其中所引用的参考文献。关于不影响所关注蛋白质的生物活性的适当氨基酸取代的指导可见于dayhoff等人,(1978)《蛋白序列和结构图集(atlasofproteinsequenceandstructure)》(《国家生物医学研究基础(natl.biomed.res.found.)》,华盛顿(washington,d.c.))的模型中。
在某些实施例中,多肽变异体包含一个或多个保守性取代。“保守性取代”为氨基酸经另一个具有类似特性的氨基酸取代,使得肽化学方法领域的技术人员将预期多肽的二级结构和亲水性质大体上不变。可对特定实施例中涵盖的多核苷酸和多肽的结构进行修饰且仍获得编码具有期望特征的变异体或衍生多肽的功能分子。当期望改变多肽的氨基酸序列以产生等效或甚至改善的变异体多肽时,所属领域的技术人员例如可改变例如根据表1的编码dna序列的密码子中的一种或多种。
表1-氨基酸密码子
可以使用所属领域中熟知的计算机程序,如dnastar、dnastrider、geneious、macvector或vectornti软件发现确定可以取代、嵌入或缺失而不消除生物活性的氨基酸残基的指导。优选地,本文中公开的蛋白变异体中的氨基酸变化是保守性氨基酸变化,即带相似电荷或不带电的氨基酸的取代。保守性氨基酸变化涉及其侧链相关的氨基酸家族中的一个的取代。天然存在的氨基酸一般分成四个家族:酸性氨基酸(天冬氨酸、谷氨酸)、碱性氨基酸(赖氨酸、精氨酸、组氨酸)、非极性氨基酸(丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、甲硫氨酸、色氨酸)和不带电极性氨基酸(甘氨酸、天冬酰胺、谷氨酰胺、半胱氨酸、丝氨酸、苏氨酸、酪氨酸)。苯丙氨酸、色氨酸和酪氨酸有时共同分类为芳香族氨基酸。在肽或蛋白质中,氨基酸的合适的保守性取代为所属领域的技术人员已知且一般在不改变所得分子的生物活性下制备。所属领域的技术人员认识到,一般来说,多肽的非必需区中的单氨基酸取代不显著改变生物活性(参见例如watson等人《基因分子生物学》,第4版,1987,thebenjamin/cummingspub.co.,第224页)。
在进行此类改变时,可以考虑氨基酸的亲水指数。所属领域中一般理解亲水性氨基酸指数在赋予蛋白质相互作用生物功能中的重要性(kyte和doolittle,1982,以引用的方式并本文中)。各氨基酸已基于其疏水性和电荷特征指定亲水指数(kyte和doolittle,1982)。这些值为:异亮氨酸(+4.5);缬氨酸(+4.2);亮氨酸(+3.8);苯丙氨酸(+2.8);半胱氨酸/半胱氨酸(+2.5);甲硫氨酸(+1.9);丙氨酸(+1.8);甘氨酸(-0.4);苏氨酸(-0.7);丝氨酸(-0.8);色氨酸(-0.9);酪氨酸(-1.3);脯氨酸(-1.6);组氨酸(-3.2);谷氨酸(-3.5);谷氨酰胺(-3.5);天冬氨酸(-3.5);天冬酰胺(-3.5);赖氨酸(-3.9);以及精氨酸(-4.5)。
所属领域中已知特定氨基酸可以经具有类似亲水指数或评分的其它氨基酸取代并且仍产生具有类似生物活性的蛋白质,即仍获得生物功能等效蛋白质。进行这类改变时,亲水指数在2之内的氨基酸取代是优选的,在1之内的那些尤其优选,并且在0.5之内的那些甚至更优选。所属领域中还应理解可以基于亲水性有效进行类似的氨基酸取代。
如美国专利第4,554,101号中所详述,已将以下亲水性值分配给氨基酸残基:精氨酸(+3.0);赖氨酸(+3.0);天冬氨酸(+3.01);谷氨酸(+3.01);丝氨酸(+0.3);天冬酰胺(+0.2);谷氨酰胺(+0.2);甘氨酸(0);苏氨酸(-0.4);脯氨酸(-0.51);丙氨酸(-0.5);组氨酸(-0.5);半胱氨酸(-1.0);甲硫氨酸(-1.3);缬氨酸(-1.5);亮氨酸(-1.8);异亮氨酸(-1.8);酪氨酸(-2.3);苯丙氨酸(-2.5);色氨酸(-3.4)。应理解,氨基酸可以是经具有类似亲水性值的另一个氨基酸取代并且仍获得生物等效蛋白质,并且尤其免疫等效蛋白质。在这类改变时,亲水性值在2之内的氨基酸取代是优选的,在1之内的那些尤其优选,并且在0.5之内的那些甚至更尤其优选。
如上文所概述,氨基酸取代可基于氨基酸侧链取代基的相对相似性,例如其疏水性、亲水性、电荷、大小等。
多肽变异体进一步包括糖基化形式、与其它分子的聚集共轭物和与不相关化学部分(例如聚乙二醇化分子)的共价共轭物。如所属领域中已知,共价变异体可以通过使官能团与氨基酸链或n或c末端残基处发现的基团连接。变异体还包括等位基因变异体、物种变异体和突变蛋白。不影响蛋白质的功能活性的区域的截短或缺失也是变异体。
在一个实施例中,在需要两种或更多种多肽的表达的情况下,编码所述多肽的多核苷酸序列可通过如本文中其它地方所论述的ires序列分离。在另一实施例中,两种或更多种多肽可表述为包含一个或多个自我裂解多肽序列的融合蛋白。
在特定实施例中涵盖的多肽包括融合多肽。在优选实施例中,提供融合多肽和编码融合多肽的多核苷酸,例如救助car或可二聚救助受体。融合多肽和融合蛋白是指具有至少两个、三个、四个、五个、六个、七个、八个、九个或十个或更多个多肽片段的多肽。融合多肽通常连接c端至n端,尽管其还可以连接c端至c端、n端至n端、或n端至c端。融合蛋白的多肽可以按任何次序或指定次序。融合多肽或融合蛋白还可以包括保守修饰变异体、多态变异体、等位基因、突变异体、子序列和种间同系物,只要保存融合多肽的所需转录活性即可。融合多肽可通过化学合成方法或通过两个部分之间的化学连接制得或一般可使用其它标准技术制备。包含融合多肽的经连接dna序列可操作地连接于如本文中其它地方所论述的合适的转录或翻译控制元件。
在一个实施例中,融合搭配物包含有助于表达蛋白质(表达增强剂)的产率高于天然重组蛋白的序列。可选择其它融合搭配物以便提高蛋白质的溶解度或使得蛋白质靶向所需胞内区室或促进融合蛋白传输穿过细胞膜。
融合多肽可进一步在本文所述的多肽域中的每一个之间包含多肽裂解信号。另外,可将多肽裂解位点置于任何连接肽序列中。示例性多肽裂解信号包括多肽裂解识别位点,如蛋白酶裂解位点、核酸酶裂解位点(例如罕见限制酶识别位点、自我裂解核酶识别位点)和自我裂解病毒寡肽(参见defelipe和ryan,2004.《交通(traffic)》,5(8);616-26)。
合适的蛋白酶裂解位点和自我裂解肽为熟练人员已知的(参见例如ryan等人,1997.《普通病毒学杂志(j.gener.virol.)》78,699-722;scymczak等人(2004)《自然生物技术(naturebiotech.)》5,589-594)。示例性蛋白酶裂解位点包括但不限于马铃薯y病毒属nia蛋白酶(例如烟草蚀刻病毒蛋白酶)、马铃薯y病毒属hc蛋白酶、马铃薯y病毒属p1(p35)蛋白酶、byo病毒nia蛋白酶、byo病毒rna-2-经编码蛋白酶、口疮病毒属l蛋白酶、肠病毒2a蛋白酶、鼻病毒2a蛋白酶、细小核糖核酸3c蛋白酶、豇豆花叶病毒组24k蛋白酶、线虫传多面体病毒24k蛋白酶、rtsv(水稻东格鲁球状病毒)3c样蛋白酶、pyvf(欧防风黄点病毒)3c样蛋白酶、肝素、凝血酶、因子xa和肠激酶的裂解位点。归因于其较高的裂解严格度,tev(烟草蚀刻病毒)蛋白酶裂解位点为优选的,在一个实施例中,例如exxyxq(g/s)(seqidno:18),例如enlyfqg(seqidno:19)和enlyfqs(seqidno:20),其中x表示任何氨基酸(通过tev裂解发生在q与g或q与s之间)。
在一特定实施例中,自我裂解肽包括从马铃薯y病毒属和心病毒属2a肽、口蹄疫病毒(foot-and-mouthdiseasevirus;fmdv)、马鼻炎a病毒、明脉扁刺蛾β四体病毒(thoseaasignavirus)和猪捷申病毒获得的那些多肽序列。
在某些实施例中,自我裂解多肽位点包含2a或2a样位点、序列或域(donnelly等人,2001.《普通病毒学杂志》82:1027-1041)。示例性2a位点显示于表2中。
表2:
在优选实施例中,多肽包含救助car多肽或可二聚救助受体多肽。
g.多核苷酸
在特定实施例中,提供编码一种或多种多肽的多核苷酸。如本文所用,术语“多核苷酸”或“核酸”是指信使rna(mrna)、rna、基因组rna(grna)、正链rna(rna(+))、负链rna(rna(-))、基因组dna(gdna)、互补dna(cdna)或重组dna。多核苷酸包括单链和双链多核苷酸。在特定实施例中,多核苷酸包括多核苷酸或变异体,其与本文中所涵盖的参考序列中的任一种具有至少约50%、55%、60%、65%、66%、67%、68%、69%、70%、71%、72%、73%、74%、75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、86%、97%、98%或99%序列一致性。在各种说明性实施例中,多核苷酸包括表达载体、病毒载体和转移质粒,以及组合物和包含其的细胞。
在特定实施例中,提供多核苷酸,其编码多肽的至少约5、10、25、50、100、150、200、250、300、350、400、500、1000、1250、1500、1750或2000个或更多个连续的氨基酸残基,以及全部中间长度。容易理解,在此情形下,“中间长度”意指所引述值之间的任何长度,例如6、7、8、9等,101、102、103等,151、152、153等,201、202、203等。
如本文中所用,术语“多核苷酸变异体”和“变异体”等是指与参考多核苷酸序列呈现相当大的序列一致性的多核苷酸或在下文所定义的严格条件下与参考序列杂交的多核苷酸。这些术语包括相较于参考多核苷酸来说一个或多个核苷酸添加或缺失或经不同核苷酸置换的多核苷酸。在这点上,在所属领域中充分理解,可以对参考多核苷酸进行包括突变、添加、缺失和取代的某些改变,由此改变的多核苷酸保留参考多核苷酸的生物功能或活性。
如本文所用,叙述“序列一致性”或例如包含“与……50%一致的序列”是指比较窗口上逐核苷酸计或逐氨基酸计的序列相同程度。因此,“序列一致性的百分比”可通过以下计算:在比较窗口上比较两个最佳对比的序列,测定在两个序列中出现相同核酸碱基(例如a、t、c、g、i)或相同氨基酸残基(例如ala、pro、ser、thr、gly、val、leu、ile、phe、tyr、trp、lys、arg、his、asp、glu、asn、gln、cys和met)的位置的数目以获得相匹配位置的数目,以相匹配位置数目除以比较窗口中的位置总数(即窗口大小),并使结果乘以100以得到序列一致性的百分比。包括与本文所述的参考序列中的任一种具有至少约50%、55%、60%、65%、66%、67%、68%、69%、70%、71%、72%、73%、74%、75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、86%、97%、98%或99%序列一致性的核苷酸和多肽,通常其中多肽变异体维持参考多肽的至少一种生物活性。
用以描述两个或更多个多核苷酸或多肽之间的序列关系的术语包括“参考序列”、“比较窗口”、“序列一致性”、“序列一致性百分比”和“实质一致性”。“参考序列”的长度为至少12个、但常是15到18个、并且通常是至少25个单体单元,包括核苷酸和氨基酸残基。因为两个多核苷酸可各自包含(1)两个多核苷酸之间类似的序列(即完全多核苷酸序列的仅一部分),和(2)在两个多核苷酸之间相异的序列,两个(或更多个)多核苷酸之间的序列比较通常通过在“比较窗口”上比较两个多核苷酸的序列以鉴别和比较局部区域的序列相似性来进行。“比较窗口”是指至少6个、通常约50到约100个、更通常约100到约150个连续位置的概念性区段,其中在将两个序列最优比对后,将序列与具有相同数目的连续位置的参考序列比较。比较窗口可包含相比于参考序列(其不包含添加或缺失)约20%或更少的添加或缺失(即缺口)以实现两个序列的最佳比对。用于比对比较窗口的序列最佳比对可以通过计算机化执行算法(美国威斯康星州的威斯康星州遗传学软件包7.0版本,遗传学计算机组,575科学驱动麦迪逊(wisconsingeneticssoftwarepackagerelease7.0,geneticscomputergroup,575sciencedrivemadison,wi,usa)中的gap、bestfit、fasta和tfasta)或通过多种选择方法中的任一个产生的检查和最佳比对(即在比较窗口上导致最高同源性百分比)来进行。还可以参考如例如altschul等人,1997,《核酸研究(nucl.acidsres.)》25:3389所公开的blast程序家族。序列分析的详细论述可以见于ausubel等人,《最新分子生物学实验方法汇编》,约翰·威利父子公司,1994-1998,第15章的19.3单元中。
如本文所用,“分离的多核苷酸”是指已经从在天然存在的状态下侧接其的序列纯化的多核苷酸,例如从通常与片段相邻的序列移出的dna片段。“分离的多核苷酸”还指互补dna(cdna)、重组dna或在自然界中不存在并且通过人力制得的其它多核苷酸。
描述多核苷酸的定向的术语包括:5'(通常是多核苷酸的具有游离磷酸酯基的末端)和3'(通常是多核苷酸的具有游离羟基(oh)的末端)。多核苷酸序列可以按5'到3'取向或3'到5'取向标注。对于dna和mrna,5'到3'链被命名为“有义”、“正”或“编码”链,因为其序列与前信使(前mrna)的序列相同[除了rna中是尿嘧啶(u),而非dna中是胸嘧啶(t)]。对于dna和mrna,作为由rna聚合酶转录的链的互补3'到5'链被命名为“模板”、“反义”、“负”或“非编码”链。如本文所用,术语“反向定向”是指以3'到5'定向书写的5'到3'序列或以5'到3'定向书写的3'到5'序列。
术语“互补的”和“互补性”是指通过碱基配对规则相关的多核苷酸(即,核苷酸序列)。举例来说,dna序列5'agtcatg3'的互补链是3'tcagtac5'。后一序列通常写成反向互补序列,5'端在左并且3'端在右,5'catgact3'。与其反向互补序列相等的序列被称为回文序列。互补性可以是“部分的”,其中仅一些核酸的碱基根据碱基配对规则匹配。或,核酸之间可以存在“完全”或“全部”互补性。
此外,所属领域的一般技术人员应了解,如本文所述,由于遗传密码的简并,存在多种编码多肽或其变异体的片段的核苷酸序列。这些多核苷酸中的一些与任何天然基因的核苷酸序列携有最小同源性。尽管如此,在特定实施例中专门涵盖归因于密码子使用差异而变化的多核苷酸,例如针对人类和/或灵长类动物密码子选择而优化的多核苷酸。在特定实施例中,多核苷酸是针对表达和/或稳定性优化的密码子。此外,还可以使用包含本文所提供的多核苷酸序列的基因的等位基因。等位基因是由于核苷酸的一个或多个突变(例如缺失、添加和/或取代)而改变的内源基因。
如本文所用,术语“核酸盒”是指载体内的可以表达rna并且随后表达蛋白质的基因序列。核酸盒含有所关注基因。核酸盒位置上并且依序地定向在载体内,使得盒中的核酸可以转录成rna,并且当需要时翻译成蛋白质或多肽,经历转化的细胞的活性所需要的适当翻译后修饰,并且通过靶向适当胞内区室或分泌到胞外区室中而易位到适当区室以获得生物活性。优选地,盒使其3'和5'端适合于简便插入到载体中,例如其在每个端具有限制性核酸内切酶位点。
在特定实施例中,多核苷酸包括至少一种所关注多核苷酸。如本文所用,术语“所关注多核苷酸”是指插入到需要表达的表达载体中,编码多肽(即所关注多肽)的多核苷酸。载体可以包含1、2、3、4、5、6、7、8、9或10种所关注多核苷酸。在某些实施例中,所关注多核苷酸编码在治疗或预防疾病或病症方面提供治疗效果的多肽。所关注多核苷酸和由其编码的多肽包括编码野生型多肽的多核苷酸以及其功能变异体和片段两者。在特定实施例中,功能变异体与相应野生型参考多核苷酸或多肽序列具有至少80%、至少90%、至少95%或至少99%一致性。在某些实施例中,功能变异体或片段具有相应野生型多肽的至少50%、至少60%、至少70%、至少80%或至少90%的生物活性。
在一个实施例中,所关注多核苷酸为转录mirna、sirna或shrna、核酶或其它抑制性rna的模板。在不同其它实施例中,多核苷酸包含编码救助car的所关注多核苷酸和一种或多种额外的所关注多核苷酸,其包括但不限于抑制性核酸序列,所述核酸序列包括但不限于:sirna、mirna、shrna和核酶。
如本文所用,术语“sirna”或“短干扰rna”是指介导动物中的序列特异性转录后基因沉默、翻译抑制、转录抑制或表观遗传rnai的过程的短多核苷酸序列(zamore等人,2000,《细胞(cell)》,101,25-33;fire等人,1998,《自然》,391,806;hamilton等人,1999,《科学》,286,950-951;lin等人,1999,《自然》,402,128-129;sharp,1999,《基因与发育(genes&dev.)》,13,139-141;和strauss,1999,《科学》,286,886)。在某些实施例中,sirna包含具有相同数目核苷的第一链和第二链;然而,第一与第二链偏移,使得第一和第二链上的两个末端核苷与互补链上的残基不配对。在某些情况下,不配对的两个核苷是胸苷残基。sirna应包括与靶基因具有充足同源性的区并且就核苷酸来说具有充足长度,使得sirna或其片段可以介导靶基因的下调。因此,sirna包括与靶rna至少部分互补的区。sirna与标靶之间不必存在完美互补性,但对应性必须足以使得sirna或其裂解产物能够导引序列特异性沉默,例如通过靶rna的rnai裂解。与标靶链的互补性或同源性程度对于反义链最为关键。虽然通常需要尤其反义链中的完美互补性,但一些实施例相对于靶rna包括一个或多个、但优选10、8、6、5、4、3、2个或更少的错配。错配最被容许在末端区中,并且如果存在的话,优选在一个或多个末端区中,例如在5'和/或3'末端的6、5、4或3个核苷酸内。有义链仅需要与反义链足够互补以维持分子的整体双链特征。
另外,sirna可以经修饰或包括核苷类似物。sirna的单链区可以经修饰或包括核苷类似物,例如发夹结构的未配对区(例如连接两个互补区的区)可以具有修饰或核苷类似物。用以例如针对核酸外切酶稳定sirna的一个或多个3'或5'末端或促进反义sirna剂进入risc中的修饰也是有用的。修饰可以包括c3(或c6、c7、c12)氨基连接子、硫醇连接子、羧基连接子、非核苷酸间隔子(c3、c6、c9、c12、无碱基、三乙二醇、六乙二醇)、以氨基磷酸酯形成出现并且具有另一dmt保护的羟基使得在rna合成期间可进行多个偶合的特殊生物素或荧光素试剂。每个sirna链的长度可以等于或少于30、25、24、23、22、21或20个核苷酸。链的长度优选是至少19个核苷酸。举例来说,每个链的长度可以在21与25个核苷酸之间。优选的sirna具有17、18、19、29、21、22、23、24或25个核苷酸对的双螺旋体区,和一个或多个2-3个核苷酸的突出端、优选一个或两个2-3个核苷酸的3'突出端。
如本文所用,术语“mirna”或“微rna”是指通常从称为前-mirna的约70个核苷酸折回rna前驱物结构切下的20-22个核苷酸的小非编码rna。mirna取决于mirna与标靶之间的互补性程度以两种方式之一负调节其标靶。首先,以完美或几乎完美的互补性结合到蛋白质编码mrna序列的mirna诱导rna介导的干扰(rnai)途径。通过结合到其mrna标靶的3'非翻译区(utr)内的不完美互补位点来发挥其调节效果的mirna通过与用于rnai途径者类似或可能相同的risc复合物明显在翻译水平下抑制转录后靶基因表达。与翻译控制一致,使用此机制的mirna降低其靶基因的蛋白质水平,但这些基因的mrna水平仅最低限度地受影响。mirna涵盖天然存在的mirna以及可以特异性靶向任何mrna序列的人工经设计的mirna两者。举例来说,在一个实施例中,熟练技术人员可以设计表达为人类mirna(例如mir-30或mir-21)初级转录物的短发夹rna构建体。此设计向发夹构建体增添了drosha加工位点并且据显示可极大地增加基因敲落效率(pusch等人,2004)。发夹茎由22nt的dsrna(例如与所要标靶具有完美互补性的反义链)和来自人类mir的15-19nt的环组成。当与不具有微rna的常规shrna设计相比时,在发夹的任一侧或两侧上添加mir环和mir30侧接序列导致所表达发夹的drosha和dicer加工有大于10倍的增加。增加的drosha和dicer加工翻译成更大的sirna/mirna产生和所表达发夹的更大效力。
如本文所用,术语“shrna”或“短发夹rna”是指通过单一自互补rna链形成的双链结构。含有与靶基因的编码或非编码序列的一部分相同的核苷酸序列的shrna构建体优选用于抑制。相对于靶序列具有插入、缺失和单点突变的rna序列也被发现可有效用于抑制。抑制性rna与靶基因部分之间的大于90%序列一致性或甚至100%序列一致性是优选的。在某些优选实施例中,shrna的双螺旋体形成部分的长度为至少20、21或22个核苷酸长,例如大小对应于通过dicer依赖性裂解制得的rna产物。在某些实施例中,shrna构建体的长度是至少25、50、100、200、300或400个碱基。在某些实施例中,shrna构建体的长度是400-800个碱基。shrna构建体充分容许环序列和环大小的变化。
如本文所用,术语“核酶”是指能够使靶mrna位点特异性裂解的催化活性rna分子。已经描述了若干亚型,例如锤头和发夹核酶。核酶催化活性和稳定性可以通过在非催化碱基处用脱氧核糖核苷酸取代核糖核苷酸而改进。虽然在位点特异性识别序列处使mrna裂解的核酶可以用以破坏特定mrna,但使用锤头核酶是优选的。锤头核酶在由与靶mrna形成互补碱基对的侧接区指定的位置处使mrna裂解。唯一要求是靶mrna具有两种碱基的以下序列:5′-ug-3′。锤头核酶的构建和产生在所属领域中是熟知的。
如本文别处所描述,包含sirna、mirna、shrna或核酶的所关注多核苷酸的优选传递方法包含一个或多个调节序列,例如强组成型poliii,例如人类u6snrna启动子、小鼠u6snrna启动子、人类和小鼠h1rna启动子以及人类trna-val启动子;或强组成型polii启动子。
如本文其它地方所公开或如所属领域中已知,本文中涵盖的聚核苷酸(无关于编码序列本身的长度)可与其它dna序列组合,所述序列如启动子和/或增强子、非翻译区(utr)、信号序列、kozak序列、聚腺苷酸化信号、其它限制酶位点、多克隆位点、内部核糖体进入位点(ires)、重组酶识别位点(例如loxp、frt和att位点)、终止密码子、转录终止信号和编码自我裂解多肽的多核苷酸、抗原决定基标签,使得其总长度可以显著变化。因此设想可以利用几乎任何长度的多核苷酸片段,总长度优选受预期重组dna方案的制备和使用便利性限制。
多核苷酸可以使用所属领域中已知并且可用的多种公认技术中的任一种制备、操纵、表达和/或递送。为了表达所需多肽,编码多肽的核苷酸序列可插入到适当载体中。
载体的说明性实例包括但不限于质粒、自主复制序列和转座因子,例如sleepingbeauty、piggybac。
载体的其它说明性实例包括但不限于质粒;噬菌粒;粘粒;人工染色体,例如酵母人工染色体(yac)、细菌人工染色体(bac)或p1衍生的人工染色体(pac);噬菌体,例如λ噬菌体或m13噬菌体;和动物病毒。
适用作载体的病毒的说明性实例包括但不限于逆转录病毒(包括慢病毒)、腺病毒、腺相关病毒、疱疹病毒(例如单纯疱疹病毒)、痘病毒、杆状病毒、乳头瘤病毒和乳多泡病毒(例如sv40)。
表达载体的说明性实例包括但不限于用于在哺乳动物细胞中表达的pclneo载体(普洛麦格);用于慢病毒介导的基因转移和在哺乳动物细胞中表达的plenti4/v5-desttm、plenti6/v5-desttm和plenti6.2/v5-gw/lacz(英杰公司)。在特定实施例中,本文所公开的多肽的编码序列可接合到用于表达哺乳动物细胞中的多肽的此类表达载体中。
在特定实施例中,载体为游离型载体或维持在染色体外的载体。如本文所用,术语“游离型”是指载体能够复制而不整合到宿主的染色体dna中并且不由分裂宿主细胞逐渐丧失,还意指所述载体在染色体外或游离地复制。载体经工程改造以庇护编码dna复制来源或来自α、β或γ疱疹病毒、腺病毒、sv40、牛乳头状瘤病毒或酵母菌的“ori”的序列。通常,宿主细胞包含活化复制的病毒复制反式活化蛋白。α疱疹病毒具有相对较短的繁殖周期、可变的宿主范围,有效摧毁感染细胞并建立主要在感觉性神经节中的潜伏感染。α疱疹病毒的说明性实例包括hsv1、hsv2和vzv。β疱疹病毒具有较长的繁殖周期和限定的宿主范围。感染细胞常常增大。潜伏期可维持在血液、肾、分泌腺和其它组织的白细胞中。β疱疹病毒的说明性实例包括cmv、hhv-6和hhv-7。γ-疱疹病毒对t或b淋巴细胞具有特异性,且潜伏期常常在淋巴组织中证实。γ疱疹病毒的说明性实例包括ebv和hhv-8。
存在于表达载体中的“表达控制序列”、“控制元件”或“调节序列”为载体的那些非翻译区-复制起点、选择卡匣、启动子、增强子、翻译起始信号(shinedalgarno序列或kozak序列)、内含子、聚腺苷酸化序列、5'和3'非翻译区-其与宿主细胞蛋白相互作用以执行转录与翻译。所述元件可以在其强度和特异性方面变化。取决于所利用的载体系统和宿主,可使用多种适合的转录与翻译元件,包括遍在启动子和诱导型启动子。
在特定实施例中,多核苷酸为包括但不限于表达载体和病毒载体的载体,且包括外源、内源或异源控制序列,例如启动子和/或增强子。“内源控制序列”是天然地与基因组中的既定基因连接的控制序列。“外源控制序列”是借助于遗传操纵(即,分子生物技术)与基因并接定位使得所述基因的转录通过所连接的增强子/启动子导引的控制序列。“异源控制序列”是来自与所遗传操纵的细胞不同的物种的外源序列。
如本文所用,术语“启动子”是指rna聚合酶所结合到的多核苷酸(dna或rna)的识别位点。rna聚合酶起始并且转录可操作地连接到启动子的多核苷酸。在特定实施例中,在哺乳动物细胞中可操作的启动子包含位于转录起始位点上游约25到30个碱基处的富at区,和/或见于转录起始上游70到80个碱基处的另一序列,n可以是任何核苷酸的cncaat区。
术语“增强子”是指含有能够提供增强的转录的序列并且在一些情况下可以独立于其相对于另一个控制序列的定向起作用的一段dna。增强子可以与启动子和/或其它增强子元件协作地或叠加地起作用。术语“启动子/增强子”是指含有能够提供启动子和增强子功能两者的序列的一段dna。
术语“可操作地连接”是指所描述的组分处于允许其以其预期方式起作用的关系的并接。在一个实施例中,所述术语是指核酸表达控制序列(例如启动子和/或增强子)与第二多核苷酸序列(例如所关注多核苷酸)之间的功能性连接,其中表达控制序列导引对应于第二序列的核酸的转录。
如本文所用,术语“组成型表达控制序列”是指不断地或连续地引起可操作地连接的序列转录的启动子、增强子或启动子/增强子。组成型表达控制序列可以是允许在多种细胞和组织类型中表达的“遍在”启动子、增强子或启动子/增强子,或允许分别在多种限定细胞和组织类型中表达的“细胞特异性”、“细胞类型特异性”、“细胞谱系特异性”或“组织特异性”启动子、增强子或启动子/增强子。
适用特定实施例中的说明性遍在表达控制序列包括但不限于巨细胞病毒(cmv)立即早期启动子、病毒猿猴病毒40(sv40)(例如早期或晚期)、莫洛尼鼠白血病病毒(moloneymurineleukemiavirus,momlv)ltr启动子、劳斯肉瘤病毒(rsv)ltr、单纯疱疹病毒(hsv)(胸苷激酶)启动子、来自牛痘病毒的h5、p7.5和p11启动子、延伸因子1-α(ef1a)启动子、早期生长应答1(egr1)、铁蛋白h(ferh)、铁蛋白l(ferl)、甘油醛3-磷酸脱氢酶(gapdh)、真核翻译起始因子4a1(eif4a1)、热休克70kda蛋白5(hspa5)、热休克蛋白90kdaβ成员1(hsp90b1)、热休克蛋白70kda(hsp70)、β-驱动蛋白(β-kin)、人类rosa26基因座(irions等人,《自然·生物技术》25,1477-1482(2007))、泛素c启动子(ubc)、磷酸甘油酸激酶-1(pgk)启动子、巨细胞病毒增强子/鸡β-肌动蛋白(cag)启动子、β-肌动蛋白启动子和骨髓增生性肉瘤病毒增强子,阴性对照区缺失的、dl587rev引物结合位点取代的(mnd)启动子(challita等人,《病毒学杂志(jvirol.)》69(2):748-55(1995))。
在一个实施例中,载体包含mnd启动子。
在一个实施例中,载体包含ef1a启动子,所述ef1a启动子包含人类ef1a基因的第一内含子。
在一个实施例中,载体包含缺乏人类ef1a基因的第一内含子的ef1a启动子。
在一个特定实施例中,可能期望使用细胞、细胞类型、细胞谱系或组织特异性表达控制序列来实现所期望的多核苷酸序列的细胞类型特异性、谱系特异性或组织特异性表达(例如,仅在细胞类型、细胞谱系或组织的子集中或在特定发展阶段期间表达编码多肽的特定核酸)。
在一特定实施例中,可能需要表达多核苷酸、t细胞特异性启动子。
如本文所用,“条件表达”可以指任何类型的条件表达,包括但不限于诱导型表达;阻抑型表达;在具有特定生理、生物或疾病状态的细胞或组织中的表达;等。此定义不打算排除细胞类型或组织特异性表达。某些实施例提供所关注多核苷酸的条件表达,例如通过使细胞、组织、生物体等经历导致多核苷酸表达或导致由所关注多核苷酸编码的多核苷酸的表达增加或减弱的处理或条件来对控制进行表达。
诱导型启动子/系统的说明性实例包括但不限于类固醇诱导型启动子,例如用于编码糖皮质激素或雌激素受体的基因的启动子(通过用相应激素处理而诱导);金属硫蛋白启动子(通过用各种重金属处理而诱导);mx-1启动子(通过干扰素诱导);“geneswitch”米非司酮可调节系统(sirin等人,2003,《基因(gene)》,323:67);二甲氨基二硫代甲酸铜(cumate)诱导型基因开关(wo2002/088346);四环素依赖性调节系统等。
诱导剂包括但不限于糖皮质激素、雌激素、米非司酮(ru486)、金属、干扰素、小分子、二甲氨基二硫代甲酸铜(cumate)、四环素、多西环素和其变异体。
条件表达还可以通过使用位点特异性dna重组酶实现。根据某些实施例,载体包含用于由位点特异性重组酶介导的重组的至少一个(通常两个)位点。如本文所用,术语“重组酶”或“位点特异性重组酶”包括参与涉及一个或多个(例如二、三、四、五、七、十、十二、十五、二十、三十、五十个等)重组位点的重组反应的切除型或整合型蛋白、酶、辅因子或相关蛋白,其可以是野生型蛋白(参看landy,《生物技术新见(currentopinioninbiotechnology)》3:699-707(1993))或其突变体、衍生物(例如含有重组蛋白序列或其片段的融合蛋白)、片段和变异体。适用于特定实施例的重组酶的说明性实例包括但不限于:cre、int、ihf、xis、flp、fis、hin、gin、φc31、cin、tn3解离酶、tndx、xerc、xerd、tnpx、hjc、gin、spcce1和para。
多核苷酸可以包含用于多种位点特异性重组酶中的任何一种的一个或多个重组位点。应理解,除了例如逆转录病毒载体或慢病毒载体的载体的整合所需的任何位点之外,还需要用于位点特异性重组酶的靶位点。如本文所用,术语“重组序列”、“重组位点”或“位点特异性重组位点”是指重组酶所识别并且结合的特定核酸序列。
举例来说,cre重组酶的一个重组位点是loxp,其是34个碱基对的序列,包含侧接8个碱基对的核心序列的两个13个碱基对的反向重复序列(充当重组酶结合位点)(参看sauerb.,《生物技术新见(currentopinioninbiotechnology)》5:521-527(1994)的图1)。其它示例性loxp位点包括但不限于:lox511(hoess等人,1996;bethke和sauer,1997)、lox5171(lee和saito,1998)、lox2272(lee和saito,1998)、m2(langer等人,2002)、lox71(albert等人,1995)以及lox66(albert等人,1995)。
适合flp重组酶的识别位点包括但不限于:frt(mcleod等人,1996)、f1、f2、f3(schlake和bode,1994)、f4、f5(schlake和bode,1994)、frt(le)(senecoff等人,1988)、frt(re)(senecoff等人,1988)。
识别序列的其它实例是attb、attp、attl和attr序列,其由重组酶λ整合酶(例如
如本文所用,“内部核糖体进入位点”或“ires”是指促进直接内部核糖体进入到顺反子(蛋白质编码区)的起始密码子(例如atg),由此导致基因的帽非依赖性翻译的元件。参看例如jackson等人,1990.《生化科学趋势(trendsbiochemsci)》15(12):477-83,和jackson和kaminski.1995.rna1(10):985-1000。所属领域的技术人员一般采用的ires的实例包括美国专利第6,692,736号中所描述的那些。所属领域中已知的“ires”的其它实例包括但不限于获自小核糖核酸病毒的ires(jackson等人,1990)和获自病毒或细胞mrna源,例如免疫球蛋白重链结合蛋白(bip)、血管内皮生长因子(vegf)的ires(huez等人1998.《分子与细胞生物学(mol.cell.biol.)》18(11):6178-6190)、成纤维细胞生长因子2(fgf-2)和胰岛素样生长因子(igfii)、翻译起始因子eif4g和酵母菌转录因子tfiid和hap4、可购自诺杰公司的脑心肌炎病毒(emcv)(duke等人,1992.《病毒学杂志(j.virol)》66(3):1602-9)和vegfires(huez等人,1998.《分子细胞生物学(molcellbiol)》18(11):6178-90)。ires也已在小核糖核酸病毒科、二顺反子病毒科和黄病毒科物种的病毒基因组中以及在hcv、弗云德鼠白血病病毒(frmlv)和莫洛尼鼠白血病病毒(momlv)中报道。
在一个实施例中,本文中所涵盖的用于多核苷酸的ires为emcvires。
在特定实施例中,多核苷酸包含具有共有kozak序列且编码所需多肽的多核苷酸。如本文所用,术语“kozak序列”是指极大地促进mrna与核糖体的小亚单位的初始结合并且增加翻译的短核苷酸序列。共有kozak序列是(gcc)rccatgg(seqidno:43),其中r是嘌呤(a或g)(kozak,1986.《细胞(cell)》.44(2):283-92,和kozak,1987.《核酸研究》15(20):8125-48)。
导引异源核酸转录物的高效终止和聚腺苷酸化的元件增加了异源基因表达。转录终止信号通常见于聚腺苷酸化信号的下游。在特定实施例中,载体包含编码待表达的多肽的多核苷酸的聚腺苷酸化序列3′。如本文所用,术语“polya位点”或“polya序列”表示通过rna聚合酶ii导引初生rna转录物的终止和聚腺苷酸化两者的dna序列。聚腺苷酸化序列可以通过添加polya尾到编码序列的3′端而提升mrna稳定性,并且因此促进翻译效率增加。重组转录物的高效聚腺苷酸化是合乎需要的,因为不具有polya尾的转录物不稳定并且快速降解。可以用于载体中的polya信号的说明性实例包括理想polya序列(例如aataaa、attaaa、agtaaa)、牛生长激素polya序列(bghpa)、兔β-珠蛋白polya序列(rβgpa)或所属领域中已知的另一适合异源或内源polya序列。
在一些实施例中,多核苷酸或具有所述多核苷酸的细胞利用自杀基因(包括诱导型自杀基因)来降低直接毒性和/或不受控增殖的风险。在具体实施例中,自杀基因对具有所述多核苷酸或细胞的宿主不具有免疫原性。可以使用的自杀基因的某一实例是半胱天冬酶-9或半胱天冬酶-8或胞嘧啶脱氨酶。半胱天冬酶-9可以使用特定化学二聚诱导剂(cid)活化。
在某些实施例中,多核苷酸包含导致免疫效应细胞(例如t细胞)容易发生体内阴性选择的基因片段。“阴性选择”意指,输注的细胞可以由于个体的体内条件的变化而消除。阴性可选表型可以由赋予对所施用试剂(例如化合物)的敏感性的基因的插入产生。阴性可选基因在所属领域中是已知的并且尤其包括以下:赋予更昔洛韦(ganciclovir)敏感性的单纯疱疹病毒i型胸苷激酶(hsv-itk)基因(wigler等人,《细胞》11:223,1977);细胞次黄嘌呤磷酸核糖基转移酶(hprt)基因、细胞腺嘌呤磷酸核糖转移酶(aprt)基因和细菌胞嘧啶脱氨酶(mullen等人,《美国国家科学院院刊》89:33(1992))。
在一些实施例中,经基因修饰的免疫效应细胞(例如t细胞)包含进一步包含实现了阴性可选表型的细胞的体外选择的阳性标记的多核苷酸。阳性可选标记可以是在引入到宿主细胞中后表达显性表型(允许携带所述基因的细胞的阳性选择)的基因。此类型的基因在所属领域中是已知的并且尤其包括:赋予对潮霉素b的抗性的潮霉素-b磷酸转移酶基因(hph);编码对抗生素g418的抗性的来自tn5的氨基糖苷磷酸转移酶基因(neo或aph);二氢叶酸还原酶(dhfr)基因;腺苷脱氨酶基因(ada);和多药物抗性(mdr)基因。
在一个实施例中,阳性可选标记和阴性可选元件经连接,以使得阴性可选元件的丧失必须还伴有阳性可选标记的丧失。在一特定实施例中,阳性和阴性可选标记经融合,以使得一者的丧失强制性地导致另一者的丧失。以表达产物形式产生赋予上文所述的所要阳性和阴性选择特征两者的多肽的融合多核苷酸的一实例是潮霉素磷酸转移酶胸苷激酶融合基因(hytk)。此基因的表达产生了赋予潮霉素b抗性用于体外阳性选择和更昔洛韦敏感性用于体内阴性选择的多肽。还参看s.d.lupton的pctus91/08442和pct/us94/05601的公开,其描述了由融合显性阳性可选标记与阴性可选标记而衍生的双功能可选融合基因的用途。
优选的阳性可选标记衍生自选自由以下组成的组的基因:hph、nco和gpt,并且优选的阴性可选标记衍生自选自由以下组成的组的基因:胞嘧啶脱氨酶、hsv-itk、vzvtk、hprt、aprt和gpt。在特定实施例中涵盖的示例性双官能可选融合基因包括但不限于其中阳性可选标记衍生自hph或neo,且阴性可选标记衍生自胞嘧啶脱氨酶或tk基因或可选标记的基因。
在特定实施例中,可通过非病毒和病毒方法两者将编码一种或多种救助car、可二聚救助受体、治疗多肽或融合多肽的多核苷酸引入免疫效应细胞(例如t细胞)中。在特定实施例中,可通过相同方法或通过不同方法,和/或通过相同载体或通过不同载体递送一种或多种多核苷酸。
术语“载体”在本文中用以指能够转移或输送另一个核酸分子的核酸分子。转移后的核酸通常连接到载体核酸分子,例如插入载体核酸分子中。载体可以包括在细胞中导引自主复制的序列,或可以包括足以允许整合到宿主细胞dna中的序列。在特定实施例中,非病毒载体用于将本文中所涵盖的一种或多种多核苷酸递送到t细胞。
非病毒载体的说明性实例包括但不限于质粒(例如dna质粒或rna质粒)、转座子、粘粒、细菌性人工染色体和病毒载体。
在特定实施例中涵盖的多核苷酸的非病毒递送的说明性方法包括但不限于:电穿孔、声致穿孔、脂质体转染、微注射、基因枪(biolistics)、病毒颗粒、脂质体、免疫脂质体、纳米粒子、聚阳离子或脂质:核酸共轭物、裸dna、人工病毒粒子、deae-右旋糖苷介导的转移、基因枪(genegun)和热休克。
在特定实施例中涵盖的适用于特定实施例的多核苷酸递送系统的说明性实例包括但不限于由amaxabiosystems、maxcyte公司、btxmoleculardeliverysystems和copernicustherapeutics公司提供的那些。脂质体转染剂是商业上出售的(例如transfectamtm和lipofectintm)。已在文献中描述适用于多核苷酸的高效受体-识别脂质体转染的阳离子和中性脂质。参见例如liu等人(2003)《基因疗法(genetherapy)》.10:180-187;和balazs等人(2011)《药物递送杂志(journalofdrugdelivery)》.2011:1-12。抗体靶向的递送、细菌衍生的递送、基于非生命纳米单元的递送也涵盖在特定实施例中。
包含特定实施例中涵盖的多核苷酸的病毒载体可以通过向个体患者施用,通常通过如下所述的全身施用(例如静脉内、腹膜内、肌肉内、皮下或颅内输液)或局部应用来体内递送。或者,可将载体递送到离体细胞,例如从个体患者移出的细胞(例如流动外周血液、淋巴细胞、骨髓穿刺液、组织活检等)或全适供血者造血干细胞,之后将所述细胞再植入患者中。
在一个实施例中,包含本文中所涵盖的多核苷酸的病毒载体直接施用到生物体以用于体内细胞转导。或者,可以施用裸dna。施用是通过通常用于将分子引入与血液或组织细胞最终接触的途径中的任一种,其包括但不限于注射、输液、局部应用和电穿孔。施用这类核酸的合适方法可以获得且为所属领域的技术人员熟知,并且虽然超过一个途径可以用于施用特定组合物,但特定途径常常可以提供比另一途径更直接且更有效的反应。
特定实施例中所涵盖的适用于特定实施例的病毒载体系统的说明性实例包括但不限于腺相关病毒(adeno-associatedvirus;aav)、逆转录病毒、单纯疱疹病毒、腺病毒、牛痘病毒载体以用于基因转移。
在各种实施例中,通过用重组腺相关病毒(raav)转导细胞来将一种或多种多核苷酸引入免疫效应细胞(例如t细胞)中,所述重组腺相关病毒(raav)转导细胞包含一种或多种多核苷酸。
aav为小(约26nm)复制缺陷型,主要为游离型无包膜病毒。aav可以感染分裂和非分裂细胞两者且可将其基因组合并到宿主细胞的基因组中。重组aav(raav)通常至少由转基因和其调节序列,以及5'和3'aav反向末端重复(itr)构成。itr序列长度为约145bp。在特定实施例中,raav包含itr和从aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9或aav10分离的衣壳序列。
在一些实施例中,使用嵌合raav,从一种aav血清型分离itr序列且从不同aav血清型分离衣壳序列。举例来说,具有衍生自aav2的itr序列和衍生自aav6的衣壳序列的raav称为aav2/aav6。在特定实施例中,raav载体可包含来自aav2的itr,和来自aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9或aav10中的任一种的衣壳蛋白。在一优选实施例中,raav包含衍生自aav2的itr序列和衍生自aav6的衣壳序列。
在一些实施例中,可将工程改造和选择方法应用于aav衣壳以使其更加可能转导所关注细胞。
raav载体的构建、其制造和纯化已公开于例如美国专利第9,169,494号;第9,169,492号;第9,012,224号;第8,889,641号;第8,809,058号;和第8,784,799号,所述专利中的每一个以全文引用的方式并入本文中。
在各种实施例中,通过用包含一种或多种多核苷酸的逆转录病毒(例如慢病毒)转导细胞来将一种或多种多核苷酸引入免疫效应细胞(例如t细胞)中。
如本文所用,术语“逆转录病毒”是指将其基因组rna逆转录成线性双链dna拷贝并且随后将其基因组dna共价整合到宿主基因组中的rna病毒。适用于特定实施例中的说明性逆转录病毒包括但不限于:莫洛尼鼠白血病病毒(m-mulv)、莫洛尼鼠肉瘤病毒(momsv)、哈维鼠(harveymurine)肉瘤病毒(hamusv)、鼠乳腺肿瘤病毒(mumtv)、长臂猿白血病病毒(galv)、猫白血病病毒(flv)、泡沫病毒、弗兰德鼠(friendmurine)白血病病毒、鼠干细胞病毒(mscv)和劳斯肉瘤病毒(rsv)和慢病毒。
如本文所用,术语“慢病毒”是指复杂逆转录病毒组(或属)。说明性慢病毒包括(但不限于):hiv(人免疫缺陷病毒;包括hiv1型和hiv2型);维斯纳-梅迪病毒(vmv)病毒;山羊关节炎-脑炎病毒(caev);马传染性贫血病毒(eiav);猫免疫缺陷病毒(fiv);牛免疫缺陷病毒(biv);和猿猴免疫缺陷病毒(siv)。在一个实施例中,基于hiv的载体骨架(即,hiv顺式作用序列元件)是优选的。
在各种实施例中,本文中所涵盖的慢病毒载体包含一种或多种ltr,和以下辅助元件中的一种或多种或全部:cppt/flap、psi(ψ)包装信号、导出元件、poly(a)序列,且可以任选地包含如本文中其它地方所论述的wpre或hpre、绝缘子元件、可选标记和细胞自杀基因。
在特定实施例中,本文中所涵盖的慢病毒载体可以为整合或非整合或整合缺陷型慢病毒。如本文所用,术语“整合缺陷型慢病毒”或“idlv”是指具有不能将病毒基因组整合到宿主细胞的基因组中的整合酶的慢病毒。整合不胜任型病毒载体已经描述于专利申请wo2006/010834中,所述专利申请以全文引用的方式并入本文中。
适合于降低整合酶活性的hiv-1pol基因中的说明性突变包括但不限于:h12n、h12c、h16c、h16v、s81r、d41a、k42a、h51a、q53c、d55v、d64e、d64v、e69a、k71a、e85a、e87a、d116n、d1161、d116a、n120g、n1201、n120e、e152g、e152a、d35e、k156e、k156a、e157a、k159e、k159a、k160a、r166a、d167a、e170a、h171a、k173a、k186q、k186t、k188t、e198a、r199c、r199t、r199a、d202a、k211a、q214l、q216l、q221l、w235f、w235e、k236s、k236a、k246a、g247w、d253a、r262a、r263a和k264h。
术语“长末端重复序列(ltr)”是指位于逆转录病毒dna的末端处的碱基对域,其在其天然序列情形下是直接重复序列并且含有u3、r和u5区。
如本文所用,术语“flap元件”或“cppt/flap”是指其序列包括逆转录病毒(例如hiv-1或hiv-2)的中央多嘌呤段和中央终止序列(cppt和cts)的核酸。合适的flap元件描述于美国专利第6,682,907号和zennou等人,2000,《细胞(cell)》,101:173中。
如本文所用,术语“包装信号”或“包装序列”是指病毒rna插入到病毒衣壳或颗粒中所需的位于逆转录病毒基因组内的psi[ψ]序列,参看例如clever等人,1995.《病毒学杂志(j.ofvirology)》,第69卷,第4期;第2101-2109页。
术语“导出元件”是指调节rna转录物从细胞的细胞核输送到细胞质的顺式作用的转录后调节元件。rna导出元件的实例包括但不限于人免疫缺陷病毒(hiv)rev应答元件(rre)(参看例如cullen等人,1991.《j.virol.(病毒学杂志)》65:1053;和cullen等人,1991.《细胞》58:423)和乙型肝炎病毒转录后调节元件(hpre)。
在特定实施例中,病毒载体中异源序列的表达通过将转录后调节元件、高效聚腺苷酸化位点和任选地转录终止信号并入到载体中而增加。多种转录后调节元件可以增加异源核酸在蛋白质的表达,例如土拔鼠肝炎病毒转录后调节元件(wpre;zufferey等人,1999,《病毒学杂志》,73:2886);存在于乙型肝炎病毒中的转录后调节元件(hpre)(huang等人,《分子与细胞生物学》,5:3864);等(liu等人,1995,《基因与发育》,9:1766)。
慢病毒载体优选地含有由于修饰ltr而引起的数种安全性增强。“自我失活”(sin)载体是指复制缺陷型载体,例如其中称为u3区的右(3')ltr增强子-启动子区已经过修饰(例如通过缺失或取代)以防止病毒转录超过第一轮病毒复制。额外安全性增强通过用异源启动子置换5'ltr的u3区以在病毒颗粒产生期间驱动病毒基因组的转录而提供。可以使用的异源启动子的实例包括例如病毒猿猴病毒40(sv40)(例如早期或晚期)、巨细胞病毒(cmv)(例如立即早期)、莫洛尼鼠白血病病毒(momlv)、劳氏肉瘤病毒(rsv)以及单纯疱疹病毒(herpessimplexvirus,hsv)(胸苷激酶)启动子。
如本文所用,术语“假型”或“假型化”是指病毒包膜蛋白已经被另一个具有优选特征的病毒的病毒包膜蛋白取代的病毒。举例来说,hiv可以经水泡性口炎病毒g蛋白(vsv-g)包膜蛋白假型化,所述包膜蛋白使得hiv感染更广泛范围的细胞,因为hiv包膜蛋白(由env基因编码)通常使病毒靶向cd4+呈现细胞。
在某些实施例中,根据已知方法制备慢病毒载体。参见例如kutner等人,《bmc生物技术(bmcbiotechnol.)》2009;9:10.doi:10.1186/1472-6750-9-10;kutner等人.《自然协议(nat.protoc.)》2009;4(4):495-505.doi:10.1038/nprot.2009.22。
根据本文中所涵盖的某些特定实施例,大多数或所有的病毒载体骨架序列都衍生自慢病毒,例如hiv-1。然而,应理解,可以使用多种不同来源的逆转录病毒和/或慢病毒序列,或可以在不削弱转移载体执行本文所描述功能的能力的情况下对某些慢病毒序列提供组合并且众多的取代和变化。此外,多种慢病毒载体是所属领域中已知的,参见naldini等人,(1996a,1996b和1998年);zufferey等人,(1997年);dull等人,1998年,美国专利第6,013,516号和第5,994,136号,所述专利申请中的许多适用于产生本文中所涵盖的病毒载体或转移质粒。
在各种实施例中,通过用包含一种或多种多核苷酸的腺病毒转导细胞来将一种或多种多核苷酸引入免疫效应细胞中。
基于腺病毒的载体能够在许多细胞类型中实现极高转导效率且不需要细胞分裂。利用这类载体,已获得高效价和高水平表达。此载体可以在相对简单的系统中大量制备。大多数腺病毒载体经工程改造使得转基因置换ade1a、e1b和/或e3基因;随后,复制缺陷型载体在供应反式缺失基因功能的人类293细胞中繁殖。ad载体可以体内转导多种类型的组织,其包括非分裂分化细胞,如在肝脏、肾和肌肉中发现的那些。常规的ad载体具有较大承载容量。
当前复制缺乏型腺病毒载体的产生和繁殖可利用称为293的独特辅助细胞系,其通过ad5dna片段从人类胚胎肾细胞转化且构成性表达e1蛋白质(graham等人,1977)。因为e3区不一定来自腺病毒基因组(jones&shenk,1978),所以当前的腺病毒载体借助于293细胞在e1、d3或两个区域中携带外来dna(graham&prevec,1991)。腺病毒载体已用于真核基因表达(levrero等人,1991;gomez-foix等人,1992)和疫苗研究(grunhaus&horwitz,1992;graham&prevec,1992)。向不同组织施用重组腺病毒的研究包括气管灌输(rosenfeld等人,1991;rosenfeld等人,1992)、肌肉注射(ragot等人,1993)、外周静脉注射(herz&gerard,1993)和立体定向接种至大脑(legallasalle等人,1993)。将ad载体用于临床试验的实例涉及利用肌肉内注射进行抗肿瘤免疫接种的多核苷酸疗法(sterman等人,《人类基因治疗(hum.genether.)》7:1083-9(1998))。
在各种实施例中,通过用包含一种或多种多核苷酸的单纯疱疹病毒(例如hsv-1、hsv-2)转导细胞来将一种或多种多核苷酸引入免疫效应细胞中。
成熟hsv病毒粒子由包膜二十面体衣壳以及由为152kb的线性双链dna分子组成的病毒基因组组成。在一个实施例中,基于hsv的病毒载体缺乏一种或多种必需或非必需hsv基因。在一个实施例中,基于hsv的病毒载体是复制缺乏型。大多数复制缺乏型hsv载体含有缺失以移除一种或多种中早期、早期或晚期hsv基因从而防止复制。举例来说,hsv载体可缺乏选自由以下组成的组的中早期基因:icp4、icp22、icp27、icp47和其组合。hsv载体的优势是其进入可以导致长期dna表达的的潜伏期的能力以及其可以容纳至多25kb的外源性dna插入物的大病毒dna基因组。基于hsv的载体描述于例如美国专利第5,837,532号、第5,846,782号和第5,804,413号,和国际专利申请wo91/02788、wo96/04394、wo98/15637和wo99/06583中,其中的每一个以全文引用的方式并入本文中。
h.经基因修饰细胞
在各种实施例中,提供一种细胞,其经修饰以表达本文中所涵盖的救助car和/或可二聚救助受体,从而用于癌症治疗。细胞可未经基因修饰以表达本文中所涵盖的救助car和/或可二聚救助受体,或在特定的优选实施例中,细胞可经基因修饰以表达本文中所涵盖的救助car和/或可二聚救助受体。如本文所用,术语“经基因工程改造”或“经基因修饰”是指添加呈dna或rna形式的额外遗传物质到细胞中的总遗传物质中。术语“经基因修饰细胞”、“经修饰细胞”和“经重导引细胞”在特定实施例中可互换地使用。如本文所用,术语“基因疗法”是指将呈dna或rna形式的额外遗传物质引入细胞中的总遗传物质,恢复、校正或修饰基因表达,或为了表达救助car多肽和/或可二聚救助受体多肽。
在特定实施例中,将本文中所涵盖的救助car引入免疫效应细胞中且在免疫效应细胞中表达以便将其特异性重导引于所关注标靶抗原。在特定实施例中,将本文中所涵盖的救助car引入免疫效应细胞且在免疫效应细胞中表达以便将其特异性重导引于所关注的初级标靶抗原且在桥接因子存在下引入可二聚救助受体且对其诱导表达以便将其特异性重导引于所关注的次级标靶抗原。
“免疫效应细胞”是免疫系统的具有一种或多种效应功能(例如细胞毒性细胞杀伤活性、细胞因子的分泌、adcc和/或cdc的诱导)的任何细胞。本文中所涵盖的说明性免疫效应细胞是t淋巴细胞,尤其细胞毒性t细胞(ctl;cd8+t细胞)、til和辅助t细胞(htl;cd4+t细胞)。在一个实施例中,免疫效应细胞包括自然杀手(nk)细胞。在一个实施例中,免疫效应细胞包括自然杀手t(nkt)细胞。免疫效应细胞可为自身的(autologous/autogeneic)(“自”)或非自身的(“非自”,例如同种异体的、同基因的或异基因的)。
如本文所用,“自身的”是指来自同一受试者的细胞。如本文所用,“同种异体的”是指与比较细胞遗传不同的同一物种的细胞。如本文所用,“同基因的”是指与比较细胞遗传相同的来自不同受试者的细胞。如本文所用,“异基因的”是指与比较细胞来自不同物种的细胞。在优选实施例中,细胞为自身的。
用于本文中所涵盖的救助car和/或可二聚救助受体的说明性免疫效应细胞包括t淋巴细胞。术语“t细胞”或“t淋巴细胞”是领域公认的并且意图包括胸腺细胞、未成熟的t淋巴细胞、成熟t淋巴细胞、静息t淋巴细胞或活化的t淋巴细胞。t细胞可以是t辅助(th)细胞,例如t辅助1(th1)或t辅助2(th2)细胞。t细胞可以是辅助t细胞(htl;cd4+t细胞)cd4+t细胞、细胞毒性t细胞(ctl;cd8+t细胞)、cd4+cd8+t细胞、cd4-cd8-t细胞或任何其它t细胞子组。适用于特定实施例中的其它说明性t细胞群体包括原初t细胞和记忆t细胞。
如熟练人员将理解,还可使用其它细胞作为免疫效应细胞用于本文中所涵盖的救助car和/或可二聚救助受体。具体来说,免疫效应细胞还包括nk细胞、nkt细胞、嗜中性白细胞和巨噬细胞。免疫效应细胞还包括效应细胞的祖细胞,其中所述祖细胞可以在体内或体外经诱导以分化成免疫效应细胞。因此,在特定实施例中,免疫效应细胞包括免疫效应细胞的祖细胞,例如含于衍生自脐血、骨髓或流动外周血液的cd34+细胞群体内的造血干细胞(hsc),其在受试者中施用后分化成成熟免疫效应细胞,或其可以在体外经诱导以分化成成熟免疫效应细胞。
如本文所用,经基因工程改造以含有特异性救助car的免疫效应细胞可以被称为“抗原特异性重导引的免疫效应细胞”。
如本文所用,术语“cd34+细胞”是指在其细胞表面上表达cd34蛋白的细胞。如本文所用,“cd34”是指通常充当细胞-细胞粘附因子并且参与t细胞进入淋巴结中的细胞表面糖蛋白(例如唾液粘蛋白)。cd34+细胞群体含有造血干细胞(hsc),其在施用到患者后分化并且贡献于所有造血谱系(包括t细胞、nk细胞、nkt细胞、嗜中性白细胞和单核细胞/巨噬细胞谱系的细胞)。
在特定实施例中提供制备免疫效应细胞的方法,所述免疫效应细胞表达本文中所涵盖的救助car和/或可二聚救助受体。在一个实施例中,所述方法包含转染或转导从个体分离的免疫效应细胞,使得免疫效应细胞表达一种或多种如本文所预期的救助car。在一个实施例中,所述方法包含转染或转导从个体分离的免疫效应细胞,使得免疫效应细胞表达一种或多种本文中所涵盖的救助car和/或可二聚救助受体。在某些实施例中,免疫效应细胞从个体分离并且在无进一步体外操纵的情况下经基因修饰。所述细胞然后可以直接再施用到个体。在另外的实施例中,免疫效应细胞在经基因修饰之前首先经活化和刺激以体外增殖。就此而言,可在经基因修饰之前和/或之后培养免疫效应细胞。
在特定实施例中,在体外操纵或遗传修饰本文所描述的免疫效应细胞之前,细胞来源是获自受试者。在特定实施例中,经修饰免疫效应细胞包含t细胞。
t细胞可以获自多种来源,包括但不限于外周血液单核细胞、骨髓、淋巴结组织、脐带血、胸腺组织、来自感染位点的组织、腹水、胸腔积液、脾组织和肿瘤。在某些实施例中,t细胞可以获自使用多种为熟练人员已知的技术(例如沉降,例如ficolltm分离)从受试者收集的血液单位。
在其它实施例中,使用经分离或经纯化t细胞群体。在一些实施例中,在分离pbmc之后,细胞毒性和辅助t淋巴细胞两者都可以在活化、扩增和/或基因修饰之前或之后分选成原初、记忆和效应t细胞亚群。
表达以下标记中的一种或多种的t细胞的特异性亚群可以进一步通过阳性或阴性选择技术分离:cd3、cd4、cd8、cd28、cd45ra、cd45ro、cd62、cd127和hla-dr。在一个实施例中,表达选自由以下组成的组的标记中的一种或多种的t细胞的特定亚群进一步通过阳性或阴性选择技术分离:cd62l、ccr7、cd28、cd27、cd122、cd127、cd197;或cd38或cd62l、cd127、cd197和cd38。在各种实施例中,所制造的t细胞组合物不表达或基本上不表达以下标记中的一种或多种:cd57、cd244、cd160、pd-1、ctla4、tim3和lag3。
在一个实施例中,经分离或经纯化t细胞群体表达包括但不限于cd3+、cd4+、cd8+或其组合的标记中的一种或多种。
在某些实施例中,t细胞从个体分离且在经修饰以表达救助car和/或可二聚救助受体之前首先经活化和刺激以体外增殖。
为了实现t细胞组合物的充足治疗剂量,t细胞通常经历一轮或多轮刺激、活化和/或扩增。t细胞可以通常使用如例如美国专利6,352,694、6,534,055、6,905,680、6,692,964、5,858,358、6,887,466、6,905,681、7,144,575、7,067,318、7,172,869、7,232,566、7,175,843、5,883,223、6,905,874、6,797,514和6,867,041中所描述的方法来活化和扩增,所述美国专利中的每一者以全文引用的方式并入本文中。在特定实施例中,在引入编码本文中所涵盖的救助car和/或可二聚救助受体的载体或mrna之前,t细胞经活化和扩增约6小时、约12小时、约18小时或约24小时。
在一个实施例中,t细胞在其经修饰的同时经活化。
在各种实施例中,产生cart细胞的方法包含活化包含t细胞的细胞群体和扩增t细胞群体。t细胞活化可以通过经由t细胞tcr/cd3复合物提供初级刺激信号和通过经由辅助分子(例如cd28)提供次级共刺激信号来实现。
tcr/cd3复合物可以通过使t细胞与适合cd3结合剂(例如cd3配体或抗cd3单克隆抗体)接触而受刺激。cd3抗体的说明性实例包括但不限于okt3、g19-4、bc3和64.1。
除了经由tcr/cd3复合物提供的初级刺激信号之外,诱导t细胞应答需要第二共刺激信号。在特定实施例中,cd28结合剂可以用以提供共刺激信号。cd28结合剂的说明性实例包括但不限于:天然cd28配体,例如cd28的天然配体(例如蛋白质b7家族的成员,例如b7-1(cd80)和b7-2(cd86));和能够交联cd28分子的抗cd28单克隆抗体或其片段,例如单克隆抗体9.3、b-t3、xr-cd28、kolt-2、15e8、248.23.2和ex5.3d10。
在一个实施例中,提供初级刺激信号的分子(例如经由tcr/cd3复合物提供刺激的分子)与共刺激分子偶合到相同表面。
在某些实施例中,提供刺激和共刺激信号的结合剂定位于细胞表面上。这可以通过用编码结合剂(呈适用于其于细胞表面上表达的形式)的核酸转染或转导细胞、或者通过使结合剂偶合到细胞表面而实现。
在另一实施例中,提供初级刺激信号的分子(例如经由tcr/cd3复合物提供刺激的分子)与共刺激分子呈现于抗原呈现细胞上。
在一个实施例中,将提供初级刺激信号的分子(例如经由tcr/cd3复合物提供刺激的分子)和共刺激分子提供于分离表面上。
在某一实施例中,提供刺激和共刺激信号的结合剂中的一种为可溶的(提供于溶液中)且将其它试剂提供于一个或多个表面上。
在一特定实施例中,提供刺激和共刺激信号的结合剂都以可溶形式提供(提供于溶液中)。
在各种实施例中,制备本文中所涵盖的救助cart细胞的方法包含用抗cd3和抗cd28抗体活化t细胞。
在一个实施例中,使通过本文所涵盖的方法活化的t细胞扩增进一步包含培养包含t细胞的细胞群体数小时(约3小时)到约7天到约28天或中间的任何每小时整数值。在另一实施例中,可以培养t细胞组合物14天。在一特定实施例中,培养t细胞约21天。在另一实施例中,培养t细胞组合物约2-3天。还可能需要若干刺激/活化/扩增循环,使得t细胞的培养时间可以是60天或更久。
在特定实施例中,适合于t细胞培养的条件包括合适的培养基(例如最小必需培养基或rpmi培养基1640或x-vivo15,(龙沙))以及增殖和存活所需的一种或多种因素,包括但不限于血清(例如胎牛或人类血清)、白介素-2(il-2)、胰岛素、ifn-γ、il-4、il-7、il-21、gm-csf、il-10、il-12、il-15、tgfβ和tnf-α或熟练技术人员已知的适用于细胞生长的任何其它添加剂。
细胞培养基的其它说明性实例包括但不限于rpmi1640、clicks、aim-v、dmem、mem、a-mem、f-12、x-vivo15和x-vivo20、optimizer,其具有添加的氨基酸、丙酮酸钠和维生素,无血清或补充有合适量的血清(血浆)或定义组的激素,和/或足以实现t细胞生长和扩增的量的细胞因子。
抗生素(例如青霉素和链霉素)仅包括于实验培养物中,不包括于待输注到受试者中的细胞培养物中。靶细胞维持在支持生长所必需的条件下,例如适当温度(例如37℃)和气氛(例如空气加5%co2)。
在特定实施例中,使pbmc或经分离t细胞与一般附着到珠粒或其它表面的刺激试剂和共刺激试剂(如抗cd3和抗cd28抗体)在具有合适的细胞因子(如il-2、il-7和/或il-15)的培养基中接触。
在其它实施例中,人工apc(aapc)通过工程改造k562、u937、721.221、t2和c1r细胞以导引多种共刺激分子和细胞因子的稳定表达和分泌而制备。在一特定实施例中,使用k32或u32aapc导引一种或多种基于抗体的刺激分子在aapc细胞表面上呈现。t细胞群体可以通过表达多种共刺激分子(包括但不限于cd137l(4-1bbl)、cd134l(ox40l)和/或cd80或cd86)的aapc扩增。最后,aapcs提供有效的平台用以扩增经基因修饰t细胞且维持在cd8t细胞上的cd28表达。在wo03/057171和us2003/0147869中提供的aapc以全文引用的方式并入本文中。
在一特定实施例中,将编码救助car和/或可二聚救助受体的多核苷酸引入t细胞群体中。多核苷酸可以通过微注射、转染、脂质体转染、热休克、电穿孔、转导、基因枪、微注射、deae-右旋糖苷-介导的转移等引入t细胞中。
在各种实施例中,产生救助cart细胞。在一些实施例中,救助cart细胞通过引入核酸经进一步基因修饰,所述核酸包含可操作地连接于编码可二聚救助受体的多核苷酸的诱导型启动子。
在一优选实施例中,通过病毒转导将多核苷酸引入t细胞中。
适用于将多核苷酸引入免疫效应细胞或cd34+细胞的病毒载体系统的说明性实例包括但不限于腺相关病毒(adeno-associatedvirus;aav)、逆转录病毒、单纯疱疹病毒、腺病毒、牛痘病毒载体以用于基因转移。
在一个实施例中,通过aav转导将多核苷酸引入t细胞中。
在一个实施例中,通过逆转录病毒转导将多核苷酸引入t细胞中。
在一个实施例中,通过慢病毒转导将多核苷酸引入t细胞中。
在一个实施例中,通过腺病毒转导将多核苷酸引入t细胞中。
在一个实施例中,通过单纯疱疹病毒转导将多核苷酸引入t细胞中。
在一个实施例中,通过牛痘病毒转导将多核苷酸引入t细胞中。
在各种实施例中,本文中所涵盖的经基因修饰细胞进一步包含一种或多种经修饰tcrα等位基因。在特定实施例中,将一种或多种经设计以在tcrα基因座处产生双链断裂的经工程改造核酸酶引入救助cart细胞中。在特定实施例中,将一种或多种经设计以在tcrα基因座处产生双链断裂的经工程改造核酸酶引入救助cart细胞中,所述救助cart细胞包含核酸,所述核酸包含可操作地连接于编码可二聚救助受体的多核苷酸的诱导型启动子。
在特定实施例中,产生经基因修饰t细胞的方法包含使细胞与刺激试剂和共刺激试剂(如可溶性抗cd3和抗cd28抗体,或附着到珠粒或其它表面的抗体)在具有合适细胞因子(如il-2、il-7和/或il-15)和/或一种或多种调节pi3k细胞信号传导的试剂的培养基中接触。
如本文所用,术语“pi3k抑制剂”是指结合到pi3k并且抑制其至少一种活性的核酸、肽、化合物或小有机分子。pi3k蛋白可以分成三类,1类pi3k、2类pi3k和3类pi3k。1类pi3k以由四种p110催化亚单位(p110α、p110β、p110δ和p110γ)之一和两种调节亚单位家族之一组成的杂二聚体形式存在。在特定实施例中,pi3k抑制剂靶向1类pi3k抑制剂。在一个实施例中,pi3k抑制剂将呈现对1类pi3k抑制剂的一种或多种同工型的选择性(即,对p110α、p110β、p110δ和p110γ、或p110α、p110β、p110δ和p110γ中的一种或多种的选择性)。在另一方面,pi3k抑制剂将不呈现同工型选择性并且被视为“泛pi3k抑制剂”。在一个实施例中,pi3k抑制剂将与atp为结合到pi3k催化域而竞争。
适用于特定实施例的pi3k抑制剂的说明性实例包括但不限于bkm120(1类pi3k抑制剂,诺华)、xl147(1类pi3k抑制剂,伊克塞利克斯)、(泛-pi3k抑制剂,葛兰素史克)和px-866(1类pi3k抑制剂;p110α、p110β和p110γ同工型,赛瑞恩肿瘤药剂)。
选择性pi3k抑制剂的其它说明性实例包括但不限于byl719、gsk2636771、tgx-221、as25242、cal-101、zstk474和ipi-145。
泛-pi3k抑制剂的其它说明性实例包括但不限于bez235、ly294002、gsk1059615、tg100713和gdc-0941。
在一优选实施例中,pi3k抑制剂是zstk474。
i.组合物和配制物
本文中所涵盖的组合物可包含一种或多种多肽、多核苷酸、包含其的载体、经基因修饰的免疫效应细胞等。组合物包括但不限于医药组合物。“医药组合物”是指配制于医药学上可接受的或生理学上可接受的溶液中用于单独或与一种或多种其它治疗模式组合向细胞或动物施用的组合物。还应理解,必要时,组合物还可以与其它试剂(例如细胞因子、生长因子、激素、小分子、化学治疗剂、前药、药物、抗体或其它各种医药学上活性剂)组合施用。对也可以包括于组合物中的其它组分几乎没有限制,只要其它试剂不会不利地影响组合物传递预期治疗的能力即可。
短语“医药学上可接受的”在本文中用以指在合理医学判断范围内,那些化合物、物质、组合物和/或剂型适用于与人类和动物的组织接触而无过量毒性、刺激、过敏反应或其它问题或并发症,与合理效益/风险比相称。
如本文所用,“医药学上可接受的载剂”包括(但不限于)已经由美国食品和药物管理局(theunitedstatesfoodanddrugadministration)批准为对于用于人类或家畜可接受的任何佐剂、载剂、赋形剂、助流剂、甜味剂、稀释剂、防腐剂、染料/着色剂、风味增强剂、表面活性剂、湿润剂、分散剂、悬浮剂、稳定剂、等张剂、溶剂、表面活性剂或乳化剂。示例性医药学上可接受的载剂包括但不限于糖,例如乳糖、葡萄糖和蔗糖;淀粉,例如玉米淀粉和马铃薯淀粉;纤维素和其衍生物,例如羧甲基纤维素钠、乙基纤维素和乙酸纤维素;黄蓍胶;麦芽;明胶;滑石;可可脂、蜡、动物和植物脂肪、石蜡、硅酮、膨润土、硅酸、氧化锌;油,例如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;二醇,例如丙二醇;多元醇,例如甘油、山梨糖醇、甘露糖醇和聚乙二醇;酯,例如油酸乙酯和月桂酸乙酯;琼脂;缓冲剂,例如氢氧化镁和氢氧化铝;海藻酸;无热原质水;等张生理盐水;林格氏溶液(ringer’ssolution);乙醇;磷酸盐缓冲溶液;以及医药配制物中采用的任何其它相容物质。
在特定实施例中,组合物包含一定量的本文中所涵盖的表达救助car的免疫效应细胞。在其它特定实施例中,组合物包含一定量的可二聚救助受体。在其它特定实施例中,组合物包含一定量的桥接因子。在其它特定实施例中,组合物包含一定量的与桥接因子结合的可二聚救助受体。
如本文所用,术语“量”是指治疗细胞、救助cart细胞、可二聚救助受体或桥接因子等实现有益或所需的防治性或治疗性结果(包括临床效果)的“有效的量(anamounteffective)”或“有效量(aneffectiveamount)”。
“预防有效量”是指治疗细胞、救助cart细胞、可二聚救助受体或桥接因子等可有效实现所需预防结果的量。通常但未必,因为预防性剂量在疾病之前或在疾病的较早阶段用于受试者,所以预防有效量小于治疗有效量。
治疗细胞、救助cart细胞、可二聚救助受体或桥接因子等的“治疗有效量”可根据各种因素变化,如个体的疾病病况、年龄、性别和重量,和组合物引发个体中的所需应答的能力。治疗有效量也是其中治疗有益效果超过治疗细胞、救助cart细胞、可二聚救助受体或桥接因子等的任何有毒或有害影响的量。术语“治疗有效量”包括可有效地“治疗”受试者(例如患者)的量。当指定治疗量时,待施用的组合物的精确量可以由医师在考虑个体在年龄、重量、肿瘤尺寸、感染或癌转移程度以及患者(受试者)的病状方面的差异情况下确定。通常可以规定,包含本文所描述t细胞的医药组合物可以按102到1010个细胞/千克体重、优选105到106个细胞/千克体重(包括那些范围内的所有整数值)的剂量施用。细胞数目将取决于组合物预期用于的最终用途和其中包括的细胞的类型。对于本文所提供的使用,细胞的体积一般为一升或更少,可以为500ml或更少、甚至250ml或100ml或更少。因此,所要细胞的密度通常大于106个细胞/毫升,并且通常大于107个细胞/毫升,通常是108个细胞/毫升或更大。临床相关数目的免疫细胞可以分配成多个累积等于或超过105、106、107、108、109、1010、1011或1012个细胞的输注。在一些实施例中,特别因为可以将全部输注细胞重导引到特定的标靶抗原,所以可以施用较低数目的细胞,在106/千克(每名患者106-1011)范围内。可以用这些范围内的剂量多次施用t细胞组合物,所述t细胞组合物包含表达救助car的t细胞。细胞对于经历治疗的患者可以是同种异体的、同基因的、异基因的或自身的。必要时,治疗还可以包括如本文所述施用有丝分裂原(例如pha)或淋巴因子、细胞因子和/或趋化因子(例如ifn-γ、il-2、il-12、tnf-α、il-18和tnf-β、gm-csf、il-4、il-13、flt3-l、rantes、mip1α等)以增强免疫应答的诱导。
一般来说,包含如本文所述活化和扩增的细胞的组合物可以用于治疗和预防在免疫功能不全的个体中产生的疾病。具体地说,本文中所涵盖的组合物用于治疗癌症。在特定实施例中,经救助car修饰的t细胞、可二聚救助受体和桥接因子可以单独或呈医药组合物形式与载剂、稀释剂、赋形剂和/或与其它组分(如il-2)或其它细胞因子或细胞群组合施用。
在特定实施例中,医药组合物包含一定量的经基因修饰的t细胞,以及一种或多种医药学上或生理学上可接受的载剂、稀释剂或赋形剂。
在特定实施例中,医药组合物包含一定量的可二聚救助受体,以及一种或多种医药学上或生理学上可接受的载剂、稀释剂或赋形剂。
在特定实施例中,医药组合物包含一定量的桥接因子,以及一种或多种医药学上或生理学上可接受的载剂、稀释剂或赋形剂。
包含表达救助car的免疫效应细胞群体(如t细胞)、可二聚救助受体或桥接因子的医药组合物可包含缓冲剂,如中性缓冲盐水、磷酸盐缓冲盐水等;碳水化合物,如葡萄糖、甘露糖、蔗糖或聚葡萄糖、甘露糖醇;蛋白质;多肽或氨基酸,如甘氨酸;抗氧化剂;螯合剂,如edta或谷胱甘肽;佐剂(例如氢氧化铝);和防腐剂。在特定实施例中,组合物优选地被调配成用于经鼻、口服、经肠或肠胃外施用,例如血管内(静脉内或动脉内)、腹膜内或肌肉内施用。
液体医药组合物(其呈溶液、悬浮液或其它类似形式)可包括以下中的一种或多种:无菌稀释剂,如注射用水、盐水溶液(优选生理盐水)、林格氏溶液、等张氯化钠;不挥发性油,如可充当溶剂或悬浮介质的合成单或二甘油酯、聚乙二醇、甘油、丙二醇或其它溶剂;抗细菌剂,如苄醇或对羟基苯甲酸甲酯;抗氧化剂,如抗坏血酸或亚硫酸氢钠;螯合剂,如乙二胺四乙酸;缓冲剂,如乙酸盐、柠檬酸盐或磷酸盐和用于调节张力的试剂,如氯化钠或右旋糖。可以将肠胃外制剂密封在由玻璃或塑料制成的安瓿、一次性注射器或多剂量小瓶中。可注射医药组合物优选地是无菌的。
在一个实施例中,本文中所涵盖的t细胞组合物在医药学上可接受的细胞培养基中配制。这类组合物适合对人类受试者施用。在特定实施例中,医药学上可接受的细胞培养基是无血清培养基。
与含有血清的培养基相比,无血清培养基具有几个优点,包括组成简化且更明确,污染程度降低,潜在感染物来源消除,并且成本更低。在各个实施例中,无血清培养基是无动物成分的,并且可以任选地是无蛋白质的。任选地,培养基可以含有生物药学上可接受的重组蛋白。“无动物成分”培养基是指其中组分来源于非动物来源的培养基。重组蛋白置换无动物成分培养基中的原生动物蛋白且营养获自合成、植物或微生物来源。相比之下,“无蛋白质”培养基被定义为基本上不含蛋白质。
特定组合物中所用的无血清培养基的说明性实例包括但不限于qbsf-60(质量生物公司(qualitybiological,inc.))、stempro-34(生命技术公司(lifetechnologies))和x-vivo10。
在一个优选实施例中,包含本文中所涵盖的t细胞的组合物在包含plasmalytea的溶液中配制。
在另一优选实施例中,包含本文中所涵盖的t细胞的组合物在包含冷冻保存培养基的溶液中配制。举例来说,可以使用含冷冻保存剂的冷冻保存培养基在解冻后维持高细胞活力结果。特定组合物中所用的冷冻保存培养基的说明性实例包括但不限于cryostorcs10、cryostorcs5和cryostorcs2。
在一更优选实施例中,包含本文中所涵盖的t细胞的组合物在包含50:50plasmalytea到cryostorcs10的溶液中配制。
在一特定实施例中,组合物包含有效量的单独或与一种或多种治疗剂组合的表达救助car的免疫效应细胞。因此,可以单独或与可二聚救助受体、桥接因子或其它已知癌症治疗组合施用表达救助car的免疫效应细胞组合物,所述其它已知癌症治疗如辐射疗法、化学疗法、移植、免疫疗法、激素疗法、光动力疗法等。组合物还可以与抗生素组合施用。这类治疗剂在所属领域中可以接受为如本文所述的特定疾病状态(例如特定癌症)的标准治疗。所涵盖的示例性治疗剂包括细胞因子、生长因子、类固醇、nsaid、dmard、消炎剂、化学治疗剂、放射治疗剂、治疗抗体或其它活性并且辅助性试剂。
在某些实施例中,包含本文所公开的表达救助car的免疫效应细胞的组合物可以与多种化学治疗剂结合施用。化学治疗剂的说明性实例包括烷基化剂,例如噻替派和环磷酰胺(cytoxantm);烷基磺酸盐,例如白消安、英丙舒凡(improsulfan)和哌泊舒凡(piposulfan);氮丙啶,例如苯唑多巴、卡波醌、米特多巴(meturedopa)和尤利多巴(uredopa);乙烯亚胺和甲基三聚氰胺,包括六甲蜜胺、三乙烯三聚氰胺、三乙烯磷酰胺、三乙烯硫代磷酰胺和三羟甲基三聚氰胺;氮芥,例如氯芥苯丁酸、萘氮芥、氯磷酰胺、雌莫司汀、异环磷酰胺、二氯甲二乙胺、二氯甲二乙胺氧化物盐酸盐、美法仑、新恩比兴、胆固醇对苯乙酸氮芥、泼尼氮芥、曲洛磷胺、尿嘧啶芥末;亚硝基脲,例如卡莫司汀、氯脲菌素、福莫司汀、洛莫司汀、尼莫司汀、雷诺莫司汀;抗生素,例如阿克拉霉素、放射菌素、奥斯拉菌素、氮杂丝氨酸、博来霉素、放线菌素c、卡奇霉素、卡柔比星、洋红霉素、嗜癌霉素、色霉素、更生霉素、道诺霉素、地托比星、6-重氮-5-氧代-l-正亮氨酸、多柔比星、表柔比星、依索比星、艾达霉素、麻西罗霉素、丝裂霉素、霉酚酸、诺加霉素、橄榄霉素、培洛霉素、泼非霉素、嘌呤霉素、奎那霉素、罗多比星、链黑霉素、链脲霉素、杀结核菌素、乌苯美司、净司他丁、左柔比星;抗代谢物,例如甲氨蝶呤和5-氟尿嘧啶(5-fu);叶酸类似物,例如迪诺特宁、甲氨蝶呤、蝶罗呤、三甲曲沙;嘌呤类似物,例如氟达拉滨、6-巯基嘌呤、噻咪嘌呤、硫鸟嘌呤;嘧啶类似物,例如安西他滨、阿扎胞苷、6-氮杂尿苷、卡莫氟、阿糖胞苷、双去氧尿苷、去氧氟尿苷、依诺他滨、氟尿苷、5-fu;雄激素,例如卡普睾酮、丙酸屈他雄酮、环硫雄醇、美雄烷、睾内酯;抗肾上腺,例如氨鲁米特、米托坦、曲洛司坦;叶酸补充剂,例如亚叶酸;醋葡醛内酯;醛磷酰胺糖苷;氨基乙酰丙酸;安吖啶;倍思塔布;比生群;艾达曲克;得弗伐胺;秋水仙碱;地吖醌;艾福米辛;乙酸依利铵;依托格鲁;硝酸镓;羟基脲;香菇多糖;氯尼达明;米托胍腙;米托蒽醌;莫哌达醇;尼曲吖啶;喷司他汀;凡那明;吡柔比星;鬼臼酸;2-乙酰肼;丙卡巴肼;
多种其它治疗剂可以与本文所描述的组合物结合使用。在一个实施例中,包含表达car的免疫效应细胞的组合物与消炎剂一起施用。消炎剂或药物包括但不限于类固醇和糖皮质激素(包括倍他米松(betamethasone)、布地奈德(budesonide)、地塞米松(dexamethasone)、乙酸氢皮质酮(hydrocortisoneacetate)、氢皮质酮(hydrocortisone)、氢皮质酮、甲基泼尼松龙(methylprednisolone)、泼尼松龙(prednisolone)、泼尼松(prednisone)、曲安西龙(triamcinolone));非类固醇消炎药物(nsaids),包括阿司匹林(aspirin)、布洛芬(ibuprofen)、萘普生(naproxen)、甲胺喋呤(methotrexate)、柳氮磺胺吡啶(sulfasalazine)、来氟米特(leflunomide)、抗tnf药剂、环磷酰胺和霉酚酸酯(mycophenolate)。
其它示例性nsaid选自由以下组成的组:布洛芬、萘普生、萘普生钠、cox-2抑制剂(例如
适用于与本文中所涵盖的经救助car修饰的t细胞组合的治疗抗体的说明性实例包括但不限于巴韦西布(bavituximab)、贝伐单抗(bevacizumab)(阿瓦斯汀(avastin))、比伐珠单抗(bivatuzumab)、布林莫单抗(blinatumomab)、康纳木单抗(conatumumab)、达土木单抗(daratumumab)、杜丽戈图单抗(duligotumab)、达西珠单抗(dacetuzumab)、达罗土珠单抗(dalotuzumab)、埃罗妥珠单抗(elotuzumab)(huluc63)、吉妥单抗(gemtuzumab)、异贝莫单抗(ibritumomab)、茚达昔单抗(indatuximab)、伊珠单抗(inotuzumab)、洛沃珠单抗(lorvotuzumab)、鲁卡木单抗(lucatumumab)、米拉珠单抗(milatuzumab)、莫昔土莫单抗(moxetumomab)、奥卡拉珠单抗(ocaratuzumab)、奥法木单抗(ofatumumab)、利妥昔单抗(rituximab)、思图昔单抗(siltuximab)、替普罗木单抗(teprotumumab)和乌布里图昔单抗(ublituximab),其单独或作为可二聚救助受体的部分。
在某些实施例中,本文所描述的组合物与细胞因子结合施用。如本文所用,“细胞因子”意指由一种细胞群体释放的以胞间介体形式作用于另一细胞的蛋白质的通称。这类细胞因子的实例是淋巴因子、单核因子和传统多肽激素。细胞因子之中包括生长激素,例如人类生长激素、n-甲硫氨酰人类生长激素和牛生长激素;副甲状腺激素;甲状腺素;胰岛素;胰岛素原;松弛素;松弛素原;糖蛋白激素,例如促卵泡激素(fsh)、促甲状腺激素(tsh)和促黄体激素(lh);肝生长因子;成纤维细胞生长因子;促乳素;胎盘催乳素;肿瘤坏死因子-α和β;苗勒氏(mullerian)抑制物质;小鼠促性腺激素相关肽;抑制素;活化素;血管内皮生长因子;整合素;血小板生成素(tpo);神经生长因子,例如ngf-β;血小板生长因子;转化生长因子(tgf),例如tgf-α和tgf-β;胰岛素样生长因子-i和ii;促红细胞生成素(epo);骨诱导因子;干扰素,例如干扰素-α、β和γ;集落刺激因子(csf),例如巨噬细胞-csf(m-csf)、粒细胞-巨噬细胞-csf(gm-csf)和粒细胞-csf(g-csf);白介素(il),例如il-1、il-1α、il-2、il-3、il-4、il-5、il-6、il-7、il-8、il-9、il-10、il-11、il-12、il-15;肿瘤坏死因子,例如tnf-α或tnf-β;和其它多肽因子,包括lif和kit配体(kl)。如本文所用,术语细胞因子包括来自天然来源或来自重组细胞培养物的蛋白质,和天然序列细胞因子的生物活性等效物。
j.治疗方法
本文中所涵盖的救助car系统提供过继性免疫疗法的改善方法,用于预防、治疗和改善癌症,或用于预防、治疗或改善与癌症相关的至少一种症状。在优选实施例中,本文中所涵盖的救助car系统提供过继性免疫疗法的改善方法,用于预防、治疗和改善复发性或难治性癌症。
在各种实施例中,本文中所涵盖的救助car系统提供过继性免疫疗法的改善方法,用于提高对复发性或难治性癌细胞的细胞毒性或用于减少复发性或难治性癌细胞的数目。
在特定实施例中,通过用针对在癌细胞上表达的第一抗原的救助car基因修饰原代t细胞将原代t细胞的特异性重导引于肿瘤或癌细胞。在一个实施例中,将救助cart细胞输注到有需要的受体。输注细胞能够杀灭受体中的肿瘤细胞。不同于抗体疗法,救助cart细胞能够体内复制;因此有助于长期持久性,其可以导致更加持续的癌症疗法。然而,在缓解或癌症消退未完成且癌症复发或变得难以治疗的情况下,在桥接因子存在下提供可二聚救助受体以将救助cart细胞疗法重新靶向于在复发性或难治性癌细胞上表达的第二抗原。
在一个实施例中,向诊断患有癌症的受试者施用救助cart细胞。在复发性或难治性癌细胞生长后,向受试者施用可二聚救助受体和桥接因子以重新起始对复发性或难治性细胞的cart细胞疗法。如果继发性肿瘤也复发,那么可以向受试者提供不同的救助cart细胞、不同的可二聚救助受体或两者。可以视需要多次重复此循环以根除受试者中的癌症。
在一个实施例中,向诊断患有癌症的受试者施用包含诱导性可二聚救助受体的救助cart细胞。在复发性或难治性癌细胞生长后,向受试者施用诱导可二聚救助受体表达的试剂,且还施用桥接因子以重新起始对复发性或难治性细胞的cart细胞疗法。如果继发性肿瘤也复发,那么可以向受试者提供不同的救助cart细胞、不同的可二聚救助受体或两者。不同的救助受体可处于同一救助cart细胞中的不同诱导型启动子的控制下或通过可二聚救助受体多肽的直接施用提供。可以视需要多次重复此循环以根除受试者中的癌症。
在特定实施例中,本文中所涵盖的救助car系统用于治疗实体肿瘤或癌症。
在特定实施例中,本文中所涵盖的救助car系统用于治疗包括但不限于以下的实体肿瘤或癌症:肾上腺癌、肾上腺皮质癌、肛门癌、阑尾癌、星形细胞瘤、非典型畸胎样/横纹肌样肿瘤、基底细胞癌、胆管癌、膀胱癌、骨癌、脑癌/cns癌、乳癌、支气管肿瘤、心脏肿瘤、子宫颈癌、胆管癌、软骨肉瘤、脊索瘤、结肠癌、结肠直肠癌、颅咽管瘤、乳腺管原位癌(dcis)、子宫内膜癌、室管膜瘤、食道癌、鼻腔神经胶质瘤、尤文氏肉瘤、颅外生殖细胞肿瘤、性腺外生殖细胞肿瘤、眼癌、输卵管癌、纤维组织肉瘤、纤维肉瘤、胆囊癌、胃癌、胃肠道类癌瘤、胃肠道间质瘤(gist)、生殖细胞肿瘤、神经胶质瘤、神经胶母细胞瘤、头颈癌、成血管细胞瘤、肝细胞癌、下咽癌、眼内黑素瘤、卡波西肉瘤、肾癌、喉癌、平滑肌肉瘤、唇癌、脂肪肉瘤、肝癌、肺癌、非小细胞肺癌、肺类癌瘤、恶性间皮瘤、髓质癌、神经管胚细胞瘤、脑膜瘤、黑素瘤、梅克尔细胞癌、中线消化道癌、嘴癌、粘液肉瘤、骨髓发育不良综合征、骨髓增生赘瘤、鼻腔和副鼻窦癌、鼻咽癌、神经母细胞瘤、少突神经胶质瘤、口腔癌(oralcancer)、口腔癌(oralcavitycancer)、口咽癌、骨肉瘤、卵巢癌、胰脏癌、胰脏胰岛细胞瘤、乳头状癌、副神经节瘤、副甲状腺癌、阴茎癌、咽癌、嗜铬细胞瘤、松果体瘤、垂体肿瘤、胸膜肺母细胞瘤、原发性腹膜癌、前列腺癌、直肠癌、视网膜母细胞瘤、肾细胞癌、肾盂和输尿管癌、横纹肌肉瘤、唾液腺癌、皮脂腺癌、皮肤癌、软组织肉瘤、鳞状细胞癌、小细胞肺癌、小肠癌、胃癌、汗腺癌、滑膜瘤、睾丸癌、喉癌、胸腺癌、甲状腺癌、尿道癌、子宫癌、子宫肉瘤、阴道癌、血管癌、外阴癌和肾母细胞瘤。
在特定实施例中,本文中所涵盖的救助car系统用于治疗实体肿瘤或癌症,其包括但不限于肝癌、胰脏癌、肺癌、乳癌、膀胱癌、脑癌、骨癌、甲状腺癌、肾癌或皮肤癌。
在特定实施例中,本文中所涵盖的救助car系统用于治疗各种各种,包括但不限于胰脏癌、膀胱癌和肺癌。
在特定实施例中,本文中所涵盖的救助car系统用于治疗液体癌或血液癌。
在特定实施例中,本文中所涵盖的救助car系统用于治疗b细胞恶性肿瘤,包括但不限于:白血病、淋巴瘤和多发性骨髓瘤。
在特定实施例中,本文中所涵盖的救助car系统用于治疗液体癌,其包括但不限于白血病、淋巴瘤和多发性骨髓瘤:急性淋巴细胞性白血病(all)、急性骨髓性白血病(aml)、骨髓母细胞白血病、前髓细胞白血病、骨髓单核细胞性白血病、单核细胞性白血病、红白血病、毛细胞白血病(hcl)、慢性淋巴细胞性白血病(cll)、和慢性骨髓白血病(cml)、慢性骨髓单核细胞性白血病(cmml)和真性红细胞增多症、霍奇金淋巴瘤、结节性淋巴细胞为主型的霍奇金淋巴瘤、伯基特淋巴瘤、小淋巴细胞性淋巴瘤(sll)、弥漫性大b细胞淋巴瘤、滤泡性淋巴瘤、成免疫细胞性大细胞淋巴瘤、前体b成淋巴细胞性淋巴瘤、套细胞淋巴瘤、边缘区淋巴瘤、蕈样真菌病、多形性大细胞淋巴瘤、塞扎莱综合征、前体t成淋巴细胞性淋巴瘤、多发性骨髓瘤、明显多发性骨髓瘤、郁积性多发性骨髓瘤、浆细胞白血病、非分泌性骨髓瘤、igd骨髓瘤、骨硬化性骨髓瘤、骨骼的孤立性浆细胞瘤,和髓外浆细胞瘤。
在特定实施例中,一种方法包含向有需要的患者施用治疗有效量的救助cart细胞和随后在复发性或难治性癌细胞生长情况下向受试者施用可二聚救助受体和桥接因子。
在特定实施例中,一种方法包含向有需要的患者施用治疗有效量的救助cart细胞和随后在复发性或难治性癌细胞生长情况下向受试者施用与桥接因子结合的可二聚救助受体。
在特定实施例中,一种方法包含向有需要的患者施用治疗有效量的救助cart细胞,和随后在复发性或难治性癌细胞生长情况下诱导可二聚救助受体的表达以及向受试者施用桥接因子。
在某些实施例中,使用细胞治疗处于罹患癌症的风险下的患者。因此,特定实施例包含治疗或预防或改善癌症的至少一种症状,其包含向有需要的患者施用治疗有效量的救助cart细胞,和随后在复发性或难治性癌细胞生长情况下向受试者施用可二聚救助受体和桥接因子。
在某些实施例中,使用细胞治疗处于罹患癌症的风险下的患者。因此,特定实施例包含治疗或预防或改善癌症的至少一种症状,其包含向有需要的患者施用治疗有效量的救助cart细胞,和随后在复发性或难治性癌细胞生长情况下向受试者施用与桥接因子结合的可二聚救助受体。
在特定实施例中,治疗处于罹患癌症风险下的患者的方法包含向有需要的患者施用治疗有效量的救助cart细胞,和随后在复发性或难治性癌细胞生长情况下诱导可二聚救助受体的表达以及向受试者施用桥接因子。
在一个实施例中,治疗有需要的受试者中的癌症的方法包含施用有效量的救助cart细胞,和随后在复发性或难治性癌细胞生长情况下向受试者施用可二聚救助受体和桥接因子。
在一个实施例中,治疗有需要的受试者中的癌症的方法包含施用有效量的救助cart细胞,和随后在复发性或难治性癌细胞生长情况下向受试者施用与桥接因子结合的可二聚救助受体。
在一个实施例中,治疗有需要的受试者中的癌症的方法包含向有需要的患者施用治疗有效量的救助cart细胞,和随后在复发性或难治性癌细胞生长情况下诱导可二聚救助受体的表达以及向受试者施用桥接因子。
施用的数量和频率由例如患者的病况以及患者疾病的类型和严重程度的因素决定,但适当剂量可以通过临床试验确定。
在一个实施例中,向受试者施用的组合物中的免疫效应细胞(例如t细胞)的量为至少0.1×105个细胞、至少0.5×105个细胞、至少1×105个细胞、至少5×105个细胞、至少1×106个细胞、至少0.5×107个细胞、至少1×107个细胞、至少0.5×108个细胞、至少1×108个细胞、至少0.5×109个细胞、至少1×109个细胞、至少2×109个细胞、至少3×109个细胞、至少4×109个细胞、至少5×109个细胞、或至少1×1010个细胞。
在特定实施例中,向受试者施用约1×107t个细胞到约1×109t个细胞、约2×107t个细胞到约0.9×109t个细胞、约3×107t个细胞到约0.8×109t个细胞、约4×107t个细胞到约0.7×109t个细胞、约5×107t个细胞到约0.6×109t个细胞、或约5×107t个细胞到约0.5×109t个细胞。
在一个实施例中,向受试者施用的组合物中的免疫效应细胞(例如t细胞)的量为至少0.1×104个细胞/千克体重、至少0.5×104个细胞/千克体重、至少1×104个细胞/千克体重、至少5×104个细胞/千克体重、至少1×105个细胞/千克体重、至少0.5×106个细胞/千克体重、至少1×106个细胞/千克体重、至少0.5×107个细胞/千克体重、至少1×107个细胞/千克体重、至少0.5×108个细胞/千克体重、至少1×108个细胞/千克体重、至少2×108个细胞/千克体重、至少3×108个细胞/千克体重、至少4×108个细胞/千克体重、至少5×108个细胞/千克体重、or至少1×109个细胞/千克体重。
在特定实施例中,向受试者施用约1×106t个细胞/千克体重到约1×108t个细胞/千克体重、约2×106t个细胞/千克体重到约0.9×108t个细胞/千克体重、约3×106t个细胞/千克体重到约0.8×108t个细胞/千克体重、约4×106t个细胞/千克体重到约0.7×108t个细胞/千克体重、约5×106t个细胞/千克体重到约0.6×108t个细胞/千克体重、或约5×106t个细胞/千克体重到约0.5×108t个细胞/千克体重。
所属领域的普通技术人员将认识到,可能需要多次施用特定实施例中所涵盖的组合物以实现所需疗法。举例来说,组合物可以历经1周、2周、3周、1个月、2个月、3个月、4个月、5个月、6个月、1年、2年、5年、10年或更久的时间间隔施用1、2、3、4、5、6、7、8、9或10次或更多次。
在某些实施例中,可能需要向受试者施用经活化t细胞且随后相继地再抽取血液(或进行析离术),活化其中的t细胞,并用这些经活化和扩增的t细胞再输注患者。此过程可以每隔数周执行多次。在某些实施例中,可以活化10cc到400cc的抽血中的t细胞。在某些实施例中,活化20cc、30cc、40cc、50cc、60cc、70cc、80cc、90cc、100cc、150cc、200cc、250cc、300cc、350cc或400cc或更多的抽血中的t细胞。不受理论束缚,使用此多次抽血/多次再输注方案可以用以选出某些t细胞群体。
特定实施例中所涵盖的组合物的施用可以按任何适宜方式执行,包括通过气溶胶吸入、注射、摄入、输注、植入或移植。在一优选实施例中,经鼻、经口、肠内或肠胃外施用组合物。如本文所用,短语“肠胃外施用(parenteraladministration/administeredparenterally)”是指除经肠和局部施用以外的施用模式,通常通过注射并且包括但不限于血管内、静脉内、肌肉内、动脉内、鞘内、囊内、眶内、瘤内、心内、皮内、腹膜内、经气管、皮下、表皮下、关节内、囊下、蛛网膜下、脊椎内和胸骨内注射和输注。在一个实施例中,本文所涵盖的组合物通过直接注射到肿瘤、淋巴结或感染位点中来向受试者施用。
在一个实施例中,向有需要的个体施用有效量的组合物以增加对受试者中癌症的细胞免疫应答。免疫应答可以包括由能够杀灭受感染细胞的细胞毒性t细胞、调节t细胞和辅助t细胞应答介导的细胞免疫应答。主要由能够活化b细胞、因此导致抗体产生的辅助t细胞介导的体液免疫应答还可以是诱导性的。多种技术可用于分析组合物诱导的免疫应答的类型,所述技术充分描述于所属领域中;例如《免疫学最新方案(currentprotocolsinimmunology)》,johne.coligan,adam.kruisbeek,davidh.margulies,ethanm.shevach,warrenstrober编(2001)johnwiley&sons,纽约,纽约州。
在一个实施例中,治疗诊断患有癌症的受试者的方法包含从受试者移出免疫效应细胞,修饰免疫效应细胞和制备经修饰免疫效应细胞的群体,以及向同一受试者施用经修饰免疫效应细胞的群体。在一优选实施例中,免疫效应细胞包含t细胞。
施用特定实施例中所涵盖的细胞组合物的方法包括可有效实现离体经修饰免疫效应细胞的再引入或引入受试者中后分化成成熟免疫效应细胞的免疫效应细胞的祖细胞的再引入的任何方法。一种方法包含修饰离体外周血液t细胞且将经修饰细胞返回受试者中。
本说明书中所引用的所有公开、专利申请和授权专利都以引用的方式并入本文中,其引用的程度如同每个个别公开、专利申请或授权专利经特定并且独立地指示以引用的方式并入一般。
尽管已经出于清楚理解的目的通过说明和实例相当详细地描述了前述实施例,但根据本文中所涵盖的传授内容,所属领域的普通技术人员将容易地显而易见,可以在不脱离所附权利要求书的精神或范围的情况下对其作出某些改变和修改。提供以下实例仅作为说明并且不具有限制性。本领域的技术人员将容易识别出多种可以被改变或修改以产生基本类似结果的非关键参数。
实例
实例1
救助car系统
功能性救助car系统使用可二聚抗cd19救助受体和桥接因子ap21967将抗bcma救助car再导引至cd19阳性、bcma阴性nalm-6细胞系。
对照抗bcmacar包含cd8α衍生的信号肽、抗bcmascfv、cd8α衍生的铰链区和跨膜域、胞内4-1bb共刺激域以及cd3ζ信号传导域(图1,左图,seqidno.1)。抗bcma救助car包含cd8α衍生的信号肽、抗bcmascfv、g4s连接子序列、frb变异体(t82l)、cd8α衍生的铰链区和跨膜域、胞内4-1bb共刺激域以及cd3ζ信号传导域(图1,中央图,seqidno.2)。可二聚救助受体包含igk衍生的信号肽、flag标签、抗cd19scfv和fkbp12域(seqidno:3)。此实验中所用的多肽是还含有t2a.1序列和mcherry荧光蛋白的多聚蛋白(seqidno:4)。将所有构建体克隆至慢病毒载体;使用已建立的方案制备慢病毒。参见例如kutner等人,《bmc生物技术(bmcbiotechnol.)》2009;9:10.doi:10.1186/1472-6750-9-10;kutner等人.《自然协议(nat.protoc.)》2009;4(4):495-505.doi:10.1038/nprot.2009.22。
二聚域的存在不影响car功能
在第0天用可溶性抗cd3和抗cd28抗体(50ng/ml)活化人类pbmc(1×106个细胞/毫升)。在24hr培育之后,用编码抗bcmacar或抗bcma救助car的慢病毒转导1×106个细胞。在第3天洗涤已转导细胞且在0.3×106个细胞/毫升生长介质中再悬浮。用每隔一天更换的含有il-2(250iu/ml)的培养基培养cart细胞7天。
抗bcmacart细胞和抗bcma救助cart细胞的细胞毒性潜能通过以5:1的e:t比值共同培养10天cart细胞(e,效应细胞)与k562-bcma阳性细胞(gfp阳性)(t,靶细胞)和k562-bcma阴性细胞(bfp阳性)的50:50混合物24小时来分析。在具有或不具有20nmap21967(非免疫抑制性雷帕霉素类似物)下共同培养细胞。k562-bcma阳性细胞与k562-bcma阴性细胞的比值是cart细胞细胞毒性的直接读数。抗bcmacart细胞与抗bcma救助cart细胞之间的bcma特异性细胞毒性不存在显著差异(图2a)。ap21967也对细胞毒性无影响。
抗原依赖性细胞因子分泌通过以1:1的e:t比值将10天cart细胞与k562-bcma阳性细胞共同培养24小时(具有或不具有ap21967)来分析。收集培养上清液且使用ifnγelisa试剂盒(ebiosciences)分析ifnγ产量。在抗bcmacart细胞与抗bcma救助cart细胞之间观测到相似的ifnγ分泌水平(图2b)。ap21967不显著影响细胞毒性。
在抗cd19救助受体和ap21967存在下可以将抗bcma救助cart细胞重导引到表达cd19的nalm-6细胞
用编码可二聚抗cd19救助受体的慢病毒转导293t细胞以产生分泌的抗cd19-scfv-fkbp12蛋白质的稳定来源(图1,右图)。从稳定的293t-710细胞收集含有可溶性抗cd19救助受体多肽(抗cd19scfvfkbp12)的上清液且将其过滤。
在ap21967存在下抗cd19救助受体形成含抗bcma救助car的杂二聚体(图3a)。抗bcma救助cart细胞(e)对bcma阴性、cd19阳性nalm-6细胞(t)的细胞毒性潜能通过以2:1的e:t比值共同培养cart细胞与nalm-6-cd19阳性细胞(gfp阳性)和k562-cd19阴性细胞(bfp阳性)的50:50混合物24小时来分析。用媒剂或100nmap21967并用不同体积的293t-710细胞上清液(0μl、10μl或30μl)处理共同培养物。抗bcma救助cart细胞在ap21967和293t-710细胞上清液两者存在下展示对nalm-6细胞的cd19特异性细胞毒性。图3b。
抗原依赖性细胞因子分泌通过以1:1的e:t比值共同培养抗bcma救助cart细胞与cd19阳性nalm-6细胞24小时来分析。用媒剂或100μl293t-710细胞上清液并用100nmap21967处理共同培养物。收集培养上清液且使用ifnγelisa试剂盒(ebiosciences)分析ifnγ分泌。在100μl293t-710细胞上清液和100nmap21967存在下抗bcma救助car共同培养物中的ifnγ分泌显著增加。图3c。
实例2
预装载可二聚抗cd19救助受体
使用编码可二聚抗cd19救助受体的慢病毒产生表达可二聚抗cd19救助受体的稳定的293t细胞系(293t-707),所述可二聚抗cd19救助受体包含人类脂质运载蛋白-2衍生的信号肽、scfv靶向cd19抗原、fkbp12域、t2a.1序列、mcherry序列和土拔鼠转录后调节区(wpre)(seqidno:5)。
通过收集和过滤(0.22μm过滤器)500ml293t-707细胞培养上清液以及结合于fkbp12特异性亲和层析柱来纯化可二聚抗cd19救助受体。通过在恒定旋转下将2ml中性抗生物素蛋白琼脂糖(neutravidinagarose)(赛默飞世尔)与400μg生物素-fk506于室温下培育30min来生成管柱。用pbs洗涤管柱以移除非偶合生物素-fk506。通过重力使过滤的293t-707上清液穿过管柱。用pbs洗涤管柱直到流过的a280约为0。可二聚抗cd19救助受体用5ml8μm雷帕霉素之后15mlpbs溶离(图4a)。使用vivaspin-20离心浓缩机(10kdmwco)浓缩(100x)溶离的蛋白质。将浓缩的蛋白质部分再稀释于20mlpbs中,之后为另一轮的vivaspin-20浓缩。用zebaspin7k管柱(赛默飞世尔)将蛋白质部分脱盐到pbs以移除残余的非结合雷帕霉素。纯化的蛋白质溶液经过滤器(0.22μm)灭菌且存储在4℃下。利用兔抗fkbp12抗体使用sdspage和西方墨点法分析来分析经纯化可二聚抗cd19救助受体的结合雷帕霉素的存在。
这些分析证实纯化的可二聚抗cd19救助受体与雷帕霉素结合(图4b)。
实例3
预装载可二聚抗cd19救助受体重导引抗bcma救助car
用编码抗bcmacar或抗bcma救助car的慢病毒载体转导t细胞。在250ng预装载可二聚抗cd19救助受体存在或不存在下,在具有或不具有100nmap21967下,以2:1e:t比值将cart细胞与表达gfp的cd19阳性nalm-6细胞和表达bfp的cd19阴性k562细胞的50:50混合物共同培养24hr。抗bcma救助cart细胞在预装载有雷帕霉素的可二聚抗cd19救助受体存在下展示对nalm-6的cd19特异性细胞毒性。图5。不需要ap21967触发cd19特异性细胞毒性。
以2:1e:t比值在减少量(125ng、62.5ng、31.3ng、15.6ng、7.8ng、3.9ng、2.0ng)的预装载可二聚抗cd19救助受体下将抗bcma救助cart细胞与表达gfp的cd19阳性nalm-6细胞和表达bfp的cd19阴性k562细胞的50:50混合物共同培养24hr。少至2ng的预装载可二聚抗cd19救助受体就足以诱导cd19特异性细胞毒性。图6。
抗bcma救助cart细胞或未转导的t细胞与cd19阳性nalm-6细胞以1:1e:t比值在减少量(125ng、62.5ng、31.3ng、15.6ng、7.8ng、3.9ng、2.0ng)的预装载可二聚抗cd19救助受体下共同培养24hr。对共同培养物上清液进行的细胞因子释放分析证实制得il-2、il-4、il-17a、tnf和ifnγ且所制备细胞因子的量与共同培养物中的预装载可二聚抗cd19救助受体的量相关。图7。
实例4
抗cd19救助受体重导引抗bcmatdaric细胞
设计、构建和检验包含可操作地连接于编码抗bcmadaric的多核苷酸序列的mnd启动子的慢病毒。bcmadaric包含cd8α衍生的信号肽、frb变异体(t82l)、cd8α衍生的跨膜域、胞内4-1bb共刺激域、cd3ζ信号传导域、p2a序列、igκ衍生的信号肽、靶向bcma抗原的单链可变片段(scfv)、g4s连接子序列、fkbp12域和无羊膜(amn)衍生的跨膜域(seqidno:6)。
评估用抗cd19救助受体将抗bcmatdaric细胞重导引于表达cd19的nalm-6细胞的能力。在存在或不存在250ng抗cd19救助受体下以2:1的效应子:标靶(e:t)比值共同培养抗bcma-darict细胞与cd19+nalm-6(gfp)和k562(bfp)靶细胞的50:50混合物。抗cd19救助受体能够将抗bcmatdaric细胞的细胞毒性重导引于cd19+nalm-6细胞。图8b。还进行细胞因子释放分析。在存在或不存在250ng抗cd19救助受体下以1:1e:t比值共同培养抗bcmatdaric细胞与nalm-6细胞24小时。ifnγ仅由含有抗cd19救助受体的共同培养物产生。图8c。
总体而言,在以下权利要求书中,所使用的术语不应理解为将权利要求书限制于本说明书和权利要求书中所公开的具体实施例,但应理解为包括所有可能的实施例以及这份权利要求书所有权获得的等效物的全部范围。因此,权利要求书不受本公开限制。
序列表
<110>蓝鸟生物公司(bluebirdbio,inc.)
梁炜亨(leung,wai-hang)
<120>救助嵌合抗原受体系统
<130>blbd-068/02wo
<150>us62/356,335
<151>2016-06-29
<150>us62/322,634
<151>2016-04-14
<160>47
<170>patentinversion3.5
<210>1
<211>493
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>用于抗bcma嵌合抗原受体的多肽序列
<400>1
metalaleuprovalthralaleuleuleuproleualaleuleuleu
151015
hisalaalaargproaspilevalleuthrglnserproproserleu
202530
alametserleuglylysargalathrilesercysargalaserglu
354045
servalthrileleuglyserhisleuilehistrptyrglnglnlys
505560
proglyglnproprothrleuleuileglnleualaserasnvalgln
65707580
thrglyvalproalaargpheserglyserglyserargthraspphe
859095
thrleuthrileaspprovalglugluaspaspvalalavaltyrtyr
100105110
cysleuglnserargthrileproargthrpheglyglyglythrlys
115120125
leugluilelysglyserthrserglyserglylysproglysergly
130135140
gluglyserthrlysglyglnileglnleuvalglnserglyproglu
145150155160
leulyslysproglygluthrvallysilesercyslysalasergly
165170175
tyrthrphethrasptyrserileasntrpvallysargalaprogly
180185190
lysglyleulystrpmetglytrpileasnthrgluthrargglupro
195200205
alatyralatyrasppheargglyargphealapheserleugluthr
210215220
seralaserthralatyrleuglnileasnasnleulystyrgluasp
225230235240
thralathrtyrphecysalaleuasptyrsertyralametasptyr
245250255
trpglyglnglythrservalthrvalserseralaalaalathrthr
260265270
thrproalaproargproprothrproalaprothrilealasergln
275280285
proleuserleuargproglualacysargproalaalaglyglyala
290295300
valhisthrargglyleuaspphealacysaspiletyriletrpala
305310315320
proleualaglythrcysglyvalleuleuleuserleuvalilethr
325330335
leutyrcyslysargglyarglyslysleuleutyrilephelysgln
340345350
prophemetargprovalglnthrthrglnglugluaspglycysser
355360365
cysargpheproglugluglugluglyglycysgluleuargvallys
370375380
pheserargseralaaspalaproalatyrglnglnglyglnasngln
385390395400
leutyrasngluleuasnleuglyargarggluglutyraspvalleu
405410415
asplysargargglyargaspproglumetglyglylysproargarg
420425430
lysasnproglngluglyleutyrasngluleuglnlysasplysmet
435440445
alaglualatyrsergluileglymetlysglygluargargarggly
450455460
lysglyhisaspglyleutyrglnglyleuserthralathrlysasp
465470475480
thrtyraspalaleuhismetglnalaleuproproarg
485490
<210>2
<211>594
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>用于包含多聚化域的抗bcma嵌合抗原受体的多肽序列
<400>2
metalaleuprovalthralaleuleuleuproleualaleuleuleu
151015
hisalaalaargproaspilevalleuthrglnserproproserleu
202530
alametserleuglylysargalathrilesercysargalaserglu
354045
servalthrileleuglyserhisleuilehistrptyrglnglnlys
505560
proglyglnproprothrleuleuileglnleualaserasnvalgln
65707580
thrglyvalproalaargpheserglyserglyserargthraspphe
859095
thrleuthrileaspprovalglugluaspaspvalalavaltyrtyr
100105110
cysleuglnserargthrileproargthrpheglyglyglythrlys
115120125
leugluilelysglyserthrserglyserglylysproglysergly
130135140
gluglyserthrlysglyglnileglnleuvalglnserglyproglu
145150155160
leulyslysproglygluthrvallysilesercyslysalasergly
165170175
tyrthrphethrasptyrserileasntrpvallysargalaprogly
180185190
lysglyleulystrpmetglytrpileasnthrgluthrargglupro
195200205
alatyralatyrasppheargglyargphealapheserleugluthr
210215220
seralaserthralatyrleuglnileasnasnleulystyrgluasp
225230235240
thralathrtyrphecysalaleuasptyrsertyralametasptyr
245250255
trpglyglnglythrservalthrvalserserglyproglyglygly
260265270
glyserileleutrphisglumettrphisgluglyleuglugluala
275280285
serargleutyrpheglygluargasnvallysglymetphegluval
290295300
leugluproleuhisalametmetgluargglyproglnthrleulys
305310315320
gluthrserpheasnglnalatyrglyargaspleumetglualagln
325330335
glutrpcysarglystyrmetlysserglyasnvallysaspleuleu
340345350
glnalatrpaspleutyrtyrhisvalpheargargileserlysala
355360365
seralalysprothrthrthrproalaproargproprothrproala
370375380
prothrilealaserglnproleuserleuargproglualacysarg
385390395400
proalaalaglyglyalavalhisthrargglyleuaspphealacys
405410415
aspiletyriletrpalaproleualaglythrcysglyvalleuleu
420425430
leuserleuvalilethrmethislysargglyarglyslysleuleu
435440445
tyrilephelysglnprophemetargprovalglnthrthrglnglu
450455460
gluaspglycyssercysargpheproglugluglugluglyglycys
465470475480
gluleuargvallyspheserargseralaaspalaproalatyrgln
485490495
glnglyglnasnglnleutyrasngluleuasnleuglyargargglu
500505510
glutyraspvalleuasplysargargglyargaspproglumetgly
515520525
glylysproargarglysasnproglngluglyleutyrasngluleu
530535540
glnlysasplysmetalaglualatyrsergluileglymetlysgly
545550555560
gluargargargglylysglyhisaspglyleutyrglnglyleuser
565570575
thralathrlysaspthrtyraspalaleuhismetglnalaleupro
580585590
proarg
<210>3
<211>387
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>用于具有t2amcherry的可二聚抗cd19救助受体的多肽序列
<400>3
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglyasptyrlysaspgluglyseraspileglnmetthr
202530
glnthrthrserserleuseralaserleuglyaspargvalthrile
354045
sercysargalaserglnaspileserlystyrleuasntrptyrgln
505560
glnlysproaspglythrvallysleuleuiletyrhisthrserarg
65707580
leuhisserglyvalproserargpheserglyserglyserglythr
859095
asptyrserleuthrileserasnleugluglngluaspilealathr
100105110
tyrphecysglnglnglyasnthrleuprotyrthrpheglyglygly
115120125
thrlysleugluilethrglyserthrserglyserglylysprogly
130135140
serglygluglyserthrlysglygluvallysleuglnglusergly
145150155160
proglyleuvalalaproserglnserleuservalthrcysthrval
165170175
serglyvalserleuproasptyrglyvalsertrpileargglnpro
180185190
proarglysglyleuglutrpleuglyvaliletrpglysergluthr
195200205
thrtyrtyrasnseralaleulysserargleuthrileilelysasp
210215220
asnserlysserglnvalpheleulysmetasnserleuglnthrasp
225230235240
aspthralailetyrtyrcysalalyshistyrtyrtyrglyglyser
245250255
tyralametasptyrtrpglyglnglythrservalthrvalserser
260265270
alaserglyserglyglyvalglnvalgluthrileserproglyasp
275280285
glyargthrpheprolysargglyglnthrcysvalvalhistyrthr
290295300
glymetleugluaspglylyslyspheaspserserargaspargasn
305310315320
lysprophelysphemetleuglylysglngluvalileargglytrp
325330335
glugluglyvalalaglnmetservalglyglnargalalysleuthr
340345350
ileserproasptyralatyrglyalathrglyhisproglyileile
355360365
proprohisalathrleuvalpheaspvalgluleuleulysleuglu
370375380
glyglyarg
385
<210>4
<211>644
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>用于具有t2amcherry的可二聚抗cd19救助受体的多肽序列
<400>4
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglyasptyrlysaspgluglyseraspileglnmetthr
202530
glnthrthrserserleuseralaserleuglyaspargvalthrile
354045
sercysargalaserglnaspileserlystyrleuasntrptyrgln
505560
glnlysproaspglythrvallysleuleuiletyrhisthrserarg
65707580
leuhisserglyvalproserargpheserglyserglyserglythr
859095
asptyrserleuthrileserasnleugluglngluaspilealathr
100105110
tyrphecysglnglnglyasnthrleuprotyrthrpheglyglygly
115120125
thrlysleugluilethrglyserthrserglyserglylysprogly
130135140
serglygluglyserthrlysglygluvallysleuglnglusergly
145150155160
proglyleuvalalaproserglnserleuservalthrcysthrval
165170175
serglyvalserleuproasptyrglyvalsertrpileargglnpro
180185190
proarglysglyleuglutrpleuglyvaliletrpglysergluthr
195200205
thrtyrtyrasnseralaleulysserargleuthrileilelysasp
210215220
asnserlysserglnvalpheleulysmetasnserleuglnthrasp
225230235240
aspthralailetyrtyrcysalalyshistyrtyrtyrglyglyser
245250255
tyralametasptyrtrpglyglnglythrservalthrvalserser
260265270
alaserglyserglyglyvalglnvalgluthrileserproglyasp
275280285
glyargthrpheprolysargglyglnthrcysvalvalhistyrthr
290295300
glymetleugluaspglylyslyspheaspserserargaspargasn
305310315320
lysprophelysphemetleuglylysglngluvalileargglytrp
325330335
glugluglyvalalaglnmetservalglyglnargalalysleuthr
340345350
ileserproasptyralatyrglyalathrglyhisproglyileile
355360365
proprohisalathrleuvalpheaspvalgluleuleulysleuglu
370375380
glyglyargserglygluglyargglyserleuleuthrcysglyasp
385390395400
valglugluasnproglyproserargvalserlysglyglugluasp
405410415
asnmetalaileilelysgluphemetargphelysvalhismetglu
420425430
glyservalasnglyhisgluphegluilegluglygluglyglugly
435440445
argprotyrgluglythrglnthralalysleulysvalthrlysgly
450455460
glyproleuprophealatrpaspileleuserproglnphemettyr
465470475480
glyserlysalatyrvallyshisproalaaspileproasptyrleu
485490495
lysleuserpheprogluglyphelystrpgluargvalmetasnphe
500505510
gluaspglyglyvalvalthrvalthrglnaspserserleuglnasp
515520525
glyglupheiletyrlysvallysleuargglythrasnpheproser
530535540
aspglyprovalmetglnlyslysthrmetglytrpglualaserser
545550555560
gluargmettyrprogluaspglyalaleulysglygluilelysgln
565570575
argleulysleulysaspglyglyhistyraspalagluvallysthr
580585590
thrtyrlysalalyslysprovalglnleuproglyalatyrasnval
595600605
asnilelysleuaspilethrserhisasngluasptyrthrileval
610615620
gluglntyrgluargalagluglyarghisserthrglyglymetasp
625630635640
gluleutyrlys
<210>5
<211>641
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>用于具有t2amcherry的可二聚抗cd19救助受体的多肽序列
<400>5
metproleuglyleuleutrpleuglyleualaleuleuglyalaleu
151015
hisalaglnalaglyseraspileglnmetthrglnthrthrserser
202530
leuseralaserleuglyaspargvalthrilesercysargalaser
354045
glnaspileserlystyrleuasntrptyrglnglnlysproaspgly
505560
thrvallysleuleuiletyrhisthrserargleuhisserglyval
65707580
proserargpheserglyserglyserglythrasptyrserleuthr
859095
ileserasnleugluglngluaspilealathrtyrphecysglngln
100105110
glyasnthrleuprotyrthrpheglyglyglythrlysleugluile
115120125
thrglyserthrserglyserglylysproglyserglygluglyser
130135140
thrlysglygluvallysleuglngluserglyproglyleuvalala
145150155160
proserglnserleuservalthrcysthrvalserglyvalserleu
165170175
proasptyrglyvalsertrpileargglnproproarglysglyleu
180185190
glutrpleuglyvaliletrpglysergluthrthrtyrtyrasnser
195200205
alaleulysserargleuthrileilelysaspasnserlyssergln
210215220
valpheleulysmetasnserleuglnthraspaspthralailetyr
225230235240
tyrcysalalyshistyrtyrtyrglyglysertyralametasptyr
245250255
trpglyglnglythrservalthrvalserseralaserglyglygly
260265270
glyserglyvalglnvalgluthrileserproglyaspglyargthr
275280285
pheprolysargglyglnthrcysvalvalhistyrthrglymetleu
290295300
gluaspglylyslyspheaspserserargaspargasnlysprophe
305310315320
lysphemetleuglylysglngluvalileargglytrpgluglugly
325330335
valalaglnmetservalglyglnargalalysleuthrileserpro
340345350
asptyralatyrglyalathrglyhisproglyileileproprohis
355360365
alathrleuvalpheaspvalgluleuleulysleugluglyglyarg
370375380
serglygluglyargglyserleuleuthrcysglyaspvalgluglu
385390395400
asnproglyproserargvalserlysglyglugluaspasnmetala
405410415
ileilelysgluphemetargphelysvalhismetgluglyserval
420425430
asnglyhisgluphegluilegluglygluglygluglyargprotyr
435440445
gluglythrglnthralalysleulysvalthrlysglyglyproleu
450455460
prophealatrpaspileleuserproglnphemettyrglyserlys
465470475480
alatyrvallyshisproalaaspileproasptyrleulysleuser
485490495
pheprogluglyphelystrpgluargvalmetasnphegluaspgly
500505510
glyvalvalthrvalthrglnaspserserleuglnaspglygluphe
515520525
iletyrlysvallysleuargglythrasnpheproseraspglypro
530535540
valmetglnlyslysthrmetglytrpglualasersergluargmet
545550555560
tyrprogluaspglyalaleulysglygluilelysglnargleulys
565570575
leulysaspglyglyhistyraspalagluvallysthrthrtyrlys
580585590
alalyslysprovalglnleuproglyalatyrasnvalasnilelys
595600605
leuaspilethrserhisasngluasptyrthrilevalgluglntyr
610615620
gluargalagluglyarghisserthrglyglymetaspgluleutyr
625630635640
lys
<210>6
<211>739
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>用于抗bcmadaric的多肽序列
<400>6
metalaleuprovalthralaleuleuleuproleualaleuleuleu
151015
hisalaalaargproglyserileleutrphisglumettrphisglu
202530
glyleugluglualaserargleutyrpheglygluargasnvallys
354045
glymetphegluvalleugluproleuhisalametmetgluarggly
505560
proglnthrleulysgluthrserpheasnglnalatyrglyargasp
65707580
leumetglualaglnglutrpcysarglystyrmetlysserglyasn
859095
vallysaspleuleuglnalatrpaspleutyrtyrhisvalphearg
100105110
argileserlysalaseralaglythrglyseraspiletyriletrp
115120125
alaproleualaglythrcysglyvalleuleuleuserleuvalile
130135140
thrmethislysargglyarglyslysleuleutyrilephelysgln
145150155160
prophemetargprovalglnthrthrglnglugluaspglycysser
165170175
cysargpheproglugluglugluglyglycysgluleuargvallys
180185190
pheserargseralaaspalaproalatyrglnglnglyglnasngln
195200205
leutyrasngluleuasnleuglyargarggluglutyraspvalleu
210215220
asplysargargglyargaspproglumetglyglylysproargarg
225230235240
lysasnproglngluglyleutyrasngluleuglnlysasplysmet
245250255
alaglualatyrsergluileglymetlysglygluargargarggly
260265270
lysglyhisaspglyleutyrglnglyleuserthralathrlysasp
275280285
thrtyraspalaleuhismetglnalaleuproproargserglyser
290295300
glyalathrasnpheserleuleulysglnalaglyaspvalgluglu
305310315320
asnproglyprosermetgluthraspthrleuleuleutrpvalleu
325330335
leuleutrpvalproglyserthrglyaspilevalleuthrglnser
340345350
proproserleualametserleuglylysargalathrilesercys
355360365
argalasergluservalthrileleuglyserhisleuilehistrp
370375380
tyrglnglnlysproglyglnproprothrleuleuileglnleuala
385390395400
serasnvalglnthrglyvalproalaargpheserglyserglyser
405410415
argthraspphethrleuthrileaspprovalglugluaspaspval
420425430
alavaltyrtyrcysleuglnserargthrileproargthrphegly
435440445
glyglythrlysleugluilelysglyserthrserglyserglylys
450455460
proglyserglygluglyserthrlysglyglnileglnleuvalgln
465470475480
serglyprogluleulyslysproglygluthrvallysilesercys
485490495
lysalaserglytyrthrphethrasptyrserileasntrpvallys
500505510
argalaproglylysglyleulystrpmetglytrpileasnthrglu
515520525
thrarggluproalatyralatyrasppheargglyargphealaphe
530535540
serleugluthrseralaserthralatyrleuglnileasnasnleu
545550555560
lystyrgluaspthralathrtyrphecysalaleuasptyrsertyr
565570575
alametasptyrtrpglyglnglythrservalthrvalserserpro
580585590
argglyglyglyglyserglyvalglnvalgluthrileserprogly
595600605
aspglyargthrpheprolysargglyglnthrcysvalvalhistyr
610615620
thrglymetleugluaspglylyslyspheaspserserargasparg
625630635640
asnlysprophelysphemetleuglylysglngluvalilearggly
645650655
trpglugluglyvalalaglnmetservalglyglnargalalysleu
660665670
thrileserproasptyralatyrglyalathrglyhisproglyile
675680685
ileproprohisalathrleuvalpheaspvalgluleuleulysleu
690695700
gluglyglyargvaltrpglyserseralaalaglyleualaglygly
705710715720
valalaalaalavalleuleualaleuleuvalleuleuvalalapro
725730735
proleuleu
<210>7
<211>5
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>7
aspglyglyglyser
15
<210>8
<211>5
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>8
thrglyglulyspro
15
<210>9
<211>4
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>9
glyglyargarg
1
<210>10
<211>5
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>10
glyglyglyglyser
15
<210>11
<211>14
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>11
gluglylysserserglyserglysergluserlysvalasp
1510
<210>12
<211>18
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>12
lysgluserglyservalsersergluglnleualaglnpheargser
151015
leuasp
<210>13
<211>8
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>13
glyglyargargglyglyglyser
15
<210>14
<211>9
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>14
leuargglnargaspglygluargpro
15
<210>15
<211>12
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>15
leuargglnlysaspglyglyglysergluargpro
1510
<210>16
<211>16
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>16
leuargglnlysaspglyglyglyserglyglyglysergluargpro
151015
<210>17
<211>18
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>示例性连接子序列
<400>17
glyserthrserglyserglylysproglyserglygluglyserthr
151015
lysgly
<210>18
<211>7
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>通过tev蛋白酶获得的裂解序列
<220>
<221>site
<222>(2)..(3)
<223>xaa是任何氨基酸
<220>
<221>site
<222>(5)..(5)
<223>xaa是任何氨基酸
<220>
<221>site
<222>(7)..(7)
<223>xaa=gly或ser
<400>18
gluxaaxaatyrxaaglnxaa
15
<210>19
<211>7
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>通过tev蛋白酶获得的裂解序列
<400>19
gluasnleutyrpheglngly
15
<210>20
<211>7
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>通过tev蛋白酶获得的裂解序列
<400>20
gluasnleutyrpheglnser
15
<210>21
<211>22
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>21
glyserglyalathrasnpheserleuleulysglnalaglyaspval
151015
glugluasnproglypro
20
<210>22
<211>19
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>22
alathrasnpheserleuleulysglnalaglyaspvalglugluasn
151015
proglypro
<210>23
<211>14
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>23
leuleulysglnalaglyaspvalglugluasnproglypro
1510
<210>24
<211>21
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>24
glyserglygluglyargglyserleuleuthrcysglyaspvalglu
151015
gluasnproglypro
20
<210>25
<211>18
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>25
gluglyargglyserleuleuthrcysglyaspvalglugluasnpro
151015
glypro
<210>26
<211>13
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>26
leuleuthrcysglyaspvalglugluasnproglypro
1510
<210>27
<211>23
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>27
glyserglyglncysthrasntyralaleuleulysleualaglyasp
151015
valgluserasnproglypro
20
<210>28
<211>20
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>28
glncysthrasntyralaleuleulysleualaglyaspvalgluser
151015
asnproglypro
20
<210>29
<211>14
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>29
leuleulysleualaglyaspvalgluserasnproglypro
1510
<210>30
<211>25
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>30
glyserglyvallysglnthrleuasnpheaspleuleulysleuala
151015
glyaspvalgluserasnproglypro
2025
<210>31
<211>22
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>31
vallysglnthrleuasnpheaspleuleulysleualaglyaspval
151015
gluserasnproglypro
20
<210>32
<211>14
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>32
leuleulysleualaglyaspvalgluserasnproglypro
1510
<210>33
<211>19
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>33
leuleuasnpheaspleuleulysleualaglyaspvalgluserasn
151015
proglypro
<210>34
<211>19
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>34
thrleuasnpheaspleuleulysleualaglyaspvalgluserasn
151015
proglypro
<210>35
<211>14
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>35
leuleulysleualaglyaspvalgluserasnproglypro
1510
<210>36
<211>17
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>36
asnpheaspleuleulysleualaglyaspvalgluserasnprogly
151015
pro
<210>37
<211>20
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>37
glnleuleuasnpheaspleuleulysleualaglyaspvalgluser
151015
asnproglypro
20
<210>38
<211>24
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>38
alaprovallysglnthrleuasnpheaspleuleulysleualagly
151015
aspvalgluserasnproglypro
20
<210>39
<211>40
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>39
valthrgluleuleutyrargmetlysargalagluthrtyrcyspro
151015
argproleuleualailehisprothrglualaarghislysglnlys
202530
ilevalalaprovallysglnthr
3540
<210>40
<211>18
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>40
leuasnpheaspleuleulysleualaglyaspvalgluserasnpro
151015
glypro
<210>41
<211>40
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>41
leuleualailehisprothrglualaarghislysglnlysileval
151015
alaprovallysglnthrleuasnpheaspleuleulysleualagly
202530
aspvalgluserasnproglypro
3540
<210>42
<211>33
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>包含2a位点的自我裂解多肽
<400>42
glualaarghislysglnlysilevalalaprovallysglnthrleu
151015
asnpheaspleuleulysleualaglyaspvalgluserasnprogly
202530
pro
<210>43
<211>10
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>
<223>共有kozak序列
<400>43
gccrccatgg10
<210>44
<211>4
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>用于测定轻链cdr-l3基元的示例性规则
<220>
<221>site
<222>(3)..(3)
<223>xaa是任何氨基酸
<400>44
pheglyxaagly
1
<210>45
<211>4
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>用于测定重链cdr-h1基元的示例性规则
<220>
<221>site
<222>(2)..(4)
<223>xaa是任何氨基酸
<400>45
cysxaaxaaxaa
1
<210>46
<211>5
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>用于测定重链cdr-h2基元的示例性规则
<400>46
leuglutrpilegly
15
<210>47
<211>4
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>
<223>用于测定重链cdr-h3基元的示例性规则
<220>
<221>site
<222>(3)..(3)
<223>xaa是任何氨基酸
<400>47
trpglyxaagly
1
- 还没有人留言评论。精彩留言会获得点赞!