二氢吲哚衍生物及其使用和制备方法与流程
本发明涉及下式的化合物:
其中n、r1和r2是如本文中所定义。本发明还涉及式i的化合物在治疗与纤维化病症相关的临床疾患中的用途。
背景技术:
纤维化病症影响许多器官系统,包括心脏、血管、肾、肝和肺。估计美国45%的死亡归因于以不同程度纤维化为特征的病症。这个惊人的统计数据往往被低估,因为‘死亡原因’经常是终末期器官衰竭,虽然在很多情况下器官衰竭归因于进行性纤维化。
最严重和致死的纤维化肺病是特发性肺纤维化(ipf),其特征在于肺实质的进行性瘢痕组织形成和不可逆破坏,导致气体交换异常并最终导致呼吸衰竭。ipf被广泛认为是衰老疾病,因为它不成比例地影响在诊断时平均年龄为66岁的老年人群。ipf与高发病率和死亡率相关,中位生存率低于3年。此外,ipf患者的生存率随着年龄而显著降低。
虽然最近有两种药物获得了fda批准用于ipf,但是尚没有药物治疗显示出明确改善ipf患者的生活或生存质量。当前的药物只是适度减缓肺衰退的进展。没有能够“逆转”纤维化的可用疗法。
因此,明确需要对于ipf和其他纤维化疾病的更有效治疗来改善患者的体验和结果。
技术实现要素:
本发明的一些方面基于本发明人发现,活性氧物种(ros)生成酶—nadph氧化酶(nox4)是肌成纤维细胞功能的关键媒介,并验证了它在肺纤维化动物模型中的作用。在ipf患者的肺中和ipf肺成纤维细胞中nox4表达升高。
自本发明人的这一发现以来,nox4已经牵涉包括肾、肝、皮肤和心脏在内的多种纤维化疾病。最近,本发明人开发了一种新的持续性肺纤维化老龄动物模型。该模型更准确地重演了ipf的持续本性,并提供了更为临床相关的疗效测试方案,其中可以评价已确立的纤维化的逆转。使用这种模型,本发明人已经证明,在老龄的情况下,肺损伤导致抗衰老和凋亡的肌成纤维细胞表型的获得,其妨害了纤维化消退。不受任何理论的束缚,认为这种肌成纤维细胞表型是由与nox4持续活化相关的氧化还原失衡介导的。此外,遗传/药理靶向nox4导致年龄相关的持续性纤维化逆转和存活增加。
目前,没有临床可用的选择性nox4抑制剂。本发明的一个具体方面提供高选择性的nox4抑制剂化合物。本发明的另一个方面提供使用本发明化合物治疗患有与纤维化病症相关的临床疾患的对象的方法。
附图说明
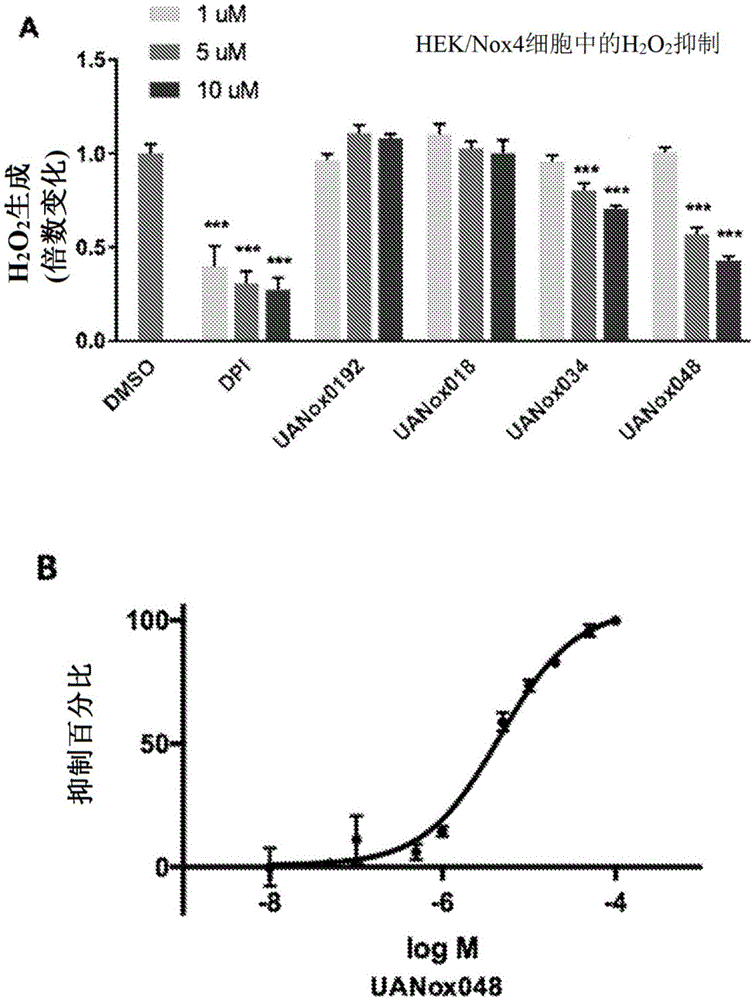
图1是显示了(a)在稳定转染为过表达nox4的hek细胞中通过amplexred试验评价的化合物的h2o2抑制;和(b)在稳定转染为过表达nox4的hek细胞中评价的uanox048的ic50的图形。
图2是显示了在用uanox048处理的稳定转染为过表达nox4的hek细胞中,通过(a)amplexred试验、(b)ros-glo试验和(c)细胞存活率评估的uanox048的h2o2清除活性的图形。
图3是显示了uanox048(a)通过amplexred试验评价的nox1选择性、(b)通过amplexred试验评价的nox2选择性、和(c)通过amplexred试验评价的黄嘌呤氧化酶选择性的图形。
图4是显示了通过amplexred试验得到的用uanox034、uanox008、uanox019和uanox048处理的人肺成纤维细胞(imr90细胞)的h2o2抑制的图形。
图5是显示了在用uanox048处理的人肺成纤维细胞(imr90细胞)中αsma的western免疫印迹(a)和光密度分析(b)的图形。
具体实施方式
定义
用于本文中时,术语“任选取代的”意指一个或多个取代基可以存在或可以不存在。另外,如本领域技术人员公知的,术语“取代基”是指非氢的基团。例如,术语“任选取代的”意指所提及的化学结构是未取代的或含有至少一个选自由下列组成的名单中的取代基:卤素,氰基,c1-6烷基,c1-6烯基,c1-6炔基,c1-6卤代烷基,-o-1-6烷基,-o-c1-6烯基,-o-c1-6炔基,-o-c1-6卤代烷基,苯基,-苯基-ome,-苯基-cf3,c1-6烷基-氟苯基,吡啶基,-o-苯基,-c1-6烷基-苯基,-o-c1-6烷基-苯基,-o-吡啶基-cf3,卤代烷基取代的-o-吡啶基,嘧啶基,-oh,-ome,-nh2,-n(h)me,-nhc(o)me,-c(o)net2,-sh,-s(o)2-哌啶基,-s(o)2-苯基-cf3,-s(o)2-苯基-ocf3,-s(o)2-氟苯基,-s(o)2nme2,-s(o)2net2和-sme。
“烷基”是指1至12个、通常1至6个碳原子的饱和直链单价烃部分,或3至12个、通常3至6个碳原子的饱和支链单价烃部分。示例性的烷基基团包括但不限于,甲基、乙基、正丙基、2-丙基、叔丁基、戊基等。
“亚烷基”是指1至12个、通常1至6个碳原子的饱和直链饱和二价烃部分,或3至12个、通常3至6个碳原子的支链饱和二价烃部分。示例性的亚烷基基团包括但不限于,亚甲基、亚乙基、亚丙基、亚丁基、亚戊基等。
“芳基”是指6至15个环原子的单价单、双或三环芳族烃部分,其任选被一个或多个取代基取代。当被取代时,芳基基团通常在环结构内被一个、两个或三个取代基取代。当芳基基团中存在两个或更多个取代基时,各取代基是独立选择的。当被取代时,芳基基团的典型取代基包括但不限于,烷基、烷氧基、卤代烷基、卤代烷氧基、杂烷基、卤代、硝基、氰基、环烷基、任选取代的苯基、任选取代的杂芳基、任选取代的杂环烷基、或任选取代的芳基。更具体地,术语芳基包括但不限于,任选取代的苯基、任选取代的1-萘基和任选取代的2-萘基等。
“芳烷基”是指式–ra1ra2的部分,其中ra1是亚烷基基团并且ra2是如本文所定义的任选取代的芳基。示例性的芳烷基基团包括但不限于,苄基、苯乙基、3-(3-氯苯基)-2-甲基戊基等。
“环烷基”是指三至十个环碳的非芳族单价单环或双环烃部分。环烷基可任选地被一个或多个取代基取代。当被取代时,环烷基通常在环结构内具有一、二或三个取代基,其中各取代基是独立选择的。环烷基也可以在环结构内包含一个或多个非芳族不饱和双键。然而,术语“饱和的”用作前缀,那么在环烷基环结构内不存在多重(例如,双重或三重)键。环烷基的合适取代基包括但不限于上文对芳基基团列出的示例性取代基。
“环烷基烷基”是指式–rb1rb2的部分,其中rb1是亚烷基基团并且rb2是如本文所定义的任选取代的环烷基基团。示例性的环烷基烷基基团包括但不限于环丙基甲基、环己基丙基、3-环己基-2-甲基丙基等。
术语“卤代”、“卤素”和“卤化物”在本文中可互换使用,并且指氟、氯、溴或碘。
“卤代烷基”是指如本文所定义的烷基基团,其中一个或多个氢原子被相同或不同的卤原子取代。术语“卤代烷基”还包括全卤化的烷基基团,其中所有烷基氢原子都被卤素原子取代。示例性的卤代烷基基团包括但不限于,-ch2cl、-cf3、-ch2cf3、-ch2ccl3等。
术语“杂芳基”是指5至12个环原子的单价单环或双环芳族部分,其含有一、二、三或四个选自n、o或s的环杂原子,其余环原子是c。杂芳基环可任选被一个或多个取代基取代。当被取代时,通常杂芳基具有一、二或三个取代基,其各自是独立选择的。杂芳基的示例性取代基包括上面对芳基基团列出的那些。示例性杂芳基基团包括但不限于,吡啶基,呋喃基,噻吩基,噻唑基,异噻唑基,三唑基,咪唑基,异噁唑基,吡咯基,吡唑基,吡嗪基,嘧啶基,苯并呋喃基,异苯并呋喃基,苯并噻唑基,苯并异噻唑基,苯并三唑基,吲哚基,异吲哚基,苯并噁唑基,喹啉基,异喹啉基,苯并咪唑基,苯并异噁唑基,苯并噻吩基,二苯并呋喃,苯并二氮杂卓-2-酮-5-基等。
术语“杂环基”和“杂环烷基”在本文中可互换使用,并且是指三至八个环原子的非芳族单环部分,其中一或两个环原子是选自n、o或s(o)n(其中n是0至2的整数)的杂原子,其余的环原子是c,其中一或两个c原子可以任选是羰基基团。杂环基环可以任选地独立被一个或多个取代基取代。当被取代时,杂环烷基通常具有一、二或三个取代基,其各自是独立选择的。杂环烷基可在环结构内包含一个或多个非芳族双键。然而,术语“饱和的”用作前缀,那么在杂环烷基环结构内不存在多重(例如,双重或三重)键。杂环烷基的合适取代基包括但不限于上文对芳基基团列出的示例性取代基。
“离去基团”具有在合成有机化学中与其常规相关的含义,即能够被亲核试剂置换的原子或基团,并包括卤素(例如氯、溴和碘)、烷烃磺酰氧基、芳烃磺酰氧基、烷基羰氧基(例如,乙酰氧基)、芳基羰氧基、甲磺酰氧基、甲苯磺酰氧基、三氟甲磺酰氧基、芳氧基(例如,2,4-二硝基苯氧基)、甲氧基、n,o-二甲基羟基氨基等。
“药学上可接受的赋形剂”是指可用于制备药物组合物的赋形剂,其一般是安全无毒的,既不是生物学上也不是其它方面不合需要的,并包括兽医用途以及人类药物用途可接受的赋形剂。
化合物的“药学上可接受的盐”是指药学上可接受的并且拥有母体化合物的期望药理学活性的盐。这样的盐包括:(1)酸加成盐,与无机酸例如盐酸、氢溴酸、硫酸、硝酸、磷酸等形成的;或与有机酸形成的,所述有机酸例如乙酸、丙酸、己酸、环戊烷丙酸、乙醇酸、丙酮酸、乳酸、丙二酸、琥珀酸、苹果酸、马来酸、富马酸、酒石酸、柠檬酸、苯甲酸、3-(4-羟基苯甲酰基)苯甲酸、肉桂酸、扁桃酸、甲磺酸、乙磺酸、1,2-乙二磺酸、2-羟基乙磺酸、苯磺酸、4-氯苯磺酸、2-萘磺酸、4-甲苯磺酸、樟脑磺酸、4-甲基双环[2.2.2]-辛-2-烯-1-羧酸、葡庚糖酸、3-苯基丙酸、三甲基乙酸、叔丁基乙酸、月桂基硫酸、葡萄糖酸、谷氨酸、羟萘甲酸、水杨酸、硬脂酸、粘康酸等;或(2)当母体化合物中存在的酸性质子被金属离子例如碱金属离子、碱土金属离子或铝离子替代或与有机碱例如乙醇胺、二乙醇胺、三乙醇胺、氨丁三醇、n-甲基葡糖胺等配位时形成的盐。
术语“前药”和“前体药物”在本文中可互换使用,并且是指当这样的前药施用于哺乳动物对象时在体内释放式i的活性母体药物的任何化合物。式i化合物的前药是通过将存在于式i化合物中的一个或多个官能团进行改性、使得所述改性可以在体内裂解以释放母体化合物而制备的。前药包含式i的化合物,其中式i化合物中的羟基、氨基或巯基基团与可在体内裂解以分别再生游离的羟基、氨基或巯基基团的任何基团键合。前药的例子包括但不限于,式(i)化合物中羟基官能团的酯(例如乙酸酯、甲酸酯和苯甲酸酯衍生物)、氨基甲酸酯(例如,n,n-二甲基氨基羰基)等。
“保护基团”是指除烷基基团外的部分,其当与分子中的反应性基团连接时掩蔽、降低或阻止该反应性。保护基团的例子可见于t.w.greene和p.g.m.wuts,《有机合成中的保护基团》(protectivegroupsinorganicsynthesis),第3版,johnwiley&sons,newyork,1999,以及harrison和harrison等,《合成有机方法纲要》(compendiumofsyntheticorganicmethods),1-8卷(johnwileyandsons,1971-1996),其通过引用整体并入本文。代表性的羟基保护基团包括酰基基团、苄基醚和三苯甲基醚、四氢吡喃基醚、三烷基甲硅烷基醚和烯丙基醚。代表性的氨基保护基团包括甲酰基、乙酰基、三氟乙酰基、苄基、苄氧基羰基(cbz)、叔丁氧基羰基(boc)、三甲基甲硅烷基(tms)、2-三甲基甲硅烷基乙磺酰基(ses)、三苯甲基和取代的三苯甲基基团、烯丙氧基羰基、9-芴基甲氧基羰基(fmoc)、硝基藜芦氧基羰基(nvoc)等。
“相应的保护基团”是指与其连接的杂原子(即n、o、p或s)相对应的适当保护基团。
“治疗有效量”是指化合物的量,所述量当施用于哺乳动物治疗疾病时,足以实现对疾病的这种治疗。“治疗有效量”将取决于化合物、疾病及其严重程度、和待治疗的哺乳动物的年龄、体重等而变化。
疾病的“治疗”包括:(1)预防疾病,即在可能暴露于或易患该疾病但尚未经历或出现疾病的症状的哺乳动物中使疾病的临床症状不发展;(2)抑制疾病,即阻止或降低疾病的发展或其临床症状;或(3)缓解疾病,即使疾病或其临床症状消退。
用于本文中时,术语“处理”、“接触”或“反应”当涉及化学反应时,是指在适当条件下添加或混合两种或更多种试剂以产生指定和/或期望的产物。应当领会,产生指定和/或期望产物的反应可能不一定直接由最初添加的两种试剂的组合引起,即,可能存在一种或多种在混合物中产生的中间体,所述混合物最终导致指定和/或期望产物的形成。
用于本文中时,术语“如上所文定义”和“如本文中所定义”当涉及变量时,通过引用并入该变量的广义定义以及任何和所有更窄的定义,如果有的话。
本发明的化合物:
本发明的一个方面提供下式的化合物:
其中
n是0至4的整数;
每个r1独立地选自由烷基、卤代烷基、卤素、硝基、杂环烷基、环烷基、任选取代的杂芳基、任选取代的芳基、和-ora组成的组,其中每个ra独立地选自由氢、烷基、杂芳基、芳基和环烷基组成的组;或者
两个相邻的r1与它们所连接的碳原子一起形成杂环烷基;
r2选自由下列组成的组:
(a)下式的部分:
(b)下式的部分:
(c)任选取代的芳基;和
(d)任选取代的杂环烷基,
其中
m是1或2,
x1是任选取代的杂环烷基、-nr4r5、-nrbso2r6、-nrbc(o)r6、-nrbso2nr4r5或-nrbconr4r5;
x2是o、nrc或s;
r3和r3’各自独立地是氢或烷基;
r4和r5各自独立地是氢或烷基,或r4和r5与它们所连接的氮原子一起形成任选取代的杂环烷基;
rb和rc各自独立地是氢或烷基;并且
r6是-n(rd)2、任选取代的芳基、任选取代的杂芳基或任选取代的杂环基;
条件是所述化合物不是:
n-(n,n-二乙基氨基磺酰基)-2-(二氢吲哚-1-基)丙烷-1-胺);
1,1-二乙基-3-(2-(二氢吲哚-1-基)乙基)脲;
(n-(n,n-二甲基氨基磺酰基)-2-(二氢吲哚-1-基)乙烷-1-胺);
4-(2-(二氢吲哚-1-基)乙基)吗啉;
1-(2-(哌啶-1-基)乙基)二氢吲哚;
n-(2-(二氢吲哚-1-基)丙基)吗啉-4-磺酰胺;
n-(2-(二氢吲哚-1-基)丙基)哌啶-1-磺酰胺;
4-氟-n-(2-(二氢吲哚-1-基)丙基)苯磺酰胺;
4-氟-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺;
n-(2-(二氢吲哚-1-基)乙基)-4-甲氧基苯磺酰胺;
3,4-二氟-n-(2-(二氢吲哚-1-基)丙基)苯磺酰胺;
n-(2-(二氢吲哚-1-基)丙基)-2,3-二氢苯并[b][1,4]二噁英-6-磺酰胺;
n-(2-(二氢吲哚-1-基)乙基)苯并[d][1,3]二氧杂环戊烯-5-磺酰胺;
n-(2-(二氢吲哚-1-基)乙基)-2,3-二氢苯并[b][1,4]二噁英-6-磺酰胺;
n,n-二乙基-4-(2-(二氢吲哚-1-基)-2-氧代乙基)哌嗪-1-磺酰胺;
1-(二氢吲哚-1-基)-2-(4-(吗啉代磺酰基)哌嗪-1-基)乙-1-酮;
1-(二氢吲哚-1-基)-2-(4-(嘧啶-2-基)哌嗪-1-基)乙-1-酮;
4-(3-(二氢吲哚-1-基)-3-氧代丙基)-n,n-二甲基哌嗪-1-磺酰胺;
n,n-二乙基-4-(3-(二氢吲哚-1-基)-3-氧代丙基)哌嗪-1-磺酰胺;
1-(二氢吲哚-1-基)-3-(4-(吗啉代磺酰基)哌嗪-1-基)丙-1-酮;
1-(二氢吲哚-1-基)-3-(4-(嘧啶-2-基)哌嗪-1-基)丙-1-酮;
2-(环庚基氨基)-1-(二氢吲哚-1-基)乙-1-酮;或
3-(环庚基氨基)-1-(二氢吲哚-1-基)丙-1-酮。
本发明的一个方面提供下式的化合物:
其中
n是0至4的整数;
每个r1独立地选自由烷基、卤素、硝基、杂环烷基、环烷基、任选取代的杂芳基、任选取代的芳基和-ora组成的组,其中每个ra独立地选自由氢、烷基、杂芳基、芳基和环烷基组成的组;
或者两个相邻的r1与它们所连接的碳原子一起形成杂环烷基;
r2是
(a)下式的部分:
(b)下式的部分:
(c)任选取代的芳基;或
(d)任选取代的杂环烷基,
其中
m是1或2,
x1是任选取代的杂环烷基、-nr4r5、-nrbso2r6、-nrbc(o)r6、-nrbso2nr4r5或-nrbconr4r5;
x2是o、nrc或s;
r3是氢或烷基,通常r3是氢或甲基;
r4和r5各自独立地是氢或烷基,
或者,r4和r5与它们所连接的氮原子一起形成任选取代的杂环烷基,
rb和rc各自独立地是氢或烷基;并且
r6是任选取代的芳基、任选取代的杂芳基。
在式i的化合物内,当r2是下式的部分:
在一个实施方式中,m是1。而在另一个实施方式中,m是2。
还在另一个实施方式中,r2是下式的部分:
其中m、x1和r3是如本文中所定义。
在其它实施方式中,r4和r5独立地选自由甲基和乙基组成的组。还在其它实施方式中,r4和r5与它们所连接的氮原子一起形成下式的杂环烷基:
其中
x3是o或-nr7;并且
r7是烷基、杂芳基或-so2nr8r9,
其中
r8和r9各自独立地选自烷基,或r8和r9与它们所连接的氮原子一起形成任选取代的杂芳基或任选取代的杂环烷基。
在这些实施方式内,在一些情况下x3是-nr7,其中r7如本文中所定义。在一些特定情况下,r7是甲基、乙基、任选取代的嘧啶-2-基、任选取代的吗啉-4-基或任选取代的哌啶-1-基。
而在其它实施方式中,x2是o。
在其它实施方式中,r2是任选取代的芳基。在一些特定实施方式中,r2是任选被烷基、卤代烷基、任选取代的环烷基、任选取代的芳基、任选取代的杂芳基、-nr4r5、-nrbso2r6、-nrbc(o)r6、-nrbso2nr4r5或-nrbconr4r5取代的苯基,其中rb、r4、r5和r6是如本文中所定义。
在其它实施方式中,r2是任选取代的杂环烷基。在一些情况下,r2是任选取代的哌啶-3-基。而在其它情况下,哌啶-3-基任选被烷基、任选取代的环烷基、任选取代的芳基、任选取代的芳烷基、任选取代的杂芳基、任选取代的杂芳基烷基取代。
在一些实施方式中,n是1。
而在其它实施方式中,r1是烷基、卤代烷基、烷氧基、任选取代的苯基、任选取代的吡唑基、任选取代的吡啶基、或任选取代的嘧啶基,或者两个彼此相邻的r1基团与它们所连接的碳原子一起形成杂环烷基。r1的一些具体例子包括选自由下列组成的组中的那些:甲基,三氟甲基,甲氧基,4-氟苯基,4-(三氟甲基)苯基,4-硝基苯基,4-(n,n-二甲基氨基)苯基,4-甲氧基苯基,3-甲氧基苯基,1-甲基-1h-吡唑-4-基,吡啶-2-基,吡啶-3-基,吡啶-4-基,嘧啶-2-基,和苯并[d][1,3]二氧杂环戊烯-5-基。还在其它例子中包括其中n是2并且两个彼此相邻的r1基团一起形成式–o[ch2]ko–的部分的情况,其中k是1或2。
在一些实施方式中,
n是0或1;
r1是任选取代的芳基;
x1是-nr4r5、-nrbc(o)r6、-nrbso2nr4r5或-nrbso2r6;
r3是氢或烷基;
r4和r5各自独立地是氢或烷基,
或者r4和r5与它们所连接的氮原子一起形成任选取代的杂环烷基;
rb是氢或烷基;并且
r6是任选取代的芳基或任选取代的杂环基。
在一些实施方式中,
x1是-nr4r5、-nhc(o)r6、-nhso2nr4r5或-nhso2r6;
r3是氢或甲基;
r4和r5是烷基,
或者r4和r5与它们所连接的氮原子一起形成任选取代的哌嗪环;并且
r6是任选取代的苯基或任选取代的吡咯烷基。
在一些实施方式中,
x1是-nr4r5、-nhc(o)r6、-nhso2nr4r5或-nhso2r6;
r3是氢或甲基;
r4和r5是乙基,
或者r4和r5与它们所连接的氮原子一起形成任选取代的哌嗪环;并且
r6是任选取代的苯基或任选取代的吡咯烷基。
在一些实施方式中,
n是1;
r1是3-甲氧基苯基;并且
r4和r5是乙基。
在一些实施方式中,
n是0;
r4和r5与它们所连接的氮原子一起形成被r7取代的哌嗪环,其中r7是烷基-so2r12或-so2nr8r9,其中
r8和r9是烷基,
r12是任选取代的芳基;并且
r6是苯基或吡咯烷基,其中苯基被卤素、卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基、氰基、-4-甲氧基苯基中的一种或多种取代。
在一些实施方式中,r3是氢。
在一些实施方式中,r3是烷基。
在一些实施方式中,r3是甲基。
一些代表性的本发明化合物提供于下面的表1-4中:
在一些实施方式中,所述化合物是
在一些实施方式中,本发明提供下式的化合物
其中
n是0或1;
r1是任选取代的芳基;
x1是-nr4r5、-nrbc(o)r6、-nrbso2nr4r5或-nrbso2r6;
r3和r3’各自独立地是氢或烷基;
r4和r5各自独立地是氢或烷基,
或者r4和r5与它们所连接的氮原子一起形成任选取代的杂环烷基;
rb是氢或烷基;并且
r6是任选取代的芳基或任选取代的杂环基。
在一些实施方式中,所述化合物是式(ia)的化合物,其中
x1是-nr4r5、-nhc(o)r6、-nhso2nr4r5或-nhso2r6;
r3和r3’各自独立地是氢或甲基;
r4和r5是烷基,
或者r4和r5与它们所连接的氮原子一起形成任选取代的哌嗪环;并且
r6是任选取代的苯基或任选取代的吡咯烷基。
在一些实施方式中,所述化合物是式(ia)的化合物,其中
x1是-nr4r5、-nhc(o)r6、-nhso2nr4r5或-nhso2r6;
r3和r3’各自独立地是氢或甲基;
r4和r5是乙基,
或者r4和r5与它们所连接的氮原子一起形成任选取代的哌嗪环;并且
r6是任选取代的苯基或任选取代的吡咯烷基。
在一些实施方式中,所述化合物是式(ia)的化合物,其中
n是1;
r1是3-甲氧基苯基;并且
r4和r5是乙基。
在一些实施方式中,所述化合物是式(ia)的化合物,其中
n是0;
r4和r5与它们所连接的氮原子一起形成被r7取代的哌嗪环,其中r7是烷基-so2r12或-so2nr8r9,其中
r8和r9是烷基,
r12是任选取代的芳基;并且
r6是苯基或吡咯烷基,其中苯基被卤素、卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基、氰基、-4-甲氧基苯基中的一种或多种取代。
在一些实施方式中,所述化合物是式(ia)的化合物,其中r3和r3’是氢。
在一些实施方式中,所述化合物是式(ia)的化合物,其中r3是氢并且r3’是甲基。
在一些实施方式中,所述化合物是式(ia)的化合物,其中r3和r3’是甲基。
在一些实施方式中,所述化合物是式(ib)的化合物
其中
x1是-nr4r5、-nhc(o)r6、-nhso2nr4r5或-nhso2r6;
r3和r3’各自独立地是氢或甲基;
当x1是-nr4r5时,r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是烷基;并且
r12是被卤素或-o-卤代烷基取代的苯基,
当x1是-nhc(o)r6时,r6是吡咯烷基,
当x1是-nhso2nr4r5时,其中r4和r5是烷基,以及
当x1是-nhso2r6时,r6是被-o-烷基、卤素、卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基中的一种或多种取代的苯基;
条件是
a)当r6是被-o-烷基取代的苯基时,r3和r3’均为甲基;
b)当r6是被一个卤素取代的苯基时,r3和r3’均为甲基;
c)当r6是被两个卤素取代的苯基时,r3和r3’均为氢,或r3和r3’均为甲基;
d)当x1是-nhso2nr4r5时,其中r4和r5是烷基,r3和r3’均为甲基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5、-nhc(o)r6、-nhso2nr4r5或-nhso2r6;
r3和r3’各自独立地是氢或甲基;
当x1是-nr4r5时,r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是乙基;并且
r12是被氟或-o-cf3取代的苯基,
当x1是-nhc(o)r6时,r6是吡咯烷基,
当x1是-nhso2nr4r5时,其中r4和r5是乙基,以及
当x1是-nhso2r6时,r6是被-o-me、氟、-cf3、-o-cf3、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基中的一种或多种取代的苯基;
条件是
a)当r6是被-ome取代的苯基时,r3和r3’均为甲基;
b)当r6是被一个氟基团取代的苯基时,r3和r3’均为甲基;
c)当r6是被两个氟基团取代的苯基时,r3和r3’均为氢,或r3和r3’均为甲基;以及
d)当x1是-nhso2nr4r5时,其中r4和r5是乙基,r3和r3’均为甲基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5或-nhso2r6;
r3和r3’各自独立地是氢或甲基;
r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是烷基;并且
r12是被卤素或-o-卤代烷基取代的苯基,并且
r6是被-o-烷基、卤素、卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基中的一种或多种取代的苯基;
条件是
a)当r6是被-o-烷基取代的苯基时,r3和r3’均为甲基;
b)当r6是被一个卤素取代的苯基时,r3和r3’均为甲基;以及
c)当r6是被两个卤素取代的苯基时,r3和r3’均为氢,或r3和r3’均为甲基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5或-nhso2r6;
r3和r3’各自独立地是氢或甲基;
r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是乙基;并且
r12是被氟或-o-cf3取代的苯基,并且
r6是被-o-me、氟、-cf3、-o-cf3、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基中的一种或多种取代的苯基;
条件是
a)当r6是被-o-me取代的苯基时,r3和r3’均为甲基;
b)当r6是被一个氟基团取代的苯基时,r3和r3’均为甲基;
c)当r6是被两个氟基团取代的苯基时,r3和r3’均为氢,或r3和r3’均为甲基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5;
r3和r3’各自独立地是氢或甲基;
r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是烷基;并且
r12是被卤素或-o-卤代烷基取代的苯基,
条件是
a)当r6是被-o-烷基取代的苯基时,r3和r3’均为甲基;
b)当r6是被一个卤素取代的苯基时,r3和r3’均为甲基;
c)当r6是被两个卤素取代的苯基时,r3和r3’均为氢,或r3和r3’均为甲基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5;
r3和r3’各自独立地是氢或甲基;
r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是乙基;并且
r12是被氟或-o-cf3取代的苯基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nhso2r6;
r3和r3’各自独立地是氢或甲基;并且
r6是被-o-烷基、卤素、卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基中的一种或多种取代的苯基;
条件是
a)当r6是被-o-烷基取代的苯基时,r3和r3’均为甲基;
b)当r6是被一个卤素取代的苯基时,r3和r3’均为甲基;以及
c)当r6是被两个卤素取代的苯基时,r3和r3’均为氢,或r3和r3’均为甲基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nhso2r6;
r3和r3’各自独立地是氢或甲基;
r6是被-o-me、氟、-cf3、-o-cf3、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基中的一种或多种取代的苯基;
条件是
a)当r6是被-o-me取代的苯基时,r3和r3’均为甲基;
b)当r6是被一个氟基团取代的苯基时,r3和r3’均为甲基;
c)当r6是被两个氟基团取代的苯基时,r3和r3’均为氢,或r3和r3’均为甲基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nhc(o)r6或-nhso2nr4r5;
r3和r3’各自独立地是氢或甲基;
r6是吡咯烷基;并且
当x1是-nhso2nr4r5时,其中r4和r5是烷基;
条件是
a)当r4和r5是烷基时,r3和r3’均为甲基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nhc(o)r6或-nhso2nr4r5;
r3和r3’各自独立地是氢或甲基;
r6是吡咯烷基;并且
当x1是-nhso2nr4r5时,其中r4和r5是乙基;
条件是
a)当r4和r5是乙基时,r3和r3’均为甲基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5、-nhc(o)r6或-nhso2r6;
r3是氢并且r3’是氢或甲基;
当x1是-nr4r5时,r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是烷基;并且
r12是被卤素或-o-卤代烷基取代的苯基,
当x1是-nhc(o)r6时,r6是吡咯烷基,
当x1是-nhso2r6时,r6是被卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基取代的苯基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5、-nhc(o)r6或-nhso2r6;
r3是氢并且r3’是氢或甲基;
当x1是-nr4r5时,r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是乙基;并且
r12是被氟或-o-cf3取代的苯基,
当x1是-nhc(o)r6时,r6是吡咯烷基,
当x1是-nhso2r6时,r6是被-cf3、-o-cf3、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基取代的苯基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5或-nhso2r6;
r3是氢并且r3’是氢或甲基;
当x1是-nr4r5时,r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是烷基;并且
r12是被卤素或-o-卤代烷基取代的苯基,
当x1是-nhso2r6时,r6是被卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基取代的苯基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5或-nhso2r6;
r3是氢并且r3’是氢或甲基;
当x1是-nr4r5时,r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是乙基;并且
r12是被氟或-o-cf3取代的苯基,
当x1是-nhso2r6时,r6是被卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基取代的苯基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5;
r3是氢并且r3’是氢或甲基;
r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是烷基;并且
r12是被卤素或-o-卤代烷基取代的苯基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nr4r5;
r3是氢并且r3’是氢或甲基;
nr4r5,r4和r5与它们所连接的氮原子一起形成哌嗪环,其中所述哌嗪环被r7取代,其中r7是-so2r12或-so2nr8r9,其中
r8和r9是乙基;并且
r12是被氟或-o-cf3取代的苯基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nhso2r6;
r3是氢并且r3’是氢或甲基;
r6是被卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基取代的苯基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nhso2r6;
r3是氢并且r3’是氢或甲基;
r6是被卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基取代的苯基。
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nhso2r6;
r3和r3’是甲基;
r6是被-o-烷基、卤素、卤代烷基、-o-卤代烷基、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基中的一种或多种取代的苯基;
在一些实施方式中,所述化合物是式(ib)的化合物,其中
x1是-nhso2r6;
r3和r3’是甲基;
r6是被-o-me、氟、-cf3、-o-cf3、-o-(5-(三氟甲基)吡啶-2-基)、-o-苯基或氰基中的一种或多种取代的苯基;
在一些实施方式中,所述化合物是
n-(n,n-二乙基氨基磺酰基)-2-(二氢吲哚-1-基)乙烷-1-胺
n-(2-(二氢吲哚-1-基)乙基)吡咯烷-1-磺酰胺
1,1-二乙基-3-(2-(二氢吲哚-1-基)丙基)脲
n-(n,n-二甲基氨基磺酰基)-2-(二氢吲哚-1-基)丙烷-1-胺
n-(2-(二氢吲哚-1-基)丙基)吡咯烷-1-磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-甲基哌嗪-1-甲酰胺
n-(2-(二氢吲哚-1-基)乙基)吗啉-4-磺酰胺
n-(2-(二氢吲哚-1-基)乙基)哌啶-1-磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-甲基哌嗪-1-甲酰胺
n-(2-(二氢吲哚-1-基)丙基)吡咯烷-1-甲酰胺
n-(2-(二氢吲哚-1-基)乙基)吡咯烷-1-甲酰胺
1-(二氢吲哚-1-基)-2-(4-(嘧啶-2-基)哌嗪-1-基)乙-1-酮
1-(二氢吲哚-1-基)-2-(4-(哌啶-1-基磺酰基)哌嗪-1-基)乙-1-酮
4-(2-(二氢吲哚-1-基)-2-氧代乙基)-n,n-二甲基哌嗪-1-磺酰胺
1-(二氢吲哚-1-基)-3-(4-(哌啶-1-基磺酰基)哌嗪-1-基)丙-1-酮
n-(2-(二氢吲哚-1-基)丙基)-2-(吡啶-4-基)噻唑-4-甲酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-甲氧基苯磺酰胺
n-(2-(5-(3-甲氧基苯基)二氢吲哚-1-基)丙基)-n,n-二乙基-1-磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-甲基哌嗪-1-磺酰胺
n-(2-(5-(3-甲氧基苯基)二氢吲哚-1-基)丙基)-4-甲基哌嗪-1-磺酰胺
n-(n,n-二乙基氨基磺酰基)-4-(二氢吲哚-1-基)-苯基-1-胺
n-(2-(二氢吲哚-1-基)丙基)-4-(三氟甲基)苯磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-(三氟甲氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-2-(4-甲氧基苯基)噻唑-4-甲酰胺
n-(2-(二氢吲哚-1-基)丙基)-2-苯基噻唑-4-甲酰胺
n-(2-(二氢吲哚-1-基)丙基)-2-(4-(三氟甲基)苯基)噻唑-4-甲酰胺
1-(2-(4-((4-(三氟甲氧基)苯基)磺酰基)哌嗪-1-基)乙基)二氢吲哚
n,n-二乙基-4-(2-(二氢吲哚-1-基)乙基)哌嗪-1-磺酰胺
1-(2-(4-((4-氟苯基)磺酰基)哌嗪-1-基)乙基)二氢吲哚
n,n-二乙基-4-(2-(二氢吲哚-1-基)乙基)哌嗪-1-甲酰胺
1-(2-(4-(2-氟苄基)哌嗪-1-基)乙基)二氢吲哚
n-(2-(二氢吲哚-1-基)丙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-苯氧基苯磺酰胺
4-氰基-n-(2-(二氢吲哚-1-基)丙基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-(三氟甲基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-(三氟甲氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-苯氧基苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺
3,4-二氟-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺
4-氰基-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺
n-(n,n-二乙基氨基磺酰基)-2-(二氢吲哚-1-基)-2-甲基丙烷-1-胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-(三氟甲基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-苯氧基苯磺酰胺
4-氟-n-(2-(二氢吲哚-1-基)-2-甲基丙基)苯磺酰胺
3,4-二氟-n-(2-(二氢吲哚-1-基)-2-甲基丙基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-(甲氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-(三氟甲氧基)苯磺酰胺
或其药学上可接受的盐。
在一些实施方式中,所述化合物是
n-(2-(二氢吲哚-1-基)丙基)-4-甲氧基苯磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-(三氟甲氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-(三氟甲基)苯磺酰胺
4-氰基-n-(2-(二氢吲哚-1-基)丙基)苯磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-苯氧基苯磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-(三氟甲基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-(三氟甲氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-苯氧基苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺
3,4-二氟-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺
4-氰基-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-(三氟甲基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-苯氧基苯磺酰胺
4-氟-n-(2-(二氢吲哚-1-基)-2-甲基丙基)苯磺酰胺
3,4-二氟-n-(2-(二氢吲哚-1-基)-2-甲基丙基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-甲氧基苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-(三氟甲氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)吡咯烷-1-甲酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-甲基哌嗪-1-甲酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-甲基哌嗪-1-磺酰胺
n-(n,n-二乙基氨基磺酰基)-2-(5-(3-甲氧基苯基)二氢吲哚-1-基)-丙烷-1-胺
n-(n,n-二乙基氨基磺酰基)-2-(二氢吲哚-1-基)-2-甲基丙烷-1-胺
1-(2-(4-((4-氟苯基)磺酰基)哌嗪-1-基)乙基)二氢吲哚
1-(2-(4-((4-(三氟甲氧基)苯基)磺酰基)哌嗪-1-基)乙基)二氢吲哚
n,n-二乙基-4-(2-(二氢吲哚-1-基)乙基)哌嗪-1-磺酰胺
n,n-二乙基-4-(2-(二氢吲哚-1-基)乙基)哌嗪-1-甲酰胺
或其药学上可接受的盐。
在一些实施方式中,所述化合物是
n-(2-(二氢吲哚-1-基)丙基)-4-(三氟甲氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-(三氟甲基)苯磺酰胺
n-(2-(二氢吲哚-1-基)丙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-(三氟甲基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-(三氟甲氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-苯氧基苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺
3,4-二氟-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺
4-氰基-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-(三氟甲基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-苯氧基苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-甲氧基苯磺酰胺
n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-(三氟甲氧基)苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)吡咯烷-1-甲酰胺
n-(n,n-二乙基氨基磺酰基)-2-(二氢吲哚-1-基)-2-甲基丙烷-1-胺
1-(2-(4-((4-氟苯基)磺酰基)哌嗪-1-基)乙基)二氢吲哚
1-(2-(4-((4-(三氟甲氧基)苯基)磺酰基)哌嗪-1-基)乙基)二氢吲哚
n,n-二乙基-4-(2-(二氢吲哚-1-基)乙基)哌嗪-1-磺酰胺
或其药学上可接受的盐。
在一些实施方式中,所述化合物是
n-(2-(二氢吲哚-1-基)乙基)-4-苯氧基苯磺酰胺
n-(2-(二氢吲哚-1-基)乙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺
3,4-二氟-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺
4-氰基-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺
或其药学上可接受的盐。
在一些实施方式中,所述化合物是
1-(2-(4-((4-(三氟甲氧基)苯基)磺酰基)哌嗪-1-基)乙基)二氢吲哚
n,n-二乙基-4-(2-(二氢吲哚-1-基)乙基)哌嗪-1-磺酰胺
1-(2-(4-((4-氟苯基)磺酰基)哌嗪-1-基)乙基)二氢吲哚
或其药学上可接受的盐。
应当领会,本发明化合物上的各种取代基可以存在于起始化合物中、加入到任何一种中间体中、或在通过已知的取代或转化反应方法形成最终产物后加入。如果取代基本身是反应性的,那么取代基本身可以根据本领域已知的技术受到保护。各种保护基团是本领域已知的,并且可以采用。许多可能的基团的例子可以在t.w.green的“有机合成中的保护基团(protectivegroupsinorganicsynthesis)”,johnwileyandsons,1981中找到。例如,可以通过硝化加入硝基基团,并且可以通过还原将硝基基团转化为其它基团,例如氨基,以及通过氨基基团的重氮化并用卤素置换重氮基团来加入卤素。酰基基团可以通过friedel-crafts酰化加入。然后可以通过各种方法,包括wolff-kishner还原和clemmenson还原,将酰基基团转变为相应的烷基基团。可以将氨基基团烷基化而形成单和二烷基氨基基团;并且可以将巯基和羟基基团烷基化而形成相应的醚。伯醇能够通过本领域已知的氧化剂氧化而形成羧酸或醛,而仲醇可以被氧化形成酮。因此,取代或改变反应可用于在起始材料、中间体或最终产物、包括分离的产物的整个分子中提供各种取代基。
更进一步,本文描述的各种可变基团的组合形成其它实施方式。以这种方式,在本发明内包涵了多种化合物。
在另一个方面,本发明提供药物组合物。在一个实施方式中,所述药物组合物可包含如本文所述的化合物和药学上可接受的载体。
在另一个方面,本发明的化合物是nox4的选择性抑制剂,因此能够治疗性地用于特别是治疗与纤维化病症相关的临床疾患。
在一些实施方式中,本发明提供治疗与纤维化病症相关的临床疾患的方法,所述方法包括给需要这样的治疗的对象施用治疗可接受量的本文所述化合物或其药学上可接受的盐、或本文所述的药物组合物,以治疗与纤维化病症相关的临床疾患。
在一些实施方式中,与纤维化病症相关的临床疾患包括肾、肝、皮肤、肺或心脏的纤维化疾病。
在一些实施方式中,与纤维化病症相关的临床疾患包括特发性肺纤维化。
本发明的化合物可以施用于患者以达到期望的生理效应。该化合物可以用适合于所选择的施用途径的各种形式施用,即口服或肠胃外。在这方面,肠胃外施用包括通过以下途径施用:静脉内;肌内;皮下;眼内;滑膜内;经上皮,包括透皮、眼,舌下和颊;局部,包括通过吹入和气溶胶经眼部、真皮、眼睛、直肠和鼻吸入;腹膜内;和直肠全身。在一些实施方式中,施用通过口腔吸入完成,例如,通过使用口腔吸入器。
所述活性化合物能够口服施用,例如,用惰性稀释剂或用可吸收的可食载体,或者它可以包装在硬或软壳明胶胶囊中,或者它可以压制成片剂,或者它可以直接与饮食的食物合并。对于口服治疗施用,所述活性化合物可以与赋形剂合并并以可摄入的片剂、颊含片、锭剂、胶囊,酏剂、悬液、糖浆、膜剂(wafers)等形式使用。这样的组合物和制剂可含有至少0.1%的活性化合物。当然,所述组合物和制剂的百分比可以变化,并且可以适宜在单位的重量的约1至约10%之间。在这样治疗有用的组合物中活性化合物的量要使得将会获得合适的剂量。优选的本发明组合物或制剂的制备要使得口服剂量单位形式含有约1至约1000mg的活性化合物。
片剂、锭剂、丸剂、胶囊等还能含有以下物质:粘合剂例如黄蓍胶、阿拉伯树胶、玉米淀粉或明胶;赋形剂如磷酸二钙;崩解剂例如玉米淀粉、马铃薯淀粉、海藻酸等;润滑剂例如硬脂酸镁;和甜味剂例如蔗糖、乳糖或糖精可以添加,或调味剂例如胡椒薄荷、冬青油或樱桃调味剂。当剂量单位形式是胶囊时,除了上述类型的材料外,它还可以含有液体载体。各种其它材料可以作为包衣存在或以其它方式改变剂量单位的物理形式。例如,片剂、丸剂或胶囊可以用虫胶、糖或两者包衣。糖浆或酏剂可含有所述活性化合物、作为甜味剂的蔗糖、对羟基苯甲酸甲酯和丙酯防腐剂、染料和调味剂例如樱桃或橙子风味。当然,用于制备任何剂量单位形式的任何材料应该是药学上纯的并且在所使用的量上基本无毒。此外,所述活性化合物可以并入缓释制剂和配方中。
所述活性化合物也能够胃肠外施用。作为游离碱或药学上可接受的盐的活性化合物的溶液可以在水中适当地与表面活性剂例如羟丙基纤维素混合而制备。也可以在甘油、液体聚乙二醇及其混合物中和油中制备分散体。在平常的储存和使用条件下,这些制剂含有防腐剂以防止微生物生长。
适于注射使用的药物形式包括无菌水溶液或分散体以及用于临时制备无菌注射溶液或分散体的无菌粉末。在所有情况下,所述形式必须是无菌的并且必须是达到存在易于注射性的程度的流体。它在制造和储存条件下可以是稳定的,并且必须免受微生物例如细菌和真菌的污染作用。载体可以是分散介质的溶剂,其含有例如水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇等)、其合适的混合物、以及植物油。适当的流动性可例如通过使用包衣例如卵磷脂、在分散体的情况下通过维持所需要的粒度、和通过使用表面活性剂来维持。防止微生物的作用可通过各种抗细菌剂和抗真菌剂、例如对羟基苯甲酸酯、氯丁醇、苯酚、山梨酸、硫柳汞等来实行。在许多情况下,将优选包含等渗剂,例如糖或氯化钠。延迟吸收剂例如单硬脂酸铝和明胶延长可注射组合物的吸收。
无菌注射溶液通过将所需量的活性化合物根据需要与上面列举的各种其它成分一起掺入适当的溶剂中、然后过滤灭菌来制备。通常,通过将各种灭菌的活性成分掺入含有基础分散介质和来自上面列举的那些的所需其它成分的无菌介质中来制备分散体。在用于制备无菌注射溶液的无菌粉末的情况下,优选的制备方法是真空干燥和冷冻干燥技术,其产生活性成分加上来自其先前无菌过滤溶液的任何额外所需成分的粉末。
如上所述,本发明的治疗化合物能够单独或与药学上可接受的载体相结合施用于哺乳动物,其比例由所述化合物的溶解度和化学性质、所选择的施用途径和标准药学实践决定。
本发明的治疗化合物能够与一种或多种用于治疗特发性肺纤维化(ipf)的药物和/或抗氧化剂联合施用。例如,本发明化合物可以与吡非尼酮、n-乙酰半胱氨酸、三联疗法(即,n-乙酰半胱氨酸与泼尼松和硫唑嘌呤联合)、尼达尼布或其组合联合施用。
医生将决定将最适合于预防或治疗的本治疗剂的剂量,它将随施用形式和所选择的特定化合物而异,并且它还将随治疗中的特定患者而异。医生通常希望以小剂量开始治疗,通过小的增量直到达到在此情况下的最佳效果。治疗剂量一般可以为约0.1至约1000毫克/天,优选约10至约100毫克/天,或约0.1至约50毫克/千克体重/天,优选约0.1至约20毫克/千克体重/天,并能够以几种不同的剂量单位施用。口服施用可能需要更高的剂量,约2x至约4x左右。
本领域技术人员在研究本发明的以下实施例后,本发明的其它目的、优点和新颖特征将变得显而易见,这些实施例并不意图是限制性的。在实施例中,推定付诸实践的程序以现在时描述,而已在实验室中进行的程序以过去时阐述。
实施例
使用以下缩写:hobt(1-羟基苯并三唑);dcm(二氯甲烷);etoac(乙酸乙酯);meoh(甲醇);hbtu(2-(1h-苯并三唑-1-基)-1,1,3,3-四甲基脲鎓六氟磷酸盐);diea(n,n-二异丙基乙胺);dmf(n,n-二甲基甲酰胺);pd2(dba)3(三(二亚苄基丙酮)二钯(0));boc(叔丁氧基羰基);(boc)2o(二碳酸二叔丁酯);acoh(乙酸);etoh(乙醇);et3n(三乙胺);tlc(薄层色谱法);和nmr(核磁共振)。
一般程序:所有化学品都从商业供应商购买。所有溶剂均得自fischerscientific。快速色谱法用硅胶(230/400目,fisherscientific)进行。所有无水反应均在氮气正压下进行。hplc-ms分析在agilent1100系列仪器上用zorbaxc18反相柱进行。梯度为以10ml/min在20分钟内90至95的acn水溶液。手性hplc分析在agilent1100系列仪器上用chiralcelod-rh,5um,4.6x150mm柱进行。手性化合物的hplc纯化在phenomenexluxamylose-2,axiapacked,5um,21.20x250mm上进行。使用的溶剂系统是60%的acn水溶液以1ml/min等度运行(没有梯度)。hrms结果在apex-qe仪器上获得。所有1h-nmr和13c-nmr光谱都使用氘代溶剂在brukeravance-iii400mhznmr仪器上记录。所述光谱以ppm报告并参考氘代dmso(1h为2.49ppm,13c为39.5ppm)或氘代氯仿(1h为7.26ppm,13c为77ppm)。高分辨率质谱(hrms)在bruker9.4tapex-qhfticr质谱仪上获取。所有微波辅助反应使用biotageinitiator仪器进行。所有化合物都通过hplc使用ms或uv吸光度检测器分析纯度。
方案1:2-(二氢吲哚-1-基)乙烷-1-胺(i)的合成
在配备有氮气入口、磁力搅拌棒和回流冷凝器的圆底烧瓶中,添加二氢吲哚(4.52g,35.68mmol,4ml)在30mldmf中的溶液。向上述溶液添加k2co3(14g,101mmol),然后将混合物搅拌3min。然后向混合物添加碘化钾(0.58g,3.57mmol,0.1eq)和2-氯乙胺盐酸盐(4.64g,39.25mmol)。然后将所述混合物在110℃下加热过夜。然后将反应用200ml水稀释,用etoac(100mlx3)提取。合并的有机层经无水na2so4干燥,浓缩,然后真空干燥,产生8.35g粗产物。然后将粗产物用乙醚稀释,然后添加2nhcl。然后分离相,然后将水层用2.5nnaoh碱化。然后用etoac提取水溶液,合并的有机层经无水na2so4干燥,浓缩,然后真空干燥,产生6.32g粗产物。产物经硅胶柱色谱用1:1乙酸乙酯:己烷纯化以分离过量的二氢吲哚,并用10%meoh的ch2cl2溶液洗脱目标产物。将合并的级分浓缩,然后真空干燥,产生2.38g(41%)棕色油状化合物,为目标产物。1hnmr(400mhz,cdcl3)δ7.10(t,j=6.8hz,1h),7.07(t,j=8hz,1h),6.71(t,j=8hz,1h),6.52(d,j=8hz,1h),3.56(q,j=8hz,2h),3.38(t,j=8hz,2h),3.23(t,j=8hz,2h),3.30(t,j=8hz,2h)。
化合物uanox001(n-(n,n-二乙基氨基磺酰基)-2-(二氢吲哚-1-基)乙烷-1-胺)
在配备氮气入口和磁力搅拌棒的圆底烧瓶中,添加0.21g(1.22mmol)n,n-二乙基氨磺酰氯在5mlch2cl2中的溶液。向上述溶液添加0.235g(1mmol)的2-(二氢吲哚-1-基)乙烷-1-胺二盐酸盐(i·2hcl)和0.40ml(2.87mmol)的三乙胺。将反应在室温下剧烈搅拌18h,然后用20ml水淬灭。然后用ch2cl2(15mlx3)提取水层。将合并的有机提取液经无水na2so4干燥,浓缩,然后真空干燥,给出0.40g粗产物。然后将粗产物通过柱色谱法用30%etoac的己烷溶液纯化。浓缩级分,然后真空干燥,产生170mg(57%)的目标产物,为浅黄色油。1hnmr(400mhz,cdcl3)δ7.13(d,j=8.0hz,1h),7.11(t,j=8hz,1h),6.74(t,j=8hz,1h),6.57(d,j=8hz,1h),4.63(s,2h),3.38(t,j=8hz,2h),3.32(q,j=8hz,4h),3.28-3.23(m,4h),3.02(t,j=8hz,2h),1.23(t,j=8hz,6h)。hplc-ms:预期:298(mh+);实测:298。
uanox002(1,1-二乙基-3-(2-(二氢吲哚-1-基)乙基)脲)
化合物uanox002按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.28-7.09(m,2h),6.74(t,j=8hz,1h),6.55(d,j=8hz,1h),4.63(bs,1h),3.38(t,j=8hz,2h),3.32(四重峰,j=8hz,4h),3.28-3.23(m,4h),3.02(t,j=8hz,2h),1.23(t,j=8hz,6h)。hplc-ms:预期:262(mh+);实测:262。
uanox003(n-(n,n-二甲基氨基磺酰基)-2-(二氢吲哚-1-基)乙烷-1-胺)
uanox003按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.13(d,j=8.0hz,1h),7.10(t,j=8hz,1h),6.74(t,j=8hz,1h),6.56(d,j=8hz,1h),4.69(s,1h),3.39(t,j=8hz,2h),3.34-3.25(m,4h),3.02(t,j=8hz,2h),2.85(s,6h)。hplc-ms:预期:270(mh+);实测:270。
uanox004(n-(2-(二氢吲哚-1-基)乙基)吡咯烷-1-磺酰胺)
uanox004按照对化合物uanpx001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.13(d,j=8.0hz,1h),7.10(t,j=8hz,1h),6.74(t,j=8hz,1h),6.56(d,j=8hz,1h),4.70(s,1h),3.39(t,j=8hz,2h),3.36-3.26(m,8h),3.02(t,j=8hz,2h),1.95(s,4h)。hplc-ms:预期:296(mh+);实测:296。
uanox011(n-(2-(二氢吲哚-1-基)乙基)-4-甲基哌嗪-1-甲酰胺)
uanox011按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.11(d,j=8hz,1h),7.08(t,j=8hz,1h),6.70(t,j=8hz,1h),6.58(d,j=8hz,1h),4.65(bs,1h),3.53(q,4hz,2h),3.43(t,j=8hz,2h),3.39-3.30(m,6h),3.26(t,j=8hz,2h),2.85(s,3h),1.9–1.88(m,2h),1.86–1.82(m,2h)。hplc-ms:预期:310(m+na);实测:310。
uanox012(n-(2-(二氢吲哚-1-基)乙基)吗啉-4-磺酰胺)
uanox012按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.17-7.07(m,2h),6.75(t,j=8hz,1h),6.58(d,j=8hz,1h),4.70(bs,1h),3.78–3.75(m,6h),3.39(t,j=8hz,2h),3.26–3.23(m,6h),3.03(t,j=8hz,2h)。hplc-ms:预期:312(mh+);实测:312。
uanox021(n-(2-(二氢吲哚-1-基)乙基)吡咯烷-1-甲酰胺)
uanox021按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.12-7.06(m,2h),6.70(t,j=8hz,1h),6.57(d,j=8hz,1h),4.61(bs,1h),3.52(四重峰,j=8hz,2h),3.42(t,j=8hz,2h),3.32(t,j=8hz,4h),3.25(t,j=8hz,2h),3.01(t,j=8hz,2h),1.90(t,j=8hz,4h)。hplc-ms:预期:260(mh+);实测:260。
uanox013(n-(2-(二氢吲哚-1-基)乙基)哌啶-1-磺酰胺)
uanox013按照对化合物uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.23–6.99(m,2h),6.76(td,j=7.4,0.9hz,1h),6.59(d,j=7.8hz,1h),4.60(bs,1h),3.40(t,j=8.2hz,2h),3.36–3.26(m,4h),3.25–3.20(m,4h),3.02(t,j=8.2hz,2h),1.77–1.46(m,6h)。hplc-ms:预期:311(m+2);实测:311。
uanox051(4-氟-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺)
uanox051按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)1hnmr(400mhz,氯仿-d)δ7.92(dd,j=9.0,5.1hz,2h),7.21(t,j=9.2,2h),7.11(d,j=7.2hz,1h),7.07(t,j=7.7hz,1h),6.73(t,j=7.8hz,1h),6.39(d,j=7.2hz,1h),3.44–3.07(m,6h),2.95(t,j=8.2hz,2h)。hplc-ms:预期:321(mh+);实测:321。
uanox050(4-甲氧基-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺)
uanox050按照对化合物uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.84(d,j=9.1hz,2h),7.10(d,j=7.9hz,1h),7.06(d,j=8hz,1h),7.00(d,j=9.1hz,2h),6.72(t,j=8hz,1h),6.38(d,j=8.1hz,1h),3.90(s,3h),3.24–3.12(m,6h),2.94(t,j=8.3hz,2h)。hplc-ms:预期:333(mh+);实测:333。
uanox075(4-三氟甲基-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺)
uanox075按照对化合物uanox001描述的程序合成。
1hnmr(400mhz,氯仿-d)δ7.96(d,j=8.7hz,2h),7.73(d,j=8.2hz,2h),7.04(d,j=7.2hz,1h),7.00(t,j=7.7hz,1h),6.67(t,j=7.4hz,1h),6.29(d,j=7.9hz,1h),5.08(bs,1h),3.26–3.06(m,6h),2.87(t,j=8.3hz,2h)。hplc-ms:预期:371(mh+);实测:371。
uanox076(4-三氟甲氧基-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺)
uanox076按照对化合物uanox001描述的程序合成。
1hnmr(400mhz,氯仿-d)δ7.90(d,j=9.7hz,2h),7.31(d,j=8.7hz,2h),7.05(d,j=7.2hz,1h),7.01(t,j=7.7hz,1h),6.68(t,j=7.4hz,1h),6.32(d,j=7.2hz,1h),4.94(bs,1h),3.25–3.04(m,6h),2.89(t,j=7.7hz,2h)。hplc-ms:预期:387(mh+);实测:387。
uanox077(n-(2-(二氢吲哚-1-基)乙基)苯并[d][1,3]二氧杂环戊烯-5-磺酰胺)
uanox077按照对化合物uanox001描述的程序合成。
1hnmr(400mhz,氯仿-d)δ7.41(dd,j=8.2,1.8hz,1h),7.23(dd,j=7.2,1.3hz,1h),7.04(d,j=7.2hz,1h),7.01(t,j=7.7hz,1h),6.84(d,j=8.2hz,1h),6.66(t,j=7.4hz,1h),6.34(d,j=7.9hz,1h),6.04(s,2h),4.83(bs,1h),3.24–3.02(m,6h),2.89(t,j=8.2hz,2h)。hplc-ms:预期:347(mh+);实测:347。
uanox078(n-(2-(二氢吲哚-1-基)乙基)-2,3-二氢苯并[b][1,4]二噁英-6-磺酰胺)
uanox078按照对化合物uanox001描述的程序合成。
1hnmr(400mhz,氯仿-d)δ7.37(dd,j=2.2,1.2hz,1h),7.32(ddd,j=8.5,2.2,1.3hz,1h),7.04(d,j=7.0hz,1h),7.01(t,j=7.7hz,1h),6.92(dd,j=8.5,0.9hz,1h),6.66(t,j=7.4hz,1h),6.34(d,j=7.9hz,1h),4.77(bs,1h),4.35–4.12(m,4h),3.22–3.00(m,6h),2.89(t,j=8.2hz,2h)。hplc-ms:预期:361(mh+);实测:361。
uannox079(n-(2-(二氢吲哚-1-基)乙基)-4-苯氧基苯磺酰胺)
uanox079按照对化合物uanox001描述的程序合成。
1hnmr(400mhz,氯仿-d)δ7.79(d,j=8.8hz,2h),7.39(t,j=8.0hz,2h),7.20(t,j=7.4hz,1h),7.08–6.85(m,6h),6.67(t,j=7.3hz,1h),6.34(d,j=7.9hz,1h),4.86(t,j=5.6hz,1h),3.21–3.06(m,6h),2.90(t,j=8.2hz,2h)。hplc-ms:预期:395(mh+);实测:395。
uanox080(n-(2-(二氢吲哚-1-基)乙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺)
uanox080按照对化合物uanox080描述的程序合成。
1hnmr(400mhz,氯仿-d)δ8.41(s,1h),7.95(dd,j=8.6,2.5hz,1h),7.91(d,j=8.9hz,2h),7.27(d,j=8.5hz,2h),7.09(d,j=9.2hz,1h),7.05(d,j=7.2hz,1h),7.01(t,j=8.0hz,1h),6.67(t,j=7.4hz,1h),6.37(d,j=7.8hz,1h),4.90(t,j=5.7hz,1h),3.29–3.07(m,6h),2.91(t,j=8.1hz,2h)。hplc-ms:预期:464(mh+);实测:464。
uanox082(4-氰基-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺)
uanox082按照对化合物uanox001描述的程序合成。
1hnmr(400mhz,氯仿-d)δ7.92(d,j=7.7hz,2h),7.71(d,j=7.4hz,2h),7.04(d,j=7.2hz,1h),7.00(t,j=7.7hz,1h),6.68(t,j=7.4hz,1h),6.29(d,j=7.9hz,1h),5.11(bs,1h),3.27–3.03(m,6h),2.87(t,j=8.2hz,2h)。13cnmr(101mhz,氯仿-d)δ151.68,144.25,132.85,129.77,127.52,127.32,124.70,118.87,117.21,116.26,107.08,53.57,49.57,41.25,28.49。hplc-ms:预期:328(mh+);实测:328。
uanox081(3,4-二氟-n-(2-(二氢吲哚-1-基)乙基)苯磺酰胺)
uannox081按照对化合物uanox001描述的程序合成。
1hnmr(400mhz,氯仿-d)δ7.67(t,j=8.1hz,1h),7.61(d,j=8.4hz,1h),7.30–7.22(m,1h),7.05-6.99(m,2h),6.67(t,j=7.3hz,1h),6.34(d,j=7.8hz,1h),4.94(bs,1h),3.27–3.03(m,6h),2.89(t,j=8.1hz,2h)。hplc-ms:预期:339(mh+);实测:339。
uanox017(4-(2-(二氢吲哚-1-基)乙基)吗啉)的合成
在配备氮气入口、磁力搅拌棒和回流冷凝器的圆底烧瓶中,添加二氢吲哚(0.2ml,0.213g,1.78mmol)在2mldmf中的溶液。向上述溶液添加k2co3(0.707g,5.11mmol),然后将混合物搅拌30分钟。然后添加碘化钾(0.03g,0.19mmol)和4-(2-溴乙基)吗啉盐酸盐(0.34g,1.78mmol)。然后将反应混合物在110℃加热6hr。然后将混合物用水(20ml)稀释,然后用etoac(15mlx3)提取。将合并的有机层经无水na2so4干燥,浓缩,然后真空干燥。粗产物利用柱色谱法纯化,首先用30%etoac的己烷溶液(以洗脱二氢吲哚),然后用10%meoh的ch2cl2溶液,得到0.246g(59%)目标产物。1hnmr(400mhz,cdcl3)δ7.04-7.00(m,2h),6.60(t,j=8hz,1h),6.45(d,j=8hz,1h),3.70(t,j=4hz,4h),3.37(t,j=8hz,2h),3.20(t,j=4hz,2h),2.93(t,j=8hz,2h),2.58(t,j=8hz,2h),2.51(m,4h)。hplc-ms:预期:233(mh+);实测:233。
uanox018(1-(2-(哌啶-1-基)乙基)二氢吲哚)
uanox018根据对合成化合物uanox017所述的程序,由二氢吲哚和1-(2-溴乙基)哌啶合成。1hnmr(400mhz,cdcl3)δ7.10-7.06(m,2h),6.66(t,j=8hz,1h),6.52(d,j=8hz,1h),3.42(t,j=8hz,2h),3.28(t,j=8hz,2h),3.01-2.97(m,2h),2.62(t,j=8hz,2h),2.53(t,j=8hz,4h),1.66(quintet,j=4hz,4h),1.52-1.47(m,2h)。hplc-ms:预期:231(mh+);实测:231。
2-(二氢吲哚-1-基)丙酰胺(iia)的合成:在配备氮气入口、磁力搅拌棒和回流冷凝器的圆底烧瓶中,添加二氢吲哚(5.315g,44.6mmol,5ml)在42mldmf中的溶液。向上述溶液添加k2co3(18g,130mmol),然后将混合物搅拌30min。然后向混合物添加碘化钾(0.8g,4.91mmol,0.1eq)和2-溴丙酰胺(7.46g,49.06mmol)。然后将混合物在110℃加热2hr。然后将混合物用水(200ml)稀释,用ch2cl2(70mlx3)提取。将合并的有机层经无水na2so4干燥,浓缩,然后真空干燥,产生13.45g的粗产物。在静置48小时后晶体从粗产物中析出。除去上清油,用最少量的无水乙醚洗涤晶体。产物用无水乙醚重结晶,给出1.65g(19%)纯产物(通过noesy发现是对映体之一)。将上清酒红色油状粗产物(11.5g)用5%meoh的ch2cl2溶液进行柱色谱分离,产生两个级分。1hnmr用于确认这两个级分是相同的化合物。单独浓缩这两个含有目标产物的级分的合并有机层,然后真空干燥,得到目标产物,为棕色油。这种油状产物在进一步干燥时变成固体。然后将固体用己烷洗涤以除去过量的dmf并真空干燥,产生6.85g(79%)目标产物,为棕色固体。总收率为98%。1hnmr(400mhz,cdcl3)δ7.14(d,j=8.0hz,1h),7.09(t,j=8hz,1h),6.76(t,j=8hz,1h),6.49(d,j=8hz,1h),3.95(q,j=8hz,1h),3.49(q,j=8hz,1h),3.42(q,j=8hz,1h),3.02(t,j=8hz,2h),1.43(d,j=8hz,3h)。hplc-ms:预期:191(mh+);实测:191。
2-(二氢吲哚-1-基)-2-甲基丙酰胺(iib)根据对合成化合物iia所述的程序,由二氢吲哚和2-溴-2-甲基丙酰胺合成。1hnmr(400mhz,氯仿-d)δ7.27(d,j=7.3hz,1h),7.18(t,j=7.7hz,1h),6.90(t,j=7.4hz,1h),6.62(d,j=7.9hz,1h),5.67(bs,1h),3.56(td,j=8.2,1.4hz,2h),3.11(t,j=8.1hz,2h),2.13(t,j=1.1hz,3h),1.57(t,j=1.1hz,3h)。lcms:预期:205(mh+);实测:205。
2-(二氢吲哚-1-基)丙烷-1-胺(iiia)的合成:在配备氮气入口和回流冷凝器的圆底烧瓶中,添加溶解在1mbh3·thf(25ml)中的2-(二氢吲哚-1-基)丙酰胺(8.04mmol,1.53g)。然后将反应混合物加热至回流达18h。将反应混合物冷却至室温,然后用meoh缓慢淬灭。将溶液浓缩,溶解在meoh中,并再次浓缩。将所生成的油用乙醚稀释,并用1nhcl提取两次。将水相用2.5nnaoh处理以调节ph>10,然后用etoac提取。将合并的etoac提取液经na2so4干燥,浓缩,提供0.97g淡黄色油,为粗产物。粗产物通过硅胶柱色谱法使用10-20%meoh的ch2cl2溶液进行纯化。将合并的级分蒸发,然后真空干燥,产生0.78g(55%)纯产物,为两种对映体的混合物。1hnmr(400mhz,cdcl3)δ7.09-7.05(m,2h),6.64(t,j=8hz,1h),6.49(d,j=8hz,1h),3.73-3.64(m,1h),3.37(四重峰,j=8hz,1h),3.29(四重峰,j=8hz,1h),2.99(dd,j=8hz,7hz,2h),2.82(ddd,j=36hz,8hz,12hz,2h),1.07(d,j=8hz,3h)。
2-(二氢吲哚-1-基)-2-甲基丙烷-1-胺(iiib)根据对合成化合物iia所述的程序来合成。1hnmr(400mhz,氯仿-d)δ7.31(d,j=7.6hz,1h),7.24(t,j=8.1hz,1h),7.00(d,j=7.9hz,1h),6.88(t,j=7.3hz,1h),3.68(t,j=8.6hz,2h),3.20(s,2h),3.14(t,j=8.6hz,2h),1.85-1.64(bs,1h),1.63(d,j=30.5hz,3h),1.55(s,3h)。lcms:预期:191(mh+);实测:191。
uanox006(1,1-二乙基-3-(2-(二氢吲哚-1-基)丙基)脲)
uanox006按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.09-7.05(m,2h),6.65(t,j=8hz,1h),6.52(d,j=8hz,1h),4.73(bs,1h),3.93-3.81(m,1h),3.60-3.54(ddd,j=20,12,8hz,1h),3.34-3.29(m,2h),3.33-3.31(m,5h),3.24-3.91(m,2h),1.14(d,j=8hz,3h),1.06(t,j=8hz,6h)。在质子nmr中还观察到少量构象异构体:1hnmr(400mhz,cdcl3)δ7.62(dq,j=8,0.8hz),7.42(dq,j=8,0.8hz),7.21(d,j=3.6hz),7.19(dt,j=8,1.2hz),7.13(dd,j=20,1.2hz),6.58(d,j=3.6hz),1.60(d,j=8hz),0.87(t,j=8hz)。hplc-ms:预期:276(mh+);实测:276。
uanox007(n-(n,n-二甲基氨基磺酰基)-2-(二氢吲哚-1-基)丙烷-1-胺)
uanox007按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.12-7.07(m,2h),6.71(t,j=8hz,1h),6.52(d,j=8hz,1h),4.80(bs,1h),3.93-3.84(m,1h),3.40-3.26(m,2h),3.19(t,j=8hz,2h),3.02-2.98(m,2h),2.82(s,6h),1.11(d,j=6.8hz,3h)。hplc-ms:预期:284(mh+);实测:284。
uanox008(n-(2-(二氢吲哚-1-基)丙基)吡咯烷-1-磺酰胺)
uanox008按照对化合物uanox001描述的程序合成。7.14-7.07(m,2h),6.70(t,j=8hz,1h),6.51(d,j=8hz,1h),4.79-4.74(m,1h),3.87(六重峰,j=7hz,1h),3.39-3.25(m,6h),3.22-3.18(m,2h),3.14(t,j=8hz,1h),3.02-2.97(m,2h),1.97-1.91(m,4h),1.11(d,j=6.4hz,3h)。hplc-ms:预期:310(mh+);实测:310。
uanox019(n-(2-(二氢吲哚-1-基)丙基)-4-甲基哌嗪-1-甲酰胺)
uanox019按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.09-7.04(m,2h),6.65(t,j=8hz,1h),6.51(d,j=8hz,1h),3.89-3.81(m,1h),3.58-3.52(ddd,j=20,12,8hz,1h),3.36-3.19(m,7h),3.00-2.96(m,2h),2.34(t,j=5hz,4h),2.29(s,3h),1.12(d,j=8hz,3h)。hplc-ms:预期:304(m+2);实测:304。
uanox010(n-(2-(二氢吲哚-1-基)丙基)吗啉-4-磺酰胺)
uanox010按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.12(d,j=8hz,1h),7.09(t,j=8hz,1h),6.71(t,j=8hz,1h),6.51(d,j=8hz,1h),4.78(t,j=8hz,1h),3.91–3.83(m,1h),3.77(t,j=8hz,4h),3.38-3.25(m,2h),3.23–3.20(m,6h),3.02-2.98(m,2h),1.12(d,j=8hz,3h)。hplc-ms:预期:326(mh+);实测:326,以及预期:348(m++na);实测:348。
uanox020(n-(2-(二氢吲哚-1-基)丙基)吡咯烷-1-甲酰胺)
uanox020按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.10-7.05(m,2h),6.66(t,j=8hz,1h),6.53(d,j=8hz,1h),4.56(bs,1h),3.92-3.84(m,1h),3.62-3.56(ddd,j=20,12,8hz,1h),3.42-3.31(m,2h),3.27-3.19(m,5h),3.02-2.97(m,2h),1.89-1.83(m,4h),1.14(d,j=8hz,3h)。hplc-ms:预期:274(mh+);实测:274。
uanox009(n-(2-(二氢吲哚-1-基)丙基)哌啶-1-磺酰胺)
uanox009按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.12-7.07(m,2h),6.71(t,j=8hz,1h),6.52(d,j=8hz,1h),4.76(t,j=8hz,1h),3.91-3.82(m,1h),3.40-3.26(m,2h),3.21-3.16(m,6h),3.02-2.98(m,2h),1.69-1.62(m,4h),1.61-1.53(m,2h),1.11(d,j=6.8hz,3h)。hplc-ms:预期:324(mh+);实测:324
uanox033(n-(2-(二氢吲哚-1-基)丙基)-2-(吡啶-4-基)噻唑-4-甲酰胺)
在配备磁力搅拌棒和氮气入口的圆底烧瓶中,添加2-(二氢吲哚-1-基)丙烷-1-胺(iii)(0.15g,0.60mmol)、2-(吡啶-4-基)噻唑-4-羧酸(0.149g,0.72mmol)和hobt-水合物(0.11g,0.72mmol)在6mldmf中的混合物。还向上述溶液添加hbtu(0.27g,0.72mmol)和二异丙胺(0.28ml,1.60mmol)。将混合物在室温下搅拌16h。向反应混合物添加饱和k2co3水溶液,然后用ch2cl2提取。然后将合并的有机层用水、盐水洗涤,经na2so4干燥并浓缩。粗产物通过柱色谱法用0-2%meoh的ch2cl2溶液进行纯化。化合物通过hplc进一步纯化,给出20mg(9%)纯的目标化合物。1hnmr(400mhz,cdcl3)δ8.71(d,j=6hz,2h),8.22(s,1h),7.71(d,j=6hz,2h),7.68(bs,nh),7.11(d,j=7hz,1h),7.07(t,j=7hz,1h),6.66(t,j=7hz,1h),6.56(d,j=7hz,1h),4.06-3.97(m,1h),3.79(ddd,j=13.8,7.0,5.3hz,1h),3.62–3.31(m,3h),3.04(t,j=9hz,2h),1.24(d,j=9hz,3h)。hplc-ms:预期:365(mh+);实测:365。
uanox034(n-(2-(二氢吲哚-1-基)丙基)-4-甲氧基苯磺酰胺)
uanox034按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.82(d,j=8hz,2h),7.09-7.04(m,2h),7.01(d,j=8hz,2h),6.69(t,j=8hz,1h),6.31(d,j=8hz,1h),4.94-4.91(m,1h),3.92(s,3h),3.73-3.64(m,1h),3.20-3.11(m,2h),3.06-2.96(m,2h),2.94-2.84(m,2h),1.01(dj=8hz,3h)。hplc-ms:预期:347(mh+);实测:347。
uanox035(4-氟-n-(2-(二氢吲哚-1-基)丙基)苯磺酰胺)
uanox035按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.93-7.89(m,2h),7.22(t,j=8hz,2h),7.09(d,j=8hz,1h),7.05(t,j=8hz,1h),6.71(t,j=8hz,1h),6.32(d,j=8hz,1h),4.98(d,j=8hz,1h),3.75-3.66(m,1h),3.23-3.13(m,2h),3.08-2.86(m,4h),1.03(dj=8hz,3h)。hplc-ms:预期:335(mh+);实测:335。所述消旋混合物通过制备型手性hplc分离。
对映体a:1hnmr(400mhz,cdcl3)δ7.92-7.89(m,2h),7.21(t,j=8hz,2h),7.09(d,j=8hz,1h),7.07(t,j=8hz,1h),6.69(t,j=8hz,1h),6.32(d,j=8hz,1h),5.07(bs,1h),3.74-3.66(m,1h),3.21-3.13(m,2h),3.09-2.85(m,4h),1.04(dj=8hz,3h)。hplc-ms:预期:335(mh+);实测:335。
对映体b:1hnmr(400mhz,cdcl3)δ7.92-7.89(m,2h),7.21(t,j=8hz,2h),7.09(d,j=8hz,1h),7.07(t,j=8hz,1h),6.69(t,j=8hz,1h),6.32(d,j=8hz,1h),5.07(bs,1h),3.74-3.66(m,1h),3.21-3.13(m,2h),3.09-2.85(m,4h),1.04(dj=8hz,3h)。hplc-ms:预期:335(mh+);实测:335.
uanox037(4-羟基-n-(2-(二氢吲哚-1-基)丙基)哌嗪-1-磺酰胺)
uanox037按照对化合物uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.11-7.07(m,2h),6.70(t,j=8hz,1h),6.51(d,j=8hz,1h),5.14(bs,1h),3.92-3.84(m,1h),3.74(bs,4h),3.40-3.34(m,2h),3.19(t,j=8hz,2h),2.99(t,j=8hz,2h),2.75(bs,4h),2.49(bs,3h),1.11(d,j=6.8hz,3h)。hplc-ms:预期:339(mh+);实测:339。
uanox049(n-(2-(二氢吲哚-1-基)丙基)-4-(三氟甲氧基)苯磺酰胺)
uanox049按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.93(d,j=12hz,2h),7.35(d,j=8hz,2h),7.08(d,j=8hz,1h),7.04(t,j=8hz,1h),6.70(t,j=8hz,1h),6.30(d,j=8hz,1h),5.17(dd,j=8.4,2.3hz,1h),3.74-3.66(m,1h),3.32-3.13(m,2h),3.09-3.00(m,2h),2.97-2.84(m,2h),1.05(d,j=6.8hz,3h)。hplc-ms:预期:401(mh+);实测:401。
uanox048(n-(2-(二氢吲哚-1-基)丙基)-4-(三氟甲基)苯磺酰胺)
uanox048按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ8.01(d,j=7.6hz,2h),7.78(d,j=8.2hz,2h),7.08(d,j=8.3hz,1h),7.04(t,j=7.1hz,1h),6.70(t,j=7.8hz,1h),6.28(d,j=7.9hz,1h),5.32-5.26(m,1h),3.77–3.64(m,1h),3.29–2.77(m,6h),1.05(d,j=6.7hz,3h)。hplc-ms:预期:385(mh+);实测:385。
uanox055(n-(2-(二氢吲哚-1-基)丙基)-2-苯基噻唑-4-甲酰胺)
uanox055按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.10(s,1h),7.90-7.87(m,2h),7.71(s,nh),7.4-7.44(m,3h),7.12-7.06(m,2h),6.67(t,j=8hz,1h),6.57(d,j=8hz,1h),4.01(dp,j=9.4,6.6hz,1h),),3.78(ddd,j=13.7,7.0,5.6hz,1h),3.59-3.39(m,3h),3.04(t,j=8hz,2h),3.03(d,j=8hz,3h)。hplc-ms:预期:364(mh+);实测:364。
uanox073(4-氟-n-(2-(二氢吲哚-1-基)丙基)苯磺酰胺)
uanox073按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.98(d,j=8.7hz,1h),7.80(d,j=8.7hz,1h),7.11–7.00(m,2h),6.72(t,j=7.8hz,1h),6.30(d,j=7.9hz,1h),5.15(d,j=6.9hz,1h),3.80–3.52(m,1h),3.31–3.13(m,2h),3.13–3.00(m,2h),2.98–2.83(m,2h),1.06(d,j=6.7hz,3h)。hplc-ms:预期:342(mh+);实测:342。
uanox056(n-(2-(二氢吲哚-1-基)丙基)-2-(4-(三氟甲基)苯基)噻唑-4-甲酰胺)
uanox056按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.53(s,1h),8.34(d,j=8hz,2h),8.06(d,j=12hz,2h+1nh),7.48(d,j=8hz,1h),7.44(t,j=8hz,1h),7.03(t,j=8hz,1h),6.92(d,j=8hz,1h),4.40-4.34(m,1h),4.18-4.12(m,1h),3.93-3.75(m,3h),3.39(d,j=8hz,2h),1.59(d,j=8hz,3h)。hplc-ms:预期:432(mh+);实测:432。
uanox054(n-(2-(二氢吲哚-1-基)丙基)-2-(4-(甲氧基)苯基)噻唑-4-甲酰胺)
uanox05按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.02(s,1h),7.82(d,j=8hz,2h),7.71(s,nh),7.11(d,j=8hz,1h),7.09(t,j=8hz,1h),6.96(d,j=8hz,2h),6.66(t,j=8hz,1h),6.57(d,j=8hz,1h),4.03-3.97(m,1h),3.89(s,3h),3.81-3.74(m,1h),3.58-3.39(m,3h),3.04(t,j=8hz,2h),1.23(d,j=8hz,3h)。hplc-ms:预期:394(mh+);实测:394。
uanox069(n-(2-(二氢吲哚-1-基)丙基)-2,3-二氢苯并[b][1,4]二噁英-6-磺酰胺)
uanox069按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.42(d,j=2.2hz,1h),7.37(dd,j=8.5,2.2hz,1h),7.13–7.02(m,2h),6.98(d,j=8.7hz,1h),6.69(td,j=7.4,0.9hz,1h),6.34(d,j=7.9hz,2h),4.89(d,j=8.8hz,1h,nh),4.41–4.20(m,4h),3.76–3.66(m,1h),3.21–3.10(m,2h),3.06(td,j=8.4,4.4hz,1h),2.99(ddd,j=12.7,10.5,2.4hz,1h),2.95–2.89(m,2h),1.04(d,j=6.7hz,3h)。hplc-ms:预期:375(mh+);实测:375。
uanox071(n-(2-(二氢吲哚-1-基)丙基)-4-苯氧基苯磺酰胺)
uanox071按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.84(d,j=8.9hz,2h),7.45(dd,j=8.5,7.5hz,2h),7.28–7.21(m,1h),7.13–7.01(m,6h),6.70(t,j=7.4hz,1h),6.33(d,j=7.9hz,1h),4.97(d,j=9.6hz,1h,nh),3.80–3.51(m,1h),3.24–3.12(m,2h),3.07(dt,j=8.6,4.0hz,1h),3.01(dt,j=12.6,10.4,1h),2.98–2.83(m,2h),1.05(d,j=6.7hz,3h)。hplc-ms:预期:409(mh+);实测:409。
uanox070(n-(2-(二氢吲哚-1-基)丙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺)
uanox070按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ8.47(dt,j=2.6,0.9hz,1h),8.01(ddd,j=8.6,2.5,0.6hz,1h),7.95(d,j=8.6hz,2h),7.33(d,j=9.0hz,2h),7.15(dp,j=8.6,0.6hz,1h),7.09(d,j=7.1hz,1h),7.04(t,j=7.7hz,1h),6.71(dd,j=7.4,0.8hz,1h),6.37(d,j=7.9hz,1h),5.02(d,j=9.7hz,1h,nh),3.72(dt,j=11.1,6.8hz,1h),3.33–3.14(m,2h),3.14–3.00(m,2h),2.99–2.87(m,2h),1.06(d,j=6.7hz,3h)。hplc-ms:预期:478(mh+);实测:478。
uanox072(3,4-二氟-n-(2-(二氢吲哚-1-基)丙基)苯磺酰胺)
uanox072按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.73(ddd,j=9.3,7.2,2.2hz,1h),7.70–7.63(m,1h),7.33(ddd,j=9.6,8.6,7.3hz,1h),7.12–7.02(m,2h),6.71(t,j=7.4hz,1h),6.35(d,j=7.9hz,1h),5.07(d,j=9.8hz,1h,nh),3.73(dt,j=11.0,6.8hz,1h),3.28–3.14(m,2h),3.10(td,j=8.7,4.1hz,1h),3.02(tdd,j=12.6,10.4,2.4hz,1h),2.96–2.89(m,2h),1.06(d,j=6.7hz,3h)。hplc-ms:预期:353(mh+);实测:353。
uanox083(n-(n,n-二乙基氨基磺酰基)-2-(二氢吲哚-1-基)-2-甲基丙烷-1-胺)
uanox083按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ6.69(d,j=7.5hz,1h),6.61(t,j=8.1hz,1h),6.45–6.02(m,2h),4.25(t,j=6.4hz,1h),3.00(t,j=8.6hz,2h),2.93–2.74(m,6h),2.49(t,j=8.3hz,2h),0.95(s,6h),0.78(t,j=7.1hz,6h)。hplc-ms:预期:326(mh+);实测:326。
uanox084(n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-(三氟甲基)苯磺酰胺)
uanox084按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.81(d,j=8.3hz,2h),7.62(d,j=8.4hz,2h),6.95(d,j=7.1hz,1h),6.63(t,j=7.7hz,1h),6.56(d,j=7.7hz,1h),6.06(d,j=7.9hz,1h),5.02(t,j=5.4hz,1h),3.24(t,j=8.3hz,2h),3.12(d,j=5.4hz,2h),2.76(t,j=8.3hz,2h),1.19(s,6h)。hplc-ms:预期:399(mh+);实测:399。
uanox085(n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-苯氧基苯磺酰胺)
uanox085按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.98(d,j=8.9hz,2h),7.67(t,j=7.9hz,2h),7.52–7.43(m,1h),7.33(d,j=7.8hz,2h),7.29(d,j=7.0hz,1h),7.24(d,j=8.9hz,2h),7.06(t,j=7.7hz,1h),6.89(t,j=7.3hz,1h),6.51(d,j=8.0hz,1h),5.20(t,j=5.6hz,1h),3.59(t,j=8.3hz,2h),3.44(d,j=5.6hz,2h),3.11(t,j=8.3hz,2h),1.53(s,6h)。hplc-ms:预期:423(mh+);实测:423。
uanox086(4-氟-n-(2-(二氢吲哚-1-基)-2-甲基丙基)苯磺酰胺)
uanox086按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.85-7.81(m,2h),7.18(td,j=8.6,2.6hz,2h),7.09(d,j=7.0hz,1h),6.81(t,j=7.9hz,1h),6.69(td,j=7.4,2.2hz,1h),6.24(dd,j=8.1,2.2hz,1h),5.02(s,1h),3.37(td,j=8.3,2.5hz,2h),3.22(dd,j=5.6,2.6hz,2h),2.90(t,j=8.0hz,2h),1.31(s,6h)。hplc-ms:预期:349(mh+);实测:349。
uanox087(3,4-二氟-n-(2-(二氢吲哚-1-基)-2-甲基丙基)苯磺酰胺)
uanox087按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.69(t,j=9.2hz,1h),7.67–7.58(m,1h),7.31(q,j=8.0hz,1h),7.13(d,j=7.2hz,1h),6.86(d,j=7.8hz,1h),6.73(t,j=7.3hz,1h),6.30(d,j=8.0hz,1h),5.13(s,1h),3.41(t,j=8.3hz,2h),3.27(d,j=5.4hz,2h),2.93(t,j=8.2hz,2h),1.35(s,6h)。lcms:预期(m+h):367(m+h)+和389(m+na)+;实测:367和389。
uanox088(n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-((5-(三氟甲基)吡啶-2-基)氧基)苯磺酰胺)
uanox088按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ8.42(s,1h),7.94(dd,j=8.5,2.6hz,1h),7.81(d,j=8.9hz,2h),7.26–7.20(m,2h),7.08(d,j=8.1hz,1h),7.02(d,j=7.9hz,1h),6.81(t,j=7.7hz,1h),6.61(t,j=7.3hz,1h),6.23(d,j=8.0hz,1h),4.94(t,j=5.8hz,1h),3.32(t,j=8.4hz,2h),3.20(d,j=5.5hz,2h),2.84(t,j=8.4hz,2h),1.26(s,6h)。lcms:预期:492(mh+);实测:492。
uanox089(n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-甲氧基苯磺酰胺)
uanox089按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.77(d,j=10.7hz,2h),7.10(d,j=7.3hz,1h),6.99(d,j=7.2hz,2h),6.82(t,j=8.0hz,1h),6.69(t,j=7.8hz,1h),6.26(d,j=7.9hz,1h),4.93(t,j=5.5hz,1h),3.94(s,3h),3.39(t,j=8.7hz,2h),3.21(d,j=7.1hz,2h),2.91(t,j=8.3hz,2h),1.33(s,6h)。lcms:预期:361(mh+);实测:361。
uanox090(n-(2-(二氢吲哚-1-基)-2-甲基丙基)-4-(三氟甲氧基)苯磺酰胺)
uanox090按照对uanox001描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.84(d,j=8.5hz,2h),7.30(d,j=8.3hz,2h),7.06(d,j=7.1hz,1h),6.75(d,j=7.8hz,1h),6.67(d,j=7.3hz,1h),6.20(d,j=8.0hz,1h),5.09(s,1h),3.35(t,j=8.3hz,2h),3.22(d,j=5.4hz,2h),2.87(t,j=8.3hz,2h),1.29(s,6h)。lcms:预期:415(m+h)和437(m+na);实测:415和437。
5-溴二氢吲哚-1-羧酸叔丁酯(iv)的合成:向配备氮气入口和磁力搅拌棒的圆底烧瓶中,添加5-溴二氢吲哚(5g,25.24mmol)在200mlmeoh中的溶液。向上述溶液添加k2co3(4.2g,30.89mmol),然后将反应搅拌30分钟,之后添加boc酐(7.0g,32.07mmol)。然后将混合物在室温下搅拌72hr,然后用水(300ml)稀释。含水混合物用ch2cl2(100mlx3)提取。将合并的有机层用无水na2so4干燥,浓缩,得到7.25g粗产物。粗产物通过柱色谱法纯化。目标混合物用10-20%etoac的己烷溶液洗脱,产生5.65g(75%)目标产物。1hnmr(400mhz,cdcl3)δ7.28(bs,3h),4.00(t,j=8hz,2h),3.10(t,j=8hz,2h),1.58(s,9h)。
5-(3-甲氧基苯基)二氢吲哚-1-羧酸叔丁酯(v)的合成:在配备磁力搅拌棒和氮气入口的圆底烧瓶中,添加5-溴二氢吲哚-1-羧酸叔丁酯(1.2g,4.04mmol)和(3-甲氧基苯基)硼酸(0.73g,4.80mmol)、na2co3(0.852g,8.04mmol)和pd(pph3)4(0.464g,0.40mmol)在24mldmf/h2o(1:1)中的溶液。将反应混合物在90℃加热18hr。然后将反应混合物冷却至室温并添加80ml水。然后用ch2cl2(50mlx4)提取水溶液,经na2so4干燥,浓缩,产生2.53g黑油。然后将粗产物通过柱色谱法用10-20%etoac的己烷溶液纯化,给出0.846g(64%)的目标混合物,为白色固体。1hnmr(400mhz,氯仿-d)δ7.44–7.38(m,3h),7.35(t,j=7.9hz,1h),7.17(ddd,j=7.7,1.7,1.0hz,1h),7.11(dd,j=2.4,1.7hz,1h),6.88(ddd,j=8.2,2.6,0.9hz,1h),4.07(t,j=8hz,2h),3.89(s,3h),3.17(t,j=8hz,2h),1.61(s,9h)。
5-(3-甲氧基苯基)二氢吲哚(vi)的合成:在配备氮气入口和磁力搅拌棒的圆底烧瓶中,添加5-(4-甲氧基苯基)二氢吲哚-1-羧酸叔丁酯(0.846g,2.6mmol)在40mlch2cl2中的溶液。向上述溶液添加11mlcf3cooh,并将混合物在室温下搅拌过夜。通过tlc监测反应。反应完成后,除去溶剂。将残余物溶于水中,然后添加饱和na2co3水溶液调节ph=11。然后用ch2cl2(30mlx3)提取水层。将合并的有机层浓缩,然后真空干燥,给出0.60mg(100%)的目标产物。1hnmr(400mhz,cdcl3)δ7.40(bs,1h),7.32(四重峰,j=8hz,2h),7.15(dd,j=8hz,2hz,jmeta=0.8hz,1h),7.10-7.09(m,1h),6.68(dd,j=8hz,2.6hz,jmeta=0.8hz,1h),6.62(d,j=8hz,1h),3.89(s,3h),3.65(t,j=8hz,2h),3.13(t,j=8hz,2h)。
2-(5-(3-甲氧基苯基)二氢吲哚-1-基)丙酰胺(vii)的合成:向配备氮气入口和回流冷凝器的圆底烧瓶中,添加5-(3-甲氧基苯基)二氢吲哚(829mg,3.68mmol)在7mldmf中的溶液。向上述溶液添加k2co3(1.39g,10.1mmol),并将反应混合物搅拌30min。然后向混合物添加碘化钾(70mg,0.42mmol)和2-溴丙酰胺(616mg,1.71mmol),然后在110℃加热2hr。将反应冷却至室温,然后用40ml水稀释。用ch2cl2(20mlx3)提取含水混合物。将合并的有机层经无水na2so4干燥并浓缩,产生棕色油,为粗产物。将粗产物用70%etoac的己烷作为洗脱液纯化,给出1.024g(94%)浅棕色油,为目标产物。1hnmr(400mhz,cdcl3)δ7.39(bs,1h),7.34-7.31(m,2h),7.13(ddd,j=7.6,1.6,0.9hz,1h),7.08-7.07(m,1h),6.84(ddd,j=8.2,2.5,0.8hz,1h),6.55(d,j=8hz,1h),4.02(四重峰,j=8hz,1h),3.87(s,3h),3.56(四重峰,j=8hz,1h),3.50(四重峰,j=8hz,1h),3.09(t,j=8hz,2h),1.47(d,j=8hz,3h)。
2-(5-(3-甲氧基苯基)二氢吲哚-1-基)丙烷-1-胺(viii)的合成:将溶于1mbh3·thf(20ml)中的2-(5-(3-甲氧基苯基)二氢吲哚-1-基)丙酰胺(6.83mmol,2.024g)添加到配备氮气入口和回流冷凝器的圆底烧瓶中。将反应混合物加热回流24小时。通过tlc监测反应。反应完成后,让混合物冷却至室温,然后用meoh缓慢淬灭。浓缩溶液,溶解在meoh中,并再次浓缩。将所生成的油用醚稀释,并用1nhcl提取两次。将水溶液用2.5nnaoh处理以调节ph>10并用氯仿提取。将合并的氯仿提取液经na2so4干燥,浓缩,提供黄色油,为粗产物。将粗产物用5%meoh的ch2cl2溶液进行柱色谱分离。将含有目标产物的合并级分浓缩,然后真空干燥,得到820mg(43%)的产物。1hnmr(400mhz,cdcl3)δ7.35–7.29(m,3h),7.13(dd,j=8hz,2hz,jmeta=0.8hz,1h),7.09-7.08(m,1h),6.84(dd,,j=8hz,3.6hz,jmeta=1.2hz,1h),6.55(d,j=8hz,1h),3.88(s,3h),3.75-3.66(m,1h),3.48-3.36(m,2h),3.06(t,j=8hz,2h),2.94-2.78(m,2h),1.12(d,j=8hz,3h)。
uanox036(n-(2-(5-(3-甲氧基苯基)二氢吲哚-1-基)丙基)-n,n-二乙基-1-磺酰胺)
uanox036按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.35-7.33(m,3h),7.14(d,j=8hz,1h),7.08(t,j=2.4hz,1h),6.84(dd,j=7hz,2.4hz,1h),6.56(d,j=8hz,1h),4.60(bs,1h),3.96-3.87(m,1h),3.88(s,3h),3.45-3.36(m,2h),3.33(四重峰,j=6.8hz,4h),3.18-3.11(m,2h),3.08-3.04(m,2h),1.23(t,j=8hz,6h),1.15(d,j=6.8hz,3h)。hplc-ms:预期:418(mh+);实测:418。
uanox0254(n-(2-(5-(3-甲氧基苯基)二氢吲哚-1-基)丙基)-4-甲基哌嗪-1-磺酰胺)
uanox0254按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.36-7.32(m,2h),7.30(bs,1h),7.14(dd,j=8hz,2hz,jmeta=0.8hz,1h),7.09-7.08(m,1h),6.82(dd,j=7hz,2.4hz,1h),3.91(t,j=8hz,1h),3.88(s,3h),3.44-3.32(m,2h),3.29(t,j=5hz,4h),3.22(t,j=6.8hz,2h),3.08-3.04(m,2h),2.51(t,j=8hz,4h),2.35(s,3h),1.15(d,j=8hz,3h)。hplc-ms:预期:445(mh+);实测:445。
2-溴-1-(二氢吲哚-1-基)乙-1-酮(中间体ixa)的合成
向配备氮气入口和磁力搅拌棒的圆底烧瓶中,添加二氢吲哚(1.07g,8.9mmol,1ml)在10mlch2cl2中的溶液。向上述溶液添加et3n(0.90g,1.24mmol)并随后添加2-溴乙酰溴(1.8g,0.78ml,8.9mmol)。将混合物在室温下搅拌过夜。然后浓缩混合物。将残余物用水、然后用et2o洗涤,真空干燥产生2.12g(99%)的目标产物。1hnmr(400mhz,cdcl3)δ8.10(d,j=8hz,1h),7.27(d,j=8hz,1h),7.19(四重峰,j=8hz,1h),7.09(t,j=8hz,jmeta=1.2hz,1h),4.25(t,j=8hz,2h),4.15(s,2h),3.23(t,j=8hz,2h)。hplc-ms:预期:364(mh+);实测:364。
3-溴-1-(二氢吲哚-1-基)丙-1-酮(中间体ixb)的合成
将二氢吲哚(1.07g,8.9mmol,1ml)在10mlch2cl2中的溶液添加到配备氮气入口和磁力搅拌棒的圆底烧瓶中。向上述溶液添加et3n(0.90g,1.24mmol)并随后添加3-溴丙酰氯(1.53g,0.9ml,8.9mmol)。将混合物在室温下搅拌过夜。然后浓缩混合物,给出2.92g粗产物。将残余物用水、然后用et2o洗涤,真空干燥产生2.4g(100%)的粗产物,将其就此用于下一步。1hnmr(400mhz,cdcl3)δ8.13(d,j=8hz,1h),7.25(d,j=8hz,1h),7.18(t,j=8hz,1h),7.04(t,j=8hz,1h),4.16(t,j=8hz,2h),3.74(t,j=8hz,2h),3.32(t,j=8hz,2h),3.15(t,j=8hz,2h)。hplc-ms:预期:254(mh+);实测:254。
4-(2-(二氢吲哚-1-基)-2-氧代乙基)哌嗪-1-羧酸叔丁酯(中间体xa)的合成
在配备氮气入口和磁力搅拌棒的圆底烧瓶中,添加2-溴-1-(二氢吲哚-1-基)乙-1-酮(0.2g,0.83mmol)在5mlch2cl2中的溶液。向上述溶液添加k2co3(0.29g,2.10mmol)和哌嗪-1-羧酸叔丁酯(0.31g,1.67mmol)。将混合物在室温下搅拌过夜,然后用水(15ml)洗涤。然后用ch2cl2(10mlx3)提取水层。将合并的有机层浓缩,并使用柱色谱法纯化粗产物。用2%meoh的ch2cl2溶液洗脱目标产物,产生176mg(61%)的目标产物。1hnmr(400mhz,cdcl3)δ8.24(d,j=8hz,1h),7.23-7.19(m,2h),7.04(t,j=8hz,1h),4.16(t,j=8hz,2h),3.50(t,j=8hz,4h),3.28(s,2h),3.21(t,j=8hz,2h),2.58(t,j=8hz,4h),1.61(s,9h)。hplc-ms:预期:346(mh+);实测:346。
4-(3-(二氢吲哚-1-基)-3-氧代丙基)哌嗪-1-羧酸叔丁酯(中间体xb)的合成
化合物xb按照对化合物xa描述的程序合成。1hnmr(400mhz,cdcl3)δ8.24(d,j=8hz,1h),7.24-7.20(m,2h),7.04(t,j=8hz,1h),4.10(t,j=8hz,2h),3.47(t,j=8hz,4h),3.24(t,j=8hz,2h),2.88(t,j=8hz,2h),2.67(t,j=8hz,2h),2.50(t,j=8hz,4h),1.61(s,9h)。hplc-ms:预期:360(mh+);实测:360。
1-(二氢吲哚-1-基)-2-(哌嗪-1-基)乙-1-酮(中间体xia)的合成
在配备氮气入口和磁力搅拌棒的圆底烧瓶中,添加3-溴-1-(二氢吲哚-1-基)丙-1-酮(1.1g,4.58mmol)在25mlch2cl2中的溶液。向上述溶液添加k2co3(1.56g,11.30mmol)和哌嗪-1-羧酸叔丁酯(1.70g,9.16mmol)。将混合物在室温下搅拌过夜,然后溶解在35ml水中。然后用ch2cl2(25mlx3)提取水层。将合并的有机层浓缩,产生1.86g粗产物。将粗产物通过柱色谱法纯化并用2%meoh的ch2cl2溶液洗脱目标产物,产生1.46g(92%)目标产物。1hnmr(400mhz,cdcl3)δ8.25(d,j=8hz,1h),7.24-7.21(m,2h),7.06(t,j=8hz,1h),4.19(t,j=8hz,2h),3.52(t,j=8hz,4h),3.30(s,2h),3.23(t,j=8hz,2h),2.59(t,j=8hz,4h)。hplc-ms:预期:246(mh+);实测:246。
1-(二氢吲哚-1-基)-3-(哌嗪-1-基)丙-1-酮(中间体xib)的合成
将4-(3-(二氢吲哚-1-基)-3-氧代丙基)哌嗪-1-羧酸叔丁酯(1.2g,3.34mmol)在50mlch2cl2中的溶液添加到配备氮气入口和磁力搅拌棒的圆底烧瓶中。向上述溶液添加12mlcf3cooh,将混合物在室温下搅拌过夜。然后用饱和na2co3水溶液将混合物调节至ph11,然后分离层。然后用ch2cl2(40mlx3)提取水层。将合并的有机层浓缩,产生0.78g(90%)的目标产物。1hnmr(400mhz,氯仿-d)δ8.26(d,j=8.2hz,1h),7.22(t,j=7.9hz,2h),7.12–6.96(m,1h),4.21(t,j=8.5hz,2h),3.23(t,j=8.5hz,2h),3.02–2.93(m,4h),2.66-2.58(m,4h),1.86-1.75(m,4h)。hplc-ms:预期:260(mh+);实测:260。
uanox028(4-(2-(二氢吲哚-1-基)-2-氧代乙基)-n,n-二甲基哌嗪-1-磺酰胺)
uanox028按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.21(d,j=8hz,1h),7.20-7.17(m,2h),7.04(t,j=8hz,1h),4.11(t,j=8hz,2h),3.33(t,j=8hz,4h),3.29(s,2h),3.20(t,j=8hz,2h),2.83(s,6h),2.68(t,j=8hz,4h)。hplc-ms:预期:353(mh+);实测:353。
uanox025(n,n-二乙基-4-(2-(二氢吲哚-1-基)-2-氧代乙基)哌嗪-1-磺酰胺)
uanox025按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.21(d,j=8hz,1h),7.21-7.17(m,2h),7.03(t,j=8hz,1h),4.13(t,j=8hz,2h),3.30-3.25(m,10h),3.20(t,j=8hz,2h),2.68(t,j=8hz,4h),1.16(t,j=7hz,6h)。hplc-ms:预期:381(mh+);实测:381。
uanox026(1-(二氢吲哚-1-基)-2-(4-(吗啉代磺酰基)哌嗪-1-基)乙-1-酮)
uanox026按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.24(d,j=8hz,1h),7.24-7.21(m,2h),7.06(t,j=8hz,1h),4.14(t,j=8hz,2h),3.75(t,j=5hz,4h),3.39(t,j=5hz,4h),3.34(s,2h),3.26(t,j=8hz,4h),3.24(t,j=8hz,2h),,2.73(t,j=8hz,4h)。hplc-ms:预期:395(mh+);实测:395。
uanox027(1-(二氢吲哚-1-基)-2-(4-(哌啶-1-基磺酰基)哌嗪-1-基)乙-1-酮)
uanox027按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.23(d,j=8hz,1h),7.22-7.18(m,2h),7.04(t,j=8hz,1h),4.13(t,j=8hz,2h),3.34-3.30(m,6h),3.25-3.19(m,6h),2.69(t,j=8hz,4h),1.65-1.60(m,4h),1.58-1.53(m,2h)。hplc-ms:预期:393(mh+);实测:393。
uanox0192(1-(二氢吲哚-1-基)-2-(4-(嘧啶-2-基)哌嗪-1-基)乙-1-酮)
在配备氮气入口和磁力搅拌棒的圆底烧瓶中,添加2-溴-1-(二氢吲哚-1-基)乙-1-酮(0.2g,0.83mmol)在5mlch2cl2中的溶液。向上述溶液添加k2co3(0.29g,2.10mmol)并还添加2-(哌嗪-1-基)嘧啶(0.27g,1.64mmol)。将混合物在室温下搅拌过夜,然后用15ml水洗涤。然后用ch2cl2(10mlx3)洗涤水层。将合并的有机层浓缩,给出粗产物。粗产物利用柱色谱法用2%meoh的ch2cl2溶液纯化,产生120mg(45%)的目标产物。获得的级分使用相同条件进一步纯化,得到106mg纯的目标产物。1hnmr(400mhz,cdcl3)δ8.33(d,j=4hz,2h),8.27(d,j=8hz,1h),7.25-7.21(m,2h),7.05(t,j=8hz,1h),6.50(t,j=4hz,1h),4.21(t,j=4hz,2h),3.92(t,j=8hz,4h),3.33(s,2h),3.24(t,j=8hz,2h),2.71(t,j=8hz,4h)。hplc-ms:预期:324(mh+);实测:324。
uanox032(4-(3-(二氢吲哚-1-基)-3-氧代丙基)-n,n-二甲基哌嗪-1-磺酰胺)
uanox032按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.22(d,j=8hz,1h),7.23-7.19(m,2h),7.04(t,j=8hz,1h),4.09(t,j=8hz,2h),3.30(t,j=5hz,4h),3.23(t,j=8hz,2h),2.90(t,j=8hz,2h),2.86(s,6h),2.65(t,j=5hz,2h),2.60(t,j=5hz,4h)。hplc-ms:预期:367(mh+);实测:367。
uanox029(n,n-二乙基-4-(3-(二氢吲哚-1-基)-3-氧代丙基)哌嗪-1-磺酰胺)
uanox029按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.23(d,j=8hz,1h),7.21-7.19(m,2h),7.04(t,j=8hz,1h),4.09(t,j=8hz,2h),3.29(四重峰,j=8hz,4h),3.35-3.21(m,6h),2.89(t,j=8hz,2h),2.65(t,j=8hz,2h),2.60(d,j=8hz,4h),1.21(t,j=8hz,6h)。hplc-ms:预期:395(mh+);实测:395。
uanox030(1-(二氢吲哚-1-基)-3-(4-(吗啉代磺酰基)哌嗪-1-基)丙-1-酮)
uanox030按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.23(d,j=8hz,1h),7.24-7.20(m,2h),7.04(t,j=8hz,1h),4.10(t,j=8hz,2h),3.76-3.74(m,4h),3.33(t,j=8hz,4h),3.27-3.22(m,6h),2.91(t,j=8hz,2h),2.66(t,j=8hz,2h),2.61(t,j=5hz,4h)。hplc-ms:预期:409(mh+);实测:409。
uanox031(1-(二氢吲哚-1-基)-3-(4-(哌啶-1-基磺酰基)哌嗪-1-基)丙-1-酮)
uanox031按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ8.23(d,j=8hz,1h),7.24-7.20(m,2h),7.04(t,j=8hz,1h),4.10(t,j=8hz,2h),3.30(t,j=5hz,4h),3.26-3.22(m,6h),2.91(t,j=8hz,2h),2.67(t,j=8hz,2h),2.61(t,j=5hz,4h),1.67-1.56(m,6h)。hplc-ms:预期:407(mh+);实测:407。
uanox022(1-(二氢吲哚-1-基)-3-(4-(嘧啶-2-基)哌嗪-1-基)丙-1-酮)
uanox022按照对化合物50描述的程序合成。1hnmr(400mhz,cdcl3)δ8.32(d,j=4hz,2h),8.24(d,j=8hz,1h),7.25-7.21(m,2h),7.03(t,j=8hz,1h),6.49(t,j=4hz,1h),4.10(t,j=8hz,2h),3.87(t,j=8hz,4h),3.22(t,j=8hz,2h),2.90(t,j=8hz,2h),2.70(t,j=8hz,2h),2.60(t,j=8hz,4h)。hplc-ms:预期:338(mh+)和339(m+2);实测:338和339。
uanox023(2-(环庚基氨基)-1-(二氢吲哚-1-基)乙-1-酮)
将环庚胺(1.87mmol,0.22g,0.24ml)在4mlch3cn中的溶液添加到配备氮气入口和磁力搅拌棒的圆底烧瓶中。向上述溶液滴加在2mlch3cn中的2-溴-1-(二氢吲哚-1-基)乙-1-酮(0.15g,0.624mmol)。将混合物在室温下搅拌过夜,然后浓缩,给出粗产物。产物利用柱色谱法用含2%meoh的ch2cl2溶剂纯化,产生110mg(65%)的目标产物。该化合物使用上述相同的方法再次纯化,给出68mg(40%)如hplc指示的纯化合物。1hnmr(400mhz,cdcl3)δ8.24(d,j=8hz,1h),7.23-7.19(m,2h),7.02(t,j=8hz,1h),4.04(t,j=8hz,2h),3.52(s,2h),3.24(t,j=8hz,2h),2.70(septet,4hz,1h),1.94-1.86(m,2h),1.74-1.67(m,2h),1.62-1.53(m,4h),1.51-1.43(m,4h)。hplc-ms:预期:274(m+2);实测:274。
uanox024(3-(环庚基氨基)-1-(二氢吲哚-1-基)丙-1-酮)
uanox024按照对化合物uanox023描述的程序合成。1hnmr(400mhz,cdcl3)δ8.10(d,j=8hz,1h),7.23-7.19(m,2h),7.08(t,j=8hz,1h),4.08(t,j=8hz,2h),3.41(t,j=8hz,2h),3.36-3.31(m,1h),3.30(四重峰,j=4hz,2h),3.20(t,8hz,2h),2.32-2.25(m,2h),1.97-1.90(m,2h),1.89-1.81(m,2h),1.64-1.61(m,4h),1.59-1.48(m,2h)。hplc-ms:预期:228(m+2);实测:228和339.
1-(4-硝基苯基)二氢吲哚(xii)的合成:将微波小瓶装入4-溴硝基苯(2.16g,10.69mmol)、二氢吲哚(1.28g,10.70mmol)、pd2(dba)3(0.059mmol,53mg)、k2co3(42.69mmol,5.9g)和dmf(5ml)。将混合物在biotageinitiator中以中等功率在140℃加热30min。将反应混合物倒入水中,并用ch2cl2(x3)提取水溶液。将合并的有机层经na2so4干燥,过滤,旋转蒸发,然后真空干燥。将粗产物上样到快速硅胶柱上,用己烷–etoac(4:1)洗脱,得到2.27g(88%)纯化产物,为橙红色固体。1hnmr(400mhz,cdcl3)δ8.24(d,j=8hz,2h),7.37(d,j=8hz,1h),7.30-7.28(m,2h),7.24(d,j=8hz,2h),6.96(t,j=7.4hz,1h),4.10(t,j=8hz,2h),3.24(t,j=8hz,2h)。
4-(二氢吲哚-1-基)苯胺(xiii)的合成:将1-(4-硝基苯基)二氢吲哚(1.43g,9.44mmol)在15mletoh中的溶液添加到配备氮气入口和磁力搅拌棒的圆底烧瓶中。向上述溶液添加sncl2·2h2o(3.35g,14.85mmol),然后将混合物在70℃搅拌过夜。向混合物添加4nnaoh,用etoac(x3)提取水溶液。合并的有机层经无水na2so4干燥,浓缩,然后真空干燥,产生橙褐色油,为粗产物。粗产物用20%etoac的己烷溶液进行色谱分离产生630mg(50%)纯的目标化合物,为紫色固体。1hnmr(400mhz,cdcl3)δ7.16(d,j=8hz,1h),7.12(d,j=8hz,2h),7.05(t,j=8hz,1h),6.82(d,j=8hz,1h),6.76-6.69(m,3h),3.99-3.77(m,2h),3.13(t,j=8hz,2h)。hplc-ms:预期:210(m)+;实测:210。
uanox038(n-(n,n-二乙基氨基磺酰基)-4-(二氢吲哚-1-基)苯胺)
uanox038按照对uanox001描述的程序合成。1hnmr(400mhz,cdcl3)δ7.20-7.18(m,5h),7.10-7.09(m,2h),6.80-6.76(m,1h),3.95(t,j=8hz,2h),3.30(t,j=7hz,2h),3.16(t,j=8hz,2h),1.13(t,j=7hz,2h)。hplc-ms:预期:345(mh+);实测:345。
4-(2-溴乙基)哌嗪-1-羧酸叔丁酯(xvii)的合成
在配备n2入口、磁力搅拌棒和加料漏斗的圆底烧瓶中,添加n-boc-4-(2-羟基乙基)哌嗪(xvi)(1g,4.34mmol)、pph3(1.23g,4.7mmol)ch2cl2(10ml)。在0℃下用2h向上述混合物滴加四溴化碳(1.58g.,4.7mmol)在10mlch2cl2中的溶液。将混合物在室温下搅拌20h。蒸发有机相得到油,将其通过快速色谱法(乙酸乙酯/己烷2/8)纯化,通过目标产物,其为在储存时缓慢结晶的油状化合物(1.32,收率100%)。1hnmr(400mhz,氯仿-d)δ3.51–3.30(m,6h),2.82–2.67(m,2h),2.50–2.23(m,4h),1.43(s,9h)。根据j.med.chem,2004,47,3,711-719和2013年5月10日的pct国际申请,2013064919中报告的程序合成。
4-(2-(二氢吲哚-1-基)乙基)哌嗪-1-羧酸叔丁酯(xviii)的合成
在配备氮气入口和回流冷凝器的圆底烧瓶中,添加二氢吲哚(0.55g,4.62mmol,0.52ml)在5mldmf中的溶液。向上述溶液添加k2co3(1.25g,9.04mmol),然后将混合物搅拌30min。向上述混合物,然后将4-(2-溴乙基)哌嗪-1-羧酸叔丁酯(1.35g,4.60mmol,1eq)添加到混合物中。然后将混合物在110℃加热2hr。然后将混合物用去离子水稀释,用ch2cl2(x3)提取。合并的有机层经无水na2so4干燥,浓缩,然后真空干燥,产生17g粗产物。将油状粗产物用50-70%etoac的己烷溶液进行色谱分离,给出1.3g(87%)纯的目标化合物。1hnmr(400mhz,氯仿-d)δ7.14–6.96(m,2h),6.64(d,j=8.2hz,1h),6.46(d,j=7.6hz,1h),3.43(t,j=4.9hz,4h),3.38(t,j=8.3hz,2h),3.22(t,j=8.3hz,2h),2.94(t,j=6.6hz,2h),2.60(t,j=7.0hz,2h),2.46(t,j=5.0hz,4h),1.44(s,9h)。hplc-ms:预期:333(m+2)+;实测:333。
1-(2-(哌嗪-1-基)乙基)二氢吲哚(xix)的合成
在配备氮气入口和磁力搅拌棒的圆底烧瓶中,添加4-(2-(二氢吲哚-1-基)乙基)哌嗪-1-羧酸叔丁酯(1.3g,3.92mmol)在60mlch2cl2中的溶液。向上述溶液添加17mlcf3cooh,并将混合物在室温下搅拌过夜。用tlc监测反应。将混合物旋转蒸发,溶于水中,然后用饱和na2co3水溶液碱化至ph11,倒入分液漏斗中并分离层。然后用ch2cl2(x3)洗涤水层。将合并的有机层使用旋转蒸发器浓缩,然后真空干燥,产生930mg(100%)目标产物。1hnmr(400mhz,氯仿-d)δ7.06-7.02(m,2h),6.62(t,j=7.4hz,1h),6.47(d,j=8.0hz,1h),3.38(t,j=8.3hz,2h),3.22(t,j=7.8hz,2h),3.00–2.83(m,6h),2.58(t,j=7.1hz,2h),2.55–2.43(m,4h)。hplc-ms:预期:232(mh)+;实测:232。
uanox062(1-(2-(4-((4-(三氟甲氧基)苯基)磺酰基)哌嗪-1-基)乙基)二氢吲哚)
在配备氮气入口和磁力搅拌棒的25-ml圆底烧瓶中,添加154mg(0.67mmol)的1-(2-(哌嗪-1-基)乙基)二氢吲哚、210mg(0.81mmol)的4-(三氟甲氧基)苯磺酰氯、0.19ml(1.36mmol)的三乙胺和5ml的ch2cl2。将混合物在室温下剧烈搅拌18h。向混合物添加去离子水,然后将混合物转移到分液漏斗中,分离层。然后用ch2cl2(x3)洗涤水层。合并的有机提取液经无水na2so4干燥,通过过滤除去干燥剂,并通过旋转蒸发浓缩滤液。将残余物进一步真空干燥,给出浅黄色油,为粗产物。然后将粗产物通过制备型tlc用60%乙酸乙酯的己烷溶液纯化,给出185mg(61%)纯的目标产物,为白色固体。1hnmr(400mhz,氯仿-d)δ7.84(d,j=9.0hz,2h),7.41-7.37(m,2h),7.12–7.00(m,2h),6.66(td,j=7.5,1.0hz,1h),6.45(d,j=7.8hz,1h),3.36(t,j=8hz,2h),3.19(t,j=8hz,2h),3.10(t,j=8hz,4h),2.97(t,j=8hz,2h),2.71–2.60(m,6h)。hplc-ms:预期:456(mh)+;实测:456和454
uanox063(n,n-二乙基-4-(2-(二氢吲哚-1-基)乙基)哌嗪-1-磺酰胺的合成)
uanox063按照对uanox062描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.10-7.06(m,2h),6.67(td,j=7.5,1.0hz,1h),6.50(d,j=7.6hz,1h),3.42(t,j=8.4hz,2h),3.30(q,j=7.0hz,4h),3.27–3.22(m,6h),2.99(t,j=8.3hz,2h),2.66(t,j=8.3hz,2h),2.63–2.59(m,4h),1.21(t,j=7.1hz,6h)。hplc-ms:预期:367(mh)+;实测:367。
uanox064(1-(2-(4-((4-氟苯基)磺酰基)哌嗪-1-基)乙基)二氢吲哚)
uanox064按照对uanox062描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.80(dd,j=9.0,5.1hz,2h),7.24(dd,j=9.0,8.3hz,2h),7.10–7.02(m,2h),6.66(td,j=7.4,1.0hz,1h),6.45(d,j=7.8hz,1h),3.36(t,j=8.4hz,2h),3.19(t,j=8.4hz,2h),3.12–3.06(m,4h),2.96(t,j=8.3hz,2h),2.70–2.60(m,6h)。hplc-ms:预期:390(mh)+;实测:390。
uanox066(1-(2-(4-(苯并[d][1,3]二氧杂环戊烯-5-基磺酰基)哌嗪-1-基)乙基)二氢吲哚的合成)
uanox066按照对uanox062描述的程序合成。1hnmr(400mhz,氯仿-d)δ7.11–7.04(m,2h),6.67(td,j=7.3,1.0hz,1h),6.51(d,j=7.4hz,1h),3.42(t,j=8.4hz,2h),3.31–3.26(m,6h),3.23(q,j=7.1hz,4h),2.99(t,j=8.4hz,2h),2.66(t,j=8.4hz,2h),2.60–2.53(m,4h),1.15(t,j=7.1hz,6h)。hplc-ms:预期:331(mh)+;实测:331
uanox067(1-(2-(4-(2-氟苄基)哌嗪-1-基)乙基)二氢吲哚的合成)
在配备氮气入口和磁力搅拌棒的圆底烧瓶中,添加2-氟苯甲醛(83mg,0.67mmol)、1-(2-(哌嗪-1-基)乙基)二氢吲哚(154mg,0.67mmol)和ch2cl2(5ml)。向上述混合物添加acoh(38μl,0.67mmol)。将反应在室温下搅拌1小时。在2小时时间内分次向混合物添加na(oac)3bh(426mg,2.01mmol)。让反应混合物在室温下搅拌过夜。将反应混合物倒入h2o中并用ch2cl2(x3)提取水溶液。有机层经na2so4干燥,过滤,然后旋转蒸发。粗产物通过制备tlc用含10%meoh的ch2cl2纯化,给出208mg目标产物。该产物使用与上述相同的条件再纯化,得到81mg(36%)纯的目标化合物,为琥珀色油。1hnmr(400mhz,氯仿-d)δ7.39(td,j=7.5,1.8hz,1h),7.31–7.23(m,1h),7.13(td,j=7.5,1.2hz,1h),7.10–7.02(m,3h),6.67(td,j=7.4,1.0hz,1h),6.50(d,j=9.1hz,1h),3.69(d,j=1.3hz,2h),3.40(t,j=8.3hz,2h),3.29(t,j=8.3hz,2h),2.98(t,j=8.3hz,2h),2.73(t,j=8.3hz,4h),2.67-2.58(m,4h),2.10-2.06(m,2h)。hplc-ms:预期:340(mh)+;实测:340。
nox4介导对肺损伤的纤维化反应
nadph氧化酶(nox)酶是一种进化上保守的基因家族,与宿主防御机制、包括肺纤维化的关联最为一致(bernardk等人,antioxidants&redoxsignaling20:2838-2853,2014;thannickalvj,zhouy,gaggara,和duncansr.纤维化:最终和最接近的原因(fibrosis:ultimateandproximatecauses).thejournalofclinicalinvestigation124:4673-4677,2014)。nox4在损伤诱导的纤维化中的作用使用鼠肺损伤模型评估。在这种动物模型中,气管内滴注化疗剂博来霉素来诱导上皮损伤,导致损伤后2-3周达到峰值纤维化(heckerl等人,nadph氧化酶-4介导对肺损伤的肌成纤维细胞活化和纤维化反应(nadphoxidase-4mediatesmyofibroblastactivationandfibrogenicresponsestolunginjury).naturemedicine15:1077-1081,2009;izbickig等人,博莱霉素诱导肺纤维化的时间过程(timecourseofbleomycin-inducedlungfibrosis).internationaljournalofexperimentalpathology83:111-119,2002)。nox4以时间依赖性方式诱导,从第7天开始增加至第28天,支持了肺损伤后nox4表达、肌成纤维细胞活化和纤维化之间的时间关系(naturemedicine15:1077-1081,2009)。相反,nox2同种型(主要在吞噬细胞中表达)在第7天(峰值炎症阶段)增加,并在后来当炎症反应消退时的时间点返回基线水平(naturemedicine15:1077-1081,2009)。
nox4在人类ipf患者的肺中上调
在nox家族的七个成员中,nox4现已牵涉多种纤维化疾病,包括肝脏(aoyamat等人,hepatology56:2316-2327,2012;bettaieba等人,gastroenterology149:468-480e410,2015;sanchop等人,plosone7:e45285,2012)、皮肤(spadonit等人,arthritis&rheumatology67:1611-1622,2015)、肾脏(barnesjl等人,kidneyinternational79:944-956,2011;sedeekm等人,americanjournalofphysiologyrenalphysiology299:f1348-1358,2010)、心脏(agot等人,aging2:1012-1016,2010;kurodaj等人,proceedingsofthenationalacademyofsciencesoftheunitedstatesofamerica107:15565-15570,2010)、和肺脏(griffithb等人,antioxidants&redoxsignaling11:2505-2516,2009;harrisonc等人,natrevdrugdiscov8:773-773,2009;heckerl等人,sciencetranslationalmedicine6:231ra247,2014;naturemedicine15:1077-1081,2009)。已经证明nox4在人ipf患者的肺肌成纤维细胞中上调(amaran等人,thorax65:733-738,2010;sciencetranslationalmedicine6:231ra247,2014)。
治疗性靶向nox4在小鼠中抑制了纤维化的发展并导致已确立/持续的纤维化的逆转。
同时已经表明,基因靶向nox改善了年轻小鼠中损伤诱导的肺纤维化的发展(naturemedicine15:1077-1081,2009)。已经证明,在持续性肺纤维化的动物模型中,nox4的基因击倒(通过气管内递送nox4-sirna至受伤小鼠的肺)导致已确立的纤维化的逆转(sciencetranslationalmedicine6:231ra247,2014)。这后来通过使用具有nox4基因缺失的小鼠的类似发现而证实(carnesecchis等人,antioxidredoxsignal15:607-619,2011)。总体而言,这些研究证明nox4在介导肺纤维化中起关键作用。自从最初发现nox4介导肺组织纤维化(naturemedicine,2009)以来,nox4已经牵涉各种器官系统(肝脏,皮肤,肾脏和心脏)的纤维化疾病。nox4现在被认为是纤维化疾病最有希望的治疗靶之一(natrevdrugdiscov8:773-773,2009;liepelta等人,annalsoftranslationalmedicine3:s13,2015)。然而,临床上没有选择性nox4抑制剂。
类似物抑制nox4依赖性h2o2的功效
利用稳定过表达nox4的hek293细胞(hek/nox4细胞),其产生高水平的h2o2,建立了对nox4抑制的高通量筛选(hts)(chengg等人,gene:2001,131-140页)。已经筛选了超过30,000种化合物,并且药物化学已经导致了众多类似物的合成以及化学上不同的选择性nox4抑制剂系列的鉴定。表1显示了合成的各种类似物的剂量依赖性活性。图1a显示了这些类似物的子集相对于介质和dpi(阳性对照,因为dpi抑制所有nox活性)。通过amplexred试验来测量,用uanox048或uanox034处理导致剂量依赖性减少hek/nox4细胞的h2o2生成(图1a)。评价uanox048的ic-50(图1b)。
表1:nox4-依赖性h2o2的抑制功效
将稳定转染为过表达nox4的hek细胞用在dmso中的测试化合物和合成类似物处理并温育1h。通过amplexred试验评价h2o2产生。数值表示用1、5和10μm(最终浓度)测试化合物和合成类似物处理后的h2o2产生的均值和sd。h2o2产生相对于介质对照报告;n=3-10/组。
将稳定转染为过表达nox4的hek细胞用不同浓度的测试化合物、dpi(全nox抑制剂阳性对照)或dmso(介质对照)处理并温育1h(图1)。(图1a)通过amplexred试验评价h2o2存在。(图1b)在hek/nox4细胞中评价uanox048的ic50,然后被确定为4.8μm。数值表示均值±sem;n=4。p值通过student’s双尾t检验计算。*p<0.05,**p<0.01,***p<0.001。
化合物通过假阳性测试
进行筛选以排除假阳性。uanox048未表现清除剂活性(图2a),未呈现试验干扰(通过抑制hrp活性)(图2b),并且不影响细胞活力(图2c)。
将uanox048、dmso(介质对照)、或过氧化氢酶(已知的清除剂阳性对照)添加到含有外源h2o2(5mm)的无细胞试验中,并通过(图2a)amplexred试验和(图2b)ros-glo试验(无hrp试验系统以排除试验干扰)来评估对h2o2的清除剂活性。(图2c)将稳定转染为过表达nox4的hek细胞用uanox048、洋地黄皂苷(细胞死亡诱导剂)或dmso(介质对照)处理并温育1h。通过celltiter-glo试验评估细胞活力。数值表示均值±sem;n=4;p值通过学生氏双尾t检验计算。*p<0.05,**p<0.01,***p<0.001。
化合物对nox4-依赖性h2o2有高度选择性
没有临床可用的选择性nox4抑制剂。开发了评价针对nox1和nox2的选择性的筛选试验以求鉴定nox4的高选择性抑制剂,而对密切相关的nox同系物具有低选择性。重要的是,类似物对nox2-和nox1-依赖性h2o2几乎没有抑制(图3)。另外,如通过影响黄嘌呤氧化酶(xo)依赖性h2o2生成所测量的,类似物不抑制nox非依赖性机制的h2o2产生。这些数据支持鉴定对nox4有高度选择性的小分子抑制剂。
将caco-2细胞用骨化三醇(1μm,18h,以诱导nox1依赖性h2o2生成)和测试化合物、dpi(全nox抑制剂阳性对照)或dmso(介质对照)共同处理。通过amplexred试验评价h2o2产生(图3a)。将raw264.7细胞用pma(20μm,2h,以诱导nox2-依赖性h2o2生成)和测试化合物、dpi(全nox抑制剂)或dmso(介质)共同处理。通过amplexred试验评价nox2-依赖性h2o2(图3b)。在测试化合物或介质对照(dmso)存在下引发xo-依赖性h2o2产生。将反应温育30m并通过amplexred试验量化h2o2存在(图3c)。数值表示均值±sem;n=3;p值通过学生氏双尾t检验计算。*p<0.05,**p<0.01,***p<0.001。
化合物表现出对人肺成纤维细胞中疾病相关细胞表型的抑制
已经证明,tgf-β1(一种已知在纤维化疾病中高度表达的细胞因子)导致诱导nox4-依赖性h2o2,后者介导关键的促纤维化肺肌成纤维细胞表型,包括分化、收缩和ecm生成(naturemedicine15:1077-1081,2009)。人肺成纤维细胞中的全基因组affymetrix分析显示,响应tgf-β1,nox4是人类基因组中被最高诱导的基因之一(naturemedicine15:1077-1081,2009)。tgf-β1对nox4-依赖性h2o2的诱导性是nox4的高度特异和独特的功能(martynkd等人,cellularsignalling18:69-82,2006;serranderl等人,thebiochemicaljournal406:105-114,2007;vonlohneysenk等人,thejournalofbiologicalchemistry287:8737-8745,2012;vonlohneysenk等人,thejournalofbiologicalchemistry283:35273-35282,2008;vonlohneysenk等人,molecularandcellularbiology30:961-975,2010);没有其它nox家族基因成员在mrna水平受到影响(naturemedicine15:1077-1081,2009)。nox4的这一独特特征已被用于筛选工作中验证前沿候选药物。类似物证明了在人肺成纤维细胞中抑制tgf-β-诱导的nox4-依赖性h2o2的高效力(图4)。
类似物在人肺成纤维细胞中抑制tgf-β-诱导的nox4-依赖性h2o2
将人肺成纤维细胞(imr90细胞)血清饥饿16h,然后用/不用tgf-β1(2ng/ml)刺激12h。然后将细胞用测试化合物、dpi(全nox抑制剂阳性对照)或dmso(介质对照)处理,并再温育4h。通过amplexred试验评价h2o2(图4)。数值表示均值±sem;n=3;*p<0.05,使用学生氏双尾t检验。*p<0.05,**p<0.01,***p<0.001。
tgf-β1-诱导的nox4-依赖性h2o2介导成纤维细胞向肌成纤维细胞分化,其以α-平滑肌肌动蛋白(αsma)的合成为特征。这些关键效应细胞在纤维化“瘢痕”生成中起中心作用,因为它们是负责细胞外基质(ecm)组分合成的收缩细胞。the表达αsma的肌成纤维细胞的积累是纤维化疾病的关键病理标志(desmoulierea等人,theamericanjournalofpathology146:56-66,1995)。评价化合物它们抑制成纤维细胞向肌成纤维细胞分化的能力。类似物有效抑制人肺成纤维细胞中tgf-β诱导的nox4-依赖性肌成纤维细胞分化(图5)。总之,这些数据表明,类似物证明了抑制人肺成纤维细胞中关键促纤维化细胞表型的能力。
类似物抑制tgf-β1-诱导的成纤维细胞向肌成纤维细胞分化
将人肺成纤维细胞(imr90细胞)血清饥饿16h,然后用/不用tgf-β1(2ng/ml)刺激,并用测试化合物、dpi(全nox抑制剂阳性对照)或dmso(介质对照)共处理并温育48h。通过western-免疫印迹(图5a)和光密度分析(图5b)评价αsma存在。数值表示均值±sem;n=4;*p<0.05,使用学生氏双尾t检验。*p<0.05,**p<0.01,***p<0.001。
类似物的生物物理表征和显微镜检查
对所选的类似物的生物物理表征进行了研究,以证明旨在指导合理配方设计和确保在规模放大、制造和储存期间化合物完整性的再现性(即质量控制)的基本要求的可行性。使用差示扫描量热法(dsc),这是一种高灵敏度的热分析技术,用于量化候选药物的热致性质和相变。发现uanox048是高度稳定的,具有比较高的固-液熔融相变;在固-液相变期间测量能量学,t开始89.72±0.22(℃),t峰值92.3±0.05(℃),焓64.87±21.39(j/g)(图6a)。从药物观点来看这很重要,因为这些数据表明uanox048在室温和体温(32-37℃;药物制造/加工和递送温度)下都是高度稳定的。x射线粉末衍射(xrpd)是用于测量粉末中长程分子有序度的非破坏性材料科学“金标准”方法。这对于固态表征至关重要,其中候选药物在任何给定的结晶相下产生独特的图案;这为结晶度鉴定提供了“分子指纹”。uanox048的xrpd显示出独特的分子标签,其在不同时间以不同量合成的uanox048批次之间是一致的(图6b)。衰减全反射傅里叶变换红外(atr-ftir)光谱是一种基于通过共价键中的振动跃迁来吸收红外光的非破坏性分子鉴定工具。这为化学鉴定提供了“分子指纹”。atr-ftir允许在类似的材料和/或批与批间质量验证之间进行精细区分;它用于鉴别活性药物成分(api)。atr-ftir光谱展示来自在不同时间合成的两个不同批次的uanox048的一致分子指纹。xrpd和atr-ftir结果合起来证明了成功和一致的uanox048规模放大的概念验证和可行性。用能量色散x射线(edx)的扫描电子显微术(sem)用于显现合成粒子它们的天然固态并量化直接影响配方的重要粒子性质,包括表面结构、粒子形态和尺寸、以及粒度范围分布。uanox048的sem表明了是具有结晶性质的小分子量药物的典型表面结构。共焦拉曼显微光谱是一种非破坏性分析工具,用于评价配方内化学组分的空间分布;这容许表征配方均匀性和检测外来颗粒污染物。这种关键的分子鉴定工具常规用于确定专利侵权。uanox048的共聚焦拉曼显微光谱展现了其化学身份的独特分子指纹。
类似物证明了口服制剂/递送的有利的体外adme特征
对选定的类似物进行体外吸收、分布、代谢和排泄(adme),以评估它们继续临床前开发的可能性。uanox048类似物具有有利的药代动力学/药效学性质,包括低的分子量(384.4g/mol)、计算logd值(4.07)和极性表面积
已经出于说明和描述的目的介绍了本发明的前述讨论。前述内容并非旨在将本发明限制于本文所公开的形式。虽然本发明的描述包括一个或多个实施方式以及某些变化和修改的描述,但是变化变化和修改也在本发明的范围内,例如,在理解本公开之后,可以在本领域技术人员的技术和知识范围内的。旨在要获得包括在允许程度上的替代实施方式的权利,包括对所要求保护的内容的替代、可互换和/或等同的结构、功能,范围或步骤,无论这样的替代、可互换和/或等同的结构、功能、范围或步骤是否在本文中公开,并且不打算向公众奉献任何可取得专利的主题。本文中引用的所有参考文献通过引用以其整体并入。
- 还没有人留言评论。精彩留言会获得点赞!