具有薄膜台阶覆盖性的涂覆膜、具备该膜的结构基体的制作方法
本发明涉及在至少一部分表面具备最大膜厚与最小膜厚之差为
背景技术:
对于向由各种材料形成的结构基体赋予涂覆膜从而根据目的对其表面性质进行改性的涂覆技术而言,由于各种涂覆剂的开发,其用途逐渐扩展。例如,在从电子材料用途至医疗用材料用途中,已开发·市售有共形涂覆剂(conformalcoatingagent),所述共形涂覆剂即使在具有复杂形状的结构基体的情况下也能够赋予追随其表面形状的涂层。
例如,医疗领域中使用的典型的结构基体为:由将多个(6、24、96、384个等)凹坑(洞或孔;容量:数μl~数ml)以2∶3的比例配置而得的平面基板形成的实验·检测器件即微孔板。通常,基板由树脂制成,设置于该基板上的各孔被用作试管或培养皿,用于有机反应、生化分析或临床检查等。此时,可以根据基板材料的性质、孔的目的对基板、各孔的内表面施以涂覆膜。
为了缓和在化学反应及生物测定中使用光纤面板的相关问题(例如,在邻近的反应室间的光流失及物理干涉等),已报道了具备下述基板的阵列,所述基板为具有表面(所述表面具备多个反应室)及位于上述表面上的薄膜涂层的光纤面板,该薄膜的厚度为0.1~5.0微米且对水呈非渗透性;例如,作为薄膜涂层的例子,可举出二氧化硅(例如,参见专利文献1)。另外,作为细胞培养用载体的表面修饰,报道了赋予可利用热响应性聚合物、ph响应性聚合物或它们的组合来制作的涂层,例如,作为ph响应性聚合物的例子,可举出丙烯酸、丙烯酸二甲基氨基乙酯及丙烯酸羟基乙酯的共聚物(例如,参见专利文献2)。
此外,本申请的发明人着眼于作为具有抑制各种生物材料附着的能力的涂覆材料而受到期待的具有磷酸酯基的聚合物,反复进行了研究。结果,报道了用包含特定的阴离子性基团和阳离子性基团的共聚物涂覆表面的至少一部分而得到的细胞培养容器不仅可抑制细胞向容器表面(内部表面)的附着,并且,涂层可牢固地固着于容器表面,因此,作为涂层向培养液中的溶出、耐放射线性得以改善的细胞培养容器是有用的(例如,参见专利文献3)。
现有技术文献
专利文献
专利文献1:日本特表2008-537679号公报
专利文献2:日本特表2014-501099号公报
专利文献3:国际公开第2014/0196652号公报
技术实现要素:
发明要解决的课题
就可与生物试样接触的结构基体而言,存在下述问题:在基体的表面产生由源自生物试样的细胞、蛋白质带来的粘附,导致堵塞、分析精度降低、灵敏度降低。为了解决该问题,已尝试了使用具有抑制生物材料附着的能力的涂覆剂来涂覆结构基体,但对于存在许多容量为数μl~数ml的孔的微孔板这样的、具有复杂且微细的结构的基体而言,存在下述问题:在各孔的边缘部分、底面产生涂覆剂的积存,无法得到均匀厚度的涂覆膜。另外,在实施使用了平板读取器(platereader)等的光学测定时,若涂覆膜厚超过测定波长,则会有对光学测定造成影响等问题。
因此,本发明的目的在于提供具备均匀且薄的涂覆膜的结构基体及其制造方法,所述涂覆膜具有优异的抑制生物材料附着的能力,并且不对光学测定等造成影响。
用于解决课题的手段
本申请的发明人发现,具有抑制生物材料附着的能力的聚合物、尤其是包含特定阴离子结构和特定阳离子结构的共聚物通过极其简单的操作即能够在结构基体的表面形成最大膜厚与最小膜厚之差为
本发明如下所述。
[1]一种结构基体,其在至少一部分表面具备最大膜厚与最小膜厚之差为
上述涂覆膜包含下述共聚物,所述共聚物包含:含有下式(a)表示的基团的重复单元;和含有下式(b)表示的基团的重复单元,
[化学式1]
(式中,
ua1、ua2、ub1、ub2及ub3各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基,an-表示选自由卤化物离子、无机酸根离子、氢氧根离子及异硫氰酸根离子组成的组中的阴离子)。
[2]如[1]所述的结构基体,其中,上述共聚物包含下式(a1)及(b1)表示的重复单元,
[化学式2]
[式中,
ta及tb各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
qa及qb各自独立地表示单键、酯键或酰胺键;
ra及rb各自独立地表示可被卤原子取代的碳原子数1至10的直链或支链亚烷基;
ua1、ua2、ub1、ub2及ub3各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
an-表示选自由卤化物离子、无机酸根离子、氢氧根离子及异硫氰酸根离子组成的组中的阴离子;
m表示0至6的整数]。
[3]如[1]或[2]所述的结构基体,其中,上述共聚物是通过使包含下式(a)及(b)表示的化合物的单体混合物聚合而得到的,
[化学式3]
[式中,
ta、tb、ua1、ua2、ub1、ub2及ub3各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
qa及qb各自独立地表示单键、酯键或酰胺键;
ra及rb各自独立地表示可被卤原子取代的碳原子数1至10的直链或支链亚烷基;
an-表示选自由卤化物离子、无机酸根离子、氢氧根离子及异硫氰酸根离子组成的组中的阴离子;
m表示0至6的整数]。
[4]如上述[3]所述的结构基体,其中,上述共聚物是通过将还包含下式(d)或(e)表示的化合物的单体混合物聚合而得到的,
[化学式4]
[式中,
td、te及ue各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
rd及re各自独立地表示可被卤原子取代的碳原子数1至10的直链或支链亚烷基;n表示1至6的整数]。
[5]如[1]~[4]中任一项所述的结构基体,其中,上述结构基体包含由至少两个彼此相接的平面构成、并且两个平面相交的角度为0<θ<180°的结构部分。
[6]如[1]~[5]中任一项所述的结构基体,其中,涂覆膜为抑制生物材料附着的涂覆膜。
[7]如[1]~[6]中任一项所述的结构基体,结构基体为细胞培养容器及/或光学测定用基体。
[8]如[1]~[7]中任一项所述的结构基体,其中,结构基体表面在大气中的水接触角为0~120°、或在水中的气泡接触角为80~180°。
[9][1]所述的结构基体的制造方法,所述制造方法包括下述工序:将涂覆剂经一步涂布于结构基体,在该结构基体的至少一部分表面形成最大膜厚与最小膜厚之差为
上述涂覆剂包含下述共聚物,所述共聚物包含:含有下式(a)表示的基团的重复单元;和含有下式(b)表示的基团的重复单元,
[化学式5]
(式中,
ua1、ua2、ub1、ub2及ub3各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基、an-表示选自由卤化物离子、无机酸根离子、氢氧根离子及异硫氰酸根离子组成的组中的阴离子)。
[10]如[9]所述的制造方法,其中,上述共聚物包含下式(a1)及(b1)表示的重复单元,
[化学式6]
[式中,
ta及tb各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
qa及qb各自独立地表示单键、酯键或酰胺键;
ra及rb各自独立地表示可被卤原子取代的碳原子数1至10的直链或支链亚烷基;
ua1、ua2、ub1、ub2及ub3各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
an-表示选自由卤化物离子、无机酸根离子、氢氧根离子及异硫氰酸根离子组成的组中的阴离子;
m表示0至6的整数]。
[11]如[9]或[10]所述的制造方法,其中,上述共聚物是通过使包含下式(a)及(b)表示的化合物的单体混合物聚合而得到的,
[化学式7]
[式中,
ta、tb、ua1、ua2、ub1、ub2及ub3各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
qa及qb各自独立地表示单键、酯键或酰胺键;
ra及rb各自独立地表示可被卤原子取代的碳原子数1至10的直链或支链亚烷基;
an-表示选自由卤化物离子、无机酸根离子、氢氧根离子及异硫氰酸根离子组成的组中的阴离子;
m表示0至6的整数]。
[12]如上述[11]所述的结构基体,其中,上述共聚物是通过使还包含下式(d)或(e)表示的化合物的单体混合物聚合而得到的,
[化学式8]
[式中,
td、te及ue各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
rd及re各自独立地表示可被卤原子取代的碳原子数1至10的直链或支链亚烷基;n表示1至6的整数]。
[13]如[9]~[12]中任一项所述的制造方法,其中,上述结构基体包含由至少两个彼此相接的平面构成、并且两个平面相交的角度为0<θ<180°的结构部分。
[14]如[9]~[13]中任一项所述的制造方法,其中,涂覆膜为抑制生物材料附着的涂覆膜。
[15]如[9]~[14]中任一项所述的制造方法,其中,结构基体表面在大气中的水接触角为0~120°、或在水中的气泡接触角为80~180°。
[16]一种方法,其是仅利用涂布及干燥工序来向结构基体上的至少一部分表面赋予涂覆膜的方法,其中,该涂覆膜的最大膜厚与最少膜厚之差为
[17]如[16]所述的方法,其中,结构基体表面在大气中的水接触角为0~120°、或在水中的气泡接触角为80~180°。
[18]如[1]~[7]中任一项所述的结构基体,其中,结构基体所具备的涂覆膜表面在大气中的水接触角为0~120°、或在水中的气泡接触角为130~180°。
[19]如[9]~[14]中任一项所述的制造方法,其中,结构基体所具备的涂覆膜表面在大气中的水接触角为0~120°、或在水中的气泡接触角为130~180°。
[20]如[16]所述的方法,其中,结构基体所具备的涂覆膜表面在大气中的水接触角为0~120°、或在水中的气泡接触角为130~180°。
发明的效果
本发明的结构基体在其至少一部分表面以最大膜厚与最小膜厚之差为
此外,本发明的结构基体即使包含由至少两个彼此相接的平面构成、并且两个平面相交的角度为0<θ<180°的结构部分,也不存在涂覆剂积存于该结构部分的边缘部分或底面、边缘部分或底面的厚度显著增加的情况,能够具备最大膜厚与最小膜厚之差为
附图说明
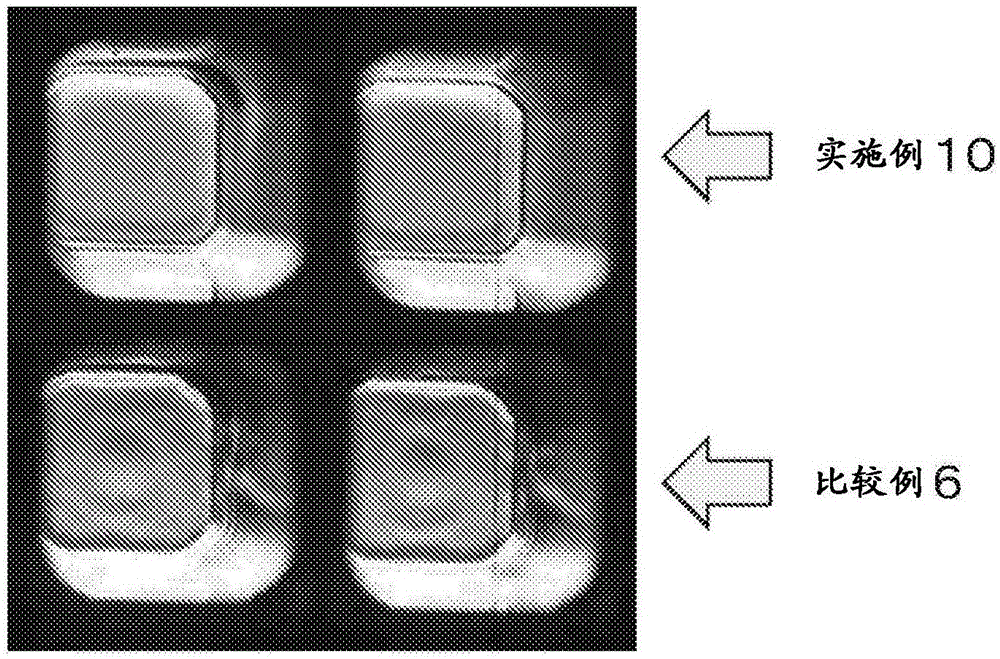
[图1]为在实施例10/比较例6中得到的具有涂覆膜的微孔板中、从上部对各孔的内部进行拍摄的照片。
[图2](a)及(b)分别为实施例10及比较例6中得到的具有涂覆膜的各孔的截面sem照片。
[图3](a)至(f)为试验例1(细胞附着的观察)中在培养4天后使用倒置型显微镜(olympus公司制,ckx31)对细胞向阳性对照及阴性对照的孔、以及由实施例1、3、比较例1及2的涂覆剂涂覆后的孔(no.1、3、5及6)上的附着进行观察的结果(倍率:4倍)。
[图4a]为将实施例1的涂覆剂滴加至试验例3的硅基板上并进行旋涂、干燥而形成的涂覆台阶基板的截面sem照片。
[图4b]为图4a中的(b)的放大图。
[图4c]为图4a中的(c)的放大图。
[图4d]为图4a中的(d)的放大图。
[图4e]为图4a中的(e)的放大图。
[图5a]为将比较例1的涂覆剂滴加至试验例3的硅基板上并进行旋涂、干燥而形成的涂覆台阶基板的截面sem照片。
[图5b]为图5a中的(b)的放大图。
[图5c]为图5a中的(c)的放大图。
[图5d]为图5a中的(d)的放大图。
[图5e]为图5a中的(e)的放大图。
具体实施方式
《术语的说明》
只要没有其他特别说明,本发明中使用的术语具有以下的定义。
本发明中,“卤原子”是指氟原子、氯原子、溴原子或碘原子。
本发明中,“烷基”是指直链或支链的、饱和脂肪族烃的一价基团。作为“碳原子数1至5的直链或支链烷基”,例如可举出甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、1-甲基丁基、2-甲基丁基、3-甲基丁基、1,1-二甲基丙基、1,2-二甲基丙基、2,2-二甲基丙基或1-乙基丙基。作为“碳原子数1至18的直链或支链烷基”,除了上述碳原子数1至5的直链或支链烷基的例子外,还可举出己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基、十三烷基、十四烷基、十五烷基、十六烷基、十七烷基或十八烷基、或它们的异构体。同样地,作为“碳原子数1至10的直链或支链烷基”,除了“碳原子数1至5的直链或支链烷基”的例子外,还可举出己基、庚基、辛基、壬基、癸基、或它们的异构体。
本发明中,“可被卤原子取代的碳原子数1至5的直链或支链烷基”是指上述碳原子数1至5的直链或支链烷基,或者被1个以上的上述卤原子取代的上述碳原子数1至5的直链或支链烷基。“碳原子数1至5的直链或支链烷基”的例子如上所述。另一方面,“被1个以上卤原子取代的碳原子数1至5的直链或支链烷基”是指上述碳原子数1至5的直链或支链烷基中的1个以上的任意氢原子被卤原子取代而得到的产物,作为例子,可举出氟甲基、二氟甲基、三氟甲基、氯甲基、二氯甲基、三氯甲基、溴甲基、碘甲基、2,2,2-三氟乙基、2,2,2-三氯乙基、全氟乙基、全氟丁基、或全氟戊基等。
本发明中,“酯键”是指-c(=o)-o-或-o-c(=o)-,“酰胺键”是指-nhc(=o)-或-c(=o)nh-,“醚键”是指-o-。
本发明中,“可被卤原子取代的碳原子数1至10的直链或支链亚烷基”是指碳原子数1至10的直链或支链亚烷基、或者被1个以上卤原子取代的碳原子数1至10的直链或支链亚烷基。此处,“亚烷基”是指与上述烷基相对应的二价有机基团。作为“碳原子数1至10的直链或支链亚烷基”的例子,可举出亚甲基、亚乙基、1,2-亚丙基、1,3-亚丙基、1,4-亚丁基、1-甲基-1,2-亚丙基、2-甲基-1,2-亚丙基、二甲基亚乙基、乙基亚乙基、1,5-亚戊基、1-甲基-1,4-亚丁基、2-甲基-1,4-亚丁基、1,1-二甲基-1,3-亚丙基、1,2-二甲基-1,3-亚丙基、2,2-二甲基-1,3-亚丙基、1-乙基-1,3-亚丙基、1,6-亚己基、1,8-亚辛基及1,10-亚癸基等,这些之中,优选亚乙基、1,2-亚丙基、1,8-亚辛基及1,10-亚癸基,更优选例如亚乙基、1,2-亚丙基、1,3-亚丙基、1,4-亚丁基等碳原子数1至5的直链或支链亚烷基,尤其优选亚乙基或1,2-亚丙基。“被1个以上卤原子取代的碳原子数1至10的直链或支链亚烷基”是指上述亚烷基中的1个以上的任意氢原子被卤原子取代而得到的产物,尤其优选为亚乙基或1,2-亚丙基的氢原子的一部分或全部被卤原子取代而得到的产物。
本发明中,“碳原子数3至10的环式烃基”是指碳原子数3至10的、单环式或多环式的、饱和或部分不饱和的脂肪族烃的一价基团。这些之中,优选碳原子数3至10的、单环式或二环式的饱和脂肪族烃的一价基团,例如,可举出环丙基、环丁基或环己基等碳原子数3至10的环烷基、或者双环[3.2.1]辛基、冰片基、异冰片基等碳原子数4至10的双环烷基。
本发明中,“碳原子数6至10的芳基”是指碳原子数6至10的、单环式或多环式的芳香族烃的一价基团,例如可举出苯基、萘基或蒽基等。“碳原子数6至10的芳基”可被1个以上的上述“可被卤原子取代的碳原子数1至5的直链或支链烷基”取代。
本发明中,“碳原子数7至15的芳烷基”是指基团-r-r’(其中,r表示上述“碳原子数1至5的亚烷基”,r’表示上述“碳原子数6至10的芳基”),例如可举出苄基、苯乙基、或α-甲基苄基等。“碳原子数7至15的芳烷基”的芳基部分可被1个以上的上述“可被卤原子取代的碳原子数1至5的直链或支链烷基”取代。
本发明中,“碳原子数7至15的芳基氧基烷基”是指基团-r-o-r’(其中,r表示上述“碳原子数1至5的亚烷基”,r’表示上述“碳原子数6至10的芳基”),例如可举出苯氧基甲基、苯氧基乙基、或苯氧基丙基等。“碳原子数7至15的芳基氧基烷基”的芳基部分可被1个以上的上述“可被卤原子取代的碳原子数1至5的直链或支链烷基”取代。
本发明中,“卤化物离子”是指氟化物离子、氯化物离子、溴化物离子或碘化物离子。
本发明中,“无机酸根离子”是指碳酸根离子、硫酸根离子、磷酸根离子、磷酸氢根离子、磷酸二氢根离子、硝酸根离子、高氯酸根离子或硼酸根离子。
作为上述an-,优选卤化物离子、硫酸根离子、磷酸根离子、氢氧根离子及异硫氰酸根离子,尤其优选卤化物离子。
本发明中,(甲基)丙烯酸酯化合物是指丙烯酸酯化合物和甲基丙烯酸酯化合物这两者。例如,(甲基)丙烯酸是指丙烯酸和甲基丙烯酸。
本发明中,作为生物材料,可举出蛋白质、糖、核酸及细胞或它们的组合。例如,作为蛋白质,可举出纤维蛋白原、牛血清白蛋白(bsa)、人白蛋白、各种球蛋白、β-脂蛋白、各种抗体(igg、iga、igm)、过氧化物酶、各种补体、各种凝集素、纤连蛋白、溶菌酶、冯·维勒布兰德因子(vwf,vonwillebrand’sfactor)、血清γ-球蛋白、胃蛋白酶、卵清白蛋白、胰岛素、组蛋白、核糖核酸酶、胶原蛋白、细胞色素c;例如,作为糖,可举出葡萄糖、半乳糖、甘露糖、果糖、肝素、透明质酸;例如,作为核酸,可举出脱氧核糖核酸(dna)、核糖核酸(rna);例如,作为细胞,可举出成纤维细胞、骨髓细胞、b淋巴细胞、t淋巴细胞、嗜中性粒细胞、红细胞、血小板、巨噬细胞、单核细胞、骨细胞、骨髓细胞、周皮细胞、树突状细胞、角质化细胞、脂肪细胞、间质细胞、上皮细胞、表皮细胞、内皮细胞、血管内皮细胞、肝实质细胞、软骨细胞、卵丘细胞、神经细胞、神经胶质细胞、神经元、少突胶质细胞、小胶质细胞、星形胶质细胞、心脏细胞、食道细胞、肌肉细胞(例如,平滑肌细胞或骨骼肌细胞)、胰脏β细胞、黑素细胞、定向造血干细胞、单核细胞、胚胎干细胞(es细胞)、胚胎肿瘤细胞、胚胎生殖干细胞、诱导多能干细胞(ips细胞)、神经干细胞、造血干细胞、间充质干细胞、肝干细胞、胰干细胞、肌干细胞、生殖干细胞、肠干细胞、癌干细胞、毛囊干细胞、巨核细胞、cd34阳性的源自脊髓的巨核细胞及各种细胞株(例如,hct116、huh7、hek293(人源胚胎肾细胞)、hela(人宫颈癌细胞株)、hepg2(人肝癌细胞株)、ut7/tpo(人白血病细胞株)、cho(中国仓鼠卵巢细胞株)、mdck、mdbk、bhk、c-33a、ht-29、ae-1、3d9、ns0/1、jurkat、nih3t3、pc12、s2、sf9、sf21、highfive、vero)等,本发明的涂覆膜尤其对细胞及蛋白质具有高的抑制附着的能力。
《本发明的说明》
本发明的结构基体只要在至少一部分表面具备膜厚为至少
所具备的涂覆膜的最大膜厚与最小膜厚之差为
所谓具有抑制生物材料附着的能力,例如在生物材料为成纤维细胞的情况下是指:利用实施例中记载的方法进行的、与无涂覆膜的情况比较时的相对吸光度(利用吸光度计得到)(wsto.d.450nm)(%)((实施例的吸光度(wsto.d.450nm))/(比较例的吸光度(wsto.d.450nm)))为9%以下,优选为6%以下,进一步优选为3%以下。
所谓具有抑制生物材料附着的能力,例如在生物材料为蛋白质的情况下是指,利用实施例中记载的方法进行的、与无涂覆膜的情况比较时的tmb溶液的相对光密度(450nm)(%)((实施例的光密度(450nm))/(比较例的光密度(450nm))为40%以下,优选为30%以下,进一步优选为20%以下,进一步优选为10%以下,更进一步优选为5%以下。
本说明书中,作为具有抑制生物材料附着的能力的聚合物的例子,可举出烯键式不饱和单体的聚合物、或者多糖类或其衍生物。作为烯键式不饱和单体的聚合物的例子,可举出选自由(甲基)丙烯酸及其酯;乙酸乙烯酯;乙烯基吡咯烷酮;乙烯;乙烯醇;以及它们的亲水性的官能性衍生物组成的组中的一种或两种以上的烯键式不饱和单体的聚合物。作为多糖类或其衍生物的例子,可举出羟基烷基纤维素(例如,羟基乙基纤维素或羟基丙基纤维素)等纤维素系高分子、淀粉、葡聚糖、凝胶多糖。
作为亲水性的官能性衍生物的亲水性官能性基团的例子,可举出磷酸、膦酸及它们的酯结构;甜菜碱结构;酰胺结构;亚烷基二醇残基;氨基;以及亚磺酰基等。
此处,磷酸及其酯结构是指下式表示的基团:
[化学式9]
[其中,r11、r12及r13彼此独立地为氢原子或有机基团(例如,碳原子数1至5的直链或支链烷基等)]
膦酸及其酯结构是指下式表示的基团:
[化学式10]
[其中,r14及r15彼此独立地为氢原子或有机基团(例如,碳原子数1至5的直链或支链烷基等)]。
作为具有这样的结构的烯键式不饱和单体的例子,可举出(甲基)丙烯酸(酸式磷酰氧基)乙酯、乙烯基膦酸等。
甜菜碱结构是指具有季铵型阳离子结构和酸性阴离子结构的两性中心的化合物的一价或二价基团,例如,可举出磷酰胆碱基团:
[化学式11]
作为具有这样的结构的烯键式不饱和单体的例子,可举出2-甲基丙烯酰氧基乙基磷酰胆碱(mpc)等。
酰胺结构是指下式表示的基团:
[化学式12]
[其中,r16、r17及r18彼此独立地为氢原子或有机基团(例如,甲基、羟甲基或羟乙基等)]
作为具有这样的结构的烯键式不饱和单体的例子,可举出(甲基)丙烯酰胺、n-(羟甲基)(甲基)丙烯酰胺等。此外,具有这样的结构的单体或聚合物例如已在日本特开2010-169604号公报等中公开。
亚烷基二醇残基是指亚烷基二醇(ho-alk-oh;其中,alk为碳原子数1至10的亚烷基)的单末端或两末端的羟基与其他化合物进行缩合反应后所残留的亚烷基氧基(-alk-o-),也包括重复亚烷基氧基单元而成的聚(亚烷基氧基)基团。作为具有这样的结构的烯键式不饱和单体的例子,可举出(甲基)丙烯酸2-羟基乙酯、甲氧基聚乙二醇(甲基)丙烯酸酯等。此外,具有这样的结构的单体或聚合物例如已在日本特开2008-533489号公报等中公开。
氨基是指式:-nh2、-nhr19或-nr20r21[其中,r19、r20及r21彼此独立地为有机基团(例如,为碳原子数1至5的直链或支链烷基等)]表示的基团。本说明书中的氨基包括经季铵化或氯化的氨基。作为具有这样的结构的烯键式不饱和单体的例子,可举出(甲基)丙烯酸二甲基氨基乙酯、(甲基)丙烯酸2-(叔丁基氨基)乙酯、甲基丙烯酰基胆碱氯化物(methacroylcholinechloride)等。
亚磺酰基是指下式表示的基团:
[化学式13]
[其中,r22为有机基团(例如为碳原子数1至10的有机基团,优选为具有1个以上羟基的碳原子数1至10的烷基等)]。
作为具有这样的结构的聚合物,可举出已在日本特开2014-48278号公报等中公开的共聚物。
其中,具备包含下述共聚物的涂覆膜的结构基体是优选的,所述共聚物包含:含有下式(a)表示的基团的重复单元;和含有下式(b)表示的基团的重复单元,
[化学式14]
[式中,ua1、ua2、ub1、ub2及ub3各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;an-表示选自由卤化物离子、无机酸根离子、氢氧根离子及异硫氰酸根离子组成的组中的阴离子]。
另外,上述涂覆膜中包含的共聚物可以还包含含有下式(c)表示的基团的重复单元,
[化学式15]
[式中,rc表示碳原子数1至18的直链或支链烷基、碳原子数3至10的环式烃基、碳原子数6至10的芳基、碳原子数7至15的芳烷基或者碳原子数7至15的芳基氧基烷基(其中,上述芳基部分可以经可被卤原子取代的碳原子数1至5的直链或支链烷基取代)]。
上述涂覆膜中包含的共聚物只要为包含含有上述式(a)表示的基团的重复单元、含有上述式(b)表示的基团的重复单元、以及根据情况存在的含有上述式(c)表示的基团的重复单元的共聚物,就没有特别限制。需要说明的是,含有上述式(c)表示的基团的重复单元与含有上述式(a)表示的基团的重复单元及含有上述式(b)表示的重复单元不同。共聚物优选为将含有上述式(a)表示的基团的单体、含有上述式(b)表示的基团的单体、以及根据情况存在的含有上述式(c)表示的基团的单体进行自由基聚合而得到的共聚物,也可以使用将它们进行缩聚、加聚反应而得到的共聚物。作为共聚物的例子,可举出使烯烃进行反应而得到的乙烯基聚合聚合物、聚酰胺、聚酯、聚碳酸酯、聚氨酯等,这些之中,尤其优选使烯烃进行反应而得到的乙烯基聚合聚合物或者使(甲基)丙烯酸酯化合物进行聚合而得到的(甲基)丙烯酸系聚合物。
共聚物中的含有式(a)表示的基团的重复单元的比例为3摩尔%至80摩尔%。需要说明的是,共聚物可以包含两种以上的含有式(a)表示的基团的重复单元。
共聚物中的含有式(b)表示的基团的重复单元的比例为3摩尔%至80摩尔%。需要说明的是,共聚物可以包含两种以上的含有式(b)表示的基团的重复单元。
共聚物中的含有式(c)表示的基团的重复单元的比例可以是从共聚物整体中减去上述式(a)及(b)后的剩余部分,例如为0摩尔%至90摩尔%。需要说明的是,共聚物可以包含两种以上的含有式(c)表示的基团的重复单元。
上述涂覆膜中包含的共聚物的一个实施方式为包含下式(a1)及(b1)的重复单元的共聚物。
[化学式16]
式中,ta及tb各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基,qa及qb各自独立地表示单键、酯键或酰胺键,ra及rb各自独立地表示可被卤原子取代的碳原子数1至10的直链或支链亚烷基,ua1、ua2、ub1、ub2及ub3各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基,an-表示选自由卤化物离子、无机酸根离子、氢氧根离子及异硫氰酸根离子组成的组中的阴离子,m表示0至6的整数。
共聚物可以还包含下式(c1)的重复单元。
[化学式17]
式中,tc各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基,qc表示单键、醚键或酯键,rc表示碳原子数1至18的直链或支链烷基、碳原子数3至10的环式烃基、碳原子数6至10的芳基、碳原子数7至15的芳烷基或者碳原子数7至15的芳基氧基烷基(其中,上述芳基部分可以经可被卤原子取代的碳原子数1至5的直链或支链烷基取代)。
式(a1)中,m表示0至6的整数,优选表示1至6的整数,更优选表示1至5的整数,尤其优选为1。
共聚物中包含的式(a1)表示的重复单元的比例为3摩尔%至80摩尔%。需要说明的是,共聚物可以包含两种以上的式(a1)表示的重复单元。
共聚物中包含的式(b1)表示的重复单元的比例为3摩尔%至80摩尔%。需要说明的是,共聚物可以包含两种以上的式(b1)表示的重复单元。
本发明涉及的共聚物中包含的式(c1)表示的重复单元的比例可以是从共聚物整体中减去上述式(a1)及式(b1)后的剩余部分,例如为0摩尔%至90摩尔%。需要说明的是,本发明涉及的共聚物可以包含两种以上的式(c1)表示的重复单元。
上述涂覆膜中包含的共聚物的另一实施方式是通过使包含下式(a)及(b)表示的化合物的单体混合物在溶剂中进行反应(聚合)而得到的共聚物,
[化学式18]
[式中,
ta及tb各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
qa及qb各自独立地表示单键、酯键或酰胺键;
ra及rb各自独立地表示可被卤原子取代的碳原子数1至10的直链或支链亚烷基;
ua1、ua2、ub1、ub2及ub3各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
an-表示选自由卤化物离子、无机酸根离子、氢氧根离子及异硫氰酸根离子组成的组中的阴离子;
m表示0至6的整数]。
共聚物可以是由还包含下式(c)表示的化合物的单体混合物得到的共聚物,
[化学式19]
[式中,
tc各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基;
qc表示单键、醚键或酯键;
rc表示碳原子数1至18的直链或支链烷基、碳原子数3至10的环式烃基、碳原子数6至10的芳基、碳原子数7至15的芳烷基或者碳原子数7至15的芳基氧基烷基(其中,上述芳基部分可以经可被卤原子取代的碳原子数1至5的直链或支链烷基取代)]。
作为ta、tb及tc,优选氢原子、甲基或乙基,更优选氢原子或甲基。作为qa、qb及qc,优选单键或酯键,更优选酯键。作为ra及rb,优选碳原子数1至5的直链或支链亚烷基,更优选亚甲基、亚乙基或1,2-亚丙基。作为rc,优选碳原子数4至18的直链或支链烷基或者碳原子数3至10的环烷基,更优选丁基、戊基、己基或它们的异构体、或者环己基。作为ua1、ua2、ub1、ub2及ub3,优选氢原子、甲基、乙基或叔丁基,作为式(a)的ua1及ua2,更优选氢原子,作为式(b)的ub1、ub2及ub3,更优选氢原子、甲基、乙基或叔丁基。
作为上述式(a)的具体例,可举出乙烯基膦酸、(甲基)丙烯酸(酸式磷酰氧基)乙酯、(甲基)丙烯酸3-氯-2-酸式磷酰氧基丙酯、(甲基)丙烯酸(酸式磷酰氧基)丙酯、(甲基)丙烯酸(酸式磷酰氧基)甲酯、酸式磷酰氧基聚氧乙二醇单(甲基)丙烯酸酯、酸式磷酰氧基聚氧丙二醇单(甲基)丙烯酸酯等,其中优选使用乙烯基膦酸、甲基丙烯酸(酸式磷酰氧基)乙酯(=磷酸2-(甲基丙烯酰氧基)乙酯)或酸式磷酰氧基聚氧乙二醇单甲基丙烯酸酯,最优选甲基丙烯酸(酸式磷酰氧基)乙酯(=磷酸2-(甲基丙烯酰氧基)乙酯)。
乙烯基膦酸、甲基丙烯酸(酸式磷酰氧基)乙酯(=磷酸2-(甲基丙烯酰氧基)乙酯)、酸式磷酰氧基聚氧乙二醇单甲基丙烯酸酯及酸式磷酰氧基聚氧丙二醇单甲基丙烯酸酯的结构式分别由下式(a-1)~式(a-4)表示。
[化学式20]
这些化合物在合成时,有时包含如下文所述的通式(d)或(e)所示那样的具有两个官能团的(甲基)丙烯酸酯化合物。
作为上述式(b)的具体例,可举出(甲基)丙烯酸二甲基氨基乙酯、(甲基)丙烯酸二乙基氨基乙酯、(甲基)丙烯酸二甲基氨基丙酯、(甲基)丙烯酸2-(叔丁基氨基)乙酯、甲基丙烯酰基胆碱氯化物等,其中优选使用(甲基)丙烯酸二甲基氨基乙酯、甲基丙烯酰基胆碱氯化物或(甲基)丙烯酸2-(叔丁基氨基)乙酯,最优选使用(甲基)丙烯酸二甲基氨基乙酯。
丙烯酸二甲基氨基乙酯(=丙烯酸2-(二甲基氨基)乙酯)、甲基丙烯酸二乙基氨基乙酯(=甲基丙烯酸2-(二乙基氨基)乙酯)、甲基丙烯酸二甲基氨基乙酯(=甲基丙烯酸2-(二甲基氨基)乙酯)、甲基丙烯酰基胆碱氯化物及甲基丙烯酸2-(叔丁基氨基)乙酯(=甲基丙烯酸2-(叔丁基氨基)乙酯)的结构式分别由下式(b-1)~式(b-5)表示。
[化学式21]
作为上述式(c)的具体例,可举出(甲基)丙烯酸丁酯、(甲基)丙烯酸2-乙基己酯、(甲基)丙烯酸月桂基酯、(甲基)丙烯酸硬脂基酯等(甲基)丙烯酸的直链或支链烷基酯类;(甲基)丙烯酸环己酯、(甲基)丙烯酸异冰片酯等(甲基)丙烯酸的环状烷基酯类;(甲基)丙烯酸苄酯、(甲基)丙烯酸苯乙酯等(甲基)丙烯酸的芳烷基酯类;苯乙烯、甲基苯乙烯、氯甲基苯乙烯等苯乙烯系单体;甲基乙烯基醚、丁基乙烯基醚等乙烯基醚系单体;乙酸乙烯酯、丙酸乙烯酯等乙烯基酯系单体。其中优选使用(甲基)丙烯酸丁酯或(甲基)丙烯酸环己酯。
甲基丙烯酸丁酯(=甲基丙烯酸丁基酯)及甲基丙烯酸环己酯(=甲基丙烯酸环己基酯)的结构式分别由下式(c-1)及式(c-2)表示。
[化学式22]
就上述涂覆膜中包含的共聚物的又一实施方式而言,除了上述式(a)、(b)及根据情况存在的(c)表示的化合物外,可以还共聚有任选的第4成分。例如,共聚有具有2个以上官能团的(甲基)丙烯酸酯化合物作为第4成分,聚合物的一部分可以部分地进行三维交联。作为这样的第4成分,例如,可举出下式(d)或(e)表示的双官能性单体,
[化学式23]
[式中,td、te及ue各自独立地表示氢原子或者碳原子数1至5的直链或支链烷基,rd及re各自独立地表示可被卤原子取代的碳原子数1至10的直链或支链亚烷基;n表示1至6的整数]。
即,本发明涉及的共聚物优选为含有由这样的双官能性单体衍生的交联结构的共聚物。
式(d)及(e)中,td及te优选各自独立地为氢原子、甲基或乙基,更优选各自独立地为氢原子或甲基。
式(e)中,ue优选为氢原子、甲基或乙基,更优选为氢原子。
式(d)中,rd优选为可被卤原子取代的碳原子数1至3的直链或支链亚烷基,更优选各自独立地为亚乙基或1,2-亚丙基、或者被1个氯原子取代的亚乙基或1,2-亚丙基,尤其优选为亚乙基或1,2-亚丙基。另外,式(d)中,n优选表示1至5的整数,尤其优选为1。
式(e)中,re优选为可被卤原子取代的碳原子数1至3的直链或支链亚烷基,更优选各自独立地为亚乙基或1,2-亚丙基、或者被1个氯原子取代的亚乙基或1,2-亚丙基,尤其优选为亚乙基或1,2-亚丙基。另外,式(e)中,n优选表示1至5的整数,尤其优选为1。
对于式(d)表示的双官能性单体,可优选举出乙二醇二(甲基)丙烯酸酯、三乙二醇二(甲基)丙烯酸酯、丙二醇二(甲基)丙烯酸酯、或者来自上述式(a-3)或(a-4)的双官能性单体等。
对于式(e)表示的双官能性单体,可优选举出磷酸双(甲基丙烯酰氧基甲酯)、磷酸双[(2-甲基丙烯酰氧基)乙酯]、磷酸双[3-(甲基丙烯酰氧基)丙酯]、或者来自上述式(a-3)或(a-4)的双官能性单体。
另外,作为三官能(甲基)丙烯酸酯化合物,可举出三丙烯酸氧次膦基三(氧基-2,1-乙烷二基)酯(triacrylicacidphosphinylidynetris(oxy-2,1-ethanediyl)ester)。
在上述第4成分中,尤其优选乙二醇二甲基丙烯酸酯、来自上述式(a-3)及(a-4)的双官能性单体中的具有乙二醇及丙二醇的重复单元的二甲基丙烯酸酯、磷酸双[2-(甲基丙烯酰氧基)乙酯]、以及来自上述式(a-3)及(a-4)的双官能性单体中的介由磷酸酯基而具有乙二醇及丙二醇的重复单元的二甲基丙烯酸酯,其结构式分别由下式(d-1)~(d-3)及式(e-1)~(e-3)表示。
[化学式24]
共聚物中可以包含上述第4成分中的一种或两种以上。
上述共聚物中的由第4成分、例如上述式(d)或(e)表示的双官能性单体衍生的交联结构的比例为0摩尔%至50摩尔%,优选为5摩尔%至45摩尔%,最优选为10摩尔%至40摩尔%。
式(a)表示的化合物相对于形成上述共聚物的全部单体的比例为3摩尔%至80摩尔%。另外,式(a)表示的化合物可以为两种以上。
式(b)表示的化合物相对于形成上述共聚物的全部单体的比例为3摩尔%至80摩尔%。另外,式(b)表示的化合物可以为两种以上。
式(c)表示的化合物相对于形成上述共聚物的全部单体的比例可以为减去上述式(a)及(b)的比例后的剩余部分,例如为0摩尔%至90摩尔%。另外,式(c)表示的化合物可以为两种以上。
上述涂覆膜中包含的共聚物可利用常规的丙烯酸系聚合物或甲基丙烯酸系聚合物等的合成方法即自由基聚合、阴离子聚合、阳离子聚合等方法来合成。其方式可以是溶液聚合、悬浮聚合、乳液聚合、本体聚合等各种方法。
作为聚合反应中的溶剂,可以为水、磷酸缓冲液或乙醇等醇或者将它们组合而成的混合溶剂,优选包含水或乙醇。进一步优选包含10质量%以上且100质量%以下的水或乙醇。进一步优选包含50质量%以上且100质量%以下的水或乙醇。进一步优选包含80质量%以上且100质量%以下的水或乙醇。进一步优选包含90质量%以上且100质量%以下的水或乙醇。优选水和乙醇的总量为100质量%。
作为反应浓度,例如优选使上述式(a)或式(b)表示的化合物在反应溶剂中的浓度为0.01质量%至4质量%。浓度大于4质量%时,由于例如式(a)表示的磷酸基所具有的强缔合性而导致共聚物有时在反应溶剂中发生凝胶化。浓度小于0.01质量%时,得到的清漆的浓度过低,因此难以制成用于得到膜厚充分的涂覆膜的涂覆剂。浓度更优选为0.01质量%至3质量%,例如3质量%、2质量%或1质量%。
另外,在上述涂覆膜所包含的共聚物的合成中,可以在制成例如下式(1)所记载的盐后,根据情况与式(c)表示的化合物一起进行聚合而制作共聚物。
[化学式25]
含有磷酸基的单体为容易缔合的单体,因此在被滴加到反应体系中时,可以逐次少量地滴加到反应溶剂中,以使其能够快速地分散。
此外,为了提高单体及聚合物的溶解性,可以对反应溶剂进行加热(例如40℃至100℃)。
为了有效地进行聚合反应,优选使用聚合引发剂。作为聚合引发剂的例子,可使用2,2’-偶氮双(异丁腈)、2,2’-偶氮双(2-甲基丁腈)、2,2’-偶氮双(2,4-二甲基戊腈)(和光纯药工业(株)制;va-065,10小时半衰期温度:51℃)、4,4’-偶氮双(4-氰基戊酸)、2,2’-偶氮双(4-甲氧基-2,4-二甲基戊腈)、1,1’-偶氮双(环己烷-1-甲腈)、1-[(1-氰基-1-甲基乙基)偶氮]甲酰胺、2,2’-偶氮双[2-(2-咪唑啉-2-基)丙烷]、2,2’-偶氮双(2-甲基丙脒)二盐酸盐、2,2’-偶氮双[2-甲基-n-(2-羟乙基)丙酰胺](和光纯药工业(株)制;va-086,10小时半衰期温度:86℃)、过氧化苯甲酰(bpo)、2,2’-偶氮双[n-(2-羧基乙基)-2-甲基丙脒]n-水合物(和光纯药工业(株)制;va-057,10小时半衰期温度:57℃)、4,4’-偶氮双(4-氰基戊酸)(和光纯药工业(株)制;v-501)、2,2’-偶氮双[2-(2-咪唑啉-2-基)丙烷]二盐酸盐(和光纯药工业(株)制;va-044,10小时半衰期温度:44℃)、2,2’-偶氮双[2-(2-咪唑啉-2-基)丙烷]二硫酸盐二水合物(和光纯药工业(株)制;va-046b,10小时半衰期温度:46℃)、2,2’-偶氮双[2-(2-咪唑啉-2-基)丙烷](和光纯药工业(株)制;va-061,10小时半衰期温度:61℃)、2,2’-偶氮双(2-脒基丙烷)二盐酸盐(和光纯药工业(株)制;v-50,10小时半衰期温度:56℃)、过二硫酸或叔丁基过氧化氢等。
考虑到在水中的溶解性、离子平衡及与单体的相互作用时,优选从2,2’-偶氮双[2-甲基-n-(2-羟乙基)丙酰胺]、2,2’-偶氮双[n-(2-羧基乙基)-2-甲基丙脒]n-水合物、4,4’-偶氮双(4-氰基戊酸)、2,2’-偶氮双[2-(2-咪唑啉-2-基)丙烷]二盐酸盐、2,2’-偶氮双[2-(2-咪唑啉-2-基)丙烷]二硫酸盐二水合物、2,2’-偶氮双[2-(2-咪唑啉-2-基)丙烷]、2,2’-偶氮双(2-脒基丙烷)二盐酸盐及过二硫酸中选择。
考虑到在有机溶剂中的溶解性、离子平衡及与单体的相互作用时,优选使用2,2’-偶氮双(2,4-二甲基戊腈)或2,2’-偶氮双(异丁腈)。
作为聚合引发剂的添加量,相对于聚合中使用的单体的总重量而言,为0.05质量%~10质量%。
对于反应条件而言,通过用油浴等将反应容器加热到50℃至200℃并进行1小时至48小时搅拌,更优选加热到80℃至150℃并进行5小时至30小时搅拌,由此使得聚合反应进行,可得到本发明的共聚物。反应气氛优选为氮气氛。
作为反应步骤,可以将全部反应物质均放入到室温的反应溶剂中,然后加热至上述温度而使其聚合,也可以将反应物质的混合物的全部或一部分逐次少量地滴加到预先经加热的溶剂中。
根据后者的反应步骤,本发明的共聚物可以通过包括下述工序的制造方法来制备:将包含上述式(a)、(b)表示的化合物及根据情况而使用的(c)表示的化合物、溶剂及聚合引发剂的混合物滴加到保持为比聚合引发剂的10小时半衰期温度更高的温度的溶剂中,使其进行反应(聚合)。
上述涂覆膜中包含的共聚物的分子量只要为数千至数百万左右即可,优选为5,000至5,000,000。更优选为5,000至2,000,000,进一步优选为5,000至1,000,000。另外,为无规共聚物、嵌段共聚物、接枝共聚物均可,对用于制造该共聚物的共聚反应本身没有特别限制,可以使用利用了自由基聚合、离子聚合、光聚合、乳液聚合的聚合等已知的在溶液中进行合成的方法。根据它们的目标用途,可单独使用本发明的共聚物中的任一种,也可以将多种共聚物混合、并且改变其比率而使用。
就用于形成上述涂覆膜的涂覆剂而言,可通过将期望的共聚物在根据情况添加的适当溶剂中稀释为规定的浓度而制备。
作为这样的溶剂,可举出水、磷酸缓冲生理盐水(pbs)、醇。作为醇,可举出碳数2至6的醇,例如乙醇、丙醇、异丙醇、1-丁醇、2-丁醇、异丁醇、叔丁醇、1-戊醇、2-戊醇、3-戊醇、1-庚醇、2-庚醇、2,2-二甲基-1-丙醇(=新戊醇)、2-甲基-1-丙醇、2-甲基-1-丁醇、2-甲基-2-丁醇(=叔戊醇)、3-甲基-1-丁醇、3-甲基-3-戊醇、环戊醇、1-己醇、2-己醇、3-己醇、2,3-二甲基-2-丁醇、3,3-二甲基-1-丁醇、3,3-二甲基-2-丁醇、2-乙基-1-丁醇、2-甲基-1-戊醇、2-甲基-2-戊醇、2-甲基-3-戊醇、3-甲基-1-戊醇、3-甲基-2-戊醇、3-甲基-3-戊醇、4-甲基-1-戊醇、4-甲基-2-戊醇、4-甲基-3-戊醇及环己醇,溶剂可以单独使用或者使用它们的组合的混合溶剂,从共聚物的溶解的观点考虑,优选从水、pbs、乙醇、丙醇、及它们的混合溶剂中选择,更优选从水、乙醇、及它们的混合溶剂中选择。
涂覆剂可以从含有共聚物的清漆制备。含有共聚物的清漆例如可以通过包括下述工序的制造方法来制备:在溶剂中,使上述式(a)、(b)及(c)表示的化合物以化合物的总浓度为0.01质量%至20质量%的方式进行反应(聚合)。
作为涂覆剂中的固态成分的浓度,为了均匀地形成涂覆膜,优选为0.01至50质量%。另外,作为涂覆剂中的共聚物的浓度,优选为0.01至4质量%,更优选为0.01至3质量%,尤其优选为0.01至2质量%,进一步优选为0.01至1质量%。共聚物的浓度小于0.01质量%时,涂覆剂中的共聚物的浓度过低,无法形成膜厚充分的涂覆膜,大于4质量%时,涂覆剂的保存稳定性变差,可能发生溶解物的析出、凝胶化。
此外,对于涂覆剂而言,除了上述共聚物和溶剂以外,还可根据需要在不损害得到的涂覆膜的性能的范围内添加其他物质。作为其他物质,可举出防腐剂、表面活性剂、提高与基材的密合性的底漆、防霉剂及糖类等。
为了调节涂覆剂中的共聚物的离子平衡,可以还包括预先调节涂覆剂中的ph的工序。ph调节例如可通过下述方式实施:向包含上述共聚物和溶剂的组合物中添加ph调节剂,使该组合物的ph成为3.5~8.5、进一步优选为4.0~8.0。可使用的ph调节剂的种类及其量可根据上述共聚物的浓度、其阴离子与阳离子的存在比等而适当选择。
作为ph调节剂的例子,可举出氨、二乙醇胺、吡啶、n-甲基-d-葡萄糖胺、三(羟甲基)氨基甲烷等有机胺;氢氧化钾、氢氧化钠等碱金属氢氧化物;氯化钾、氯化钠等碱金属卤化物;硫酸、磷酸、盐酸、碳酸等无机酸或其碱金属盐;胆碱等季铵阳离子;或者它们的混合物(例如,磷酸缓冲生理盐水等缓冲液)。这些之中,优选氨、二乙醇胺、氢氧化钠、胆碱、n-甲基-d-葡萄糖胺、三(羟甲基)氨基甲烷,尤其优选氨、二乙醇胺、氢氧化钠及胆碱。
本发明的结构基体在至少一部分表面具备最大膜厚与最小膜厚之差为
上述结构基体可以包含由至少两个彼此相接的平面构成、并且两个平面相交的角度θ为0<θ<180°、优选30°<θ<150°、尤其优选70°<θ<110°的结构部分。需要说明的是,可以平面中的一者或两者的一部分或全部为曲面。利用现有技术对具有这样的结构部分的结构基体进行涂覆时,有在具有上述角度θ的边缘部分、底面产生涂覆剂的积存这样的缺点,但通过使涂覆膜特别地包含下述共聚物,即可避免这样的缺点,所述共聚物包含:含有上述式(a)表示的基团的重复单元;含有上述式(b)表示的基团的重复单元;以及根据情况存在的含有上述式(c)表示的基团的重复单元。
典型的结构基体可以为实验设备类、分析设备类、或医疗器械类。结构基体尤其可以为实验设备类、分析设备类、或医疗器械类中与生物体内组织、血液相接触而使用的设备的整体或至少其一部分的结构物。作为实验设备类的例子,可举出细胞的培养中通常使用的陪替氏培养皿、培养皿等皿/培养皿类、培养瓶、旋转瓶等瓶类、培养袋、teflon(注册商标)袋等塑料袋类、复合皿(multi-dish)/复合板(multi-plate)、微板/微孔板、深孔板等多孔板类、腔室载玻片等载玻片及其相关制品、培养管、离心管、微管等管类、托盘、滚瓶等培养容器,可优选举出6~1536孔的多孔板及皿/培养皿。此处,上述多孔板的各孔的形状可以为大致半球状、大致长方体状或大致圆柱状等,其底面可以为平底,也可以为圆底。例如,在各孔的形状为大致长方体状或大致圆柱状的情况下,上述“至少两个彼此相接的平面”是指孔的底面的内部表面和壁面的内部表面,上述“两个平面相交的角度θ”是指由各孔的底面的内部表面与壁面的内部表面构成的角度。需要说明的是,在底面为圆底的情况下,上述“底面的内部表面”可替换为圆底的最底部的切平面。此外,在各孔的形状为大致半球状的情况下,上述“至少两个彼此相接的平面”可替换为半球状孔的最底部的切平面、和从最底部至端部为止的弧的中点的切平面,上述“两个平面相交的角度θ”是指由上述两个切平面构成的角度。
作为医疗器械类的例子,可举出嵌入体内型人造器官、治疗器具、体外循环型人造脏器类、导管、管、人造瓣膜、支架、人造关节等的整体或至少其一部分的结构物。
特别地,作为光学测定用基体,只要是供于光学测定的基体(基材),就没有特别限定,除了例如以上述结构基体供于光学测定(测定波长为例如340~850nm)外,还可举出例如平板读取器中使用的基体(基材)(细胞培养板等)、相位差显微镜用板、uv测定用比色皿、透明电极(ito电极)等。
另外,作为结构基体的材质,可举出玻璃、金属、含有金属的化合物或含有准金属的化合物、活性炭或树脂。就金属而言,可举出典型金属:(碱金属:li、na、k、rb、cs;碱土金属:ca、sr、ba、ra);镁族元素:be、mg、zn、cd、hg;铝族元素:al、ga、in;稀土类元素:y、la、ce、pr、nd、sm、eu;锡族元素:ti、zr、sn、hf、pb、th;铁族元素:fe、co、ni;酸土元素:v、nb、ta;铬族元素:cr、mo、w、u;锰族元素:mn、re;贵金属:cu、ag、au;铂族元素:ru、rh、pd、os、ir、pt等。就含有金属的化合物或含有准金属的化合物而言,例如可举出基本成分为金属氧化物、经高温下的热处理进行烧结而成的烧结体即陶瓷、硅这样的半导体、金属氧化物或准金属氧化物(硅氧化物、氧化铝等)、金属碳化物或准金属碳化物、金属氮化物或准金属氮化物(硅氮化物等)、金属硼化物或准金属硼化物等无机化合物的成型体等无机固体材料、铝、镍钛、不锈钢(sus304、sus316、sus316l等)。
作为结构基体的材质的树脂,为天然树脂或其衍生物、或者合成树脂均可,作为天然树脂或其衍生物,可优选使用纤维素、三乙酸纤维素(cta)、硝基纤维素(nc)、固定了硫酸葡聚糖的纤维素等,作为合成树脂,可优选使用聚丙烯腈(pan)、聚酯系聚合物合金(pepa)、聚苯乙烯(ps)、聚砜(psf)、聚对苯二甲酸乙二醇酯(pet)、聚甲基丙烯酸甲酯(pmma)、聚乙烯醇(pva)、聚氨酯(pu)、乙烯-乙烯醇(eval)、聚乙烯(pe)、聚酯、聚丙烯(pp)、聚偏二氟乙烯(pvdf)、聚醚砜(pes)、聚碳酸酯(pc)、聚氯乙烯(pvc)、聚四氟乙烯(ptfe)、超高分子量聚乙烯(uhpe)、聚二甲基硅氧烷(pdms)、丙烯腈-丁二烯-苯乙烯树脂(abs)、teflon(注册商标)、尼龙、聚甲基戊烯(pmp)或各种离子交换树脂等。
结构基体中,带涂覆膜的表面的材质可以为一种,也可以为两种以上的组合。这些材质中,优选玻璃、硅、硅氧化物、聚苯乙烯(ps)、聚丙烯(pp)、teflon(注册商标)、环烯烃聚合物(cop)、聚二甲基硅氧烷(pdms)中的一种或不锈钢(sus304、sus316、sus316l等)、或者选自它们中的组合。本发明的涂覆膜可通过低温干燥而形成,因此还可使用耐热性低的树脂等。
上述结构基体中使用的基体可以直接使用,或在用水或适当的介质洗涤后使用,或者在实施等离子体处理等表面处理后使用。
本发明的另一实施方式涉及在至少一部分表面具备最大膜厚与最小膜厚之差为
另外,就利用上述方法得到的结构基体表面的涂覆膜而言,在上述涂布工序后,优选可在实施干燥工序(例如,也可以不经历干燥工序而直接使用)后、进一步优选在用水或适当的介质洗涤后,作为结构基体使用。
上述干燥工序在大气下或真空下、优选在温度-200℃至200℃的范围内进行。在通过干燥工序将上述涂覆剂中的溶剂去除的同时,涂覆膜中包含的共聚物的式(a)及式(b)彼此形成离子键而完全地固着于基体。
涂覆膜例如也可以通过在室温(10℃至35℃、例如25℃)下的干燥而形成,但为了更迅速地形成涂覆膜,例如也可以于40℃至50℃使其干燥。另外,还可以使用基于冷冻干燥法的极低温~低温(-200℃至-30℃左右)下的干燥工序。冷冻干燥被称为真空冷冻干燥,通常是用制冷剂将想要干燥的物质冷却、并在真空状态下利用升华而将溶剂除去的方法。关于冷冻干燥中使用的常规制冷剂,可举出干冰与甲醇的混合介质(-78℃)、液氮(-196℃)等。
干燥温度低于-200℃时,必须使用非常规的制冷剂,欠缺通用性,并且,为了将溶剂升华,需要进行长时间干燥,效率差。干燥温度高于200℃时,涂覆膜表面的离子键合反应过度进行,该表面丧失亲水性,无法发挥抑制生物材料附着的能力。更优选的干燥温度为10℃至180℃,进一步优选的干燥温度为25℃至150℃,最优选为40℃至80℃。
另外,为了除去残留在涂覆膜上的杂质、未反应单体等,并进一步调节涂层中的共聚物的离子平衡,可以实施用选自水及含有电解质的水溶液中的至少一种溶剂进行洗涤的工序。洗涤优选为流水洗涤或超声波洗涤等。上述水及含有电解质的水溶液例如可以在40℃至95℃的范围内进行了加热。含有电解质的水溶液优选为pbs、生理盐水(仅含有氯化钠的水溶液)、杜氏磷酸盐缓冲生理盐水、tris缓冲生理盐水、hepes缓冲生理盐水及veronal缓冲生理盐水,尤其优选为pbs。固着后,即使用水、pbs及醇等进行洗涤,涂覆膜也不溶出,保持牢固地固着于基体的状态。优选地,即使在所形成的涂层上附着有生物材料,也可以通过随后进行的水洗等而容易地除去,形成有涂覆膜的结构基体的表面具有抑制生物材料附着的能力。
在上述涂布后不经过干燥工序而直接制造结构基体的情况下,可以在针对上述结构基体的表面的至少一部分进行涂布工序后,在48小时以内(优选24小时以内、进一步优选12小时以内、进一步优选6小时以内、进一步优选3小时以内、进一步优选1小时以内),不经过干燥工序而直接或者用例如水或适当的介质(例如含有电解质的水溶液)进行洗涤后,用作结构基体。洗涤条件与实施干燥工序后的洗涤工序相同。
本申请中使用的结构基体的表面在大气中的水接触角显示为0~120°、优选50~115°、更优选60~115°,或者在水中的气泡接触角显示为80~180°、优选80~180°、更优选80~170°、尤其优选80~160°。上述水接触角可利用例如实施例中记载的静态接触角进行评价。
本申请的赋予了涂覆膜的结构基体的表面具有充分的抑制生物材料附着的能力及亲水性。亲水性可利用例如实施例中记载的静态接触角进行评价,本发明涉及的结构基体的表面在大气中的水接触角显示为0~120°、优选10~110°、更优选20~110°,或者在水中的气泡接触角显示为130~180°、优选140~170°、更优选145~160°、尤其优选149~159°。
实施例
以下,基于合成例、实施例、试验例等,对本发明进一步详细地说明,但本发明并不限定于此。
下述合成例中所示的共聚物的重均分子量为基于凝胶过滤色谱法(gelfiltrationchromatography)(以下,简称为gfc)的测定结果。测定条件等如下所述。
·装置:prominence(岛津制作所制)
·gfc柱:tskgelgmpwxl(7.8mmi.d.×30cm)×2~3根
·流速:1.0ml/min
·洗脱液:含有离子性物质的水溶液、或etoh的混合溶液
·柱温:40℃
·检测器:ri
·进样浓度:聚合物固态成分为0.05~0.5质量%
·进样量:100μl
·标准曲线:三次近似曲线
·标准试样:聚环氧乙烷(agilent公司制)×10种
<合成例1>
在维持60℃的状态下对甲基丙烯酸(酸式磷酰氧基)乙酯(制品名:phosmerm,unichemical(株)制,干固法100℃·1小时条件下的非挥发成分:91.8%,甲基丙烯酸(酸式磷酰氧基)乙酯(44.2质量%)、磷酸双[2-(甲基丙烯酰氧基)乙酯](28.6质量%)、其他物质(27.2质量%)的混合物)28.00g进行搅拌,并滴加甲基丙烯酸2-(二甲基氨基)乙酯21.37g。在保持为20℃以下的状态下,向其中依次加入纯水133.96g、以及乙醇(东京化成工业(株)制)44.65g、2,2’-偶氮双(n-(2-羧基乙基)-2-甲基丙脒)n-水合物(制品名:va-057,和光纯药工业(株)制)0.25g。将充分搅拌均匀的加入有上述全部物质的混合液导入至滴液漏斗中。另一方面,另行将纯水267.93g加入至带有冷凝管的三颈瓶中,对其吹送氮气,一边搅拌一边升温至回流温度。在维持该状态的同时,将导入有上述混合液的滴液漏斗设置于三颈瓶中,经2小时将混合液滴加到纯水的沸腾液内。滴加后,在维持上述环境的状态下加热搅拌24小时,由此得到固态成分为约9.70质量%的含有共聚物的清漆496.16g。得到的透明液体的利用gfc测得的重均分子量为约280,000。
<合成例2>
将甲基丙烯酸(酸式磷酰氧基)乙酯(制品名:phosmerm,unichemical(株)公司制,干固法100℃·1小时条件下的非挥发成分:91.8%,甲基丙烯酸(酸式磷酰氧基)乙酯(44.2质量%)、磷酸双[2-(甲基丙烯酰氧基)乙酯](28.6质量%)、其他物质(27.2质量%)的混合物)25.00g冷却至35℃以下,同时加入胆碱(48-50%水溶液:东京化成工业(株)制)29.95g,进行搅拌直至均匀。在保持为35℃以下的状态下,向该混合液中依次加入甲基丙烯酰基胆碱氯化物80%水溶液(东京化成工业(株)制)20.95g、甲基丙烯酸丁酯(东京化成工业(株)制)28.67g、2,2’-偶氮双(2,4-二甲基戊腈)(制品名:v-65,和光纯药工业(株)制)0.70g、乙醇110.84g。进而,在保持为35℃以下的状态下,将在纯水27.71g中溶解2,2’-偶氮双(n-(2-羧基乙基)-2-甲基丙脒)n-水合物(制品名:va-057,和光纯药工业(株)制)0.70g而得到的水溶液加入至上述溶液中,将充分搅拌均匀的加入有上述全部物质的混合液导入至滴液漏斗中。另一方面,另行将纯水56.81g和乙醇131.62g加入至带有冷凝管的三颈瓶中,对其吹送氮气,一边搅拌一边升温至回流温度。在维持该状态的同时,将导入有上述混合液的滴液漏斗设置于三颈瓶上,经1小时将混合液滴加至纯水与乙醇的沸腾液内。滴加后,在维持上述环境的状态下加热搅拌24小时。24小时后进行冷却,由此得到固态成分为约19.68质量%的含有共聚物的清漆432.92g。得到的胶体状液体的利用gfc测得的重均分子量为约8,500。
<实施例1>
向上述合成例1中得到的含有共聚物的清漆5.00g中,加入纯水28.73g、乙醇13.95g、1mol/l氢氧化钠水溶液(1n)(关东化学(株)制)0.85g,并充分搅拌,制备涂覆剂。ph为7.5。在得到的涂覆剂中,浸渍半导体评价用的市售硅晶片及培养板(corning(注册商标)#351172(96孔;容积0.37ml)(材质:聚苯乙烯)),用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计(ellipsometer)对硅晶片的涂覆膜的膜厚进行确认,结果为
<实施例2>
向上述合成例1中得到的含有共聚物的清漆4.00g中,加入纯水50.14g、乙醇22.80g、1mol/l氢氧化钠水溶液(1n)(关东化学(株)制)0.68g,并充分搅拌,制备涂覆剂。ph为7.5。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<实施例3>
向上述合成例1中得到的含有共聚物的清漆3.00g中,加入纯水64.77g、乙醇28.74g、1mol/l氢氧化钠水溶液(1n)(关东化学(株)制)0.51g,并充分搅拌,制备涂覆剂。ph为7.5。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<实施例4>
向上述合成例1中得到的含有共聚物的清漆1.00g中,加入纯水66.86g、乙醇28.98g、1mol/l氢氧化钠水溶液(1n)(关东化学(株)制)0.17g,并充分搅拌,制备涂覆剂。ph为7.5。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,浸渍于pbs中24小时,并用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<实施例5>
向上述合成例2中得到的含有共聚物的清漆20.00g中,加入1mol/l盐酸(1n)(关东化学(株)制)2.45g、纯水46.61g和乙醇130.19g,并充分搅拌,制备涂覆剂。ph为3.5。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<实施例6>
向上述合成例2中得到的含有共聚物的清漆10.00g中,加入1mol/l盐酸(1n)(关东化学(株)制)1.23g、纯水52.83g和乙醇133.97g,并充分搅拌,制备涂覆剂。ph为3.5。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<实施例7>
向上述合成例2中得到的含有共聚物的清漆5.00g中,加入1mol/l盐酸(1n)(关东化学(株)制)0.61g、纯水55.93g和乙醇135.87g,并充分搅拌,制备涂覆剂。ph为3.5。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<实施例8>
向上述合成例2中得到的含有共聚物的清漆5.00g中,加入1mol/l盐酸(1n)(关东化学(株)制)2.31g、纯水95.29g和乙醇227.71g,并充分搅拌,制备涂覆剂。ph为3.5。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<实施例9>
向上述合成例2中得到的含有共聚物的清漆1.00g中,加入1mol/l盐酸(1n)(关东化学(株)制)0.12g、纯水58.42g和乙醇137.38g,并充分搅拌,制备涂覆剂。ph为3.5。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<比较例1>
使聚(甲基丙烯酸2-羟乙酯)(sigma-aldrichjapan(株)制)1.2g溶解于乙醇29.98g和纯水2g中,并充分搅拌,制备涂覆剂。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<比较例2>
使聚(甲基丙烯酸2-羟乙酯)(sigma-aldrichjapan(株)制)1.0g溶解于乙醇95.0g和纯水4.0g中,并充分搅拌,制备涂覆剂。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<比较例3>
使聚(甲基丙烯酸2-羟乙酯)(sigma-aldrichjapan(株)制)0.5g溶解于乙醇95.0g和纯水4.5g中,并充分搅拌,制备涂覆剂。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<比较例4>
使聚(甲基丙烯酸2-羟乙酯)(sigma-aldrichjapan(株)制)0.3g溶解于乙醇95.0g和纯水4.7g中,并充分搅拌,制备涂覆剂。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<比较例5>
使聚(甲基丙烯酸2-羟乙酯)(sigma-aldrichjapan(株)制)0.1g溶解于乙醇95.0g和纯水4.9g中,并充分搅拌,制备涂覆剂。在得到的涂覆剂中,浸渍与实施例1同样的硅晶片及培养板,用烘箱于50℃干燥24小时。之后,用纯水充分地进行洗涤,在硅晶片或板上得到涂覆膜。用椭圆偏振计对硅晶片的涂覆膜的膜厚进行确认,结果为
<实施例10/比较例6>
向corning(注册商标)#3712(384孔;容积100μl/孔)(材质:聚苯乙烯)的各孔中,分别注入100μl的实施例1及比较例1中制备的涂覆剂。用烘箱将其于50℃干燥24小时。之后,用100μl的pbs和纯水各进行3次洗涤,将从上部拍摄孔内部的照片而得到的结果示于图1。就照片的上部2个孔(实施例10)而言,观察到孔的底部的透明性没有问题,膜被均匀地涂覆,与此相对,就照片的下部2个孔(比较例6)而言,观察到膜不均匀地凝集。
另外,为了对其进行更详细的观察,进行截面sem观察。将结果示于图2(a)及(b)。在图1的照片的上部孔(实施例10)的截面sem照片图2(a)中,明确地观察到底部与壁面部的角(约90~95°)的边缘。从上述实施例1中形成了
即,通过实施例1中制备的涂覆剂,能够经由一步的涂布工序而在包含由至少两个彼此相接的平面构成、并且两个平面相交的角度为0<θ<180°的结构部分的结构基体上形成均匀的极薄膜(例如
<试验例1:抑制细胞附着的效果>
(涂覆板的制备)
向corning#351172(96孔;容积0.37ml)(材质:聚苯乙烯)的各孔(no.1~4)中,分别注入200μl的实施例1~4的涂覆剂。将它们静置1小时,然后除去,用烘箱于50℃干燥24小时。关于比较例1~5的涂覆剂,分别以30μl注入各孔(no.5~9)中,用烘箱于50℃干燥24小时。之后,用200μl的纯水,对由实施例1~4及比较例1~5的涂覆剂涂覆的孔(no.1~9)各进行3次洗涤,用于试验中。作为阳性对照的样品,使用市售的细胞低粘附板(corning公司制,#3474)。作为阴性对照,使用未实施涂覆的96孔细胞培养板(corning公司制,#351172)。
(细胞的制备)
作为细胞,使用小鼠胚胎成纤维细胞c3h10t1/2(dspharmabiomedical公司制)。作为细胞的培养中使用的培养基,使用含有10%fbs(hyclone公司制)和l-谷氨酰胺-青霉素-链霉素稳定化溶液(sigma-aldrich公司制)的bme培养基(thermofisherscientific公司制)。使用直径为10cm的培养皿(培养基10ml),在37℃/co2培养箱内,在保持5%二氧化碳浓度的状态下,将细胞静置培养2天以上。接下来,用pbs5ml对该细胞进行洗涤,然后添加胰蛋白酶-edta溶液(invitrogen公司制)1ml,将细胞剥离,分别悬浮于上述的培养基10ml中。将该悬浮液进行离心分离(tomyseikoco.,ltd.制,型号lc-200,1000rpm/3分钟,室温)后,除去上清液,添加上述培养基,制备细胞悬浮液。
(细胞附着实验)
向上文中制备的板的各孔(no.1~9)、阳性对照及阴性对照中,添加各100μl的各细胞悬浮液,使得成为2×103个细胞/孔。之后,在保持为5%二氧化碳浓度的状态下,于37℃在co2培养箱内静置4天。
(细胞附着的观察)
培养4天后,用倒置型显微镜(olympus公司制,ckx31)观察(倍率:4倍)细胞在上文中制备的板的各孔(no.1~9)、阳性对照、及阴性对照上的附着情况,基于观察结果进行比较。在由实施例1~3、比较例1的涂覆剂涂覆的板的各孔(no.1~3、5)、及阳性对照的板的孔中,未观察到细胞的附着。在由实施例4及比较例2~5的涂覆剂涂覆的板的各孔(no.4、6~9)中,观察到了细胞的附着。将各孔(阳性对照及阴性对照、以及no.1、3、5及6)的结果(培养4天后)分别示于图3(a)~(f)。另外,每孔添加10μl的cellcountingkit-8溶液(同仁化学研究所制),于37℃在co2培养箱内静置2小时。之后,用吸光度计(moleculardevices公司制,spectramax)测定450nm处的吸光度。从各测定值中减去仅添加有各培养基的孔的测定值。将其结果示于表1。
[表1]
吸光度测定
在由实施例1~3、比较例1的涂覆剂涂覆的板的各孔、及阳性对照的板的孔中,细胞未附着。此时,未附着的细胞形成了细胞凝集块(球体)。
<试验例2:抑制蛋白质吸附的效果>
(涂覆板的制备)
向youkenscience公司制平底板(96孔;容积0.37ml)(材质:聚苯乙烯)的各孔中,分别注入250μl的实施例6~9和比较例1~5的涂覆剂。将它们静置1小时,然后除去,于室温干燥18小时。之后,用250μl的纯水对经涂覆的孔(no.10~18)各进行3次洗涤,并使其干燥,用于试验。作为阴性对照,使用未实施涂覆的96孔板。
(蛋白质吸附实验)
用磷酸缓冲生理盐水对辣根过氧化物酶(horseradishperoxidase)(简称为hrp)标记山羊抗小鼠igg(goatanti-mouseigg)(southerbioteck公司制)进行稀释,并加入至上文中经涂覆的孔内,于室温静置30分钟。用磷酸缓冲生理盐水进行洗涤后,加入tmb单组分微孔过氧化物酶底物(tmb1-componentmicrowellperoxidasesubstrate),sureblue(kirkegaard&perrylaboratories,inc.制,简称为tmb),使其与hrp反应,加入tmb终止液(tmbstopsolution)(kirkegaard&perrylaboratories,inc.制),使反应停止。用平板读取器(spectramax190,moleculardevices)对此时的tmb溶液的光密度(450nm)进行测定,评价为蛋白质吸附量。将其结果示于表2。
[表2]
吸光度测定
确认了实施例6~9、比较例1的涂覆膜具有抑制蛋白质附着的能力。
<试验例3:台阶覆盖性的评价>
(涂覆台阶基板的制备)
向包含l/s=1/1、间距为50μm、台阶为100μm的结构体的硅基板,滴加实施例1及比较例1中制备的涂覆剂,以1500rpm/1min的速度进行旋涂,以50℃/24h的条件进行干燥,由此制成涂覆台阶基板(no.1及2)。
(涂覆台阶基板的sem评价)
以l/s=1/1、间距为50μm、台阶为100μm的结构体的截面形状露出的方式切割涂覆台阶基板(no.1、2),在表面蒸镀铂后,进行截面形状的sem评价。分别观察台阶基板的凸部中央、凹部中央、壁面中央,对附着于硅台阶基板上的使用实施例1及比较例1的涂覆剂而得到的涂覆膜的膜厚
[表3]
就使用实施例1的涂覆剂而得到的涂覆膜而言,无论在包含结构体的硅基板的凸部中央、凹部中央、壁面中央中的任何位置上,均成为
<实施例11>
向上述合成例1中得到的含有共聚物的清漆5.00g中,加入纯水31.5g、乙醇1.35g、1mol/l氢氧化钠水溶液(1n)(关东化学(株)公司制)0.24g,并充分搅拌,制备涂覆剂。ph为7.3。在得到的涂覆剂中,浸渍下述硅晶片及各种基板,利用烘箱于45℃干燥24小时。之后,用pbs和纯水充分地进行洗涤,得到形成有涂覆膜的硅晶片及各种基板。用光学式干涉膜厚计确认硅晶片的涂覆膜的膜厚,结果为
<实施例12>
向上述合成例2中得到的含有共聚物的清漆10.00g中,加入1mol/l盐酸(1n)(关东化学(株)公司制)1.19g、纯水26.78g和乙醇62.54g,并充分搅拌,制备涂覆剂。ph为3.5。利用与实施例11同样的方法,得到形成有涂覆膜的硅晶片及各种基板。用光学式干涉膜厚计确认硅晶片的涂覆膜的膜厚,结果为
(硅晶片)
直接使用半导体评价用的市售硅晶片。
(各种基板)
使用的各种基板如下所示:聚氯乙烯(pvc)、细胞培养用聚苯乙烯培养皿(ps培养皿)、聚苯乙烯(ps)、聚醚砜(pes)、聚对苯二甲酸乙二醇酯(pet)、聚丙烯(pp)、聚乙烯(pe)、玻璃、两种环烯烃聚合物(cop)片材(zeonor(日本zeon制)、zeonex(日本zeon制))、两种聚二甲基硅氧烷(pdms)片材。关于玻璃,准备未进行等离子体处理的玻璃和进行了等离子体处理的玻璃这两者。
等离子体处理条件:
装置:meiwafosis(株)制sede-ge(softetchingdevice)
蚀刻气体:空气
等离子体处理时间:1分钟
加热阶段温度:25℃
电流值:5ma
<试验例4>
[静态接触角计的评价]
使用全自动接触角计(协和界面化学株式会社,dm-701),对实施例11及12中得到的形成有涂覆膜的各种基板进行评价。评价于25℃的温度下进行(大气中及水中)。对于静态接触角而言,除了在大气中测定水滴的接触角以外,还将各种基板倒过来而设置于水中,进行气泡的接触角测定而得到水中接触角,利用这两者进行评价。将大气中的测定结果示于表4,将水中的测定结果示于表5。
[表4]
[表5]
从大气中的测定结果来看,对于形成有涂覆膜的各种基板的接触角而言,均没有观察到与未涂布的情况有显著性差异。即,未能确认到通过涂覆而使得各种基板发生亲水化这样的行为。另一方面,从水中的测定结果来看,形成有涂覆膜的各种基板的接触角与未涂布的情况相比,可观察到显著的亲水化。这表明在各种基板上形成有涂层。
产业上的可利用性
本发明的结构基体在其至少一部分表面具备最大膜厚与最小膜厚为
- 还没有人留言评论。精彩留言会获得点赞!