新型槲皮素类化合物的制作方法
本说明书涉及一种新型槲皮素类化合物。
背景技术:
绿茶以叶子的形式作为粗茶引用,或作为发酵茶饮用以感受更浓的味道。发酵绿茶意味着绿茶叶子已被氧化。它包括由茶叶子中存在的氧化酶氧化的发酵茶和由除茶叶子中存在的酶之外的微生物发酵的后发酵茶。根据发酵程度可分为弱发酵茶、半发酵茶、全发酵茶等。根据发酵类型和发酵程度将发酵绿茶称为不同的名称,例如绿茶、乌龙茶、红茶、普洱茶。
拥有世界领先的后发酵茶生产技术的国家是中国和日本。中国的有氧发酵茶使用真菌作为发酵菌株生产,主要在云南省西双版纳西部种植。日本的有氧发酵茶包括黑茶,所述黑茶使用真菌作为发酵菌株生产并且主要在富山种植。日本的厌氧发酵茶包括番茶和黑茶,所述番茶使用厌氧乳酸菌(anaerobiclactobacillus)作为发酵菌株生产并且主要在阿波种植,所述黑茶使用厌氧真菌作为发酵菌株生产并且主要在石鎚种植。起源于中国普洱市的传统普洱茶通过以下步骤生产:在收集绿茶叶子时故意损伤绿茶叶子,加热和烘烤绿茶叶子,施加适量的水,以及使用空气中的微生物对绿茶叶子进行自然发酵。在韩国,发酵茶在智异山和保宁由家庭手工业间歇地生产以用于消费。
发酵茶在风味方面与粗茶有所不同。根据具体的发酵过程和微生物的种类,发酵茶还可在活性成分的种类和含量方面表现出巨大差异。因此,可以从中生产和分离各种化合物,已经进行了各种尝试来使用绿茶分离和鉴定未知的新型化合物。
槲皮素类化合物是一种类黄酮,并且其中大多数以天然存在的糖苷形式存在,根据糖类的类型,槲皮素类化合物包括槲皮苷、异槲皮苷、槲皮黄苷(quercimeritrin)、扁蓄苷、金丝桃苷、瑞诺苷(reynoutrin)、葡萄糖醛酸苷(querciturone)和芸香苷。
技术实现要素:
技术问题
一方面,本发明的目的是从后发酵茶中发现一种新型槲皮素类化合物并在工业上使用该槲皮素类化合物。
另一方面,本发明的目的是提供一种制备新型槲皮素类化合物的方法,以提高该槲皮素类化合物工业实用性。
技术方案
为了实现上述目的,根据一个方面,本发明提供由下式1表示的化合物、其异构体、其药学上可接受的盐、其水合物或其溶剂化物:
其中r1可以是c15h9o7,r2可以是h或c6h11o5,r3可以是c9h7o2。
另一方面,本发明提供了制备该化合物、其异构体、其药学上可接受的盐、其水合物或其溶剂化物的方法。
有益效果
一方面,本发明使得能够从后发酵茶分离特定的新型化合物并在工业上利用该新型化合物,以便该新型化合物可以广泛地用于后发酵茶相关工业和可以使用该化合物的各种领域,从而满足了相关消费者的需求。
附图说明
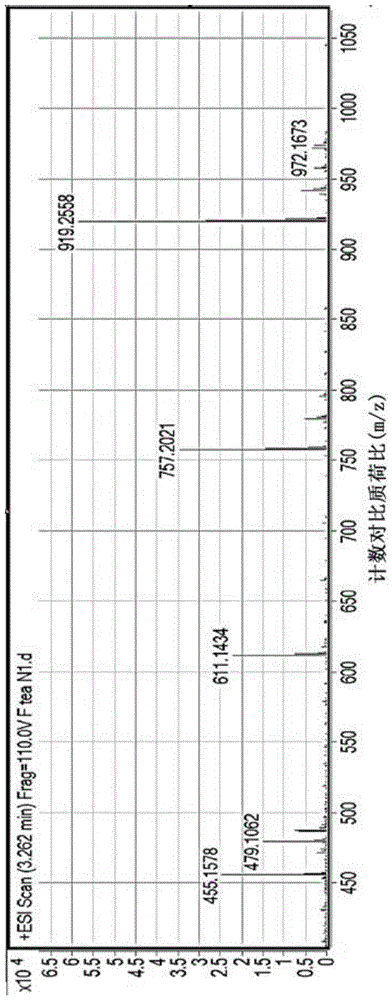
图1示出槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的ms谱。
图2示出槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的1h-nmr(核磁共振)谱。
图3示出槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的13c-nmr谱。
图4示出槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的1h-13chsqc(异核单量子相干)谱。
图5示出槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的1h-13chmbc(异核多键相干)谱。
图6示出槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的ms谱。
图7示出槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的1h-nmr谱。
图8示出槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的13c-nmr谱。
图9示出槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的1h-13chsqc(异核单量子相干)谱。
图10示出槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的1h-13chmbc(异核多键相干)谱。
图11示出根据本发明的一个方面的化合物对β淀粉样蛋白聚集的影响。
具体实施方式
[实施方式]
如本文所用,术语“后发酵”包括使用除茶叶子中存在的酶之外的微生物或物质进行的发酵。后发酵茶包括通过上述方法发酵的绿茶。
如本文所用,术语“级分”包括通过使用某种溶剂将特定物质或提取物分级所获得的那些物质或分级后留下的那些物质,以及通过再次用特定溶剂提取它们所获得的那些物质。分级方法和提取方法可以是本领域技术人员已知的任何方法。
如本文所用,“异构体”不仅包括光学异构体(例如,基本上纯的对映异构体、基本上纯的非对映异构体或其混合物),还包括构象异构体(即,仅在一个或多个化学键的角度上彼此不同的异构体)、位置异构体(特别是互变异构体)或几何异构体(例如顺-反异构体)。
如本文所用,“基本上纯的”是指,例如当在对映异构体或非对映异构体中使用时是指,特定化合物(例如对映异构体或非对映异构体)以约90%(w/w)或更多,优选约95%或更多,更优选约97%或更多或约98%或更多,更优选约99%或更多,甚至更优选约99.5%或更多的量存在。
如本文所用,“药学上可接受的”是指当以通常使用的药物剂量使用时没有实质毒性作用,因此能够被或被政府或同等监管机构批准或在药典中列举或在其他一般药典中公认用于动物,尤其是人类。
如本文所用,“药学上可接受的盐”是指药学上可接受并且具有期望的母体化合物的药理活性的根据本发明的一方面的盐。所述盐可包括(1)利用无机酸形成的酸加成盐,无机酸为例如盐酸、氢溴酸、硫酸、硝酸和磷酸;或利用有机酸形成的酸加成盐,有机酸为例如乙酸、丙酸、己酸、环戊烷丙酸、乙醇酸、丙酮酸、乳酸、丙二酸、丁二酸、苹果酸、马来酸、富马酸、酒石酸、柠檬酸、苯甲酸、3-(4-羟基苯甲酰基)苯甲酸、肉桂酸、扁桃酸、甲磺酸、乙磺酸、1,2-乙烷-二磺酸、2-羟基乙磺酸、苯磺酸、4-氯苯磺酸、2-萘磺酸、4-甲苯磺酸、樟脑磺酸、4-甲基二环[2,2,2]-辛-2-烯-1-羧酸、葡庚糖酸、3-苯基丙酸、三甲基乙酸、叔丁基乙酸、月桂基硫酸、葡糖酸、谷氨酸、羟基萘甲酸、水杨酸、硬脂酸或粘康酸;或(2)当存在于母体化合物中的酸性质子被取代时形成的盐。
如本文所用,“水合物”是指与水键合的化合物。该术语被广义地使用,包括缺少与水的化学键合的包合物。
如本文所用,“溶剂化物”是指溶质的分子或离子与溶剂的分子或离子之间形成的高级化合物。
一方面,本发明提供由下式1表示的化合物、其异构体、其药学上可接受的盐、其水合物或其溶剂化物:
其中r1可以是c15h9o7,r2可以是h或c6h11o5,r3可以是c9h7o2。
在一个实施方式中,r1可以是由下式2表示的化合物:
在另一个实施方式中,r2可以是由下式3表示的化合物:
r3可以是由下式4表示的化合物:
在另一个实施方式中,该化合物可以是槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]。槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]可由下式表示:
在另一个实施方式中,该化合物可以是槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]。槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]可由下式表示:
一方面,本发明涉及现有技术中未知的新物质。本发明人在对后发酵茶进行持续研究后发现并分离了该新物质。根据本发明的一个方面的化合物具有例如抑制β淀粉样蛋白聚集的有用性(参见图11)。β淀粉样蛋白聚集是药物和相关领域中的临床适用性质,因此可以清楚地理解本发明在工业上是可应用的。对该化合物的有用性的进一步研究可使该化合物用于各种工业应用。
在一个实施方式中,化合物的含量可以是0.01重量%或更多、0.05重量%或更多、0.1重量%或更多、0.2重量%或更多、0.3重量%或更多、0.4重量%或更多、0.5重量%或更多、0.7重量%或更多、0.9重量%或更多、1.0重量%或更多、1.3重量%或更多、1.5重量%或更多、1.7重量%或更多、2.0重量%或更多、2.2重量%或更多、2.5重量%或更多、2.8重量%或更多、3.0重量%或更多、3.3重量%或更多、3.5重量%或更多、3.8重量%或更多、4.0重量%或更多、4.5重量%或更多、5.0重量%或更多、5.5重量%或更多、6.0重量%或更多、8.0重量%或更多、10重量%或更多、12重量%或更多、15重量%或更多、或20%重量%或更多。另外,化合物的含量可以是18重量%或更少、15重量%或更少、12重量%或更少、10重量%或更少、8.0重量%或更少、6.0重量%或更少、5.5重量%或更少、5.0重量%或更少、4.5重量%或更少、4.0重量%或更少、3.8重量%或更少、3.5重量%或更少、3.3重量%或更少、3.0重量%或更少、2.8重量%或更少、2.5重量%或更少、2.2重量%或更少、2.0重量%或更少、1.7重量%或更少、1.5重量%或更少、1.3重量%或更少、1.0重量%或更少、0.9重量%或更少、0.8重量%或更少、0.7重量%或更少、0.5重量%或更少、0.4重量%或更少、0.3重量%或更少、0.2重量%或更少、0.1重量%或更少、0.05重量%或更少、或0.03重量%或更少。
在另一方面,本发明提供了制备该化合物、其异构体、其药学上可接受的盐、其水合物或其溶剂化物的方法。制备方法可包括合成、从天然产物中分离等。
在一个实施方式中,制备方法可以是使绿茶发酵,然后分离绿茶。制备方法可以包括将发酵生物接种到绿茶叶子中,使绿茶叶子发酵,用热空气干燥并使它们陈化的步骤。该制备方法还可以包括在陈化之后进行提取和分级以分离化合物的步骤。
可以使用水、有机溶剂等进行提取和分级,并采用本领域技术人员已知的任何方法。
在另一方面,可以在提取之后进行分级。分级可以使用酮进行,或者可以通过使用醇(例如乙醇)提取已用酮分级的成分来进行。酮的实例包括:丙酮、香芹酮、胡薄荷酮、异长叶烷酮、2-庚酮、2-戊酮、3-己酮、3-庚酮、4-庚酮、2-辛酮、3-辛酮、2-壬酮、3-壬酮、2-十一烷酮、2-十三烷酮、甲基异丙基酮、乙基异戊基酮、亚丁基丙酮、甲基庚烯酮、二甲基辛烯酮、香叶基丙酮、法尼基丙酮、2,3-戊二酮、2,3-己二酮、3,4-己二酮、2,3-庚二酮、戊基环戊酮、戊基环戊烯酮、2-环戊基环戊酮、己基环戊酮、2-正庚基环戊酮、顺式茉莉酮、二氢茉莉酮、3,4-二甲基-2-羟基-2-环戊烯-1-酮(methylcorylone)、2-叔丁基环己酮、对叔丁基环己酮、2-仲丁基环己酮、芹菜酮、隐品酮(cryptone)、对叔戊基环己酮、甲基环己烯基乙酮(methylcyclocitrone)、橙花酮(nerone)、4-环己基-4-甲基-2-戊酮、氧化酮、乙基甲基羟基呋喃酮(emoxyfurone)、甲基萘基酮、α-甲基茴香酰丙酮(α-methylanisalacetone)、茴香基丙酮、对甲氧基苯基丙酮、亚苄基丙酮、对甲氧基苯乙酮、对甲基苯乙酮、苯丙酮、苯乙酮、α-王朝酮(α-dynascone)、鸢尾香酮(iritone)、紫罗兰酮、假紫罗兰酮、甲基紫罗兰酮、甲基鸢尾香酮、2,4-二叔丁基环己酮、烯丙基紫罗兰酮、2-乙酰基-3,3-二甲基降冰片烷、马鞭草烯酮、葑酮(fenchone)、环十五烷酮、环十六烯酮等。酮的实例还包括通常用于本领域作为溶剂的酮及其混合物,优选可以为丙酮。
在另一个实施方式中,发酵可以通过后发酵方法来进行。后发酵可以通过菌株接种来进行,菌株可以是选自酵母属(saccharomycessp.)、芽孢杆菌属(bacillussp.)、乳杆菌属(lactobacillussp.)或肠系膜明串珠菌属(leuconostocmesenteroidessp.)的菌株,优选地,可以选自酿酒酵母(saccharomycescerevisiae)、干酪乳杆菌(lactobacilluscasei)、枯草芽孢杆菌(bacillussubtilis)、保加利亚乳杆菌(lactobacillusbulgarius)或肠系膜明串珠菌(leuconostocmesenteroides)。
在下文中,将通过实施例和测试例更详细地描述本发明的构成和效果。然而,提供以下实施例仅用于说明目的,以便于理解本发明,并且本发明的范围不限于此。
实施例1:后发酵茶样品的制备
将水添加到由绿茶(camelliasinensisvar.yabukita)叶子制成的绿茶中,并将水含量调节至40wt%。用5×106cfu/g的枯草芽孢杆菌接种绿茶,在50℃下发酵3天,然后在80℃下发酵4天。
将陈化的茶样品粉碎15秒,然后使用筛孔尺寸为1mm的不锈钢筛进行筛分。随后,将50mg粉碎的产品添加到1.5mleppendorf管中,向其中添加1ml去离子水。将混合物在60℃的恒温水浴中以恒定速度搅拌30分钟,然后在25℃和13,000rpm下离心15分钟。分离出干燥的发酵绿茶提取物中不溶于水的部分。
实施例2:获得级分和分离化合物
通过使用丙酮对150g后发酵茶样品进行分级来除去儿茶素衍生物和咖啡因,并获得富集有其它化合物的可溶性物质。通过硅胶柱色谱法,使用氯仿:甲醇混合物(5:1,v/v)作为溶剂来首先分级出40g可溶于丙酮的物质。
使用高效逆流色谱法(hpccc,dynamicextractionsltd,英国),分级出8.9g不含咖啡因的氯仿:甲醇(5:1,v/v)级分。所使用的溶剂是正己烷-tbme(甲基叔丁基醚)-buoh-mecn-水(0.25:3:1:1:5,v/v),流速为25ml/分钟。在上述条件下,级分总共被分成10个亚级分,通过小容量hpccc(dynamicextractionsltd,英国)、hplc(高效液相色谱法)、sephadexlh-20柱(gehealthcarebio-sciences,瑞典)等分离每个级分中所含的成分。
结果,从级分中分离出槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]和槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷],这些是现有技术中未知的化合物。此外,使用1h-nmr(核磁共振光谱法)、13c-nmr、uv(紫外光谱法)和esi-ms(电喷雾电离质谱法)鉴定每种化合物的结构。对于1h和13c核磁共振(nmr),使用甲醇-d3作为溶剂,使用brukeradvancedpx-500(bruker,美国)作为仪器。使用6200系列精确质量飞行时间(tof)lc/ms(agilent,美国)分析每种化合物的ms谱。
作为分析的结果,发现所述化合物是现有技术中未知的新型化合物,所述化合物为用c42h46o23表示且分子量为918.2430的槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷],以及用c36h36o18表示且分子量为756.1902的槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]。
槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的化学式和nmr数据如下:
表1
槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的ms谱如图1所示,其1h-nmr谱和13c-nmr谱分别如图2和图3所示。其hsqc(异核单量子相干)谱如图4所示,其hmbc(异核多键相干)谱如图5所示。
槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的化学式和nmr数据如下:
表2
槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的ms谱如图6所示。其1h-nmr谱和13c-nmr谱分别如图7和图8所示。其hsqc(异核单量子相干)谱如图9所示,其hmbc(异核多键相干)谱如图10所示。
测试例1:对β-淀粉样蛋白聚集的抑制效果的确认
通过荧光分析(硫磺素t测定)确定槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]和槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]对β-淀粉样蛋白聚集的抑制作用。
具体地,获得β-淀粉样蛋白(aβ1-42,anaspecinc,美国)并以0.1mg/ml的浓度使用。在使用前将β-淀粉样蛋白储存在-80℃。桑色素(20μm)、酚红(20μm)、槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷](1mg/ml)、和槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷](1mg/ml)中的每种在dmso中稀释至这些浓度。为了确定对aβ1-42聚集的抑制程度,将如上浓度的每种化合物在50μl的0.01m的磷酸钠缓冲液稀释成10μm。然后,向其中添加40μl的0.1mg/mlaβ1-42,然后添加10μl的2mm硫磺素t。然后用荧光光谱仪(rf-5300pc,shimadzucorporation,日本)在37℃下以5分钟为间隔测量荧光150分钟。
结果在下表和图11中示出。
表3
在上表中,“rfu”表示相对荧光单位,“增加的rfu”表示聚集的β-淀粉样蛋白的量。“增加的rfu(阳性对照的百分比)”表示与阳性对照相比聚集的β-淀粉样蛋白的百分比。“新物质31”表示槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷],“新物质32”表示槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]。
当阳性对照的聚集(由“阳性对照”表示,未用化合物处理的β淀粉样蛋白聚集)设为100%时,与阳性对照相比,槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]和槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]分别减少11.2%和16.8%的聚集。该结果表明该物质与已知的抑制剂桑色素(21.4%)和酚红(6.4%)在抑制β-淀粉样蛋白聚集方面一样优异。因此,这两种化合物具有上述用途,因此可用于各种工业领域。
测试例2:累积皮肤刺激试验
进行hript(人重复性损伤性斑贴试验)以评估槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]和槲皮素3-o-[3-o”-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]的累积皮肤刺激性,并确定适用于皮肤的浓度范围。
具体地,随机选择15名健康成人受试者,并且将各自含有0.5重量%、1重量%或3重量%的化合物的20μl测试组合物(除了上述每种化合物之外的包含乳化剂、稳定剂、纯净水等的皮肤组合物)滴入每个室(iq室,epitestltd,芬兰)中。将斑贴施用在受试者背部右上侧,并且在施用24小时后将其替换为新斑贴。以这种方式,共施用9个斑贴,每周3次,持续3周。在施用每个斑贴之前和之后检查皮肤反应。在去除最后的斑贴的48小时后检查皮肤反应,并计算平均反应性。
结果如下表所示。
表4
根据国际接触性皮炎研究组(icdrg)的标准评估皮肤反应。在上表中,“新物质31”表示槲皮素3-o-[3-o”-(e)-p-香豆酰基][β-d-吡喃葡萄糖基-(1→3)-o-α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷],“新物质32”表示3-o-[3-o"-(e)-p-香豆酰基][α-l-吡喃鼠李糖基-(1→6)-o-β-d-吡喃葡萄糖苷]。在该含量范围内,两种物质均显示(-)反应性(没有受试者显示±,+,++或+++反应性),这表明该物质不会引起累积的皮肤刺激,因此可以安全地用于皮肤。
虽然已经描述了本发明的特定实施例,但是对于本领域技术人员来说显而易见的是,以上描述仅是优选实施方式,并且本发明的范围不限于此。因此,本发明的范围应由所附权利要求及其等同物限定。
- 还没有人留言评论。精彩留言会获得点赞!