含氮、氧、氧三取代六元环内脂化合物及制备方法和用途与流程
本发明属于酶催化杂环化合物合成技术领域,具体涉及含氮、氧、氧三取代六元环内脂化合物及制备方法和用途。
背景技术
杂环化合物是分子中含有杂环结构的有机化合物,构成环的原子除碳原子外,还至少含有一个杂原子。杂环化合物是数目最为庞大的一类有机化合物。最常见的杂原子是氮原子、硫原子、氧原子。杂环化合物的应用极为广泛,涉及人类日常生产及生活的方方面面,如染料、食物添加剂、炸药、农药及医药等等。尤其是在化学药研发领域,杂环类化合物占到了总数的一半以上,是名副其实的新药研发源泉。
杂环化合物的种类繁多,合成方法也是多种多样。随着杂环大小的增加及杂原子种类及数量的增加,其合成难度也呈指数倍的增长。以往报道过的杂环化合物合成普遍存在步骤长、收率低等缺点,反应过程中经常需要使用到强酸、强碱、高温高压等反应条件,不仅增加了生产安全隐患,而且对生态环境造成较大的伤害。杂环化合物合成工业中,多采用传统的重金属催化剂,对环境会有负面影响,重复利用度低,不利于大规模生产杂环化合物。更为重要的是,之前有相关文献报道过酶催化合成杂环化合物的研究,但其所用脂肪酶calb价格昂贵,每克售价高达300元人民币,无形中增加杂环化合物的生产成本,不适合今后的大规模生产。
技术实现要素:
本发明的目的在于克服现有杂环化合物合成技术中存在的缺陷,如:制备成本高、污染大、能耗大等问题,本发明提供了一种含氮、氧、氧三取代六元环内脂化合物。
所述化合物的结构式为:
r1为丙基、异丙基、丁基、异丁基、己基、苯基、对氟苯基或间位吡啶基;r2为甲基。
本发明还提供了一种氮、氧、氧三取代六元环内脂化合物的制备方法,具体地,本发明按以下技术方案进行:
将化合物1与2-羟基乙酸甲酯溶于有机溶剂中,得到混合液1;向混合液1中顺次加入脂肪酶、碳酸氢钠、乙酸苯酯、
上述步骤中,化合物1的结构式为
所述有机溶剂为甲基叔丁基醚;
上述步骤中,化合物1、2-羟基乙酸甲酯与碳酸氢钠的摩尔比为0.005-0.1:0.025-0.5:0.04-0.3;碳酸氢钠与苯酸乙酯摩尔比为0.04-0.3:0.06-0.3;
上述步骤中,化合物1与脂肪酶的质量比为2.7-15.4:0.09~1.0;
上述步骤中,所述脂肪酶为猪胰腺脂肪酶、卡门培尔青霉脂肪酶、洋葱伯克霍尔德菌脂肪酶、novozyme435或im-100;
上述步骤中,反应温度为-18-40℃,反应时间为24-48h。
本发明还提供了含氮、氧、氧三取代六元环内脂化合物的用途,所述化合物用于抗菌。与现有技术相比较,本发明的有益效果体现如下:
(1)本发明提供的合成含氮、氧、氧三取代六元环内脂化合物的方法,所利用的原料廉价易得,反应步骤简单,产率高,几乎无污染,反应无需高温加热,无刻薄危险反应条件,产品易提纯,适合于国内大规模生产。
(2)本发明合成含氮、氧、氧三取代六元环内脂化合物所用催化剂为绿色无毒的生物酶催化剂,相较传统杂环化合物合成中常用的金属催化剂,安全环保且易于回收,价格更加低廉且重复利用率高。整个制备方法步骤短,产率高,达72%。反应中所用脂肪酶催化剂除novozyme435外均来自国内企业,不受国外技术限制且成本低廉,所用脂肪酶每克价格均不超过10元人民币,适合于国内大量生产。
附图说明
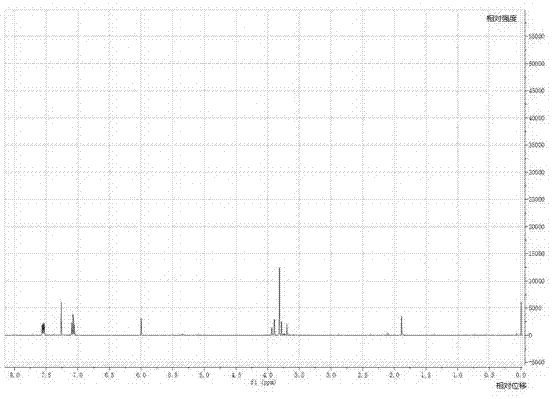
图1为本发明实施例1制备的含氮、氧三取代六元环内脂化合物的核磁共振氢谱;
图2为本发明实施例2制备的含氮、氧三取代六元环内脂化合物的核磁共振氢谱。
具体实施方式
为了加深对本发明的理解,下面将结合实施例和附图对本发明作进一步详述,该实施例仅用于解释本发明,并不构成对本发明保护范围的限定。
本发明所采用的具体反应式如下:
化合物1的结构式为
实施例1:
向装有15.4克化合物1(0.1mol,r1=对氟苯基,r2=甲基)、28毫升2-羟基乙酸甲酯(0.37mol)、0.8克im-100、4.8克
图1为本发明实施例1制备的含氮、氧三取代六元环内脂化合物的核磁共振氢谱。由图1可以得出,实施例1制备的化合物的核磁共振氢谱具体为:1hnmr(cdcl3)δ=3.80(1h,d,j=16.0hz),3.81(3h,s),3.91(1h,dd,j=16.0,4.0hz),6.00(1h,s),7.07(2h,t,8.0hz),7.44-7.49(2h,dd,8.0,4.0hz),说明含氮、氧三取代六元环内脂化合物1被成功制备。
实施例1制备的含氮、氧三取代六元环内脂化合物1的产率为72%,说明反应过程中,化合物1(r1=对氟苯基,r2=甲基)能够与脂肪酶im-100的酶结合位点进行较好的特异性结合,使得含氮、氧三取代六元环内脂化合物1的产率较高;另外,国产脂肪酶im-100的成本低,每克价格不超过10元人民币,并且催化活性高,降低了生产含氮、氧三取代六元环内脂化合物的成本,提高了产物的产率。
实施例2:
向装有10.2克化合物1(0.1mol,r1=丙基,r2=甲基)、28毫升2-羟基乙酸甲酯(0.37mol)、1.0克novozyme435、6.0克
图2为本发明实施例2制备的含氮、氧三取代六元环内脂化合物的核磁共振氢谱。由图2可以得出,1hnmr(cdcl3)δ=0.97(3h,t,j=7.27hz),1.36-1.45(1h,m),1.46-1.55(1h,m),1.65-1.74(1h,m),1.78-1.88(1h,m),3.30(1h,d,j=13.3hz),3.58(1h,d,j=13.3hz),4.21(1h,dd,j=3.3,9.9hz),说明含氮、氧三取代六元环内脂化合物2被成功制备。
实施例2制备的含氮、氧三取代六元环内脂化合物2的产率为70%,说明反应过程中,化合物1(r1=丙基,r2=甲基)能够与脂肪酶novozyme435的酶结合位点进行特异性结合,使得含氮、氧三取代六元环内脂化合物2的产率高;但是与实施例1采用的国产脂肪酶im-100相比,脂肪酶novozyme435的成本相对偏高。
实施例3:
向装有5.1克化合物1(50mmol,r1=异丙基,r2=甲基)、3.8毫升2-羟基乙酸甲酯(50mmol)、0.4克im-100、3.0克
实施例3制备的含氮、氧三取代六元环内脂化合物3的产率为42%,说明反应过程中,化合物1(r1=异丙基,r2=甲基)能够与脂肪酶im-100的酶结合位点进行特异性结合。与实例2相比,脂肪酶im-100对r1为直链丙基的化合物1底物选择性更高。
实施例4:
向装有13.6克化合物1(0.1mol,r1=苯基,r2=甲基)、38毫升2-羟基乙酸甲酯(0.5mol)、0.8克im-100、4.8克
本实施例4中化合物1底物与实施例1类似而产率相对较低,说明亲核试剂2-羟基乙酸甲酯过量时,会降低含氮、氧三取代六元环内脂化合物的产率。
实施例5:
向装有2.7克化合物1(20mmol,r1=间位吡啶基,r2=甲基)、3.0毫升2-羟基乙酸甲酯(40mmol)、90毫克猪胰腺脂肪酶、3克
实施例5制备的含氮、氧三取代六元环内脂化合物5的产率为20%,说明反应过程中,脂肪酶猪胰腺脂肪酶对r1为间位吡啶基的化合物1底物选择性较低,间位吡啶基的基团较大,使得r1为间位吡啶基的化合物1与脂肪酶im-100的酶结合位点进行特异性结合比较困难。有文献报道过带间位吡啶基团的底物对酶有一定抑制作用,此实例中较低的产率进一步验证了此类假设。
实施例6:
向装有8.7克化合物1(50mmol,r1=丁基,r2=甲基)、19毫升2-羟基乙酸甲酯(250mmol)、260毫克洋葱伯克霍尔德菌脂肪酶、2克
实施例6制备的含氮、氧三取代六元环内脂化合物6的产率为60%,说明洋葱伯克霍尔德菌脂肪酶的选择催化活性相较im-100稍低。
实施例7:
向装有8.7克化合物1(50mmol,r1=异丁基,r2=甲基)、14毫升2-羟基乙酸甲酯(0.19mol)、522毫克卡门培尔青霉脂肪酶、3克
实施例7制备的含氮、氧三取代六元环内脂化合物7的产率为37%,说明卡门培尔青霉脂肪酶的选择催化活性相较im-100明显降低。
实施例8:
向装有14.4克化合物1(0.1mol,r1=己基,r2=甲基)、28毫升2-羟基乙酸甲酯(0.37mol)、0.8克洋葱伯克霍尔德菌脂肪酶、4.8克
实施例8制备的含氮、氧三取代六元环内脂化合物8的产率为55%。与实施例6结果对照可明显得出以下结论:随着r1取代基团长度的增加,含氮、氧三取代六元环内脂化合物产率明显随之下降。
本发明中采用的有机溶剂为甲基叔丁基醚,本发明是在大量的有机溶剂中最终筛选的结果,选用其他的有机溶剂时,制备的含氮、氧三取代六元环内脂化合物产率较低,生成的副产物较多,不利于分离纯化;而使用甲基叔丁基醚,制备得到的含氮、氧三取代六元环内脂化合物时,生产的副产物极少,有利于后续进行分离纯化。
抗菌实验测试:
本发明采用96孔板法对实施例1-2制备的含氮、氧三取代六元环内脂化合物1(结构式为
表1实施例1-2制备的含氮、氧三取代六元环内脂化合物对12种细菌的最低抑制浓度
由表1可以看出,两种含氮、氧三取代六元环内脂化合物对12种细菌呈现出了较低的最低抑制浓度;与克拉霉素相比,除了金黄色葡萄球菌5676、肺炎链球菌1210、肺炎链球菌2860、嗜血杆菌流感2412、嗜血杆菌流感5096之外,含氮、氧三取代六元环内脂化合物1、含氮、氧三取代六元环内脂化合物2对其他细菌的抑菌效果均优于克拉霉素。本发明制备的含氮、氧三取代六元环内脂化合物1、含氮、氧三取代六元环内脂化合物2对上述细菌均呈现出了良好的抑菌效果。
因此,本发明制备的含氮、氧、氧三取代六元环内脂化合物能够用于抗菌领域,包括金黄色葡萄球菌、肺炎链球菌、嗜血杆菌流感等。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!