一种壳寡糖硫脲类衍生物、由其制备的纳米银及该纳米银的应用的制作方法
本发明属于壳寡糖衍生物应用技术领域,具体涉及一种壳寡糖硫脲类衍生物、由其制备的纳米银及该纳米银的应用。
背景技术:
植物三类病害(真菌、细菌和病毒病害)中,由病原真菌引起的约占病害总数的70%-80%,每年因真菌病害引起的作物产量损失很大。如小麦的200多种病害中,真菌病害就占了90%,每年造成的损失占总产量的10-20%;由青枯病菌引起的玉米叶过早枯萎会使玉米产量损失20-30%,严重的损失可达50%以上甚或绝收。尽管不断有新的抑菌剂研制出来,但易抗药性使得新药的研制仍是一项十分重要的任务。
银纳米粒子因为在抑菌、催化和表面增强拉曼等领域的广泛应用而一直倍受关注。目前,由于抗生素滥用引起抗生素拮抗造成的威胁日益严峻,使得对纳米银抑菌活性的研究兴趣复苏。纳米银是利用前沿纳米技术将银纳米化,使银在纳米状态下的抑菌能力产生了质的飞跃。纳米银的性能与其粒径有直接关系。一般而言,粒径越小,杀菌性能越强。纳米银杀菌具有以下特点:1、广谱抑菌,纳米银颗粒直接进入菌体与氧代谢酶(-sh)结合,使菌体窒息而死的独特作用机制,可杀死与其接触的大多数细菌、真菌、霉菌、孢子等微生物。2、强效杀菌,据研究发现,纳米银可在数分钟内杀死650多种细菌。3、渗透性强,纳米银颗粒具有超强的渗透性,可迅速渗入皮下2mm杀菌,对普通细菌、顽固细菌、耐药细菌以及真菌引起的较深处的组织感染均有良好的杀菌作用。4、修复再生,纳米银可促进伤口愈合,促进受损细胞的修复与再生。5、抑菌持久,纳米银颗粒利用专利技术生产,外有一层保护膜,在人体内能逐渐释放,所以抑菌效果持久。6、无耐药性,纳米银属于非抗菌素杀菌剂,能杀灭各种致病微生物,10nm大小的纳米银颗粒独特抗菌机理可迅速直接杀死细菌,使其丧失繁殖能力,无法生产耐药性的下一代,能有效避免因耐药性而导致反复发作久治不愈。
纳米银的这些抑菌特点无疑给纳米银抑菌的广泛应用开辟了广阔的前景,是最新一代的天然抑菌剂。
纳米银的制备方法按反应机理分主要可以分为两大类:物理方法和化学方法。物理方法主要是用物理手段如机械研磨、辐射等来使银单质变为纳米级尺寸。如:xu等人在-196℃的低温下对银粉进行高能机械球磨,得到了平均粒径约为20nm的银颗粒粉末;chang等人在nacl溶液中用激光烧蚀溅射银片,使其破裂,同时不断搅拌防止烧蚀形成的纳米银颗粒团聚,可以制备平均粒径26nm的银颗粒。虽然各种物理方法原理简单,但由于仪器设备的要求高,生产费用昂贵,使其使用受到限制。化学方法是被广泛应用于制备纳米银的方法,主要有化学还原法、物理还原法和生物还原法。化学还原法是目前实验室和工业上使用比较广泛的方法之一。用还原剂将银从它的化合物或盐中还原出来,采用的银盐主要是agno3或其配合物,还原剂主要有硼氢化钠、水合肼、甲醛、多元醇、抗坏血酸以及比ag活泼的金属等,常加入分散剂或保护剂聚乙烯吡咯烷酮(pvp)、山梨醇、聚乙烯醇等控制生成物的粒径及形状。化学还原中所用试剂在使用过程中可能对环境或者生物体有危害作用,因此,环境友好、绿色的银纳米粒子制备方案亟待出现。张晟卯等依据离子液体的环境友好的特性,在室温离子液体中合成银纳米微粒,实验中离子液体不仅作为溶剂而且作为修饰剂阻止银纳米微粒的团聚。还可用化学合成法制备纳米银材料,zhou等利用紫外光辐射agno3,在聚乙烯醇的保护下制备出银纳米棒和树枝状纳米晶体。yin等利用微波合成法,在柠檬酸三钠存在的状态下用甲醛作为还原剂可以制各种粒径分布较窄的纳米银粉。通常,纳米粒子在形成过程中因其疏水性而容易发生聚集,为了合成分散性好的金属纳米粒子,需要在制备过程中加入稳定剂,如:大分子聚合物、枝状化合物、聚电解质、表面活性剂等。由于壳寡糖分子结构中存在大量自由的氨基和羟基,因而具有ph可控的溶解性聚阳离子、螯合以及易成膜和水凝胶的性能。壳聚糖在金属纳米粒子的制备过程中常被用作保护剂,因为它的水溶性及与亲水聚合物相似的性质,在纳米粒子的制备过程中可以吸附在金属离子的表面形成配合物,从而起到稳定剂的作用。
壳聚糖是其从甲壳动物的贝壳和细胞壁获得的几丁质经脱乙酰化处理的衍生物,是来源广泛、储量丰富、成本低廉的天然生物高分子材料。作为一种生物多聚糖,壳聚糖同时具有生物可降解、生物相容和无毒、抗菌、抗凝血等特性,其分子结构中含有丰富的氨基和羟基。但由于壳聚糖不溶于水,只溶于某些酸和少数有机溶剂,使其使用范围严重受限。壳聚糖降解为壳寡糖,其水溶性虽有改善,但其抑菌性能的提升效果甚微。因此,对壳寡糖进行改性和化学修饰十分必要。目前的改性方法有季铵盐化、酰化、羧基化等。其中有关一系列壳寡糖季铵盐衍生物抗真菌活性的报道显示,与壳聚糖相比,所有的季铵化壳寡糖衍生物具有更好的抑菌活性,而且最大抑制指数是在体外86.7%。壳寡糖季铵盐的抑菌机理比较复杂,tokura认为具有季铵基团阳离子的壳寡糖季铵盐与细菌细胞壁表面的酸性高分子相互作用,可形成高分子电解质聚合物,在细胞周围形成不具有渗透性的表层,阻止营养物质透过细胞壁而使细菌不能进行新陈代谢而致其死亡。
在过去的几十年里,壳寡糖硫脲类化合物因具有良好的抑菌性能一直备受关注。eweis,elkholy和elsabee制备了壳寡糖硫脲类衍生物(tucs),生物活性测试结果发现这些化合物对实验真菌具有显著抑制作用。本申请是参考文献方法制备寡糖硫脲衍生物,并利用它作为还原剂和保护剂与硝酸银反应在较低温度下制备稳定、单分散的纳米银溶液,并研究其对常见的作物病原菌的抑制活性。
技术实现要素:
为了解决上述问题,本发明提供一种壳寡糖硫脲类衍生物、由其制备的纳米银及该纳米银的应用,以壳寡糖为原料,合成壳寡糖硫脲类衍生物,然后作为还原剂和稳定剂,制备纳米银溶液。探究制备纳米银的最佳反应条件,并对其结构进行了表征,最后对壳寡糖硫脲类衍生物以及制备的纳米银溶液对几种常见的植物致病菌进行抑菌活性实验。
本发明的目的是以下述方式实现的:
一种壳寡糖硫脲类衍生物,所述壳寡糖硫脲类衍生物是如下式的化合物;其中7≦n≦23,n为整数:
r为
一种制备上述的壳寡糖硫脲类衍生物的方法,先将壳寡糖溶解于乙醇溶液和氨水中,再依次加入cs2溶液、氯乙酸钠和底物,边加边搅拌,壳寡糖先和cs2溶液反应生成二硫代氨基甲酸壳寡糖铵,二硫代氨基甲酸壳寡糖铵与氯乙酸钠反应生成羧甲基二硫代氨基甲酸壳寡糖钠,羧甲基二硫代氨基甲酸壳寡糖钠再与底物反应生成壳寡糖硫脲类衍生物。
如上述的制备壳寡糖硫脲类衍生物的方法,包括以下步骤:
(1)溶解壳寡糖:将壳寡糖加入到95%的乙醇溶液中搅拌均匀,得混合物ⅰ,将混合物ⅰ加入氨水中,边加边搅拌,混合物ⅰ添加完毕后,溶液呈深棕色粘性液体,继续搅拌0.5-1h,得混合物ⅱ;壳寡糖单元与95%的乙醇溶液的摩尔体积比为(0.010-0.060)mol:(15-60)ml,壳寡糖单元与氨水的摩尔体积比为(0.010-0.060)mol:(10-40)ml;
(2)合成二硫代氨基甲酸壳寡糖铵:将cs2溶液滴加到混合物ⅱ中,搅拌2-3h,溶液颜色加深,得混合物ⅲ,壳寡糖单元与cs2的摩尔比为(0.010-0.060)mol:(0.03-0.10)mol;
(3)合成羧甲基二硫代氨基甲酸壳寡糖钠:将氯乙酸钠加入到混合物ⅲ中,搅拌0.5-2h,得混合物ⅳ,壳寡糖单元与氯乙酸钠的摩尔比为(0.010-0.060)mol:(0.03-0.15)mol;
(4)合成壳寡糖硫脲类衍生物:将胺类化合物加入到混合物ⅳ中,壳寡糖单元与胺类化合物的摩尔比为(0.010-0.060)mol:(0.03-0.12)mol,溶液颜色变为深褐色,在室温下搅拌反应2-4h,将反应溶液加入到50-100ml无水乙醇中,有棕色沉淀析出,减压抽滤,用无水乙醇反复洗涤滤饼,得产物;将产物在50-60℃下真空干燥10-12h,得壳寡糖硫脲类衍生物纯品。
所述胺类化合物为水合肼、乙二胺、乙醇胺、苯肼、2-氨基吡啶或甲基肼。
所述水合肼为80%的水合肼水溶液。
一种利用上述的壳寡糖硫脲类衍生物制备纳米银的方法,它是通过壳寡糖硫脲类衍生物溶液与agno3溶液反应生成纳米银。
包括以下步骤:壳寡糖硫脲类衍生物溶液与agno3溶液混合,混合溶液中壳寡糖硫脲类衍生物与agno3的单元摩尔比为(2-8):(3-9),于20-60℃下反应30-100min得纳米银。
所述混合溶液中,壳寡糖硫脲类衍生物的浓度为0.001-0.01mol/l,agno3的浓度为0.001-0.04
mol/l。
一种纳米银,它为采用上述方法制备获得。
如上述的纳米银在植物抑菌方面的应用。
相对于现有技术,本发明利用合成的壳寡糖硫脲类衍生物作为还原剂和稳定剂制备了纳米银,并单独探究了苯氨基硫脲壳寡糖(a4)还原制备纳米银溶的影响因素:一定条件下,温度越高反应越迅速;一定条件下苯氨基硫脲壳寡糖(a4)浓度越大,生成纳米银(b4)吸收峰越强;一定条件下,硝酸银的用量有最优选择,并非越多越好;
利用紫外可见吸收光谱,通过追踪壳寡糖-水合肼硫脲衍生物还原制备纳米银溶液的过程,基本认识清楚了纳米银的形成过程;
通过透射电镜照片观察了不同的纳米银的形貌,6种壳寡糖硫脲类衍生物所得到的纳米银颗粒均为小于10nm左右的球形颗粒,纳米银溶液表现为透明的血红色。证明了壳寡糖硫脲类衍生物还原制备纳米银方法的可行性;对药品及纳米银进行抑菌活性实验的探究,基本了解了壳寡糖硫脲类衍生物及纳米银溶液的抑菌活性的强弱。修饰后的壳寡糖衍生物及其形成的纳米银溶液均比未修饰的壳寡糖活性高。
附图说明
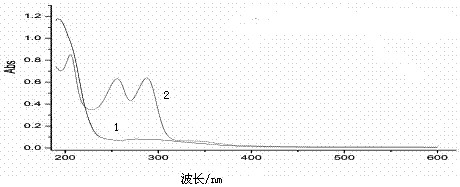
图1是壳寡糖与铵硫代氨基硫脲壳寡糖紫外吸收光谱,其中1是壳寡糖,2是铵硫代氨基硫脲壳寡糖。
图2是壳寡糖、铵硫代氨基硫脲壳寡糖与苯氨基硫脲壳寡糖(a4)紫外吸收光谱,其中1是壳寡糖,2是铵硫代氨基硫脲壳寡糖,3是苯氨基硫脲壳寡糖(a4)。
图3是壳寡糖、铵硫代氨基硫脲壳寡糖与吡啶-2-氨基硫脲壳寡糖(a5)紫外吸收光谱,其中1是壳寡糖,2是铵硫代氨基硫脲壳寡糖,3是n-(2-吡啶)-n'-壳寡糖硫脲(a5)。
图4是壳寡糖、铵硫代氨基硫脲壳寡糖与甲氨基硫脲壳寡糖(a6)紫外吸收光谱,其中1是壳寡糖,2是铵硫代氨基硫脲壳寡糖,3是甲氨基硫脲壳寡糖(a6)。
图5是壳寡糖、苯氨基硫脲壳寡糖(a4)红外吸收光谱对比图。
图6是壳寡糖、吡啶-2-氨基硫脲壳寡糖(a5)红外吸收光谱对比。
图7是壳寡糖、甲氨基硫脲壳寡糖(a6)红外吸收光谱对比图。
图8是氨基硫脲壳寡糖(a1)还原制备银纳米粒子(b1)的uv-vis吸收光谱,图中箭头从下到上依次为氨基硫脲壳寡糖(a1)与agno3反应开始0min、10min、20min、30min、40min生成纳米银的紫外吸收光谱。
图9是氨基硫脲壳寡糖(a1)还原制备纳米银(b1)溶液随着时间的颜色变化,从左至右为从反应开始0min、10min、20min、30min、40min。
图10是不同浓度苯氨基硫脲壳寡糖(a4)还原制备银纳米粒子(b4)的uv-vis吸收光谱,其中1:0.001mol/l,2:0.002mol/l,3:0.003mol/l,4:0.004mol/l,5:0.005mol/l。
图11是不同浓度苯氨基硫脲壳寡糖(a4)(1:0.001mol/l,2:0.002mol/l,3:0.003mol/l,4:0.004mol/l,5:0.005mol/l)制备纳米银(b4)的颜色比较。
图12是n-(2-吡啶)-硫脲(a5)制备纳米银(b5)过程的紫外-可见吸收光谱,其中1.n-(2-吡啶)-n'-壳寡糖硫脲(a5);2.0min(反应开始);3.10min;4.20min;5.30min;6.40min;7.48h。
图13是n-(2-吡啶)-硫脲(a5)制备纳米银(b5)的颜色随时间的变化,从左至右依次为0min、10min、20min、30min、40min。
图14是甲氨基硫脲壳寡糖(a6)制备纳米银(b6)过程的紫外-可见吸收光谱,其中1.甲氨基硫脲壳寡糖(a6);2.0min(反应开始);3.10min;4.20min;5.30min;6.40min;7.48h。
图15是甲氨基硫脲壳寡糖(a6)制备纳米银(b6)的颜色随时间的变化,从左至右为从反应开始0min、10min、20min、30min、40min。
图16是氨基硫脲壳寡糖(a1)还原制备纳米银(b1)的扫描电镜结果。
图17是n-(2-氨乙基)-硫脲(a2)还原制备纳米银(b2)的电镜扫描结果。
图18是苯氨基硫脲壳寡糖(a4)做还原剂制备纳米银(b4)的电镜扫描结果。
图19是n-(2-吡啶)-硫脲(a5)做还原剂制备纳米银(b5)的电镜扫描结果。
图20是甲氨基硫脲壳寡糖(a6)做还原剂制备纳米银(b6)的电镜扫描结果。
具体实施方式
因硫脲结构具有温和的还原性,本发明以低分子量壳寡糖(分子量1100-3600)为主要原料合成了壳寡糖硫脲衍生物的合成,并分别用制备的壳寡糖硫脲衍生物为还原剂在室温下制备了稳定的纳米银溶液,对其结构进行了表征。
本发明的化学反应方程式如下:
a1为:
一种壳寡糖硫脲类衍生物,所述壳寡糖硫脲类衍生物是如下式的化合物;其中7≦n≦23:
r为
一种制备上述的壳寡糖硫脲类衍生物的方法,先将壳寡糖溶解于乙醇溶液和氨水中,再依次加入cs2溶液、氯乙酸钠和底物,边加边搅拌,壳寡糖先和cs2溶液反应生成二硫代氨基甲酸壳寡糖铵,二硫代氨基甲酸壳寡糖铵与氯乙酸钠反应生成羧甲基二硫代氨基甲酸壳寡糖钠,羧甲基二硫代氨基甲酸壳寡糖钠再与底物反应生成壳寡糖硫脲类衍生物。
如上述的制备壳寡糖硫脲类衍生物的方法,包括以下步骤:
(1)溶解壳寡糖:将壳寡糖加入到95%的乙醇溶液中搅拌均匀,得混合物ⅰ,将混合物ⅰ加入氨水中,边加边搅拌,混合物ⅰ添加完毕后,溶液呈深棕色粘性液体,继续搅拌0.5-1h,得混合物ⅱ;壳寡糖单元与95%的乙醇溶液的摩尔体积比为(0.010-0.060)mol:(15-60)ml,壳寡糖单元与氨水的摩尔体积比为(0.010-0.060)mol:(10-40)ml;
(2)合成二硫代氨基甲酸壳寡糖铵:将溶液滴加到混合物ⅱ中,搅拌2-3h,溶液颜色加深,得混合物ⅲ,壳寡糖单元与的摩尔比为(0.010-0.060)mol:(0.03-0.10)mol;
(3)合成羧甲基二硫代氨基甲酸壳寡糖钠:将氯乙酸钠加入到混合物ⅲ中,搅拌0.5-2h,得混合物ⅳ,壳寡糖单元与氯乙酸钠的摩尔比为(0.010-0.060)mol:(0.03-0.15)mol;
(4)合成壳寡糖硫脲类衍生物:将胺类化合物加入到混合物ⅳ中,壳寡糖单元与胺类化合物的摩尔比为(0.010-0.060)mol:(0.03-0.12)mol,溶液颜色变为深褐色,在室温下搅拌反应2-4h,将反应溶液加入到50-100ml无水乙醇中,有棕色沉淀析出,减压抽滤,用无水乙醇反复洗涤滤饼,得产物;将产物在50-60℃下真空干燥10-12h,得壳寡糖硫脲类衍生物纯品。
所述胺类化合物为水合肼、乙二胺、乙醇胺、苯肼、2-氨基吡啶或甲基肼。
所述水合肼为80%的水合肼水溶液。
一种利用上述的壳寡糖硫脲类衍生物制备纳米银的方法,它是通过壳寡糖硫脲类衍生物溶液与agno3溶液反应生成纳米银。
包括以下步骤:壳寡糖硫脲类衍生物溶液与agno3溶液混合,混合溶液中壳寡糖硫脲类衍生物与agno3的单元摩尔比为(2-8):(3-9),于20-60℃下反应30-100min得纳米银。
所述混合溶液中,壳寡糖硫脲类衍生物的浓度为0.001-0.01mol/l,agno3的浓度为0.001-0.04mol/l。
一种纳米银,它为采用上述方法制备获得。
如上述的纳米银在植物抑菌方面的应用。
实施例:均相条件下合成壳寡糖衍生物:
实施例1:氨基硫脲壳寡糖a1及纳米银溶液b1的合成
称取壳寡糖8.0g(单元摩尔数0.05mol)于圆底烧瓶中,用20.0ml95%的乙醇溶解后,在搅拌状态下将15.0ml(0.04mol)氨水缓慢加入该溶液中,室温下搅拌0.5h;接着将cs2(3.8ml,0.06mol))滴加到上述溶液中,室温搅拌反应2h;再将氯乙酸钠(5.8g,0.05mol)缓慢加入到该反应液中,反应0.5h;然后再量取80%水合肼6.0ml(0.12mol)缓慢加入到上述反应液中,搅拌反应3h;最后将反应液缓慢倒入到约50ml无水甲醇中,有青灰絮状沉淀析出,静置,去除上清液,换用无水乙醇反复洗涤7次,抽滤,得产物,真空干燥(50℃,7h),得5.97g(单元摩尔数0.04mol)青灰色粉末。
10ml(单元摩尔质量235,单元摩尔数0.034mmol)氨基硫脲壳寡糖a1溶液与1.5mlagno3溶液(10mg/ml,0.088mmol)混合,氨基硫脲壳寡糖a1溶液的浓度为0.8mg/ml;混合溶液中,氨基硫脲壳寡糖a1的单元摩尔浓度为0.0029mol/l,agno3的浓度为0.0077mol/l,于20℃下反应60min得纳米银b1。
实施例2:氨基硫脲壳寡糖a1纳米银溶液b1的合成
称取壳寡糖1.6g(单元摩尔数0.01mol)于圆底烧瓶中,用15.0ml95%的乙醇溶解后,在搅拌状态下将35.0ml(0.04mol)氨水缓慢加入该溶液中,室温下搅拌0.8h;接着将cs2(1.9ml,0.03mol))滴加到上述溶液中,室温搅拌反应2.5h;再将氯乙酸钠(3.48g,0.03mol)缓慢加入到该反应液中,反应1h;然后再量取80%水合肼1.5ml(0.03mol)缓慢加入到上述反应液中,搅拌反应2h;最后将反应液缓慢倒入到约50ml无水甲醇中,有青灰絮状沉淀析出,静置,去除上清液,换用无水乙醇反复洗涤7次,抽滤,得产物,真空干燥(50℃,7h),得1.19g(单元摩尔数0.008mol)青灰色粉末。
10ml(单元摩尔质量235,单元摩尔数0.034mmol)氨基硫脲壳寡糖a1溶液与1.0mlagno3(10mg/ml,0.059mmol)溶液混合,氨基硫脲壳寡糖a1溶液的浓度为0.8mg/ml;混合溶液中,氨基硫脲壳寡糖a1的单元摩尔浓度为0.0029mol/l,agno3的浓度为0.0053mol/l,于30℃下反应30min得纳米银b1。
实施例3:n-(2-氨乙基)-硫脲壳寡糖a2及纳米银溶液b2的合成
称取壳寡糖(8g,单元摩尔数0.05mol)缓慢加入95%乙醇(20ml)中搅拌溶解后,将溶液缓慢加入氨水(20ml,0.52mol)中,呈深棕色粘性液体,室温下搅拌0.5h;接着将cs2(3.8ml,0.06mol)缓慢滴加到混合液中搅拌反应2h;称取氯乙酸钠(6g,0.05mol)缓慢加入到上述反应液中,继续搅拌反应0.5h;再量取乙二胺(6ml,0.09mol)滴加到反应液中,颜色变为墨绿色,在室温下再搅拌反应3h。最后将反应液缓慢加入到约50ml无水乙醇中,有浅灰色絮状沉淀析出,静置,去除上清液,用无水乙醇反复洗涤8次,抽滤,并用无水乙醇淋洗3次,将得到的产物真空干燥(55℃,8h),得土黄色粉末9.96g(单元摩尔数0.06mol)。
10ml(单元摩尔质量262,单元摩尔数0.032mmol)n-(2-氨乙基)-硫脲壳寡糖a2的溶液与1.5mlagno3(10mg/ml,0.088mmol)溶液混合,壳寡糖衍生物a2溶液的浓度为0.85mg/ml;混合溶液中,n-(2-氨乙基)-硫脲壳寡糖a2的的单元摩尔浓度为0.0028mol/l,agno3的浓度为0.0077mol/l,于30℃下反应70min得纳米银b2。
实施例4:n-(2-氨乙基)-硫脲壳寡糖a2及纳米银溶液b2的合成
称取壳寡糖(9.6g,单元摩尔数0.06mol)缓慢加入95%乙醇(60ml)中搅拌溶解后,将溶液缓慢加入氨水(40ml,0.52mol)中,呈深棕色粘性液体,室温下搅拌1h;接着将cs2(6.33ml,0.10mol)缓慢滴加到混合液中搅拌反应3h;称取氯乙酸钠(18g,0.15mol)缓慢加入到上述反应液中,继续搅拌反应2h;再量取乙二胺(6ml,0.09mol)滴加到反应液中,颜色变为墨绿色,在室温下再搅拌反应4h。最后将反应液缓慢加入到约100ml无水乙醇中,有浅灰色絮状沉淀析出,静置,去除上清液,用无水乙醇反复洗涤8次,抽滤,并用无水乙醇淋洗3次,将得到的产物真空干燥(60℃,10h),得土黄色粉末10.79g(单元摩尔数0.065mol)。
12ml(单元摩尔质量262,单元摩尔数0.046mmol)壳寡糖衍生物a2溶液与1.0mlagno3(10mg/ml,0.0059mmol)溶液混合,壳寡糖衍生物a2溶液的浓度为1.0mg/ml;混合溶液中,壳寡糖衍生物a2的浓度为0.0035mol/l,agno3的浓度为0.0045mol/l,于25℃下反应70min得纳米银b2。
实施例5:n-(2-羟乙基)-硫脲壳寡糖a3及纳米银溶液b3的合成
称取壳寡糖(8g,单元摩尔数0.05mol)缓慢加入95%乙醇(25ml)中搅拌溶解后,将溶液在搅拌状态下加入氨水(25ml,0.65mol)中,室温下搅拌0.5h;接着将cs2(3.9ml,0.065mol)溶液缓慢滴加到该混合液中搅拌反应2h;再称取氯乙酸钠(6.2g,0.053mol)缓慢加入到上述溶液中,继续搅拌反应0.5h;然后量取乙醇胺(6ml,0.10mol)缓慢加入到反应液中,室温下再反应3h;最后将反应液缓慢加入到55ml无水乙醇中,有棕色絮状沉淀析出,静置,去除上清液,用无水乙醇反复洗涤6次,抽滤,将产物真空干燥(60℃,9h),得到浅棕色粉末4.22g(单元摩尔数0.03mol)。
8ml(单元摩尔质量264,单元摩尔数0.027mmol)壳寡糖衍生物a3溶液与1.5mlagno3(10mg/ml,0.088mmol)溶液混合,壳寡糖衍生物a3溶液的浓度为0.9mg/ml;混合溶液中,壳寡糖衍生物a3的浓度为0.0028mol/l,agno3的浓度为0.0093mol/l,于40℃下反应80min得纳米银b3。
实施例6:苯氨基硫脲壳寡糖a4及纳米银溶液b4的合成
称取壳寡糖(8g,单元摩尔数0.05mol)缓慢加入95%乙醇(30ml)中搅拌溶解后,将溶液缓慢加入氨水(30ml,0.78mol)中,呈深棕色粘性液体,在室温下搅拌0.5h;接着将cs2(4ml,0.066mol)缓慢滴加到上述混合液中搅拌反应2h,溶液颜色加深;称取氯乙酸钠(6.5g,0.056mol)加入到反应液中,继续搅拌反应0.5h;再将苯肼(6ml,0.061mol)缓慢滴加到上述反应液中,室温下再反应2h;最后将反应液加入到约60ml无水乙醇中,有棕色絮状沉淀析出,静置,去除上清液,用无水乙醇反复洗涤8次,抽滤,并用无水乙醇淋洗2次,将得到的产物真空干燥(55℃,8h),得浅棕色粉末8.56g(单元摩尔数0.053mol)。
10ml(单元摩尔质量297,单元摩尔数0.032mmol)苯氨基硫脲壳寡糖a4溶液与2.0mlagno3(10mg/ml,0.12mmol)溶液混合,苯氨基硫脲壳寡糖a4溶液的浓度为0.95mg/ml;混合溶液中,苯氨基硫脲壳寡糖a4的浓度为0.0027mol/l,agno3的浓度为0.0098mol/l,于50℃下反应90min得纳米银b4。
实施例7:n-(2-吡啶)-n'-壳寡糖硫脲a5及纳米银溶液b5的合成
将2-氨基吡啶4.7g(0.05mol)溶于95%乙醇(10ml)中,加入氨水(10ml,0.26mol),溶液呈橙黄色,在室温下搅拌0.5h;在该溶液中缓慢滴加cs2(4.4ml,0.073mol),搅拌反应2h,溶液变为橙红色;接着在该反应液中加入氯乙酸钠(7g,0.06mol),继续反应0.5h,溶液变为橙黄色;称取壳寡糖(8g,单元摩尔数0.05mol)溶于95%乙醇(10ml)中,然后将其滴加到上述反应液中,并补加氨水(10ml,0.26mol),溶液呈黑褐色,室温下再反应4h;最后将反应液缓慢倒入约50ml无水乙醇中,有黄色絮状沉淀析出,静置,去除上清液,用无水乙醇反复洗涤7次,抽滤,并用无水乙醇淋洗2次,将得到的产物真空干燥(55℃,8h),得浅黄色固体粉末7.78g(单元摩尔数0.048mol)。
10ml(单元摩尔质量297,单元摩尔数0.034mmol)的n-(2-吡啶)-n'-壳寡糖硫脲a5溶液与浓度为1.0mlagno3(10mg/ml,0.059mmol)溶液混合,n-(2-吡啶)-n'-壳寡糖硫脲a5溶液的浓度为1.0mg/ml;混合溶液中,n-(2-吡啶)-n'-壳寡糖硫脲a5的浓度为0.0031mol/l,agno3的浓度为0.0053mol/l,于40℃下反应80min得纳米银b5。
实施例8:甲氨基硫脲壳寡糖a6及纳米银溶液b6的合成
称取壳寡糖(4g,单元摩尔数0.025mol)缓慢加入95%乙醇(10ml)搅拌溶解后,加入氨水(10ml,0.26mol)中,溶液呈深棕色,在室温下搅拌0.5h;接着将cs2(2.1ml,0.035mol)缓慢滴加到该混合液中,搅拌反应2h,溶液颜色加深;称取氯乙酸钠(3.4g,0.029mol)缓慢加入到上述反应液中,继续搅拌反应0.5h;然后再取甲基肼(3ml,0.057mol)滴加到反应液中,在室温下再反应3h;最后将反应液缓慢倒入到约40ml无水乙醇中,有浅灰色絮状沉淀析出,静置,去除上清液,用无水乙醇反复洗涤8次,抽滤,并用无水乙醇淋洗3次,将得到的产物真空干燥(55℃,8h),得浅灰色固体粉末3.8g(单元摩尔数0.024mol)。
10ml(单元摩尔质量249,单元摩尔数0.040mmol)甲氨基硫脲壳寡糖a6溶液与1.0mlagno3(10mg/ml,0.059mmol)溶液混合,甲氨基硫脲壳寡糖(a6)溶液的浓度为1.2mg/ml;混合溶液中,甲氨基硫脲壳寡糖a6的浓度为0.0036mol/l,agno3的浓度为0.0053mol/l,于50℃下反应100min得纳米银b6。
壳寡糖硫脲类衍生物利用一锅煮方法制得,在反应过程中小分子壳寡糖容易团聚形成大分子壳寡糖,影响反应继续进行,减少壳寡糖衍生物的产率。在试验过程中我们发现:加大氨水用量,使壳寡糖乙醇溶液与氨水混合后形成均相溶液,在电磁搅拌器中不断进行搅拌,可减少团聚现象的出现,提高壳寡糖衍生物的产率。
1.壳寡糖衍生物的紫外表征
1.1二硫代氨基甲酸脱乙酰壳寡糖铵紫外-可见吸收光谱
如图1所示,二硫代氨基甲酸脱乙酰壳寡糖铵的紫外光谱扫描曲线与壳寡糖原料的紫外扫描曲线完全不同,这是由于壳寡糖与氨水与二硫化碳发生了加成反应后的紫外吸收峰与原料壳寡糖相比有了改变。这进一步证实了该化学反应已经发生,有铵硫代氨基硫脲壳寡糖生成。
从图1可以看出:壳寡糖在277nm处有个弱而宽的吸收峰,在大于277nm波长范围无明显吸收。铵硫代氨基硫脲壳寡糖在205nm的吸收是-css-的吸收峰、在256nm、288nm处的吸收峰,是受壳寡糖影响发生红移的硫脲结构吸收峰,说明有铵代氨基硫脲结构存在。反应得到了目标产物。
1.2实施例6制备的苯氨基硫脲壳寡糖紫外吸收光谱如图2所示,苯氨基硫脲壳寡糖紫外吸收光谱与壳寡糖、铵硫代氨基硫脲壳寡糖紫外吸收光谱相比,有着明显的不同,说明三者结构有着本质的不同,有反应发生生。苯氨基硫脲壳寡糖在276nm处有较强吸收,是苯环b带,由苯环共轭双键在270nm处的吸收,并且在-hn-nh-作用下红移,说明有苯氨基结构存在,苯肼已经加成到铵硫代氨基硫脲上,得到目标产物。
1.3实施例7制备的n-(2-吡啶)-n'-壳寡糖硫脲(a5)紫外-可见吸收光谱如图3所示,n-(2-吡啶)-n'-壳寡糖硫脲(a5)在254nm、289nm处有吸收峰,与铵硫代氨基硫脲205nm、256nm、288nm吸收峰相比,205nm处吸收峰消失是因为-css-结构被破环,有取代反应发生。吡啶的吸收峰带有两条:一条在240~260nm相应于π→π*跃迁;另一条在270nm的区域,相应于n→π*跃迁。吡啶的存在使铵硫代氨基硫脲壳寡糖256nm与288nm两个吸收峰分别发生蓝移和红移。
1.4实施例8制备的甲氨基硫脲壳寡糖(a6)紫外吸收光谱如图4所示,铵硫代氨基硫脲壳寡糖与甲氨基硫脲壳寡糖并无明显区别,前者在256nm、288nm处有明显吸收峰,为硫脲结构吸收峰,后者的吸收峰位置为254nm、286nm,是因为甲基的存在使吸收发生了蓝移。甲氨基硫脲壳寡糖破坏了-css-键所以205nm处的紫外吸收峰消失。
2.壳寡糖硫脲类衍生物的红外表征
2.1实施例6制备的苯氨基硫脲壳寡糖(a4)红外吸收光谱如图5所示,3425.43cm-1、3329.91cm-1、3133.99cm-1是变成缔合的-oh伸缩振动吸收峰-nh的伸缩振动吸收峰重叠而增宽的多重吸收峰,在1083cm-1处的则是醇羟基的变角振动吸收峰,在852cm-1处存在β-型糖苷键的特征吸收峰,说明壳聚糖为β-多糖。苯氨基硫脲壳寡糖在1450cm-1和1600cm-1附近出现了苯环的骨架振动,700cm-1处的是苯环单取代的特征峰。说明经过一系列反应,目标产物正确。
2.2实施例7制备的n-(2-吡啶)-n'-壳寡糖硫脲(a5)红外吸收光谱如图6所示,3170cm-1、3324cm-1、3418cm-1是变成缔合的-oh伸缩振动吸收峰-nh的伸缩振动吸收峰的多重吸收峰,在1073cm-1处的则是醇羟基的变角振动吸收峰,1616cm-1为氨基变形振动吸收峰,896cm-1处存在β-型糖苷键的特征吸收峰,1664、1241、1204、1154、是吡啶环的红外特征吸收峰。反应生成目标产物。
2.3实施例8制备的甲氨基硫脲壳寡糖(a6)红外吸收光谱如图7所示,3133cm-1是变成缔合的-oh伸缩振动吸收峰-nh的伸缩振动吸收峰重叠而增宽吸收峰,在1082cm-1处的则是醇羟基的变角振动吸收峰,1593cm-1为氨基变形振动吸收峰,在831cm-1处存在β-型糖苷键的特征吸收峰,说明壳聚糖为β-多糖,1401cm-1强吸收峰是ch弯(面内)的特征峰,相比壳寡糖吸收更强。反应生成目标产物。
3.壳寡糖及壳寡糖衍生物制备纳米银的结构表征
3.1氨基硫脲壳寡糖(a1)制备纳米银(b1)过程的紫外-可见吸收光谱
在20℃下,将1.5ml10mg/ml的硝酸银溶液加入到10ml0.8mg/ml(单元摩尔浓度0.005mol/l)的氨基硫脲壳寡糖(a1)溶液中,图8为扫描各时间点的紫外吸收曲线,反应过程中的颜色变化如图9所示。
3.2苯氨基硫脲壳寡糖(a4)制备纳米银(b4)过程的紫外-可见吸收光谱
在20℃下,将1.5ml10mg/ml的硝酸银溶液加入到10ml0.95mg/ml(单元摩尔浓度0.0059mol/l)的苯氨基硫脲壳寡糖(均相)溶液中,图10不同浓度苯氨基硫脲壳寡糖(a4);1:0.001mol/l;2:0.002mol/l;3:0.003mol/l;4:0.004mol/l;5:0.005mol/l)还原制备银纳米粒子(b4)的uv-vis吸收光谱,图11为不同浓度苯氨基硫脲壳寡糖(a4)制备纳米银(b4)的颜色比较。
3.3n-(2-吡啶)-n'-壳寡糖硫脲(a5)制备纳米银过程的紫外-可见吸收光谱
在20℃下,将1.5ml10mg/ml的硝酸银溶液加入到10ml1mg/ml的n-(2-吡啶)-n'-壳寡糖硫脲溶液中,图12为扫描各时间点的紫外吸收曲线,反应过程的中的颜色变化如图13所示。
3.4甲氨基硫脲壳寡糖(a6)制备纳米银过程的紫外-可见吸收光谱
在20℃下,将1.5ml10mg/ml的硝酸银溶液加入到10ml1mg/ml的甲氨基硫脲壳寡糖溶液中,图14为扫描各时间点的紫外吸收曲线,反应过程的中的颜色变化如图15所示。
4.壳寡糖硫脲类衍生物还原制备纳米银的透射电子显微镜(tem)结果
实验采用feitecnalg2型透射电子显微镜(荷兰fei公司)对材料的形貌进行表征,加速电压为200kv。取0.2ml的纳米银溶液滴加于覆有碳膜的铜网网格上,然后将铜网置于红外灯下干燥30min,待溶剂挥发后用透射电镜观察纳米银粒子的形貌。
如图16、图18所示,壳寡糖-水合肼硫脲衍生物(a1)制备的纳米银(b1)粒径在10nm左右,苯氨基硫脲壳寡糖(a4)制备的纳米银(b1)纳米粒子粒径约为4-10nm,分布比较均匀,在410nm左右能测出紫外吸收峰(见图8、10),壳寡糖-乙二胺硫脲衍生物(a2)制备纳米银(b2)时溶液颜色发生明显变化,溶液为血红色,但在410nm左右未能测出紫外吸收峰,却在透射电子显微镜下能看到分布均匀的球形纳米颗粒,可能是纳米粒径太小,由于所用还原剂的不同,得到的纳米银粒子呈现不同的分布。
图17所示n-(2-氨乙基)-n'-壳寡糖硫脲(a2)还原制备纳米银(b2),图19所示n-(2-吡啶)-n'-脲壳寡糖硫脲(a5)做还原剂制备纳米银(b5)及图20所示甲氨基硫脲壳寡糖(a6)做还原剂制备纳米银(b6)的电镜扫描结果显示在电子扫描电镜下有明显的纳米粒子存在,有纳米银生成,纳米粒子粒径约为4-10nm,分布比较均匀。但n-(2-氨乙基)-n'-壳寡糖硫脲、甲氨基硫脲壳寡糖还原制备纳米银的紫外-可见扫描光谱上在410nm处没有吸收峰(见图12、14)。
5.壳寡糖硫脲类衍生物制备的纳米银抑菌活性的探究
5.1氨基硫脲壳寡糖a1制备的纳米银b1抑菌活性的探究
5.1.1实验原理
采用抑制菌丝生长速率法,探究氨基硫脲壳寡糖(a1)制备的纳米银b1对小麦茎基腐病菌、烟草黑胫病菌、玉米青枯病菌、串珠病菌、番茄早疫病菌、玉米弯孢病菌、禾谷镰刀病菌的抑制活性,以水、壳寡糖、市售药三唑酮作为对照来对比其抗真菌活性的效果。计算公式:
5.1.2实验步骤
实验前一天灭菌:培养皿用报纸包好(十个一摞)、准备一个锥形瓶(里边加200ml纯净水)用牛皮纸封好、包好的试管,放于高压灭菌锅内灭菌2h。灭菌完毕后放于烘箱中烘干备用。培养基配制:1000ml水对应200g土豆,18g琼脂,20g葡萄糖。按比例配制。具体操作,把称好的土豆切成片,放入沸腾的水中煮到一定程度(用玻璃棒能把土豆扎透就可以了),把水滤到烧杯中,土豆扔掉。继续把滤液倒入锅中煮,先加入葡萄糖,搅拌,再缓慢加入琼脂,并不断搅拌,待琼脂全部溶解后倒入烧杯中(体积不够最初要求再加适量热水)。然后倒入锥形瓶中用牛皮纸封口,在高压灭菌锅中灭菌(同时灭菌的有镊子、打孔器、接种针、枪头等)。药品配制。倒皿:进入无菌操作台,用酒精棉擦手,培养皿编号,编号完毕后开始倒培养基,从高压锅中取一锥形瓶,用移液枪从小药瓶中取定量的药品,摇匀,将培养液先到入10ml的试管中,再将试管中的培养液倒入对应药品名称的培养皿中,得到不同浓度的培养基,同种药品倒三个皿,重复操作。接种:倒完培养基后在紫外灯下灭菌并冷却0.5h,待培养基冷却凝固后,然后接种,封口。菌种培养:在智能生化培养箱里恒温培养数天。测量:运用十字交叉法测量菌种直径记录数据并拍照。数据整理。
注:以上所有操作需在无菌操作台进行无菌操作,动作要迅速,以免染菌。
5.1.3氨基硫脲壳寡糖a1制备的纳米银b1的抑菌试验结果与分析
5.1.3.1氨基硫脲壳寡糖(a1)制备的纳米银b1对小麦茎基腐病菌的抑制活性
表1氨基硫脲壳寡糖(a1)制备的纳米银(b1)对小麦茎基腐病菌的抑制活性
由表1可知:纳米银对小麦茎基腐的抑菌效果较好,低浓度(10μg/ml)纳米银就已经表现出了抑菌性,且抑菌率与纳米银浓度呈正相关,随浓度的增大而增大,相关系数达到0.9984,相关性较强。当纳米银浓度为60μg/ml时,抑菌率达到65.29%,但是还是不如相三唑酮(50μg/ml)时的抑菌效果(88.97%)好。纳米银对小麦茎基腐病菌的ec50值(μg/ml)为42.2364,抑菌效果较好。
5.1.3.2氨基硫脲壳寡糖(a1)制备的纳米银(b1)对烟草黑胫病菌的抑制活性
表2氨基硫脲壳寡糖(a1)制备的纳米银(b1)对烟草黑胫病菌的抑制活性
由表2可知:纳米银对烟草黑胫的抑菌效果一般,抑菌率与纳米银浓度呈正相关,随浓度的增大而增大,相关系数达到0.9984,相关性较强。当纳米银浓度为60μg/ml时,抑菌率只有达到46.55%,低于三唑酮(50μg/ml)的抑菌效果(80.31%)好。纳米银对烟草黑胫病菌的ec50值(μg/ml)为60.7501。
5.1.3.3氨基硫脲壳寡糖(a1)制备的纳米银(b1)对玉米青枯病菌的抑制活性
表3氨基硫脲壳寡糖(a1)制备的纳米银(b1)对玉米青枯病菌的抑制效果
由表3可知:纳米银对玉米青枯的抑菌效果较好,抑菌率与纳米银浓度呈正相关,随浓度的增大而增大,相关系数达到0.9847,相关性较强。当纳米银浓度为60μg/ml时,抑菌率达到56.01%,低于三唑酮(50μg/ml)抑菌效果(89.89%)。纳米银对玉米青枯病菌的ec50值(μg/ml)为14.7149。
5.1.3.4氨基硫脲壳寡糖(a1)制备的纳米银(b1)对串珠病菌的抑制活性
表4氨基硫脲壳寡糖(a1)制备的纳米银(b1)对串珠病菌的抑制活性
由表4可知:纳米银对串珠的抑菌效果较好,抑菌率与纳米银浓度呈正相关,随浓度的增大而增大,相关系数为0.9847。当纳米银浓度为60μg/ml时,抑菌率达到53.61%,低于三唑酮(50μg/ml)的抑菌率(85.28%)。纳米银对串珠病菌的ec50值(μg/ml)为51.1072。
5.1.3.5氨基硫脲壳寡糖(a1)制备的纳米银(b1)对番茄早疫病菌的抑制活性
表5氨基硫脲壳寡糖(a1)制备的纳米银(b1)对番茄早疫病菌的抑制活性
由表5可知:纳米银对番茄早疫的抑菌效果很好,抑菌率与纳米银浓度呈正相关,随浓度的增大而增大,相关系数为0.9720。当纳米银浓度为60μg/ml时,抑菌率达到67.31%,低于三唑酮(50μg/ml)时的抑菌率(91.76%)。纳米银对串珠病菌抑制的ec50值(μg/ml)为21.2889。
5.1.3.6氨基硫脲壳寡糖(a1)制备的纳米银(b1)对玉米弯孢病菌的抑制活性
表6氨基硫脲壳寡糖(a1)制备的纳米银(b1)对玉米弯孢病菌的抑制活性
由表6可知:纳米银对玉米弯孢菌的抑菌效果最好,低浓度(10μg/ml)的纳米银就表现出来较为优势的抑菌率(19.83%),且抑菌率与纳米银浓度呈正相关,随浓度的增大而增大,相关系数为0.9880。当纳米银浓度为60μg/ml时,抑菌率达到95.69%,抑菌效果和三唑酮(50μg/ml)时的抑菌效果相同,但纳米银相对于三唑酮有着污染小,绿色等优点,纳米银对玉米弯孢菌的ec50值为54.3393μg/ml。
5.1.3.7氨基硫脲壳寡糖(a1)制备的纳米银(b1)对禾谷镰刀病菌的抑制活性
表7氨基硫脲壳寡糖(a1)制备的纳米银(b1)对禾谷镰刀病菌的抑制活性
由表7可知:纳米银对禾谷镰刀的抑菌效果较好,低浓度(10μg/ml)的纳米银就表现出较好的抑菌率(5.43%),抑菌率与纳米银浓度呈正相关,随浓度的增大而增大,相关系数为0.9450。当纳米银浓度为60μg/ml时,抑菌率为78.22%,高于三唑酮(50μg/ml)的抑菌率(73.64%),纳米银对串珠病菌的ec50值为32.4018μg/ml。
通过对壳寡糖-水合肼硫脲衍生物a1以及以此为还原剂和稳定剂制备的纳米银溶液对六种常见植物治病真菌进行了抗菌活性的探究,可初步得出结论,与对照壳寡糖相比壳寡糖硫脲类衍生物及其制备的纳米银溶液对真菌的抑制率增强,合成的壳寡糖-水合肼硫脲衍生物a1对不同的菌种都有一定的抗菌性,对不同菌种的抗菌性也有所不同,并随着溶液中药品本身的浓度增大而增大。而其还原硝酸银得到的纳米银溶液的抗菌活性比相应的壳寡糖硫脲类衍生物本身的抗菌活性要高,其中对小麦致病菌具有更强的抗菌性,如对小麦赤霉抑菌率达48.02%,对小麦茎基腐抑菌率达55.6%。对于玉米小斑菌来说,纳米银的抗菌活性比市场卖的抗菌剂三唑酮高15%左右,随着纳米银溶液的浓度减小,抗菌性减小。均相合成的药品普遍比非均相合成的抗菌性高,说明取代度对抗菌性的提高起重要作用。
5.2苯氨基硫脲壳寡糖a4及以此为还原剂和稳定剂制备的纳米银b4抑菌活性的探究
5.2.1实验原理
采用抑制菌丝生长速率法,探究苯氨基硫脲壳寡糖a4本身、以此为还原剂制备的纳米银b4对禾谷镰刀病菌,小麦赤霉菌,小麦茎基腐病菌,棉花枯萎病菌,玉米小斑病菌,烟草黑胫病菌的抑制活性,以水、壳寡糖、市售药三唑酮作为对照来对比其抗真菌活性的效果。计算公式:
5.2.2实验步骤
5.2.2.1培养基
pda培养基:马铃薯300g,葡萄糖30g,琼脂27g,蒸馏水1500ml。
步骤:(1).将马铃薯切成厚度1-2cm的薄片,用沸腾的蒸馏水煮10-15min;(2).将马铃薯滤去,留下滤液,并加至1500ml;(3).继续加热,加入葡萄糖;(4).缓慢加入琼脂粉;(5).高压灭菌120min。
5.2.2.2供试真菌
禾谷镰刀病菌,小麦赤霉菌,小麦茎基腐病菌,棉花枯萎病菌,玉米小斑病菌,烟草黑胫病菌,所有菌种均为本实验室保存。
5.2.2.3实验方法
抑制菌丝生长速率法:分别取样品组和对照组溶液2ml与18ml融化的pda培养基混匀,均匀倒入两个无菌培养皿中制成带药培养基平板,同时是各个溶液第二次稀释十倍,以加入无菌水的pda培养基为生长对照。接种供试真菌菌饼,封口膜密封,28℃恒温箱中培养4-5天后,用十字交叉法测量供试菌菌落直径,每处理重复3次。按下式计算菌丝生长抑制率:菌丝生长抑制率/%=(对照菌落生长直径-处理菌落生长直径)/对照菌落生长直径×100%。
5.2.3苯氨基硫脲壳寡糖a4及以此为还原剂和稳定剂制备的纳米银b4的抑菌试验结果与分析
5.2.3.1对禾谷镰刀菌种的抑制活性
表8苯氨基硫脲壳寡糖a4及其制备的纳米银b4对禾谷镰刀菌的抑菌活性
由表8可以得出:以小麦赤霉为菌种时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液浓度为130μg/ml时抑菌率(78.86%)最高,高于三唑酮(400ug/ml)的抑菌率(65.04%),纳米银溶液抑菌率与其浓度呈正相关。
5.2.3.2对小麦赤霉菌抑菌活性
表9苯氨基硫脲壳寡糖a4及其制备的纳米银b4对小麦赤霉菌抑菌活性
由表9可以得出:以小麦赤霉为菌种时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液的浓度为130μg/ml时抑菌率最高(87.30%),高于三唑酮(400ug/ml)的抑菌率(79.37%)抑菌率与其浓度呈正相关。
5.2.3.3对小麦茎基腐菌的抑菌活性
表10苯氨基硫脲壳寡糖a4及其制备的纳米银b4对小麦茎基腐菌的抑菌活性
由表10可以得出:以小麦茎基腐为菌种时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液浓度为130μg/ml时抑菌率最高(78.40%),高于三唑酮(400ug/ml)的抑菌率(69.60%),纳米银溶液抑菌率与其浓度呈正相关。
5.2.3.4对棉花枯萎菌的抑制活性
表11苯氨基硫脲壳寡糖a4及其制备的纳米银b4对棉花枯萎菌的抑菌活性
由表11可以得出:以棉花枯萎为菌种时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液浓度为130μg/ml的抑菌率(55.47%),低于三唑酮(400ug/ml)的抑菌率(69.53%),纳米银溶液抑菌率与其浓度呈正相关。
5.2.3.5对玉米小斑菌的抑制活性
表12苯氨基硫脲壳寡糖(a4)及其制备的纳米银(b4)对玉米小斑菌的抑菌活性
由表12可以得出:以玉米小斑为菌种时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液浓度为130μg/ml时抑菌率(63.27%)最高,高于三唑酮(400ug/ml)的抑菌率(29.20%),纳米银抑菌率与其浓度呈正相关。
5.2.3.6对烟草黑胫菌的抑制活性
表13苯氨基硫脲壳寡糖a4及其制备的纳米银b4对烟草黑胫菌的抑菌活性
由表13可以得出:以烟草黑胫为菌种时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液浓度为130μg/ml时抑菌率(35.66%)最高,低于三唑酮(400ug/ml)的抑菌率(66.67%),纳米银的抑菌率与其浓度呈正相关。
活性实验中看出壳寡糖及其简单衍生物具有一定的抑菌性,但由苯氨基硫脲壳寡糖还原成的纳米银具有较强的广谱抑菌性:菌种为禾谷镰刀菌时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液(130μg/ml)的抑菌率(78.86%)最高,高于三唑酮(400ug/ml)的抑菌率(65.04%);菌种为小麦赤霉菌种时苯氨基硫脲壳寡糖还原制备的纳米银溶液(130μg/ml)的抑菌率(87.30%)最高,高于三唑酮(400ug/ml)的抑菌率(79.37%);菌种为小麦茎基腐菌时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液(130μg/ml)的抑菌率最高(73.2%),高于三唑酮(400ug/ml)的抑菌率(69.60%);以棉花枯萎为菌种时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液(130μg/ml)的抑菌率(55.47%),低于三唑酮(400ug/ml)的抑菌率(69.53%);以玉米小斑为菌种时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液(130μg/ml)抑菌率(63.27%)最高,高于三唑酮(400ug/ml)的抑菌率(29.20%);以烟草黑胫为菌种时,由苯氨基硫脲壳寡糖还原制备的纳米银溶液(130μg/ml)抑菌率(35.66%)最高,低于三唑酮(400ug/ml)的抑菌率(66.67%)。
以上所述的仅是本发明的优选实施方式,应当指出,对于本领域的技术人员来说,在不脱离本发明整体构思前提下,还可以作出若干改变和改进,这些也应该视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!