一种线性pH梯度缓冲液及其应用的制作方法
本发明涉及一种线性ph梯度缓冲液及其应用,属于缓冲试剂技术领域。
背景技术
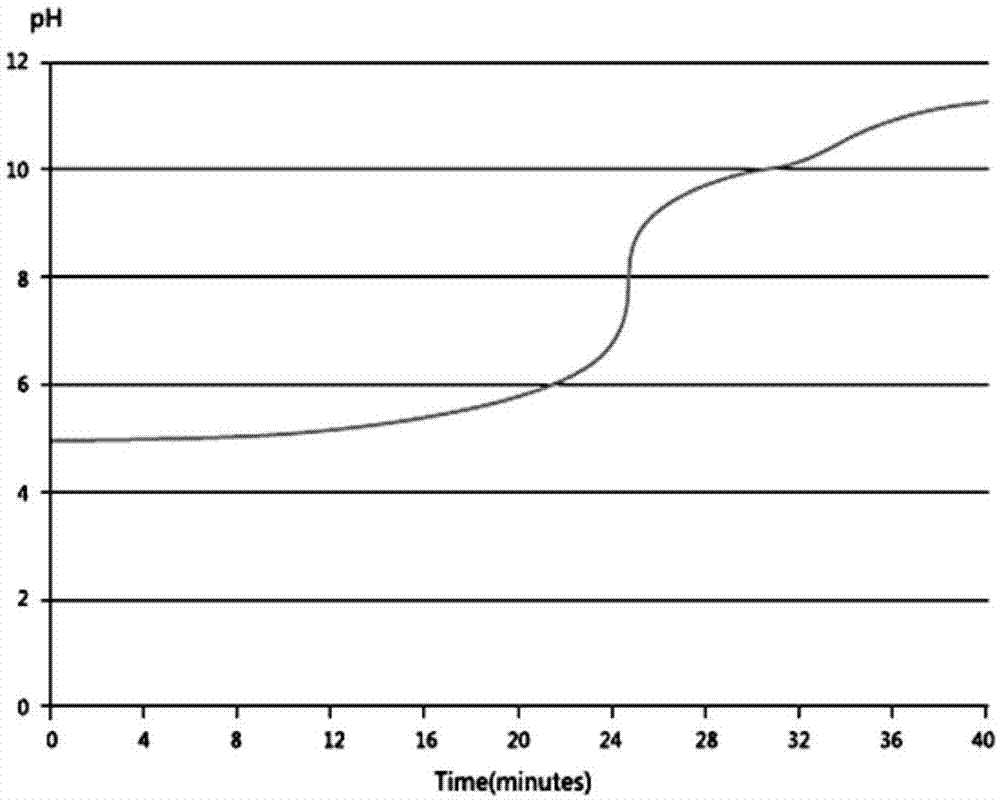
生物制药(包括以蛋白为基础的治疗药物和单克隆抗体mabs)下游的提纯,例如蛋白的分离纯化,目前普遍采用离子交换层析法(iec),以盐缓冲溶液作为流动相来使药用蛋白质从潜在的污染物中分离:根据蛋白质的电荷,选取亲和填料(介质),以盐缓冲溶液作为流动相进行离子交换,这样的下游层析方法是现在行业的主流工艺。但是,由于进行蛋白分离特别是单克隆抗体蛋白分离纯化中,亲和填料普遍使用美国generalelectric公司生产的亲和填料,亲和填料纯化原理主要是根据蛋白与配基之间的特异性结合的原理,将能与蛋白特异性结合的配基交联到填料上,就可以纯化特定的蛋白,亲和填料由于选择单一,因此成本较高。并且,普通的酸碱溶液混合为在弱酸性溶液中加入弱碱,ph值从5到8.5会发生跳变,只会得到一个s形曲线,如图1所示。ph值的突然急剧上升,经常导致蛋白质和与之密切相关的电荷相近的杂质同时在iec柱上洗脫出来,无法达到以分离为目的的生产和质量检测。同时,采用盐分离出的目标蛋白质需要除去大量的来自盐缓冲溶液中的盐成分,才能再进行下一道工序,浪费时间也增加生产成本。
技术实现要素:
为了克服现有技术的不足,本发明的第一个目的在于提供一种线性ph梯度缓冲液,第一缓冲液和第二缓冲液混合时,可以得到ph呈线性梯度变化的缓冲液,并且该溶液含有的盐远远少于盐缓冲溶液,在生产应用的时候,可以省去除盐的步骤,节约成本。
本发明的第二个目的在于提供上述线性ph梯度缓冲液的应用,可应用于离子交换层析法中作为洗脱液。
实现本发明的第一个目的可以通过采取如下技术方案达到:一种线性ph梯度缓冲液,包括第一缓冲液和第二缓冲液;第一缓冲液为ph≤3的缓冲液,其包括负一价的酸根离子;第二缓冲液为ph≥8的缓冲液,其包括负二价的酸根离子、负三价的酸根离子和正一价的阳离子。
进一步地,负一价的酸根离子为h2po4-(磷酸二氢根离子)。
进一步地,负二价的酸根离子为hpo42-(磷酸氢根离子);负三价的酸根离子为c5h5o5coo3-(负三价柠檬酸根离子);正一价阳离子为na+。
进一步地,第一缓冲液包括磷酸和柠檬酸;磷酸和柠檬酸的摩尔之比为1:(0.5-3)。
进一步地,磷酸和柠檬酸的摩尔之比为1:(1-2)。
进一步地,第二缓冲液包括磷酸氢二钠和柠檬酸三钠;磷酸氢二钠和柠檬酸三钠的摩尔之比为4:(3-5)。
进一步地,磷酸氢二钠和柠檬酸三钠的摩尔之比为4:(3-4)。
进一步地,第一缓冲液包括磷酸二氢钠和柠檬酸;磷酸二氢钠和柠檬酸的摩尔之比为(1-3):2。
进一步地,磷酸二氢钠和柠檬酸的摩尔之比为(1-2):2。
进一步地,第二缓冲液包括磷酸氢二钠和柠檬酸三钠;磷酸氢二钠和柠檬酸三钠的摩尔之比为(1-4):2。
进一步地,磷酸氢二钠和柠檬酸三钠的摩尔之比为(2-4):2。
实现本发明的第二个目的可以通过采取如下技术方案达到:一种如上所述的线性ph梯度缓冲液的应用,进行蛋白分离纯化时,以第一缓冲液和第二缓冲液的混合液作为洗脱溶液。
进一步地,将第一缓冲液和第二缓冲液分别装载于两个输液器中;洗脱时,第一缓冲液和第二缓冲液分别从各自的输液器中流出,第一缓冲液流量逐渐减少,第二缓冲液的流量逐渐增加,而第一缓冲液和第二缓冲液的总流量始终恒定不变,在限定时间内,第一缓冲液流量减至0。
进一步地,第一缓冲液和第二缓冲液的总流量为0.5-9.9ml/min或1-6l/min。
本发明的线性ph梯度缓冲液配方设计原理如下:
第一缓冲液和第二缓冲液进行混合时,混合液产生线性的ph值的梯度变化,根据目标蛋白质和杂质具有不同的pi(等电点),使蛋白和杂质分离,完成提纯过程。
相比现有技术,本发明的有益效果在于:
1、本发明线性ph梯度缓冲液可以实现稳定的线性ph变化,适用于蛋白的分离纯化,克服了常规盐缓冲溶液ph不稳定而使得杂质不易分离的缺陷;
2、本发明线性ph梯度缓冲液的稳定线性ph变化范围广,适用于不同的蛋白分离过程;
3、本发明线性ph梯度缓冲液作为蛋白分离纯化的洗脱溶液,含有的盐远远少于盐缓冲溶液,在生产应用的时候,可以省去除盐的步骤,节约成本;
4、本发明线性ph梯度缓冲液应用于蛋白单克隆分离纯化中,不需使用亲和填料,可以大大降低成本。
附图说明
图1为常规的酸碱溶液混合时的ph变化图示;
图2-3为组合一使用时的ph线性梯度变化示意图;
图4-5为组合二使用时的ph线性梯度变化示意图;
图6为实施例1的层析法分离示意图;
图7为实施例2的层析法分离示意图。
具体实施方式
下面,结合附图以及具体实施方式,对本发明做进一步描述:
一种线性ph梯度缓冲液,包括第一缓冲液和第二缓冲液;第一缓冲液为ph≤3的缓冲液,其包括负一价的酸根离子;第二缓冲液为ph≥8的缓冲液,其包括负二价的酸根离子、负三价的酸根离子和正一价的阳离子。
其中,第一缓冲液中的负一价的酸根离子为h2po4-(磷酸二氢根离子),可以通过添加磷酸或者磷酸二氢钠,使得第一缓冲液中含有h2po4-。
其中,第二缓冲液中的负二价的酸根离子为hpo42-(磷酸氢根离子),负三价的酸根离子为c5h5o5coo3-(负三价柠檬酸根离子),正一价阳离子为na+,可以通过添加磷酸氢二钠和柠檬酸三钠,使得第二缓冲液中含有hpo42-、c5h5o5coo3-和na+。
线性ph梯度缓冲液有两种组合:
组合一:
第一缓冲液包括磷酸和柠檬酸;磷酸的摩尔浓度为20mm,柠檬酸的摩尔浓度为20-40mm;
第二缓冲液包括磷酸氢二钠和柠檬酸三钠;磷酸氢二钠的摩尔浓度为40mm;柠檬酸三钠的摩尔浓度为30-40mm;
组合一中第一缓冲液和第二缓冲液混合可以得到ph在4-8.5范围内的线性梯度变化的缓冲液。
组合二:
第一缓冲液包括磷酸二氢钠和柠檬酸;磷酸二氢钠的摩尔浓度为15-30mm;柠檬酸的摩尔浓度为30mm;
第二缓冲液包括磷酸氢二钠和柠檬酸三钠;磷酸氢二钠的摩尔浓度为15-30mm;柠檬酸三钠的摩尔浓度为15mm;
组合二中第一缓冲液和第二缓冲液混合可以得到ph在3-7范围内的线性梯度变化的缓冲液。
线性ph梯度缓冲液的应用方式:以离子交换层析法(iec)进行蛋白分离纯化时,以第一缓冲液和第二缓冲液的混合液作为洗脱溶液。
将第一缓冲液和第二缓冲液分别装载于液相色谱分析仪的两个输液泵中;洗脱时,第一缓冲液和第二缓冲液分别从各自的输液泵中泵出,第一缓冲液流量逐渐减少至0,第二缓冲液的流量从0逐渐增加,而第一缓冲液和第二缓冲液的总流量始终恒定不变,在限定时间内,第一缓冲液流量减至0。
第一缓冲液和第二缓冲液的总流量为0.5-9.9ml/min,该总流量为实验室使用的流量;或者1-6l/min,该总流量可以进行工业化生产。
如图2-3所示为组合一应用时的ph梯度变化示意图,图2为总流量0.5ml/min,geaktapure蛋白质分离纯化系统,图3为总流量3l/min,中试设备(supremepharmaceuticaltechnologypilot-scaleequipment),图3中横轴为时间,约30min。
如图2所示,ph在4-8.5范围内成稳定的线性梯度变化,如图3所示,ph在4-7.8范围内成稳定的线性梯度变化。
如图4-5所示为组合二应用时的ph梯度变化示意图,图4为总流量0.5ml/min,geaktapure蛋白质分离纯化系统;图5为总流量3l/min,中试设备(supremepharmaceuticaltechnologypilot-scaleequipment),图5中横轴为时间,约25min。
如图4和5所示,ph在3-7范围内成稳定的线性梯度变化。
实施例1:
单克隆抗体提纯试验:
填料:nanosp15l阳离子填料;
试剂:组合一的线性ph4-8.5梯度缓冲液:
第一缓冲液:磷酸和柠檬酸组成;磷酸的摩尔浓度为20mm;柠檬酸的摩尔浓度为40mm;
第二缓冲液:磷酸氢二钠和柠檬酸三钠组成;磷酸氢二钠的摩尔浓度为40mm;柠檬酸三钠的摩尔浓度为40mm;
将第一缓冲液和第二缓冲液分别装载于液相色谱分析仪的两个输液泵中;洗脱时,第一缓冲液和第二缓冲液分别从各自的输液泵中泵出,第一缓冲液流量从1ml/min逐渐减少至0,第二缓冲液的流量从0逐渐增加至1ml/min,而第一缓冲液和第二缓冲液的总流量始终恒定不变,第一缓冲液流量减至0。如图6所示,ph梯度缓冲液呈现ph为4-8.5的线性变化。
柱子:pp7.7×100mm(4.65ml)
流速:1ml/min
程序
平衡:3cv1cv=4.65ml
上样:8mlmabigg1(4.5mg/ml单抗液稀释5倍)
洗脱:30-100%b,10cv;(30%bph=4.27)
结果如图6所示,线性ph梯度配合阳离子填料,50.33min时可从单抗原液中提取单抗。
实施例2:
单抗igg二次纯化试验:
填料:nanogel50sp,0.66×29cm;
试剂:组合一的线性ph梯度缓冲液:
第一缓冲液:磷酸和柠檬酸组成;磷酸的摩尔浓度为20mm;柠檬酸的摩尔浓度为40mm;
第二缓冲液:磷酸氢二钠和柠檬酸三钠组成;磷酸氢二钠的摩尔浓度为40mm;柠檬酸三钠的摩尔浓度为40mm;
将第一缓冲液和第二缓冲液分别装载于液相色谱分析仪的两个输液泵中;洗脱时,第一缓冲液和第二缓冲液分别从各自的输液泵中泵出,第一缓冲液流量从1.9ml/min逐渐减少至0,第二缓冲液的流量从0逐渐增加至1.9ml/min,而第一缓冲液和第二缓冲液的总流量始终恒定不变,第一缓冲液流量减至0。如图7所示,ph梯度缓冲液呈现ph为4.5-8.5(图中为第一缓冲液占总流量体积的30%时的图示,因此图上ph显示为4.5起始,完整的ph线性范围为4-8.5)的线性变化。
上样:igg1.44mg/ml,5ml,稀释到55ml,进样40ml
系统最大压力0.6mpa
总流速1.9ml/min,1cv=9.8ml,5mins
平衡5cv,30%b
冲洗3cv,30%b
洗脱20cv,30-100%b
延时5cv,100%b。
结果如图7所示,线性ph梯度配合阳离子填料,144min时可从单抗原液中提取单抗。
对于本领域的技术人员来说,可根据以上描述的技术方案以及构思,做出其它各种相应的改变以及变形,而所有的这些改变以及变形都应该属于本发明权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!