CLIP3基因的SNP位点的应用的制作方法
本发明涉及生物医学领检测技术领域,具体涉及与主动脉夹层疾病相关的clip3基因的snp位点的应用。
背景技术
主动脉夹层(aorticdissection,ad)系指主动脉在一系列外在因素作用下(如高血压、外伤等因素),基于主动脉壁本身存在或不存在病变,主动脉内膜出现破口,血液自主动脉内膜破口侵入主动脉壁的中层,主动脉中层不断撕裂、纵向分离,导致呈现出一种主动脉管腔真假两腔并存的状态。主动脉夹层起病急骤,发展迅速,预后凶险。尽管目前的各种治疗手段不断改进,但是ad的发病率和死亡率依然居高不下,并且如果不进行恰当和及时的治疗,ad死亡率极高。有报道称约有近20%的ad患者在到达医院之前死亡,而30%的患者在住院治疗期间死亡。目前临床上对ad缺乏有效的药物干预手段,主要采用外科手术进行血管置换、介入手术进行主动脉腔内支架植入以及两者结合应用,但是手术风险大,费用高,并且远期的复发率和再手术率仍然较高。伴随着影像学技术及医疗设备条件的进步,ad疾病检出率呈上升趋势,对于ad的发生及发病机制的研究也在不断深入。ad生成机制与遗传学密切相关。ad相关易感基因是目前ad遗传学研究热点,从基因角度分析与ad相关的易感基因很有意义。
伴随着人类基因组测序计划完成和高通量测序技术的发展,医学领域的科研工作者对人类基因组有了更深入的认识,对疾病相关遗传变异、相关基因的功能及调控网络的认识也逐渐加深,高通量测序得到广泛应用。全外显子组测序(wholeexomesequencing,wes)技术是利用外显子捕获试剂盒捕捉整个外显子区域dna,然后进行高通量测序,是目前基因组学研究中非常成熟的一部分。近两年来,采用wes技术研究复杂疾病的文献报道开始出现,展现出该技术的巨大优势。ziganshinba等学者对102例胸主动脉瘤和ad患者进行wes分析,发现21.6%患者存在1个或多个其它基因的突变,3.9%患者存在fbn1、col5a1、mylk、flna基因的有害突变。janicel.farlow等对45位颅内动脉瘤患者进行了wes,发现68个基因存在变异,tmem132b基因的表达在患者和对照者中显著不同(44vs16)。表明在常见复杂疾病中可通过高通量测序鉴别罕见变异。并且,有越来越多的证据表明稀有变异对常见疾病易患性有中到强度的效应影响,可解释很大部分的遗传缺失。罕见突变(maf<1%或5%)的局限性,而且费用、时间成本均较高。全基因组关联分析(genomewideassociationstudies,gwas)只能识别常见变异(commonvariants,cv:maf>5%),忽略了某些未知的与ad发病相关的功能候选基因。wes相较于全基因组测序(wholegenomesequencing,wgs)、gwas具有对基因组编码区域的高深度测序,除大片段的缺失重复及snp外,还能发现低频突变、罕见突变,识别范围更广,具有低成本、高效率的优势,是寻找疾病易感基因或位点特别是发现新易感基因或位点最常用的方法之一,可弥补gwas不能筛选未知候选基因的缺陷。
ad血管风险高,不容易早期发现,基于已知致病基因的遗传学诊断阳性率有限,难于做早期风险评估,亟待发现新的分子标志物。
技术实现要素:
为了解决上述问题,本发明的目的在于提供一种基于全外显子测序技术筛选与主动脉夹层疾病相关的snp位点,所述snp位点包括以下主动脉夹层易感性snp位点:clip3:nm_001199570:exon1:c.32c>t:p.p11l。
进一步地,本发明提供了所述的snp位点在制备检测主动脉夹层疾病的试剂中的应用。
进一步地,本发明还提供了所述的snp位点在制备预测主动脉夹层疾病早期诊断试剂盒中的应用。
优选的,所述的试剂盒包括检测主动脉夹层易感性snp位点clip3:nm_001199570:exon1:c.32c>t:p.p11l是否发生突变的试剂。
优选的,所述试剂盒可以为采用本领域已知的任何技术检测snp的试剂,只要其能够检出样本中易感snp位点clip3:nm_001199570:exon1:c.32c>t:p.p11l是否存在突变。其包括但不限于下面列举的各实施方式。
在第一实施方式中,该试剂盒包括利用测序法检测样本中易感snp位点clip3:nm_001199570:exon1:c.32c>t:p.p11l位点t等位基因存在的试剂。测序法是本领域所公知的技术,所需的引物等试剂,本领域普通技术人员均可根据需要自行选择(参见abi、beckman等公司测序仪相关使用说明),在此不再赘述。利用该试剂盒,通过测序法可以直接测得样本中易感snp位点clip3:nm_001199570:exon1:c.32c>t:p.p11l的序列,从而判断其是否携带相应位点等位基因的变异,进而判断其主动脉夹层的易感性。
在第二实施方式中,所述试剂盒包括利用taqman探针snp检测法检测样本中易感snp位点clip3:nm_001199570:exon1:c.32c>t:p.p11l基因型的试剂。其中所用taqman探针为针对易感snp位点clip3:nm_001199570:exon1:c.32c>t:p.p11l设计的探针,该探针可以使用试剂公司提供的探针;也可使用软件自行设计,如premierbiosoft公司的beacondesigner7.5。
在第三实施方式中,所述试剂盒为利用pcr-单链构象多态性法检测样本中易感snp位点clip3:nm_001199570:exon1:c.32c>t:p.p11l基因型的试剂盒。该试剂盒中包括用于扩增易感snp位点clip3:nm_001199570:exon1:c.32c>t:p.p11l的引物,pcr试剂、对照样本和检测构象的电泳所需试剂。所述电泳优选非变性聚丙烯酰胺凝胶电泳。对照样本中包括易感snp位点clip3:nm_001199570:exon1:c.32c>t:p.p11lcc纯合子的阴性对照样本和位点tt纯合子的阳性对照样本中的至少一个,此外还可以包括也可以不包括杂合子相应杂合子的对照样本。优选同时包括上述三类对照样本。待测样本扩增产物与对照样本的扩增产物同时电泳,比较其电泳结果可以得出待测样本中是否携带相应等位基因变异的检测结果。
更进一步地,本发明提供了所述的snp位点在制备诊断主动脉夹层疾病装置中的应用。
优选的,所述诊断装置是测序芯片。
再进一步地,本发明提供一种筛选与主动脉夹层疾病相关的snp位点的方法,所述方法包括以下步骤:
(1)提取主动脉夹层患者和正常对照的外周血样本的dna;
(2)将dna进行超声片段化,打断片段末端补平,3’端加a,连接adaptor,选择350~400bp之间的片段制备全基因组文库;
(3)应用gencap液相捕获目标基因技术进行全外显子检测;用高通量测序仪进行双端测序,读长为100bp;
(4)外显子测序后,进行常规过滤分析,以hg19、dbsnp(v147)为参考基因组版本为筛选过滤标准;留下致病位点、正常人频率在5%以下,及有文献报道的同义突变致病位点;为了更准确的筛选疾病相关位点,过滤掉sift、polyphen2、mutationtaster、gerp++预测全为良性的snp;过滤掉mutcount>5,mutratio>30%,正常数据库中maf>1%的indel;
(5)进行假阳性位点的排除工作,一是通过igv软件对去冗余duplicates后的bam文件(rmdup.sorted.bam)进行查看验证,突变情况不符合的视为假阳性位点;同时通过samtools软件对bam文件进行查看。然后,分别以突变的基因(a)、突变的位点(b)做为maker,进行稀有突变负荷(rvb)分析,统计病例组与对照组中该基因突变的样本数并计算or值,or>1,p<0.01。结果发现有多个突变位点与ad有统计学关联;
(6)通过基因功能和相关通路的注释分析以及文献检索数据对测序结果进行深度分析,最终发明人从48个突变位点筛选出一个主动脉夹层易感性snp位点:clip3:nm_001199570:exon1:c.32c>t:p.p11l。
本发明有益效果:
本发明通过发现了一个主动脉夹层易感snp位点并研究了其在主动脉夹层早期预测的应用前景,本发明提供的主动脉夹层相关的基因位点可能是主动脉夹层的早期生物标志物,为进一步研究主动脉夹层的遗传分子机制,探索主动脉夹层早期防治的药物靶点提供了新的方向。
附图说明
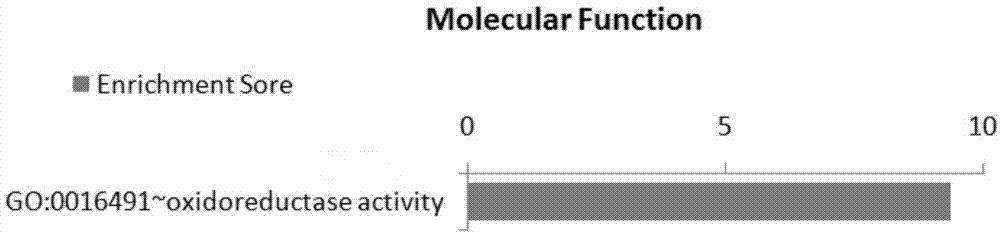
图148个位点go通路分析(molecularfunction)选取通路中包括两个及以上基因,pvalue小于等于0.05的通路,对富集得分作图;
图248个位点go通路分析(biologicalprocess)选取通路中包括两个及以上基因,pvalue小于等于0.05的通路,对富集得分作图。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段。
本发明中术语解释如下:
go(geneontology):描述基因功能的综合性数据库,可分为分子功能(molecularfunction,mf),生物过程(biologicalprocess,bp),和细胞组成(cellularcomponent,cc)三个部分。go富集以p小于0.05为显著富集。
实施例1样品收集
自2017年1月至2018年4月在深圳市孙逸仙心血管医院通过主动脉cta确诊stanforda型主动脉夹层的59例患者,收集全血2ml和590例正常对照样本来自迈基诺测序公司检索的数据库。已取得患者的知情同意,并通过伦理委员会审核。
样本处理:将edta抗凝全血按1:1比例与trizol混合,充分混匀后置于1.8ml细胞冻存管中,在液氮中迅速冷却30s后置于-80℃的冰箱保存。
实施例2提取血液样品dna
(1)将1ml通过edta(0.01m,china,huameibioengineer)抗凝处理的血液中加入1mlcl细胞裂解液,轻柔地颠倒混匀6次,用3600rpm的转速离心5min,弃除上清液;
(2)像离心管中再次倒入1mlcl细胞裂解液,轻柔地颠倒混匀6次,用3600rpm的转速离心5min,弃除上清液;确保沉淀保留在管内的前提下,将离心管倒置在清洁的吸水纸上静置2min;
(3)配置蛋白酶k和缓冲液fg的混合液;
(4)加入500μl蛋白酶k和缓冲液fg的混合液,随即混匀至溶液无团块;
(5)65℃水浴30min,期间颠倒混匀数次;
(6)加入1ml异丙醇,随即颠倒混匀至出现簇状或丝状基因组dna;
(7)用3600rpm的转速离心8min,弃除上清液;确保沉淀保留在管内的前提下,将离心管倒置在清洁的吸水纸上静置2min;
(8)加入1ml70%乙醇,振荡5sec,用3600rpm的转速离心3min,弃除上清液;
(9)重复步骤(8);
(10)确保沉淀保留在管内的前提下,将离心管倒置在清洁的吸水纸上静置5min;
(11)常温状态下,空气干燥基因组dna沉淀至所有液体完全挥发(至少5min)振荡5sec,用3600rpm的转速离心3min,弃除上清液;
(12)加入200μltb缓冲液,低速涡旋振荡5sec,65℃水浴加热1h,期间轻弹助溶数次;
(13)使用nanodropnd8000(thermo,usa)鉴定所提取的基因组dna浓度和纯度。浓度>30ng/μl,1.8<od260/od280<2.0,且总量>3μg的基因组dna样本视为合格,保存于-80℃的冰箱备用;
(14)在dna初步定量基础上,进一步采用琼脂糖凝胶电泳检测(胶浓度:0.8%,电压:120v,时间:20min)精确定量dna。电泳后出现弱带或主带之外存在杂带,说明dna可能有降解现象或存在杂质,如果电泳后出现一条强带,则说明提取的dna质量较高。全外显子测序要求dna浓度≥50ng/μl,总量不低于5μg,od260/280在1.8~2.0之间,od260/230在2.0左右,样本无rna污染,无降解或者轻微降解。
实施例3全外显子测序
1、dna文库构建
将3μgdna进行超声片段化,打断片段末端补平,3’端加a,连接adaptor,选择350~400bp之间的片段制备全基因组文库。文库样本使用agilent2100生物分析仪(安捷伦科技公司,美国)进行质控。
2、目标区域捕获测序
应用gencap液相捕获目标基因技术(北京迈基诺公司)进行全外显子检测。将1μgdna文库与bl缓冲液和探针混合,95℃加热7min,65℃加热2min加入23μl预热至65℃的hy缓冲液,65℃杂交22h。用500μl1x结合缓冲液清洗50μlmyone磁珠(美国lifetechnology公司)3次,重悬于80μl1x结合缓冲液。加入64μl2x结合缓冲液至杂交混合物中,转移至含有80μlmyone磁珠的试管中。旋转混匀1h。用wb1缓冲液室温清洗磁珠15min,用wb3缓冲液65℃清洗3次,每次15min。然后用洗脱缓冲液将结合的dna洗脱下来。洗脱的dna进行pcr反应,反应条件如下:98℃预变性30s;98℃变性25s,65℃退火30s,72℃延伸30s,共进行15个循环;最后72℃延伸5min。根据产品说明书用spribeads(美国beckmancoμlter)纯化pcr产物。富集的文库用illuminahiseq2000测序仪进行双端测序,读长为100bp。
3、数据分析
测序得到的原始测序序列,里面含有带接头的、低质量的reads,会对后续信息分析造成干扰。为了保证信息分析质量,对原始数据用cutadapt软件进行过滤,将去除接头序列和低质量碱基的测序数据用burrows-wheeleraligner(bwa)比对到人类基因组(版本grch37/hg19)上,并用picard工具去除冗余。目标区域的深度用coveragebed工具计算。通过gatk软件对indel位点附近进行重比对从而提高序列的质量。gatkhaplotypecaller检测snp与indel突变信息,并用annovar对突变注释,注释数据库包括dbsnp147,1000genomesproject,exomesequencingproject(esp6500),inhousedatabase(mygenostics),gnomad_genome_eas.onlinemendelianinheritanceinman(omim)andhumangenemutationdatabase(hgmdprofessional2016.10)。致病性预测数据库包括sift,polyphen-2andmutationtaster,以及通过acmg标准指南对致病性进行划分。
4、变异过滤
为了找出潜在的致病性突变,需要对数据进行过滤筛选。主要针对外显子区和可变剪切区域的突变,第一步:留下致病性分析(pathogenic_analysis)中的致病性突变(pathogenic)位点。
第二步(过滤筛选标准):筛选突变碱基测序次数大于5,突变频率大于等于30%以及1000g2015apr、esp6500si、inhouse、exac_all、exac_eas五个正常人突变数据库中保留没有出现或小于5%的位点;去除数据集中的同义突变位点,另外有文献报道的突变位点留下。
5、统计分析
对上述过滤后的突变结果进行稀有突变负荷分析,选择迈基诺590例数据作为对照样本,利用r语言中的metabin分析or值与95%置信区间,并用mantel-haenszel’s方法进行统计检验,p值小于0.01的认为显著。
6、结果
外显子测序后,进行常规过滤分析,筛选过滤标准:以hg19、dbsnp(v147)为参考基因组版本。留下致病(pathogenic)位点、正常人频率在5%以下,及有文献报道的同义突变致病位点,得到59351个点突变。为了更准确的筛选疾病相关位点,进一步过滤掉sift、polyphen2、mutationtaster、gerp++预测全为良性的snp;过滤掉mutcount>5,mutratio>30%,正常数据库中maf>1%的indel;经上述筛选得到29979个点突变。
之后,发明人进行了假阳性位点的排除工作,一是通过igv软件对去冗余duplicates后的bam文件(rmdup.sorted.bam)进行查看验证,突变情况不符合的视为假阳性位点;同时通过samtools软件对bam文件进行查看。然后,分别以突变的基因(a)、突变的位点(b)做为maker,进行稀有突变负荷(rvb)分析,统计病例组与对照组中该基因突变的样本数并计算or值,or>1,p<0.01。结果发现有48个突变位点与ad有统计学关联。
进一步,发明人对筛选出的48个突变位点进行基因功能和相关通路的注释。
48个突变位点所在基因的通路注释中选取count大于等于2的作图,如图1、2所示,在bp分析中,这些位点所在基因显著富集于氧化还原生物过程。
在48个突变位点的筛选结果中发现:
clip3:nm_001199570:exon1:c.32c>t:p.p11l可能与ad存在联系。
发明人结合基因功能和相关通路的注释分析以及文献检索数据对测序结果进行深度分析,最终发明人筛选出在病例组中发生突变的基因clip3,所述基因携带的突变snp位点如表1所示。clip3:nm_001199570:exon1:c.32c>t:p.p11l突变位点可能是导致ad的关键性分子,其可作为ad新型生物标志物,为指导其临床早期干预及靶向治疗提供了重要理论依据。
表1主动脉夹层snp位点信息
注:gene,基因名称;chr,染色体;pos,snp位置;aa_change,氨基酸改变。
实施例4与主动脉夹层易感性相关基因snp位点的鉴定
1.研究对象
主动脉夹层组:所选取的对象为深圳市孙逸仙心血管医院的通过主动脉cta确诊stanforda型主动脉夹层的25例患者,收集血液样本。
对照组:对照组受试者为深圳市孙逸仙心血管医院体检中心的无主动脉夹层及病史的人群,共30例受试者,收集血液样本。
2.病理及临床资料
记录入组患者病因、发病过程及治疗经过,并对一般临床资料如年龄、性别、病史等进行登记建立数据库。
两组均为无亲缘关系、地区及性别匹配的中国人群,本过程遵循程序符合人体试验委员会制定的伦理学标准,并取得受试者的知情同意。受试者经过肘静脉取血10ml全血或收集临床检查后剩余血样,柠檬酸钠抗凝,用于全基因组dna提取和血清学指标的检测。
3.试验样本提取同实施例2
4.包含snp位点的pcr反应
4.1设计引物
采用primerpremier5.0软件设计合成引物,引物序列如下:
正向引物:5’-taagacagatcctgccccga-3’(seqidno.1)
反向引物:5’-tcacgatcgttcacatggca-3’(seqidno.2)
扩增产物长度:336bp(seqidno.3)
4.2pcr反应
pcr反应体系如表2所示。pcr扩增程序为:95℃预变性10min,94℃变性15s,61℃退火15s,72℃延伸30s,进行30个循环,最后72℃延伸30min,于4℃保存,过夜需放置-20℃冷冻。
表2反应体系
5.测序
pcr扩增结束后,取5μl扩增产物,1%琼脂糖凝胶电泳,电泳30min,染色20min,然后将凝胶块置于凝胶成像仪中观察,根据比对marker的片段大小情况,初步判断扩增片段是否正确。进而对符合要求的扩增产物进行纯化:采用mag-bindoligonucleotidepurificationkit试剂盒,并按试剂盒要求进行操作。上样测序:采用abi公司bigdye3.1sequencingkit试剂盒,并按试剂盒要求进行操作;用abi公司3730型测序仪进行测序。
6.结果分析
通过chromas序列分析软件,将测序结果与标准序列进行比对,寻找snp位点,通过分析snp位点处碱基的类型,就可以得到snp位点的基因型。结果显示:发现clip3基因中如seqidno.3所示序列的第27位发现了一个snp位点,该位点存在等位基因c和等位基因t,组成了三种基因型,ct、cc和tt。在25例主动脉夹层患者测序得到336bp的片段的核苷酸序列(如seqidno.3所示)中,其在第27位的基因型为ct、tt;而在30例健康受试者对照测序得到336bp的片段的核苷酸序列(如seqidno.3所示)中,其在第27位的等位基因的基因型为cc;证实了该位点为ct、tt基因型时判断为主动脉夹层的易感基因型,该位点为cc基因型时判断为主动脉夹层的非易感基因型,从而进一步确认所述clip3:nm_001199570:exon1:c.32c>t:p.p11l的snp位点可用于主动脉夹层的检测、治疗、诊断、预后评估等辅助诊断。
实施例5用于预测主动脉夹层疾病早期诊断试剂盒的制作
组装本发明所述的用于主动脉夹层的试剂盒:
所述试剂盒包括检测clip3:nm_001199570:exon1:c.32c>t:p.p11l位点是否发生突变的试剂。
所述试剂包括用于扩增clip3:nm_001199570:exon1:c.32c>t:p.p11l位点的特异性引物,该引物可以采用软件来设计,如使用primer5、oligo6等;所述试剂还可以有相应pcr技术所需的常用试剂,如:dntps,mgcl2,双蒸水,taq酶等,这些常用试剂都是本领域技术人员熟知的,另外还可以有标准品和对照(如确定基因型的标准品和空白对照等)。此试剂盒的价值在于只需要外周血而不需要其他组织样品,通过最精简和特异的引物对检测snp,再通过snp谱辅助判断主动脉夹层,不仅稳定,检测方便,且精确,大大提高疾病诊断的敏感性和特异性,因此将此试剂盒投入实践,可以帮助指导诊断和更有效的个体化治疗。
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
序列表
<110>蒲佐
<120>clip3基因的snp位点的应用
<130>p18073
<160>3
<170>siposequencelisting1.0
<210>1
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>1
taagacagatcctgccccga20
<210>2
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>2
tcacgatcgttcacatggca20
<210>3
<211>336
<212>dna
<213>homosapiens
<400>3
taagacagatcctgccccgatggccccgccaccccgaggagaggaggaagaagaggagga60
ggaggatgaacccgtccccgaggcccccagccccacccaggagcgccggcagaagcctgt120
tgtgcacccctcggcacctgcccccctccctaaggactacgctttcaccttcttcgatcc180
caatgacccggcgtgccaggagatcctgtttgaccctcagaccaccatccccgagctgtt240
tgccattgtgcgccagtgggtgccccaagtccagcacaagatagacgtcatcggcaatga300
gattctgcgccgaggctgccatgtgaacgatcgtga336
- 还没有人留言评论。精彩留言会获得点赞!