一种用胆绿素Ⅸα二酯制备高含量胆红素Ⅸα的方法与流程
本发明属于胆红素制备领域,具体涉及一种用胆绿素ⅸα二酯非色谱分离法制备胆红素ⅸα的方法。
背景技术:
胆红素ⅸα,英文名是bilirubinⅸα(化合物1),单体结构式的二维示意图如下:
cas号是:635-65-4,分子式c33h36n4o6,分子量584.67。
胆红素ⅸα的纯品是一种橘红色结晶性固体(粉末),但难以得到含量96%以上的纯品,商业上的产品为深橘红色粉末,室温放置渐渐变成棕红色。胆色素类(bilepigments)是一种生物色素,是某些卟啉(porphyrin)代谢中形成的黄色、绿色、红色或褐色非金属开环化合物系列之一。除出现于兽类中的胆色素以外,无脊椎动物、低等脊椎动物、某些鸟的蛋壳、红藻和绿色植物中也有这种色素类。它不仅给动物体某些部位以不同的颜色,而且也是绿色植物光周期中不可缺少的,也是红藻光合作用过程中的辅助色素。
胆红素(bilirubin)是胆色素家族中的一类化合物,而胆红素ⅸα只是胆红素系列化合物中的一员(chemicalsocietyreviews,no.3,page363,1975).胆红素ⅸα具有广泛的生理活性,有抗氧化功能,可以抑制亚油酸和磷脂的氧化,在癌症的光动力治疗中,胆红素及其卟啉类似物有很大的应用潜力,目前,已有几个半合成卟啉药物在国内外上市,用于癌症的光动力治疗,但都有或多或少的副作用,已经上市的几个癌症的光动力治疗药物(例如photofrin)稳定性太差,成分复杂多变,因此,研究全合成高含量的胆红素并且对其结构进行改造是癌症的光动力治疗药物研究的方向之一。另外,胆红素ⅸα是体外培养牛黄的主要原料之一。中国药典(2015版)规定体外培养牛黄中胆红素ⅸα含量不得低于35.0%。中国药典的胆红素ⅸα含量化验方法是用紫外方法,规定胆红素ⅸα项下用紫外检测胆红素ⅸα的含量不得低于90%。胆红素ⅸα是一个在室温不稳定的化合物(febslett.18,315,1971),能够在室温发生一系列氧化、异构化、歧化、降解、聚合、分子内“关门”等复杂的反应,这些反应产生的杂质(包括胆红素iiiα和胆红素xiiiα),难以分离出,其紫外吸收等物性不是很清楚(大部分杂质的分子结构还没有完全搞清楚),导致紫外方法检测胆红素ⅸα的结果不科学和准确。
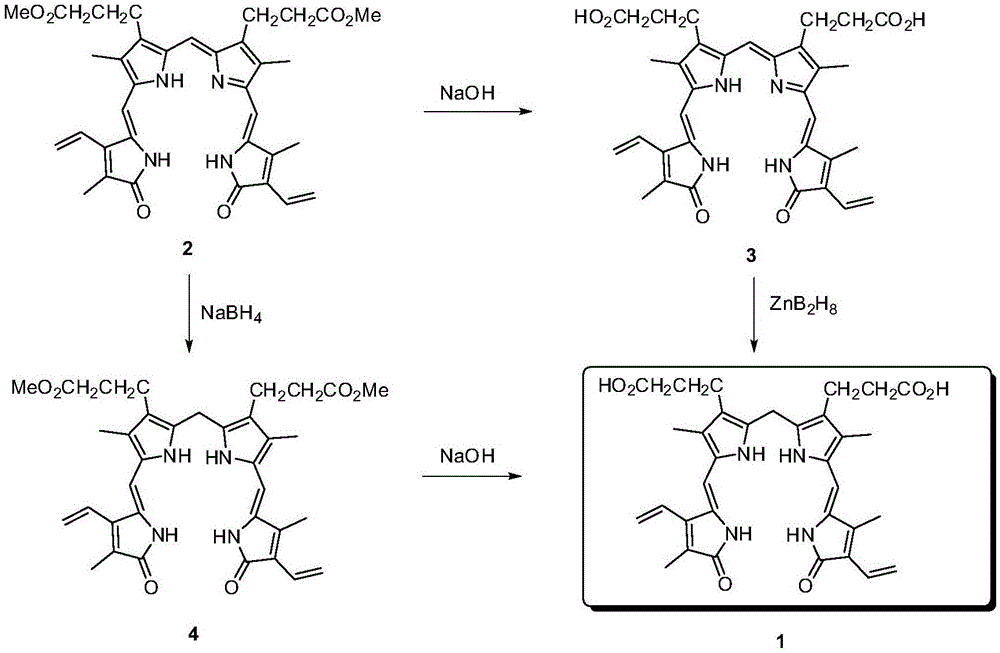
胆红素ⅸα首先由德国化学家fisher全合成(z.physiol.chem.,1942,vol.274,page231;1941,vol.268,page197)(尽管当时结构还没有完全搞清楚),最关键的最后二步,即胆绿素二甲酯ⅸα(图1中的化合物2)先水解成胆绿素ⅸα(图1中的化合物3)然后还原成胆红素ⅸα,还原剂是四价或低价的硫(例如保险粉)或锌粉-乙酸体系,收率都很低(低于25%),含量没有说明。fatiadi报道用硼氢化钠还原胆绿素ⅸ(化合物3)得到收率60%的胆红素ⅸα(experientia1139,1971),但没有报道详细的实验操作和纯化过程,也没有报道纯度和含量。胆红素ⅸα是一个非常不稳定的化合物(febslett.18,315,1971),特别是在溶液中或是在酸或碱存在下容易产生杂质。尽管在八十年前就提取和合成了胆红素ⅸα,但直到上个世纪七十年代才基本搞清楚胆红素ⅸα的分子结构(r.bonnett,nature,262,page327,1976)。在国外,胆红素ⅸα无商业价值(无市场),科研机构对它的化学研究基本是以理论研究为主,其合成研究基本停留在1~10毫克级,合成出初品后接着用色谱分离。sturrock报道了先水解后还原路线(sturrock;bull;kirsch,journaloflabelledcompoundsandradiopharmaceuticals,1994,vol.34,no.3,page263),即用5毫克胆绿素二甲酯ⅸα先水解(不经过分离),马上用过量的硼氢化钠还原、然后tlc分离、甲醇-氯仿精制后得到3.8毫克胆红素ⅸα,纯度没报道(仅有分解温度、核磁和紫外,纯度、含量不详)。本申请发明人重复了sturrock的实验操作,tlc监控发现还原过程比较复杂,杂质斑点难以控制,重复性较差。
目前,如图1所示,以胆绿素ⅸα二甲酯(化合物2)为原料出发,有二条路线可以合成胆红素ⅸα。有文献报道胆绿素ⅸα二甲酯先还原后水解成胆红素ⅸα(biochem.j.155,405-417,1976;biochim.biophys.acta,184,173-183,1969),采用了复杂的色谱分离,且收率不详,此路线中胆红素ⅸα在水解的条件下(室温,ph大于12)稳定性很差,会发生一系列副反应,导致难以分离得到纯的胆红素ⅸα;经本申请发明人重复文献,发现先还原后水解路线产物更加复杂(与先水解后还原路线比),反应混合物中tlc杂质点太多,表明先还原后水解路线不适合工业化。用硼氢化钠、硼氢化锂、锌粉、保险粉等还原剂还原胆绿素ⅸα成胆红素ⅸα,文献中已有报道(毫克级实验研究),但都缺乏纯度/含量数据。先水解后还原路线的主要问题是还原剂的量难以控制,容易把胆红素ⅸα还原过头,即胆红素ⅸα会被还原剂进一步还原。
张恒洲用提取的胆红素ⅸα制备了含量为90%的胆红素ⅸα二钠盐(cn105399655,2016),纯度不详。另外,以血红素(从猪血中提取,来源有保证)为底物,用生化法制备胆红素ⅸα,国内外都有文献报道,但都没有得到较纯的样品,仅紫外检测到了在溶液中有很稀的胆红素ⅸα存在,因为血红素的α位开环,无论是生化法还是化学法,选择性都难有保证,无法进一步深入研究,目前基本停止了该方法的研究。
目前市场上的胆红素ⅸα全部从动物(主要是牛、猪)的胆(用氯仿)提取生产的,含有相当多的未知杂质,包括少量高分子杂质(tlc发现在原点,hplc不出峰)。提取的低含量(尽管含量已达中国药典规定的90%)胆红素ⅸα必须进一步精制后才能用于体外培养牛黄。中国的胆红素ⅸα工业化提取已有三十多年的历史,尽管产业化已经十分成熟,但因屠宰的动物的胆汁中胆红素ⅸα分子结构随时在变化,提取的胆红素ⅸα含量难以达到97%以上,另外,胆源资源有限,越来越难以满足市场需求。
因此,开发不用色谱分离技术、具有工业化生产潜力的合成工艺(来制备高含量、高纯度的胆红素ⅸα)具有很大的工业价值,高含量、高纯度胆红素ⅸα的合成工艺是一个迫切的研究课题。
技术实现要素:
本发明的目的是提供一种用胆绿素ⅸα二酯制备胆红素ⅸα的方法,属于先水解再还原的路线,且不需要用色谱分离。该方法可以突破现有合成方法中需要用色谱进行分离,因而无法工业化大量生产的技术瓶颈,同时解决现有的工业化提取的胆红素ⅸα含量低、纯度低、质量不稳定(影响体外培养牛黄)的技术难题,使含量达到97%以上。
为了实现上述目的,本发明提供如下技术方案:
一种用胆绿素ⅸα二酯制备胆红素ⅸα的方法,其包含下列步骤:
(1)水解反应:在胆绿素ⅸα二酯的醇溶液中,于5~30℃滴加氢氧化钠的醇溶液,加入水后,于5~30℃水解,然后用弱酸调节ph到4~5,旋转蒸发除溶剂,水洗除无机盐,真空干燥后得到胆绿素ⅸα(室温条件下远比胆红素ⅸα稳定);
(2)还原反应:在胆绿素ⅸα的醇溶液中,加入游离基清除剂,即稳定剂,加入硼氢化物,在反应结束时,立即加入酮分解过量的还原剂,然后加弱酸溶液调节ph到4~5,旋转蒸发除溶剂,然后水洗,用甲醇-氯仿精制后得到含量超97%的胆红素ⅸα。
优选地,上述制备方法中,步骤(1)水解反应温度为优选为10~15℃。
优选地,上述制备方法中,步骤(2)加入的游离基清除剂的量为胆绿素ⅸα质量的0.05%~0.5%,优选0.1%~0.2%。
优选地,上述制备方法中,步骤(2)所述的游离基清除剂包括但不限于烷基苯酚。
进一步地,所述烷基苯酚为叔丁基对苯二酚。
优选地,上述制备方法中,步骤(2)的硼氢化物为硼氢化锌、硼氢化锂、硼氢化钠,硼氢化钾中的任意一种。
进一步地,所述硼氢化物为硼氢化锌。
优选地,上述制备方法中,步骤(2)的酮包括但不限于丙酮。
优选地,上述制备方法中,步骤(2)的还原反应用薄层色谱(thinlayerchromatography,tlc)监控,一旦胆绿素ⅸα还原完毕,立即加入酮分解过量的还原剂,避免还原过头。
优选地,上述制备方法中,步骤(2)所述的弱酸包括但不限于乙酸,优选10%乙酸。
本发明的有益效果是:
在还原反应中加入稳定剂,用中性(非强碱性)温和的还原剂硼氢化锌,还原反应一旦完成,立即用酮分解过量的还原剂,极大地减少了生成的胆红素ⅸα在还原反应及后处理过程中产生的副反应,从而避免了难以分离的杂质生成,因而也就不需要色谱分离,而且收率较高(二步反应最高达到85%)、含量高(hplc外标法含量超过97%),反应条件温和,成本低,操作方便,适合于工业化,为工业化大生产高含量胆红素ⅸα提供了重要理论依据和工艺参数。
附图说明
图1为现有技术中胆红素ⅸα的二条合成路线。
图2为实施例2制备的胆绿素ⅸα的nmr谱图。
图3为实施例2制备的胆红素ⅸα的1hnmr(cdcl3)谱图。
图4为实施例2制备的胆红素ⅸα的1hnmr(dmso-d6)谱图。
图5为实施例2制备的胆红素ⅸα的dept13cnmr(dmso-d6)谱图。
图6为实施例2制备的胆红素ⅸα的hplc谱图。
具体实施方式
通过以下详细说明结合附图可以进一步理解本发明的特点和优点。所提供的实施例仅是对本发明方法的说明,而不以任何方式限制本发明揭示的其余内容。下列实施例中未注明具体条件的实验方法,按照常规方法和条件。
常规试剂:ar级,国药试剂。tlc板:青岛海洋化工厂。
nmr仪器:bruck400兆,上海有机化学研究所。hplc仪器:安捷伦1200型
本发明中胆绿素ⅸα二甲酯按照smith,tetrahedron,vol.40,no.10,第1749页,1984的制备方法制得。
【实施例1】胆绿素ⅸα(化合物3)的制备
a、在一个250毫升的三口瓶中,投入0.350克(0.5735mmol)胆绿素ⅸα二甲酯加入100毫升甲醇,室温磁力搅拌全部溶解后,于10℃滴加5%氢氧化钠的甲醇溶液(1.38克,1.725mmol),然后搅拌下加入5克水,于10℃氮气保护下搅拌过夜(15小时),次日tlc(展开剂:二氯甲烷:乙酸乙酯v/v=50:1),表明二甲酯完全水解完毕,然后用10%乙酸调节ph到4~5,旋转蒸发除溶剂,得绿色固体,加20毫升水,搅拌一小时后过滤,20毫升含10%甲醇的水(w%)洗涤至ph6。五氧化二磷室温真空干燥过夜,得到0.331克蓝绿色粉末,收率99.1%。1hnmr(dmso-d6)见附图2。
b.于30℃氮气保护下搅拌水解,其它操作同a,8小时后tlc原料点消失,得到的反应混合物(中和后)tlc明显有拖尾现象,表明升高温度会带来杂质,同上处理后得到0.331克蓝绿色粉末,然后用50毫升甲醇-氯仿(甲醇:氯仿v/v=2:1)精制一次,得到0.305克蓝绿色粉末,收率91.3%。在这个温度下水解虽然时间缩短了,但发生了副反应,必须精制后才能得到tlc单一纯产物(点)。
【实施例2】胆红素ⅸα(化合物1)的制备
a.用硼氢化锌为还原剂
在一个500毫升的三口瓶中,氮气保护,投入0.300克(0.515mmol)胆绿素ⅸα,加入300毫升甲醇,室温磁力搅拌全部溶解后,加入1毫升含0.45毫克叔丁基对苯二酚的甲醇溶液,降温至0℃,于30分钟滴加完新鲜制备的含0.245克硼氢化锌(2.58mmol)的四氢呋喃溶液(20毫升)(thejournaloftheamericanchemicalsociety.1960,vol.82,page6074),反应液颜色由深绿色变为浅绿色,加完后再搅拌10分钟,反应液变成浅黄绿色,tlc(甲醇:氯仿v/v=1:50)表明仅仅有黄红色斑点,原料点(绿色)消失,立即滴加10毫升丙酮,有气体产生,搅拌15分钟至无气体产生后,用10%乙酸调ph4~5,搅拌10分钟,旋转蒸发除溶剂,得橘红色固体,加20毫升水,搅拌一小时后过滤,20毫升含10%甲醇的水(w%)洗涤至ph6.得到橘红色粉末,用30毫升2:1v/v甲醇-氯仿在室温搅拌2小时,冷却到10℃后过滤,6毫升2:1v/v甲醇-氯仿洗涤,五氧化二磷室温真空干燥过夜,得到0.259克橘红色粉末,收率86.0%。1hnmr(cdcl3)见附图3,1hnmr(dmso-d6)见附图4,dept13cnmr(dmso-d6)见附图5。
含量测定:
色谱条件与系统适用性试验:以十八烷基硅烷健键合硅胶为填充剂;检测波长为450nm。理论塔板数按胆红素峰计算应不低于3000。
对照品溶液的制备:精密称取胆红素对照品(干燥至恒重,低温保存)适量,加二氯甲烷制成每1ml中含有12μg的溶液,即得。
供试品溶液的制备:取本品约10mg,精密称定,置于50ml容量瓶中,加二氯甲烷适量,溶至刻度,摇匀,精密量取3ml,置于50ml容量瓶中,加二氯甲烷稀释至刻度,摇匀,用0.45μm微孔滤膜滤过,取续滤液,即得。
测定法:分别精密吸取对照品溶液与供试品溶液各5μl,注入液相色谱仪,测定。按外标法计算含量。
按干燥品计算,含胆红素ⅸα97.1%。hplc图谱见附图6。
b.用硼氢化钠为还原剂
用0.500克固体硼氢化钠(13.2mmol)代替硼氢化锌溶液,其它操作同a,得到的产物tlc明显有原点(极性大的)杂质,再用50毫升1:1v/v甲醇-氯仿精制一次,得到0.207克橘红色粉末,tlc显示无杂质,收率68.7%。
c.用硼氢化钾为还原剂
用0.500克固体硼氢化钾(9.27mmol)代替硼氢化锌溶液,其它操作同a,得到的产物tlc明显有原点(极性大的)杂质,再用50毫升1:1v/v甲醇-氯仿精制一次,得到0.198克橘红色粉末,tlc显示无杂质,收率65.8%。
d.用硼氢化锂为还原剂
用1.00克固体硼氢化锂(45.9mmol)代替硼氢化锌溶液,用乙醇代替甲醇作为溶剂,其它操作同a,得到的产物tlc明显有原点(极性大的)杂质,再用50毫升1:1v/v甲醇-氯仿精制一次,得到0.181克橘红色粉末,tlc显示无杂质,收率60.1%。
- 还没有人留言评论。精彩留言会获得点赞!