一种具有抗肿瘤活性的铜配合物、其制备方法及其用途与流程
本发明涉及化学合成的技术领域,具体而言,涉及一种具有抗肿瘤活性的铜配合物及其制备方法,以及所述铜配合物用于制备抗癌药物的用途。
背景技术:
自然界中广泛存在的金属离子对环境、医学、生物、化学科学都起着重要作用。其中一些重金属和过渡金属离子虽然在生物体内含量很低,但由于它们大多以金属蛋白质和金属酶的形式存在,参与到生物体内的许多重要反应及信息传递、能量转移等过程中,对生物体的代谢发展有重要的影响,在医药化学中也占据着重要的位置。铜是人体所需的微量元素,在各种有机体的基本生理过程中发挥着重要的作用。铜是人体内多种酶的辅基,含铜的酶多以氧分子或氧的衍生物为底物。如细胞色素氧化酶、多巴胺β-羟基酶、单胺氧化酶、酪氨酸酶、胞质超氧化物歧化酶等。铜蓝蛋白可催化fe2+氧化成fe3+,后者转入运铁蛋白,有利于铁的运输。
血清中铜的浓度与肿瘤发生,肿瘤负荷,肿瘤恶性进展及肿瘤复发有着密切的联系,其中包括肉癌、血癌、宫颈癌、肝癌、肺癌、脑癌和乳腺癌。例如,铜在肿瘤血管生成中起到重要的作用。虽然铜在癌组织的血管生成过程中的作用并未明确,但是近来x-射线荧光研究表明在血管生成过程中细胞中的铜大量细胞迁移和大规模重排。这个发现表明在血管生成过程中铜的转化可能促使铜的蛋白质的迁移。这样铜的螯合剂能通过与携带铜的蛋白质竞争作用阻碍癌的血管生成过程,从而抑制依赖铜的蛋白质的功能和肿瘤血管生成。
许多肿瘤细胞能富集高浓度的铜离子。人们利用肿瘤细胞这个特性将一些与铜离子亲和性高的配体加入到肿瘤细胞中使其与细胞内的铜离子形成具有蛋白酶体抑制活性的复合物,由于正常细胞中铜含量很小,形成的复合物浓度也极小,因此其对正常细胞的损害很小;相反,肿瘤细胞中富集的高浓度的铜离子,就可以形成较高浓度的蛋白酶体抑制剂从而导致肿瘤细胞凋亡。因此一些抗铜试剂在肿瘤治疗过程中发挥着一定的功效,所以制备一种含铜的抗癌药物是非常必要的。
技术实现要素:
有鉴于此,本发明要解决的技术问题在于克服现有技术的缺陷,提供了一种具有抗肿瘤活性的铜配合物及其制备方法,以及所述铜配合物用于制备抗癌药物的用途。
所述具有抗肿瘤活性的铜配合物的制备方法,包括以下步骤:
s1:将2,6-二氯-3-氰基-4甲基吡啶、水合肼混合至溶解,冷凝回流,冷却析出淡黄色固体,过滤,洗涤,烘干后得到浅黄色中间体a;
s2:称取1-苯基-1,3-丁二酮,溶解于乙醇溶液后滴入所述中间体a中,反应后冷却至室温,过滤,洗涤,烘干得到黄色配体l;
s3:在所述黄色配体l与六水合氯化铜中,滴加乙醇和水,混合均匀,加热,得到浅绿色长条状晶体i,将所述浅绿色长条状晶体i用水和乙醇洗涤后,真空干燥,得到所述铜配合物。
在某些实施方式中,所述s1中取2mmol2,6-二氯-3-氰基-4甲基吡啶加入4mmol水合肼,摇匀至所述2,6-二氯-3-氰基-4甲基吡啶溶解。
在某些实施方式中,所述s1中所述2,6-二氯-3-氰基-4甲基吡啶与水合肼溶解后,于120℃冷凝回流3h,冷却析出淡黄色固体,过滤,用冰乙醇洗涤,烘干后得到浅黄色中间体a。
在某些实施方式中,所述s1中得到的浅黄色中间体a的产率为93.6%。
在某些实施方式中,所述s2中取3mmol1-苯基-1,3-丁二酮,溶解于35ml的乙醇溶液后滴入所述中间体a中进行反应。
在某些实施方式中,所述s2中反应温度为80℃,反应时间为2h。
在某些实施方式中,所述s2中反应后冷却至室温,过滤,用乙醚洗涤,烘干得到所述黄色配体l。
在某些实施方式中,所述s2中得到的黄色配体l的产率为82.8%。
在某些实施方式中,所述s3中在0.023nmol黄色配体l与0.1nmol六水合氯化铜中,滴加2ml乙醇和0.5ml水,混合均匀。
在某些实施方式中,所述s3中,加热的温度为90℃,加热时间为3天。
在某些实施方式中,所述s3中得到的铜配合物的产率为65%。
本发明还保护根据上述方法制备的具有抗肿瘤活性的铜配合物。
本发明还保护所述铜配合物用于制备抗肿瘤的药物的应用。
在某些实施方式中,所述肿瘤包括但不限于肝癌、膀胱移行细胞癌、胃癌和宫颈癌。
本发明提供的一种具有抗肿瘤活性的铜配合物具有较高的抗肿瘤活性和较低的细胞毒性,尤其是对人膀胱移行细胞癌细胞(t-24)的杀伤能力较强,能高效诱导肿瘤细胞凋亡,但其对正常的人肝细胞株(hl-7702)的毒性相对较低,有望开发为新型的高效、广谱、低毒副作用的癌症治疗的化疗药物,属于本领域的首创发明。所述具有抗肿瘤活性的铜配合物的合成方法简单实用,成本低廉,重复性好,产品纯度和产量高,具有广泛的产业价值,有利于商业化的推广应用。
附图说明
应当理解的是,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
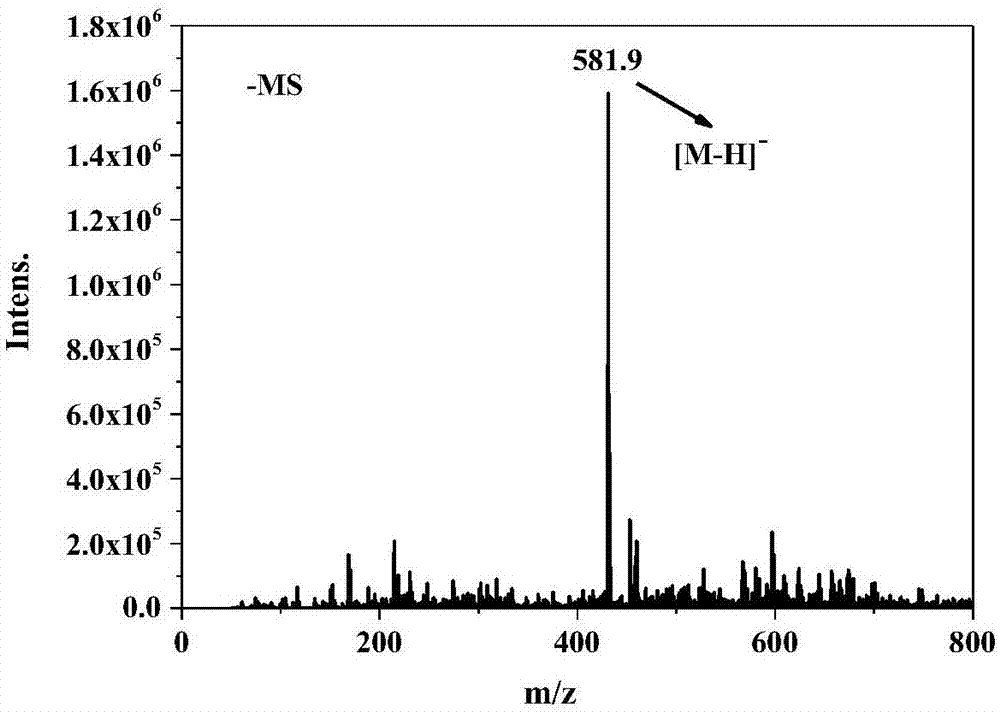
图1是所述铜配合物的质谱图;
图2是所述铜配合物的晶体结构图;
图3是所述铜配合物对人膀胱癌细胞t-24作用24h后对其细胞凋亡的影响;
图4是铜配合物对人膀胱癌细胞t-24作用8h后对其细胞中活性氧的影响;
图5是铜配合物对人膀胱癌细胞t-24作用24h后对其细胞中钙离子的影响。
具体实施方式
在下文中,将结合附图更全面地描述本公开的各种实施例。本公开可具有各种实施例,并且可在其中做出调整和改变。因此,将参照在附图中示出的特定实施例更详细地描述本公开。然而,应理解:不存在将本公开的各种实施例限于在此公开的特定实施例的意图,而是应将本公开理解为涵盖落入本公开的各种实施例的精神和范围内的所有调整、等同物和/或可选方案。结合附图的描述,同样的附图标号标示同样的元件。
在下文中,可在本公开的各种实施例中使用的术语“包括”或“可包括”指示所公开的功能、操作或元件的存在,并且不限制一个或更多个功能、操作或元件的增加。
在本公开的各种实施例中,表述“或”或“a或/和b中的至少一个”包括同时列出的文字的任何组合或所有组合。例如,表述“a或b”或“a或/和b中的至少一个”可包括a、可包括b或可包括a和b二者。
在本公开的各种实施例中使用的表述(诸如“第一”、“第二”等)可修饰在各种实施例中的各种组成元件,不过可不限制相应组成元件。例如,以上表述并不限制所述元件的顺序和/或重要性。以上表述仅用于将一个元件与其它元件区别开的目的。例如,第一用户装置和第二用户装置指示不同用户装置,尽管二者都是用户装置。例如,在不脱离本公开的各种实施例的范围的情况下,第一元件可被称为第二元件,同样地,第二元件也可被称为第一元件。
应注意到:如果描述将一个组成元件“连接”到另一组成元件,则可将第一组成元件直接连接到第二组成元件,并且可在第一组成元件和第二组成元件之间“连接”第三组成元件。相反地,当将一个组成元件“直接连接”到另一组成元件时,可理解为在第一组成元件和第二组成元件之间不存在第三组成元件。
在本公开的各种实施例中使用的术语仅用于描述特定实施例的目的并且并非意在限制本公开的各种实施例。如在此所使用,单数形式意在也包括复数形式,除非上下文清楚地另有指示。除非另有限定,否则在这里使用的所有术语(包括技术术语和科学术语)具有与本公开的各种实施例所属领域普通技术人员通常理解的含义相同的含义。所述术语(诸如在一般使用的词典中限定的术语)将被解释为具有与在相关技术领域中的语境含义相同的含义并且将不被解释为具有理想化的含义或过于正式的含义,除非在本公开的各种实施例中被清楚地限定。
实施例
本发明提供了一种具有抗肿瘤活性的铜配合物及其制备方法。
该种具有抗肿瘤活性的铜配合物的制备方法包括以下步骤:
1.中间体a的合成:
称取2,6-二氯-3-氰基-4甲基吡啶(0.374g,2mmol),放入150ml的圆底烧瓶中,缓慢加入水合肼(0.20g,4mmol),摇匀使2,6-二氯-3-氰基-4甲基吡啶全部溶解,120℃冷凝回流3h,反应结束后冷却,逐渐析出淡黄色固体,过滤,用冰乙醇洗涤,烘干后得到浅黄色中间体a0.35g,产率93.6%。1hnmr(400mhz,d-6dmso):11.25(s,1h,pyrazole-h),7.63(s,1h,py-h),6.02(s,1h,-nh-),4.79(s,2h,-nh-nh2),4.09(s,2h,pyrazole–nh2),2.41(s,3h,py-ch3).
2.配体l的合成:
称取1-苯基-1,3-丁二酮(0.50g,3mmol),溶解于35ml的乙醇溶液后,逐渐滴入上述所得的中间体a中,保持温度为80℃反应2h,冷却至室温,过滤,用乙醚洗涤,烘干后得到黄色配体l0.29g,产率82.8%。1hnmr(400mhz,d6-dmso,fig.s2):8.12(s,2h,py-h),7.676(s,2h,ph-h),7.612(s,2h,ph-h),7.492(s,1h,ph-h),7.274(s,4h,ph-h),6.533(s,1h,pyrazole-h),3.34,3.005(s,3h,pyrazole-ch3),2.773(s,3h,-ch3),2.323(s,3h,-ch3).13cnmr(100mhz,d6-dmso,fig.s2)δ=103.98,110.14,112.51,113.61,128.59,128.97,130.11,144.77,145.03,147.70,150.13,154.82,158.60,158.64.hrms:431.1971(m+h)+(calcdforc27h22n6,430.19).ir(kbr):1629,1577,1498,1443,1381,1161,1067,976cm-1.
中间体a和配体l的合成反应式如下:
3.铜配合物culcl2(h2o)的合成:
在一根一端封闭的长20cm厚0.1cm的硬质玻璃管加入配体l(0.023mmol,0.01g),cucl2·6h2o(0.1mmol,0.0178g),滴加乙醇2ml和水0.5ml,混合均匀后熔融密封开口端,置于90℃的烘箱中加热3天,管内有浅绿色长方体状的晶体i生成,把晶体i从管中取出,分别用少量水、乙醇洗涤,真空干燥(产率:65%)。选择适合x-射线单晶衍射的晶体i,以确定晶体结构。ir(kbr):1626,1577,1498,1381,1364,1316,1254,1161,1068,995cm-1.anal.calc.(forc27h24cucl2n6o)c55.62;h4.15;n14.42%,found.c55.70;h4.11;n14.37%,esi-msm/z:581.9[m-h]-(calcdforc27h24cucl2n6o,582.96),参见图1和图2。
本发明具有抗肿瘤活性的铜配合物的制备方法简单实用,成本低廉,重复性好,产品纯度和产量高,具有广泛的产业价值,有利于商业化的推广应用。
本发明还提供了所述具有抗肿瘤活性的铜配合物抗肿瘤活性测试。包括以下步骤:
一、铜配合物的抗肿瘤活性测试
所述铜配合物culcl2(h2o)的分子式为:c27h24cucl2n6o,分子量为:582.96,晶体结构数据见表1。对本实验选用卵巢癌细胞(skov-3),人肝癌体外细胞株(7402),人膀胱移行细胞癌细胞(t-24),胃癌细胞(mgc80-3),宫颈癌细胞(hela),正常人肝细胞株(hl-7702)等肿瘤细胞生长的抑制率见表2,对多种人肿瘤细胞株及人正常肝细胞株的ic50值见表3。
表1铜配合物的晶体结构数据
表220μm浓度下铜配合物对各细胞株的抑制率
表3铜配合物对各细胞株的ic50值(μm)
采用mtt法对化合物进行了skov-3、7402、t-24、mgc80-3和hela等五种肿瘤细胞株的体外抗肿瘤活性测试,同时测试其对hl-7702正常肝细胞株的毒性。初筛实验中用含体积分数10%新生牛血清的培养液配成单个细胞悬液,以每孔4000~5000个细胞接种到96孔板,每孔体积190μl,培养12h待细胞贴壁后,每孔分别加入不同浓度的受试配合物(分别为1.25、2.5、5、10、20μg/ml),每个浓度平行设4个复孔,其中助溶剂dmso终体积分数小于等于1%,每个组也平行设4个复孔,药物作用时间48h。培养结束前4h每孔加入10μlmtt(5g/lpbs),继续培养4h,生成的蓝色结晶加入dmso(150μl/孔),平板震荡器振荡5min,充分溶解结晶物,最后比色以空白调零。用酶标仪以570nm/630nm双波长测定去除本底光吸收值后的吸光度值(od),计算出细胞增殖抑制率。抑制率=(1-样品组od值/对照组od值)×100%;bliss法拟合计算ic50;所有实验重复3次后取平均值。由结果可知,铜配合物对7402、t-24、mgc80-3和hela这四种肿瘤细胞株的体外抗肿瘤活性较好,特别是对人膀胱移行细胞癌细胞t-24对抗肿瘤活性最强,其ic50值为3.12±0.13μm,对skov-3细胞的稍弱,而对hl-7702正常肝细胞株的毒性的毒性较弱。以下实验二至四均采用t-24细胞。
二.ao/eb染色检测凋亡实验:
取处于对数期细胞用pbs缓冲液洗涤后,用胰蛋白酶消化,1000r/min离心10min,收集细胞,用血球计数板计数取约2ml细胞悬浮液(约1×106个细胞),接种于共聚焦小皿后放入细胞培养箱继续培养;待单层细胞贴壁长至85%左右时,换新的10%新生牛血清的培养液,同时按一定浓度梯度分别加入铜配合物储备液,摇匀后重新放入细胞培养箱在作用24h,弃去培养液,pbs洗涤三次,滴加100μg/ml的丫碇橙(ao)和溴乙啶(eb)染色液,37℃染色30min,弃去染色液,pbs洗涤三次,荧光显微镜下观察、拍照记录。结果如图3所示,随着配合物浓度的增加,t-24细胞凋亡数目增多,细胞体积变小,橘红色加深,这是细胞凋亡的特征。说明这个配合物能高效率地诱导t-24细胞的凋亡。
三.活性氧ros的检测:
取处于对数期细胞用pbs缓冲液洗涤后,用胰蛋白酶消化,1000r/min离心10min,收集细胞,用血球计数板计数取约2ml细胞悬浮液(约1×106个细胞),接种于六孔板中后放入细胞培养箱继续培养;待单层细胞贴壁85%左右时,换新的10%新生牛血清的培养液,同时按一定浓度梯度分别制备铜配合物储备液,摇匀后重新放入细胞培养箱再作用8h,弃掉培养基,加入1:1000稀释好的dcfh-da,置于细胞培养箱中37℃孵育30min,每隔3~5min颠倒摇匀一次,然后用不含血清的培养基洗涤三次,应用cytation5细胞成像微孔板检测仪检测细胞中ros变化的情况。活性氧自由基ros在正常的细胞中处于一种平衡、稳定的状态;若细胞受到外界的刺激,其细胞内ros水平将被打破,ros增大,对细胞造成损伤,从而引起细胞凋亡。dcfh-da本身没有荧光,能穿过细胞膜进入细胞,进入细胞后被细胞内的酯酶水解成dcfh,而dcfh不能穿过细胞膜,dcfh进一步被细胞内的活性氧氧化成发绿色荧光的dcf,所以可以通过dcf的荧光强度来反映细胞内的活性氧水平。实验结果表明配合物能升高t-24细胞内的活性氧水平。结果如图4所示,不同浓度的铜配合物对t-24细胞作用8h后,经cytation5细胞成像微孔板检测仪检测,与空白对照组t-24细胞相比较,加药组的细胞显现出明显的绿色荧光,且配合物浓度越大,绿光荧光越明显,实验结果表明所述铜配合物诱导t-24细胞中活性氧增加,进而引起细胞凋亡。
四.ca2+离子释放的检测:
取处于对数期细胞用pbs缓冲液洗涤后,用胰蛋白酶消化,1000r/min离心10min,收集细胞,用血球计数板计数取约2ml细胞悬浮液(约1×106个细胞),接种于六孔板中后放入细胞培养箱继续培养;待单层细胞贴壁85%左右时,换新的10%新生牛血清的培养液,同时按一定浓度梯度分别铜配合物储备液,摇匀后重新放入细胞培养箱在作用24h,弃掉培养基,加入1:2000稀释好的fluo-3am,置于细胞培养箱中37℃孵育30min,每隔3~5min颠倒摇匀一次,然后用不含血清的培养基洗涤三次,应用cytation5细胞成像微孔板检测仪检测细胞中ca2+离子变化的情况。fluo-3am是一种用于检测细胞内钙离子的荧光探针,其自身荧光强度非常弱,但其可以穿透细胞膜,当fluo-3am进入细胞后可以被细胞内的酯酶剪切形成fluo-3,fluo-3可以和细胞内钙离子结合而产生较强的荧光,且荧光强度随着钙离子浓度的升高而不断增强。结果如图5所示,不同浓度的铜配合物对t-24细胞作用24h后,与空白组相比较,加药组中fluo-3am与细胞中的ca2+离子结合荧光强度明显增强,且配合物浓度越大,荧光越明显,初步说明铜配合物可使t-24细胞中ca2+离子大量释放,从而导致细胞凋亡。
综上所述,本发明提供的铜配合物具有较高的抗肿瘤活性和较低的细胞毒性等诸多的优点及价值,并在同类产品中未见有类似的方法公开发表或使用而确属创新,产生了好用且实用的效果,较现有的技术具有增进的多项功效,从而较为适于实用,并具有广泛的产业价值。
应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施方式中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
发明人声明,本发明通过上文所列出的一系列的详细说明仅仅是针对本发明的可行性实施方式的具体说明,但本发明并不局限于上述详细工艺设备和工艺流程。并且即不意味着本发明应依赖上述详细工艺设备和工艺流程才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
- 还没有人留言评论。精彩留言会获得点赞!