一种自组装树状纳米复合物及其应用的制作方法
本发明涉及生物技术领域,特别是涉及一种基于适配体识别及催化dna探针自组装成的树状纳米复合物及其在检测和原位成像循环肿瘤细胞膜蛋白中的应用。
背景技术:
肿瘤相关膜蛋白(tmp)是一种在癌细胞中异常表达的蛋白质。它们通常作为鉴定癌细胞在癌症发生和恶性肿瘤发展中的生理状态的标志。据估计,人类基因组的30%是编码膜蛋白,大约30-40%的市售药物靶向细胞表面膜蛋白。因此,分析tmp对肿瘤诊断,药物靶向转运和细胞类型分类至关重要。膜蛋白通常含有疏水区域,相互作用的异质结构和复杂的环境,使得它们分离和纯化非常麻烦,因此导致膜蛋白的分析程序复杂、繁琐且依赖于贵重仪器。除此之外,许多肿瘤细胞膜蛋白丰度极低。目前检测肿瘤细胞膜蛋白的主要策略是膜蛋白标记,分离和纯化,随后使用免疫荧光、蛋白质印迹(wb)或质谱(ms)为基础的技术进行蛋白质测定。wb尽管在半定量检测特定蛋白质方面取得了成功,但仍然存在一些缺点:灵敏度低,可能出现非特异性条带,并且需要复杂的操作。免疫荧光是最具代表性和最常用的成像方法之一,但目前还远未达到令人满意的程度。dna纳米探针技术由于具有高灵敏度、非损伤性、能原位检测等优点而受到了极大的关注。现已报道的检测方法大部分都是基于抗体特异性识别肿瘤细胞表面膜蛋白,抗体一般都具有价格高,不易保存,效价不稳定等缺点,亟待设计新方法以克服上述缺陷。
技术实现要素:
鉴于以上所述现有技术的缺点,本发明的目的在于提供一种基于适配体识别及催化dna探针自组装成树状纳米复合物用于检测和原位成像循环肿瘤细胞膜蛋白,用于解决现有技术中肿瘤相关膜蛋白的检测灵敏度低、特异性差、操作复杂、成本高等问题。
为实现上述目的及其他相关目的,本发明第一方面提供一种用于肿瘤相关膜蛋白检测及原位成像的触发链,包括识别区、触发区,所述识别区序列包括5’-ggtggtggtggttgtggtggtggtgg-3’,所述触发区序列包括5’-tgacgaactagttgatgaagctg-3’。
在本发明的一些实施例中,所述触发链还包括隔离区。
在本发明的一些实施例中,所述隔离区碱基数为至少一个。
在本发明的一些实施例中,所述隔离区碱基数为3个。
在本发明的一些实施例中,所述隔离区序列为5’-ttt-3’。
本发明第二方面提供一种用于肿瘤相关膜蛋白检测及原位成像的自组装树状纳米复合物,由f链、q链、辅助链1、f’链、q’链、辅助链2自组装获得,
所述f链的核苷酸序列包括:
5’-gtgtgcctattatgtctcctcctgtgtgcctattatgtctcctcctcagcttcatcaactagttcgtca-3’;
所述q链的核苷酸序列包括:
5’-aactagttgatgaagctggacataataggcacacgacataataggcacac-3’;
所述辅助链1的核苷酸序列包括:
5’-gtgtgcctattatgtcgtgtgcctattatgtccagctt-3’;
所述f’链的核苷酸序列包括:
5’-aggaggagacataataggcacactgacgaactagttgatgaagctg-3’;
所述q’链的核苷酸序列包括5’-cagcttcatcaactaggtgtgcctattatgtctc-3’;
所述辅助链2的核苷酸序列包括5’-gcacacctagttgatgaagctgtg-3’。
在本发明的一些实施例中,所述自组装树状纳米复合物还连接有所述触发链。
在进行肿瘤相关膜蛋白检测时,触发链先与待检测细胞悬液反应,再将未连接触发链的自组装树状纳米复合物加入其中,反应结束后,通过检测荧光强度,进而计算出膜蛋白含量。
在进行肿瘤相关膜蛋白成像时,将连接有触发链的自组装树状纳米复合物加入待检测细胞悬液中,反应结束后,通过荧光显微镜、激光共聚焦显微镜等获得成像图。
在本发明的一些实施例中,所述f链的5’端、f’链的3’端、辅助链1的5’端、辅助链2的3’端均连接有荧光基团,所述q’链的5’端、q链的3’端均连接有淬灭基团。
在本发明的一些实施例中,所述荧光基团选自fam、hex中的任一种。
在本发明的一些实施例中,所述淬灭基团选自bhq1。
当然,也可以采用其他的荧光基团或淬灭基团。
本发明第三方面提供上述自组装树状纳米复合物的制备方法,包括如下步骤:
1)将f链、f’链、q链、q’链、辅助链1、辅助链2分别溶解至缓冲液中,制得含有相应核苷酸链的溶液;
2)将含有f链的溶液与含有q链的溶液混合,变性退火处理,制得第一底物,将含有f’链的溶液与含有q’链的溶液混合,变性退火处理,制得第二底物,将退火的第一底物与含有辅助链1的溶液混合,将退火的第二底物与含有辅助链2的溶液混合,反应结束后,将两种溶液混合,反应制得所述自组装树状纳米复合物。
在本发明的一些实施例中,所述步骤2)中,按摩尔计,f链:q链=2:3,f’链:q’链=3:4,辅助链1:辅助链2=1:2,f链:f’链:辅助链1=12:27:20。
在本发明的一些实施例中,两种溶液混合后,加入所述触发链,制得连接有触发链的自组装树状纳米复合物。
在本发明的一些实施例中,所述步骤2)中,加入所述触发链后,所述触发链在混合液中的浓度为5nm-150nm。
本发明第四方面提供上述触发链或自组装树状纳米复合物在检测及原位成像循环肿瘤细胞膜蛋白中的应用。
在本发明的一些实施例中,所述f链、f’链用于原位成像肿瘤细胞膜蛋白。
在本发明的一些实施例中,所述辅助链1、辅助链2用于检测肿瘤细胞膜蛋白。
本发明第五方面提供利用上述触发链或自组装树状纳米复合物检测及原位成像循环肿瘤细胞膜蛋白的方法,包括:取待测细胞悬液,加入连接有所述触发链的自组装树状纳米复合物,反应结束后,离心,去掉上清液,通过显微镜获得成像图。该显微镜包括但不限于荧光显微镜、激光共聚焦显微镜。
在本发明的一些实施例中,还包括:取待测细胞悬液,加入触发链,反应结束后,离心,去掉上清液,加入未连接触发链的自组装树状纳米复合物,反应结束后检测荧光,根据荧光强度值计算膜蛋白含量。
在本发明的一些实施例中,肿瘤细胞膜蛋白标准曲线方程为y=748.38-275.96lgx,r2=0.989,y为荧光强度,x为肿瘤细胞浓度,单位cell*ml-1。可以根据肿瘤细胞的膜蛋白平均含量,进一步计算出膜蛋白含量。
如上所述,本发明的一种基于适配体识别及催化dna探针的自组装树状纳米复合物及其应用,具有以下有益效果:①本发明基于适配体识别及催化dna探针自组装成树状纳米复合物,该复合物的组装合成方法简单、稳定性好,dna链在催化链存在下能够自组装成树状纳米复合物,而不需要苛刻的反应条件和贵重的仪器;②dna树状纳米复合物检测肿瘤细胞表面膜蛋白含量的同时也能成像肿瘤细胞表面膜蛋白;③通过利用适配体和催化链结合在一起能够特异性识别并主动靶向癌细胞膜蛋白和荧光成像;④该dna树状纳米复合物是由dna链自组装而成,具有较低的生物毒性和免疫原性,利于其生物应用。
附图说明
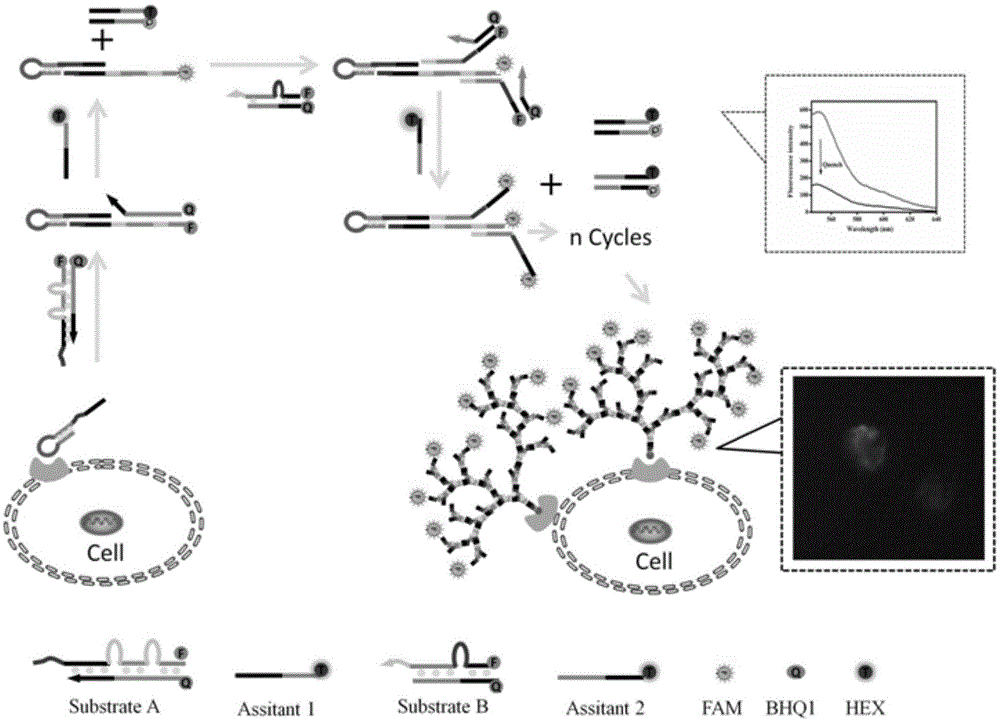
图1显示为本发明实施例1的dna树状纳米复合物实验原理图。
图2显示为本发明实施例1的聚丙烯酰胺凝胶电泳(page)表征dna树状纳米复合物组装图。
图3显示为本发明实施例1中不同浓度的触发链催化dna树状纳米复合物自组装的荧光强度图。
图4显示为本发明实施例1的dna树状纳米复合物原位成像肿瘤细胞膜蛋白图。
图5显示为本发明实施例1的激光共聚焦显微镜成像肿瘤细胞图。
图6显示为本发明实施例2的dna树状纳米复合物检测肿瘤细胞膜蛋白标准曲线图。
具体实施方式
以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
须知,下列实施例中未具体注明的工艺设备或装置均采用本领域内的常规设备或装置;所有压力值和范围都是指绝对压力。
此外应理解,本发明中提到的一个或多个方法步骤并不排斥在所述组合步骤前后还可以存在其他方法步骤或在这些明确提到的步骤之间还可以插入其他方法步骤,除非另有说明;还应理解,本发明中提到的一个或多个设备/装置之间的组合连接关系并不排斥在所述组合设备/装置前后还可以存在其他设备/装置或在这些明确提到的两个设备/装置之间还可以插入其他设备/装置,除非另有说明。而且,除非另有说明,各方法步骤的编号仅为鉴别各方法步骤的便利工具,而非为限制各方法步骤的排列次序或限定本发明可实施的范围,其相对关系的改变或调整,在无实质变更技术内容的情况下,当亦视为本发明可实施的范畴。
适配体是用指数富集的配体系统进化技术(selex)从人体外合成的随机寡核苷酸序列库中反复筛选得到的能与靶标特异性相互作用的一段寡核苷酸(dna或rna)。适配体能以高亲和力和特异性识别多种靶标,包括蛋白质,小分子甚至整个细胞。与抗体相比,适配体具有容易合成和修饰,成本低,复合物具有可控性和极低的免疫原性等优点。本发明中,我们利用适配体特异性识别并结合肿瘤细胞表面膜蛋白催化dna探针自组装成树状样dna纳米复合物,用于同时检测和原位成像肿瘤细胞表面膜蛋白,取代传统检测肿瘤细胞蛋白的westernblot和免疫组化等方法。
本发明适用于核仁蛋白表达较高的细胞成像及检测。
实施例1
实验设计原理如图1所示,具体过程如下:底物链a由标记荧光基团(fam)的dna链(f链)和标记淬灭基团(bhq1)的dna链(q链)组成。当f链和q链在95℃变性5min,然后在30min内缓慢降温至室温,根据碱基互补配对原则,f链和q链形成互补双链。由于荧光基团和猝灭基团非常接近,导致底物链a的荧光呈现“淬灭”状态。辅助链1设计成与其相应底物链a中的q链上的特定区域互补。同理,底物链b由标记荧光基团(fam)的dna链(f’链)和标记淬灭基团(bhq1)的dna链(q’链)组成。当f’链和q’链在95℃变性退火后,根据碱基互补配对原则,f’链和q’链形成互补双链。由于荧光基团和猝灭基团非常接近,导致底物链b的荧光呈现“淬灭”状态。辅助链2设计成与其相应底物链b中的q’链上的特定区域互补。当引入触发链as1411-1时,其与底物链a暴露的立足点杂交并对接,导致分支迁移反应,从f链置换部分q链并打开第一个环,然后辅助链1通过对接到新暴露的立足点将q链置换,并且产生副产物a。通过从f链中解离带有淬灭基团的q链,f链中的荧光得到恢复。底物链a中的f链暴露出两个串联连接的相同序列,其可以同时被两个底物链b的立足点与之杂交。同理,在辅助链2的帮助下将q’链置换,并且产生副产物b,更多的荧光报告基团被释放,并且由与触发链dna相同的序列组成的两个单链区域被暴露从而进入新一轮反应。通过循环反应最终形成树状纳米复合物,并产生更多的副产物a和副产物b。通过荧光仪检测副产物a和副产物b荧光强度的降低来检测肿瘤细胞膜蛋白表达的量,as1411-1催化形成的树状纳米复合物与肿瘤细胞表面的核仁蛋白结合,从而成像肿瘤细胞膜蛋白。
上述过程涉及的序列如下:
as1411-trigger:
fstrand:
fam-gtgtgcctattatgtctcctcctgtgtgcctattatgtctcctcctcagcttcatcaactagttcgtca(seqidno.2);
qstrand:
aactagttgatgaagctggacataataggcacacgacataataggcacac-bhq1(seqidno.3);
assistant1:hex-gtgtgcctattatgtcgtgtgcctattatgtccagctt(seqidno.4);
f'strand:
aggaggagacataataggcacactgacgaactagttgatgaagctg-fam(seqidno.5);
q'strand:bhq1-cagcttcatcaactaggtgtgcctattatgtctc(seqidno.6);
assistant2:gcacacctagttgatgaagctgtg-hex(seqidno.7)。
适配体识别及催化dna探针自组装成树状纳米复合物的构建过程如下:
杂交缓冲液tris-hcl缓冲液的配制:ph为7.4,由tris、nacl、mgcl2和去离子水组成,其中tris、nacl和mgcl2的终浓度依次为20mmol*l-1、100mmol*l-1、5mmol*l-1。
1xte缓冲液:ph为8.0,成分为10mmtris、1mmedta(购买于生工生物工程(上海)有限公司)lot:6703569。
①在生工生物工程(上海)有限公司合成上述序列后,按说明书用te缓冲液溶解,溶解后的浓度为10μm,并按10μl每管分装到200μl的ep管中,置于-20℃保存备用。
用tris-hcl缓冲液分别将f链和f’链配成浓度为3.0μm的溶液;用tris-hcl缓冲液分别将q链和q’链配成浓度为4.5μm的溶液;用tris-hcl缓冲液分别将辅助链1和辅助链2配成浓度为5.0μm。
②将f链(2μl,3μm)和q链(2μl,4.5μm)的混合物加入到200μl的ep管中,震荡混匀然后放到pcr仪加热至95℃作用5分钟,然后在30分钟内缓慢冷却至室温制备第一底物;同理,通过将f’链(3μl4.5μm)和q’链(4μl4.5μm)加入到另一个200μl的ep管中,震荡混匀然后放到pcr仪加热至95℃作用5分钟,然后在30分钟内缓慢冷却至室温制备第二底物。将退火的第一底物和第二底物分别加入相应的辅助链1(2μl5μm)、辅助链2(4μl5μm),震荡混匀后在室温下温育30分钟。最后,将两个ep管中的反应液混合在一起,加入as1411-1,使其终浓度达到150nm,在室温下温育30分钟。将反应后的产物用聚丙烯酰胺凝胶电泳(page)进行表征dna树状纳米复合物组装,结果如图2所示,从page电泳图可以看出,加入了适配体-引发链(as1411-1)的第一底物的条带消失,出现具有低得多的迁移率的条带,表明第一底物装配成具有较高分子量的产物,进而表明dna纳米复合物能够自组装形成树状形态。而没加入as1411-1时,第一底物的条带没有消失,也没有出现具有低得多的迁移率的条带,表明dna链无法形成树状纳米复合物。
③通过将f链(2μl3μm)和q链(2μl4.5μm)的混合物加热至95℃并保持5分钟,并在30分钟内冷却至室温制备第一底物。同理,通过将f’链(3μl4.5μm)和q’链(4μl4.5μm)的混合物加热至95℃作用5分钟并在30分钟内冷却至室温制备第二底物。然后,将第一底物和第二底物分别与相应的辅助链1(2μl5μm)、辅助链2(4μl5μm)混合并在室温下温育30分钟。最后,将两者混合在一起并加入不同浓度(5nm,10nm,25nm,50nm,100nm,150nm)的as1411-1,在室温下温育30分钟。然后用荧光仪检测其荧光值,结果如图3所示,曲线方程为y=748.38-275.96lgx,r2=0.989。随着trigger浓度的增加,辅助链的荧光强度降低,并且成线性关系。
④特异性成像肿瘤细胞膜蛋白:将培养皿中处于指数生长期的mcf-7细胞、mda-mb-231细胞、mcf-10a细胞、16hbe细胞从孵箱中取出,用pbs缓冲液洗涤2次,然后用胰酶消化细胞,1000rpm离心3min,取一定数量的细胞并用结合液制备成细胞悬液。加入按照步骤②组装好的dna树状纳米复合物,置于设置好37℃的杂交仪的震荡1小时。然后1000rpm离心3min,弃掉上清液(游离的dna树状纳米复合物)。用pbs重复洗涤3次,确保没能结合上肿瘤细胞的dna树状纳米复合物被洗涤掉。最后,在倒置荧光显微镜下观察荧光,结果如图4所示,乳腺癌mcf-7、mda-mb-231细胞可以观察到荧光,而正常的乳腺上皮细胞mcf-10a细胞和支气管上皮细胞16hbe细胞几乎观察不到荧光,表明该方法能够特异性识别高表达核仁蛋白的肿瘤细胞。
⑤激光共聚焦显微镜成像肿瘤细胞:将24孔培养皿中处于指数生长期的mcf-7细胞、mda-mb-231细胞、mcf-10a细胞、16hbe细胞从孵箱中取出,用pbs缓冲液洗涤2次。加入1毫升的无血清培养基和按照步骤②组装好的dna树状纳米复合物,置于二氧化碳培养箱(37度,co2浓度为5%)继续培养3小时。然后弃掉培养基,用pbs洗涤2遍,在激光共聚焦显微镜下观察。
如图5所示为激光共聚焦显微镜成像肿瘤细胞图,高表达核仁素蛋白的mcf-7细胞和mda-mb-231细胞可以观察到有绿色荧光,而低表达或不表达核仁素的16hbe和不加适配体的mcf-7几乎观察不到绿色荧光,表明组装的dna树状纳米能够特异性识别高表达核仁蛋白的肿瘤细胞。
实施例2
将培养皿中处于指数生长期的mcf-7细胞从孵箱中取出,用pbs缓冲液洗涤2次,然后用胰酶消化细胞,1000rpm离心3min,取一定数量的细胞并用结合液制备成细胞悬液。加入适配体-引发链(as1411-1),置于设置好37℃的杂交仪中震荡1小时。然后1000rpm离心3min,弃掉上清液(游离的as1411-1)。用pbs重复洗涤3次,确保没能结合上肿瘤细胞的as1411-1被充分去除。将步骤②中第一底物与辅助链1反应、第二底物与辅助链2反应所得的反应液混合,形成未连接as1411-1的dna树状纳米复合物,然后将该dna树状纳米复合物加入前述结合有as1411-1的细胞液中,反应30min后,用荧光仪检测荧光,荧光强度值与肿瘤细胞上的膜蛋白成反比。
如图6所示为dna树状纳米复合物检测肿瘤细胞膜蛋白标准曲线图,曲线方程为y=748.38-275.96lgx;r2=0.989,最低检测限18个细胞,可见,本发明有效提高检测灵敏度。
综上所述,本发明基于适配体识别及催化dna探针自组装成树状纳米复合物,该复合物的组装合成方法简单、稳定性好,dna链在催化链存在下能够自组装成树状纳米复合物,而不需要苛刻的反应条件和贵重的仪器;dna树状纳米复合物检测肿瘤细胞表面膜蛋白含量的同时也能成像肿瘤细胞表面膜蛋白;通过利用适配体和催化链结合在一起能够特异性识别并主动靶向癌细胞膜蛋白和荧光成像;该dna树状纳米复合物是由dna链自组装而成,具有较低的生物毒性和免疫原性,利于其生物应用。
上述实施例仅例示性说明本发明的原理及其功效,而非用于限制本发明。任何熟悉此技术的人士皆可在不违背本发明的精神及范畴下,对上述实施例进行修饰或改变。因此,举凡所属技术领域中具有通常知识者在未脱离本发明所揭示的精神与技术思想下所完成的一切等效修饰或改变,仍应由本发明的权利要求所涵盖。
sequencelisting
<110>南方医科大学南方医院
<120>一种自组装树状纳米复合物及其应用
<130>pcqnf185685
<160>7
<170>patentinversion3.5
<210>1
<211>52
<212>dna
<213>artificial
<220>
<223>as1411-trigger
<400>1
ggtggtggtggttgtggtggtggtggttttgacgaactagttgatgaagctg52
<210>2
<211>69
<212>dna
<213>artificial
<220>
<223>fstrand
<400>2
gtgtgcctattatgtctcctcctgtgtgcctattatgtctcctcctcagcttcatcaact60
agttcgtca69
<210>3
<211>50
<212>dna
<213>artificial
<220>
<223>qstrand
<400>3
aactagttgatgaagctggacataataggcacacgacataataggcacac50
<210>4
<211>38
<212>dna
<213>artificial
<220>
<223>assistanta
<400>4
gtgtgcctattatgtcgtgtgcctattatgtccagctt38
<210>5
<211>46
<212>dna
<213>artificial
<220>
<223>f'strand
<400>5
aggaggagacataataggcacactgacgaactagttgatgaagctg46
<210>6
<211>34
<212>dna
<213>artificial
<220>
<223>q'strand
<400>6
cagcttcatcaactaggtgtgcctattatgtctc34
<210>7
<211>24
<212>dna
<213>artificial
<220>
<223>assistantb
<400>7
gcacacctagttgatgaagctgtg24
- 还没有人留言评论。精彩留言会获得点赞!
- 一种基于纳米材料自组装的土霉素sers检测方法
- 暴露高能晶面纳米片自组装的三维网络结构α?Fe<sub>2</sub>O<sub>3</sub>的制备方法
- 一种三氧化钨纳米带自组装成微纳米星的制备方法
- 一种葡萄糖和温度敏感性的自组装纳米粒子及其制备方法和应用
- 允许通过嵌段共聚物的自组装产生纳米结构体的方法
- 一种自组装纳米止血剂、其制备方法及应用
- 一种纳米片自组装棱台状(NH<sub>4</sub>)<sub>2</sub>V<sub>3</sub>O<sub>8</sub>的制备方法
- 一种干燥介导金纳米颗粒自组装制备金基底的方法及其应用
- 一种以杆菌肽为模板自组装合成球状金纳米粒子的方法
- 一种果胶-多臂聚乙二醇自组装制备纳米药物的方法
- 一种具有葡萄糖敏感性和温度敏感性的自组装纳米粒子及其制备方法
- 一种基于纳米材料自组装的土霉素sers检测方法
- 暴露高能晶面纳米片自组装的三维网络结构α?Fe<sub>2</sub>O<sub>3</sub>的制备方法
- 一种三氧化钨纳米带自组装成微纳米星的制备方法
- 一种葡萄糖和温度敏感性的自组装纳米粒子及其制备方法和应用
- 允许通过嵌段共聚物的自组装产生纳米结构体的方法
- 一种自组装纳米止血剂、其制备方法及应用
- 一种纳米片自组装棱台状(NH<sub>4</sub>)<sub>2</sub>V<sub>3</sub>O<sub>8</sub>的制备方法
- 一种干燥介导金纳米颗粒自组装制备金基底的方法及其应用
- 一种以杆菌肽为模板自组装合成球状金纳米粒子的方法