腮腺炎病毒荧光PCR检测试剂盒的制作方法
本发明涉及一种采用荧光pcr技术特异性检测样品中腮腺炎病毒核酸存在的试剂盒,属于腮腺炎病毒的体外诊断领域。
背景技术:
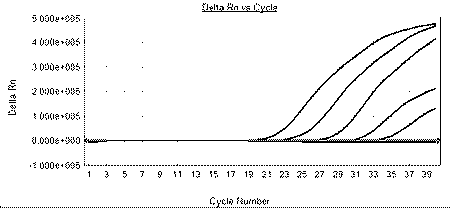
:腮腺炎病毒(mumpsvirus)是流行性腮腺炎的病原体,属副粘病毒科。腮腺炎病毒为球形,核衣壳呈螺旋对称,有包膜。包膜上有血凝素-神经氨酸酶刺突(hn)和融合因子刺突(f),基因组为单负链rna。腮腺炎病毒仅有一个血清型。抵抗力较弱,56℃30分钟可被灭活,对紫外线及脂溶剂敏感。人是腮腺炎病毒惟一宿主,病毒经飞沫传播,易感者为学龄期儿童,好发于冬春季节。本病潜伏期约2~3周,病毒侵入呼吸道上皮细胞和局部淋巴结内增殖后,进入血流,然后经血流侵入腮腺及其它腺体器官如睾丸、卵巢、胰腺、肾脏和中枢神经系统等。临床表现主要为一侧或双侧腮腺肿大,伴发热、乏力、肌肉疼痛等。病程1~2周,青春期感染者易并发睾丸炎(20%)或卵巢炎(5%),约0.1%的患儿可并发病毒性脑膜炎。并发睾丸炎者可导致男性不育症,腮腺炎也是导致儿童期获得性耳聋的常见原因。腮腺炎病后可获牢固的免疫力。在实验室检测中,pcr法由于其快速简便的特点逐渐呈现出要替代以细胞培养和血清学检测为主的传统检测方法的趋势。而对于pcr方法来说,引物的特异性是其检测的特异性和敏感性的基础。本发明针对腮腺炎病毒特异的靶序列设计引物和taqman探针,利用real-timert-pcr的方法,用来鉴别检测样品中腮腺炎病毒核酸,可以快速获得特异性检测结果。技术实现要素:本发明主要解决的技术问题是快速准确地检测样品中是否存在腮腺炎病毒,提供一种特异性检测腮腺炎病毒的荧光pcr试剂盒。本发明所要解决的技术问题是通过以下技术方案来实现的:一种特异性检测样品中腮腺炎病毒的试剂盒,组分包括pcr反应液、酶混合液、阴性质控品和阳性质控品。其中pcr反应液主要含有相关的引物和探针、反应缓冲液、mg2+和dntp等,酶混合液主要含有逆转录酶和热启动taq酶,阴性质控品为无rnase和dnase水,阳性质控品为含有腮腺炎病毒检测靶序列的rna。pcr反应液中用于核酸扩增的引物为p1和p2,p1和p2为针对腮腺炎病毒基因组群特异性保守序列设计并经预实验筛选出的特异性引物;pcr反应液中用于荧光信号监测的寡核苷酸探针为probe1,probe1为针对腮腺炎病毒基因组群特异性保守序列设计并经预实验筛选出的特异性探针,其中荧光报告基团x1为fam,荧光淬灭基团y1为eclipse(见表1)。表1检测腮腺炎病毒的引物和探针序列名称序列p15`-cataggrgayatgtggggaccaac-3`p25`-cagacccagcctcttgagttgaa-3`probe15`-x1-ccatgcaggcggtcacattccra-y1-3`本发明的另一个目的是提供本荧光pcr检测试剂盒在检测腮腺炎病毒的应用方法,包括:试剂盒选用的pcr反应体系为20µl,包括2×pcr缓冲液10µl、10mmol/ldntp1.0µl、25µmol/l引物各0.5µl、10µmol/l探针0.2µl、逆转录酶和热启动taq酶混合液0.8µl、样品rna2µl,加灭菌水至终体系20µl。试剂盒的pcr反应循环参数为逆转录阶段:42℃,10min;预变性阶段:94℃,10sec;预扩增阶段:变性94℃,5sec;退火50℃,20sec;延伸72℃,20sec;共5个循环。注意本阶段不采集荧光信号。检测阶段:变性94℃,5sec;退火56℃,50sec;延伸72℃,15sec;共40个循环。在退火步骤检测荧光信号。质量控制:每次实验应设立阴、阳性对照,阴性对照无ct值(或ct值为0),阳性对照ct值≤30,否则实验结果不成立。结果判读:阳性:出现“s”型扩增曲线,ct值≤35;可疑:出现“s”型扩增曲线,但ct值>35;阴性:没有出现“s”型扩增曲线,或者曲线虽然超过了阈值,但不呈“s”型;对可疑结果,应重复实验,如果重复实验还是出现“s”型扩增曲线,阴性对照没有污染,可判断为阳性。样本要求:临床样本类型包括咽拭子、漱口液和病毒分离物;临床样本采集后应带冰运输,-20℃保存,不能反复冻融;从临床样本提取rna,建议采用性能稳定可靠的商品化试剂盒,具体方法参见相应商品化试剂盒说明书,提取的rna应立即检测,否则,应将rna分装后-80℃~-20℃保存。本发明提供的试剂盒具有很好的特异性,可以检出腮腺炎病毒的核酸,但不能检出非腮腺炎病毒病原体的核酸;对腮腺炎病毒核酸的检测下限为10拷贝每反应体系;只需要2小时即可完成检测,可为腮腺炎病毒的疾病监测和临床诊断提供实验依据。附图说明图1为单重实时荧光pcr检测腮腺炎病毒核酸灵敏度的扩增曲线图。从左至右的5条曲线分别为腮腺炎病毒体外转录rna梯度稀释后(2×106-2×102copies/µl)扩增结果。横坐标为反应循环数,纵坐标为不同循环数荧光检测信号的△rn值。图2为单重实时荧光pcr检测体系对腮腺炎病毒核酸检测特异性扩增曲线图。腮腺炎病毒出现s型扩增曲线,而其他病原微生物质控毒株均未出现s型扩增曲线。横坐标为反应循环数,纵坐标为不同循环数荧光检测信号的△rn值。具体实施方式下面结合具体实施例详细说明本发明的优选实施方式。需要指出的是,这里列出的实施例仅仅为示例性说明的目的,而不应将其解释为对本发明范围的任何限制。其中使用的试剂盒、缓冲液等试剂仅仅为该具体实施例中具体选择的试剂,应理解,本领域技术人员可根据需要选择其他公司的相应试剂以实现本发明的目的。1、引物和taqman探针的设计与合成利用blast工具对genbank和国内外文献中所有的腮腺炎病毒基因组序列进行分析,分别选择其稳定的保守区域作为检测靶序列,并针对这检测靶序列设计和合成引物和探针(见表1)。引物和探针均由日本takara大连宝生物公司合成,其中腮腺炎病毒的检测探针5’端标记fam荧光基团,3’端标记eclipse荧光淬灭基团。2、检测菌种的准备本实施例中所使用的腮腺炎病毒以及其他阴性对照毒株(冠状病毒,腺病毒3型、7型,麻疹病毒,风疹病毒,流感病毒ah1n1、ah3n2、ah7n9,副流感病毒3型)均购买于中国药品生物制品检定所。3、菌株rna的抽提选用德国qiagen公司生产的核酸提取或纯化试剂qiaampdspvirusspinkit(国械备20140008qiagengmbh)提取毒株rna。具体步骤参考试剂盒操作说明书。4、引物和探针的筛选采用设计的引物和探针分别检测提取的腮腺炎病毒和阴性对照毒株的基因组rna,经反复实验,筛选出灵敏度、特异性和重复性最佳的引物探针组合(见序列表,腮腺炎病毒正向引物p1、反向引物p2和探针probe1)。5、标准品的构建与制备分别利用p1、p2引物,rt-pcr扩增腮腺炎病毒特异性基因片段,并克隆至含有t7启动子序列的质粒(如pgem-teasyvector),使用大连宝生物公司的rnapolymerase,合成rna,加入无rna酶的胰dna酶i以终止体外转录反应,通过用酚:氯仿抽提纯化rna。利用紫外可见分光光度计分别测定在波长260nm处、280nm处的吸光率,然后计算rna浓度与纯度,然后10倍梯度稀释至200拷贝每微升。6、反应条件优化对引物、探针、酶等要素逐一优化,确定的反应体系为:2×pcr缓冲液10µl、10mmol/ldntp1.0µl、25µmol/l引物各0.5µl、10µmol/l探针0.2µl、逆转录酶和热启动taq酶混合液0.8µl、模板2ul,加灭菌水至终体系20µl。根据扩增片段长短、引物和探针的退火温度以及酶的特性,主要对反应的退火温度和延伸时间进行了优化,最终确定循环参数为:逆转录阶段:42℃,10min;预变性阶段:94℃,10sec;预扩增阶段:变性94℃,5sec;退火50℃,20sec;延伸72℃,20sec;共5个循环。注意本阶段不采集荧光信号。检测阶段:变性94℃,5sec;退火56℃,50sec;延伸72℃,15sec;共40个循环。在退火步骤检测荧光信号。在扩增结束后按同一条件分析数据,确定各样品的ct值。7、检测限的评价以上述5中的阳性标准品评价本发明提供的试剂盒的检测限,阳性标准品浓度为:2×106copies/µl、2×105copies/µl、2×104copies/µl、2×103copies/µl、2×102copies/µl,本发明提供的试剂盒对腮腺炎病毒核酸的检测下限为10拷贝每反应体系。8、检测特异性的评价以上述2中的毒株rna为模板评价了本试剂盒的特异性。对腮腺炎病毒rna进行检测时均可见明确的扩增曲线,对上述9种其他呼吸道常见病原微生物rna检测时,未产生阳性扩增曲线,说明我们使用的探针和引物与我们选定的其他毒株之间不存在交叉反应。尽管上文中以优选的方式,通过具体实施例示例性说明了本发明的某些实施方式,但是本领域技术人员应了解,本发明并不限于上面所公开的实施方式,而是可以根据本发明所属
技术领域:
的知识对其进行修改,所作修改不会超出本发明要求保护的范围。例如,本发明所使用的荧光实时pcr也可以根据需要采用说明书中所列出的实施例中指出的荧光报告基团和荧光淬灭基团以外的标记物质,如tet、hex、tamra、rox、cy3、txrd、joe等标记物;或使用taqman技术之外的其他标记体系,例如mgb探针、分子信标mb探针、蝎形探针、荧光双杂交探针等荧光探针标记技术;或使用染料嵌合法如sybrgreeni等不饱和染料与lcgreen等饱和染料,只要其使用了本发明所述的特异性引物序列,即可定性或定量检测目的基因的存在,进而特异性地检测腮腺炎病毒的存在。所以,这些本领域技术人员所了解的改变和惯用手段的替换也落入本发明的保护范围内。本发明的保护范围应由所附的权利要求书所限定。序列表<110>江苏和创生物科技有限公司<120>腮腺炎病毒荧光pcr检测试剂盒<160>3<170>siposequencelisting1.0<210>1<211>24<212>dna/rna<213>腮腺炎病毒(mumpsvirus)<400>1cataggrgayatgtggggaccaac24<210>2<211>23<212>dna/rna<213>腮腺炎病毒(mumpsvirus)<400>2cagacccagcctcttgagttgaa23<210>3<211>23<212>dna/rna<213>腮腺炎病毒(mumpsvirus)<400>3ccatgcaggcggtcacattccra23当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1