一种S-亚硝基谷胱甘肽的制备方法与流程
本发明涉及一种s-亚硝基谷胱甘肽的制备方法,属于生物医药领域。
背景技术:
一氧化氮(nitricoxide,no)作为一种小分子活性物质,其在生物体的生理、生化、病理、和药理过程中扮演着重要的作用,no可以维持血管内环境的稳定和血压的稳定,临床上一氧化氮供体药物可以用来治疗心肌缺血和心力衰竭等心血管疾病,此外no对血小板和其他细胞之间的黏附有抑制作用,no也可以多方面的影响机体免疫系统,no具有抗炎作用,可以阻止白细胞的聚集,刺激粘液分泌,此外no还可以灭杀细菌、真菌及寄生虫等病原体。
s-亚硝基谷胱甘肽(s-nitrosoglutathione,gsno)是一种广泛存在于生物体内的小分子亚硝基硫醇化合物,是no最重要的供体之一。gsno是体内no的主要承载体,no与体内重要的抗氧化剂和自由基清除剂谷胱甘肽(glutatione,gsh)相结合形成gsno,可以起到储存no的作用。gsno在生物体内具有多种多样的生物学作用,既可以释放no,起到舒张血管、抗血小板凝集等作用;也可以通过转移no修饰细胞内的其他含硫基蛋白质,调控蛋白质的结构和功能;同时一定浓度的gsno对细菌和病毒都有杀伤作用。gsno作为谷胱甘肽亚硝基化的产物,已作为一种潜在的治疗药物引起广泛的关注。
目前,gsno的主要合成方式是利用谷胱甘肽(gsh)的亚硝化作用:将高浓度盐酸(通常2m或更高浓度)、高浓度金属亚硝酸盐(例如3-4m亚硝酸钠)和gsh水溶液混合搅拌;然后,加入大量丙酮继续搅拌,析出大量粉红色颗粒状gsno粗品,产品经过多次水洗和乙醚冲洗,以除去大部分的强酸和金属无机盐原料。该方法采用多种强酸为反应物,合成产物复杂,不易于直接利用,需使用有机溶剂,如采用丙酮对产物提纯、采用乙醚清洗产物,从而产生大量有机废液。
技术实现要素:
发明目的:针对现有的gsno合成方法存在的问题,本发明提供一种s-亚硝基谷胱甘肽的制备方法。
技术方案:本发明所述的一种s-亚硝基谷胱甘肽的制备方法,包括如下步骤:
(1)配制谷胱甘肽水溶液;
(2)将一氧化氮气体与空气或氧气的混合气体通入谷胱甘肽水溶液中,室温或冰浴条件下搅拌反应,得到s-亚硝基谷胱甘肽水溶液。
其中,配制的谷胱甘肽水溶液的浓度大于等于0.5mmol/l;相应的,单位时间内通入谷胱甘肽水溶液中的一氧化氮气体的浓度大于等于100ppm。上述浓度为no气体与谷胱甘肽水溶液反应能得到较好转化率的最低浓度。通入gsh溶液的no的浓度低于100ppm时,反应效率和转化率较低。单位时间内通入谷胱甘肽水溶液中一氧化氮气体的浓度是指每分钟通入谷胱甘肽水溶液中的no的平均气体浓度。
优选的,单位时间内通入谷胱甘肽水溶液中的一氧化氮气体浓度与谷胱甘肽水溶液的浓度之比大于等于1:140,此时,底物转化率可达90%以上。混合气体中空气或氧气的量不限,微量空气也可促进no与谷胱甘肽水溶液的反应。
谷胱甘肽水溶液可通过现有的发酵、化学合成、酶法合成等方式制得;优选采用经酵母菌发酵得到的谷胱甘肽溶解于水溶液,得到谷胱甘肽水溶液,发酵来源的原料可直接用于化妆品、保健品等终端产品。
较优的,步骤(2)中,在室温或冰浴条件下搅拌反应4~7h。冰浴条件为常规冰浴条件,即0~4℃的冰浴,室温或冰浴条件下反应,底物的转化率不同,冰浴条件下反应底物转化率更高。
该s-亚硝基谷胱甘肽的制备方法还可包括步骤(3),通过将步骤(2)制得的gsno水溶液冷冻干燥,可得到gsno固体。
有益效果:(1)本发明直接利用一氧化氮气体为原料,导入谷胱甘肽水溶液中,生成可直接用于终端用途的gsno水溶液和固体,反应底物转化率高,可达到99%以上,且反应液中gsno纯度较高;(2)本发明简化了制备工艺,反应物仅为一氧化氮气体和谷胱甘肽,不使用任何其它无机和有机试剂和原料,反应液为纯粹的gsno水溶液,不含其它金属离子和有机溶剂,该gsno水溶液可直接用于制备一氧化氮缓释产品,或通过冷冻干燥等方式得到gsno固体;(3)本发明合成条件温和,仅需在冰浴、常压下进行,合成过程中无需腐蚀性试剂,无固废和液废产生,符合绿色化学的理念。
附图说明
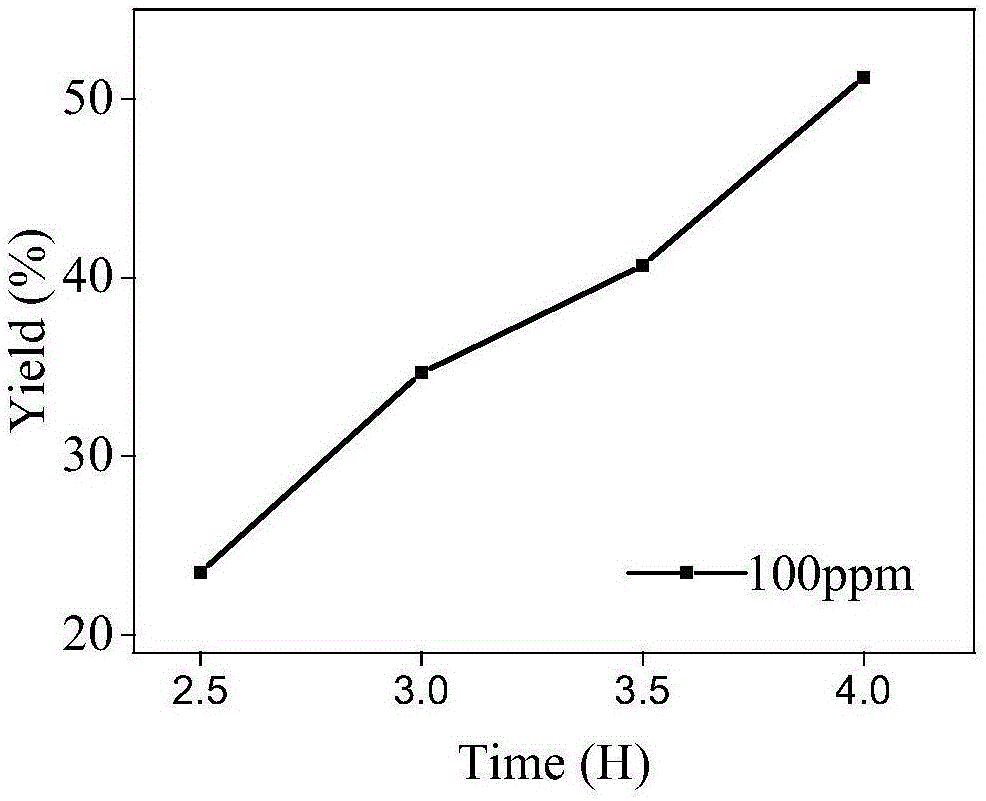
图1为实施例1制备gsno的反应转化率图;
图2为实施例1制得的gnso溶液的释放稳定性;
图3为实施例2制备gsno的反应转化率图;
图4为实施例3制备gsno的反应转化率图;
图5(a)和5(b)分别为实施例5中在室温和冰浴条件下gsh制备gsno的反应进程图及转化率图;
图6(a)和6(b)分别为实施例6中不同浓度gsh制备gsno的反应进程图及转化率图;
图7为实施例6制得的gnso溶液的保存稳定性。
具体实施方式
下面结合附图对本发明的技术方案作进一步说明。
下述实施例中,对s-亚硝基谷胱甘肽的定量测定方法如下,通过该定量测定方法确定底物的转化率。
分别称量s-亚硝基谷胱甘肽(gsno)16.8mg、8.4mg、4.2mg、2.1mg、1.05mg,溶解于1ml超纯水中,摇匀后得到浓度为50、25、12.5、6.25、3.125mmol/l的gsno水溶液,稀释80倍,用1~5分别编号不同浓度gsno水溶液,以水溶液做空白,在334nm处测定各ep管中溶液的吸光度值,如下表1。
表1不同浓度的gsno水溶液的紫外吸收值
根据表1中的数据,以gsno水溶液浓度为纵坐标,吸光度值为横坐标,绘制gsno水溶液浓度与吸光度值间数值关系的标准曲线。后续实施例中,可通过测定反应液的吸光度,从标准曲线计算得到反应液中gsno的浓度和含量。
下述实施例1-6中,“单位时间内通入谷胱甘肽水溶液中的no气体浓度”是指每分钟通入谷胱甘肽水溶液中的no的平均气体浓度。
实施例1
称量谷胱甘肽(gsh)1.54mg,溶解于10ml超纯水中,得到浓度为0.5mmol/l的gsh水溶液,使用no发生器作为no供体,气体流速10ml/min,将no与空气的混合气体通入至gsh水溶液中,单位时间内通入gsh水溶液中的no气体浓度为100ppm,常温条件下控制反应时间,经亚硝化和氧化还原反应,直接催化生成gsno水溶液。反应完成后,gsno水溶液于4℃中低温保存。
本实施例制备gsno的底物转化率如图1,可以看到,反应于4h后结束,底物转化率达51%;可见,较低浓度的谷胱甘肽水溶液及no也能制得gsno。
测试制得的gsno水溶液的释放稳定性。将4℃低温保存过夜后的10mlgsno水溶液分别置于日光灯、紫光灯下,控制空气流速0.7l/min,连接noa测量仪器,测试结果如图2,可以看到,gsno水溶液在正常日光灯和紫外灯下均能释放no,其中,在紫外光下可迅速分解释放no,10min内可达到最大释放浓度,释放效率相比正常日光灯下提高6倍。
实施例2
称量谷胱甘肽(gsh)1.54mg,溶解于10ml超纯水中,得到浓度为0.5mmol/l的gsh水溶液,使用no发生器作为no供体,气体流速10ml/min,将no与空气的混合气体通入至gsh水溶液中,单位时间内通入gsh水溶液中的no气体浓度为200ppm,常温条件下控制反应时间,经亚硝化和氧化还原反应,直接催化生成gsno水溶液。其中底物转化率70%,反应完成后,gsno水溶液于4℃中低温保存。
本实施例制备gsno的底物转化率如图3,可以看到,反应于5.5h后结束,底物转化率达70%。
实施例3
称量谷胱甘肽(gsh)1.54mg,溶解于10ml超纯水中,得到浓度为0.5mmol/l的gsh水溶液;使用亚硝酸钠作为no供体,混合空气,于密闭容器中混匀,气体流速20ml/min,将no与空气的混合气体通入至gsh水溶液中,单位时间内通入gsh水溶液中的no气体浓度为143ppm,即单位时间内通入的一氧化氮气体浓度与谷胱甘肽水溶液的浓度之比为1:140,在冰浴条件下反应6.5h,经亚硝化和氧化还原反应,直接催化生成gsno水溶液。反应完成后,gsno水溶液于4℃中低温保存。
本实施例制备gsno的底物转化率如图4,可以看到,反应于6.5h后结束,底物转化率达90%。
实施例4
称量谷胱甘肽(gsh)1.54mg,溶解于10ml超纯水中,得到浓度为0.5mmol/l的gsh水溶液;使用亚硝酸钠作为no供体,混合空气,于密闭容器中混匀,气体流速20ml/min,将no与空气的混合气体通入至gsh水溶液中,单位时间内通入gsh水溶液中的no气体浓度为200ppm,冰浴条件下经亚硝化和氧化还原反应,直接催化生成gsno水溶液。反应完成后,gsno水溶液于4℃中低温保存。反应结束后底物转化率达95%以上。
实施例5
称量谷胱甘肽(gsh)1.54mg,溶解于10ml超纯水中,得到浓度为0.5mmol/l的gsh水溶液;使用亚硝酸钠作为no供体,混合空气,于密闭容器中混匀,气体流速20ml/min,将no与空气的混合气体通入至gsh水溶液中,单位时间内通入gsh水溶液中的no气体浓度为143ppm,分别在冰浴和室温条件下反应5h,经亚硝化和氧化还原反应,直接催化生成gsno水溶液。反应完成后,gsno水溶液于4℃中低温保存。
反应进程及底物转化率分别如图5(a)和5(b)。可以看到,与室温条件反应相比,冰浴条件下底物谷胱甘肽浓的转化率大大提高,冰浴条件下底物转化率比室温条件高30%以上。
实施例6
分别称量谷胱甘肽(gsh)6.45g、9.22g、11.06g,溶解于300ml超纯水中,得到浓度分别为0.07、0.10、0.12mol/l的gsh水溶液;通过转子流量计分别控制no流速6ml/min,空气流速15ml/min,空气与no气体比例为2.5:1,于密闭容器中混匀,将no与空气的混合气体通入至gsh水溶液中,冰浴条件下,分别控制反应时间,经亚硝化和氧化还原反应,直接催化生成gsno水溶液;反应完成后,gsno水溶液于4℃中低温保存。
不同浓度gsh制备gsno的反应进程如图6(a),随着底物谷胱甘肽浓度增加,反应时间逐渐延长,分别于4h、6h和7h后反应结束。不同浓度gsh制备gsno的底物转化率如图6(b),可以看到,采用本发明的方法制备gsno水溶液,底物转化率可高达99%。
测量不同浓度gsh制备的gsno水溶液在4℃保存条件下的稳定性。如图7,gsno水溶液0.07mol/l,4℃保存24h,分解30%,gsno水溶液0.10mol/l,4℃保存24h,分解40%,gsno水溶液0.12mol/l,4℃保存24h,分解17%,有利于后期gsno水溶液的提纯、加工。
- 还没有人留言评论。精彩留言会获得点赞!