用于灌注应用的切向流过滤设备的制作方法
相关申请
本申请要求于2017年6月1日提交的美国临时申请号62/513,793的权益。上述申请的全部教导通过引用并入本文。
背景技术:
单克隆抗体(mabs)用作多种适应症的治疗剂,包括例如癌症、移植排斥和心血管疾病。存在多种用于从宿主细胞产生和收获mabs的生物制药技术,包括例如流加法(fed-batch)和灌注法。在流加式生物反应器系统中,在设定的时间段内分批培养细胞,例如约七至二十一天,在此之后宿主细胞消耗了培养基营养,并且积累了废物。在细胞培养期之后,该批料经历收获步骤,其中将目标蛋白质(例如产物,如单克隆抗体或mab)从细胞团中分离出来。与流加系统相比,灌注式生物反应器在更长的时间段内培养细胞,例如数周或数月,同时连续地向细胞提供新鲜培养基、去除用过的培养基并收获产品。灌注系统比流加系统具有多个优势。例如,在连续收获和纯化产品的过程中,在将目标蛋白质暴露于大量废物之前,在灌注系统中降低了产品降解。另外,灌注式生物反应器可以产生与流加式生物反应器相似的产物产量,同时占据明显较小的空间。由于灌注优于流加工艺,因此灌注正成为生物制药行业的优选制造技术。然而,灌注法依赖于在每个生产过程中维持高密度的宿主细胞以及连续的收获,这涉及多次重复过滤,并且可能对宿主细胞造成物理损害。
技术实现要素:
常规的灌注系统和方法使用具有开孔进料通道的过滤器元件,以避免可能对宿主细胞造成损伤的障碍物。然而,在这种常规系统和方法中使用的过滤器元件的寿命相对较短,由于膜结垢因此在低收获产量下显示出显著减少的筛分。提供了用于灌注系统和方法的过滤器元件,与现有的开孔通道和中空纤维设备相比,其显示出改善的mabs筛分和通过量。
在一个实施方案中,本发明包括一种过滤器元件片,其包括平均孔径为至少约0.65μm的微孔膜和包括编织纤维并且具有至少约35%的开孔面积的进料间隔件。
包括编织纤维并且具有至少约35%的开孔面积的进料间隔件可在过滤器元件的进料通道内提供低剪切速率,使得宿主细胞在过滤过程中不被损害。进料间隔件可以具有例如约35%至约55%的开孔面积,并且可以包括平均纤维直径为至少约270μm,例如约300μm至约500μm的纤维。进料间隔件的孔径可以为例如约0.8μm至约10μm,或约1.0μm至约5μm。进料隔离件的纤维密度可以为约6纤维/cm至约13纤维/cm。进料间隔件的纤维可以以二上一下(two-over-one)的斜纹图案或一上一下(one-over-one)的编织图案编织。
在另一实施方案中,本发明提供一种过滤器元件,其包括至少一个如本文所述的过滤器元件片。过滤器元件可以是螺旋卷式过滤器元件或盒式过滤器元件。
在另一实施方案中,本发明包括一种灌注系统,该灌注系统包括至少一个如本文所述的过滤器元件和配置为控制液体进料流动通过该至少一个过滤器元件的泵。
这样的灌注系统可以配置为以例如切向流过滤(tff)模式、再循环模式和/或交替流模式运行。该泵可以是例如磁悬浮泵、蠕动泵或隔膜泵。
在又一个实施方案中,本发明涉及一种灌注方法,其包括使液体进料通过至少一个过滤器元件的进料通道,并通过过滤器元件中的切向流过滤(tff)将所述液体进料分离为渗透物和截留物。过滤器元件包括微滤膜和位于进料通道内的编织进料间隔件。细胞和靶蛋白可以存在于液体进料中。
在进一步的实施方案中,本发明的灌注方法还可以包括回收渗透物中的靶蛋白和/或将细胞保留在截留物中。在一些实施方案中,至少一部分截留物可通过至少一个过滤器元件再循环。另外或可替代地,可以交替地使液体流过至少一个过滤器元件,以自清洁过滤器元件。该灌注方法还可包括将一定量的新鲜培养基供应至截留物并将截留物和新鲜培养基返回至生物反应器。该灌注方法可以连续运行,初始灌注运行的截留物是后续灌注运行的液体进料。
在另一个实施方案中,本发明提供了用于从含有宿主细胞的液体进料中收获靶蛋白的灌注方法。该方法包括将包含靶蛋白和宿主细胞的液体进料输送至至少一个过滤器元件的进料通道,并在该至少一个过滤器元件中将靶蛋白与宿主细胞分离。该至少一个过滤器元件包括微滤膜和位于进料通道内的编织进料间隔件。靶蛋白可以是例如单克隆抗体,其可以通过tff与宿主细胞分离并从该至少一个过滤器元件中回收。该灌注方法可以进一步包括从该至少一个过滤器元件回收宿主细胞,向回收的宿主细胞提供一定量的新鲜培养基,以及将回收的宿主细胞返回至生物反应器。该灌注方法可以连续运行,初始灌注运行的回收宿主细胞是后续灌注运行的液体进料。
与涉及开孔通道过滤设备的常规灌注方法相比,本发明的灌注方法可提供改进的筛分。在一些实施方案中,可以以至少约500l/m2过滤器元件的收获产量从液体进料中回收至少约80%,至少约90%或至少约95%的靶蛋白。在其他实施方案中,可以以至少约1000l/m2过滤器元件的收获产量从液体进料中回收至少约80%,至少约90%或至少约95%的靶蛋白。
附图说明
通过以下如附图所示的对本发明示例实施方案的更具体描述,上述内容将显而易见,在附图中,不同的视图中相似的附图标记指代相同的部分。附图不一定按比例绘制,而是将重点放在说明本发明的实施方案上。
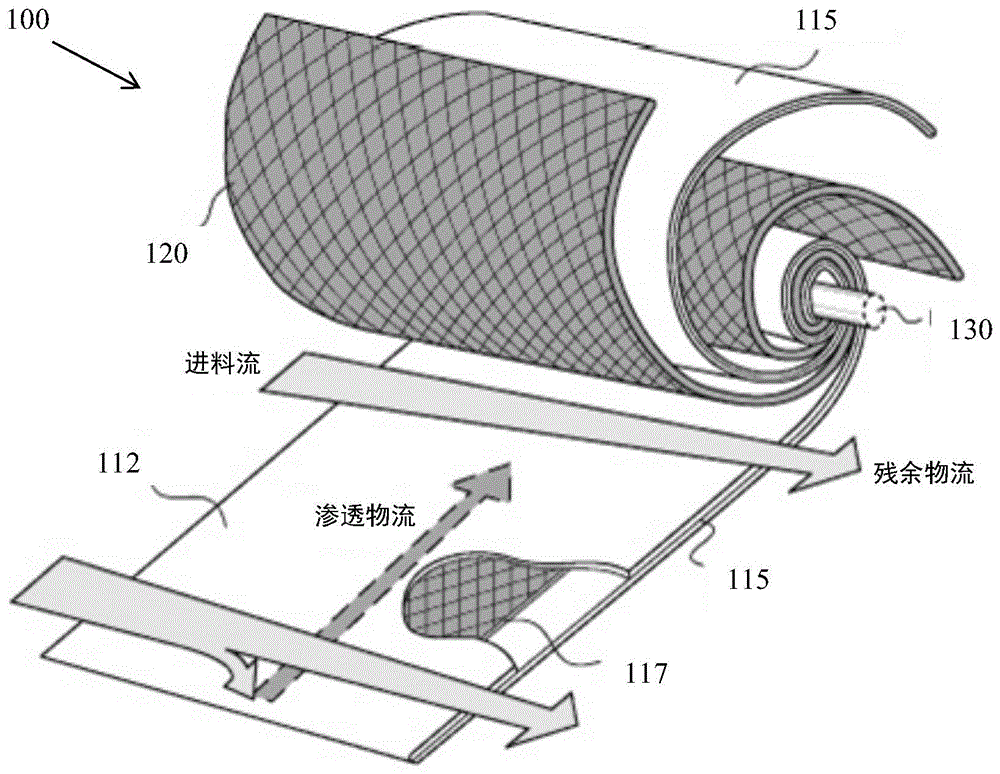
图1是示出螺旋卷式过滤器元件的示例的图。
图2是盒式过滤器元件的示例的分解图。
图3是示出tff系统的示例的示意图。
图4a是编织纤维进料间隔件的模拟图像。
图4b是图3a的编织纤维进料间隔件的三维图。
图4c是图4a的编织纤维进料间隔件的剪切建模结果的三维图。
图5是在具有编织纤维进料间隔件的环境中的模型剪切速率的图。
图6是编织纤维进料间隔件的模型结果和实验结果的表。
图7是切向流过滤设备的筛分对收获产量的实验结果的图。
图8a是在开孔通道过滤设备中膜结垢的实验结果的图。
图8b是在具有prostaktm超滤(uf)筛网的设备中膜结垢的实验结果的图。
图8c是在具有d3筛网的设备中膜结垢的实验结果的图。
图8d是在具有d筛网的设备中膜结垢的实验结果的图。
图9是具有1微米膜和d3筛网的切向流过滤设备的筛分对收获产量的实验结果的图。
图10是具有1微米膜和一上一下的编织筛网的切向流过滤设备的筛分对收获产量的实验结果的图。
具体实施方式
定义
除非另有定义,否则本文所用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常所理解的相同的含义。
如本文中所用,单数形式“一个”、“一种”和“该”包括复数,除非上下文另外明确指出。
表述“螺旋卷式过滤器元件”是指围绕芯螺旋缠绕的过滤膜。螺旋卷式过滤器元件可被包含在壳体内,并且可替代地被称为螺旋卷式过滤器模块。
“压降”是指在进料通道内在过滤器元件的整个长度上的压力下降(例如psid)。
“通量”是面积归一化的流速。
“渗透物通量”是渗透物通道中渗透物的面积归一化流速(例如升/小时/平方米,lmh)。
“错流通量”是进料通道中截留物的面积归一化平均流速(例如升/分钟/平方米,lmm)。
“错流”是过滤器或一系列过滤器中进料通道的入口和出口之间的截留物流速。除非另有说明,否则“错流”是指平均错流。
术语“剪切”是指通过压力产生的物质的结构中的应变。
术语“剪切速率”是指施加渐进剪切变形的速率(例如s-1)。
术语“进料”、“进料样品”和“进料流”是指引入到用于分离的过滤模块中的溶液。
术语“分离”通常是指将进料样品分成两股流,即渗透物流和截留物流的动作。
术语“渗透物”和“渗透物流”是指进料中已经渗透过膜的那部分。
术语“截留物”和“截留物流”是指溶液中已被膜截留的部分,截留物是富含截留物的流。
“进料通道”是指用于进料的过滤组件、模块或元件中的管道。
“渗透物通道”是指用于渗透物的过滤组件、模块或元件中的管道。
表述“流动路径”是指包括过滤膜(例如超滤膜、微滤膜)的通道,被过滤的溶液通过该通道(例如以切向流模式)。流动路径可以具有支持切向流动的任何拓扑结构(例如直线、盘绕、以之字形布置)。流动路径可以是开放的,例如在由中空纤维膜形成的通道的实施例中,或者具有一个或多个流动障碍物,例如在由编织或非织间隔件隔开的平片膜形成的矩形通道的情况下。
“tff组件”、“tff系统”和“tff设备”在本文中可互换使用,是指配置为以单程模式和/或再循环模式(例如全循环或部分再循环)和/或交替流动模式运行的切向流过滤系统。
“单叶”螺旋是螺旋卷式过滤器元件,其可以形成一个连续的进料通道。它们通常用一片膜制成。
“多叶”螺旋是具有多个进料通道的螺旋卷式过滤器元件。它们通常是用超过一片的膜制成;但也可以用1片膜制成。
“盒架”是指用于一个或多个盒的压缩组件。通常,当一个盒架容纳超过一个的盒时,这些盒被配置用于并行处理,不过在一些实施方案中,这些盒可以被配置用于串行处理。
“盒”是指盒或平板模块,其包括适合于tff工艺的过滤(例如超滤或微滤)膜片。
“过滤膜”是指能够在过滤系统例如tff系统中使用的选择性渗透的膜。
术语“微滤膜”和“mf膜”在本文中用于指具有约0.1微米至约10微米的孔径的膜。
“流体连接”是指多个螺旋卷式膜tff模块,它们通过用于液体的一个或多个管道如进料通道、截留物通道和/或渗透物通道彼此连接。
“产物”是指目标化合物。通常,产物将是目标生物分子(如蛋白质),例如单克隆抗体(mab)。
“处理”是指过滤(例如通过tff)含有目标产物的进料并随后回收该产物(例如以纯化形式)的行为。可以根据产物的尺寸和滤膜的孔径,在截留物流或渗透物流中从过滤系统(例如tff组件)回收产物。
表述“并行处理”、“并行的处理”、“并行操作”和“并行的操作”是指在包含多个处理单元的tff组件中处理产品,所述多个处理单元是通过直接将进料从进料通道或歧管分配到组件中的每个处理单元中而流体连接的。
表述“串行处理”、“串行的处理”、“串行操作”和“串行的操作”是指在包含多个处理单元的tff组件中处理产品,所述多个处理单元是通过直接将进料从进料通道仅分配到组件中的第一处理单元而流体连接的。在串行处理中,组件中的其他后续处理单元每个都从前一个处理单元的截留物线接收其进料(例如,来自第一处理单元的截留物用作第二相邻处理单元的进料)。
以下是本发明的示例实施方案的描述。
灌注系统中的切向流过滤
与流加系统相反,灌注系统和方法涉及细胞培养基的连续过滤。在过滤期间,从细胞培养基中除去靶蛋白如mab,以及任选地其他可溶性组分如细胞废物(例如乳酸和氨)。灌注系统(也称为细胞截留系统)相对于流加系统提出了独特的挑战,因为灌注系统中包含的细胞反复通过过滤设备,这可能会对细胞造成物理损害,进而减少系统的生产率。希望在灌注系统中的过滤过程中使细胞损伤最小化,以便保留尽可能多的细胞以持续生产靶蛋白。
切向流过滤(tff)是一种分离过程,该过程使用膜根据大小、分子量或其他差异来分离液体溶液或悬浮液中的组分。tff用于灌注方法,以从细胞培养基中去除目标蛋白,同时将细胞保留在培养基中。在tff过程中,将流体沿膜表面切向泵送,并且太大以至于无法通过膜的颗粒、分子或细胞将被拒绝并返回到处理槽中。tff过程可能涉及流体额外穿过膜(例如再循环),直到工艺流体被充分澄清、浓缩或纯化。tff的错流性质使膜结垢最小化,从而允许每批次大量的处理。膜包含在过滤器元件内,所述过滤器元件可以具有多种构造,例如螺旋卷式过滤器元件(图1)和盒式过滤器元件(图2)。
当前在灌注系统中使用的tff设备包括中空纤维设备和开孔通道的盒式设备,也称为板框设备。当前可用的用于灌注系统的过滤设备的实例包括xcelltmatf系统(repligen,waltham,ma)和
提供了用于灌注系统的过滤器元件,其与开孔通道设备相比,显示出改善的mab筛分和产量,同时使过滤期间的细胞损伤最小化。特别地,提供了包括开孔微孔膜和低剪切进料间隔件的组合的灌注过滤器元件片。开孔膜(例如孔径大于约0.65μm,大于约1.0μm或大于约3μm的膜)与低剪切进料间隔件的组合促进了进料通道中的混合,从而使结垢最小化,同时还保持膜和纤维表面的剪切速率在细胞稳定性极限之内。
在一个实施方案中,本发明包括一种灌注过滤器元件片,其包括微孔膜和编织纤维进料间隔件。所述微孔膜可具有至少约0.65μm(例如0.62μm、0.65μm、0.67μm、0.8μm),至少约1.0μm(例如0.95μm、1.0μm、1.2μm),或至少约3.0μm(例如2.9μm、3.0μm、5μm)的平均孔径。所述平均孔径可以为约0.8μm至约10μm(例如0.77μm、0.8μm、0.9μm、2μm、4μm、6μm、8μm、10.3μm),或约1.0μm至约5μm(例如0.97μm、1.2μm、3μm、5.3μm)。可以选择平均孔径以提供从细胞培养液中对靶蛋白和/或废料的筛分,同时将细胞保留在细胞培养液中。合适的微孔膜的实例包括下表1中列出的膜。
表1.微孔膜的实例。
进料间隔件可以包括以二上一下的斜纹图案或一上一下的编织图案编织的编织纤维。进料间隔件可具有至少约35%,或约35%至约55%(例如34.5%、35%、36%、39%、40%、50%、55%、55.5%)的开孔面积。进料间隔件的纤维密度可以为约6根纤维/cm至约13根纤维/cm(例如5.5根纤维/cm、6根纤维/cm、8根纤维/cm、10.6根纤维/cm、12.2根纤维/cm、13.5根纤维/cm)。进料间隔件纤维的平均纤维直径可以为至少约270μm(例如265μm、270μm、275μm),或约300μm至约500μm(例如290μm、300μm、400μm、500μm、510μm)。
合适的进料间隔件的实例包括具有二上一下的斜纹图案,开孔面积为36%,纤维密度为12.2根纤维/cm,纤维直径为340μm,厚度为610μm的d筛网(
在另一个实施方案中,本发明提供了一种过滤器元件,其包括如上所述的过滤片。该过滤器元件可以是螺旋卷式过滤器元件或盒式过滤器元件。
图1示出了螺旋卷式过滤器元件100的实例,其中箭头指示进料流动方向,并且箭头指示外膜115内的渗透物流动。外膜115包括折叠在任选存在的渗透物间隔件117上的膜112。螺旋卷式过滤器元件中可包括一个或多个外膜115。外膜115与进料间隔件120的外表面平面接触。外膜115和进料间隔件120围绕穿孔的渗透物收集管130缠绕。
在灌注方法中,将细胞培养基引入到膜112的进料侧。当液体进料(例如细胞培养基)穿过膜112的表面并透过到达进料间隔件120的周围时,它被分离为渗透物和截留物。具体地,靶蛋白穿过膜112,并通过收集管130从离开过滤器的渗透物中回收。细胞被保留并从离开过滤器的截留物中回收。然后可以将截留物中的细胞培养基返回到生物反应器中,并且可以将渗透物中包含的靶蛋白收集在单独的容器中进行进一步处理。
图2中示出了盒式过滤器20的实例。盒式过滤器20包括盒式过滤器元件28,该盒式过滤器元件具有至少一个进料板25和至少一个膜板27。进料板25可以包括编织纤维进料间隔件或部分由其形成。膜板27包括膜63。过滤器元件28位于歧管32和歧管34之间。歧管32包括进料入口12和截留物出口36。歧管34包括渗透物出口38和进料入口40。位于进料板和膜板25、27上的孔48、49被密封,其结构使得进入过滤器20(例如通过进料入口12、40)的液体进料沿箭头51、53、55和57表示的路径依次行进,并分离为渗透物和截留物。不穿过膜63的截留物行进到截留物管道44,并通过截留物出口36离开过滤器(如箭头67所示)。穿过膜63的渗透物然后沿箭头59、61和65表示的路径依次行进,穿过渗透物管道42,并通过渗透物出口38离开过滤器。
本发明的过滤器元件(例如螺旋卷式过滤器元件或盒式过滤器元件)相比灌注系统中使用的现有中空纤维和盒式设备,提供了多个优点。用于纯化单克隆抗体的常规过滤设备通常包括平均孔径为约0.2μm至约0.5μm的膜。相对比,本发明的实施方案中包括的微孔膜可以被认为是“开孔”微孔膜,其平均孔径为至少约0.65μm,例如至少约1.0μm或至少约3μm。本文实施例3和5的结果证明,与具有孔径为0.2μm或0.5μm的膜的常规过滤设备相比,开孔微孔膜提供了改进的筛分性能。随着膜孔径的增加,可能有更多的细胞碎片通过膜。如本发明的发明人所理解的,并且在不遵循任何特定理论的情况下,据信细胞碎片片段通过静电和疏水相互作用与蛋白质和dna发生相互作用,从而在常规灌注过滤设备中的膜表面上形成凝胶状层。这种相互作用增加了结垢并降低了具有“更紧密”膜(例如孔径为0.2μm或0.5μm的膜)的设备的筛分。另外,在现有的灌注设备中不包括进料筛网,因为筛网被认为对穿过过滤器的细胞施加不可接受的剪切应力,这在细胞截留系统中是不希望的。传统的过滤设备的筛分性能在操作过程中急剧下降,在收获产量仅为200l/m2或400l/m2之后,筛分降低到大约40%,如图7所示。如在实施例3和5中进一步描述的,本发明的示例性实施方案具有开孔微孔膜和编织纤维进料间隔片,能够在至少约500l/m2(例如膜孔径为约1μm)或至少约1000l/m2(例如膜孔径为约3μm或约5μm)的收获产量上实现约100%的筛分。因此,与现有的灌注过滤器相比,本发明的过滤器元件的实例在较长的操作周期内表现出改进的筛分。另外,本文实施例1-4的结果表明,具有至少约35%的开孔面积的编织纤维间隔片可以促进进料通道中的充分湍流以减少结垢,同时为通过进料通道的细胞产生可接受的剪切速率。
灌注系统
本发明的过滤器元件可以包括在灌注系统中。所述灌注系统可以包括tff系统,该tff系统具有一个或多于一个的本文所述的螺旋卷式过滤器元件或盒式过滤器元件。在具有多于一个的过滤器元件的系统中,过滤器元件可以串行或并行流体连接,或两者都有。
图3中示出了实例tff系统300。来自进料罐的加压进料连接到螺旋卷式过滤器模块的进料口或盒式过滤器的歧管。进料在施加的跨通道压降下流过tff设备的膜衬进料通道,所述跨通道压降通常通过使用泵对进料加压来实现。来自进料流的一些溶剂流过膜的表面进入渗透物通道,并带有一部分渗透性物质(例如靶蛋白、废产物)。剩余的浓缩进料流通过截留物端口流出模块或歧管。从模块的渗透物端口流出的渗透物被引导到一个取决于方法的位置,在该位置渗透物被收集(例如与目标蛋白一起)或被丢弃(例如与废产物一起)。
tff系统可以在再循环模式下操作,其中全部或部分截留物返回到过滤器元件进行进一步过滤。在灌注系统中,过滤后截留物可以返回到生物反应器中,在那里细胞培养基可以保留一段时间,然后再通过tff系统再循环。
含有用于再循环tff方法的过滤器元件的tff系统可以包括至少一个用于使截留物再循环通过系统的全部或一部分的泵或控制阀,以及至少一个用于再循环(例如携带)截留物的管道。再循环的截留物的量可以使用例如泵或阀来控制。流量计可用于为泵或阀提供过程值,以控制再循环的截留物的量。因此,在一些实施方案中,所描述的tff系统可以进一步包括用于控制截留物的再循环的阀或泵和/或流量计。阀或泵和/或流量计可以位于截留物出口上,也可以位于将截留物带出系统到截留物容器的流线上。可替代地或另外地,阀或泵和/或流量计可以位于渗透物出口上或位于将渗透物带出系统之外的流线中,以控制或限制渗透物流。
通过选择用于渗透物排放的适当的跨膜压力(tmp),可以获得tff系统运行期间可达到的最大通量。这适用于压力相关的和传质受限的操作区域。对于螺旋卷式过滤器,通过模块末端的测定来确定所需的tmp。对于具有例如两个渗透物出口的盒式过滤器,所需的tmp的获得通过平均进料通道压力来确定。跨膜压力必须足以支持通过膜的压降和从渗透物通道排出渗透物的最大压力。可替代地或另外地,通过选择用于渗透物排放的适当的渗透物流速,可以获得tff系统运行期间可达到的最大通量。可以通过使用渗透物阀或泵将渗透物流速控制为恒定值。对于灌注应用,可能需要将渗透物的流速保持在比不受控制的渗透物流更低的水平,并保持更稳定的流动。
tff系统也可以以交替流动模式运行。交替流动模式可以通过各种方法来实现。在第一种方法中,将泵例如隔膜泵连接到过滤器元件的截留物端口。进料被泵抽入到过滤器元件的进料口,并通过过滤器内的进料通道,从截留物端口出来,进入泵中。然后将泵倒转,并将液体介质(以前包含进料溶液)从泵中推出,通过过滤器元件的截留物侧进入进料通道,从过滤器的进料口出来,然后返回到生物反应器。在第二种方法中,泵交替地推动和抽吸液体介质通过过滤器元件。例如,通常将液体进料引入到过滤器元件的进料侧。进料通过泵(例如连接至过滤器元件进料口的泵)从生物反应器中被抽吸出,并通过进料口被推入到过滤器元件中。然后,液体介质穿过进料通道,离开截留物端口,回到生物反应器。然后,泵反转方向,将进料从生物反应器中抽吸出,通过截留物端口进入到过滤器元件中。然后,液体介质穿过进料通道,离开进料口,通过泵,然后从泵中推回到生物反应器中。在第三种方法中,可以通过使用泵和阀组以交替流动模式运行tff系统。在这种方法中,泵从生物反应器中连续抽吸液体介质流,并将介质推入到设备的进料通道中。通过泵后,使用阀改变进入过滤器的液体介质的流动方向。例如,液体介质流最初通过泵并进入过滤器的进料口。介质通过进料通道,并通过截留物端口离开过滤器,返回到生物反应器。一段时间后,阀切换位置,导致液体介质流从泵进入过滤器的截留物端口,通过进料通道,再通过进料口离开过滤器,然后返回到生物反应器。交替流动可产生过滤器膜反冲洗,以自清洁该膜并减少结垢。
如图3所示的进料泵可以被配置为以再循环模式和/或交替流动模式运行。进料泵可以是不会损坏细胞的泵,例如磁悬浮泵、隔膜泵、蠕动泵或回旋叶片式泵。合适的磁悬浮泵的实例包括
灌注方法
在一个实施方案中,本发明涉及一种使液体进料通过本发明的至少一个过滤器元件,将液体进料在过滤器元件中分离成渗透物和截留物;以及从过滤器元件中回收渗透物和至少一部分截留物的方法。所述液体进料可以包括细胞培养基,其含有细胞和靶蛋白。靶蛋白可以在渗透物中回收,细胞可以留在截留物中。
该方法可以包括使至少一部分截留物通过过滤器元件再循环。可以持续进行再循环,也可以定期进行再循环,以从细胞培养基中持续收获产物。
另外,在启动过程中再循环全部或部分截留物提供了一种方法,通过该方法确保系统达到平衡并且在将截留物收集到产品容器中之前,该截留物已经达到所需的浓度。它还提供了一种方便的方法以在处理过程中响应系统故障,从而提供了更强大的处理。可以通过调节泵或控制阀来调节截留物的再循环比例,作为调节系统的方式,以确保每次运行时到产品收集容器中有均匀的截留物浓度和/或恒定的渗透物流速,即使细胞浓度、新膜渗透性、膜结垢、膜渗透性或膜传质或压降因批次而异。这种策略在其中后续操作的成功取决于先前操作的产出的连续处理的情况下具有特别的优势。截留物的再循环可通过增加错流速度来提高清洁效果,并通过再循环减少清洁溶液。
正在再循环的截留物可以返回到tff系统中或之前的任何上游位置(例如位于tff系统上游的生物反应器)。在一个实施方案中,截留物再循环到进料罐。在另一个实施方案中,截留物再循环至tff系统上的进料入口之前的进料泵附近的进料管线。
在实施方案中,本文所述的方法包括进行灌注(例如以从生物反应器中去除蛋白质产物和细胞废物成分,以及向液体进料提供新鲜的培养基)。灌注是一种渗滤,其中进行连续的生物处理。当灌注细胞培养基经过定期过滤以除去目标蛋白和废物时,可以定期或连续重新补充新鲜培养基。在一个实施方案中,通过以与从tff系统中除去渗透物相同的速率将新鲜培养基添加到生物反应器中来进行灌注,该过程在本领域中被称为连续或恒定体积灌注。为了进行灌注或渗滤,tff系统可包括用于新鲜培养基或渗滤溶液的贮存器或容器,以及用于将新鲜培养基或渗滤溶液从新鲜培养基或渗滤溶液容器运送至生物反应器的一个或多个管道。
在另一个实施方案中,本文描述的方法还包括使液体交替流过过滤器元件。该方法可以包括使进料泵的方向反向,使得液体进料通过截留物侧进入过滤器并在一段时间内通过进料侧离开以反冲洗膜。流动方向可以例如大约每十二秒或更长时间反转一次。
在另一个实施方案中,本发明涉及用于从含有宿主细胞的液体进料中收获靶蛋白的灌注方法。该方法包括将含有靶蛋白和宿主细胞的液体进料递送至本发明的至少一个过滤器元件的进料通道,并在过滤器元件中将靶蛋白与宿主细胞分离。靶蛋白可以是单克隆抗体,其通过tff与宿主细胞分离并从过滤器元件的渗透物中回收。
如上所述,在本文的实施例4中,本发明的灌注方法相对于涉及使用开孔通道盒式过滤器元件和中空纤维过滤器元件的灌注方法具有多个优点。具体地,包括将含有宿主细胞的液体进料输送到包括开孔微孔膜和低剪切进料间隔件的过滤器的灌注方法提供了过滤器元件使用寿命的延长。如例如在图7中所示和本文的实施例4进一步描述的,与常规灌注方法相比,使用本发明的灌注方法可以在更长的时间段内从细胞培养溶液中回收更高量的靶蛋白。
在一些实施方案中,可以以至少约500l/m2,至少约800l/m2,或至少约1000l/m2过滤器元件的收获产量从细胞培养溶液中回收至少约80%,至少约90%或至少约95%的靶蛋白。
实施例
实施例1:进料间隔件筛网的建模
进行了建模研究以评价进料筛网参数对剪切速率的影响。使用autodeskinventor(autodesk,inc.boston,ma)中的参数几何功能,为模型生成了三个进料筛网中的每一个的几何形状。建模的进料筛网包括:(1)具有二上一下斜纹图案的c筛网(
然后将进料筛网的几何形状导入到comsol
表2.comsol模型条件
图4c示出了图4b的模型中进料通道中有6lmm错流通量时的速度大小。每个筛网在膜和纤维表面上的最大剪切速率均示于图5中。约3500s-1的剪切速率是中国仓鼠卵巢(cho)细胞可接受的极限,cho细胞是生产治疗性蛋白质如mab的主要宿主细胞类型。如图5所示,含有c筛网的灌注过滤器元件片的膜和纤维表面的剪切速率均在可接受的极限以上,这表明穿过包含此类片材的过滤器元件的cho细胞将经受不可接受的高剪切力。同样如图5所示,包含d筛网或d3筛网的灌注过滤器元件的剪切速率低于可接受的极限。
实施例2:模型结果与实验结果的比较
制造了两个原型过滤器元件,每个都包括以
实施例3:过滤器元件和泵的测试
评估了六个不同的细胞截留系统(即灌注系统),包括四个具有市售过滤器元件的系统和四个具有原型过滤器元件的系统。系统包括:
(1)具有隔膜泵和0.13m2、0.2微米pes中空纤维过滤器元件的xcelltmatf-2系统(repligen,waltham,ma)。该系统在推荐的错流速率下以交替流动模式运行。
(2)具有隔膜泵和0.13m2、0.5微米pes中空纤维过滤器元件的xcelltmatf-2系统。该系统在推荐的错流速率下以交替流动模式运行。
(3)磁悬浮泵
(4)蠕动泵(watsonmarlow)和具有0.06m2、0.22微米pvdf膜的prostaktm盒(milliporesigma,billerica,ma)。该系统在推荐的错流速率下以再循环模式运行。
(5)螺旋卷式过滤器元件,包括0.06m2、3微米径迹蚀刻膜(sterlitech)和d3进料间隔件(sefar),并带有蠕动泵(watsonmarlow)。该系统在推荐的错流速率下以再循环模式运行。
(6)螺旋卷式过滤器元件,包括0.06m2、3微米径迹蚀刻膜(sterlitech)和d3进料间隔件(sefar),并带有levitronix磁悬浮泵。该系统在推荐的错流速率下以再循环模式运行。
(7)螺旋卷式过滤器元件,包括0.06m2、3微米径迹蚀刻膜(sterlitech)和d3进料间隔件(sefar),并带有repligen隔膜泵。该系统在推荐的错流速率下以交替流动模式运行。
(8)螺旋卷式过滤器元件,包括0.06m2、5微米
所有系统都用包括cho细胞的进料进行了测试。特别地,将milliporesigma
结果在图7中示出。随着每个设备的膜面积变化,将每个设备的筛分性能绘制为设备产量(l/m2,处理量)的函数。如图7所示,系统(5)-(8)相对于系统(1)-(4)显示出作为产量函数的产品筛分的显著改善。另外,以交替流动模式运行的系统(8)显示出最高的产品筛分百分比。
实施例4:膜结垢测试
在milliporesigma开发的单层测试单元中,用0.65微米的
测试过滤器元件包括:
(1)开孔进料通道(不包括进料间隔件),
(2)prostaktm超滤(uf)筛网(66%的开孔面积,6.5根纤维/cm的纤维密度,326μm的纤维直径,590μm的厚度),
(3)d筛网,以及
(4)d3筛网。
所测得的测试过滤器元件的错流通量(lmh)显示在图8a-8d中。如图8a中所示,测试过滤器元件(1)显示出在整个膜表面上的最低通量值,表明在开孔通道设备中发生了最大量的膜结垢。如图8b-8d中所示,过滤器元件(3)和(4)显示出比过滤器元件(2)更高的通量值,表明d筛网和d3筛网都比更紧密编织的uf筛网更大程度地减少了膜表面上的颗粒积聚。
实施例5:1微米膜的建模/测试
用repligen隔膜泵测试了包括0.06m2、1微米
实施例6:一上一下编织进料筛网的建模/测试
一种螺旋卷式过滤器元件,包括0.06m2、1微米
结果在图10中示出。如图10所示,一上一下筛网显著改善了筛分到约500l/m2的通量。
本文引用的所有专利、公开的申请和参考文献的教导通过引用整体并入本文。
尽管已经参考本发明的示例实施方案具体示出并描述了本发明,但是本领域技术人员将理解,在不脱离由所附权利要求涵盖的本发明的范围的情况下,可以在形式和细节上进行各种改变。
- 还没有人留言评论。精彩留言会获得点赞!