制备吲哚萘并吡喃的方法与流程
本发明涉及光致变色化合物,如光致变色吲哚萘并吡喃化合物,以及用于由苯基萘酚合成中间体生产光致变色吲哚萘并吡喃化合物的高效方法。
背景技术:
光致变色化合物响应于电磁辐射(例如,“光化辐射”)的某些波长而经受从一种状态(或形式)至另一种状态的转变。各状态具有特征吸收光谱。例如,许多光致变色化合物在暴露于光化辐射时从未活化(例如,发白或基本上无色)状态转变至活化(例如,着色)状态。当去除光化辐射时,光致变色化合物可逆地从活化状态转变回到未活化状态。
先前在wo99/23071中描述了光致变色吲哚萘并吡喃化合物的合成。制备中的具体步骤使用下式a中所示的叠氮化物合成中间体,将其光化学分解以便获得式b中所示的相应的吲哚萘酚化合物。
吲哚萘酚化合物进一步反应形成吲哚萘并吡喃化合物。
这种合成路线具有几个缺点。这种光化学反应所需的uv光使此步骤难以大规模进行,因为反应速率受到反应物的uv光暴露的限制。此外,由于在室温和压力下来自叠氮化钠的水解的叠氮酸(爆炸性液体)的潜在释放,因此式a中所示的叠氮化物中间体的生产造成安全隐患。另外,有机叠氮化物化合物必须小心处理,因为它们可能对热和冲击敏感,并且可能爆炸性分解。因此,希望提供一种用于生产光致变色吲哚萘并吡喃化合物的方法,该方法可规模化并避免了叠氮化物中间体的制备。
本发明的苯基萘酚化合物提供了用于光致变色吲哚萘并吡喃化合物的制备的有用的合成中间体。本文披露的方法避免了与现有技术方法相关的问题,并提供了一种用于制备光致变色化合物的合成路线,该合成路线具有适合于各种取代基,具有良好产率的可规模化反应。
技术实现要素:
提供了一种苯基萘酚化合物,其包括由下式(i)表示的核心骨架结构,
其中m是0至4,n是0至4,r1和r2各自独立地是羟基、氰基、(甲基)丙烯酸酯、氨基、卤基、取代或未取代的烷基、硼酸酯、硼酸、聚醚、聚酯、聚碳酸酯、聚氨酯、取代或未取代的芳基、取代或未取代的杂环芳基、取代或未取代的杂芳基、取代或未取代的烷氧基、取代或未取代的芳氧基、取代或未取代的烷硫基、取代或未取代的芳硫基、酮、醛、酯、羧酸、羧酸酯、酰胺、碳酸酯、氨基甲酸酯、脲、硅氧烷、烷氧基硅烷、或聚硅氧烷,并且相邻碳原子上的两个r1基团和/或两个r2基团可以连接形成环;r3选自取代或未取代的2-吡啶基或取代或未取代的2-喹啉基;并且r4选自氢、取代或未取代的烷基、烷氧基甲基、取代或未取代的甲硅烷基、或酰基。
还提供了一种用于生产吲哚萘酚化合物的方法,该吲哚萘酚化合物包括由下式(ii)表示的核心骨架结构:
其中r1、r2和r4如以上所述,该方法包括在催化剂的存在下将式(i)中所示的苯基萘酚化合物环化。
在权利要求书中具体指出了表征本发明的特征,将其附在本披露内容中并使其构成本披露内容的一部分。从以下详细说明中将更全面地理解本发明的这些和其他特征、其操作优点以及通过其使用所获得的具体目的,在以下详细说明中展示并描述了本发明的非限制性实施例。
附图说明
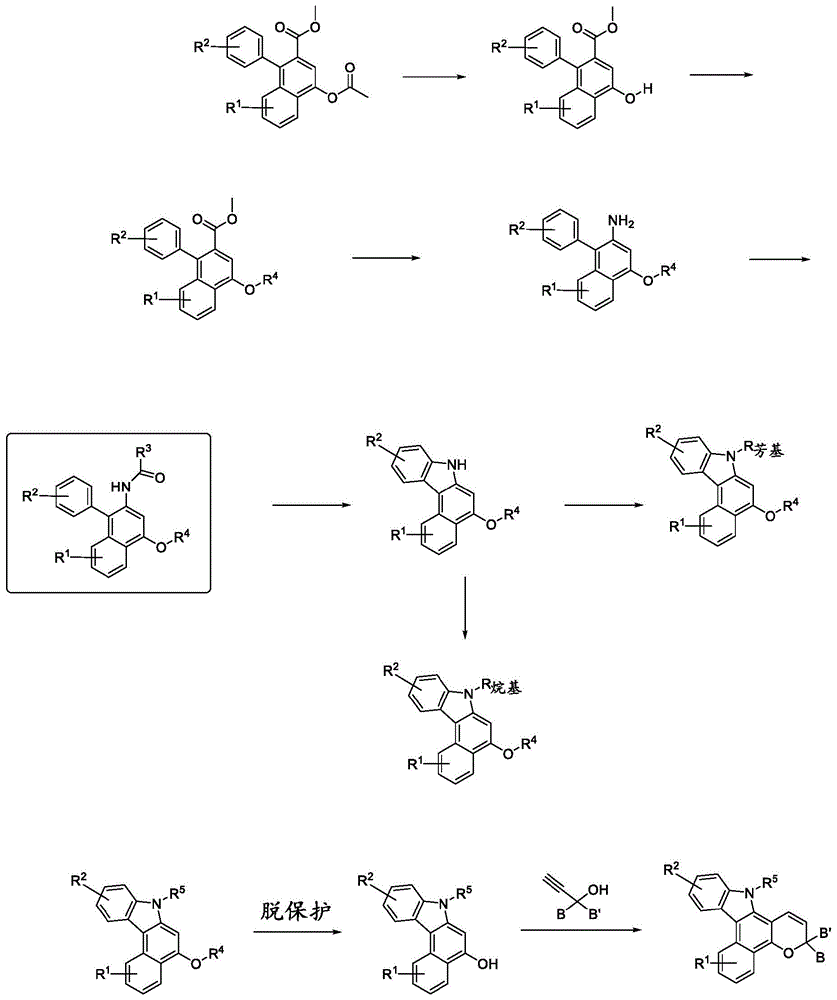
图1示出了本发明的用于制备光致变色吲哚萘并吡喃化合物的示例性方法的通用方案,方案1。
具体实施方式
如本文所使用的,冠词“一个/种(a/an)”、以及“所述(the)”包括复数指示物,除非另有清楚地且明确地限于一个指示物。
如本文所使用的,术语“包括(includes)”与“包含/包括(comprises)”同义。
除非另有指明,否则本文所披露的所有范围或比率应理解为涵盖其中所包含的任何和所有子范围或子比率。例如,叙述的范围或比率“1至10”应视为包括在最小值1与最大值10之间(并且包含端点)的任何和所有子范围;即,以最小值1或更大值开始并且以最大值10或更小值结束的所有子范围或子比率,诸如但不限于,1至6.1、3.5至7.8、以及5.5至10。
如本文所使用的,除非另有指明,连接基团(诸如二价连接基团)的从左至右表示包括其他合适的取向,诸如但不限于从右至左取向。出于非限制性说明的目的,二价连接基团
除了在操作实例中、或在另有指明的情况下,在说明书和权利要求书中所使用的表示成分、反应条件等的量的所有数字应理解为在所有情况下由术语“约(about)”修饰。“约”意指所述值的正或负百分之二十五,诸如所述值的正或负百分之十。然而,不应将其视为对等效原则下的值的任何分析的限制。
如本文所使用的,聚合物的分子量值,诸如重均分子量(mw)和数均分子量(mn)通过凝胶渗透色谱法使用合适的标准物(诸如聚苯乙烯标准物)来确定。
如本文所使用的,术语“聚合物”意指均聚物(例如,由单一单体种类所制备的)、共聚物(例如,由至少两种单体种类所制备的)、以及接枝聚合物。
如本文所使用的,术语“(甲基)丙烯酸酯((meth)acrylate)”和类似术语,诸如“(甲基)丙烯酸酯((meth)acrylicacidester)”,意指丙烯酸和甲基丙烯酸的衍生物,包括丙烯酸酯类、甲基丙烯酸酯类、丙烯酰胺类、甲基丙烯酰胺类、丙烯酸和甲基丙烯酸。如本文所使用的,术语“(甲基)丙烯酸((meth)acrylicacid)”意指甲基丙烯酸和/或丙烯酸。
对于一些实施例,本发明的光致变色化合物在本文中也称为光致变色-二向色性化合物(如,当它们包括一个或多个含介晶的基团时)。
本发明的化合物,如本文所述,包括但不限于由式(i)、式(ii)、式(iii)和式(iv)表示的光致变色化合物,在每种情况下可任选地进一步包括一种或多种由此类化合物的合成产生的副产物。
如本文所使用的,术语“光致变色(的)(photochromic)”和类似术语(如“光致变色化合物”意指具有响应于至少光化辐射的吸收而变化的至少可见辐射的吸收光谱。进一步地,如本文所使用的,术语“光致变色材料”意指适于显示光致变色特性(诸如适于具有响应于至少光化辐射的吸收而变化的至少可见辐射的吸收光谱)并且包括至少一种光致变色化合物的任何物质。
如本文所使用的,术语“光化辐射”意指能够在材料中引起响应的电磁辐射,诸如但不限于将光致变色材料从一种形式或状态转变至另一种形式或状态,如本文将进一步详细讨论的。
如本文所使用的,术语“二向色性”意指能够比另一种更强地吸收至少透过辐射的两种正交平面偏振分量中的一种。
如本文所使用的,术语“光致变色-二向色性”和类似术语(诸如“光致变色-二向色性化合物”)意指拥有和/或提供光致变色特性(即,具有响应于至少光化辐射而变化的至少可见辐射的吸收光谱)和二向色性特性(即,能够比另一种更强地吸收至少透过辐射的两种正交平面偏振分量中的一种)两者。
如本文所使用的,并且除非另有说明或另有限制,术语“光致变色材料”包括热可逆光致变色材料和化合物以及非热可逆光致变色材料和化合物。如本文所使用的术语“热可逆光致变色化合物/材料”意指能够响应于光化辐射从第一状态(例如“透明状态”)转换至第二状态(例如“着色状态”)、并且响应于热能返回至第一状态的化合物/材料。如本文所使用的术语“非热可逆光致变色化合物/材料”意指能够响应于光化辐射从第一状态(例如“透明状态”)转换至第二状态(例如“着色状态”)、并且响应于与着色状态的吸收基本上相同波长的光化辐射(例如,停止暴露于此光化辐射)返回至第一状态的化合物/材料。
如本文所使用的,为了修饰术语“状态”,术语“第一”和“第二”不旨在指任何特定顺序或时间顺序,而是指两种不同的条件或特性。出于非限制性说明的目的,光致变色化合物的第一状态和第二状态可以在至少一种光学特性方面不同,诸如但不限于可见辐射和/或uv辐射的吸收。因此,根据本文所披露的各种非限制性实施例,本发明的光致变色化合物可以在第一和第二状态中的每一个中具有不同的吸收光谱。例如,虽然本文没有限制,本发明的光致变色化合物可以在第一状态下是透明的并且在第二状态下是着色的。替代性地,本发明的光致变色化合物可以在第一状态下具有第一颜色并且在第二状态下具有第二颜色。
如本文所使用的,术语“光学(的)(optical)”意指涉及光和/或视觉或者与光和/或视觉相关。例如,根据本文所披露的各种非限制性实施例,光学制品或元件或器件可以选自眼科制品、元件和器件;显示制品、元件和器件;窗;镜;或有源和无源液晶盒制品、元件和器件。
如本文所使用的,术语“眼科(的)(ophthalmic)”意指涉及眼睛和视觉或者与眼睛和视觉相关。眼科制品或元件的非限制性实例包括矫正和非矫正镜片(其包括单视或多视镜片,多视镜片可以是分段的或非分段的多视镜片(诸如但不限于双焦镜片、三焦镜片和渐进镜片)、以及用于矫正、保护或增强(美容或其他)视觉的其他元件(其包括但不限于接触镜片、眼内镜片、放大镜片、以及保护性镜片或护目镜)。
如本文所使用的,术语“显示(display)”意指呈字、数字、符号、设计或图的信息的可见的或机器可读的表示。显示元件的非限制性实例包括屏幕、监视器、以及安全元件,诸如安全标记。
如本文所使用的,术语“窗(window)”意指适于允许辐射透射穿过那里的孔。窗的非限制性实例包括汽车和飞机的透明体、挡风玻璃、滤光片、遮光器、以及光学开关。
如本文所使用的,术语“镜(mirror)”意指镜面反射很大部分的入射光的表面。
如本文所使用的,术语“液晶盒(liquidcrystalcell)”是指含有能够被有序化的液晶材料的结构。液晶盒元件的非限制性实例是液晶显示器。
如本文所使用的,术语“形成在…上/在…上形成(formedover)”、“沉积在…上/在…上沉积(depositedover)”、“提供在…上/在…上提供(providedover)”、“施用在…上/在…上施用(appliedover)”、“驻留在…上/在…上驻留(residingover)”或“定位在…上/在…上定位(positionedover)”意指形成、沉积、提供、施用、驻留或定位在上面、但不必然与下面的元件、或下面的元件的表面直接(或邻接)接触。例如,“定位在基底上(positionedover)”的层不排除位于所定位或形成的层与基底之间存在相同或不同组成的一个或多个其他层、涂层、或膜。
如本文所使用的,涉及环位置(诸如但不限于位置-x(例如,位置-3或位置-13)的叙述意指化学化合物(诸如本发明的吲哚萘并吡喃光致变色化合物)在环结构(诸如核心骨架结构)中的特定位置,并且其在本文根据一些实施例通过代表性化学式(诸如但不限于式(i)和/或(ia))的环结构内的数字描绘。
“核心骨架结构”意指至少包含相关式中所描绘的骨架结构的化合物。出于识别经编号的环位置的目的提供核心骨架结构。然而,应理解的是,除非明确地相反示出,否则一种或多种核心骨架结构可以具有键合至核心骨架结构上的一个或多个经编号的环位置的一个或多个原子或一个或多个基团(在相应的式中未具体展示),该一个或多个原子或一个或多个基团可以彼此相同或不同。
关于术语“核心骨架结构”在本文中涉及本发明的光致变色化合物,该术语可以由一个或多个式表示,如但不限于式(i)、(ii)、(iii)和/或(iv)。
本文所涉及、并且除非另有指明,所有文献或部分文献(诸如但不限于公布的专利和专利申请)均视为“通过援引以其全文并入”。
“芳基”是指芳族环状单价烃基,并且术语“芳族”是指具有稳定性(由于离域)显著大于假定的定域结构的稳定性的环状共轭烃。芳基的实例包括c6-c14芳基,诸如但不限于苯基、萘基、菲基、以及蒽基。
如本文所使用的,“卤代(的)”和相关术语(诸如但不限于卤代烷基、卤代烯基、卤代炔基、卤代芳基和卤代杂芳基)的叙述意指其中其至少一个、且至多且包括所有可用氢基团被卤素基团取代的基团。术语“卤代(的)”包括“全卤代(的)”。如本文所使用的,术语全卤代基团和相关术语(诸如但不限于全卤代烷基、全卤代烯基、全卤代炔基、全卤代芳基或全卤代杂芳基)意指其中其所有可用氢基团被卤素基团取代的基团。例如,全卤代甲基是-cx3;全卤代苯基是-c6x5,其中x表示一个或多个卤代基团,诸如但不限于f、cl或br。
如本文所使用的,“直链或支链(的)”基团(诸如直链或支链烷基)的叙述在本文被理解为包括:直链(或“直链(straightchain)”)基团,诸如直链c1-c25烷基;以及适当支化的基团,诸如支链c3-c25烷基。
本文所使用的术语“烷基”意指直链或支链的、环状或非环状的c1-c25烷基。直链或支链烷基可以包括c1-c25烷基,诸如c1-c20烷基,诸如c2-c10烷基,诸如c1-c12烷基,诸如c1-c6烷基。本发明的各种烷基可以选自其的烷基的实例包括但不限于本文进一步列举的那些。烷基可以包括“环烷基”基团。本文所使用的术语“环烷基”意指适当环状的基团,诸如但不限于c3-c12环烷基(包括但不限于环状c5-c7烷基、或环状c3-c10烷基)基团。环烷基的实例包括但不限于本文进一步列举的那些。本文所使用的术语“环烷基”还包括:桥环多环烷基(polycycloalkyl)基团(或桥环多环(polycyclic)烷基),诸如但不限于双环[2.2.1]庚基(或降冰片基)和双环[2.2.2]辛基;以及稠环多环烷基(polycycloalkyl)基团(或稠环多环(polycyclic)烷基),诸如但不限于八氢-1h-茚基、以及十氢萘基。
本文所使用的术语“杂环烷基”意指适当环状的基团,诸如但不限于c2-c12杂环烷基,诸如c5-c7杂环烷基、诸如c2-c10杂环烷基,并且其在环状环中具有至少一个杂原子,诸如但不限于o、s、n、p、以及它们的组合。杂环烷基的实例包括但不限于咪唑基、四氢呋喃基、四氢吡喃基和哌啶基。本文所使用的术语“杂环烷基”还包括:桥环多环杂环烷基,诸如但不限于7-氧杂双环[2.2.1]庚烷基;以及稠环多环杂环烷基,诸如但不限于八氢环戊并[b]吡喃基和八氢-1h-异色烯基。
如本文所使用的,术语“杂芳基”包括但不限于c3-c18杂芳基,诸如但不限于c3-c10杂芳基(包括稠环多环杂芳基)并且意指在芳族环中或在稠环多环杂芳基的情况下在至少一个芳族环中具有至少一个杂原子的芳基。杂芳基的实例包括但不限于呋喃基、吡喃基、吡啶基、异喹啉、以及嘧啶基。
如本文所使用的,术语“稠环多环-芳基-烷基”和类似术语(诸如稠环多环-烷基-芳基、稠环多环-芳基-烷基、以及稠环多环-烷基-芳基)意指包括稠合在一起以形成稠环结构的至少一个芳基环和至少一个环烷基环的稠环多环基团。出于非限制性说明的目的,稠环多环-芳基-烷基的实例包括但不限于茚基、9h-芴基、环戊并萘次甲基(cyclopentanaphthenyl)、以及引达省基(indacenyl)。
如本文所使用的术语“芳烷基”包括但不限于c6-c24芳烷基,诸如但不限于c6-c10芳烷基,并且意指被芳基取代的烷基。芳烷基的实例包括但不限于苄基和苯乙基。
代表性的烷基包括但不限于甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、新戊基、己基、庚基、辛基、壬基和癸基。代表性烯基包括但不限于乙烯基、烯丙基和丙烯基。代表性炔基包括但不限于乙炔基、1-丙炔基、2-丙炔基、1-丁炔基、以及2-丁炔基。代表性环烷基包括但不限于环丙基、环丁基、环戊基、环己基、以及环辛基取代基。代表性杂环烷基包括但不限于咪唑基、四氢呋喃基、四氢吡喃基和哌啶基。代表性芳基包括但不限于苯基、萘基、蒽基、菲基、以及并四苯基(包括它们的结构性异构体)。代表性杂芳基包括但不限于呋喃基、吡喃基、吡啶基、异喹啉基、以及嘧啶基。代表性芳烷基包括但不限于苄基和苯乙基。
如本文所使用的,术语“含氮杂环”包括但不限于含氮环,其中含氮环通过环氮键合。含氮杂环的实例包括但不限于环氨基类,诸如吗啉代、哌啶子基、以及吡咯烷子基;以及杂芳族化合物,诸如咪唑、吡咯、吲哚、以及咔唑。
如本文所使用的,术语“酰基”包括但不限于具有式raco-的烷酰基或芳酰基,其中ra表示取代或未取代的烷基或取代或未取代的芳基。
如本文所使用的,术语“聚硅氧烷”(诸如关于本发明的光致变色化合物的各种基团的取代基)包括由以下式(g)表示的材料:
关于式(g),在每种情况下,下标t’是从2至200,诸如从2至100、或2至50、或从2至25、或从2至15、或从2至10、或从2至5,包括所述值。进一步关于以下式(g):对于各t’,r32和r33各自独立地选自烷基或芳基;并且r34选自氢、烷基、或芳基。在一些实施例中:对于各t’,r32和r33各自独立地选自甲基、乙基、或苯基;并且r34选自氢、甲基、乙基、或苯基。
如本文所使用的,术语“聚硅氧烷”,如关于本发明的光致变色化合物的不同基团的取代基,替代于由式(g)表示的物质或除其以外,包括由下式(h)表示的材料:
关于式(h),下标u’是0-2并且下标x’是1-3,前提是u’+x’是3;并且下标v’是0-2并且下标w’是1-3,前提是v’+w’是3。进一步关于式(h),在各情况下,对于各u’,r35独立地、对于各v’和各x’,r36独立地、以及对于各w’和各x’,各r37独立地选自烷基(诸如但不限于甲基或乙基)或芳基(诸如但不限于苯基)。
如本文所使用的,“取代”基团的叙述意指包括但不限于以下的基团:烷基、杂环烷基、芳基和/或杂芳基,其中其至少一个氢已被除氢以外的基团(如但不限于烷氧基)替代或取代;卤素基团(例如,f、cl、i、以及br);羟基;硫醇基团;烷硫基;芳硫基;酮基团;醛基团;酯基团;羧酸基团;磷酸基团;磷酸酯基团;磺酸基团;磺酸酯基团;硝基;氰基;烷基(包括芳烷基);烯基;炔基;卤代烷基;全卤代烷基;杂环烷基;芳基(包括烷芳基,包括羟基取代的芳基,诸如苯酚,并且包括多稠环芳基);杂芳基(包括多稠环杂芳基);氨基,诸如-n(r11’)(r12’),其中r11’和r12’各自独立地选自例如氢、烷基、杂环烷基、芳基、或杂芳基;羧酸酯基团;硅氧烷基团;烷氧基硅烷基团;聚硅氧烷基团;酰胺基团;氨基甲酸酯基团;碳酸酯基团;脲基团;聚酯基团;聚醚基团;聚碳酸酯基团;聚氨酯基团;丙烯酸酯基团;甲基丙烯酸酯基团;含氮杂环化合物;或它们的组合,包括如本文进一步描述的那些类别和实例。
如本文所使用的,术语“苯基萘酚”和“吲哚萘酚”包括受保护的苯基萘酚和吲哚萘酚化合物,以及苯基萘酚和吲哚萘酚衍生物。
如本文所使用的,“…中的至少一个/种”与“…中的一个/种或多个/种”同义,无论要素是结合地列出还是分离地列出。例如,短语“a、b、以及c中的至少一个/种”和“a、b、或c中的至少一个/种”各自意指a、b、或c中的任意一个/种,或者a、b、或c中的任意两个/种或更多个/种的任意组合。例如,单独的a;或单独的b;或单独的c;或a和b;或a和c;或b和c;或全部的a、b、以及c。
如本文所使用的,“选自(selectedfrom)”与“选自(chosenfrom)”同义,无论要素是结合地列出还是分离地列出。例如,短语“选自a、b和c”和“选自a、b或c”各自意指a、b或c中的任一个,或a、b或c中任意两个或更多个的任意组合。例如,单独的a;或单独的b;或单独的c;或a和b;或a和c;或b和c;或全部的a、b、以及c。
本发明的讨论可以将某些特征描述为“特别地”或“优选地”在某些限制内(例如,“优选地”、“更优选地”、或“甚至更优选地”在某些限制内)。应理解的是,本发明不限于这些特定或优选的限制,而是涵盖本披露的整个范围。
本发明包括、或基本上由本发明的以下方面以任何组合组成。
根据本发明的化合物可以由以下所述的核心骨架结构中的一种或多种表示。
关于式(i),r1和r2各自独立地是羟基、氰基、(甲基)丙烯酸酯、氨基、卤基(如氟、氯、溴或碘)、取代或未取代的烷基、硼酸酯或硼酸、聚醚、聚酯、聚碳酸酯、聚氨酯、取代或未取代的芳基、取代或未取代的杂环烷基、取代或未取代的杂芳基、取代或未取代的烷氧基、取代或未取代的芳氧基、取代或未取代的烷硫基、取代或未取代的芳硫基、酮、醛、酯、羧酸、羧酸酯、酰胺、碳酸酯、氨基甲酸酯、脲、硅氧烷、烷氧基硅烷、或聚硅氧烷。相邻碳原子上的两个r1基团或两个r2基团可以连接形成环。r3选自取代或未取代的2-吡啶基或取代或未取代的2-喹啉基。取代的2-吡啶基和取代的2-喹啉基的取代基各自独立地选自取代或未取代的烷基、取代或未取代的烷氧基、取代或未取代的芳氧基、取代或未取代的芳基、取代或未取代的杂芳基、卤素、氨基、酯、羧酸酯、或羟基。r4选自氢、取代或未取代的烷基、烷氧基甲基、取代或未取代的甲硅烷基、或酰基。
从其中可以选择r1的基团的实例包括但不限于卤基(如氟)、取代或未取代的烷基(如甲基)、取代或未取代的杂芳基、取代或未取代的烷氧基(如甲氧基)、取代或未取代的烷硫基、或取代或未取代的芳硫基。从其中可以选择r2的基团的实例包括但不限于卤基(如氟)、取代或未取代的烷基(如甲基或三氟甲基)、取代或未取代的杂芳基、取代或未取代的烷氧基、取代或未取代的烷硫基、或取代或未取代的芳硫基。从其中可以选择r3的基团的实例包括但不限于2-吡啶基。从其中可以选择r4的基团的实例包括但不限于取代或未取代的烷基(如苄基或取代的苄基)、取代的甲硅烷基(如三烷基甲硅烷基,如三甲基甲硅烷基)、烷氧基甲基(如甲氧基甲基)、或酰基(如乙酰基或苯甲酰基)。
本发明的化合物可根据本领域公认的方法如下制备。出于非限制性说明的目的并参照图1,通用合成方案1,根据本发明的化合物的制备如下描述。本发明化合物的制备的进一步详细描述在本文的实例中进一步提供。在图1中,所描绘的各种中间体、反应物、和/或化合物的各种基团,诸如r1、r2、r3、r4、b、b’、r芳基、以及r烷基各自如本文所描述的、和/或表示此类基团的前体。
以下如式(ia)所示化合物的合成已描述于许多文献,如us6,296,785或us7,262,295中,其具有不同的取代基。
羟基和羧酸可以被保护。例如,羟基可以通过与苄基氯和碱如碳酸钠或碳酸钾反应而被苄化,以形成其中r4是苄基的化合物。然后可以通过用于酯水解的酸或碱方法将所形成的羧酸酯转化成羧酸。所得产物如下式(ib)所示。
然后可以将羧酸基团通过库尔修斯重排条件使用二苯基磷酰叠氮化物(这生成异氰酸酯基团,然后水解产生胺基团)转化为nh2基团,如下式(ic)所示。
通过传统的酰胺形成反应,如使胺与酰氯、酯或羧酸基团反应,将胺基团转化为酰胺基团,如式(i)中所示。例如,胺与吡啶甲酰氯(picolinoylchloride)和碱如三乙胺反应以高产率得到吡啶甲酰胺,其中r3是2-吡啶基。
根据本发明的方法涉及生产包括下式(ii)中表示的核心骨架结构的吲哚萘酚化合物。
关于式(ii),m、n、r1、r2和r4如以上在式(i)中所述。
用于生产吲哚萘酚化合物的方法包括在催化剂的存在下将式(i)中所示的苯基萘酚化合物环化。参见以下所描绘的反应。催化剂可以是过渡金属催化剂。合适的过渡金属催化剂可包括铜、锌、钯、铂、铑或铱。环化可以在铜催化剂下进行,如描述于takumatso,k.等人org.lett.[有机快报]2014,16,2892。
本发明的方法可以进一步包括将式(ii)的吲哚萘酚化合物烷基化或芳基化以产生包括下式(iii)表示的核心骨架结构的吲哚萘酚化合物。
关于式(iii),m、n、r1、r2和r4如以上在式(i)中所述。r5选自取代或未取代的烷基、取代或未取代的芳基、或酰基。从其中可以选择r5的基团的实例包括但不限于烷基、苯基或取代的苯基。该方法的非限制性合适的烷基化和芳基化反应描述如下。
如式(iiia)中所示的吲哚基团的烷基化可以通过在碱的存在下与烷基卤化物、三氟甲磺酸酯或甲苯磺酸酯反应来完成。合适的碱包括叔丁醇钠或叔丁醇钾。吲哚可以通过强碱如氢化钠或正丁基锂去质子化,并然后将阴离子与烷基卤化物、三氟甲磺酸酯或甲苯磺酸酯反应。参见以下所描绘的反应。
吲哚基团可以通过与过渡金属催化剂和芳基卤化物的交叉偶联反应而芳基化,如式(iiib)中所示。交叉偶联反应可以是与铜催化剂和芳基卤化物如苯基卤化物的乌尔曼偶联反应。参见以下所描绘的反应。
吲哚还可以通过亲核芳族取代,如通过在合适的溶剂如四氢呋喃或二甲基甲酰胺中与芳基氟化物反应而芳基化,如式(iiib)中所示。
本发明的方法可以进一步包括当r4是取代或未取代的烷基、烷氧基甲基、取代或未取代的甲硅烷基、或酰基时,将r4脱保护以生成羟基。保护基团可以通过钯氢化条件或用强酸除去。参见以下所示的反应,其中式(iii)的r4是取代或未取代的烷基、烷氧基甲基、取代或未取代的甲硅烷基、或酰基,并且脱保护产物在式(iiid)中所示。
该方法可以进一步包括与二芳基炔丙醇反应以形成包括在下式(iv)中所示的核心骨架结构的吲哚萘并吡喃化合物。
关于式(iv),m、n、r1、r2和r4如以上在式(i)中所述,并且r5如上式(iii)中所述。b和b’各自独立地选自取代或未取代的芳基、或取代或未取代的杂芳基。b和b’可以各自独立地是取代或未取代的苯基。各苯基取代基可以选自烷氧基、卤素、烷基、或芳氧基。
在式(iii)中所示的吲哚萘酚化合物可以在酸性条件下与芳基炔丙醇反应以产生吲哚萘并吡喃化合物,如式(iv)中所示的。
参见以下所描绘的反应。
根据本发明的方法制备的光致变色吲哚萘并吡喃化合物,如以上关于式(iv)所述的那些,可以各自单独使用,或与一种或多种其他光致变色化合物组合使用。例如,本发明的光致变色化合物可以与一种或多种具有在300纳米至1,000纳米范围内的活化吸收最大值的其他光致变色化合物结合使用。此外,根据本发明制备的吲哚萘并吡喃化合物可以与一种或多种互补的常规可聚合或相容的光致变色化合物,例如像美国专利号6,113,814(第2栏,第39行至第8栏,第41行)和6,555,028(第2栏,第65行至第12栏,第56行)中所述的那些结合使用;或与其他光致变色化合物的混合物组合使用以获得某些活化的颜色,如接近中性的灰色或接近中性的棕色。参见例如美国专利号5,645,767第12栏第66行至第13栏第19行,其描述了定义中性灰色和棕色的参数。
根据本发明制备的吲哚萘并吡喃化合物可以单独使用或与如上刚刚讨论的其他光致变色化合物组合使用以制备光致变色组合物。例如,此类光致变色组合物可包含:(i)有机材料,其中有机材料是聚合物材料、低聚物材料、或单体材料中的至少一种;以及(ii)如根据本发明制备的吲哚萘并吡喃光致变色化合物(单独或与其他光致变色化合物组合),其被掺入有机材料的至少一部分中。对于一些实施例,合适的有机材料的实例可包括但不限于选自聚合物材料、低聚物材料和/或单体材料的那些中的任一者。可以与本发明的光致变色组合物一起使用的聚合物材料的实例包括但不限于:聚(碳酸酯)、乙烯和乙酸乙烯酯的共聚物;乙烯和乙烯醇的共聚物;乙烯、乙酸乙烯酯、以及乙烯醇的共聚物(诸如由乙烯和乙酸乙烯酯的共聚物的部分皂化得到的那些);乙酸丁酸纤维素;聚氨酯;聚(丙烯酸酯);聚(甲基丙烯酸酯);环氧化合物;氨基塑料官能聚合物;聚(酸酐);聚(脲氨基甲酸乙酯);n-烷氧基甲基(甲基)丙烯酰胺官能聚合物;聚(硅氧烷);聚(硅烷);以及它们的组合和混合物。可以与本发明的光致变色组合物一起使用的聚合物材料的进一步的类别和实例包括但不限于在us9,028,728b2的第39栏第45行直至第40栏第67行处所披露的那些。此类光致变色组合物可包含添加剂材料,如光引发剂、热引发剂、阻聚剂、溶剂、光稳定剂、热稳定剂、脱模剂、流变控制剂、流平剂、自由基清除剂、和/或粘合促进剂。根据本发明的光致变色组合物可以是光致变色涂料组合物,其可以是以本领域公认的液体涂料和粉末涂料的形式。本发明的光致变色涂料组合物可以是热塑性或热固性或可固化涂料组合物。此类组合物可用于制备光致变色制品,如眼科制品、显示制品、窗、镜、有源液晶盒制品和无源液晶盒制品。此类光致变色制品(例如,光致变色镜片)在暴露于光化辐射时可以从第一未活化状态(例如,透明和非蓝光阻挡状态)转变至第二活化状态(例如,着色和蓝光阻挡状态)。在移除光化辐射源后,制品可以恢复到第一未活化(且透明)状态。因此,根据本发明的光致变色制品在室外活动期间提供对与蓝光暴露相关的健康风险的增强的保护,同时在室内维持可接受的美观性。
在以下实例中更具体地描述了本发明,这些实例仅旨在作为说明性的,因为其中的许多修改和变化对于本领域技术人员将是显而易见的。
实例
提供以下实例以说明本发明的化合物、用于生产本发明的化合物的方法以及用于使用此类化合物制备光致变色化合物的方法。这些实例提供了本发明苯基萘酚化合物的合成描述和本发明用于生产吲哚萘酚和吲哚萘并吡喃化合物的方法的描述。
实例1-10的制备
在以下实例中,详述了用于制备苄基保护的苯基萘酚和吲哚萘酚化合物的代表性合成程序。
实例1
以下示出了用于合成实例1的方案。“ac”是指乙酰基,“bn”是指苄基,“dppa”是指二苯基磷酰基叠氮化物,“etoh”是指乙醇,“dcc”是指n,n'-二环己基碳二亚胺,“dmf”是指二甲基甲酰胺,“iproh”是指异丙醇,“dmap”是指4-(二甲基氨基)吡啶,并且“dcm”是指二氯甲烷。以下进一步描述合成的每个步骤。
步骤1
在氮气下搅拌的同时,将二苯甲酮(84.0g,461mmol)和琥珀酸二甲酯(80.84g,553mmol)溶解在甲苯(1.0l)中。在室温下在2小时内滴加叔五氧化钾(1.7m在甲苯中,352.5ml,599mmol)。20小时后,向反应混合物中添加水(1.5l)并使各层分离。丢弃有机相。用甲苯(1×200ml)萃取水相并丢弃有机相。用2n盐酸溶液酸化水相至ph4,然后溶液变得浑浊。通过用乙酸乙酯(3×300ml)萃取混合物来分离产物。将有机层合并、用硫酸钠干燥并在减压下浓缩。将所得固体用己烷洗涤、收集并在真空下干燥,以给出132.8g(97%产率)无色粉末。
步骤2
在氮气下搅拌的同时,将来自步骤1的产物(132.8g,448.2mmol)与乙酸酐(254.2ml,2.69mol)和甲苯(250ml)组合并加热至回流。16小时后,将反应混合物在减压下浓缩,并将所得油在己烷中沉淀,以给出灰白色固体。将固体收集并干燥以给出125.5g(88%产率)。
步骤3
在搅拌下将来自步骤2的产物(150g,468mmol)悬浮在甲醇(400ml)中。向悬浮液中添加浓盐酸(10ml)并将反应混合物加热至回流持续2小时。一旦完成,使反应混合物冷却至室温并在不搅拌的情况下静置50小时,同时产物重结晶。将晶体收集并干燥以给出完全转化(130g)。
步骤4
在氮气下搅拌的同时,将来自步骤3的产物(130g,467mmol)溶解在无水二甲基甲酰胺(400ml)中。将碳酸钾(130g,934mmol)悬浮在混合物中,随后缓慢添加苄基氯(71.0g,560mmol)。将反应混合物在75℃下加热16小时。一旦冷却,将反应混合物缓慢倒入冰水中并萃取到乙酸乙酯(3×500ml)中。将有机层合并、用盐水(2×300ml)洗涤、用硫酸钠干燥并在减压下浓缩。将所得固体用甲醇洗涤、收集并在真空下干燥,以给出无色固体(155.4g,90%产率)。
步骤5
在搅拌下将来自步骤4的产物(155.4g,422mmol)悬浮在2-丙醇(300ml)中。添加氢氧化钠溶液(10%w/w在水中,300ml)并将反应混合物加热至回流持续18小时。一旦冷却,将反应混合物倒入酸性冰水浴(ph3-4)中以形成无色沉淀物。将粉末收集并干燥以给出148.9g(99%产率)。
步骤6
在氮气下搅拌的同时,将来自步骤5的产物(149.1g,421mmol)悬浮于无水甲苯(800ml)中。添加三乙胺(111g,1.1mol)和无水乙醇(100ml),溶解悬浮液。将二苯基磷酰基叠氮化物(174g,632mmol)分批添加到反应混合物中,该反应混合物自行放热至回流,并且将向回流添加热量持续共计2小时。一旦冷却,将反应混合物添加到水(1.5l)和乙酸乙酯(500ml)中并分离各层。将有机层用水(3×1l)洗涤、用硫酸钠干燥并在减压下浓缩,以给出带红色的油,将其不经进一步纯化使用。
步骤7
将来自步骤6的所得油与氢氧化钠(86g,2.2mol)分散在四氢呋喃(600ml)、乙醇(400ml)和水(1.1l)中。将反应混合物加热至回流持续5天。一旦冷却,将盐水(200ml)添加到反应混合物中,分离各层,并用乙酸乙酯(3×300ml)洗涤水层。将有机层合并、用硫酸钠干燥并在减压下浓缩,以给出带红色的半固体,将其无需进一步纯化使用。
步骤8,实例1
在氮气下搅拌的同时,将来自步骤7的产物吸收在二氯甲烷(1.2l)中。添加吡啶甲酸(78g,632mmol)和4-(二甲基氨基)吡啶(5.2g,42mmol),随后添加n,n’-二环己基碳二亚胺(130.4g,632mmol)。允许反应混合物在室温下搅拌16小时。将反应混合物过滤并在减压下浓缩,以得到黑色固体,将其用甲醇洗涤,以得到呈灰白色粉末的受保护的苯基萘酚化合物(实例1)(160.85g,3步89%产率)。
步骤9,实例1a
在氮气下搅拌的同时,将来自步骤8的产物(76.5g,178mmol)溶解在无水二甲基甲酰胺(500ml)中,并向其中添加乙酸铜(ii)(65.0g,356mmol)和冰乙酸(10.7g,178mmol)。将反应混合物加热至150℃持续20小时,以给出70%的起始材料转化率。将反应混合物经硅藻土垫过滤,并用500ml的乙酸乙酯洗涤垫。将滤液与含有乙二胺(10ml)的水(1.0l)一起添加至分液漏斗中,并分离各层。将有机层用水(3×300ml)洗涤、用硫酸钠干燥并在减压下浓缩以给出灰白色固体。使材料经受反应条件的第二次重复和相同的分离程序。将所得固体用甲醇(300ml)洗涤两次,以得到灰白色粉末(实例1a,49.5g,86%产率)。产物通过1hnmr和质谱法证实。
实例2-9和实例2a-9a以类似方式制备并总结在表1中。所有化合物均通过1hnmr和质谱法表征。
表1
1产率对应于从步骤6-8中累积的分离出的苯基萘酚中间体;
2产率对应于来自步骤9中的分离出的吲哚萘酚中间体。
实例11和12的制备
在以下实例中,详述了用于制备吲哚萘吡喃光致变色化合物的代表性合成程序。以下示出了用于合成实例11和12的方案。“nbui”是指碘丁烷,“dmf”是指二甲基甲酰胺,“ptsa”是指对甲苯磺酸,并且“ph”是指苯基。以下进一步描述合成的每个步骤。
实例11
步骤1a
在氮气下搅拌的同时,将实例1a(4.0g,12.4mmol)溶解在无水二甲基甲酰胺(30ml)中并缓慢添加氢化钠(0.9g,37.1mmol)。15分钟后,添加碘丁烷(2.50g,13.6mmol)并将反应混合物在室温下搅拌45分钟。将反应混合物吸收在乙酸乙酯(200ml)中并用水(3×200ml)洗涤。将有机层用硫酸钠干燥并在减压下浓缩以给出棕色固体。将固体用甲醇洗涤以产生灰白色粉末(4.20g,89%产率)。
步骤2a
在氮气下搅拌的同时,将来自步骤1的产物(4.0g,10.5mmol)与甲酸铵(2.75g,43.6mmol)和碳载钯(德固赛公司(degussa)的型号e1003u/w,0.37g,3.2mmol)在二甲基甲酰胺(100ml)中组合。将反应混合物加热至85℃持续2小时。一旦冷却,将反应混合物经硅藻土的垫过滤并用乙酸乙酯(250ml)洗涤该垫。将滤液用水(3×300ml)洗涤,用硫酸钠干燥并在减压下浓缩,以得到棕色固体。将固体从二氯甲烷中沉淀到己烷中,以得到灰白色粉末(2.76g,91%产率)。
步骤3a
在氮气下搅拌的同时,将来自步骤2的产物(0.85g,2.90mmol)与1,1-二苯基丙-2-炔-1-醇(0.73g,3.5mmol)在甲苯(25ml)中组合并加热至回流。添加对甲苯磺酸(5-10mg)并将反应混合物加热至回流持续1小时。一旦冷却,将反应混合物吸收在乙酸乙酯(25ml)中、用饱和碳酸氢钠溶液(25ml)和水(2×50ml)洗涤。将有机层用硫酸钠干燥并在减压下浓缩至硅胶上。色谱法(硅胶,己烷中的0-25%二氯甲烷)产生深色油状物。将产物从甲基叔丁基醚、四氢呋喃和甲醇中重结晶两次,以得到呈灰白色粉末的实例11(0.73g,53%产率),并通过质谱法证实。
实例12
步骤1b
在氮气下搅拌的同时,将实例1a(7.0g,21.6mmol)与溴苯(13.6g,86.4mmol)、碘化铜(2.06g,10.8mmol)、碳酸钾(6.0g,43.2mmol)、1,10-菲咯啉(0.78g,4.30mmol)和二苯并-18-冠-6-醚(0.80g,2.20mmol)在无水二甲基甲酰胺(50ml)中组合。将反应混合物加热至150℃持续4小时。一旦冷却,将反应混合物吸收在乙酸乙酯(250ml)中并最初用水(200ml)、用乙二胺(10ml)洗涤,随后用水(2×250ml)洗涤。将有机层用硫酸钠干燥并在减压下浓缩至硅胶上。色谱法(硅胶,己烷中的0-25%二氯甲烷)产生无色粉末,将其用己烷洗涤并真空干燥(7.82g,90%产率)。
步骤2b
在氮气下搅拌的同时,将来自步骤1的产物(2.5g,6.26mmol)与甲酸铵(1.60g,25.0mmol)和碳载钯(德固赛公司的型号e1003u/w,0.22g,1.9mmol)在二甲基甲酰胺(30ml)中组合。将反应混合物加热80℃持续2小时。一旦冷却,将反应混合物经硅藻土的垫过滤并用乙酸乙酯(250ml)洗涤该垫。将滤液用水(3×300ml)洗涤,用硫酸钠干燥并在减压下浓缩,以得到棕色油状物,其不经进一步纯化即可使用。
步骤3b
在氮气下搅拌的同时,将来自步骤2的产物(0.50g,1.60mmol)与1,1-二苯基丙-2-炔-1-醇(0.40g,2.0mmol)在甲苯(30ml)中组合并加热至回流。添加对甲苯磺酸(5-10mg)并将反应混合物加热至回流持续1小时。一旦冷却,将反应混合物在减压下浓缩到硅胶上。色谱法(硅胶,己烷中的0-5%二氯甲烷)产生黄色固体。将产物从二氯甲烷和己烷中重结晶两次,以得到呈浅黄色晶体的实例12(0.22g,27%产率)并通过质谱法证实。
本发明可以进一步地由以下非限制性条款中的一项或多项表征。
条款1.一种苯基萘酚化合物,其具有由式(i)表示的核心骨架结构:
其中,
m是0至4;
n是0至4;
r1和r2各自独立地是羟基、氰基、(甲基)丙烯酸酯、氨基、卤基、取代或未取代的烷基、硼酸酯、硼酸、聚醚、聚酯、聚碳酸酯、聚氨酯、取代或未取代的芳基、取代或未取代的杂环烷基、取代或未取代的杂芳基、取代或未取代的烷氧基、取代或未取代的芳氧基、取代或未取代的烷硫基、取代或未取代的芳硫基、酮、醛、酯、羧酸、羧酸酯、酰胺、碳酸酯、氨基甲酸酯、脲、硅氧烷、烷氧基硅烷、或聚硅氧烷;
其中相邻碳原子上的两个r1基团或两个r2基团可以连接形成环;
r3选自取代或未取代的2-吡啶基或取代或未取代的2-喹啉基;
其中所述吡啶基和喹啉基取代基选自取代或未取代的烷基、取代或未取代的烷氧基、取代或未取代的芳氧基、取代或未取代的芳基、取代或未取代的杂芳基、卤素、氨基、酯、羧酸酯、或羟基;并且
r4选自氢、取代或未取代的烷基、烷氧基甲基、取代或未取代的甲硅烷基、或酰基。
条款2.如条款1所述的苯基萘酚化合物,其中,每个烷基取代基、每个芳基取代基、每个杂环烷基取代基、每个杂芳基取代基、每个烷氧基取代基、每个芳氧基取代基、每个烷硫基取代基、每个芳硫基取代基以及每个甲硅烷基取代基在每种情况下独立地选自卤素、氰基、硝基、烷基、烯基、炔基、卤代烷基、全卤代烷基、杂环烷基、芳基、杂芳基、烷氧基、羟基、烷硫基、芳硫基、酮、醛、酯、羧酸、羧酸酯、硅氧烷、烷氧基硅烷、聚硅氧烷、酰胺、胺、氨基甲酸酯、碳酸酯、脲、聚酯基团、聚醚基团、聚碳酸酯基团、聚氨酯基团、丙烯酸酯基团、(甲基)丙烯酸酯基团、芳基胺、烷基胺、环状氨基、杂芳族化合物、或其组合。
条款3.如条款1或2所述的苯基萘酚化合物,其中,r1和r2独立地选自卤基、取代或未取代的烷基、取代或未取代的杂芳基、取代或未取代的烷氧基、取代或未取代的芳氧基、取代或未取代的烷硫基、或取代或未取代的芳硫基。
条款4.如条款3所述的苯基萘酚化合物,其中,r1或r2是烷氧基、烷基、卤基、三卤代烷基、或芳硫基。
条款5.如条款4所述的苯基萘酚化合物,其中,r1或r2是甲氧基、甲基、氟、三氟甲基、或芳硫基。
条款6.如条款4所述的苯基萘酚化合物,其中,r1或r2是烷氧基。
条款7.如条款4至6中任一项所述的苯基萘酚化合物,其中,r1或r2是甲氧基。
条款8.如条款1至4中任一项所述的苯基萘酚化合物,其中,r1或r2的每个卤基选自氟、氯、溴或碘。
条款9.如条款1至8中任一项所述的苯基萘酚化合物,其中,r3是2-吡啶基。
条款10.如条款1至9中任一项所述的苯基萘酚化合物,其中,r4是苄基。
条款11.如条款1至10中任一项所述的苯基萘酚化合物,其中,r1在下式(i’)的核心骨架结构中所示的位置处:
其中每个z独立地是0或1。
条款12.如条款1至11中任一项所述的苯基萘酚化合物,其中,r2在下式(i”)的核心骨架结构中所示的位置处:
其中每个y独立地是0或1。
条款13.一种用于生产吲哚萘酚化合物的方法,所述吲哚萘酚化合物包括由式(ii)表示的核心骨架结构:
其中,
m是0至4;
n是0至4;
r1和r2各自独立地是羟基、氰基、(甲基)丙烯酸酯、氨基、卤基、取代或未取代的烷基、硼酸酯、硼酸、聚醚、聚酯、聚碳酸酯、聚氨酯、取代或未取代的芳基、取代或未取代的杂环烷基、取代或未取代的杂芳基、取代或未取代的烷氧基、取代或未取代的芳氧基、取代或未取代的烷硫基、取代或未取代的芳硫基、酮、醛、酯、羧酸、羧酸酯、酰胺、碳酸酯、氨基甲酸酯、脲、硅氧烷、烷氧基硅烷、或聚硅氧烷;
其中相邻碳原子上的两个r1基团或两个r2基团可以连接形成环;
r3选自取代或未取代的2-吡啶基或取代或未取代的2-喹啉基;
其中所述吡啶基和喹啉基取代基选自取代或未取代的烷基、取代或未取代的烷氧基、取代或未取代的芳氧基、取代或未取代的芳基、取代或未取代的杂芳基、卤素、氨基、酯、羧酸酯、或羟基;并且
r4选自氢、取代或未取代的烷基、烷氧基甲基、取代或未取代的甲硅烷基、或酰基;并且
所述方法包括在催化剂的存在下将如条款1至12中任一项所述的苯基萘酚化合物环化。
条款14.如条款13所述的方法,其中,所述催化剂是过渡金属催化剂。
条款15.如条款13或14所述的方法,其中,所述催化剂包括铜、锌、钯、铂、铑或铱。
条款16.如条款13至15中任一项所述的方法,其中,所述催化剂包括铜。
条款17.如条款13至16中任一项所述的方法,所述方法进一步包括烷基化或芳基化以产生包括所述由式(iii)表示的核心骨架结构的吲哚萘酚化合物:
其中r5选自取代或未取代的烷基、取代或未取代的芳基、或酰基。
条款18.如条款17所述的方法,其中,r5是烷基。
条款19.如条款17或18所述的方法,所述方法包括通过在碱的存在下与烷基卤化物、三氟甲磺酸酯或甲苯磺酸酯反应而烷基化。
条款20.如条款19所述的方法,所述方法包括用碱使吲哚去质子化,以及使所得阴离子与所述烷基卤化物、三氟甲磺酸酯或甲苯磺酸酯反应。
条款21.如条款17所述的方法,其中,r5是取代或未取代的苯基。
条款22.如条款17或21所述的方法,所述方法包括通过与过渡金属催化剂和芳基卤化物的交叉偶联反应而芳基化。
条款23.如条款22所述的方法,其中,所述交叉偶联反应是与铜催化剂的乌尔曼偶联反应。
条款24.如条款17或21所述的方法,所述方法包括通过与芳基氟化物的亲核芳族取代反应而芳基化。
条款25.如条款13至24中任一项所述的方法,所述方法进一步包括当r4是取代或未取代的烷基、烷氧基甲基、取代或未取代的甲硅烷基、或酰基时,将r4脱保护以生成羟基。
条款26.如条款25所述的方法,其中,脱保护在钯加氢条件下或用强酸进行。
条款27.如条款26所述的方法,其中,脱保护是在碳载钯下进行的。
条款28.如条款13至27中任一项所述的方法,所述方法进一步包括与二芳基炔丙醇反应以形成包括由式(iv)表示的核心骨架结构的吲哚萘并吡喃化合物:
其中b和b’各自独立地是取代或未取代的芳基、或取代或未取代的杂芳基。
条款29.如条款28所述的方法,其中,与二芳基炔丙醇反应在酸性条件下进行。
条款30.如条款28或29所述的方法,其中,b和b’各自独立地是取代或未取代的苯基。
条款31.如条款30所述的方法,其中,各苯基取代基在各情况下独立地是烷氧基、卤素、烷基、或芳氧基。
已经根据本发明的特定实施例的具体细节描述了本发明。这并不旨在认为这些细节是对本发明的范围的限制,除非在它们包括在所附权利要求中的程度上。
- 还没有人留言评论。精彩留言会获得点赞!