PD-L2单克隆抗体及其应用的制作方法
本发明涉及生物技术领域,特别涉及pd-l2单克隆抗体及其应用。
背景技术:
杂交瘤技术(hybridomatechnique),是最广泛应用的单克隆抗体技术。1975年koehler和milstein证明,将骨髓瘤细胞与免疫的动物脾细胞进行融合,形成的杂交瘤细胞株可产生针对某一抗原的特异性强的单克隆抗体,同时又能不断扩增。杂交瘤技术利用了骨髓瘤细胞能在体外连续传代和淋巴细胞能分泌特异性抗体的特征,将两种细胞的功能都得到有效发挥,使单克隆抗体制备大规模应用成为可能。
程序性死亡受体(programmeddeath-1,pd-1)是cd28超家族成员,为一种重要的免疫抑制分子,主要表达在激活的t细胞和b细胞上。pd-1的配体pd-ls(programmeddeath-1ligands)主要有pd-l1(b7-h1/cd274)和pd-l2(b7-dc/cd273),其中pd-l1是主要配体。目前临床应用的阻断pd-1/pd-l1的抗体药物对于pd-l1阴性病人无效,亟需开发pd-l2的单克隆抗体。
pd-l2蛋白是由pdcd1lg2基因编码的一个含274个氨基酸残基组成的i型跨膜蛋白,与pd-l1同源性达40%,但也有一定差异。pd-l2在体内组织中只表达于巨噬细胞、树突状细胞和一些b细胞亚类的膜表面,但近年来研究表明在特定微环境刺激下,pd-l2在其他多种免疫细胞和非免疫细胞中均可诱导表达,如肺癌、乳腺癌、胸腺瘤等肿瘤细胞中高表达。大量研究表明pd-l2可以作为一种重要的生物标志物在各种肿瘤的诊断、靶向治疗和预后中发挥重要作用。pd-l2单克隆抗体的优劣决定着各种免疫检测方法(如免疫组织化学,酶联免疫反应,流式细胞检测等)的灵敏度和特异性,决定着靶向治疗的安全性和有效性。目前市场上大力推广针对pd1/pd-l1的抗体用于癌症治疗,缺乏针对pd-l2治疗用单克隆抗体,用于检测的pd-l2抗体特异性及灵敏度仍然不高。因此,研制出亲和性高特异性高的抗pd-l2单克隆抗体具有重要意义。
技术实现要素:
有鉴于此,本发明提供了pd-l2单克隆抗体及其应用。本发明提供的pd-l2抗体具有高的生物活性和独特的抗体可变区序列,且具有很好的抗肿瘤效果。
为了实现上述发明目的,本发明提供以下技术方案:
本发明提供了pd-l2的单克隆抗体,
(i)、其重链的三个cdr区的氨基酸序列分别具有如seqidno:5、6和7所示的氨基酸序列;且
(ii)、其轻链的三个cdr区的氨基酸序列分别具有如seqidno:8、9和10所示的氨基酸序列;或
(iii)、(i)或(ii)所述氨基酸序列经取代、缺失或添加一个或多个氨基酸获得的氨基酸序列,且与(i)或(ii)所示的氨基酸序列功能相同或相似的氨基酸序列;或
(iv)、与(i)、(ii)或(iii)所述序列至少有80%同源性的氨基酸序列。
在本发明的一些具体实施方案中,所述的单克隆抗体,
(v)、其重链可变区具有如seqidno:2所示的氨基酸序列;且
(vi)、其轻链可变区具有如seqidno:4中任一项所示的氨基酸序列;或
(vii)、(v)或(vi)所述氨基酸序列经取代、缺失或添加一个或多个氨基酸获得的氨基酸序列,且与(v)或(vi)所示的氨基酸序列功能相同或相似的氨基酸序列;或
(viii)、与(v)、(vi)或(vii)所述序列至少有80%同源性的氨基酸序列。
在本发明的一些具体实施方案中,所述的单克隆抗体,所述多个为2个、3个、4个或5个。
本发明还提供了编码所述的单克隆抗体的核苷酸。
在本发明的一些具体实施方案中,所述的核苷酸,
(ix)、其重链具有seqidno:1所示的核苷酸序列;且
(x)、其轻链具有seqidno:3所示的核苷酸序列;或
(xi)、(ix)或(x)所述的核苷酸序列经修饰、取代、缺失或添加一个或多个碱基获得的核苷酸序列;
(xii)、与(ix)、(x)或(xi)所述的核苷酸序列具有至少80%同源性的序列;
(xiii)、如(ix)、(x)、(xi)或(xii)所述的核苷酸序列的互补序列。
本发明还提供了一种表达载体,包括编码所述单克隆抗体的核苷酸。
在此基础上,本发明还提供了转化或转染所述表达载体的宿主细胞。
本发明还提供了所述单克隆抗体的制备方法,包括:培养所述宿主细胞、诱导pd-l2的单克隆抗体的表达。
此外,本发明还提供了结合物,包含经化学标记或生物标记的所述的单克隆抗体。
在上述研究的基础上,本发明还提供了所述单克隆抗体或所述结合物与固体介质或半固体介质偶联制得的偶联物。
本发明还提供了所述单克隆抗体或所述结合物或所述偶联物在制备诱导癌细胞凋亡、预防和/或治疗自身免疫性疾病的药物中的应用或用于制备westernblot检测、elisa检测、流式细胞检测的产品中的应用。
本发明还提供了药物,包括所述单克隆抗体或所述结合物或所述偶联物以及药学上可接受的辅料。
此外,本发明还提供了试剂盒,包括所述单克隆抗体或所述结合物或所述偶联物以及可接受的助剂。
本发明提供了pd-l2的单克隆抗体,(i)、其重链的三个cdr区的氨基酸序列分别具有如seqidno:5、6和7所示的氨基酸序列;且(ii)、其轻链的三个cdr区的氨基酸序列分别具有如seqidno:8、9和10所示的氨基酸序列;或(iii)、(i)或(ii)所述氨基酸序列经取代、缺失或添加一个或多个氨基酸获得的氨基酸序列,与(i)或(ii)所示的氨基酸序列功能相同或相似的氨基酸序列;或(iv)、与(i)、(ii)或(iii)所述序列至少有80%同源性的氨基酸序列。
本发明拓宽了阻断pd1/pd1配体的抗体疗法的可能性,同时与现有pd-l2单克隆抗体相比,3f4抗体具有独特的氨基酸序列和cdr区序列,具有高亲和力,高特异性。能用于elisa、westernblot和流式细胞检测,用途广泛。本发明的pd-l2抗体具有高的生物活性和独特的抗体可变区序列,且具有很好的抗肿瘤效果。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。
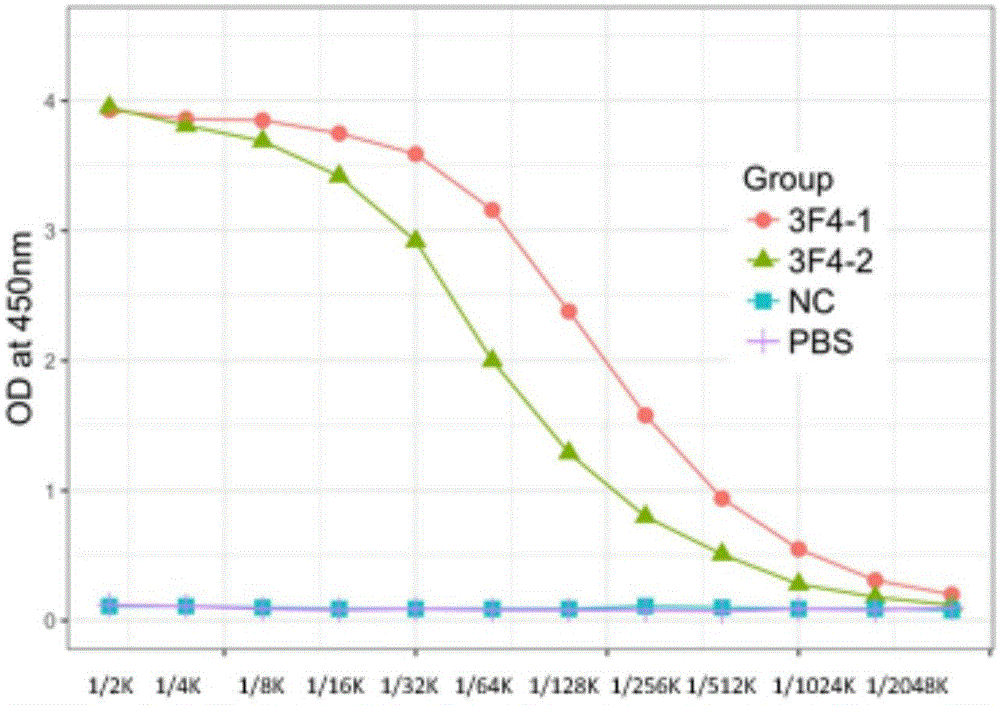
图1示elisa筛选得到能分泌pd-l2抗体的单克隆杂交瘤细胞株3f4;
图2示3f4抗体亚型鉴定图;
图3示pd-l2单克隆抗体用于westernblot;
图4示pd-l23f4抗体流式检测daudi细胞图;
图5示pd-l23f4抗体检测载体引入表达pd-l2的293t细胞。
具体实施方式
本发明公开了pd-l2单克隆抗体及其应用,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
本发明提供了pd-l2单克隆抗体的氨基酸序列,可经取代、缺失或添加一个或多个氨基酸获得新的氨基酸序列,且具有与本发明提供的氨基酸序列功能相同或相似的氨基酸序列。或者与公开序列至少有80%同源性的氨基酸序列可作为替代方案。
本发明提供了pd-l2单克隆抗体的核苷酸序列,其互补序列或因遗传密码的简并性而与本发明公开核苷酸序列不同,但编码相同蛋白的序列,或与本发明公开序列至少有80%同源性的序列可作为替代方案。
本发明提供了pd-l2单克隆抗体的核苷酸序列,经取代、缺失或添加一个或多个核苷酸序列获得的核苷酸序列,且与本发明公开核苷酸序列功能相同或相似的核苷酸序列可作为替代方案。
本发明采用小鼠腹水生产抗体,也可以采用大规模培养分泌抗体的杂交瘤细胞或稳定表达抗体基因的cho细胞或293f细胞进行抗体的生产。
本发明提供了小鼠抗人pd-l2单克隆抗体的可变区氨基酸序列和核苷酸序列,通过抗体人源化改造,可以获得抗人pd-l2的人鼠嵌合抗体和人源化抗体。抗人pd-l2的人鼠嵌合抗体将鼠源单克隆抗体基因的可变区和人的恒定区连接在一起,然后在哺乳动物细胞中进行表达产生;而抗人pd-l2的人源化抗体则是除了将抗体的恒定区换成人源的之外,更进一步的将可变区的fr区转换成人源的,从而降低免疫原性。
本发明提供了抗人pd-l2单克隆抗体的可变区氨基酸序列和核苷酸序列,在此基础上可以产生基因工程抗体,其所含的重链和轻链可变区序列与本发明公开的可变区序列是一致的。该基因工程抗体包括但不限于:抗体的功能性片段fab,或者是单链抗体,或者是重链可变区和完整轻链融合的抗体功能性片段vh-l,或者是重链和轻链的一个或多个cdr的排列、串联或组合而成的抗体功能性片段,或者是上述抗体和抗体功能片段和其他各种蛋白或多肽进行连接、拼接、融合而得到的类抗体的功能性的融合蛋白。
本发明公开的抗人pd-l2的抗体,除了单独使用,还可以与常用的肿瘤放、化疗药物联合使用。
本发明公开的抗人pd-l2的抗体或为基础产生的基因工程抗体可以作为靶向部分,与放射性核素或化学药物或毒素偶联。
本发明公开了抗人pd-l2的抗体对肿瘤的杀伤效果,可用于其它有pd-l2表达的多种肿瘤类型的治疗。
本发明提供的pd-l2单克隆抗体及其应用中所用原料及试剂均可由市场购得。
下面结合实施例,进一步阐述本发明:
实施例1pd-l2单克隆抗体的生产
采用杂交瘤法(由kohler等,nature,256:495(1975)首先提出)。用pd-l2蛋白抗原(购买于sinobiological,货号10292-h08h-1mg)免疫雌性balb/c小鼠(6周龄),首次免疫使用弗氏完全佐剂进行乳化抗原,第二次免疫开始,使用弗氏不完全佐剂乳化抗原,皮下5~6点注射,每只小鼠注射的抗原量为~100ug。在第3次免疫后10天,对小鼠剪尾采集少量血液进行血清效价elisa检测,选择抗体滴度高(>1:100000)的小鼠进行加强第4次免疫,通过腹腔注射抗原蛋白,每只小鼠注射100ug。第4次免疫后3~5天,处死小鼠取其脾细胞与sp2/0细胞融合,通过hat培养基培养获得稳定的杂交瘤细胞。通过elisa法筛选得到能分泌pd-l2抗体的杂交瘤细胞,通过有限稀释的方法进行亚克隆,elisa法筛选得到能分泌pd-l2抗体的单克隆杂交瘤细胞株3f4(如图1所示),通过逐级扩大培养,液氮冻存保种。
实施例2pd-l2单克隆抗体杂交瘤细胞的抗体基因可变区测序
收获处于对数生长期的单克隆抗体3f4杂交瘤细胞,trizol裂解进行rna提取,反转录后获得cdna,扩增并获得重链和轻链可变区,非功能性vk基因去除,克隆至pmd18-t载体,测序,使用imgt/v-quest数据库进行测序结果比对,进一步分析。
重链碱基序列如seqidno.1所示:
重链可变区氨基酸序列如seqidno.2所示:
轻链碱基序列如seqidno.3所示:
轻链可变区氨基酸序列如seqidno.4所示:
经与imgt/v-quest数据库进行比对,重链:
cdr1-imgt(seqidno.5):
cdr2-imgt(seqidno.6):
cdr3-imgt(seqidno.7):
轻链:
cdr1-imgt(seqidno.8):
cdr2-imgt(seqidno.9):
cdr3-imgt(seqidno.10):
实施例3pd-l2单克隆抗体的亚型鉴定
使用商品化小鼠单克隆抗体isotyping试剂盒(sinobiological,sek003)进行单抗亚型鉴定,结果如图2所示,3f4为igg1型抗体。
实施例4抗pd-l2单克隆抗体检测dauti细胞的pd-l2
1、收集daudi细胞,吹散计数,分装5个离心管,每管3×105个细胞,500g离心5min,去上清,分别加入1mlpbs,500g离心5min,去上清。
2、按表1加入试剂:
表1
放入冰上,孵育,30min。
3、各加入1mlpbs+5%fbs,500g离心5min,去上清,各加入100uldmem培养液+1ulpegoatanti-mouselgg(minimalx-reactivity)antibody(biolegend,405307),冰上孵育20min。
4、各加入1mlpbs+5%fbs,500g离心5min,去上清。
5、每管加入300ulpbs+5%fbs,重悬,使用贝克曼流式细胞仪(beckmancytoflexcm)检测。
如图4所示,3f4抗体能与daudi细胞表面pd-l2蛋白结合,应用于流式细胞检测,且检测灵敏度优于商品化阳性对照。
实施例5抗pd-l2单克隆抗体检测质粒载体引入pd-l2的293t细胞
1、用pd-l2表达载体(sinobiologicalhg10292转染293t细胞
2、收集293t细胞,吹散计数,分装5个离心管,每管3×105个细胞,500g离心5min,去上清,分别加入1mlpbs,500g离心5min,去上清。
3、按表2加入试剂:
表2
放入冰上,孵育,30min。
4、各加入1mlpbs+5%fbs,500g离心5min,去上清,各加入100uldmem培养液+1ulpegoatanti-mouselgg(minimalx-reactivity)antibody(biolegend,405307),冰上孵育20min。
5、各加入1mlpbs+5%fbs,500g离心5min,去上清。
6、每管加入300ulpbs+5%fbs,重悬,使用贝克曼流式细胞仪(beckmancytoflexcm)检测。
如图5所示,3f4抗体能与293t细胞表面过表达的pd-l2蛋白结合,可以应用于流式细胞检测。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!