一种微生物催化去消旋化制备L-草铵膦的方法与流程
本发明属于生物技术领域。具体地说,涉及一种解木糖赖氨酸芽孢杆菌(lysinibacillusxylanilyticus)xx-2用于制备l-草铵膦的方法。
背景技术:
草铵膦是一种手性除草剂,有l-和d-两种对映体。其中,l-草铵膦除草活性是消旋体的2倍。草铵膦以l-构型的纯光学异构体形式使用,可使草铵膦的使用量降低50%,这对于降低使用成本、减轻环境压力都具有十分重要的意义。
l-草铵膦的制备方法主要包括化学法和生物法。相比于化学法,生物法具有立体选择性严格、反应条件温和、收率高及产物易分离纯化的优点,是实现l-草铵膦工业化生产最具潜力的方法。
生物法包括生物不对称合成法和生物拆分法。
生物不对称合成法主要包括氨基酸脱氢酶法和转氨酶法。氨基酸脱氢酶法以2-羰基-4-(羟基甲基膦酰基)丁酸为原料,草铵膦脱氢酶/甲酸脱氢酶共表达的基因工程菌为生物催化剂,在辅酶nadp+和辅底物甲酸铵存在下制备l-草铵膦(zl201710195364.3,cn108588045a)。该方法中不仅l-草铵膦收率低,光学纯度不高,而且辅酶nadh需再生,难以在工业化生产中应用。转氨酶法以2-羰基-4-(羟基甲基膦酰基)丁酸为底物,在氨基供体如丙氨酸存在的条件下,利用离体的转氨酶或体外表达转氨酶的细胞催化底物与氨基供体发生转氨反应,得到l-草铵膦,转化率85-100%,ee>99.9%(zl201610045121.7,cn108660167a)。由于转氨化是一个可逆反应,存在两个l-氨基酸和两个α-酮酸的反应平衡,分离难度大。
生物拆分法主要包括以n-乙酰-dl-草铵膦为原料,以含羧肽酶基因的工程菌经发酵培养获得的湿菌体或湿菌体超声破碎后提取的纯酶为催化剂,制备l-草铵膦。d-n-乙酰草铵膦消旋化后用于循环拆分(cn108690854a)以及以2-氨基-4-(羟基甲基磷酰基)丁腈为原料的腈水解酶拆分法(zl201310201317.7)。生物拆分法的理论收率为50%。通常情况下,生物拆分法需要以衍生的dl-草铵膦为原料,涉及无效对映体的化学消旋和循环拆分。
夏仕文等(cn105567780a)公开了一种l-草铵膦的酶-化学催化去消旋化制备方法。该方法采用固定化d-氨基酸氧化酶-钯碳/甲酸铵组合体系实现dl-草铵膦去消旋化,l-草铵膦收率>90%,ee>99%,但制备成本偏高。杨立荣等(cn107502647a)公开了一种生物酶法去消旋化制备l-草铵膦的方法,该方法以dl-草铵膦为原料,利用d-氨基酸氧化酶将d-草铵膦氧化为2-羰基-4-(羟基甲基膦酰基)丁酸,l-草铵膦因不参与反应而被完全保留;而2-羰基-4-(羟基甲基膦酰基)丁酸又被氨基酸脱氢酶催化还原为l-草铵膦,进而实现了dl-草铵膦的原位去消旋化,得到的l-草铵膦中无其他副产物,产品总收率>99%,光学纯度可超过99%。
开发一种简捷、高效、低廉、绿色的生物催化去消旋化方法将是今后生产l-草铵膦的重要突破口和发展方向。
技术实现要素:
本发明的目的是提供一种微生物催化去消旋化制备l-草铵膦的方法。采用“一锅煮”反应方式,以未经衍生的dl-草铵膦为原料,利用微生物细胞中的d-氨基酸氧化酶对映选择性催化dl-草铵膦中的d-对映体氧化脱氨为2-羰基-4-(羟基甲基膦酰基)丁酸,l-草铵膦完全保留。利用细胞中共表达的氨基酸脱氢酶体系将2-羰基-4-(羟基甲基膦酰基)丁酸原位还原氨化为l-草铵膦,通过生物氧化脱氨-生物还原氨化实现dl-草铵膦的去消旋化。
技术路线如下:
本发明中的解木糖赖氨酸芽孢杆菌xx-2保藏于中国典型培养物保藏中心,保藏号为cctccno.m2015520。
本发明所需的d-氨基酸氧化酶/氨基酸脱氢酶体系来源于解木糖赖氨酸芽孢杆菌xx-2。解木糖赖氨酸芽孢杆菌xx-2的培养条件为:
斜面培养基:3g/l牛肉膏、5g/l酵母膏、5g/l氯化钠、15g/l琼脂,ph6.0。
种子培养基:3g/l牛肉膏、5g/l酵母膏、5g/l氯化钠,ph6.0。
产酶培养基:3g/l牛肉膏、5g/l酵母膏、5g/l氯化钠,3g/ld-草铵膦(诱导剂),ph6.0。
斜面培养:将木糖赖氨酸芽孢杆菌xx-2接种于斜面培养基上,30℃培养24~64小时;
种子培养:将斜面培养的菌株,无菌条件下用接种环接种于5ml发酵培养基中,30℃下摇床振荡(180rpm)培养48小时,制得种子液;
摇瓶培养:以10%接种量将种子液接入新鲜的产酶培养基中,30℃下摇床振荡(180rpm)培养48小时。
菌体收集:摇瓶培养的菌液在4℃、8000转/分条件下离心5分钟,收集菌体,用磷酸盐缓冲液(100mmol/l,ph8.0)洗涤2次,得到湿菌体。
一种解木糖赖氨酸芽孢杆菌(lysinibacillusxylanilyticus)xx-2在去消旋化制备l-草铵膦中的应用,即利用解木糖赖氨酸芽孢杆菌催化去消旋化制备l-草铵膦的方法。按照上述方法将木糖赖氨酸芽孢杆菌xx-2接入灭菌后的产酶培养基中,培养后离心收集菌体,用磷酸盐缓冲液洗涤2次,菌体重新悬浮在磷酸盐缓冲液中,制成一定细胞浓度的菌悬液,加入dl-草铵膦,恒温摇床振荡反应,直至d-草铵膦反应完全。
本发明中解木糖赖氨酸芽孢杆菌xx-2细胞可回收循环使用。
作为优选,磷酸盐缓冲液浓度为100mmol/l,ph8.0。
作为优选,细胞浓度为20~50g/l(干重)。
作为优选,dl-草铵膦终浓度为20~200mmol/l。
作为优选,反应温度为20~40℃,振荡速度为150~200转/分,反应时间为24~48小时。
与现有的l-草铵膦制备方法相比,本发明提出的微生物催化去消旋制备l-草铵膦的方法具有以下优点:1)工艺简单。生物催化氧化脱氨-生物催化还原氨化在同一反应体系中进行。高浓度dl-草铵膦不经衍生,直接作为d-氨基酸氧化酶的反应底物。2-羰基-4-(羟基甲基膦酰基)丁酸不经分离,直接原位转化为l-草铵膦。2)分离过程简单。产物流中仅含l-草铵膦,只需采用简单的浓缩、结晶方法即可以高的收率和高的光学纯度实现l-草铵膦的分离。3)成本低廉。微生物细胞可回收重复使用多次,有效降低了过程成本。
附图说明
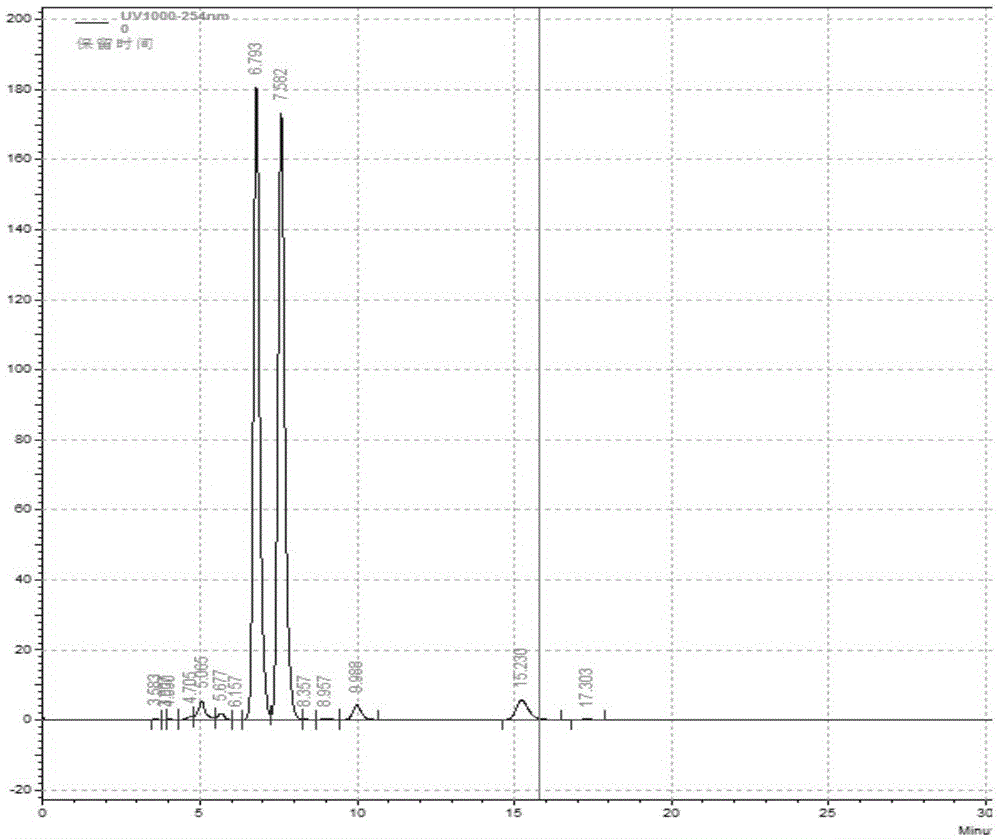
图1为草铵膦两个光学异构体的高效液相色谱检测图(柱前手性衍生-hplc法),其中,保留时间6.793min为d-草铵膦,保留时间7.582min为l-草铵膦。
图2为实施例3中dl-草铵膦微生物催化去消旋化后的高效液相色谱检测图(柱前手性衍生-hplc法),其中,保留时间7.573min为l-草铵膦。
具体实施方式
以下所述实施例仅为本发明构思下的基本说明,根据本发明的技术方案所作的任何等效变换,均属于本发明保护的范围。
下列实施例中的催化反应采用高效液相色谱(hplc)监测并对反应物和产物进行分析。柱前手性衍生-hplc条件为:反应上清液中加入4g/l三乙胺/乙腈溶液和2g/l2,3,4,6-四-o-乙酰基-β-d-吡喃葡萄糖异硫氰酸酯(gitc)/乙腈溶液,30℃下水浴加热20min。离心,采用hplc测定上清液中的d-和l-草铵膦浓度,根据校正曲线计算转化率。色谱柱:c18柱;流动相:0.1%三氟乙酸水溶液/甲醇(51:49,v/v),ph2.5;流速:1.0ml/min;检测波长:254nm;柱温:25℃。
实施例1:菌体培养
解木糖赖氨酸芽孢杆菌xx-2在摇瓶中发酵培养。以10%接种量将种子液接入灭菌后的产酶培养基中,30℃下摇床振荡(180rpm)培养48小时。菌液在4℃、8000转/分条件下离心5分钟,收集菌体,用磷酸钠缓冲液((100mmol/l,ph8.0)洗涤2次。菌体重新悬浮在磷酸钠缓冲液(100mmol/l,ph8.0)中备用。
实施例2:d-草铵膦的立体反转
反应液(10ml)含100mmol/l磷酸盐缓冲液(ph8.0),100mmol/ld-草铵膦,500mg(干重)解木糖赖氨酸芽孢杆菌xx-2细胞。30℃、180rpm下恒温摇床振荡反应。每隔一定时间取样,离心去除细胞收集上清液,采用柱前手性衍生-hplc测定上清液中l-和d-草铵膦浓度。24h后,d-草铵膦反应完全,反应液中l-草铵膦的生成浓度为66mmol/l,ee99.8%。
实施例3:dl-草铵膦去消旋化
反应液(10ml)含100mmol/l磷酸盐缓冲液(ph8.0),200mmol/ldl-草铵膦,500mg(干重)解木糖赖氨酸芽孢杆菌xx-2细胞。30℃、180rpm下恒温摇床振荡反应。每隔一定时间取样,离心去除细胞收集上清液,采用柱前手性衍生-hplc测定上清液中l-和d-草铵膦浓度。24h后,d-草铵膦反应完全,反应液中l-草铵膦的生成浓度为166mmol/l,ee99.5%。
实施例4:细胞循环使用
反应体系同实施例3。实施例3中的细胞离心后,加入反应体系中,30℃、180rpm下摇床振荡反应28h后,柱前手性衍生-hplc监测d-草铵膦反应完全,l-草铵膦生成浓度为160mmol/l,ee99.4%。
实施例5:细胞循环使用
反应体系同实施例3。实施例4中的细胞离心后,加入反应体系中,30℃、180rpm下摇床振荡反应32h后,柱前手性衍生-hplc监测d-草铵膦反应完全,l-草铵膦浓度为156mmol/l,ee99.5%。
实施例6:细胞循环使用
反应体系同实施例3。实施例5中的细胞离心后,加入反应体系中,30℃、180rpm下摇床振荡反应40h后,柱前手性衍生-hplc监测d-草铵膦反应完全,l-草铵膦的生成浓度为150mmol/l,ee99.3%。
实施例7:细胞循环使用
反应体系同实施例3。实施例6中的细胞离心后,加入反应体系中,30℃、180rpm下摇床振荡反应48h后,柱前手性衍生-hplc监测d-草铵膦反应完全,l-草铵膦的生成浓度为140mmol/l,ee99.2%。
- 还没有人留言评论。精彩留言会获得点赞!