衍生醛基嘧啶的方法、检测5-醛基胞嘧啶的方法以及醛基嘧啶衍生物的应用与流程
本发明涉及核酸化学技术领域,具体涉及一种衍生醛基嘧啶的方法、检测5-醛基胞嘧啶的方法以及醛基嘧啶衍生物的应用。
背景技术:
哺乳动物细胞或组织dna中,特别是cpg岛,都存在着不同程度的甲基化修饰,这与胚胎发育,肿瘤、精神、血液系统等重大疾病的发生发展密切相关。dna甲基化是指dna甲基转移酶(dnmt)以腺甲硫氨酸为甲基供体在胞嘧啶的5位碳上添加甲基使之转变为5-甲基胞嘧啶(5mc)的过程,并且此过程是动态可逆的,即dna去甲基化。dna去甲基化可分为主动和被动两种不同的形式。前者是由于dna甲基化维持机制受到抑制,例如dnmt1失活,dna甲基化水平在dna的连续半保留复制过程中逐渐被稀释;后者是指在tet等多种酶的参与下,5mc持续氧化并经由一系列中间体最终转化为胞嘧啶的过程。
5-醛基胞嘧啶(5fc)作为主动去甲基化过程的中间体,对于维持生命体正常的甲基化水平具有重要意义。2015年,有文献报道称通过监测不同生长阶段小鼠组织dna中所有胞嘧啶衍生物的含量变化,首次提出5fc是一种稳定的表观遗传学修饰,其丰度与其上游产物5-甲基胞嘧啶(5mc)、5-羟甲基胞嘧啶(5hmc)及下游产物5-羧基胞嘧啶(5cac)没有必然联系。另有报道表明,与5hmc、5cac相比,5fc拥有更多的蛋白结合位点及更为独特的碱基分布规律,使之在基因调控、改变dna结构、细胞分化及重大疾病等特殊生物事件中扮演着更为重要的角色。
在复杂的生理过程中要想更加深入地研究5fc的生理学功能,关键在于开发高选择性、高灵敏度的检测技术来准确测定dna中的5fc水平。
液相色谱-串联质谱(lc-ms/ms)因其自身特点在这方面具有显著优势,但是5fc在体内的丰度极低,离子化效率也低,再加上其他高含量经典碱基或稀有碱基以及样品基质中各种各样的杂质干扰,使用lc-ms/ms技术准确测定5fc仍然具有一定的挑战性。
鉴于此,研究者们开始尝试利用化学反应将一些更为疏水的或易于离子化的基团共价修饰到5fc的骨架上去,从而改善5fc在液相分离时与诸多干扰项的分离分辨率,同时提高在质谱检测过程中的离子化效率。但是目前,针对5fc的活泼醛基,仅有酰肼和磺酰肼类衍生物涉及到此类应用。但是,这种基于席夫碱反应机理生成的c=n双键不够稳定,易于水解,这对本身就比较耗时的lc-ms/ms来说极为不利。
另外,相比于传统的lc-ms/ms,荧光传感技术拥有选择性好、响应时间短、操作简单、可裸眼观察等优势,先后被广泛应用于活细胞乃至动物体内活性氧、活性硫、酶、核酸等生物靶标的检测。特别是有机小分子荧光探针因其具有易修饰、成本低等特点,受到了众多科研工作者的青睐。近年来,着眼于5fc的c-5位醛基,相继有报道称其能被-nh2、-nhnh2、-onh2、吲哚等衍生物荧光标记。然而,5-醛基尿嘧啶(5fu)作为胸腺嘧啶(t)的氧化产物,与5fc的结构极为类似,但其醛基的反应活性远胜于5fc,所以上述基于席夫碱反应或aldol缩合的荧光探针将优先与5fu反应。也就是说,这类试剂并不能区分这两种醛基嘧啶,无法实现5fc的特异性荧光识别。
目前,有研究者利用含有侧链活性基团的活泼亚甲基化合物,例如丙二腈、1,3-茚满二酮、乙酰乙酸乙酯等,首次实现了5fc的特异性化学标记,并将此法进一步应用于5fc相关的测序、检测、成像及诊疗等方面。公开的这类试剂,除了含有与醛基缩合的活泼亚甲基之外,还在紧邻亚甲基的位置设置了能与5fc的环外4-nh2发生分子内环化反应的侧链活性基团。如此一来,要想成功被这类试剂衍生,5-cho和4-nh2缺一不可,这也是实现5fc高度特异性标记的关键所在。另外一则类似的报道,公开了一例含有-ch2cn结构的有机小分子,其中-ch2-负责与5fc的5-cho缩合,而-cn则负责与4-nh2环化,从而选择性点亮5fc。
但是,上述鲜见的两例拥有高度特异性的醛基化试剂在标记5fc时均存在耗时较长,需10~24h,推测可能的原因是-ch2-对-cho的亲核性较弱导致反应活性低。
因此,发展更为高效、快速的5fc标记试剂及检测方法在本领域具有重大意义。
技术实现要素:
本发明的目的在于提供一种衍生醛基嘧啶的方法、检测5-醛基胞嘧啶的方法以及醛基嘧啶衍生物的应用,以解决现有5fc的检测和识别工艺中存在的耗时长、条件苛刻的问题。
wittig反应(叶立德反应)是德国化学家g.wittig于1953年发现的,主要用于醛、酮直接合成烯烃。该方法具有收率高、反应条件温和、选择性好等优点。本发明的申请人鉴于5fc带有一个活泼的醛基,同时总结前人的经验,采用氰基取代的wittig试剂,通过wittig烯化及光辅助的分子内关环反应实现对5fc的选择性荧光识别和定量检测。同时,由于5fu的反应活性高于5fc,wittig烯化定能同时衍生这两种醛基嘧啶,这也为5fc/5fu的lc-ms/ms分析提供了一种新的衍生策略。
本发明的技术方案如下:
一种衍生醛基嘧啶的方法,将醛基嘧啶与氰基取代的wittig试剂于有机溶剂中混合,然后用紫外光进行辐射,制得醛基嘧啶衍生物;其中,醛基嘧啶为5-醛基胞嘧啶或5-醛基尿嘧啶。
进一步地,在本发明较佳的实施例中,上述wittig试剂具有如下结构式:
其中,r1为氢,氰基,卤素,烃基或者含o、n、卤素、p、s或si的烃基。
进一步地,在本发明较佳的实施例中,5-醛基胞嘧啶衍生物包括具有如下结构式的两种衍生物:
其中,r为氢、烃基、核糖基或脱氧核糖基,r1为氢,氰基,卤素,烃基或者含o、n、卤素、p、s或si的烃基。
进一步地,在本发明较佳的实施例中,5-醛基尿嘧啶衍生物具有如下结构式:
其中,r为氢、烃基、核糖基或脱氧核糖基,r1为氢,氰基,卤素,烃基或者含o、n、卤素、p、s或si的烃基。
进一步地,在本发明较佳的实施例中,上述有机溶剂包括甲醇、乙醇、异丙醇、乙二醇甲醚、乙二醇二甲醚、乙腈、甲苯、二氯甲烷、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、二氧六环和二甲基亚砜中的一种或多种组合。当为多种溶剂组合时,混合比例可以是任意比。
进一步地,在本发明较佳的实施例中,醛基嘧啶和wittig试剂的摩尔比为1:(1-500),反应温度为15-80℃,反应时间为5min-48h,紫外光的波长为200-400nm,辐射时间为1min-24h。
醛基嘧啶和wittig试剂的摩尔比优选为1:(20-250),更优选为1:(20-50),最优选为1:20。
反应温度优选为50-70℃,更优选为55-65℃,最优选为60℃。
反应时间优选为0.5h-6h,更优选为0.5h-2h,最优选为1h。
紫外光的波长优选为253-365nm,更优选为280-310nm,最优选为280nm。
紫外光的辐射时间优选为0.5h-12h,更优选为0.5h-4h,最优选为1.5h。
上述的方法制得的醛基嘧啶衍生物。
上述的醛基嘧啶衍生物在检测5-醛基胞嘧啶和5-醛基尿嘧啶中的应用。
进一步地,在本发明较佳的实施例中,采用化学衍生辅助的lc-ms/ms技术检测5-醛基胞嘧啶和5-醛基尿嘧啶;采用荧光识别技术识别和检测5-醛基胞嘧啶。
根据本发明制得醛基嘧啶衍生物:5-醛基胞嘧啶衍生物和5-醛基尿嘧啶衍生物通过lc-ms/ms技术可以同时检测出5-醛基胞嘧啶和5-醛基尿嘧啶;进一步地,通过荧光识别技术可以识别出5-醛基胞嘧啶,将5-醛基胞嘧啶与5-醛基尿嘧啶区分。
一种检测5-醛基胞嘧啶的方法,将5-醛基胞嘧啶与wittig试剂于有机溶剂中混合,然后用紫外光进行辐射,得到5-醛基胞嘧啶衍生物,然后,采用荧光识别技术进行识别和检测5-醛基胞嘧啶衍生物。
本发明具有以下有益效果:
本发明先利用wittig试剂同时实现5fc和5fu的化学衍生,由于疏水性丙烯腈结构的引入,使得衍生后的醛基嘧啶保留时间延长,与其他碱基的分离分辨率也得到提高,由此对化学衍生辅助的lc-ms/ms分析更为有利。进一步地,在wittig试剂烯化之后,结合光催化的“多米诺”反应,实现5fc的选择性荧光识别和定量检测。与传统的胺基衍生物基于席夫碱反应构建的c=n双键相比,本发明利用磷叶立德基于wittig反应构建的c=c双键要稳定得多。此外,本发明筛选所得的氰基取代的wittig试剂可通过三步连续反应特异性靶向5fc,这也是胺基、吲哚等衍生物所不具备的。最后,本发明优选的高反应活性的磷叶立德及光辅助的快速关环策略有效弥补了活泼亚甲基类化合物反应耗时长的缺陷。本发明针对5-醛基胞嘧啶提供的wittig衍生反应具有条件温和、高效快速、原料经济易得的优势。
附图说明
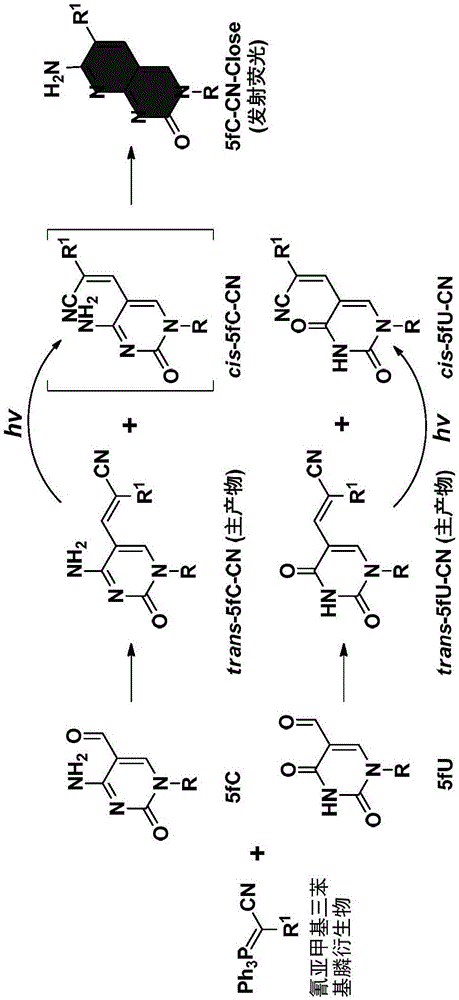
图1为本发明实施例衍生醛基嘧啶的工艺路线图。
图2为5fc与5fu在衍生前后与其他经典碱基或稀有碱基的hplc轨迹对比图。
图3为本发明实施例衍生得到的关环产物5fc-cn-close的激发光谱和发射光谱。
图4为trans-5fc-cn在紫外光辐射下荧光强度随时间的变化曲线图。
图5为本发明实施例的5fc衍生样品的荧光选择性检测图谱。
图6为氰亚甲基三苯基膦对5fc进行荧光定量的标准曲线。
图7为本发明实施例的5fc衍生样品在γ射线辐射前后的荧光强度随时间的变化曲线图。
具体实施方式
以下结合附图对本发明的原理和特征进行描述,所举实例只用于解释本发明,并非用于限定本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
以下实施例中用于标记醛基嘧啶的wittig试剂为氰亚甲基三苯基膦,其结构式为
本发明实施例的合成路线如图1所示,将醛基嘧啶与wittig试剂于有机溶剂中混合,然后用紫外光进行辐射,制得醛基嘧啶衍生物;其中,醛基嘧啶为5-醛基胞嘧啶或5-醛基尿嘧啶。
实施例1
本实施例衍生醛基嘧啶的方法,包括:
将醛基嘧啶与wittig试剂按照摩尔比为1:1的比例于乙醇中混合,在15℃下反应为48h,然后用波长为200nm的紫外光辐射24h,制得醛基嘧啶衍生物;其中,醛基嘧啶为5-醛基胞嘧啶或5-醛基尿嘧啶。
实施例2
本实施例衍生醛基嘧啶的方法,包括:
将醛基嘧啶与wittig试剂按照摩尔比为1:500的比例于n,n-二甲基甲酰胺中混合,在80℃下反应为5min,然后用波长为400nm的紫外光辐射1min,制得醛基嘧啶衍生物;其中,醛基嘧啶为5-醛基胞嘧啶或5-醛基尿嘧啶。
实施例3
本实施例衍生醛基嘧啶的方法,包括:
将醛基嘧啶与wittig试剂按照摩尔比为1:20的比例于乙二醇二甲醚中混合,在50℃下反应为6h,然后用波长为253nm的紫外光辐射12h,制得醛基嘧啶衍生物;其中,醛基嘧啶为5-醛基胞嘧啶或5-醛基尿嘧啶。
实施例4
本实施例衍生醛基嘧啶的方法,包括:
将醛基嘧啶与wittig试剂按照摩尔比为1:250的比例于乙二醇二甲醚中混合,在70℃下反应为0.5h,然后用波长为365nm的紫外光辐射0.5h,制得醛基嘧啶衍生物;其中,醛基嘧啶为5-醛基胞嘧啶或5-醛基尿嘧啶。
实施例5
本实施例衍生醛基嘧啶的方法,包括:
将醛基嘧啶与wittig试剂按照摩尔比为1:50的比例于乙二醇二甲醚中混合,在65℃下反应为1h,然后用波长为300nm的紫外光辐射45min,制得醛基嘧啶衍生物;其中,醛基嘧啶为5-醛基胞嘧啶或5-醛基尿嘧啶。
实施例6
本实施例衍生醛基嘧啶的方法,包括:
将醛基嘧啶与wittig试剂按照摩尔比为1:40的比例于乙二醇二甲醚中混合,在65℃下反应为40min,然后用波长为310nm的紫外光辐射30min,制得醛基嘧啶衍生物;其中,醛基嘧啶为5-醛基胞嘧啶或5-醛基尿嘧啶。
实施例7
本实施例衍生醛基嘧啶的方法,包括:
将醛基嘧啶与wittig试剂按照摩尔比为1:20的比例于乙二醇二甲醚中混合,在60℃下反应为1h,然后用波长为280nm的紫外光辐射1.5h,制得醛基嘧啶衍生物;其中,醛基嘧啶为5-醛基胞嘧啶或5-醛基尿嘧啶。
通过本发明实施例衍生得到醛基嘧啶衍生物:5-醛基胞嘧啶衍生物和5-醛基尿嘧啶衍生物,可用于检测醛基胞嘧啶和醛基尿嘧啶。检测的方法可采用lc-ms/ms分析法。
基于本发明实施例的衍生方法,还可以对5-醛基胞嘧啶进行检测,以确定dna中的5fc水平。5-醛基胞嘧啶在与wittig试剂反应后,其产物trans-5fc-cn在紫外光辐射转变为其异构结构:cls-5fc-cn,cis-5fc-cn的环外4-nh2与距离较近的-cn进行分子内缩合环化反应,得到能够发射荧光的最终衍生物:5fc-cn-close。以此,再通过荧光标记方法可实现对5fc的检测和定量分析。
试验例15fc和5fu经氰亚甲基三苯基膦衍生后的hplc行为变化研究
取两个1.5ml离心管,分别加入0.5mg5fc和0.5mg5fu,然后分别加入11.8mg氰亚甲基三苯基膦(20eq.)以及0.75ml甲醇于两个离心管中,超声溶解并混匀,置于60℃摇床反应1h,然后加入等体积的水稀释一倍,进行hplc分析。同时,将未经修饰的经典碱基或稀有碱基配成0.5mg/ml的水溶液,包括腺嘌呤(a)、鸟嘌呤(g)、尿嘧啶(u)、胞嘧啶(c)、5-羟甲基尿嘧啶(5hmu)、t、5mc、5hmc、5fc和5fu,并在同等条件下进行hplc分析。
如图2所示,除a之外,其他碱基的保留时间均集中在4~6min,且相互之间的分离分辨率较低,尤其是g、t、5mc三种碱基非常逼近5fc和5fu,这对于lc-ms/ms分析来说是极为不利的。而经wittig试剂衍生后的醛基嘧啶,保留时间直接延长到10min以上,明显与其他碱基区别开,如此一来可以尽可能地减小他们对5fc、5fu在lc-ms/ms分析过程中的离子抑制。另外,衍生引入的丙烯腈结构导致疏水性增加,意味着需要极性更小的流动相(也就是更大比例的有机溶剂)来洗脱,这也有利于提高目标分析物的离子化效率。
由此,本发明利用wittig试剂可以同时高效地衍生5fc和5fu,生成的核苷加合物保留时间延长,与其他碱基的分离度也大大提升,这可以提高5fc和5fu在lc-ms/ms检测中的灵敏度。
图3为关环产物5fc-cn-close的激发光谱和发射光谱。
试验例2光辅助的分子内关环反应研究
将750μltrans-5fc-cn的pbs水溶液(0.1mm)置于1cm石英比色皿中,搅拌条件下,用280nm的led光源辐射石英比色皿的一侧,每隔一段时间取出50μl稀释至3mlpbs中测荧光(λex=345nm),记录410nm处的荧光发射强度,并绘制强度-时间变化曲线。
如图4所示,在开始辐射的1.5h内,荧光强度随辐射时间迅速增长,随后趋于平衡,并在很长一段时间内保持荧光强度基本不变,说明关环产物的光稳定性较好。由此可知,1.5h的紫外光辐射足以使trans-5fc-cn完全转化为关环产物。因此,先经wittig试剂衍生,再经历1.5h的紫外光辐射,可以直接扫描样品的荧光光谱进行定量分析。加上1h的衍生反应时间,本发明的反应总时可缩短至2.5h,相比于现有技术的10~24h,有很大进步,大大节约了时间成本,提高了检测效率。
试验例3氰亚甲基三苯基膦对5fc的荧光选择性研究
将核苷(10mm溶于dmso,1μl)、氰亚甲基三苯基膦(100mm溶于dmso,2μl)以及100μl甲醇加入1.5ml离心管中,混匀,60℃反应1h。反应结束后,加入900μlpbs,混匀后转移至1cm石英比色皿中,搅拌条件下,用280nm的led光源辐射1.5h,随后不经额外纯化直接扫描荧光光谱(λex=345nm)。
如图5所示,仅5fc对应得到的衍生样品在410nm处有明显的荧光增强,a、g、c、t、u、5mc、5hmc、5hmu,甚至5fu,与wittig试剂共孵并光照后,其荧光发射光谱与探针组基本重叠,说明氰亚甲基三苯基膦对5fc具有高度特异性的荧光识别能力。
试验例4氰亚甲基三苯基膦对γ射线辐射造成的5fc突变进行荧光定量分析
据文献报道(madugundu,g.s.etal.nucleicacidsres.2014,42,7450),5mc经γ射线辐射可突变为5fc。本试验例意欲检测γ射线对5mc的突变能力。
首先,将500μl5mc的水溶液(10mm)暴露于60coγ射线源之下,并以16.7gy/min的速率辐射90min。辐射结束后,冻干,继续加入氰亚甲基三苯基膦和100μl甲醇,混匀,60℃反应1h。反应结束后,加入900μlpbs,混匀后转移至1cm石英比色皿中,搅拌条件下,用280nm的led光源辐射1.5h,随后不经额外纯化直接扫描荧光光谱(λex=345nm),如图7所示。记录410nm处的荧光强度,再根据如图6所示的标准曲线计算经γ射线辐射后样品中的5fc含量,进而求得γ射线对5mc的突变能力为(0.255fc/106碱基)/gy。
综上所述,本发明利用氰基取代的wittig试剂采用一锅法同时完成5-醛基胞嘧啶(5fc)和5-醛基尿嘧啶(5fu)的高效衍生,得到包含丙烯腈结构的核苷加合物,并以e式构型为主。本发明所得核苷加合物疏水性增加,在进行反相hplc分离时保留时间延长,同时与其他经典碱基或稀有碱基的分离度也大大提高,这对于提高5fc和5fu在lc-ms/ms分析过程中的检测灵敏度十分有利。5fc对应的e式核苷衍生物,其丙烯腈结构在紫外光辐射下可发生顺反异构化,从而拉近氰基与环外4-氨基的空间距离,为分子内环加成反应创造了有利条件,最终生成发射强荧光的新型核苷;而5fu因缺乏环外4-氨基,不能完整地经历上述过程,这使得选择性荧光检测5fc的策略得以实现。
本发明筛选所得的氰基取代的wittig试剂已经商业化,同时该衍生反应条件温和、高效快速,有效拓展了wittig试剂在表观遗传学领域的应用,也为醛基嘧啶的化学标记和反应型5fc荧光探针的设计提供了新思路。
以上对本发明所提供的利用wittig试剂高效衍生5-醛基胞嘧啶的方法及其在lc-ms/ms分析和荧光定量检测方面的应用进行了详细介绍。为了更清楚地阐述本发明的原理和技术方案,本文应用了部分具体实施例及相关附图辅助说明。应当指出,以上实施例及相关附图只是用于帮助理解本发明的方法及中心思想,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也落入本发明权利要求的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!