脂肪基取代的噻唑啉酮化合物、其制备方法、药用组合物及应用与流程
本发明涉及药物化学技术领域,尤其涉及一种脂肪基取代的噻唑啉酮化合物、其制备方法、药用组合物及应用。
背景技术:
炎症小体是由固有免疫相关感受器蛋白组成的一种大的蛋白复合物,主要包括nlrp1、nlrp3、ipaf以及aim2、ifi16炎症小体。在激动剂的作用下,感受器蛋白能够通过接头蛋白asc,招募pro-caspase1,形成大的多聚蛋白复合物,即炎症小体。活化的炎症小体可以导致pro-caspase1自剪切,形成有活性的caspase1,而活化的caspase1,可以介导细胞的焦亡,以及il-1β、il-18的成熟和分泌。而不同于其他的炎症小体,nlrp3炎症小体既能识别外源的病因相关分子模式,又能识别内源的危险相关分子模式,nlrp3炎症小体的过度活化与很多疾病相关,如肠炎、肝炎、硅肺、石棉肺和矽肺、白塞病、类风湿关节炎、紫外线所诱导的皮肤晒伤和接触性超敏反应、脓毒血症、肿瘤、阿尔海默,帕金森病、抑郁症、二型糖尿病、动脉粥样硬化、痛风、非酒精性脂肪肝炎以及非酒精性脂肪肝病、酒精性肝病、肾病、家族性冷自发炎综合征(fcas),muckle-wells综合征(mws),慢性婴儿神经皮肤和关节(cinca)综合征和新生儿发作多系统炎性疾病(nomid)、肌萎缩侧索硬化、哮喘、急性呼吸窘迫综合征等。这也提示可以通过抑制nlrp3炎症小体的活化来抑制相关的疾病。
目前临床治疗nlrp3炎症小体过度活化的疾病是通过抑制il-1β的功能来实现的,主要包括il-1β受体拮抗剂、il-1β单克隆抗体以及il-1β受体阻断剂,在治疗nlrp3炎症小体相关疾病过程中起到了一定作用,但是也存在一定的缺陷。首先,nlrp3炎症小体活化时,不只导致il-1β的成熟和分泌,其他的炎性细胞因子il-18、hmgb1以及细胞焦亡都有发生,而这些也参与到了nlrp3炎症小体相关疾病的发生发展过程中去。另外,il-1β不止nlrp3炎症小体活化会产生,其他炎症小体活化过程也有产生,而通过抑制il-1β,可能对机体的其他正常生理功能造成影响,从而产生一系列副作用。这也提示靶向nlrp3炎症小体,能更好的起到治疗相关疾病的目的。
目前的nlrp3炎症小体抑制剂虽然对nlrp3炎症小体相关的疾病都有一定的缓解作用,但是其作用机制并不够直接,而是通过其他一些信号通路起作用,副作用未知,其应用前景不明。而除了通过抑制nlrp3炎症小体相关上游信号来抑制炎症小体的活化之外,还可以直接靶向nlrp3炎症小体的组分来影响nlrp3炎症小体的组装,但是asc以及caspase1不仅在nlrp3炎症小体中起作用,在其他炎症小体活化过程中也起着至关重要的作用。所以特异性靶向nlrp3是抑制nlrp3炎症小体相关疾病的最佳选择。
技术实现要素:
有鉴于此,本发明要解决的技术问题在于提供一种脂肪基取代的噻唑啉酮化合物、其制备方法、药用组合物及应用,具有抑制nlrp3炎症小体的活性。
为解决以上技术问题,本发明提供了一种脂肪基取代的噻唑啉酮化合物,具有式ⅰ所示结构或其异构体、前药、药学上可接受的溶剂化物或盐:
其中,r1选自取代或非取代的c3~c10的支链烷基,c1-c10含氧烷基,c1-c10含硫烷基,c1-c10含氮烷基,c2~c10的含不饱和键的烷基,c1-c10烷氧基,c1-c10烷氨基或c3-c12环烷基;
r2,r3,r4,r5和r6各自独立地选自:
氢,卤素,硝基,羟基,巯基,氨基,氰基,四唑基;取代或非取代的c1-c6烷基,c1-c6含氧烷基,c1-c6含氮烷基,c1-c6烷氧基,c1-c6烷氨基,c3-c7环烷基;取代或非取代的甲酰基或磺酰基;
x1和x2各自独立地选自o或s;
n为1~6的任意整数。
更优选的,所述r1选自取代或非取代的c3~c6的支链烷基,c2-c6含氧烷基,c1-c6含硫烷基,c2-c6含氮烷基,c2~c6的含碳碳不饱和键的烷基,c1-c6烷氧基,c1-c6烷氨基或c3-c12环烷基。
进一步优选的,所述r1选自取代或非取代的异丙基,异丁基,仲丁基,叔丁基,异戊基,新戊基,3-戊基;取代或非取代的c3-c7环烷基;所述c3-c7环烷基任选的被c1~c6烷基,卤素,硝基,羟基,巯基,氨基或氰基取代。
本发明中,所述支链烷基的碳原子个数优选为3~10个,更优选为3~6个,进一步优选为3~5个。在本发明的一些具体实施例中,所述支链烷基具体为异丙基,异丁基,仲丁基,叔丁基,异戊基,新戊基,3-戊基(即1-乙基丙基)。
所述含氧烷基的碳原子个数优选为1~10个,更优选2~10个,进一步优选为2~6个,再进一步优选为2~5个。当碳原子个数大于1个,如为2~10个时,亦称脂肪醚基,是指烷基骨架被一个或多个烷氧基取代所成的基团,碳原子总数为2~10个。在本发明的一些具体实施例中,所述含氧烷基具体为甲氧基甲基、甲氧基乙基、乙氧基甲基、乙氧基乙基或甲氧基乙氧基甲基等。
所述含硫烷基的碳原子个数优选为1~10个,更优选为1~6个,进一步优选为1~5个。指在烷基的一个或多个碳碳键之间具有s原子,或者r1的烷基基团通过硫原子与母核连接,所述含硫烷基的硫原子个数可以为一个或多个,在此没有特殊限定,优选为1~5个,进一步优选为1~3个。在本发明的一些具体实施例中,所述含硫烷基具体为甲硫基、乙硫基、甲硫基甲基、甲硫基乙基、乙硫基甲基或乙硫基乙基等。
所述含氮烷基的碳原子个数优选为1~10个,更优选2~10个,进一步优选为2~6个,再进一步优选为2~5个。当碳原子个数大于1个,如为2~10个时,指在烷基的一个或多个碳碳键之间具有n原子,所述含氮烷基的氮原子个数可以为一个或多个,在此没有特殊限定,优选为1~5个,进一步优选为1~3个。在本发明的一些具体实施例中,所述含氮烷基具体为n-甲基氨基甲基、n-甲基氨基乙基、n-乙基氨基甲基或n-乙基氨基乙基等。
所述c2~c10的含不饱和键的烷基优选为c2~c10的含碳碳不饱和键的烷基,所述碳碳不饱和键进一步优选为碳碳双键或碳碳三键。所述含不饱和键的烷基的碳原子个数进一步优选为2~6个,在本申请的一些具体实施例中,所述含不饱和键的烷基具体为烯丙基、4-烯基丁基、炔丙基或4-炔基丁基等。
所述烷氧基的碳原子个数优选为1~10个,进一步优选为1~6个,再进一步优选为1~5个,是指烷基通过氧原子与母核相连。在本发明的一些具体实施例中,所述烷氧基具体为甲氧基、乙氧基、丙氧基、异丙氧基等。
所述烷氨基的碳原子个数优选为1~10个,进一步优选为1~6个,再进一步优选为1~5个,是指烷基通过氮原子与母核相连。在本发明的一些具体实施例中,所述烷氨基具体为甲氨基、乙氨基、丙氨基、异丙氨基等。
所述环烷基的碳原子个数优选为3~12个,更优选为3~7个。所述环烷基可以为三元~七元环烷基。在本申请的一些具体实施例中,所述环烷基具体为环丙基、环丁基、环戊基、环己基或环庚基。
本发明中,上述c3~c10的支链烷基,c1-c10含氧烷基,c1-c10含硫烷基,c1-c10含氮烷基,c2~c10的含不饱和键的烷基,c1-c10烷氧基,c1-c10烷氨基或c3-c12环烷基均为取代或非取代基团。
可任选的被以下基团取代:
卤素,硝基,羟基,巯基,氨基,氰基,磺酸基、酰胺基和c1~c6烷基中的一种或多种。
所述卤素为氟、氯、溴或碘。
所述c1~c6烷基更优选为c1~c5烷基,进一步优选为c1~c3烷基。在本申请的一些具体实施例中,所述c1~c6烷基具体为甲基、乙基、丙基、异丙基、丁基、异丁基,仲丁基或叔丁基等。
上述取代基的个数可以为一个或多个,本发明中没有特殊限定。
本发明优选的,所述r2,r3,r4,r5和r6各自独立地选自:
氢,卤素,硝基,羟基,巯基,氨基,氰基,四唑基;取代或非取代的c1-c6烷基,c2-c6含氧烷基,c2-c6含氮烷基,c1-c6烷氧基,c1-c6烷氨基,c3-c7环烷基;羧基,磺酸基;取代或非取代的c1~c10烷基甲酰基,c3-c7环烷基甲酰基,氨基甲酰基,c1~c10烷氨基甲酰基,c3~c10环烷基氨基甲酰基,三元~六元杂环基氨基甲酰基,c6~c12芳基氨基甲酰基,c5~c12杂芳基氨基甲酰基或三元~六元含氮杂环基甲酰基;取代或非取代的c1~c10烷基磺酰基,c3-c7环烷基磺酰基,氨基磺酰基,c1~c10烷氨基磺酰基,c3~c10环烷基氨基磺酰基,三元~六元杂环基氨基磺酰基,c6~c12芳基氨基磺酰基,c5~c12杂芳基氨基磺酰基或三元~六元含氮杂环基磺酰基。
所述c1~c6烷基更优选为c1~c5烷基。在本发明的一些具体实施例中,所述c1~c6烷基具体为甲基、乙基、丙基、异丙基,正丁基、异丁基,仲丁基,叔丁基,正戊基、异戊基,新戊基或3-戊基(即1-乙基丙基)等。
所述c1~c6含氧烷基优选为c2~c6含氧烷基,进一步优选为c2~c5含氧烷基,再进一步优选为c2~c3含氧烷基。当碳原子个数大于1个,如为2~6个时,亦称脂肪醚基,是指烷基骨架被一个或多个烷氧基取代所成的基团,碳原子总数为2~6个。在本发明的一些具体实施例中,所述含氧烷基具体为甲氧基甲基、甲氧基乙基、乙氧基甲基,乙氧基乙基或甲氧基乙氧基甲基等。
所述c1~c6含氮烷基优选为c2~c6含氮烷基,进一步优选为c2~c5含氮烷基,再进一步优选为c2~c3含氮烷基。当碳原子个数大于1个,如为2~6个时,指在烷基的一个或多个碳碳键之间具有n原子,所述含氮烷基的氮原子个数可以为一个或多个,在此没有特殊限定,优选为1~5个,进一步优选为1~3个。在本发明的一些具体实施例中,所述含氮烷基具体为n-甲基氨基甲基、n-甲基氨基乙基、n-乙基氨基甲基或n-乙基氨基乙基等。
所述c1~c6烷氧基更优选为c1~c5烷氧基,进一步优选为c1~c3烷氧基,是指烷基通过氧原子与母核相连。在本发明的一些具体实施例中,所述烷氧基具体为甲氧基、乙氧基、丙氧基、异丙氧基等。
所述c1~c6烷氨基更优选为c1~c5烷氨基,进一步优选为c1~c3烷氨基,是指烷基通过氮原子与母核相连。在本发明的一些具体实施例中,所述烷氨基具体为甲氨基、乙氨基、丙氨基、异丙氨基等。
所述c3~c7环烷基更优选为c3~c6环烷基。所述环烷基可以为三元~七元环烷基,优选为三元~六元环烷基。在本申请的一些具体实施例中,所述环烷基具体为环丙基、环丁基、环戊基、环己基或环庚基等。
本发明中,所述c1-c6烷基,c1-c6含氧烷基,c1-c6含氮烷基,c1-c6烷氧基,c1-c6烷氨基,c3-c7环烷基,c1~c10烷基磺酰基,c3-c7环烷基磺酰基,氨基磺酰基,c1~c10烷氨基磺酰基,c3~c10环烷基氨基磺酰基,三元~六元杂环基氨基磺酰基,c6~c12芳基氨基磺酰基,c5~c12杂芳基氨基磺酰基或三元~六元含氮杂环基磺酰基均为取代或非取代基团。
可任选的被以下基团取代:
卤素,硝基,羟基,巯基,氨基,氰基,取代或非取代的c1~c6烷基,c6~c10芳基中的一种或多种。
所述卤素为氟、氯、溴或碘。
所述c1~c6烷基进一步优选为c1~c3烷基。在本申请的一些具体实施例中,所述c1~c6烷基具体为甲基、乙基、丙基、异丙基、丁基、异丁基,仲丁基或叔丁基。
所述c6~c10芳基进一步优选为苯基。
所述c1~c6烷基、c6~c10芳基为取代或非取代基团,可任选的被卤素、c1~c3烷基或c1~c3烷氧基取代。
在本发明的一些具体实施例中,所述取代的c6~c10芳基为甲氧基苯基。
优选的,所述三元~六元含氮杂环基中,n原子与磺酰基或甲酰基相连接。
上述取代基的个数可以为一个或多个,本发明中没有特殊限定。
本发明优选的,所述r2,r3,r4,r5和r6各自独立地选自:
氢,卤素,硝基,羟基,巯基,氨基,氰基,羧基,磺酸基,氨基甲酰基,甲基甲酰基,乙基甲酰基,丙基甲酰基,异丙基甲酰基,丁基甲酰基,异丁基甲酰基,叔丁基甲酰基,甲基氨基甲酰基,乙基氨基甲酰基,丙基氨基甲酰基,异丙基氨基甲酰基,丁基氨基甲酰基,异丁基氨基甲酰基,叔丁基氨基甲酰基,n,n-二甲基氨基甲酰基,n,n-二乙基氨基甲酰基,n,n-二丙基氨基甲酰基,n,n-二异丙基氨基甲酰基,n,n-二丁基氨基甲酰基,n,n-二异丁基氨基甲酰基,n,n-二叔丁基氨基甲酰基;取代或非取代的苯基氨基甲酰基,苄基氨基甲酰基,甲氧基苄基氨基甲酰基,苯乙基氨基甲酰基,环丙基氨基甲酰基,环丁基氨基甲酰基,环戊基氨基甲酰基,环己基氨基甲酰基,1-哌啶基甲酰基,4-吗啉基甲酰基,1-哌嗪基甲酰基,1-吡咯基甲酰基,氨基磺酰基,甲基磺酰基,乙基磺酰基,丙基磺酰基,异丙基磺酰基,丁基磺酰基,异丁基磺酰基,叔丁基磺酰基,甲基氨基磺酰基,乙基氨基磺酰基,丙基氨基磺酰基,异丙基氨基磺酰基,丁基氨基磺酰基,异丁基氨基磺酰基,叔丁基氨基磺酰基,n,n-二甲基氨基磺酰基,n,n-二乙基氨基磺酰基,n,n-二丙基氨基磺酰基,n,n-二异丙基氨基磺酰基,n,n-二丁基氨基磺酰基,n,n-二异丁基氨基磺酰基,n,n-二叔丁基氨基磺酰基;取代或非取代的苯基氨基磺酰基,苄基氨基磺酰基,甲氧基苄基氨基磺酰基,苯乙基氨基磺酰基,环丙基氨基磺酰基,环丁基氨基磺酰基,环戊基氨基磺酰基,环己基氨基磺酰基,1-哌啶基磺酰基,4-吗啉基磺酰基,1-哌嗪基磺酰基或1-吡咯基磺酰基。
本发明中,
术语“甲酰基”指-co-r残基。其中,r为一般取代或非取代氨基、烷基等本发明限定的取代基团。
术语“磺酰基”指-s(o)2-r残基。其中,r为一般取代或非取代氨基、烷基等本发明限定的取代基团。
术语“三元~六元杂环基”指成环的碳原子和杂原子总数为3~6的杂环基。
术语“三元~六元含氮杂环基”指成环的碳原子和杂原子总数为3~6的含n原子的杂环基。
术语“三元~七元环烷基”指成环的碳原子总数为3~7的环烷基。
本发明中,x1和x2各自独立地选自o或s,在本发明的一些具体实施例中,x1为s,x2为o。
n为1~6的任意整数,优选为1~3的任意整数。
在本发明的一些具体实施例中,所述脂肪基取代的噻唑啉酮化合物具有以下任一结构或其顺反异构体:
本发明公开了上述脂肪基取代的噻唑啉酮化合物的制备方法,包括以下步骤:
a)式a所示的脂肪胺类化合物与二氯硫化碳,在碱性条件下进行反应,得到式b所示化合物;
b)式b所示化合物进行碱催化的环化反应,得到式c所示化合物;
c)式c所示化合物与式d所示化合物进行加成反应,得到式ⅰ所示化合物;
上述结构中的r1,r2,r3,r4,r5,r6,n的范围同上,在此不再赘述。
本发明提供的上述化合物的制备方法不限定于上述制备方法,本领域技术人员熟知的其他制备方法也在本发明的保护范围之内。
本发明还提供了一种药物组合物,包括上述脂肪基取代的噻唑啉酮化合物或其盐或上述制备方法制备的脂肪基取代的噻唑啉酮化合物或其盐,以及药学上可接受的载体,赋形剂,稀释剂,辅剂,媒介物或它们的组合。
本发明对所述载体,赋形剂,稀释剂,辅剂,媒介物并无特殊限定,可以为本领域技术人员熟知的适用于药物组合物的载体,赋形剂,稀释剂,辅剂,媒介物。
本发明还提供了一种脂肪基取代的噻唑啉酮化合物或上述药物组合物在制备nlrp3炎症小体抑制剂中的应用,所述脂肪基取代的噻唑啉酮化合物具有式ⅰ所示结构或其异构体、前药、药学上可接受的溶剂化物或盐:
其中,r1选自取代或非取代的c1~c10的烷基,c1-c10含氧烷基,c1-c10含硫烷基,c1-c10含氮烷基,c2~c10的含不饱和键的烷基,c1-c10烷氧基,c1-c10烷氨基,c3-c12环烷基或三元~六元杂环基;
r2,r3,r4,r5和r6各自独立地选自:
氢,卤素,硝基,羟基,巯基,氨基,氰基,四唑基;取代或非取代的c1-c6烷基,c1-c6含氧烷基,c1-c6含氮烷基,c1-c6烷氧基,c1-c6烷氨基,c3-c7环烷基;取代或非取代的甲酰基或磺酰基;
x1和x2各自独立地选自o或s;
n为1~6的任意整数。
其中,所述c1~c10烷基优选为c1~c6的烷基,进一步优选为c1~c5烷基,在本发明的一些具体实施例中,所述c1~c10烷基具体为甲基、乙基、正丙基、异丙基,正丁基、异丁基,仲丁基,叔丁基,正戊基、异戊基,新戊基或3-戊基等。
所述c1~c10烷基为取代或非取代基团,可任选的被以下基团取代:
卤素,硝基,羟基,巯基,氨基,氰基,磺酸基、酰胺基和c1~c6烷基中的一种或多种。
所述卤素为氟、氯、溴或碘。
所述c1~c6烷基更优选为c1~c5烷基,进一步优选为c1~c3烷基。在本申请的一些具体实施例中,所述c1~c6烷基具体为甲基、乙基、丙基、异丙基、丁基、异丁基,仲丁基或叔丁基等。
上述取代基的个数可以为一个或多个,本发明中没有特殊限定。
所述三元~六元杂环基优选为环氧乙烷,环硫乙烷,环氧丁烷,环硫丁烷,呋喃基,吡咯基,噻吩基,咪唑基,吡唑基,噻唑基,噁唑基,吡啶基,嘧啶基,哒嗪基,吡嗪基,吗啉基,吡喃基等。
上述三元~六元杂环基为取代或未取代基团,可任选的被c1~c6烷基,卤素,硝基,羟基,巯基,氨基或氰基取代。
所述c1-c10含氧烷基,c1-c10含硫烷基,c1-c10含氮烷基,c2~c10的含不饱和键的烷基,c1-c10烷氧基,c1-c10烷氨基,c3-c12环烷基的范围同上,在此不再赘述。
r2,r3,r4,r5和r6,x1,x2和n的范围同上,在此不再赘述。
在本发明的一些具体实施例中,上述应用中,所述脂肪基取代的噻唑啉酮化合物具有以下任一结构或其顺反异构体:
本发明经研究发现,上述化合物通过特异性抑制nlrp3炎症小体的活化,进而抑制il-1β和il-18的成熟及分泌,来抑制由nlrp3炎症小体的活化而引起的相关疾病的发生发展。
优选的,所述nlrp3炎症小体抑制剂用于治疗、减轻或预防nlrp3炎症小体引发的炎症性疾病。
上述炎症优选包括中枢系统炎症和/或外周系统炎症。
上述炎症性疾病优选包括:
肠炎、肝炎、硅肺、石棉肺、矽肺、白塞病、类风湿关节炎、紫外线所诱导的皮肤晒伤、接触性超敏反应、肿瘤、帕金森病、阿尔海默病、抑郁症、二型糖尿病、动脉粥样硬化、痛风、非酒精性脂肪肝炎以及非酒精性脂肪肝病、酒精性肝病、肾病、家族性冷自发炎综合征,muckle-wells综合征,慢性婴儿神经皮肤和关节综合征、新生儿发作多系统炎性疾病、多发性硬化症、肌萎缩侧索硬化,哮喘和急性呼吸窘迫综合征中的一种或多种。
上述痛风优选为尿酸盐结晶堆积引起的炎症性疾病。
本发明上述化合物或组合物在应用于制备nlrp3炎症小体抑制剂时,可以单独使用,或与其他药物联合使用。
与现有技术相比,本发明发现了一系列对炎症小体具有抑制活性的化合物,提供了具有式ⅰ所示结构的脂肪基取代的噻唑啉酮化合物,其互变异构体、前药、药学上可接受的溶剂化物或盐,具有抑制nlrp3炎症小体的活性,可用于nlrp3炎症小体相关疾病的治疗。
附图说明
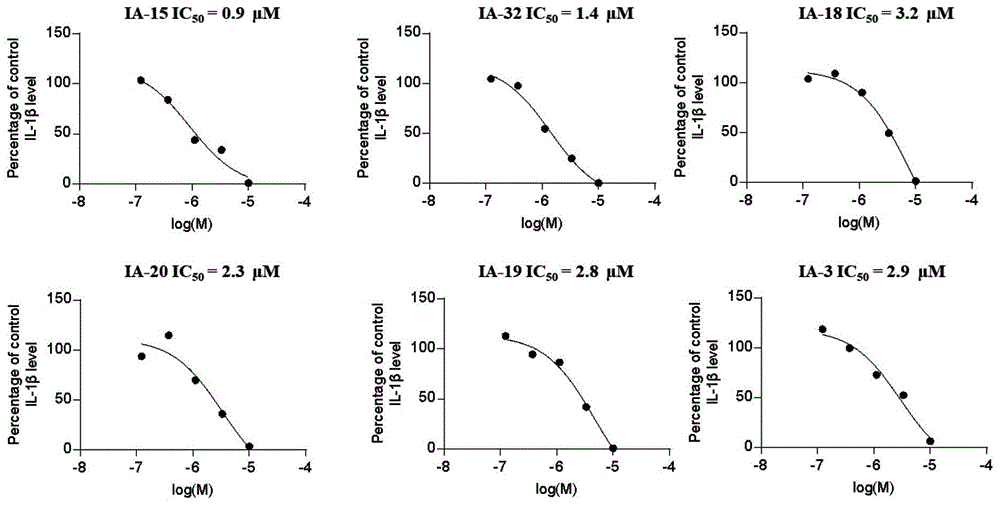
图1为本发明提供的化合物抑制nigericin诱导的nlrp3炎症小体活化的ic50曲线图。
具体实施方式
为了进一步说明本发明,下面结合实施例对本发明提供的脂肪基取代的噻唑啉酮化合物、其制备方法、药用组合物及应用进行详细描述。
实施例1
按照以下路线制备化合物ⅰa-1:
1)化合物2的制备
将化合物1(213mg,3mmol)溶于10ml二氯甲烷中,加入由1230gnahco3和20ml水配成的混合溶液,0℃下缓慢加入硫代光气(0.306ml,4.2mmol)溶于10ml二氯甲烷所得的溶液,然后继续反应1-2h。静置,分液,水相用氯仿萃取,合并有机相用饱和食盐水洗涤,无水na2so4干燥。过滤,浓缩,得到粗品化合物2(158g),淡黄色油状液体。
ms(esi)m/z:113[m+h]+。
2)化合物3的制备
将化合物2(158mg)和巯基乙酸甲酯(0.087ml,1.54mmol)溶于10.0ml无水二氯甲烷中,冰浴中冷却至0℃,逐滴缓慢加入tea(0.058ml),冰浴下继续反应15min后,撤去冰浴,室温反应3-5h,反应体系呈酒红色。120mlch2cl2稀释体系,50ml水萃取一遍,50ml饱和食盐水洗一遍,静置分层,有机相用无水na2so4干燥,过滤,浓缩,油泵抽1-3h,得酒红色固体3(64.2mg,24.5%)。
ms(esi)m/z:187[m+h]+。
3)化合物ia-1的制备
称取化合物3(21mg,0.112mmol),对甲醛苯甲酸(16.8mg,0.112mmol)和无水醋酸钠(92mg,1.12mmol)溶于1ml无水醋酸,130℃微波反应0.5h。待体系冷却至室温,5ml水和3ml甲醇充分混匀离心(3000r/min),得到黄色固体沉淀,玻璃柱纯化(dcm+0.5%hoac)得ia-1(10.9mg,30.4%)。
ms(esi)m/z:320[m+h]+。
按照以上方法,制备表1所示化合物,表1是化合物结构以及结构表征数据。
表1.化合物ia-1—ia-55的结构及表征
生物实验
下述实施案例中的实验方法,如无特殊说明,均为常规实验方法。下述实施案例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到。
il-1βelisa试剂盒:r&d
ultrapurelps:invivogen。
nigericin(尼日利亚菌素):sigma,n7143。
l-929细胞:atcc
实施例2脂肪基取代的噻唑啉酮化合物对nigericin活化的nlrp3炎症小体的抑制分析一、实验方法
1、l-929培养上清的收取
将l-929细胞培养至15cm处理的培养皿中,待细胞铺满后收取培养上清,离心去死细胞,然后过滤去掉其中杂质,-20摄氏度冰箱保存。
2、bmdm细胞的获取
(1)取六周左右野生型小鼠,颈椎脱臼处死小鼠,取后肢腿骨。
(2)在超净台内,将骨中骨髓吹出,离心。
(3)弃上清,裂解红细胞,然后用正常培养基中和,离心。
(4)弃上清,加入含有10%l-929培养上清的正常培养基重悬细胞,分入未处理的细胞培养皿,4天后可以使用。
3、炎症小体刺激
将分化好的bmdm细胞以5×105/ml分入12孔板,第二天换成含有50ng/mllps的opti-mem,刺激3小时。然后加入脂肪基取代的噻唑啉酮化合物0.5小时,再加入nigericin(10μm),0.5小时。上清收集用于elisa。
4、elisa
实验步骤按照r&d公司说明书进行,简述如下:
(1)按比例稀释捕获抗体,然后包板过夜。
(2)用pbst洗三次,然后用10%血清的pbs封闭,室温1h。
(3)用pbst洗三次,加入标准品及样品,室温2h。
(4)用pbst洗三次,按比例稀释并加入检测抗体,室温2h。
(5)用pbst洗三次,按比例稀释并加入hrp,室温20分钟。
(6)用pbst洗三次,加入tmb进行显色。
(7)待变色适度后加入1m硫酸进行终止,然后利用酶标仪进行检测。
(8)做标准曲线,并带入求值。
二、实验结果
1、化合物ia活性数据见下表:
表2化合物ia活性数据
a化合物测试浓度为1μm。
2、根据以上数据结果,对ⅰa-3、ⅰa-15、ⅰa-18、ⅰa-19、ⅰa-20、ⅰa-32抑制nigericin诱导的nlrp3炎症小体活化的ic50进行了分析,结果显示,ⅰa-15效果最好(图1)。
由上述实施例可知,本发明提供的化合物,对nlrp3炎症小体具有高效的抑制作用,其中n=1,2或3的化合物,具有更佳的抑制活性,尤其具有优良的药物应用前景。
以上实施例的说明只是用于帮助理解本发明的方法及其核心思想。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也落入本发明权利要求的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!