本发明涉及生物制药领域,具体涉及一种新型人成纤维细胞生长因子18及其可溶性重组表达方法、制备方法、制剂和应用。
背景技术:
成纤维细胞生长因子(fibroblastgrowthfactor,fgf)是一类由fgf基因家族成员编码的结构相关的蛋白质,对内皮细胞、成纤维细胞、平滑肌细胞等多种中胚层和神经外胚层来源的细胞有促进dna合成和细胞分裂作用,主要由成纤维细胞、内皮细胞、骨细胞、惰性细胞分泌,相对分子量一般在17~34kd。成纤维细胞生长因子18(fibroblastgrowthfactor18,以下简称fgf18)最早由日本科学家ohbayashi在1998年首次从老鼠胚胎中分离得到,在骨骼生长发育过程中扮演着重要的角色。
文献报道(ornitzandmarie,genes&development,16:1446-1465(discussingtheroleofallfgfs,includingfgf18inbonedevelopment),fgf18具有广泛的生理功能,对骨发育、胚胎发育、伤口愈合有影响。文献(ellsworthetal.,osteoarthritisandcartilage(2002)10,308-320;ellsworthetal.stroke(2003)34(6):1507-12)证明fgf18是软骨细胞和成骨细胞的增值剂。研究发现fgf18通过调控fgfr、twist1和bmp骨形态发生蛋白的表达参与整个生命活动过程。临床上研究将fgf18应用于治疗软骨疾病,如骨关节炎(oa)、软骨损伤(ci)、软骨障碍、软骨发育不全、骨骼修复等骨骼性病变。
merckserono公司(默克雪兰诺)研发的fgf18(商品名sprifermin),可引发软骨细胞刺激骨基质合成和软骨细胞更新。2017年acr大会报告的一项国际多中心2期临床研究(forward研究)探讨了骨关节内注射sprifermin对膝关节oa的疗效,其结果显示,关节内注射sprifermin可有效阻止关节软骨的丢失。治疗2年后,sprifermin组的胫骨关节软骨厚度呈剂量耐性增加,每6个月100mg组和每12个月100mg组的软骨厚度分别增加了0.03mm和0.02mm,而安慰剂组减少了0.02mm(p<0.001),各治疗组的womac评分均改善50%,研究期间,药物的安全性良好,各组患者不良反应的发生率相似。sprifermin治疗膝关节炎的ⅱ期临床研究已经顺利完成,正处于ⅲ临床研究。
专利(us7858341)公开了利用基因工程技术,大肠杆菌的原核表达系统,包涵体形式表达无活性的fgf18,再经变性剂溶解、复性、柱层析后得到fgf18,存在工艺繁琐的弊端。
fgf18是肝素结合蛋白,等电点为9.86,氨基酸序列中含有大量碱性氨基酸(赖氨酸和精氨酸),比例高达20.6%,大量负电荷的氨基酸聚集,互相排斥,造成肽键不稳定,n端容易断裂,用于药物制剂很不稳定。目前文献或专利报道的fgf18的结构,均属于碱性蛋白,结构不稳定,n端容易断裂;其制备方法为大肠杆菌中包涵体形式表达,胞内不能形成二硫键,前处理复杂,复性条件苛刻,工业化生产难度大。
技术实现要素:
为了实现上述目的,本发明提供了一种新型人成纤维细胞生长因子18,这种人成纤维细胞生长因子18具有稳定的n端,降低现有技术生长因子18n端容易断裂的问题;另外本发明提供了这种新型人成纤维细胞生长因子18的可溶性表达方法、制备的方法,简化制备的手段、提高其制备效率,方法简单易于推广,得到的n端缺失人成纤维细胞生长因子18可用于治疗骨关节炎或关节软骨损伤。
为实现上述目的,本发明采用了如下的技术方案:
一种新型人成纤维细胞生长因子18,其氨基酸序列如seqidno:1所示。
一种新型人成纤维细胞生长因子18的可溶性重组表达方法,包括如下步骤:
(1)选用含t7启动子的质粒作为表达载体、对应的大肠杆菌作为宿主菌;
(2)seqidno:1对应的cdna的重组子以及表达菌株;
(3)表达菌株诱导表达条件为:温度15~30℃、乳糖或iptg诱导、诱导培养时间4~16小时。
一种新型人成纤维细胞生长因子18的制备方法,包括如下步骤:
(1)利用压力匀浆低温破碎,离心收集上清;
(2)采用阴离子层析捕获细胞破碎上清中fgf18△n;
(3)采用铜离子作为二硫键正确配对促进剂;
(4)二硫键正确配对后肝素亲和层析捕获目的产物。
一种新型人成纤维细胞生长因子18的制剂,按照重量计算,包括:5~50ug/剂的fgf18△n、0.1~0.5mg/剂的表面活性剂泊洛沙姆、10~50mg/剂的稳定剂蔗糖、1.0~5.0mg/剂的n-乙酰葡萄糖醛酸反复交替形成的玻璃酸钠以及400~800ug/剂的抗氧化剂组氨酸。
进一步,这种n端缺失的人成纤维细胞生长因子18的制剂的ph范围为6.50~8.50。
这种n端缺失的人成纤维细胞生长因子18用于治疗骨关节炎或关节软骨损伤。
本发明与现有技术相比,具有如下有益效果:
本发明公开的n端缺失人成纤维细胞生长因子18,即n端缺失12个氨基酸,结构稳定,保留了生物学活性;本发明公开的这种n端缺失人成纤维细胞生长因子的可溶性表达,在不需要变形剂条件下,短时间内二硫键配对率达到90%以上,工艺简单,有利于工业化生产;本发明公开n端缺失人成纤维细胞生长因子18的制剂,保持n端缺失人成纤维细胞生长因子18的活性,用于治疗骨关节炎或关节软骨损伤。
附图说明
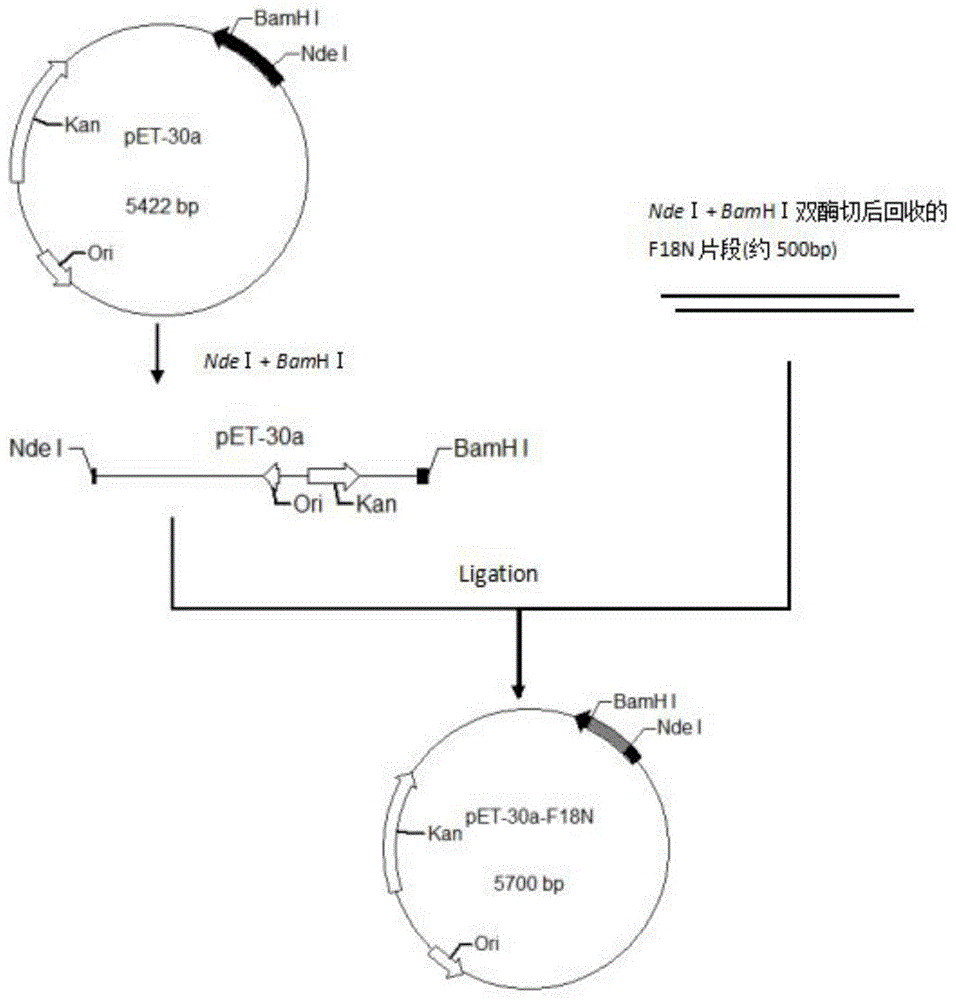
图1:pet-30a-fgf18△n重组质粒构建示意图;
图2:pet-30a-fgf18△n酶切鉴定图,其中,泳道1为酶切鉴定正确的pet-30a-fgf18△n重组质粒;
图3:fgf18的sds-page图,左边泳道柱层析前fgf18△n蛋白;中间泳道为柱层析后fgf18△n蛋白;
图4:fgf18复性前rp-hplc检测图谱,16.098min峰为复性前fgf18△n;
图5:fgf18复性后rp-hplc检测图谱,14.097min峰为复性后fgf18△n;
图6:fgf18和fgf18△n在37℃药品考察箱中考察72h后的断裂电泳检测图;
图7:fgf18和fgf18△n刺激已转染fgfr3ⅲc受体基因的baf3细胞增殖的ec50比率;
图8:fgf18和fgf18△n治疗半月板切断的模型lewis大鼠后,右骨关节增厚对比图:溶媒对照vehicle组(g1)、fgf18治疗组(g2)、fgf18△n治疗组(g3);
图9:fgf18和fgf18△n治疗半月板切断的模型lewis大鼠后,形态学观察对比图:溶媒对照vehicle组(g1)、fgf18治疗组(g2)、fgf18△n治疗组(g3);
图10:fgf18和fgf18△n治疗半月板切断的模型lewis大鼠后,病理切片苏木精-伊红染色图:溶媒对照vehicle组(g1)、fgf18治疗组(g2)、fgf18△n治疗组(g3);
图11:fgf18和fgf18△n治疗半月板切断的模型lewis大鼠后,病理切片番红固绿染色图:溶媒对照vehicle组(g1)、fgf18治疗组(g2)、fgf18△n治疗组(g3)。
具体实施方式
下面通过具体实施方式对本发明作进一步详细的说明:
一种新型人成纤维细胞生长因子18,是人成纤维细胞生长因子18(以下简称fgf18)的n端缺失部分氨基酸所得,以取得具有稳定n端的新型人成纤维细胞生长因子18以下简称为fgf18△n。
一种新型人成纤维细胞生长因子18,其氨基酸序列如seqidno:1所示。
一种新型人成纤维细胞生长因子18的可溶性重组表达方法,包括如下步骤:
(1)选用含t7启动子的质粒作为表达载体、对应的大肠杆菌作为宿主菌;
(2)seqidno:1对应的cdna的重组子以及表达菌株;
(3)表达菌株诱导表达条件为:温度15~30℃、乳糖或iptg诱导、诱导培养时间4~16小时。
一种新型人成纤维细胞生长因子18的制备方法,包括如下步骤:
(1)利用压力匀浆低温破碎,离心收集上清;
(2)采用阴离子层析捕获细胞破碎上清中fgf18△n;
(3)采用铜离子作为二硫键正确配对促进剂;
(4)二硫键正确配对后肝素亲和层析捕获目的产物。
本发明公开的新型人成纤维细胞生长因子18的制备方法包括以下具体步骤:
s1选用含有t7启动子的表达系统作为表达质粒载体、相应的大肠杆菌作为宿主菌;
s2选用两种合适的核苷酸内切酶,分别双酶切质粒载体和n端缺失人成纤维化细胞生长因子18的基因后,连接构建重组质粒,将重组质粒转入大肠杆菌宿主菌筛选重组表达菌菌株;
s3将重组表达菌株转至培养基中一定温度下发酵培养,用适合的诱导剂诱导表达目的蛋白;
s4阴离子层析捕获前体,补入二硫键配对促进剂,短时间内二硫键配对正确,肝素亲和层析得到具有生物活性的fgf18△n蛋白;
步骤s1所述的质粒载体为pet-30a和pet-30c,优选为pet-30a。
步骤s1所述的表达宿主菌为大肠杆菌,更具体为e.colibl21、e.colibl21(de3)、e.colibl21(de3)plyss,优选为e.colibl21(de3)plyss。
步骤s2所述的核苷酸内切酶分别为5'端为ndeⅰ核酸内切酶、3'端为bamhⅰ核酸内切酶。
步骤s3所述的培养基选用适合大肠杆菌生长的培养基,可以是lb、m9ca、m9-ye-glu培养基或在这些培养基基础上的改进及其组合。
步骤s3所述的培养温度,选用为20℃~37℃,优选为37℃。
步骤s3所述的诱导剂,可以选用乳糖、半乳糖或iptg(异丙基-β-d-硫代半乳糖苷),优选为iptg。
步骤s3所述的诱导剂iptg浓度,可以选用0.1mm~2mm,优选为0.2mm。
步骤s3所述的培养时间,可以选用4h~16h,优选为6h。
步骤s4所述的复性促进剂为胱氨酸/半胱氨酸、还原型谷胱甘肽(gsh)/氧化型谷胱甘肽(gssg)、dtt/gssg、铜离子,优选为铜离子。
另外,专利(wo2012172072)公开了一种包含fgf18的冻干制剂,包括fgf18、缓冲剂、泊洛萨姆表面活性剂和蔗糖作为稳定剂,所述fgf18冻干制剂在治疗骨性关节炎或软骨损伤方面显示具有前景的结果。
骨性关节炎(osteoarthritis,oa):又名退行性关节炎,增生性骨关节炎,是一种以关节软骨的变性、破坏及骨质增生为特征的慢性关节病,骨性关节炎的发生率随年龄的增高而增多,是一种常见的老年人的关节病。骨性关节炎的治疗包括药物治疗、手术治疗、非药物治疗。其中药物治疗包括氨基葡萄糖(glcnh2)、非甾体镇痛抗炎药(nsaids)、硫酸软骨素(cs)、透明质酸钠(ha)。
专利(cn106029085)公开了一种包含fgf18的木糖葡聚糖的水凝胶及制剂方法,用于治疗骨关节炎或软骨损伤等软骨疾病。在治疗软骨损伤的疾病中,将包含有fgf18和木糖葡聚糖的水凝胶定向注射到软骨损伤处,促进受损区域中的软骨生长,且不会诱导其它健康区域中正常的软骨失控生长。
在制备包含生物活性蛋白质的药物组合时,制备方式必须使蛋白质的活性维持适当的时间。蛋白质的断裂、变性、聚集、氧化可能造成蛋白质的活性、稳定性的丢失。虽然赋形剂和保护剂可提高蛋白质的稳定性,但这些赋形剂的稳定作用高度依赖于药物制剂中的聚合物、赋形剂的性质、以及生物活性蛋白质本身。
玻璃酸钠(sodiumhyaluronate)又名透明质酸钠,是由n-乙酰葡萄糖醛酸反复交替而形成的一种高分子多糖体生物材料。玻璃酸钠为关节滑液的主要成分,是软骨基质的成分之一,具有参与细胞外液中电解质及水分调节、润滑关节、抗御感染、参与创伤愈合等多种生理功能,对关节的保护、营养及功能的发挥均起重要的作用,主要表现为关节腔的润滑、覆盖屏障及缓冲应力,玻璃酸钠对轻中度的膝关节骨性关节炎具有良好的疗效。由于玻璃酸钠基本上为化学惰性物质,同大多数化学物质具有相容性,在滴眼液中可为许多药物做媒介,产生增效、缓释和降低药物副反应的作用。时下,用玻璃酸钠作为媒介已不局限于骨科和眼科用药,还被加于抗肿瘤药物、非甾体类消炎止痛药物及糖皮质激素中,也具有明显的药物增效和缓释作用。
因此,可用本发明公开的这种新型人成纤维细胞生长因子18为原料来研究开发一种治疗骨性关节炎或软骨损伤性能更好、生物安全性更高的剂型。
本发明公开了这种新型人成纤维细胞生长因子18的制剂,按照重量计算,包括:5~50ug/剂的fgf18△n、0.1~0.5mg/剂的表面活性剂泊洛沙姆、10~50mg/剂的稳定剂蔗糖、1.0~5.0mg/剂的n-乙酰葡萄糖醛酸反复交替形成的玻璃酸钠以及400~800ug/剂的抗氧化剂组氨酸。
其中,fgf18△n含量优选为30ug/剂;表面活性剂泊洛沙姆,含量优选为0.2mg/剂;稳定剂蔗糖含量优选为30mg/剂;n-乙酰葡萄糖醛酸反复交替形成的玻璃酸钠含量优选为2.5mg/剂;抗氧化剂组氨酸含量优选为775ug/剂。
这种新型人成纤维细胞生长因子18的制剂的ph范围为6.50~8.50;制剂ph范围优选为7.0~7.5;最优为7.20。
这种新型人成纤维细胞生长因子18用于治疗骨关节炎或关节软骨损伤。
实例1.n端缺失人成纤维细胞生长因子18的基因工程菌株构建和诱导表达
根据n端缺失人成纤维细胞生长因子18的氨基酸序列(seqidno:1)设计的cdna序列(seqidno:2)。全基因合成,并插入载体质粒puc-57中,得到puc-57-fgf18△n质粒。通过使用ndei,bamhi酶切位点,将fgf18△n基因,与载体质粒pet-30a连接,构建得到pet-30a-fgf△n重组质粒,将上述质粒转化大肠杆菌表达宿主菌bl21(de3)plyss,经表达筛选,构建pet-30a-fgf18△n/bl21(de3)plyss重组工程菌。将工程菌株划线接种,挑选菌苔接种于含培养基试管中,活化后按转接到三角剂中,培养过夜即为上罐种子液。将上罐种子液接种于30l发酵罐中,37℃培养,通过调节转速、通空气量、通纯氧量来保持溶氧>30%,ph保持在7.0。菌液od600=10.0时,加入终浓度为0.2mmiptg,继续培养12小时后停止发酵,离心收集菌体。
实例2.n端缺失人成纤维细胞生长因子18的二硫键形成
菌体重悬后高压匀浆破菌,阴离子层析捕获fgf18△n,用稀释液(20mmtris,ph7.5)等体积比2:1稀释,加入终浓度5um铜离子,4℃低速搅拌4h,hplc检测,二硫键配对率不低于90%,获得活性高的fgf18△n。
实例3.n端缺失人成纤维细胞生长因子18制剂
称取适量泊洛沙姆、蔗糖、组氨酸溶解制成一定浓度,为辅料溶液ⅰ;另称取透明质酸适量,溶胀,高压蒸汽灭菌,为溶液ⅱ;
用注射用水将fgf18△n蛋白液稀释到一定浓度,为溶液ⅲ;
将溶液ⅰ、溶液ⅲ按一定体积比混合,无菌过滤为溶液ⅳ;
将溶液ⅱ与溶液ⅳ等体积混合,ph7.20,分装在小剂中,0.5ml/剂;
冷冻干燥:-45℃预冻180min;第一阶段升华干燥,维持真空度0.8mbar,13h内温度由-45℃~-20℃,并保持10h,10h内-20℃~-10℃,保持10h;解析干燥,-10℃~10℃,保持10h。
每剂含有fgf18△n30ug,泊洛沙姆188200ug,透明质酸2.5mg,蔗糖30mg,组氨酸775.8ug。
实例4.n端缺失人成纤维细胞生长因子18的稳定性考察
fgf18和fgf18△n冻干粉,用注射用水溶解,加入无菌的3ml规格的西林剂中(1ml/支),放置在避光的37℃药品考察箱中,分别在12h、24h、36h、48h、60h、72h时取样,进行sds-page检测,fgf18在12h时逐渐开始降解,60h时全部降解,fgf18△n在72h时没有降解。
实例5.n端缺失人成纤维细胞生长因子18的体外活性测定
已转染fgfr3ⅲc受体基因的baf3细胞,1000rmp,5min离心,用rpmi1640洗涤3次,用rpmi1640含10%fcs(不含il-3)的培养基重悬,细胞计数,将细胞以2-2.5×105个/ml.每孔加入100μl,37℃,5%co2培养26小时。将重组人fgf18标准品、fgf18△n用测活培养液(含培养基1640、10%新生牛血清白蛋白、1ug/ml肝素钠)作5倍倍比稀释(浓度范围0.002u/ml-177u/ml),共做8个稀释度,分别加入各孔,每孔100μl,设立复孔,37℃,5%co2培养48小时,48小时后加入atplite1step10μl/孔,用荧光酶标仪测定结果。根据重组人fgf18标准品和fgf18△n的ec50比率,结果显示两者活性无差异。
实例6.n端缺失人成纤维细胞生长因子18在半月板横断所致大鼠膝关节骨性关节炎模型中的应用
取雄性lewis大鼠,体重为320~380g,随机分为溶媒对照vehicle组(g1)、fgf18治疗组(g2)、fgf18△n治疗组(g3)共三组,每组8只。各组大鼠于治疗开始前右腿膝关节经手术切断内侧半月板整个厚度以模拟完全撕裂,诱导膝关节炎形成,左腿膝关节以假手术方式(手术处理方法一致,以不切断内侧半月板)作为对照。手术后21天开始经关节腔内途径给药,溶媒对照组大鼠每周给予50μl/关节溶媒,连续给药3次;fgf18治疗组大鼠每周给予3μg/关节fgf18,连续给药3次;fgf18△n治疗组大鼠每周给予3μg/关节fgf18△n,连续给药3次,治疗结束后(即治疗3周后),常规解剖收集右膝关节做潜在药理活性的组织病理学评估,以oarsi评分体系对膝关节软骨病变组织学观察进行半定量评分。结果显示,溶媒对照组中产生的修复组织主要是混合的纤维软骨(即ⅰ和ⅱ型胶原蛋白,少量组织ⅳ型胶原蛋白染色),fgf18治疗组和fgf18△n治疗组修复组织为ⅱ型胶原蛋白阳性,并具有清晰的细胞外周ⅳ型胶原蛋白染色,显示成熟的透明软骨修复,证明fgf18治疗组和fgf18△n治疗组疗效无差异。
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。
序列表
<110>重庆派金生物科技有限公司
<120>一种新型人成纤维细胞生长因子18及其可溶性重组表达方法、制备方法、制剂和应用
<160>2
<170>siposequencelisting1.0
<210>1
<211>158
<212>prt
<213>人工序列(artificialsequence)
<400>1
metalaglythralaalaalaalaalavalseralaleuglyleuala
151015
leuthrglyleuthrseralathrserglyleuhisileglyvalleu
202530
glyalaalaileseralaalaglyglyalaglyalaleuthralagly
354045
leuleuvalglythralathrproglyserglyvalalaileleugly
505560
leuglythrglyprothrleucysmetalaalaleuglyleuleuval
65707580
glyleuproalaglythrserleuglycysvalproileglyleuval
859095
leuglyalaalathrthralaleumetseralaleuthrserglythr
100105110
thrvalglyprothrleuleuglyalaproalaleuglyproleuthr
115120125
alaglyalaglyglyalavalhisprometleualathrproleugly
130135140
glyproglyleuglyleuproproleuthrthrthrvalthr
145150155
<210>2
<211>492
<212>dna
<213>人工序列(artificialsequence)
<400>2
catatgaaccagacccgtgcgcgtgacgatgtgagccgtaagcagctgcgtctgtaccaa60
ctgtatagccgtaccagcggcaaacacatccaagttctgggtcgtcgtattagcgcgcgt120
ggtgaagacggcgataaatacgcgcagctgctggttgagaccgacaccttcggcagccaa180
gttcgtatcaagggtaaagagaccgaattttatctgtgcatgaaccgtaagggtaaactg240
gtgggcaagccggatggtaccagcaaagaatgcgtgttcattgagaaggttctggaaaac300
aactacaccgcgctgatgagcgcgaaatacagcggctggtacgttggttttaccaagaaa360
ggccgtccgcgtaagggtccgaaaacccgtgagaaccagcaagatgttcacttcatgaag420
cgttacccgaaaggccagccggaactgcaaaagccgtttaaatataccaccgttaccaag480
taatgaggatcc492