一种射干苷元磺酸钠的制备方法与流程
本发明涉及药物合成领域,具体涉及一种射干苷元磺酸钠的制备方法。
背景技术:
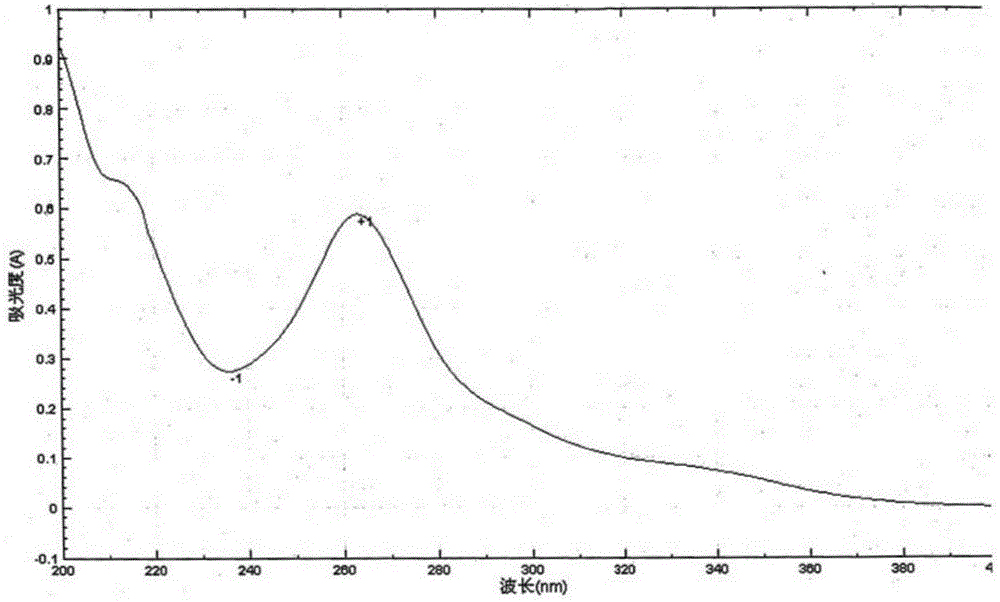
:射干苷元磺酸钠,又称射干苷元-5′-磺酸钠、鸢尾苷元-5′-磺酸钠或鸢尾苷元磺酸钠,化学名为4′,5,7-三羟基-6-甲氧基异黄酮-5′-磺酸钠,分子式c16h11o9sna,分子量402.31,为淡黄色结晶或结晶性粉末,其结构式如(ⅰ)所示:射干苷元磺酸钠为新型的抗病毒药物,其具有抗病毒、抗炎、解热和镇痛作用,可用于治疗急性上呼吸道感染和病毒性肺炎。目前,得到射干苷元磺酸钠的主要方法为:(1)通过分离中药的化学成分,得到射干苷元,再将射干苷元与硫酸通过磺化反应生成水溶性的钠盐;(2)从中药川射干中分离出有效成分射干苷,再将射干苷用盐酸水解为射干苷元,射干苷元与硫酸通过磺化反应生成水溶性的钠盐,化学反应式如下:但是,由于中药成分中苷元含量很低,采用方法(1)存在成本高、收率低的问题。而方法(2)中,需要将射干苷水解得到射干苷元,这一操作需要在加热条件下进行,反应时需要搪瓷反应釜、搅拌器及加热设备等特殊设备,不适合工业化大生产,因此该方法也存在成本高、收率低的问题。所以,现在急需一种路线简单、设备要求低、成本低、收率高的方法来制备射干苷元磺酸钠。技术实现要素:本发明的目的在于提供一种路线简单、设备要求低、成本低、收率高的制备射干苷元磺酸钠的方法。本发明提供了一种制备射干苷元磺酸钠的方法,所述方法包括以下步骤:将射干苷加入硫酸中,反应,然后将体系加入氯化钠的水溶液中,搅拌,析出沉淀,过滤,取固体,即得。进一步地,所述硫酸的浓度为70%~99%,优选为95%~98%。进一步地,所述氯化钠的水溶液为饱和氯化钠水溶液。进一步地,所述射干苷、硫酸、氯化钠的水溶液的质量体积比为1kg:(2-6)l:(20-60)l,优选为1kg:4l:40l。进一步地,所述反应时间为1-5小时,反应温度为20~40℃;优选地,所述反应时间为2小时,反应温度为室温。进一步地,所述步骤中,还包括:将所述固体提纯,提纯工艺为:取固体,在水中加热溶解,趁热过滤,保留液体,静置,析晶。进一步地,所述提纯工艺的操作次数为1-3次。通过试验证明,本发明提供了一种制备射干苷元磺酸钠的简便方法,该方法合成路线简单、设备要求低、成本低、收率高,适合工业化生产,具有广泛的应用前景。显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。附图说明图1为射干苷元磺酸钠对照品的紫外图谱。图2为实施例1制备的射干苷元磺酸钠的紫外图谱。图3为对照例1制备的射干苷元磺酸钠的紫外图谱。图4为射干苷元磺酸钠对照品的红外图谱。图5为实施例1制备的射干苷元磺酸钠的红外图谱。图6为对照例1制备的射干苷元磺酸钠的红外图谱。图7为射干苷元磺酸钠对照品的质谱。图8为实施例1制备的射干苷元磺酸钠的质谱。图9为对照例1制备的射干苷元磺酸钠的质谱。图10为射干苷元磺酸钠对照品的h谱。图11为实施例1制备的射干苷元磺酸钠的h谱。图12为对照例1制备的射干苷元磺酸钠的h谱。图13为射干苷元磺酸钠对照品的c谱。图14为实施例1制备的射干苷元磺酸钠的c谱。图15为对照例1制备的射干苷元磺酸钠的c谱。图16为射干苷元磺酸钠对照品的hplc图。图17为实施例1制备的射干苷元磺酸钠的hplc图。图18为对照例1制备的射干苷元磺酸钠的hplc图。图19为磺化反应过程的hplc监控图;左列为实验例2中对射干苷元磺化反应的hplc监控结果,其中编号为1、2、3、4、5的hplc图谱分别为反应5.0min、30.0min、1.0、2.0、12.0h的结果,a峰为射干苷元,b峰为射干苷元磺酸钠;右列为实验例2中对射干苷磺化反应的hplc监控结果,其中编号为1′、2′、3′、4′、5′的hplc图谱分别为反应5min、30.0min、1.0、2.0、12.0h的结果,a峰为射干苷元,b峰为射干苷元磺酸钠、e峰为射干苷。具体实施方式本发明所用原料与试剂均为已知产品,通过购买市售产品所得。其中:射干苷为自制(制备方法参见发明专利,专利号:zl201610939889.9实例1),含量98.52%。;射干苷元磺酸钠对照品为自制(制备方法参见申请专利,申请号:2018105810925实例3),含量99.65%实施例1、利用本发明的方法制备射干苷元磺酸钠取射干苷1kg,加4l硫酸,搅拌溶解,反应2小时,倾入40lnacl饱和水溶液中,边加边搅拌,析出大量沉淀,放置过夜,过滤,沉淀用水煮沸溶解,趁热过滤,放置,析晶,过滤,取沉淀,再用水重结晶一次,过滤,60℃减压干燥,得射干苷元磺酸钠790g,纯度98.74%,收率(以射干苷计)91.37%,为淡黄色结晶性粉末。化学反应式如下:对照例1利用对照方法制备射干苷元磺酸钠步骤(1):取射干苷1kg,置于10l圆底烧瓶中,加50%乙醇5l,搅拌均匀,再加浓盐酸500ml,摇匀。加热回流3~5小时,待薄层检查无射干苷斑点存在时停止水解反应。取出,趁热过滤,静置过夜,析出淡黄色细长针晶。过滤,用水洗涤结晶至流出液ph近中性,结晶用2l95%乙醇加热溶解,过滤,滤液趁热倾入4.5l沸水中,静置过夜,析晶,过滤,60℃减压干燥,得射干苷元600g,为淡黄色粉末。步骤(2):取步骤(1)制得的射干苷元600g,加2.4l硫酸,搅拌溶解,反应2小时,倾入24lnacl饱和水溶液中,边加边搅拌,析出大量沉淀,放置过夜,过滤,沉淀用水煮沸溶解,趁热过滤,放置,析晶,过滤,沉淀再用水重结晶一次,过滤,60℃减压干燥,得射干苷元磺酸钠700g,纯度98.42%,收率(以射干苷计)81.38%,为淡黄色结晶性粉末。以下通过实验例证明本发明的有益效果。实验例1、质量检测1、实验方法分别取射干苷元磺酸钠对照品、实施例1制备的射干苷元磺酸钠、对照例1制备的射干苷元磺酸钠,进行hplc、紫外、红外、质谱、h谱、c谱测定,图谱见图1~18。2、实验结果检测结果显示三者为同一化合物。实验例2、利用hplc检测磺化反应过程1、实验方法照高效液相色谱法(中国药典2015版四部通则0512)测定。(1)仪器:agilent1100高效液相色谱仪(2)参数设置:以十八烷基硅烷键合硅胶为填充剂;以0.02mol/l磷酸二氢钠水溶液(3.12gnah2po4.2h2o溶于1000ml水中,h3po4调ph值到3.0)为流动相(a),以乙腈为流动相(b),按照a:b=55:45比例混合洗脱;流速:1ml/min;检测波长为263nm,柱温35℃;理论板数按射干苷元磺酸钠峰计算,应不低于2000。将各样品适量注入液相色谱仪中,测定,即得。(3)制样与测试:分别取射干苷元、射干苷,加硫酸进行磺化反应,并在不同时间利用hplc监控其反应体系的组成。具体如下:取射干苷元1.0g,加硫酸4ml,搅拌溶解,放置反应,分别于5.0min、30.0min、1.0h、2.0h、12.0h分别取样,进行hplc分析,结果见图19(图中编号为1、2、3、4、5的hplc图谱分别为反应5.0min、30.0min、1.0、2.0、12.0h的样品,a峰为射干苷元,b峰为射干苷元磺酸钠)。取射干苷1.0g,加硫酸4ml,搅拌溶解,放置反应,分别于5min、30min、1.0h、2.0h、12.0h分别取样,进行hplc分析,结果见图19(图中编号为1′、2′、3′、4′、5′的hplc图谱分别为反应5min、30.0min、1.0、2.0、12.0h的样品,a峰为射干苷元,b峰为射干苷元磺酸钠、e峰为射干苷)。2、实验结果从图19中可以看出,射干苷元的磺化反应,直接生成射干苷元磺酸钠(b峰)及另一未知峰(c峰)成分,随着反应进行(2h),射干苷元(a峰)及c峰成分均消失,生成单一的b峰成分,即射干苷元磺酸钠,但此时另一杂质峰即d峰成分开始生成,若反应12h时,d峰成分明显,推测d峰可能为射干苷元二磺酸钠或射干苷元多磺酸钠。射干苷的磺化反应,反应生成极性很大的f峰成分(此时几无射干苷成分),推测f峰可能为射干苷磺酸钠,然后再逐渐转化为b峰成分即射干苷元磺酸钠(图中a、c、f峰均消失),与射干苷元磺化反应一样,反应2h后,生成单一的射干苷元磺酸钠,同时杂质峰d峰开始生成。由上可知,射干苷元磺化反应为直接生成射干苷元磺酸钠,而射干苷磺化反应先生成射干苷磺酸钠,再脱葡萄糖生成射干苷元磺酸钠。实验例3、射干苷元磺酸钠雌激素样作用评价1、实验方法为了减少内源性雌激素的分泌对试验结果产生的影响,本试验小鼠选用的是初断乳、性未成熟的雌性小鼠(昆明种小鼠30只,雌性,出生后21d(断乳鼠),体重9~12g,购自四川省中医药科学院实验动物中心)。阳性药物为雌二醇注射液(e2),2mg/ml,上海通用药业股份有限公司生产,用植物油配制成35μg/ml的悬浊液。实验动物按体重随机分为3组:阴性对照组、阳性对照组、射干苷元磺酸钠组,每组10只。实验动物适应性饲养6d后,称重,阴性对照组给予等体积植物油;阳性对照组按0.35mg/(kg·d)给予e2;射干苷元磺酸钠按35mg/(kg·d)给予,早、晚各灌胃1次,连续4d。各组动物于最后1次给药后第2天,称重,脱臼处死,分离子宫并称重,计算小鼠子宫系数(即:子宫湿重/体重×100%)及小鼠体重增幅。结果见表1、表2。2、实验结果表1射干苷元磺酸钠对小鼠子宫系数的影响组别体重(g)子宫湿重(g)子宫系数(%)阴性对照组18.563±1.2640.018±0.0030.098±0.006e2组21.438±1.1610.124±0.015*0.575±0.054*射干苷元磺酸钠组21.246±1.2070.121±0.014*0.570±0.046*备注:*与阴性对照组比较,p<0.05表2射干苷元磺酸钠对小鼠体重的影响组别增重(g)用药前后体重增幅(%)阴性对照组4.982±1.17526.81±3.682e2组7.503±0.887*34.953±2.869*射干苷元磺酸钠组7.228±0.842*34.046±2.445*备注:*与阴性对照组比较,p<0.05从上述结果可见,用药后,射干苷元磺酸钠组动物体重增幅显著高于阴性对照组,说明射干苷元磺酸钠有生长促进作用,这与射干苷元磺酸钠具有雌激素样作用有关。由此说明,射干苷元磺酸钠具有雌激素样药理活性。实例4射干苷元磺酸钠对h2o2诱导pc12细胞损伤的保护作用1、实验方法取对数生长期的pc12细胞以1×105个/l接种于96孔板,每孔加入100μl,于37℃、5%co2培养箱中培养24h,分别加入最终浓度为0μg/ml、0.01μg/ml、0.1μg/ml、1.0μg/ml的本发明药物预处理24h,除了空白对照组,其余各组(包括阳性药水溶性ve对照组)分别再加入最终浓度为60μmol/l的h2o2继续培养20h后,每孔加入mtt(5mg/ml)20μl,继续培养4h,吸除上层液体,每孔加入dmso100μl,37℃培养15min,待蓝紫色结晶物完全溶解后,酶标仪检测各组细胞在490nm下的吸光值。照前法计算细胞存活率,结果见表3。2、实验结果表3射干苷元磺酸钠对h2o2诱导pc12细胞损伤的保护作用(n=6)备注:①与空白组比较,δp<0.01;与模型组比较,*p<0.05,**p<0.01②通过试验,h2o2诱导pc12细胞损伤有效作用浓度为60μmol/l,而射干苷元磺酸钠有效作用浓度范围为0.01~1.0μg/ml。上述mtt实验显示,h2o2组od值明显降低,细胞存活率显著低于正常对照组(p<0.0l);而不同浓度射干苷元磺酸钠细胞存活率比h2o2损伤组显著提高,有显著性差异,且呈剂量相关性;射干苷元磺酸钠细胞存活率与阳性药(水溶性ve)对照组比较,相当或更好。所以,上述实验结果表明射干苷元磺酸钠对h2o2诱导pc12细胞损伤有显著的保护作用。综上,本发明提供了一种新的制备射干苷元磺酸钠的方法,该方法路线简单、设备要求低、成本低、收率高,适合工业化生产,具有广泛的应用前景。此外,本发明进一步证明了射干苷元磺酸钠具有新的药理活性,即雌激素样作用、并对h2o2诱导pc12细胞损伤有显著的保护作用,因此,射干苷元磺酸钠在制备治疗雌激素依赖性肿瘤(如乳腺癌、子宫内膜癌等)、阿尔茨海默病的药物上具有良好的应用前景。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1