用于检测CPT2F352C突变的引物、试剂盒及筛选重症EV71易感患儿的系统的制作方法
本发明属于生物医学领域,尤其涉及用于检测cpt2f352c突变的引物、试剂盒及筛选重症ev71易感患儿的系统。
背景技术:
肠道病毒71型(enterovirus71,ev71)属于肠道病毒a组的单股正链小rna病毒,是引起儿童手足口病的最主要的病原体。ev71具有高度的嗜神经性,可引起脑膜炎、脑炎、脑干脑炎及神经源性肺水肿等严重中枢神经系统损害,重症病例病情进展迅速,病死率、致残率高,给国家、社会及家庭施以庞大的压力和负担,已然成为重要的公共卫生问题,引起全球各国的关注和警惕。
前期研究发现肉毒碱棕榈酰基转移酶2(carnitinepalmitoyltransferase2,cpt2)编码基因的第4外显子c.1055t>g/p.f352c(f352c)突变增加了罹患重症ev71感染的风险。细胞内cpt2表达以及酶活性的正常是线粒体进行β-氧化为机体各器官代谢提供能量的重要因素。cpt2f352c突变后cpt2酶的功能缺陷,长链脂肪酸不能被有效转运并参与氧化磷酸化,atp产生减少,外周血中的酰基肉碱浓度明显增高,从而导致一系列的能量及代谢紊乱。
cpt2f352c突变的重症ev71脑炎患儿高热期cpt2活性和atp水平明显低于恢复期,即cpt2f352突变是ev71感染后脑损伤的重要风险因素,因其具有热不稳定性,感染并高热导致cpt2突变体酶活性降低、atp降低,及其导致的细胞因子风暴、氧化应激等加重了宿主血脑屏障的损伤,血脑屏障内皮细胞的损伤,又能进一步刺激细胞因子的产生及炎性细胞的聚集,从而加重脑损伤。然而,目前临床上尚不能及时发现重症ev71感染患儿,以便采取有效的措施在早期给予积极的预防治疗。
技术实现要素:
针对现有技术存在的不足之处,本发明所要解决的技术问题是及时而快捷地发现cpt2f352c突变,进而确定重症ev71感染患儿,有助于在早期给予重症ev71感染患儿积极有效的预防治疗,提出用于检测cpt2f352c突变的引物、试剂盒及筛选重症ev71易感患儿的系统。
为解决所述技术问题,本发明采用的技术方案为:
用于检测cpt2f352c突变的特异性引物,根据cpt2f352c设计特异性上下游引物,具体包括:
本发明还提供了包含如上述技术方案所述的用于检测cpt2f352c突变的特异性引物的试剂盒。
本发明还提供了用于筛选重症ev71易感患儿的系统,包括下述数据处理模块:
模块1,所述模块1用于分析对待测者离体样本进行ev71rna检测得到的检测结果;
模块2,所述模块2用于在所述模块1的分析结果为阳性时,进一步分析利用如上述实施例所述的试剂盒对离体样本进行cpt2f352c检测得到的检测结果;
模块3,所述模块3用于在所述模块2的分析结果为阳性时,初步筛选待测者为或候选为重症ev71易感患儿。
优选的,所述模块1包括:
模块a1,所述模块a1用于分析对待测者离体样本进行ev71rna定性检测得到的检测结果;和/或
模块b1,所述模块b1用于分析对待测者离体样本进行ev71rna病毒载量定量检测得到的检测结果。
优选的,所述模块2包括:
模块a2,所述模块a2用于在所述模块1的分析结果为阳性时,进一步分析利用如上述实施例所述的试剂盒对离体样本进行是否存在cpt2f352c突变的检测得到的检测结果;和/或
模块b2,所述模块b2用于在所述模块1的分析结果为阳性时,进一步分析利用如上述实施例所述的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测得到的检测结果。
优选的,所述模块3包括:
模块a3,所述模块a3用于在所述模块2的分析结果为阳性时,初步筛选待测者为或候选为重症ev71易感患儿;和/或
模块b3,所述模块b3用于在所述模块b2的分析结果为存在cpt2f352c突变的cpt2的表达量相对于无对应突变的离体样本的cpt2的表达量下调时,初步筛选待测者为或候选为重症ev71易感患儿。
优选的,所述离体样本为细胞、组织、脏器、血液、淋巴液、消化液、咳痰、肺胞支气管清洗液、尿或粪便中的任意一种。
与现有技术相比,本发明的有益效果在于:
1、及时而快捷地发现cpt2f352c突变,通过控制其突变者高热的发生来减少重症脑炎和脑病的发生,降低其致残率和死亡率;
2、为揭示重症ev71感染的发病机制,易感人群的早期识别以及治疗提供新的研究视点,使疾病得到更加准确化、个体化的诊断和治疗。
附图说明
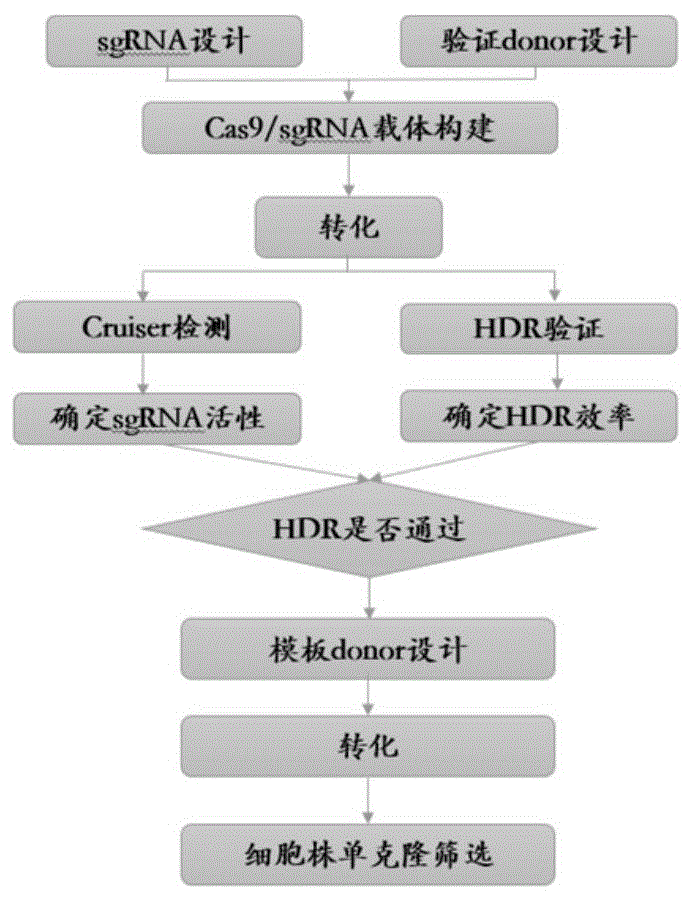
图1为本发明实施例所提供的cpt2f352c点突变星形胶质细胞模型建立流程图;
图2为本发明实施例所提供的ev71和41℃高温刺激后cpt2基因qrt-pcr曲线和cpt2基因含量趋势图;
图3为本发明实施例所提供的给予ev71感染和41℃高热刺激的cpt2f352c小鼠状态图,其中,a为未给予ev71感染和41℃高热刺激的cpt2f352c小鼠,b为ev71感染和41℃高热刺激1d后的cpt2f352c小鼠,c为ev71感染和41℃高热刺激3d后的cpt2f352c小鼠,d为ev71感染和41℃高热刺激5d后的cpt2f352c小鼠,e为ev71感染和41℃高热刺激7d后的cpt2f352c小鼠;
图4为本发明实施例所提供的脑组织的atp水平和cpt2剩余酶活性表达结果示意图,其中,a为cpt2f352c小鼠ev71感染和41℃高热刺激后脑干组织atp水平示意图,b为不同温度条件下,ev71感染和41℃高热刺激后cpt2f352c小鼠脑干组织内cpt2酶活性示意图,c为不同温度条件下,ev71感染和41℃高热刺激后野生型小鼠脑干组织内cpt2酶活性示意图;
图5为本发明实施例所提供的不同时间点电镜下小鼠脑组织线粒体超微结构的改变示意图,其中,a为无ev71感染的野生型小鼠,a为无ev71感染的cpt2f352c小鼠,b1为ev71感染且41℃高热处理3d后的野生型小鼠,b2为ev71感染且41℃高热处理5d后的野生型小鼠,b3为ev71感染且41℃高热处理9d后的野生型小鼠,a为无ev71感染的cpt2f352c小鼠,b1为ev71感染且41℃高热处理3d后的cpt2f352c小鼠,b2为ev71感染且41℃高热处理5d后的cpt2f352c小鼠,b3为ev71感染且41℃高热处理9d后的cpt2f352c小鼠;
图6为本发明实施例所提供的不同时间点电镜下小鼠血脑屏障改变情况示意图,其中,a为无ev71感染的野生型小鼠,a为无ev71感染的cpt2f352c小鼠,b1为ev71感染且41℃高热处理3d后的野生型小鼠,b2为ev71感染且41℃高热处理5d后的野生型小鼠,b3为ev71感染且41℃高热处理9d后的野生型小鼠,a为无ev71感染的cpt2f352c小鼠,b1为ev71感染且41℃高热处理3d后的cpt2f352c小鼠,b2为ev71感染且41℃高热处理5d后的cpt2f352c小鼠,b3为ev71感染且41℃高热处理9d后的cpt2f352c小鼠。
具体实施方式
下面将对本发明具体实施例中的技术方案进行详细、完整的描述。显然,所描述的实施例仅仅是本发明总的技术方案的部分具体实施方式,而非全部的实施方式。基于本发明的总的构思,本领域普通技术人员所获得的所有其他实施例,都落于本发明保护的范围。
本发明实施例提供了用于检测cpt2f352c突变的特异性引物,根据cpt2f352c设计特异性上下游引物,具体包括:
本实施例中提供的如seqidno.1、seqidno.2所示的特异性上下游引物能够有针对性的扩增cpt2f352c基因,便于对cpt2f352c基因进行检测,提高检测的准确性,从而有助于判断cpt2f352c基因是否发生突变。
本发明还提供了包含如上述实施例所述的用于检测cpt2f352c突变的特异性引物的试剂盒。本实施例中的试剂盒可以准确判断cpt2f352c基因是否发生突变,同时操作简单,使用方便。
本发明还提供了用于筛选重症ev71易感患儿的系统,包括下述数据处理模块:
模块1,所述模块1用于分析对待测者离体样本进行ev71rna检测得到的检测结果;
模块2,所述模块2用于在所述模块1的分析结果为阳性时,进一步分析利用如上述实施例所述的试剂盒对离体样本进行cpt2f352c检测得到的检测结果;
模块3,所述模块3用于在所述模块2的分析结果为阳性时,初步筛选待测者为或候选为重症ev71易感患儿。
在上述实施例中,所述数据处理模块通过对待测者检测结果的分析,初步筛选待测者为或候选为重症ev71易感患儿,便于对重症ev71易感患儿提前进行监护,及进行有效的早期预防治疗,通过对重症ev71易感患儿可能发生的高热予以控制,减少重症脑炎和脑病的发生,降低其致残率和死亡率。具体的,当模块1的分析结果为阴性时,则终止分析;当模块1的分析结果为阳性时,模块2进一步分析利用如上述实施例所述的试剂盒对离体样本进行cpt2f352c检测得到的检测结果。当模块2的分析结果为阴性时,则终止分析;当模块2的分析结果为阳性时,模块3初步筛选待测者为或候选为重症ev71易感患儿。
在一优选实施例中,所述模块1包括:
模块a1,所述模块a1用于分析对待测者离体样本进行ev71rna定性检测得到的检测结果;和/或
模块b1,所述模块b1用于分析对待测者离体样本进行ev71rna病毒载量定量检测得到的检测结果。
在上述实施例中,模块a1和模块b1分别从定性和定量两个角度对ev71rna的检测结果进行分析,一方面都可以得到待测者离体样本是否为ev71阳性的结果,另一方面,两个分析结果可以相互印证,保证分析结果的准确性。需要说明的是,当模块a1分析对待测者离体样本进行ev71rna定性检测得到的检测结果时,为了进一步提高检测结果的准确性,模块b1可以同时分析对待测者离体样本进行ev71rna病毒载量定量检测得到的检测结果。因此,本实施例中,所述模块1包括三种方式,分别对应模块a1、模块b1或模块a1和模块b1。
在一优选实施例中,所述模块2包括:
模块a2,所述模块a2用于在所述模块1的分析结果为阳性时,进一步分析利用如上述实施例所述的试剂盒对离体样本进行是否存在cpt2f352c突变的检测得到的检测结果;和/或
模块b2,所述模块b2用于在所述模块1的分析结果为阳性时,进一步分析利用如上述实施例所述的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测得到的检测结果。
在上述实施例中,模块a2和模块b2分别从定性和定量两个角度对cpt2f352c的检测结果进行分析,一方面都可以得到待测者离体样本是否为cpt2f352c阳性的结果,另一方面,两个分析结果可以相互印证,保证分析结果的准确性。
需要说明的是,在所述模块1的分析结果为阳性时,所述模块2分析利用如上述实施例所述的试剂盒对离体样本进行cpt2f352c检测得到的检测结果时,包括三种方式,三种方式分别对应模块a2、模块b2以及模块a2和模块b2。模块a2和模块b2的组合用于分析利用如上述实施例所述的试剂盒对离体样本进行cpt2f352c检测得到的检测结果时,能够进一步提高检测结果的准确性。具体的,在模块a2分析利用如上述实施例所述的试剂盒对离体样本进行是否存在cpt2f352c突变的检测得到的检测结果时,同时模块b2分析利用如上述实施例所述的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测得到的检测结果,同时从定性和定量两个角度对cpt2f352c的检测结果进行分析,提高了检测结果的准确性。
在一优选实施例中,所述模块3包括:
模块a3,所述模块a3用于在所述模块2的分析结果为阳性时,初步筛选待测者为或候选为重症ev71易感患儿;和/或
模块b3,所述模块b3用于在所述模块b2的分析结果为存在cpt2f352c突变的cpt2的表达量相对于无对应突变的离体样本的cpt2的表达量下调时,初步筛选待测者为或候选为重症ev71易感患儿。
在上述实施例中,模块a3和模块b3分别从基因水平以及基因表达量水平两个角度分析检测结果,一方面有利于准确的初步筛选待测者为或候选为重症ev71感染的易感患儿,另一方面有助于揭示重症ev71感染的发病机制,为易感人群的早期识别以及治疗提供新的研究视点,使疾病得到更加准确化、个体化的诊断和治疗。
上述模块3包括三种方式,分别对应模块a3、模块b3以及模块a3和模块b3,其中模块a3、模块b3以及模块a3和模块b3的组合在模块2的分析结果的基础上,进一步分析并初步筛选待测者为或候选为重症ev71感染的易感患儿,包括以下几种情形:
当模块a2的分析结果为阳性时,模块a3初步筛选待测者为或候选为重症ev71感染的易感患儿;
当模块b2的分析结果为阳性时,模块a3初步筛选待测者为或候选为重症ev71感染的易感患儿;
当模块b2的分析结果为阳性时,模块b3比较模块b2分析得到的存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量,如果存在cpt2f352c突变的cpt2的表达量相对于无对应突变的离体样本的cpt2的表达量下调,初步筛选待测者是否为重症ev71感染的易感患儿;
当模块b2的分析结果为阳性时,模块a3初步筛选待测者为或候选为重症ev71感染的易感患儿,进一步的,为了提高检测结果的准确性,模块b3比较模块b2分析得到的存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量,如果存在cpt2f352c突变的cpt2的表达量相对于无对应突变的离体样本的cpt2的表达量下调,初步筛选待测者是否为重症ev71感染的易感患儿;
当模块a2和模块b2的组合的分析结果为阳性时,模块a3初步筛选待测者为或候选为重症ev71感染的易感患儿;
当模块a2和模块b2的组合的分析结果为阳性时,模块b3比较模块b2分析得到的存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量,如果存在cpt2f352c突变的cpt2的表达量相对于无对应突变的离体样本的cpt2的表达量下调,初步筛选待测者是否为重症ev71感染的易感患儿;
当模块a2和模块b2的组合的分析结果为阳性时,模块a3初步筛选待测者为或候选为重症ev71感染的易感患儿,进一步的,为了提高检测结果的准确性,模块b3比较模块b2分析得到的存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量,如果存在cpt2f352c突变的cpt2的表达量相对于无对应突变的离体样本的cpt2的表达量下调,初步筛选待测者是否为重症ev71感染的易感患儿。
在一优选实施例中,所述离体样本为细胞、组织、脏器、血液、淋巴液、消化液、咳痰、肺胞支气管清洗液、尿或粪便中的任意一种。
利用上述实施例所述的试剂盒初步筛选重症ev71易感患儿的方法,包括以下步骤:
对待测者离体样本进行ev71rna检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行cpt2f352c检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者为或候选为重症ev71易感患儿。
在上述步骤中,对待测者离体样本进行ev71rna检测及对离体样本进行cpt2f352c检测分别包括定性或定量两种方式,进一步的,为了保证检测结果的准确性,还可以包括定性结合定量的方式;根据检测结果初步筛选待测者为或候选为重症ev71易感患儿也包括从定性的角度筛选或从定量的角度筛选两种方式,进一步的,为了保证筛选结果的准确性,还可以包括定性结合定量的角度筛选的方式。因此,上述利用上述实施例所述的试剂盒初步筛选重症ev71易感患儿的方法可分为以下21种情况:
情况1
对待测者离体样本进行ev71rna定性检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者为或候选为重症ev71易感患儿。
情况2
对待测者离体样本进行ev71rna定性检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者为或候选为重症ev71易感患儿。
情况3
对待测者离体样本进行ev71rna定性检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况4
对待测者离体样本进行ev71rna定性检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者是否为重症ev71感染的易感患儿,同时进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况5
对待测者离体样本进行ev71rna定性检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,同时利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者为或候选为重症ev71易感患儿。
情况6
对待测者离体样本进行ev71rna定性检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,同时利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况7
对待测者离体样本进行ev71rna定性检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,同时利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者是否为重症ev71感染的易感患儿,同时进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况8
对待测者离体样本进行ev71rna定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者为或候选为重症ev71易感患儿。
情况9
对待测者离体样本进行ev71rna定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者为或候选为重症ev71易感患儿。
情况10
对待测者离体样本进行ev71rna定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况11
对待测者离体样本进行ev71rna定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者是否为重症ev71感染的易感患儿,同时进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况12
对待测者离体样本进行ev71rna定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,同时利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者为或候选为重症ev71易感患儿。
情况13
对待测者离体样本进行ev71rna定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,同时利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况14
对待测者离体样本进行ev71rna定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,同时利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者是否为重症ev71感染的易感患儿,同时进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况15
同时对待测者离体样本进行ev71rna定性和定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者为或候选为重症ev71易感患儿。
情况16
同时对待测者离体样本进行ev71rna定性和定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者为或候选为重症ev71易感患儿。
情况17
同时对待测者离体样本进行ev71rna定性和定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况18
同时对待测者离体样本进行ev71rna定性和定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者是否为重症ev71感染的易感患儿,同时进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况19
同时对待测者离体样本进行ev71rna定性和定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,同时利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者为或候选为重症ev71易感患儿。
情况20
同时对待测者离体样本进行ev71rna定性和定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,同时利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
情况21
同时对待测者离体样本进行ev71rna定性和定量检测,得到ev71rna检测结果为阳性或阴性;
若ev71rna检测结果为阳性,则利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本进行是否存在cpt2f352c突变的检测,同时利用包含如seqidno.1、seqidno.2所示的特异性上下游引物的试剂盒对离体样本在41℃高热条件下进行cpt2表达量的检测,得到cpt2f352c检测结果为阳性或阴性;
若cpt2f352c检测结果为阳性,则初步筛选待测者是否为重症ev71感染的易感患儿,同时进一步比较存在cpt2f352c突变的cpt2的表达量与无对应突变的离体样本的cpt2的表达量是否下调,若下调,则初步筛选待测者是否为重症ev71感染的易感患儿。
在上述21种情况中,对待测者离体样本进行ev71rna定性检测采用pcr扩增进行检测,若检测结果显示无典型s型扩增曲线,则为阴性,表明待测者并未感染ev71病毒;若检测结果显示呈s型扩增曲线,则为阳性,表明待测者感染ev71病毒。对待测者离体样本进行ev71rna定量检测包括对待测者的离体样本进行定量检测ev71病毒载量,根据rt-pcr的标准梯度浓度,计算病毒载量。
通过上述方法初步筛选出重症ev71感染的易感患儿后,对筛选出的重症ev71易感患儿进行积极有效的早期预防治疗,包括通过对重症ev71易感患儿可能发生的高热予以控制,有助于减少重症脑炎和脑病的发生,降低其致残率和死亡率。
为了更清楚详细地介绍本发明实施例所提供的用于检测cpt2f352c突变的引物、试剂盒及筛选重症ev71易感患儿的系统,下面将结合具体实施例进行描述。
实施例1
星形胶质细胞水平研究cpt2f352c突变对atp水平及cpt2酶活性的影响。
(1)cpt2f352c突变的星形胶质细胞模型的构建:
利用crispr/cas9技术构建cpt2f352c点突变星形胶质细胞模型。通过电转cas9-cpt2sgrna质粒及donor质粒,基因组上靶点位置附近序列被cas9特异性切割后在模板donor质粒的指导下通过同源重组修复,从而引入突变位点。相比病毒介导的基因敲除,质粒电转的优点是基因组不会有随机插入。具体路线如下:
s1:针对cpt2基因,按照尽可能靠近编辑靶点的原则,设计目的位点基因组的guiderna序列,序列如seqidno.3所示,并进行体外转录获得guiderna;
s2:设计模板donor质粒,电转cas9-cpt2sgrna质粒及donor质粒入星形胶质细胞;
s3:嘌呤霉素筛选转化cas9-cpt2sgrna质粒的星形胶质细胞;
s4:pcr测序筛选突变细胞株。
具体流程如图1所示。
(2)培养cpt2f352c突变的星形胶质细胞和无cpt2f352c突变的星形胶质细胞,给予ev71感染和高温处理:
ev71感染及高温处理后不同基因型的星形胶质细胞的atp水平和cpt2酶活性不同。ev71感染后,cpt2f352c突变的星形胶质细胞在高温时较无cpt2f352c突变的星形胶质细胞的atp水平明显降低,cpt2剩余酶活性下降,差异有统计学意义(p<0.05,p<0.05);
绘制ev71和高温刺激后cpt2基因qrt-pcr曲线和cpt2基因表达量趋势变化,结果如图2所示,含cpt2f352c突变的星形胶质细胞在ev71病毒和高温刺激24h、72h时cpt2的基因表达水平显著低于野生组(p<0.05)。
实施例2
小鼠水平研究cpt2f352c突变致功能异常对重症ev71感染的影响。
通过与ncbi数据库,比对人源和小鼠源cpt2序列,发现人源(np-00089)和小鼠源(np-034079.2)的cpt2蛋白都有658个氨基酸,其氨基酸序列有94%是相同的,同时确认小鼠同人一样第352位的氨基酸都是苯丙氨酸(f)位于胆碱/肉毒碱o-酰基转移酶(choline/carnitineo-acyltransferase)结构内,可能对cpt2的酶活性起着重要作用。
(1)cpt2f352c突变小鼠构建
1)guide-rna位点和oligodonordna设计与合成
s1:使用zhanglab的在线设计软件进行guide-rna设计:利用http://crispr.mit.edu/,设计靶向cpt2第4外显子的guide-rna,标记为grna1,序列如seqidno.4所示,guide-rna序列在上海生工合成;
s2:在guide-rna位点附近设计全长120bp的单链供体序列oligodonordna以用于同源重组,同源臂长度是所要突变的位点为中心计算的,左右各约45-65bp,具体序列如seqidno.5所示,该序列在上海生工合成。
2)显微注射用guide-rna的制备
s1:使用megashortscripttmkit(thermofisher)对guide-rna模板进行体外转录,在rnase-free微量离心管中配置如表1所示的反应体系备用,所有操作均在冰上进行;
s2:配好反应体系后,混匀,低速离心使反应液沉于微量离心管底部,置于室温下反应2h;
s3:去除dna模板:向反应体系中加入1μlturbodnase,震荡混匀,置于室温下反应15min;
s4:利用megacleartmkit(ambionp/nam1908)试剂盒纯化转录产物。
表1guide-rna体外转录反应体系
3)显微注射用cas9mrna的制备
s1:利用内切酶将cas9质粒进行线性化:在100μl的反应体系中,加入3μlnoti消化5μgcas9质粒,将反应体系放置在37℃5h。反应结束后,使用megacleartmkit(ambionp/nam1908)试剂盒对线性产物纯化,纯化后测浓度置于-20℃备用;
s2:使用mmessagemmachinetmt7ultratranscriptionkit(lifetechnologies)进行cas9mrna体外转录,按照表2在rnase-free微量离心管中配置反应体系反应。
表2cas9mrna体外转录反应体系
4)胚胎收集
5)显微注射
s1:准备硅化的载玻片、固定针及注射针,向载玻片上滴m2培养基并用矿物油覆盖;
s2:使注射针通过毛细管作用吸入显微注射液混合物,然后将注射针固定在显微注射仪上;
s3:将培养的50个胚胎转移至载玻片上的m2培养基内,将固定针缓慢靠近胚胎,使胚胎固定在固定针上,然后再高倍镜下定位细胞核;
s4:小心推动注射针的尖端,使其穿过透明带、细胞膜、核膜,当看到细胞核慢慢肿胀是小心撤回注射针;
s5:将注射过的胚胎转移至新的m2培养基岛中,继续重复上述步骤(3-4)直至所有胚胎注射完毕。注射完后,将胚胎转移至kosm培养基中,培养箱中培养2h,排除因机械损伤而致死的胚胎,选择健康的胚胎转入新的kosm培养基中备用。
6)胚胎移植
s1:给假孕母鼠经腹腔注射阿佛丁600μl至麻醉状态,用剃毛器剃除其背部的毛,并用70%酒精消毒剃毛后的皮肤;
s2:在卵巢部位切开皮肤,用镊子钝性分离至卵巢脂肪垫,将卵巢拉出暴露,并用止血钳固定,用镊子找到漏斗状的输卵管口;
s3:转移针一次吸入m2培养基、2个小气泡、25枚备用胚胎、1个气泡;
s4:将转移针转向输卵管口,将转移针内的胚胎注入,然后小心的撤回转移针;
s5:将卵巢回置到原先的位置,缝合肌肉及皮肤切口;
s6:将手术后的假孕母鼠置于37℃恒温复苏台上,待小鼠清醒后,转移至饲养笼具中继续饲养。通常,胚胎移植成功后3周,母鼠产出f0代小鼠。
7)小鼠dna提取
s1:剪取小鼠尾巴约0.5cm放入已编号1.5mlep管中,盖好盖子,12000rpm快速离心10s;
s2:每管加0.5mldna裂解液和50μl蛋白酶k贮存液,并将盖盖紧,确保组织完全浸在溶液中;
s3:将ep管置杂交炉中,56℃转动过夜;
s4:次日将样本于室温,12000rpm离心10min;
s5:将上清转移倒入新的1.5mlep管中,加1ml无水乙醇(约2倍上清体积),盖紧盖子后轻摇,可见絮状沉淀。13000rpm离心15min,弃上清;
s6:加70%乙醇1ml,洗涤,13000rpm离心15min,弃上清,收集沉淀,室温静置15min。每管加80μl灭菌水,盖好后置37℃水浴箱中充分溶解1h;
s7:在室温中放置数小时,待dna全部溶解后-20℃保存,或直接进行pcr或杂交等实验;
s8:测量dna含量及纯度,od260/280在1.8-2.0之间,dna浓度控制在50-100ng/μl。
8)小鼠基因型鉴定
s1:合成特异性扩增引物,具体序列见seqidno.1、seqidno.2;
s2:根据takarala
s3:pcr反应条件见表4;
s4:待pcr反应结束后,取5μldna产物进行琼脂糖凝胶电泳,可看到清晰的单一条带,割胶回收后,送至测序公司进行测序。
表3cptdna扩增反应体系
表4cptdna扩增pcr反应条件
9)小鼠繁育
根据pcr和测序结果选取基因型鉴定为阳性的f0代小鼠,与野生型小鼠杂交,获得的f1代小鼠经pcr鉴定,pcr产物连接t-vector测序确认。
(2)给予cpt2f352c突变小鼠及野生型小鼠ev71感染和高热刺激
1)ev71感染和41℃高热后cpt2f352c小鼠出现少动、弓背、消瘦和肢体活动不灵等症状,死亡率增加,具体见图3。
a:未给予ev71感染和41℃高热刺激的cpt2f352c小鼠;
b:ev71感染和41℃高热刺激1d后,部分小鼠出现少动、弓背等症状;
c:ev71感染和41℃高热刺激3d后,部分小鼠出现肢体活动不灵及后肢麻痹症状;
d:ev71感染和41℃高热刺激5d后小鼠明显消瘦,部分小鼠症状略好转;
e:ev71感染和41℃高热刺激7d后小鼠大部分进入恢复期,临床症状基本消失。
2)对不同小鼠进行脑组织的atp水平和cpt2剩余酶活性表达检测。
脑组织atp水平的检测方法:
分别取各组小鼠的脑干,加入500μl1×pbs,用研钵研碎后加入注入新的ep管中,4℃低温离心10min;
弃上清,1×pbs清洗并离心2次,加入500μl1%三氯乙酸混匀;
4℃低温离心5min,立即用ph7.75的三羟基氨甲烷醋酸盐溶液中和稀释100倍,进一步进行atp水平的测定;
利用enlitenatp分析系统生物荧光试剂盒检测atp浓度,首先按说明书配置标准品,浓度梯度为10-10mol/l、10-11mol/l、10-12mol/l、10-13mol/l、10-14mol/l、10-15mol/l;
每个检测孔中加入atp检测工作液100μl,室温下静置5min,使本底性atp耗尽;
每孔中加入100μl标准品或待测样品,用移液器迅速混匀,立即用luminometer测定rlu值;
绘制标准曲线,根据标准曲线计算出待测样本atp水平。
剩余酶活性的检测方法:
利用bca蛋白定量分析试剂盒(thermoscientific,美国)进行蛋白定量,参照说明书步骤进行如下操作:
制备标准品:参照说明书,梯度稀释牛血清蛋白(bullserumalbumin,bsa),100mg/ml、50mg/ml、25mg/ml、12.5mg/ml、6.25mg/ml、3.125mg/ml、1.56mg/ml、0mg/ml;
制备bca工作液:将bca试剂a和bca试剂b按50:1的比例混合,涡旋振荡混匀,得到绿色澄清的bsa工作液;
将待测样本及bsa标准品各25μl加入96孔板中;
每孔中加入200μlbsa工作液,置于振荡器上震荡混匀,密封,室温下孵育约30min,可见标准品及待测样品颜色逐渐变紫色,标准品呈现颜色梯度;
将96孔板置于酶标仪下,设置测定波长为562nm,测其吸光值;
绘制标准曲线,计算出待测样本的蛋白浓度;
提取脑干组织总蛋白并检测总蛋白浓度;
取蛋白待测液,加入梯度浓度稀释的l-[methyl-3h]carnitine作为底物,37℃孵育2h;
通过检测palmitoyl-l-[methyl-3h]carnitine的浓度来测定cpt2的酶活性。
检测结果见图4,具体的:
a:cpt2f352c小鼠ev71感染和41℃高热刺激后脑干组织atp水平
41℃高热处理后cpt2f352c小鼠atp水平明显降低,差异具有统计学意义(p<0.05);
而野生组小鼠41℃高热处理后atp水平虽降低,但差异无统计学意义(p>0.05)。
b:不同温度条件下,ev71感染和41℃高热刺激后cpt2f352c小鼠脑干组织内cpt2酶活性,41℃时cpt2酶活性较37℃、39℃明显降低,差异有统计学意义(p<0.05)。
c:不同温度条件下,ev71感染和41℃高热刺激后野生型小鼠脑干组织内cpt2酶活性,41℃cpt2酶活性较37℃、39℃降低,但差异无统计学意义(p>0.05)。
3)cpt2f352c小鼠在ev71感染和41℃高热刺激2h后脑组织线粒体结构的损伤
不同时间点,电镜下小鼠脑组织线粒体超微结构的改变情况见图5,电镜×10000。
正常对照:
(a,a):脑组织神经元细胞线粒体膜结构完整,基质密集,呈圆形或卵圆形,线粒体嵴清晰。
野生型小鼠:
ev71感染3d后(b1):小鼠脑组织神经元细胞线粒体略肿胀,线粒体嵴减少;
ev71感染5d后(b2):神经细胞线粒体数目减少,线粒体嵴变短或消失;
ev71感染9d后(b3):神经细胞线粒体数目与结构基本恢复正常。
cpt2f352c小鼠:
ev71感染41℃高热处理,3d后(b1):神经细胞线粒体肿胀明显,基质清淡,膜结构破坏,部分有空泡化改变,线粒体嵴消失,线粒体破坏较为b1严重;
5d后(b2):小鼠脑线粒体严重肿胀,膜结构不清,线粒体嵴消失;
9d后(b3):脑线粒体基本恢复正常形态,线粒体嵴恢复。
4)cpt2f352c小鼠在ev71感染和41℃高热刺激2h后脑组织血脑屏障的损伤
不同时间点,电镜下小鼠血脑屏障改变情况见图6,电镜×10000。
正常对照:
(a,a):毛细血管管腔规则,内皮细胞、基膜、星形胶质细胞足细胞层次清楚,结构清晰。
野生型小鼠:
41℃高热处理,3d后改变(b1):内皮细胞肿胀,毛细血管管腔形状稍不规则,基膜尚完整存在;
5d后改变(b2):内皮细胞间紧密连接及基膜结构明显破坏,血脑屏障结构不完全,基膜外星形胶质细胞及其足细胞明显水肿;毛细血管管腔不规则,内皮细胞变薄;
9d改变(b3):管腔形状规则,基膜连续,内皮细胞无水肿。
cpt2f352c小鼠:
ev71感染41℃高热处理,3d后(b1):毛细血管管腔形状不规则,内皮细胞变薄,吞饮小泡明显增多,基膜局部有缺损,基膜外星形胶质细胞及其足细胞明显水肿;
5d后(b2):毛细血管结构完全破坏;
9d后(b3):毛细血管管腔形状逐渐规则,但基膜厚度仍不均,基膜外星形胶质细胞及其足细胞水肿缓解,基膜结构渐完整。
实施例3
人体水平上利用cpt2f352c突变病人的pbmc进行验证
(1)收集健康人血液标本、ev71感染患儿的血液标本,患者均知情同意,上述所有标本的取得均通过组织伦理委员会的同意。
(2)ev71感染的cpt2f352c突变患儿及无cpt2f352c突变患儿pbmc后进行atp水平及cpt2酶活性比较。培养cpt2f352c突变患儿及无突变患儿的pbmc,给予ev71感染后高温继续培养2h,与无突变者相比高温时cpt2酶活性和atp水平明显降低,差异具有统计学意义。
<110>青岛大学附属医院
<120>用于检测cpt2f352c突变的引物、试剂盒及筛选重症ev71易感患儿的系统
<160>5
<170>patentinversion3.5
<210>1
<211>24
<212>dna
<213>上游引物
<400>1
ttttcggcttttcaattcaactcg
<210>2
<211>24
<212>dna
<213>下游引物
<400>2
cagggctcagcttcttcttcttca
<210>3
<211>23
<212>dna
<213>dna
<400>3
taaaggacttatcaaaccagcgg
<210>4
<211>20
<212>dna
<213>dna
<400>4
taaaggacttatcaaaccag
<210>5
<211>120
<212>dna
<213>oligodonordna
<400>5
atcttgttcacttgtcacacaccatgctgcacggtgacggcacgaatcgctggtgtgataagtcctttaacctcattgtagccaaagatggcactgctgcagtccacttcgagcatgcgt
- 还没有人留言评论。精彩留言会获得点赞!