一种从怀菊花中制备菊花新木脂素A的方法及其应用与流程
本发明涉及医药,特别是一种从怀菊花中制备菊花新木脂素a的方法及其应用。
背景技术:
菊花(chrysanthemummorifoliumramat.)为菊科植物菊的干燥头状花序,始载于《神农本草经》,列为上品。其味甘、苦,性凉,主归肺、肝经,具有疏散风热、平肝明目、清热解毒的功效[1,2]。2015版《中国药典》新增“怀菊花”这一品种,与“亳菊”、“滁菊”、“贡菊”、“杭菊”共同作为“菊花”入药,肯定了怀菊的药用地位。怀菊花[dendranthemamorifolium(ramat.)kitam]做为“四大怀药”之一,主产于河南武陟、温县地区,种植的历史较悠久,为河南道地药材之一。怀菊花具有清热解毒、疏散风热、平肝明目之功效,其中白菊花长于平肝明目,黄菊花多用于散风清热。从怀菊花中分离并鉴定1个新的双环氧木脂素类化合物,即菊花新木脂素a。实验结果显示菊花新木脂素a可以显著性降低lps诱导raw264.7细胞释放no,具有较好的抗炎效果,但至今未见有公开报导。
技术实现要素:
针对上述情况,为克服现有技术之缺陷,本发明之目的就是提供一种从怀菊花中制备菊花新木脂素a的方法及其应用,可有效解决从怀菊花中提取菊花新木脂素a,实现菊花新木脂素a作为唯一活性成分在制备抗炎药物中的应用问题。
本发明解决的技术方案是,一种从怀菊花中制备菊花新木脂素a的方法,所述的菊花新木脂素a是从怀菊花中提取的活性成分,分子结构式为:
其制备方法是:怀菊花用丙酮水溶液组织破碎提取,提取液减压浓缩成浸膏,浸膏用水分散,依次用石油醚、乙酸乙酯、正丁醇萃取,分别得到石油醚部位、乙酸乙酯部位、正丁醇部位、水部位;乙酸乙酯部位上硅胶柱,用二氯甲烷-甲醇梯度洗脱,得到四个流分fr.1~4;
流分fr.3用甲醇溶解,离心,过滤除去不溶物,得子流分fr.3.1;子流分fr.3.1减压浓缩,上mci柱,依次用水、甲醇梯度洗脱,用茴香醛-浓硫酸喷雾检识,每100ml检识一次,合并相同流份,得到子流分fr.3.1.1-fr.3.1.7;子流分fr.3.1.6经toyopearlhw-40柱色谱,用甲醇洗脱,采用茴香醛-浓硫酸喷雾检识,每10ml检识一次,合并相同流份,得到子流分fr.3.1.6.1-fr.3.1.6.2;子流分fr.3.1.6.2用半制备hplc分离,上色谱柱,流动相为乙腈︰三氟乙酸水溶液,收集保留时间tr=61.0~63.0min的流份,浓缩干燥,得到化合物菊花新木脂素a。
该化合物菊花新木脂素a具有显著降低lps诱导raw264.7细胞释放no,有效用于制备抗炎药物,实现菊花新木脂素a作为唯一活性成分在制备抗炎药物中的应用。
本发明制备方法易操作,科学合理,所制备的菊花新木脂素a具有显著降低lps诱导raw264.7细胞释放no,有效用于制备抗炎药物,实现菊花新木脂素a作为唯一活性成分在制备抗炎药物中的应用,开拓了抗炎药物的新途径提高了怀菊花的药用价值和商业价值,有显著的经济和社会效益。
附图说明
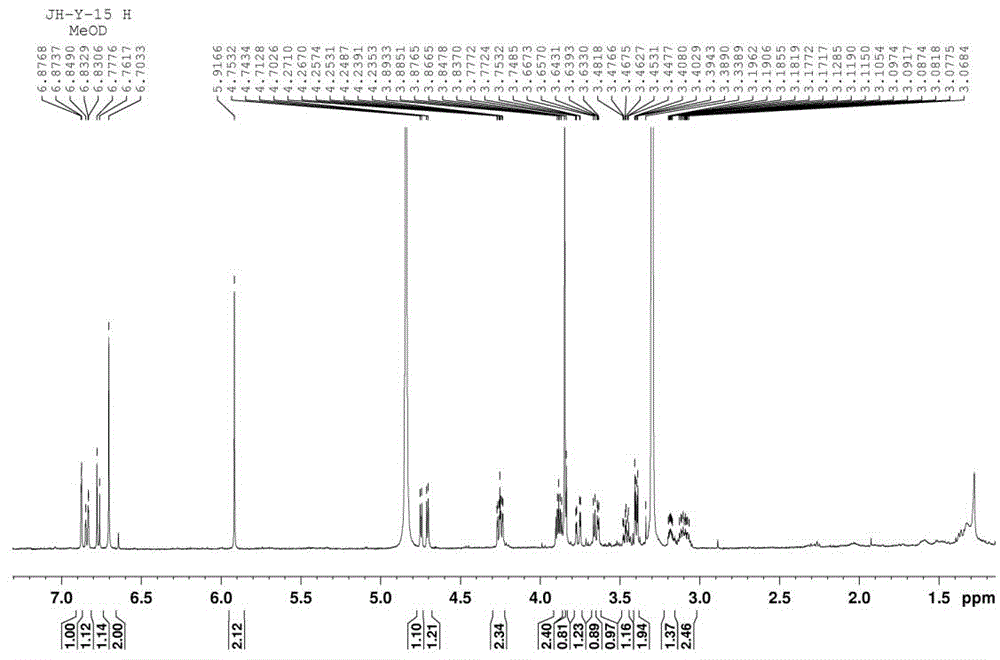
图1为本发明化合物菊花新木脂素a的1h-nmr谱(incd3od)图。
图2为本发明化合物菊花新木脂素a的13c-nmr谱(incd3od)图。
图3为本发明化合物菊花新木脂素a的dept135谱(incd3od)图。
图4为本发明化合物菊花新木脂素a的1h-1hcosy谱(incd3od)图。
图5为本发明化合物菊花新木脂素a的hsqc谱(incd3od)图。
图6为本发明化合物菊花新木脂素a的hmbc谱(incd3od)图。
图7为本发明化合物菊花新木脂素a的noesy谱(incd3od)图。
图8为本发明化合物菊花新木脂素a的hr-esi-ms谱(incd3od)图。
图9为本发明化合物菊花新木脂素a的ir谱(incd3od)图。
图10为本发明化合物菊花新木脂素a的uv谱(incd3od)图。
具体实施方式
以下结合具体情况对本发明的具体实施方式作详细说明。
本发明在具体实施中,一种从怀菊花中制备菊花新木脂素a的方法,所述的菊花新木脂素a是从怀菊花中提取的活性成分,其制备方法是:怀菊花11.2kg,用体积浓度50%的丙酮水溶液组织破碎提取2次,丙酮每次用量120l,合并2次提取液,减压浓缩得浸膏1.8kg;浸膏用9l水分散,依次用石油醚5×10l、乙酸乙酯5×10l、正丁醇5×10l萃取,分别得到石油醚部位、乙酸乙酯部位、正丁醇部位、水部位;乙酸乙酯部位上1000g硅胶柱,用二氯甲烷-甲醇50:1、30:1、20:1、5:1进行梯度洗脱,得到相应的四个流分fr.1~4;
流分fr.3用50ml甲醇溶解,用6000转的转速离心15min,温度为20℃,离心过滤除去不溶物,得子流分fr.3.1;子流分fr.3.1减压浓缩至20ml,上mci柱,依次用水、体积浓度10%、20%、30%、40%、100%甲醇洗脱,每个洗脱部位用量为柱体积的10倍,流速3ml/min,采用茴香醛-浓硫酸喷雾检识,每100ml检识一次,合并相同流份,得到子流分fr.3.1.1-fr.3.1.7;子流分fr.3.1.6经toyopearlhw-40柱色谱,用体积浓度70%甲醇洗脱,采用茴香醛-浓硫酸喷雾检识,每10ml检识一次,合并相同流份,得到子流分fr.3.1.6.1-fr.3.1.6.2;子流分fr.3.1.6.2用半制备hplc分离,上规格型号为:250×10mm,粒径5μm,孔径12nm的ymc-packods-aa色谱柱,流动相为乙腈︰三氟乙酸水溶液=23︰77,所述的三氟乙酸水溶液质量浓度万分之二,流速3ml/min,收集保留时间tr=61.0~63.0min的流份,浓缩干燥,得到化合物菊花新木脂素a。
该化合物菊花新木脂素a具有显著降低lps诱导raw264.7细胞释放no,有效用于制备抗炎药物,实现菊花新木脂素a作为唯一活性成分在制备抗炎药物中的应用。
本发明方法经反复试用,都得到了相同或相近似的结果,表明方法稳定、可靠,具有很好的实际应用价值,所制备的化合物菊花新木脂素a具有显著性降低lps诱导raw264.7细胞释放no,具有较好的抗炎效果,并经实验取得了非常好的有效技术效果,有关资料如下:
1仪器与试药
核磁共振用brukeravanceⅲ500核磁共振仪(tms内标)(bruker),红外光谱用nicoletis10microscopespectrometer(thermoscientific,usa),高分辨质谱用brukermaxishdmassspectrometer,紫外光谱用shimadzuuv-2401pcapparatus,高效液相色谱用watersalliance系列2695高效液相系统,配备2998型二极管阵列检测器,empower3色谱数据工作站,lc50型高压制备液相色谱仪,uv200型紫外检测器[赛谱锐思(北京)科技有限公司],ymc-packods-a色谱柱(250×10mm.d.s-5mm,12mm)(ymc有限公司),其余有n-1100型旋转蒸发仪(上海爱朗仪器有限公司),a-1000s型水流抽气机(上海爱朗仪器有限公司),n-1111型冷冻水循环装置(上海爱朗仪器有限公司),fdu-2110型冷冻干燥机(上海爱朗仪器有限公司),dfz-60508型真空干燥箱(上海一恒科学仪器有限公司),ab204-n万分之一精密分析天平(mettlertoledo),imark型酶标仪(美国bio-rad),二氧化碳培养箱(上海stik),超净工作台(苏净集团),arium611vf超级组合型超纯水器(sartorius),倒置显微镜(nikon),pb-10酸度计(德国赛多利斯集团),sorvallst16rcentrifuge高速低温冷冻离心机(thermofisherscientific公司);酶标仪(bio-rad680);超净工作台(江苏苏净集团);90-3磁力搅拌器(上海振捷实验设备有限公司);rd-7080全自动新型鼓风干燥箱(上海智城分析仪器制造有限公司);微量加样器(nichipetexplus);ab204-n电子读数分析天平(梅特勒-托利多仪器(上海)有限公司产品);10cm培养皿、96孔培养板、冻存管(corning);普通手术器械。
柱层析填料diaionhp-20、mcigelchp-20(日本三菱化学公司),toyopearlhw-40(日本tosoh公司),sephadexlh-20(parmaciabiotech公司),柱层析所用硅胶h(160-200目)为青岛海洋化工厂生产,培养皿、96孔培养板、细胞冻存管(corning公司),所用色谱纯试剂位天津四友精细化学品有限公司生产,所用分析纯试剂为北京化工厂和天津第三化学试剂厂生产。
小鼠巨噬细胞(raw264.7)购自中国科学院上海细胞库;dmem高糖培养基(gibco);胎牛血清((gibco);胰蛋白酶(gibco),dmso(solarbio);mtt(biosharp);氨苄青霉素、tris碱(sigma);griessreagent(sigma);inos一抗(cst)、cox2一抗(cst);水为超纯水,pbs缓冲液等为自配。
本发明所选的怀菊花,采购于河南焦作,经河南中医药大学陈随清教授鉴定为菊科植物怀菊花dendranthemamorifolium(ramat.)kitam的干燥头状花序,并按本发明给出的制备方法,制备出化合物菊花新木脂素a。
2结构鉴定
菊花新木脂素a:浅黄色结晶性粉末(ch3oh),茴香醛-浓硫酸喷雾显粉红色。hr-esi-ms给出准分子离子峰m/z:571.1771[m+na]+(calcd.forc27h32o12na571.1791),确定其分子式为c27h32o12;uv(meoh)λmax:206(2.42),228(0.59),284(0.23)nm;ir(kbr)νmaxcm-1:3361,2925,1674,1597,1443,1201,1123,1036cm-1。
菊花新木脂素a
表1菊花新木脂素a的nmr波谱数据(incd3od)
活性检测
raw264.7细胞经含胎牛血清(10%)的dmem培养基培养1周后,选取对数生长期细胞,pbs洗一次,加入dmem培养基吹打均匀,以5×104个/ml的浓度接种于96孔板内,每孔培养总体积为100μl。培养24h待细胞贴壁后,细胞分为正常组(con)、模型组(lps1μg/ml)、菊花新木脂素a组(50μm+lps1μg/ml)继续培养。37℃、5%co2培养24h后,每孔加入mtt溶液(5mg/ml)20μl,37℃继续培养4h,小心吸净培养液,每孔加入100μldmso,震荡5-10min,使紫色结晶完全溶解。用酶标仪双波长在570-630nm下测定各孔吸光度值(a),计算平均a值和细胞活力。实验平行重复三次。细胞活力=各组od值/正常组od值。
选取对数生长期raw264.7细胞,以3×105个/ml的浓度接种于96孔板内,每孔培养总体积为100μl。培养24h待细胞贴壁后,细胞分为正常组(con)、模型组(lps1μg/ml)、菊花新木脂素a组(50μm+lps1μg/ml)继续培养。37℃、5%co2培养24h后,每孔吸出细胞上清液50μl,加入50μlgriess试剂,避光反应5min后,540nm下测定各孔吸光度值(a),计算平均a值和no释放量。实验平行重复三次。no释放量=各组od值/正常组od值。
选取对数生长期raw264.7细胞,以1×105个/ml的浓度接种于6孔板内,每孔培养总体积为1ml。培养24h待细胞贴壁后,细胞分为正常组(con)、模型组(lps1μg/ml)、菊花新木脂素a组(50μm+lps1μg/ml)继续培养。37℃、5%co2培养24h后,按照试剂盒说明书仔细操作提取总蛋白(北京索莱宝科技有限公司)。总蛋白按照bca蛋白定量试剂盒(北京索莱宝科技有限公司)说明书仔细操作测定总蛋白终浓度,剩余的蛋白样本加入4份的loadbuffer100℃煮5min变性,根据总蛋白浓度调整上样蛋白浓度后经sds-page电泳分离后转移至pvdf膜上,用5%脱脂奶粉室温封闭1.5h,加入一抗inos(1:1500)、cox2(1:1500)、、β-actin(1:2000)。4℃孵育过夜,加入兔源荧光二抗(1:20000),于37℃孵育1h,近红外双色成像系统(奥德赛)采集蛋白条带,并用imagestudio软件对蛋白条带进行定量分析。
活性结果
mtt与griess结果显示,1μg/ml的lps可诱导raw264.7细胞增殖与no释放增加,但菊花新木脂素a(50μm)可降低no的释放且不杀伤raw264.7细胞;westernbolt结果显示,1μg/ml的lps可使raw264.7细胞过度表达inos与cox2蛋白,但菊花新木脂素a(50μm)显著性下调raw264.7细胞的inos与cox2蛋白表达,结果表明菊花新木脂素a具有较好的抗炎效果,作为唯一活性成分显著性降低lps诱导raw264.7细胞释放no,有效用于制备抗炎药物,开拓了抗炎药物的新途径和怀菊花的新用途和商业价值,有显著的经济和社会效益。
- 还没有人留言评论。精彩留言会获得点赞!