海带α型碳酸酐酶基因Sjα-CA2及其编码蛋白和应用的制作方法
本发明属于基因工程技术领域,具体涉及海带α型碳酸酐酶基因sjα-ca2及其编码蛋白和应用。
背景技术:
海带(saccharinajaponica)对co2的吸收有助于缓解温室气体及水体酸化。hco3-是海水无机碳的主要形式,占海水总无机碳含量的90%左右,而co2所占的比例不足无机碳总量的1%,但海带等大型海藻的光合作用效率却远远高于陆地植物(gao&mckinley,1994)。这是因为多数海藻存在一种无机碳浓缩机制(ccm),可以增加1,5-二磷酸核酮糖羧化酶/加氧酶(rubisco)周围的co2浓度,使藻体能固定更多的co2以提高其光合作用效率。在ccm中,碳酸酐酶(carbonicanhydrase,ca)是一个不可缺少的组分,ca是一种含锌金属酶,能够有效地催化
技术实现要素:
本发明的主要目的在于提供海带α型碳酸酐酶基因sjα-ca2。
本发明的另一目的在于提供上述基因sjα-ca2的编码蛋白。
本发明的目的之三在于提供通过上述基因sjα-ca2与表达载体构建以生产重组蛋白rsjα-ca2。
本发明的目的之四在于提供上述基因sjα-ca2、和/或其编码蛋白、和/或其重组蛋白rsjα-ca2在培育高产转基因海带作物上的应用。
本发明对海带高通量测序所得的12条ca基因表达序列标签(est)进行拼接,得到一条长为885bp的contig序列,在此基础上利用cdna末端快速扩增(rapidamplificationofcdnaends,race)等技术获得该基因的cdna全长序列如seqidno:1所示,其长1728bp(不含polya尾巴),包括263bp的5′-非翻译区(un-translatedregion,utr),577bp且具有明显polya尾的3′-utr和888bp的开放阅读框(openreadingframe,orf);它编码一个由295个氨基酸组成的前体蛋白,氨基酸序列如seqidno:3所示,相对分子质量为32.2kda,等电点为4.57。经signalp和ipsort预测,在28ala-29ser处有一个典型的信号肽酶切位点,酶切后的成熟蛋白由267个氨基酸组成,相对分子质量为29.27kda,等电点为4.48。通过在ncbi网站中进行同源性搜索和比对,发现该蛋白属于α-ca家族,它与海带sjα-ca(genbank登录号:aef33616.1)所编码的蛋白序列具有50.78%一致性;且基于49个ca的氨基酸序列所构建的邻接和最大似然系统进化树也显示,该ca与其它物种的α-ca聚为一支,因此将该基因命名为sjα-ca2。
将基因sjα-ca2连接至表达载体pet32a中,然后导入大肠杆菌(escherichiacoli)表达菌株bl21中,经过诱导表达和亲和层析纯化,获得重组蛋白rsjα-ca2,其氨基酸序列如seqidno:4所示。用电极法和分光光度计法对重组蛋白rsjα-ca2进行检测,发现其可将co2水合成hco3-以及将乙酸对硝基苯酯酯化成对硝基苯酚,从功能上证明基因sjα-ca2为α-ca的基因家族成员。
本发明的技术方案采用的主要操作包括:
(1)在温度17±1℃、光照强度40μmolphotons/(m2·s)和光周期16h/8h(光照/黑暗)的条件下培养海带配子体,收集海带配子体细胞,并提取总rna和基因组dna。
(2)将海带高通量测序所得的12条est拼接成一条长为885bp的contig序列,在此基础上设计引物,利用race技术获得该基因5′-和3′-末端的cdna序列,经拼接和重新设计引物验证,获得该基因的cdna全长序列。
(3)将基因sjα-ca2与搜索到的其他ca的氨基酸序列利用mega6软件进行聚类分析,显示它与其他的α-ca聚为一支。经序列比对,发现它与sjα-ca(genbank登录号:aef33616.1)所编码的蛋白只有50.78%的序列一致性,故将其命名为sjα-ca2。
(4)根据基因sjα-ca2的全长cdna序列设计引物,利用海带配子体基因组dna作为模板进行pcr扩增,经拼接和重新设计引物验证,得到sjα-ca2的dna全长序列如seqidno:2所示。
(5)根据sjα-ca2的orf序列以及克隆质粒pmd19-t和表达质粒pet32a的多克隆位点序列设计带酶切位点的引物,利用pcr方法构建克隆质粒pmd19t/sjα-ca2。
(6)利用核酸内切酶bamhi和xhoi分别对pmd19t/sjα-ca2和pet32a进行双酶切,回收目的片段,再用t4连接酶连接得到含目的片段的重组表达质粒pet32a/sjα-ca2。
(7)将测序正确的重组表达质粒pet32a/sjα-ca2利用热激法转化到大肠杆菌bl21感受态细胞中,筛选到含有目的基因的转基因菌株et32a/sjα-ca2。将该转基因菌株接种到lb液体培养基中进行放大培养,当菌液在600nm的光密度(od600)值达到0.6~0.8时,加入1mm的异丙基-β-d-硫代半乳糖苷(iptg)继续培养以诱导目的蛋白的表达。
(8)收集菌体并破碎,利用bio-scaletmminiprofinitytmimaccartridges蛋白亲和层析纯化预装柱纯化得到目的基因sjα-ca2的重组蛋白rsjα-ca2。
(9)利用纯化到的rsjα-ca2分别构建体外的co2水合反应和乙酸对硝基苯酯酯化反应体系,分别用电极法和分光光度计法测定rsjα-ca2的酶活性。结果表明,rsjα-ca2既具有co2的水合酶活性,也具有酯酶反应活性,从而鉴定了基因sjα-ca2编码蛋白的功能。
与现有技术相比,本发明的有益效果在于:
本发明首次从海带中分离得到海带α型碳酸酐酶基因sjα-ca2,并通过原核表达获得它的重组蛋白rsjα-ca2,通过电极法和分光光度计法分别检测重组蛋白rsjα-ca2在co2的水合反应酶活性和酯酶反应活性,从而说明增加sjα-ca2的基因表达量有助于提高海带的产量。
附图说明
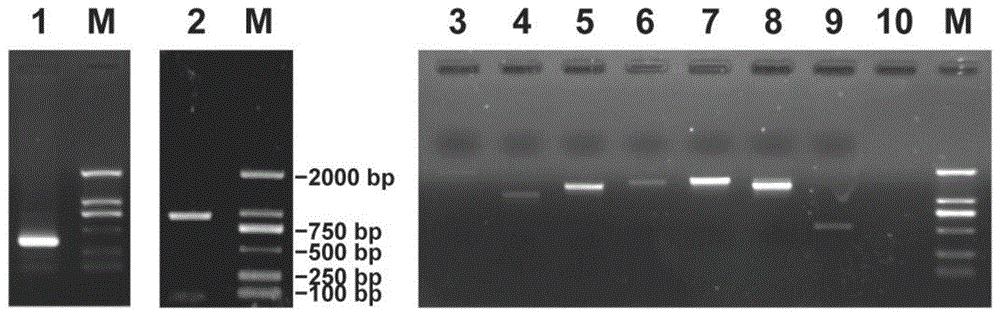
图1为基因sjα-ca2的cdna及dna扩增产物电泳图;m:dl-2000分子量标准;泳道1:5′-race的pcr产物;泳道2:3′-race的pcr产物;泳道3~9:基因sjα-ca2的dna分段扩增产物;泳道10:空白对照。
图2为sjα-ca2的基因结构示意图;灰色线为非翻译区,黑色线为内含子,黑色框为外显子。
图3为基于ca的氨基酸序列所构建的聚类图;箭号所指示的是本发明的基因sjα-ca2;每个物种拉丁名后面的括号内信息表示该物种的ca蛋白序列号;在节点处斜杠前后的数据,分别为邻接法(nj)和最大似然法(ml)的靴带值。
图4为重组表达质粒pet32a/sjα-ca2的双酶切(左)、目的蛋白诱导表达电泳图(中)及western免疫印迹图(右);m1:1kbplusdnaladder的分子量标准;m2:预染蛋白质分子量标准;泳道1:pet32a/sjα-ca2的双酶切产物;泳道2:上清蛋白;泳道3:沉淀蛋白;泳道4:全菌蛋白。
图5为pet32a质粒图谱(上)及多克隆位点区域的序列(下)。
图6为重组蛋白rsjα-ca2洗脱纯化过程中洗脱产物的电泳图;m:预染蛋白质分子量标准;泳道1~7:分别对应于用含5mm、10mm、50mm、100mm、150mm、200mm、250mm咪唑的洗脱缓冲液的洗脱产物。
具体实施方式
下面结合附图和实施例对本发明进一步说明。
1、材料
海带配子体材料自制,在温度为17±1℃、光照强度为40μmolphotons/(m2·s)和光/暗比为16h/8h的条件下培养,所用培养基为pes(starr&zeikus,1993),每两个星期换一次培养基。
大肠杆菌克隆菌株dh5α、表达菌株bl21(de3)和增强型hrp-dab底物显色试剂盒购自天根生化科技有限公司。
表达载体pet32a购自鼎国生物公司。
taqdna聚合酶、限制性核酸内切酶bamhi和xhoi、t4dna连接酶、ta克隆载体pmd19-t购自takara公司。bio-scaletmminiprofinitytmimaccartridges蛋白亲和层析纯化预装柱购自bio-rad公司。
质粒提取试剂盒、胶回收试剂盒、十六烷基三甲基溴化铵(ctab)法植物基因组dna提取试剂盒均购自北京艾德莱生物科技有限公司。
预染蛋白质分子量标准购自thermoscientific公司。
抗聚his标签抗体和辣根过氧化物酶(hrp)标记羊抗兔igg购买于上海友科生物科技有限公司。
trizol试剂、smarttmracecdna扩增试剂盒购自clontech公司。
氨苄青霉素钠(amp)、卡那霉素(kan)、异丙基-β-d-硫代半乳糖苷(iptg)、5-溴-4-氯-3-吲哚-β-d-半乳糖苷(x-gal)均购自上海生工生物公司。
2、方法
(1)取0.1g刚离心收集的新鲜藻细胞置预冷的研钵中,加入液氮充分研磨。
(2)利用ctab法提取基因组dna,-80℃保存备用;利用trizol试剂法抽提总rna,-20℃保存备用。
(3)利用反转录试剂盒对rna进行逆转录(rt)pcr反应合成cdna:
①去除基因组dna反应。pcr反应体系包含2μl的5×基因组dna去除酶缓冲液、1μl的基因组dna去除酶、总rna的量最大为500ng,然后加无rna酶的去离子h2o至10μl。pcr反应条件为42℃保持2min,冷却至4℃保存。
②cdna合成。pcr反应体系包含10μl的上述pcr反应液、4μl无rna酶去离子h2o、4μl的5×primescript缓冲液、1μl的primescriptrtenzymemix1及1μl的rtprimermix4。pcr反应条件为37℃保持15min、85℃保持5s、冷却至4℃保存,即完成cdna的合成反应。
(4)将在海带高通量测序所得到的12条est拼接成一条长为885bp的contig序列,利用ncbi进行blastx搜索,发现它与海带基因α-ca(genbank登录号:aef33616.1)所编码的蛋白具有50.78%的序列一致性。根据该contig序列设计1对引物af如seqidno:19所示(atggcaccctcagctatccggacaat)和ar如seqidno:20所示(tcacactatgtaaacggcgcgcccg),以上述合成的cdna为模板进行pcr扩增,反应产物经琼脂糖凝胶电泳并纯化及测序,以验证该contig序列。
pcr反应体系包含1μl的cdna、12.5μl的2×taqpcrmastermix及上、下游引物各1μl,最后加去离子h2o至25μl。
pcr反应条件为:94℃预变性4min;94℃变性30s,66.7℃退火30s,72℃延伸2min,运行35个循环;72℃延伸10min,10℃保存。
pcr产物经胶回收后连接至pmd19-t载体,然后利用热激法转化大肠杆菌dh5α感受态细胞,蓝白斑筛选后挑取阳性克隆,进行菌落pcr验证,将验证后含有目的片段的阳性克隆菌液送至上海生工生物工程有限公司测序,以验证目的片段的序列。
(5)根据验证的contig序列设计基因特异引物,并利用race技术分别获得该基因的5′-和3′-末端的cdna序列:
①使用smarttmracecdna扩增试剂盒先合成5′-race和3′-race的cdna第一链。
5′-race的cdna第一链合成。pcr合成体系包含1.75μl的无rna酶去离子h2o,1μl总rna,1μl的5′-racecdsprimera。pcr反应条件为72℃保持3min,冷却至4℃保存。取出并短暂离心后加入2μl的5×第一链缓冲液,1μl的二硫苏糖醇(dtt)(20mm),1μl的dntp(10mm),1μl的smartscribe逆转录酶,1μl的smarteriia,0.25μl的rna酶抑制剂。pcr反应条件为42℃保持3min,72℃保持10min,冷却至4℃保存;取出后加入100μl的tricine-edta溶液(10mmtricine-naoh,0.1mmedta,ph8.1)进行稀释后,于-20℃冰箱保存备用。
3′-race的cdna第一链合成。pcr合成体系包含2.75μl的无rna酶的去离子h2o及1μl的3′-racecdsprimera,其他的反应组成及反应条件与5′-race的cdna第一链合成反应一致。反应后同样稀释、保存备用。
②5′-race与3′-race的pcr反应。
5′-race采用巢式pcr反应。第一轮的pcr反应体系包含12.5μl的2×taqpcrmastermix,9.5μl的无rna酶去离子h2o,1μl5′-race的cdna第一链反应液作为模板,1μl的引物5gsp1(attggcggacaagttgatgg),1μl的引物upm(试剂盒自带)。反应条件为:94℃变性30s、63.8℃退火45s及72℃延伸2min,最后72℃延伸10min;20个循环。第二轮pcr的反应包含2μl第一轮pcr产物作为模板,引物为5ngsp(gttgtgaggcggcgaccagtcct)和试剂盒中的nup,其他组分同第一轮反应。反应条件为94℃变性30s、66℃退火45s和72℃延伸2min,最后72℃延伸10min;共30个循环。
3′-race也采用巢式pcr反应。第一轮的pcr反应体系基本与5′-race的第一轮pcr反应体系相同,只是模板为3′-race的cdna第一链反应液,基因特异性引物为3gsp1(aatctctccttcgacggcggcaagt)。反应条件为:94℃变性30s、68.5℃退火30s及72℃延伸2min,最后72℃延伸10min;20个循环。第二轮pcr反应体系包含2μl第一轮pcr产物作为模板,引物为3ngsp(cgtgataggcgtcttcctggatgcg)和试剂盒中的nup,其他组分同第一轮反应。反应条件为94℃变性30s、66.5℃退火1min和72℃延伸2min,最后72℃延伸10min;共30个循环。
第二轮pcr反应后的产物经上述相同的胶回收、连接、转化、蓝白斑筛选和测序等过程,获得sjα-ca2的5′-及3′-末端的cdna序列。
(6)sjα-ca2的dna全长序列获得
根据sjα-ca2的全长cdna序列设计7对引物,这些引物(相应的退火温度)如seqidno:5至seqidno:18所示,分别为dp1-f(tcttggaggcccataacttg)和dp1-r(gttgtgaggcggcgaccagtcct)(59.2℃)、dp2-f(aggactggtcgccgcctcacaac)和dp2-r(gtaggtccagtcgggaaaggaggat)(65.2℃)、dp3-f(atcctcctttcccgactggacctac)和dp3-r(caggtatcagttctgaattacaagtg)(57.3℃)、dp4-f(cacttgtaattcagaactgatacctg)和dp4-r(gcatctgcagcaggctgtac)(55.6℃)、dp5-f(gtacagcctgctgcagatgc)和dp5-r(atgcgttgtgcgtaagctacgag)(60.1℃)、dp6-f(ctcgtagcttacgcacaacgcat)和dp6-r(gaaggtcaatgtatcgatgagtg)(56.5℃)、dp7-f(cactcatcgatacattgaccttc)和dp7-r(tgaggaaacgtgaatgacgacatc)(54.8℃),以基因组dna作为模板进行pcr反应。pcr反应体系包含1μl的cdna、12.5μl的2×taqpcrmastermix及上、下游引物各1μl,最后加去离子h2o至25μl。pcr反应条件为:94℃预变性4min;94℃变性30s,在相应的退火温度退火30s,72℃延伸2min,运行35个循环;72℃延伸10min,10℃保存。反应产物经上述相同的胶回收、连接、转化、蓝白斑筛选和测序,拼接后获得sjα-ca2的dna全长序列。
(7)运用ncbi中的blastserver(http://www.ncbi.nlm.nih.gov/blast)对已获得的序列进行同源性搜索,利用mega6软件中的最大似然法和邻接法进行聚类分析。
8)带酶切位点的目的基因开放阅读框(orf)序列克隆
根据sjα-ca2的orf序列、克隆质粒pmd19-t及表达质粒pet32a多克隆位点的序列设计带酶切位点的引物hep-f(ggatcccaacggcagcgtggaccca,小写字母为bamhi酶切位点)和hep-r(ctcgagtcacactatgtaaacggcgcgcccg,小写字母为xhoi酶切位点),利用pcr扩增技术扩增sjα-ca2的orf片段。25μl扩增体系包括1μl的cdna、12.5μl的2×taqpcrmastermix、9.5μl的去离子h2o、1μl的上游引物及1μl的下游引物。pcr反应条件为:94℃预变性4min;94℃变性30s,66.7℃退火30s,72℃延伸2min,运行35个循环;72℃延伸10min,10℃保存。pcr产物经过胶回收、ta克隆,以构建携带目的片段的克隆质粒pmd19t/sjα-ca2,然后送上海生工生物工程公司测序确保目的片段序列的准确性。
(9)重组表达质粒pet32a/sjα-ca2的构建
从测序正确的菌液中抽提质粒pmd19t/sjα-ca2,用限制性内切酶bamhi和xhoi分别对其及表达质粒pet32a进行双酶切反应,37℃反应4h。酶切反应体系包含2μl的10×k缓冲液(200mmtris-hcl,100mmmgcl2,10mmdtt,1mkcl,ph8.5)、6μl的pmd19t/sjα-ca2或pet32a、1μl的bamhi、1μl的xhoi及10μl去离子h2o。胶回收酶切后的目的片段,并用t4dna连接酶将酶切后的sjα-ca2片段与pet32a片段连接得到重组表达载体pet32a/sjα-ca2。连接反应体系为:3μl的目的基因片段、7.5μl的pet32a大片段、1μl的t4连接酶及2.5μl的10×k缓冲液,然后加去离子h2o至25μl。将连接后的产物转化到大肠杆菌dh5α感受态细胞,按照上述方法进行克隆、菌落pcr验证和测序。
(10)重组表达质粒的提取与转化
利用质粒提取试剂盒从测序正确的菌液中抽提重组表达质粒pet32a/sjα-ca2,经双酶切反应验证后,将pet32a/sjα-ca2转化至大肠杆菌bl21(de3)感受态细胞。培养并吸取转化的菌液进行pcr验证,并将验证后携带目的基因的菌液送至上海生工生物工程公司测序。
(11)重组蛋白的诱导表达与检测
将测序正确的携带重组质粒pet32a/sjα-ca2的菌液按1:1000(菌液:lb液体培养基)的比例接种于lb液体培养基,在37℃下、以180转/min(rpm)的转速活化培养10~12h。再按1:100(活化菌液:lb液体培养基)的比例,将活化的转化菌液接种于lb液体培养基,放大培养至菌液的od600值为0.6~0.8,加iptg至终浓度为1mm,在37℃下、以180rpm的转速继续震荡培养,以诱导目的蛋白的表达。
取培养4h的菌液在4℃下、以7000rpm的转速离心5min,并将沉淀的菌体用1×磷酸缓冲液(pbs,含0.137mnacl、2.7mmkcl、10mmna2hpo4、2mmkh2po4,ph7.4)重悬。取50μl重悬全菌与2×蛋白上样缓冲液(100mmtris-hcl,ph6.8,200mm的dtt,4%sds,20%甘油,0.2%溴酚蓝)以1:1的比例混合,沸水中煮10min留样备用。将重悬的样品在液氮中反复冻融3次并超声破碎至溶液透亮。4℃下、以14000rpm的转速离心10min。收集上清并用1×pbs按10:1(菌液:1×pbs)的比例重悬沉淀,分别留样保存。利用十二烷基硫酸钠(sds)聚丙烯酰胺凝胶电泳(page)检测重组蛋白的诱导表达情况。
(12)重组蛋白rsjα-ca2的western免疫印迹
在将蛋白样品进行sds-page电泳时,将事先剪好的与凝胶块大小一样的硝酸纤维素膜(nc)用去离子h2o浸泡1h,95%乙醇处理5s,然后放入转膜缓冲液(将30.2g的tris和144g的gly溶解于去离子h2o中并定容至1000ml)中至少平衡10min。待电泳结束后,在电转仪上,由下至上分别放入事先用转膜缓冲液平衡过的海绵垫、三层滤纸、电泳凝胶、nc膜、三层滤纸、海绵垫,使nc膜与正极相连。于4℃冰箱中在100v电压下转膜75min。转膜结束后,将nc膜取出用丽春红染色,观察蛋白是否成功转到膜上,然后用1×tbst(含0.137m的nacl、2.7mm的kcl、0.025m的tris和0.05%的tween20,ph7.4)溶液在室温下用摇床洗3次,每次5min。清洗后,将nc膜立即浸入含5%脱脂奶粉的1×tbst封闭液中,室温下孵育60min。选用抗聚his标签的商用抗体作为一抗,用封闭液按1:1000(一抗:封闭液)的比例稀释一抗。将标记好的nc膜放入,室温孵育90min后,用1×tbst在摇床上洗3次,每次10min。用1×tbst按1:8000的比例稀释hrp标记的羊抗兔igg,室温下在摇床中孵育60min后,再用1×tbst洗3次,每次10min。用增强型hrp-dab底物显色试剂盒在暗室中进行显色,并拍照记录。
(13)重组蛋白rsjα-ca2的分离与纯化
根据his标签能够与金属离子发生亲和作用的原理,利用bio-scaletmminiprofinitytmimaccartridges蛋白亲和层析纯化预装柱来分离与纯化与组氨酸标签融合表达的重组蛋白rsjα-ca2。
①新的1ml预装层析柱要先用2倍(即2×)于层析柱柱床体积(columnvolume,cv)的20%乙醇以2ml/min左右流速清洗,再用2×cv的超纯水以相同的速度流过层析柱。经过这样处理的层析柱即可用于后续的蛋白纯化。
②用至少5×cv的洗脱缓冲液1(5mm咪唑、50mmkh2po4、300mmkcl,ph8.0)平衡层析柱,流速控制在2ml/min以内。
③将自转基因菌液中制备的上清先用滤膜过滤一下,以防止堵塞柱子,然后以0.5ml/min的流速通过层析柱。
④再用6×cv的洗脱缓冲液1以2ml/min的流速清洗层析柱。
⑤然后,依次用10×cv的洗脱缓冲液2(含10mm咪唑,其他组分同缓冲液1,以下的洗脱缓冲液都如此,均省略)、洗脱缓冲液3(含50mm咪唑)、洗脱缓冲液4(含100mm咪唑)、洗脱缓冲液5(含150mm咪唑)、洗脱缓冲液6(含200mm咪唑)、洗脱缓冲液7(含250mm咪唑)以2ml/min的流速再次清洗层析柱,分别留样,4℃保存备用。
吸取50μl每一梯度的洗脱产物与2×蛋白上样缓冲液等体积混合后于沸水中煮10min,-20℃留样保存,利用sds-page进行电泳检测。将洗脱下来经过电泳检测的目的蛋白,用50×体积20mm的tris-hcl(ph8.0)缓冲液在4℃下透析12h,然后进一步浓缩并检测蛋白的浓度,置4℃冰箱保存备用。
(14)重组蛋白rsjα-ca2的水合酶活性测定
①co2饱和水溶液的制备:将co2通入到0℃的去离子h2o中,持续通气1h。
②巴比妥混合液的配制:巴比妥0.184g,巴比妥钠1.030g,加去离子h2o至100ml,调ph至8.4,放在冰水混合物中备用。
③酶活性检测:将3ml纯化的rsjα-ca2(用1×pbs将蛋白浓度调至0.410mg/ml)溶液加入到4ml巴比妥钠的缓冲液中,测定ph值;然后加入3ml的co2饱和水,测定下降一个ph单位(即ph自8.3降至7.3)所需要的时间(min),整个过程要保持在冰水混合物中。
④酶活性计算:若1个酶活性单位(u)定义为(t0-t)/t(haglundetal.,1992),其中,t0和t分别代表加入1×pbs和蛋白酶液后下降一个ph单位所用的时间(min),那么,rsjα-ca2的比活力即可用“(t0-t)/t/mg蛋白质”来计算。
(15)重组蛋白rsjα-ca2的酯酶活性测定
①对硝基苯酚(p-np)标准曲线的绘制:先配制含10%丙酮的1×pbs缓冲液,然后用该缓冲液配制0.05、0.1、0.5、1、2、4、6μm等不同梯度浓度的p-np溶液。
②3mm乙酸对硝基苯酯(p-npa)配制(需现配现用):取0.0136g的p-npa,用丙酮溶解并定容至25ml。
③操作步骤:0.6ml的重组蛋白用0.2ml的1×pbs稀释(空白对照组是直接加入0.6ml的1×pbs缓冲液),然后加入0.1ml的p-npa迅速混合,用紫外分光光度计检测反应起始时405nm处的od值,并每隔3min反应时间记录其od405值,根据实验组和对照组的od405变化情况来确定其酯酶活性。
④酶活性计算:若一个酶活性单位(u)定义为在0℃下、每min产生1μmol的p-np(bhaktaetal.,2016),那么,rsjα-ca2的比活力即可用“(c-c0)×v/t/g蛋白质”来计算;其中,c、c0分别代表加酶液和不加酶液体系中p-np的浓度(μmol/ml),v为总反应体积(ml),t为反应时间(min)。
3、结果
(1)根据一条长为885bp的contig序列设计引物af和ar,以海带配子体的cdna为模板,扩增得到一条长888bp的产物,经重新设计引物并进行pcr扩增,明确了该contig的序列。利用race技术分别获得354bp长5′-race的pcr产物(图1泳道1)和953bp长3′-race的pcr产物(图1泳道2)。经与验证的长888bp片段拼接,并重新设计引物扩增、克隆与测序后,可知sjα-ca2的cdna全长序列大小为1728bp,如seqidno:1所示,包括一个长为888bp的orf区、263bp的5′-非翻译区(utr)以及577bp的3′-utr。
sjα-ca2编码一个由295个氨基酸组成的前体蛋白,相对分子质量为32.2kda,等电点为4.57。经signalp和ipsort预测,在28ala-29ser处有一个典型的信号肽酶切位点,酶切后的成熟蛋白由267个氨基酸组成,相对分子质量为29.27kda,等电点为4.48。
基于sjα-ca2的全长cdna序列设计7对引物(dp1-f和dp1-r、dp2-f和dp2-r、dp3-f和dp3-r、dp4-f和dp4-r、dp5-f和dp5-r、dp6-f和dp6-r以及dp7-f和dp7-r),以海带基因组dna为模板进行pcr扩增,产物(图1泳道3~9)的大小在1100bp~1900bp之间,经测序、拼接和验证,可知该基因的dna全长序列大小为8856bp,如seqidno:2所示。
将该dna序列与其对应的cdna序列进行比对,发现sjα-ca2存在9个内含子,它们的大小自5′-端开始依次为908bp、358bp、879bp、720bp、1077bp、420bp、308bp、346bp和2112bp,从而将该基因的orf分隔成10个外显子(图2)。
(2)将自ncbi中同源搜索获得的48条不同物种ca的氨基酸序列与sjα-ca2用最大似然法(ml)和邻接法(nj)进行聚类分析。结果(图2)显示,49条序列明显地被聚成3大支,分别对应于α-ca(nj和ml的靴带值分别为100%/84%)、β-ca(nj和ml的靴带值分别为100%/-)和γ-ca(nj和ml的靴带值分别为100%/86%)。本研究自海带中所克隆的ca基因在聚类图中位于α-ca分支,且与已经报道的海带另一条α-ca(genbank登录号:aef33616.1)很接近,从而表明sjα-ca2应属于α-ca家族。
(3)基于sjα-ca2的全长cdna序列、克隆质粒pmd19-t及表达质粒pet32a多克隆位点的序列,设计带酶切位点的引物hep-f和hep-r,以海带配子体的cdna为模板,扩增到sjα-ca2不含有信号肽的orf序列,并连接至克隆质粒pmd19-t上构建pmd19t/sjα-ca2;再用bamhi和xhoi进行双酶切pmd19t/sjα-ca2及表达质粒pet32a,连接目的片段以构建重组表达质粒pet32a/sjα-ca2。提取该表达质粒,经bamhi和xhoi进行双酶切反应,其产物经电泳检测(图4泳道1),只出现目的基因大小(804bp)和载体序列大小(5854bp)的片段,表明已经成功地构建了pet32a/sjα-ca2的重组表达质粒。
将pet32a/sjα-ca2转化大肠杆菌中,获得转基因细胞系et32a/sjα-ca2。经放大培养及添加iptg诱导培养后,收集菌体,反复冻融以破碎细胞,分别提取上清和沉淀中的蛋白,经sds-page电泳,发现上清(图4泳道2)和沉淀(图4泳道3)中均有目的蛋白的存在。该目的蛋白的大小为45.57kd,包含29.27kd由目的基因编码的蛋白和15.3kd由表达质粒pet32a中his标签及多克隆位点碱基所编码的多肽(图5)。由于本发明运用表达质粒pet32a中的his标签融合表达目的蛋白,因此,可利用商业提供的抗聚his标签的抗体,对自转基因细胞系中提取的总蛋白进行western免疫印迹,以确定目的蛋白的表达。western印迹结果(图4泳道4)显示在目的蛋白大小处只出现一条信号,说明该重组的蛋白中具有his标签;印迹所对应的分子量大小约为45kd,与重组蛋白预测的分子量大小相符,表明重组的就是目的基因sjα-ca2所编码的蛋白。
(4)利用bio-scaletmminiprofinitytmimaccartridges蛋白亲和层析纯化预装柱,对自上清中提取的蛋白用含不同浓度咪唑的洗脱缓冲液进行纯化。其中,用含150mm咪唑的洗脱缓冲液洗脱下来的蛋白,经sds-page电泳和染色,在目的蛋白大小处只显现一条带(图6泳道5)而无杂带。因此,可以利用150mm咪唑的洗脱缓冲液纯化重组蛋白rsjα-ca2。
(5)在体外构建co2的水合反应(即co2+h2o→hco3-+h+)体系,利用电极法测定可知,在不加rsjα-ca2的体系中,需要约4min的时间,ph才能自8.3下降到7.3;但在加入rsjα-ca2的体系中,只需要约2min的时间,ph就下降到7.3;表明rsjα-ca2具有加速co2的水合反应能力,从而使反应体系在指定时间内形成更多的h+。通过计算可知,rsjα-ca2的水合反应比活力为0.54±0.046u/mg蛋白(3次重复试验的平均值±标准差)。
鉴于α-ca还具有酯酶活性,本发明还构建体外将p-npa酯化成p-np的反应体系,来检测rsjα-ca2的酯酶活性。在不加重组蛋白的对照组中,12min时,od405值就不再发生明显的变化,表明此时在这个体系中几乎不产生新的p-np;但在加入rsjα-ca2的实验组中,od405值会随着时间的延长不断地增加,表明加入的rsjα-ca2能使p-npa逐渐酯化从而生成p-np。通过计算可知,rsjα-ca2的酯酶比活力为0.249±0.042u/g蛋白(3次重复试验的平均值±标准差)。
序列表
<110>上海海洋大学
<120>海带α型碳酸酐酶基因sjα-ca2及其编码蛋白和应用
<141>2019-05-10
<160>20
<170>siposequencelisting1.0
<210>1
<211>1758
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>1
gtggggtgtcgcggcagcgtccgtggtgtgccgcgacatgtcgcgacacgtgccacgaaa60
aagtccaataatgtattatttgtgtccgtttcacatatcgtttataacacgacagacaca120
aaggcaccctcagctatccggacaatgggcaaggtacctctcacacttagattgtcctca180
tcttcgccccacggctgtacccacttgtgtgttgtcgtttacttgtatccgtttcacata240
tcgtttataacacgacagacactatggcaccctcagctatccggacaatgggcaaggtgc300
tcttgtgctctcttctcctgccaagcttcccaggactggtcgccgcctcacaacggcagc360
gtggacccacgactgccgacgagcctgaggaatcctcctttcccgactggacctaccgcc420
gcgcttcccacgaaggagaaaggccgtacagccccagcgattgggagatcggctacccgg480
actgtggcggagactctcagagccccatcaacttgtccgccaatgttggaacgctcgtcg540
aggcaactgagttcaatcttgagcttttcggagctgaatgtgcgtcgaaagagttggact600
tcgaggccaacggacacgtctgggagatcgactttagcgagtgtacctccacctccaatc660
tctccttcgacggcggcaagtacagcctgctgcagatgcacatccactccccttccgagc720
acatggtcgcaggatcattgcacgatgccgagattcatttagtgcactcccgtgacgatt780
cggacggcacagaatctgagcttctcgtgataggcgtcttcctggatgcgaaagagcacg840
gctggaatgttgcgcttgagccactgtgggatgttctgggttctggggctaaacctaggg900
gcgtcatcaacccctacgagctgataccgtccgacatggcgtactcgcactacatgggat960
ctctcaccacccctccctgcagcgagatagtgaggtgggtcgtcatgagcacaccaaccg1020
taatcggcgatctacagcttgatatcttccgcgactcggtcgccaccgctacgaactccc1080
aggtggatgagcgctctaacacaaaccgcccgggtcaggcgatcaacgggcgcgccgttt1140
acatagtgtgagggcgcgacatgtgtccagcccgaggtgtagatggggggggtacactcg1200
agcgagtacctccttgacgccacacaaagacatcgctccaagggatggagagactgtatc1260
aatagcagtactatagtcagccgttacaaggctgtgtttggtagggctaggtacaatagt1320
tatatgggtgtatgtttcggccatacacaaaacagtgctggtatggccacgagtatcttt1380
cctccaacttagggttcgtaatattctcgacgggtatagtattggggggcggttataagg1440
atacttaaaaagacccgttggttatgttctaccggggtcaataccctgggtccctcgatg1500
taaataacgcatgcacagcgtgcagtagttttattgtatgatgtcgtggcgattccttcc1560
tcgactgatctggcatgtgcgggtacgtcacctagcgtcaagggtttgcaattgcattgg1620
gggcggtagtattgggaatatatatacccgttaggtacctcgaagtacgcaaccgtgtag1680
ttttgaagtgtatatctgtcaaaacgatgtcgtcattcacgtttcctcaaaaaaaaaaaa1740
aaaaaaaaaaaaaaaaaa1758
<210>2
<211>8856
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>2
gtggggtgtcgcggcagcgtccgtggtgtgccgcgacatgtcgcgacacgtgccacgaaa60
aagtccaataatgtattatttgtgtccgtttcacatatcgtttataacacgacagacaca120
aaggcaccctcagctatccggacaatgggcaaggtacctctcacacttagattgtcctca180
tcttcgccccacggctgtacccacttgtgtgttgtcgtttacttgtatccgtttcacata240
tcgtttataacacgacagacactatggcaccctcagctatccggacaatgggcaaggtgc300
tcttgtgctctcttctcctgccaagcttcccaggactggtcgccgcctcacaacgggtaa360
gccttccattttggcgtatgtatcgtactcgaatgcatgtaccatgtaacgtaacccgtg420
gctgctgaacggcaaccggggttgaacacaggttagactatatcatttgttgatagttat480
ccagtcaacagtaattgtaccattaactacagtgtcgatagaatgtggtgctattaataa540
tagactataatgtcatgccctgttcgtattccacgcggagtgacaacgggcggtttgtac600
gtgggagacaaacagatgtcttccgcaaatagcggaccacctggcaacaagtaccggtag660
gtattttagtatgttcgaagcagacatttagccattcactcgggctctggttgcgtaaag720
gcaccgatggcctcgctgttgctattgtcgccgattccctcctgcatttatcacacgtgt780
gtactcattcatcatatcgtgtccttcgagggtgaaaacaaattaatcccttgaattaca840
cagcagtatttatagtatgacttaattacaaatatgtgctaaacgggggccgaattcttc900
cacgacctggatggcagcaacttaaacttcttgctgttacgtacgtacgtacgtacgtac960
gtacgctcaaacgaatcgatagtcattgctctcgaacggggcgttttttgtggtccatgc1020
tcttcgccaattatattccagacacgcgtgttcagtgctcgcacatgttgcctgtttcaa1080
tccaacccttacgcgtgctttcatggcccgctgtcgctgttgtcgccctctgacgtgtga1140
aatcaccttggacaccacctgcgttcgttaaacccaccggaaaactggatggcaccttgg1200
acaccacctgcgttcgttgaacccaacggaaaactggatggcatattgtgcccatggacg1260
gcagcagcgtggacccacgactgccgacgagcctggtacgctgaggacactaccgtaggt1320
ttagctcctttggacacgtattttatgtgtcaaggcatgtggttcgttgtcaactgagtg1380
cctctaaactgcgaattgacgatgctattatgtcttcgcttcacgttgatgtacatgcat1440
acaaagttctcaaggagctgcaagcaacgttttcggaggtaaatttcgtttacttatggt1500
agtgaaacatcctctttagggaaataattgaaagctaccggtatgtgctgctgtatgtca1560
agcccacaattgaaatggatggaagacgcccgtcattcttaccttttttctccaatgggt1620
ttgccctgttccggctgctgttctgctcaacagaggaatcctcctttcccgactggacct1680
accgccgcgcttcccacgaaggagaaaggccgtacagccccaggtacgtgttacagacag1740
caccagcataacgacgtatttttcggactgtccacgcacgttccgtagcgagaccatttg1800
ttgcacaggtggccgagaccccccttcagttgcatcatgcgggaggaacaaataccgttg1860
tgggcacgctgaacactgaagcacacacataggcgtatcggatttagaggttgtcgacac1920
cttgtgggagttgctgcacggttcagctgttgccgtgtcttcacaaagcgttttggacgc1980
ccacactgtggaagggtgtactgtagagtgaggccctgcagcaaatgtcggcaaatcgaa2040
atgtagccatgcaaaccctgaagagcgcggcgaggctaccccgcggatggatgcgttttt2100
ttttatatacccctgtaccaggtagttcttgaaaaagtatgctgctctagcttgtgtatg2160
tacgatcataaactttcgtcgagtcttaccatgcggtcctttcttctctttctccattat2220
gttgagcctgcggtgggttaatcacgcactgcattggcatcaaggtacaacacctgactc2280
gccttcgtatgggcgtatgcctcgttcgctggtgcacgtatctagacacgaacactaaaa2340
cgttgaacgagtactcgtacttcaactctgtttgattgtactctacacatatatagttag2400
accgggggtgtttgacgggttctattgtagcttgtaatccttatagatgcgttatgggcc2460
agatgtagagtttattaacctgcgttcggaaaccgaagatcgttggtcaacattataaca2520
aatgccctgcattagtactcatgaccgctgcgccgccgcctgtggaataattcgtggtcc2580
tcacgccgtaatctgacgacagcgattgggagatcggctacccggactgtggcggagact2640
ctcagagccccatcaacttgtccgccaatgttggaacgctcgtcgaggtacacactaaag2700
tacggtggcagtagaaaataccgaccagatgcgaggtgcacgcgggaaatccaaagactg2760
tgtcctcgttgcttgctattgtggttggttttacacgggagtcggggtgtgaataccact2820
gtacctcgttcccggttaacgaaatttaaacggagcgcgttggtgcgtctggcaacgacg2880
taacatgtcaggaacgaaacgcctgtacttacgattatttgtcggtagaaacgtcgtgaa2940
catatataggatagacggtaggtccgtgctcgtgtgtggggctttataaacgccattcat3000
ggagctgatacaaaacataattttggtgtcaacttgcgtgttgttttttctgacgatgta3060
tagtgcgtgtaatctgtgcatgccgcgttttctgtaattcagtgttggccgcaagtttcc3120
aagattggagttggtagtaggccaacctatatatatcacttgtaattcagaactgatacc3180
tgagatggcaccgacgtagttacgacttatgttggcgacattgcagaccgtgcctgttat3240
ccttttgaccaagctaggcaatccagttaagtctggaattgttcgggcccatagcacgaa3300
aagcctcatgacgatgattggctgccgtttctcatgtaaggtgacccactgcaatgctgc3360
gcatgcctatatatcggcttgacgtgcctgtcgtttttctgacctaggcaactgagttca3420
atcttgagcttttcggagctgaatgtgcgtcgaaagagttggacttcgaggccaacggac3480
acgtctgggaggtaagccgctgcgtcggttattttctgtaatgccgtcatatgccttgga3540
atgagagacccgtgctcggtgataggaaacgcaaaatttctccgttaactctctatccca3600
ctagagtgtgaggtattgaccagtggacagctgcgtcccgtctgccgaccgtctgcatgc3660
cgggtcaccctgcatcattgttctgttttgttctgcgtactgtgctctactgtatggtgg3720
caccagccgtataattccacgtacgtgctgggctgttcggatctgcacgtacttttgcac3780
catctctacccttactcccacccggacctaatgctacccggatctgatcccatttggcac3840
cctgctcccacccacaaggtgcagaaatataatcagccctccgcaggagccgccggaggc3900
acacctggcacctcgatcccattttgtacccatgtaggccatagatatctacaacaactc3960
ctgctatacatttaaccgtattgaatgtacgaattcgaatagcctggcacgtacgtgcac4020
gttctccggagccggtatggtggtgtgtattgtactcgacggtactctggacgagtgtta4080
cggtagtaccaggtagctcctactgctgtagtttcttcggaagctcctcacttcaaaatc4140
ttcctgccacaagcgaaataaacgcatataactaacgaacaacaaaatcaaggtggataa4200
tcccatggcctgcggtaaaaaccccacgaatgatgctgtaaaacacgaatggggctccaa4260
tattaaggcttgccttattggctagttcctccgttcaagacagcgatcagcaatttttat4320
attctactgtacctctatgatatcacgcgtcggtactgctcttgttctatattgccctgc4380
attaaatttcctcgccacttcccgcatgaatttctgtgctgtgctgtactgtgtacggcc4440
ttatatgactgttctctaccgcactcgtaccgtgctgtactgtgctatgctgtggtgcgc4500
tgtgtcctttccggtattgcgctgtatcatgtctattgcacacccggctgaactaatttg4560
aggagcagatcgactttagcgagtgtacctccacctccaatctctccttcgacggcggca4620
agtacagcctgctgcagatgcacatccactccccttccgagcacatggtgagtgacagca4680
tatatattatcgatagttatagtacacctgcgaaacgccgctcaagagcttacatcgcaa4740
agtcctgagttttggtgaatctccggtgcaataagcagcggcacccaacggagactaatg4800
tccttcgttggcaaaacggtagatattaactcgtcctctgtaatagcaagaaggccatgc4860
cgttccacggagcaaacacaccaccaacaatggatttgggactttttctagacatcgtga4920
acagtcgtttcctacgtcatattttccactcctataaccttgagagcgtactgttctaaa4980
gccattgcagcagcactcgtgcactatgcatcaatatctcagctgtgaacaaaaaagcga5040
cgagtgttaacctcgcgcggctgtgtttccccctcgtatgcgagcaggtcgcaggatcat5100
tgcacgatgccgagattcatttagtgcactcccgtgacgattcggacggcacagaatctg5160
agcttctcgtgataggcgtcttcctggatgcgaaagagcacggctggaatgttgcggtaa5220
gtctgccgacgatggactacggttcttacaactgctgtgtagaacaccgaagtgctcacc5280
atgcactcttagctattgtctgcgtggttctgcgaccatcatgttgtgaaccaaacccac5340
tattattgtaactgcaatatgtctacactactacacatggacaacgtccgaaaatcccga5400
acataaaccgtcagatcccggcatacatcgctggggtccgcctctcactttgccaagaaa5460
cgcactgaacgactgacttacgcataccccctttcgcgcttcgttggcctgaatggatcg5520
acagcttgagccactgtgggatgttctgggttctggggctaaacctaggggcgtcatcaa5580
cccctacgagctgataccgtccgacatggcgtactcgcactacatgggatctctcaccac5640
ccctccctgcagcgaggtgatcagatgtttgaagcaatacacttccagttcgttccccca5700
cgtatgcggcaggttgttgcgcgcacttgtaggagaaacggggtcgagtggttttacact5760
atcatatttgccaaacacctgctatacgaagcgtacgtggtaaaacaattttcaggtggg5820
gtcttgctggcaagttaggtatatagacttacagtacacggttcgcattttttacttgaa5880
tagtcgcgttgccgtttgaagtacattcatgatatggtcttcgcctgtgccggccgctcg5940
tagcttacgcacaacgcatatcatacaaaatgttcggatgccgactgaatgacgccgcgc6000
agatagtgaggtgggtcgtcatgagcacaccaaccgtaatcggcgatctacagcttgata6060
tcttccgcgactcggtcgccaccgctacgaactcccaggtaaaccgtaaacacaatgacg6120
agagtcgggcatgcatcactacggtacgagttacctcgttgctgttttgtgtgggtggtt6180
tttggtgcgtttttgtagaatgtcagtgcgaagcaattaagaacatggttgtatgagatt6240
cgttttatactttttcctcaagtgcacttcgcgagttttaataaatatgcaactccaaag6300
aaacgagtactgtgccatgacaagacgaccaataccaagatttgggtattttttaatgtg6360
aaaaaacgcatatatatatatgataatatgttataacaccggtcgccccggtagactagt6420
ggtcagcttcaaaggctactagcattggtacccaagttcgaataccaccgtgttgagatt6480
ttcactttatttgaaaaaatagaaggaaccaattgctgagagcgcctttgtgacgtgggt6540
aggcggaatccgacgcaagttgacgagggaagaaagtgctgaaatcttgtcgcgataaaa6600
atacaaggcacgtaccgtagtggggaggggggagaagagcctgcatagttaccccggatc6660
tgagttacgactaaagagggagaaaagaagggcgaacataacaatacaagaagggcgaag6720
ataacaataaatgggatggacggtgactacacaacagccacatcgagcctgtctgaaaag6780
cggccaatattactcaacagtcatattgtatgcttgaatagcgtcccatcaagcaacccc6840
tttgcttcggcgaggtattgtatacaaatatttcgatagtattggcgatgccatcggccc6900
gaccaaagacaactgctacgtacgagctgggccagccataaaaggtttacacgtcggatt6960
ggcgatgcgatgccccatcaattttacgagtttggacttgatgtttggacactgtgtagt7020
taaagcactcatcgatacattgaccttcggccctatatatatatattctcaagagatatg7080
accgatccaacaacccgaaaaaatacaaaagcgaccaaaacttgtaaaaaaaaacaaaaa7140
aaaaatagggccgacaagtgaatgcctttgaacgtgcgattcaaatccggggttagacat7200
ccagtgcaaatttctcaaaatagagcggggcttgtagaaatgccatttttttcgtattga7260
cttgacttggtgtatggaatcggttttggtaacatctcttggtgggtggcgaattgggta7320
acgagagtttcgtcgcttttttccttgtgtgtttcaccactgactgtctcgcaccaagtt7380
tcttgatgaaaacgacgttttagttttcacgaatttggtgtagaaaagttggtgcttttt7440
tgttttcgcggatatctcggcgagatcgagccgaggaaagaaagagctacataatgtttc7500
atgtacgttttgtttgcgtaagcagtgatgtgtcagggtcattatccccaattttgtgta7560
gcctgattagcagtggttcacaagatacgacgttaggaagctttctccgttttatggctg7620
gccccgctcgtagtcattaggagtgcattgcacgtttacacgtcgccatcaccgaaatgt7680
atcatactgataattgatagctagaaaatgccgacggattgttcaaagagttgtgcctag7740
gatttattatcgaatcgaacggttcgtgcgagagtgagcatgtaaaatacacatatctac7800
ggcataggcttgattgactgtatcaccgtaaagtatcgatggaggatgaactaaggtcct7860
tgtcgacggcggtcatcggggcgtaccggacgtcaatagcttgcccgccccgacgatctg7920
ttgaatccaaattagggacggtcggccattggggaggatgtgcctgttttagtccatatt7980
actgttgtatacctacccccagcactgtgcttcctgtgttgcctgtttgctttgctgcct8040
tgttgtgcccatggaaccgaaataccgatcacgtacaatcaacgacggtggctgatacct8100
ttgagcttgtaggcggctcattggccgacgaacaaaaggcgacgcctttacagtccaact8160
cataccaccgacctacttccaccccttgctcgtttatctcggctatgcaggtggatgagc8220
gctctaacacaaaccgcccgggtcaggcgatcaacgggcgcgccgtttacatagtgtgag8280
ggcgcgacatgtgtccagcccgaggtgtagatggggggggtacactcgagcgagtacctc8340
cttgacgccacacaaagacatcgctccaagggatggagagactgtatcaatagcagtact8400
atagtcagccgttacaaggctgtgtttggtagggctaggtacaatagttatatgggtgta8460
tgtttcggccatacacaaaacagtgctggtatggccacgagtatctttcctccaacttag8520
ggttcgtaatattctcgacgggtatagtattggggggcggttataaggatacttaaaaag8580
acccgttggttatgttctaccggggtcaataccctgggtccctcgatgtaaataacgcat8640
gcacagcgtgcagtagttttattgtatgatgtcgtggcgattccttcctcgactgatctg8700
gcatgtgcgggtacgtcacctagcgtcaagggtttgcaattgcattgggggcggtagtat8760
tgggaatatatatacccgttaggtacctcgaagtacgcaaccgtgtagttttgaagtgta8820
tatctgtcaaaacgatgtcgtcattcacgtttcctc8856
<210>3
<211>295
<212>prt
<213>2ambystomalateralexambystomajeffersonianum
<400>3
metalaproseralaileargthrmetglylysvalleuleucysser
151015
leuleuleuproserpheproglyleuvalalaalaserglnarggln
202530
argglyprothrthralaaspgluproglugluserserpheproasp
354045
trpthrtyrargargalaserhisgluglygluargprotyrserpro
505560
serasptrpgluileglytyrproaspcysglyglyaspserglnser
65707580
proileasnleuseralaasnvalglythrleuvalglualathrglu
859095
pheasnleugluleupheglyalaglucysalaserlysgluleuasp
100105110
pheglualaasnglyhisvaltrpgluileasppheserglucysthr
115120125
serthrserasnleuserpheaspglyglylystyrserleuleugln
130135140
methisilehisserprosergluhismetvalalaglyserleuhis
145150155160
aspalagluilehisleuvalhisserargaspaspseraspglythr
165170175
glusergluleuleuvalileglyvalpheleuaspalalysgluhis
180185190
glytrpasnvalalaleugluproleutrpaspvalleuglysergly
195200205
alalysproargglyvalileasnprotyrgluleuileproserasp
210215220
metalatyrserhistyrmetglyserleuthrthrproprocysser
225230235240
gluilevalargtrpvalvalmetserthrprothrvalileglyasp
245250255
leuglnleuaspilepheargaspservalalathralathrasnser
260265270
glnvalaspgluargserasnthrasnargproglyglnalaileasn
275280285
glyargalavaltyrileval
290295
<210>4
<211>334
<212>prt
<213>2ambystomalateralexambystomajeffersonianum
<400>4
metserleualaglyserglyserglyhismethishishishishis
151015
hisserserglyleuvalproalaglyserglymetleuglythrala
202530
alaalaleuproglyalaglyhismetalaserproalaleuglythr
354045
alaalaalaalaleualametalaalaileglnargglnargglypro
505560
thrthralaaspgluproglugluserserpheproasptrpthrtyr
65707580
argargalaserhisgluglygluargprotyrserproserasptrp
859095
gluileglytyrproaspcysglyglyaspserglnserproileasn
100105110
leuseralaasnvalglythrleuvalglualathrglupheasnleu
115120125
gluleupheglyalaglucysalaserlysgluleuaspphegluala
130135140
asnglyhisvaltrpgluileasppheserglucysthrserthrser
145150155160
asnleuserpheaspglyglylystyrserleuleuglnmethisile
165170175
hisserprosergluhismetvalalaglyserleuhisaspalaglu
180185190
ilehisleuvalhisserargaspaspseraspglythrgluserglu
195200205
leuleuvalileglyvalpheleuaspalalysgluhisglytrpasn
210215220
valalaleugluproleutrpaspvalleuglyserglyalalyspro
225230235240
argglyvalileasnprotyrgluleuileproseraspmetalatyr
245250255
serhistyrmetglyserleuthrthrproprocyssergluileval
260265270
argtrpvalvalmetserthrprothrvalileglyaspleuglnleu
275280285
aspilepheargaspservalalathralathrasnserglnvalasp
290295300
gluargserasnthrasnargproglyglnalaileasnglyargala
305310315320
valtyrilevalalaproproproproproleualaglycys
325330
<210>5
<211>20
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>5
tcttggaggcccataacttg20
<210>6
<211>23
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>6
gttgtgaggcggcgaccagtcct23
<210>7
<211>23
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>7
aggactggtcgccgcctcacaac23
<210>8
<211>25
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>8
gtaggtccagtcgggaaaggaggat25
<210>9
<211>25
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>9
atcctcctttcccgactggacctac25
<210>10
<211>26
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>10
caggtatcagttctgaattacaagtg26
<210>11
<211>26
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>11
cacttgtaattcagaactgatacctg26
<210>12
<211>20
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>12
gcatctgcagcaggctgtac20
<210>13
<211>20
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>13
gtacagcctgctgcagatgc20
<210>14
<211>23
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>14
atgcgttgtgcgtaagctacgag23
<210>15
<211>23
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>15
ctcgtagcttacgcacaacgcat23
<210>16
<211>23
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>16
gaaggtcaatgtatcgatgagtg23
<210>17
<211>23
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>17
cactcatcgatacattgaccttc23
<210>18
<211>24
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>18
tgaggaaacgtgaatgacgacatc24
<210>19
<211>26
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>19
atggcaccctcagctatccggacaat26
<210>20
<211>25
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>20
tcacactatgtaaacggcgcgcccg25
- 还没有人留言评论。精彩留言会获得点赞!
- 腈水解酶突变体及其编码基因和应用的制造方法与工艺
- 植物抗旱相关蛋白AsTMK1及其编码基因和应用的制造方法与工艺
- 植物抗旱相关蛋白EtSnRK2.2及其编码基因和应用的制造方法与工艺
- OsSAPK7蛋白及其编码基因在提高水稻白叶枯病抗性中的应用的制造方法与工艺
- 一种抗除草剂抗虫融合基因、编码蛋白及应用的制造方法与工艺
- 毛果杨PtrZFP103基因及其编码蛋白和应用的制造方法与工艺
- 大豆bHLH转录因子基因GmFER及其编码蛋白和应用的制造方法与工艺
- 一种花狭口蛙的基因及其编码的多肽和该多肽的用途的制造方法与工艺
- 一种泽陆蛙基因及其编码的多肽和该多肽的用途的制造方法与工艺
- 一种水稻MIT1基因、其编码蛋白及应用的制造方法与工艺