芳胺基硅烷化合物、丙烯聚合催化剂及其制备与应用的制作方法
本发明属于烯烃催化聚合领域,特别是一种芳胺基硅烷化合物、丙烯聚合催化剂及其制备与应用。
背景技术:
以镁、钛、卤素和给电子体作为基本成分的固体催化剂,可用于ch2=chr丙烯聚合反应。在用于聚合反应时,要同时加入助催化剂烷基铝化合物以及外给电子体组分。对于丙烯的定向聚合,如果不加外给电子体,大多数催化剂所得聚合物等规度较低,一般低于90%,不利于工业生产和聚合物的应用。因此,对于多数丙烯聚合催化剂来说,外给电子体的加入起着十分重要的作用。
目前,外给电子体的种类己由最初的苯甲酸酯类发展到现在广泛使用的有机硅氧烷类。如us4562173中公布了一种烯烃聚合催化剂的组分,其中包含通式为sirm(or’)4-m的有机硅氧烷化合物,其中r是氢原子、烷基或者芳基,r’是烷基或芳基,m的范围是0≤m≤4。该专利公开的实施例显示,使用苯基三乙氧基硅烷为外给电子体,进行丙烯聚合,聚丙烯产物的等规度明显高于对比实施例对甲基苯甲酸乙酯外给电子体。专利cn1176258公开了一种丙烯聚合和共聚的催化剂体系及聚合方法,所述的催化剂体系包含常规载于载体上的ziegler-natta催化剂与通式为sirm(or’)4-m的外给电子体的组合,其中r为选自烷基、环烷基、芳基和乙烯基的基团,r’为烷基;m为0~3,其中当r为烷基时,r可与r’相同;当m为0、1或2时,r’基团可相同或不同;当m为1、2或3时,r基团可相同或不同。更具体的,该催化剂体系的外给电子体可以选自环己基甲基二甲氧基硅烷,二异丁基二甲氧基硅烷,二叔丁基二甲氧基硅烷,环己基异丙基二甲氧基硅烷或二环戊基二甲氧基硅烷。该催化剂体系活性较高,并可以很好的控制聚合物的二甲苯可溶物含量在0.6~3.0wt%范围内,获得高结晶度的聚丙烯产物。所述的外给电子体尤其优选二环戊基二甲氧基硅烷。该专利公开的实施例显示,二环戊基二甲氧基硅烷与其他几种外给电子体相比,聚合产物的二甲苯可溶物含量最低,等规度最高。
尽管用于烯烃催化聚合的有机硅氧烷类外给电子体己有较多的公开专利报道,但是芳胺基硅烷类外给电子体没有报道,本发明设计合成了一类新型的芳胺基硅烷化合物,并考察了将其作为外给电子体应用于丙烯聚合反应中的性能。
技术实现要素:
基于以上背景技术,本发明提供一种芳胺基硅烷化合物、丙烯聚合催化剂及其制备与应用。本发明所提供的胺基硅烷化合物用作丙烯催化聚合的外给电子体,具有较好的氢调敏感性。
为了实现以上目的,本发明采用以下技术方案:
本发明第一个方面提供一种芳胺基硅烷化合物,该芳胺基硅烷化合物具有式i所示结构:
其中,r1为c1-c8的直链或支链烷基或者c1-c8的硅烷基;
r2、r3、r4、r5和r6各自独立地为h或者c1-c12的直链或支链烷基;
r7、r8和r9各自独立地为c1-c8的直链或支链烷基或者c1-c8的直链或支链烷氧基。
本发明的芳胺基硅烷化合物式i中,优选地,r1为甲基、乙基、丙基、三甲基硅基、三乙基硅基、二甲基乙基硅基或甲基二乙基硅基。
本发明的芳胺基硅烷化合物式i中,优选地,r2、r3、r4、r5和r6各自独立地为h、甲基、乙基、丙基或异丙基;可以相同或不同。
本发明的芳胺基硅烷化合物式i中,优选地,r7、r8和r9各自独立地为甲基、乙基、正丙基、异丙基、甲氧基、乙氧基或丙氧基;可以相同或不同。
在一个优选方案中,本发明的芳胺基硅烷化合物式i中,r1为甲基或三甲基硅基;r2、r3、r4、r5和r6均为h;或者r3、r4和r5均为h,r2和r6均为异丙基;r7、r8和r9各自独立地为甲基、甲氧基或乙氧基。
本发明优选实施例中的芳胺基硅烷化合物为(n-甲基苯胺基)三甲氧基硅烷、(n-甲基苯胺基)甲基二甲氧基硅烷、(n-甲基苯胺基)三乙氧基硅烷、(n-甲基苯胺基)甲基二乙氧基硅烷、(2,6-二异丙基-n-三甲基硅基苯胺基)三甲氧基硅烷、(2,6-二异丙基-n-三甲基硅基苯胺基)甲基二甲氧基硅烷、(2,6-二异丙基-n-三甲基硅基苯胺基)三乙氧基硅烷、(2,6-二异丙基-n-三甲基硅基苯胺基)甲基二乙氧基硅烷。
本发明第二个方面提供了一种上述芳胺基硅烷化合物的制备方法,如反应式1:
该制备方法包括以下步骤:
式ii所示的芳胺与烷基锂在保护气氛围、-80℃~30℃条件下于有机溶剂中进行反应;反应体系不经分离,向其中加入r7r8r9sicl在-80℃~30℃反应,反应结束后得到所述芳胺基硅烷化合物;
式ii所示的芳胺与强碱如丁基锂反应,生成胺基锂盐化合物,不经分离直接与r7r8r9sicl反应,能得到式i所示芳胺基硅烷化合物。
本发明第二方面提供的芳胺基硅烷化合物的制备方法中,优选地,所述芳胺与烷基锂的摩尔比为1:(1~3)。
本发明第二方面提供的芳胺基硅烷化合物的制备方法中,优选地,所述芳胺与r7r8r9sicl的摩尔比1:(1~3)。
本发明第二方面提供的芳胺基硅烷化合物的制备方法中,优选地,芳胺与烷基锂反应1-48小时;加入r7r8r9sicl之后反应1-48小时。
本发明第二方面提供的芳胺基硅烷化合物的制备方法中,优选地,所述芳胺为n-甲基苯胺、n-乙基苯胺、n-丙级苯胺、n-甲基-2,6-二异丙基苯胺、n-甲基-2,6-二甲基苯胺、n-甲基-2,4,6-三甲基苯胺、n-甲基-2,4,6-三异丙基苯胺、n-乙基-2,6-二异丙基苯胺、n-乙基-2,6-二甲基苯胺、n-乙基-2,4,6-三甲基苯胺、n-乙基-2,4,6-三异丙基苯胺、2,6-二异丙基-n-三甲基硅基苯胺、2,6-二甲基-n-三甲基硅基苯胺、2,4,6-三甲基-n-三甲基硅基苯胺或2,4,6-三异丙基-n-三甲基硅基苯胺。
本发明第二方面提供的芳胺基硅烷化合物的制备方法中,优选地,所述r7r8r9sicl为(ch3o)3sicl、(c2h5o)3sicl、ch3(ch3o)2sicl、ch3(c2h5o)2sicl、(c3h7o)3sicl、(c4h9o)3sicl、(ch3o)(c2h5o)2sicl、(c2h5o)3sicl、(ch3o)(c3h7o)2sicl、(ch3o)(c2h5o)(c3h7o)sicl、ch3(c3h7o)2sicl、ch3(c4h9o)2sicl、c2h5(ch3o)2sicl、c2h5(c2h5o)2sicl、c2h5(c3h7o)2sicl或c2h5(c4h9o)2sicl。
本发明第二方面提供的芳胺基硅烷化合物的制备方法中,优选地,所述烷基锂为丁基锂。更有选为正丁基锂。
本发明第二方面提供的芳胺基硅烷化合物的制备方法中,优选地,所述保护气为氮气、氦气或氩气。
本发明第二方面提供的芳胺基硅烷化合物的制备方法中,并不特别限定有机溶剂,优选地,所述有机溶剂为甲苯、苯、乙醚、四氢呋喃、戊烷、己烷、庚烷和辛烷中的一种或几种的混合溶剂。更优选地,所述有机溶剂为四氢呋喃或甲苯。
本发明第三个方面还提供了上述芳胺基硅烷化合物的另一种制备方法,如反应式2和反应式3:
该制备方法包括以下步骤:
式ii所示的芳胺与烷基锂在保护气氛围、-80℃~30℃条件下于有机溶剂中进行反应;反应体系不经分离,向其中加入(r7)msicl4-m继续反应,反应结束后得到式iii所示中间体;其中,r7为甲基,m为0或1;
将式iii所示的中间体溶于有机溶剂中,并向其中加入roh,在0℃~60℃条件下反应,得到式iv所示化合物;
其中,r为c1-c8的烷基。
本发明第三方面提供的芳胺基硅烷化合物的制备方法中,优选地,芳胺与烷基锂反应1-48小时,优选2小时;加入(r7)msicl4-m继续反应24小时;式iii中间体与roh反应4-60小时。
本发明第三方面提供的芳胺基硅烷化合物的制备方法中,所述芳胺与烷基锂的摩尔比为1:(1~3)。
本发明第三方面提供的芳胺基硅烷化合物的制备方法中,所述芳胺与(r7)msicl4-m的摩尔比1:(1~3)。
本发明第三方面提供的芳胺基硅烷化合物的制备方法中,所述式iii中间体与roh的摩尔比为1:(1~100)。
本发明第三方面提供的芳胺基硅烷化合物的制备方法中,所述m为1,所述r为甲基或乙基。
本发明第三方面提供的芳胺基硅烷化合物的制备方法中,优选地,所述烷基锂为丁基锂。更有选为正丁基锂。
本发明第三方面提供的芳胺基硅烷化合物的制备方法中,优选地,所述保护气为氮气、氦气或氩气。
本发明第三方面提供的芳胺基硅烷化合物的制备方法中,并不特别限定有机溶剂,优选地,所述有机溶剂为甲苯、苯、乙醚、四氢呋喃、戊烷、己烷、庚烷和辛烷中的一种或几种的混合溶剂。更优选地,所述有机溶剂为四氢呋喃或甲苯。
以上制备方法中的式ii芳胺可以通过反应式4进行合成:
该反应温度可在-80℃~30℃范围内进行。两步反应时间在1~48小时均可。第一步优选反应温度为0℃-10℃,反应时间优选为2-4小时;第二步的优选反应温度为25℃-30℃,反应时间为24-30小时。第一步生成的锂盐可以通过浓缩结晶的办法分离提纯。由于这类锂盐对空气极为敏感,在本发明中不分离,直接与r1x反应。r1x中的r1如式i中定义,x为氯或溴。
以上反应式1-反应式4所涉及的反应均为无水无氧反应,用schlenk技术在真空线或手套箱里进行。所用溶剂均经无水无氧处理。整个实验过程中所用的四氢呋喃、正己烷、甲苯等溶剂都要经过常规的脱气脱水处理;在反应实例中不再特别说明。
本发明第四个方面提供一种丙烯聚合催化剂,该丙烯聚合催化剂包括固体钛催化剂成分、烷基铝化合物成分以及以上芳胺基硅烷化合物成分。
该丙烯聚合催化剂,优选地,所述丙烯聚合催化剂中各成分之间的比例,以钛:铝:硅之间的摩尔比计为1:(5~1000):(1~500)。更优选为1:(50~150):(5~50)。
本发明的丙烯聚合催化剂中,优选地,所述烷基铝化合物的通式为alrnx(3-n),式中r为氢或者c1~c20的烷基、芳烷基或芳基;x为卤素;n为1~3的整数。更优选地,所述烷基铝化合物为三甲基铝、三乙基铝、三异丁基铝、三辛基铝、一氢二乙基铝、一氢二异丁基铝、一氯二乙基铝、一氯二异丁基铝或二氯乙基铝。
本发明的丙烯聚合催化剂中,优选地,所述固体钛催化剂为以钛、镁、卤素作为主要成分的固体钛催化剂。
本发明的丙烯聚合催化剂中,优选地,以钛、镁、卤素作为主要成分的固体钛催化剂是指卤化镁和承载于其上的至少带一个ti-卤化物键的钛化合物以及内给电子体化合物。
本发明的丙烯聚合催化剂中,优选地,内给电子体化合物为多元羧酸酯、酸酐、酮、醚或磺酰基化合物。
本发明的丙烯聚合催化剂中,优选地,以钛、镁、卤素作为主要成分的固体钛催化剂可以通过以下两种方法制备得到:
方法一:将醇类和卤化镁及烃类溶剂在羧酸酐类化合物的存在下,得到卤化镁醇合物,再将醇合物均匀溶液与液态钛化合物在低温下接触,然后升高温度,基于卤化镁在钛化合物中从低温到高温的析出存在重结晶过程,在升温过程中加入一定量的内给电子体化合物反应,继续升温,当达到反应温度时,再加入一定量的内给电子体化合物继续反应,经过滤、洗涤、干燥,制得固体钛催化剂。
方法二:将通式为mgcl2·nroh的球形氯化镁醇合物颗粒低温下加入到四氯化钛溶液中,反应一段时间;逐渐升温至40℃~100℃,加入一种或两种内给电子体,继续反应一段时间;过滤,加入一定量的四氯化钛,反应一段时间,可重复加入四氯化钛和过滤步骤1~3次;最后用惰性烃类溶剂洗涤,干燥,得到球形固体催化剂。
本发明第五个方面提供以上芳胺基硅烷化合物或丙烯聚合催化剂在丙烯聚合反应中的应用。
本发明的丙烯聚合以及共聚合按照本领域公知的方法进行,在液相本体或本体于惰性溶剂中的溶液,或在气相中,或通过在气液相中的组合聚合工艺进行操作。聚合温度一般为0℃~150℃,优选50℃~100℃。聚合反应压力是常压或更高。
利用本发明的芳胺基硅烷类化合物作丙烯催化聚合的外给电子体,具有较好的氢调敏感性。
附图说明
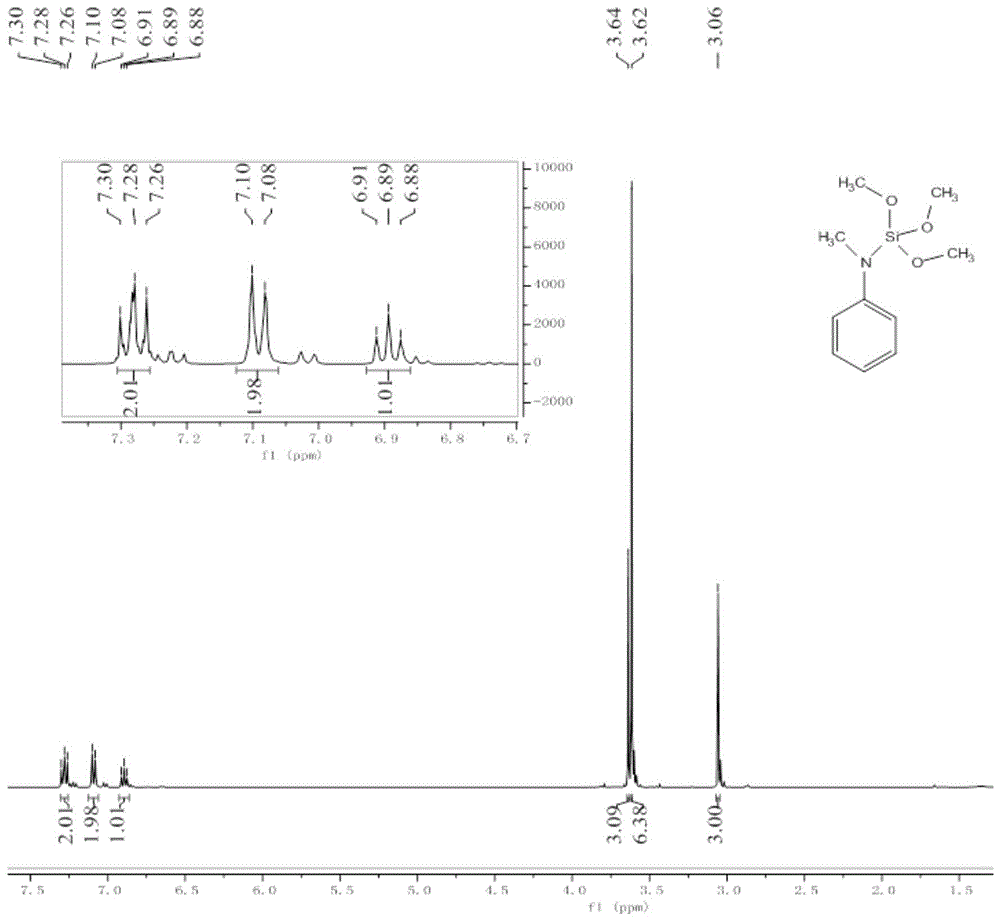
图1为本发明实施例1中的(n-甲基苯胺基)三甲氧基硅烷的1hnmr谱图。
图2为本发明实施例1中的(n-甲基苯胺基)三甲氧基硅烷的13cnmr谱图。
图3为本发明实施例2中的(n-甲基苯胺基)甲基二甲氧基硅烷的1hnmr谱图。
图4为本发明实施例2中的(n-甲基苯胺基)甲基二甲氧基硅烷的13cnmr谱图。
图5为本发明实施例3中的(n-甲基苯胺基)三乙氧基硅烷的1hnmr谱图。
图6为本发明实施例3中的(n-甲基苯胺基)三乙氧基硅烷的13cnmr谱图。
图7为本发明实施例4中的(n-甲基苯胺基)甲基二乙氧基硅烷的1hnmr谱图。
图8为本发明实施例4中的(n-甲基苯胺基)甲基二乙氧基硅烷的13cnmr谱图。
图9为本发明实施例5中的(2,6-二异丙基-n-三甲基硅基苯胺基)三甲氧基硅烷的1hnmr谱图。
图10为本发明实施例5中的(2,6-二异丙基-n-三甲基硅基苯胺基)三甲氧基硅烷的13cnmr谱图。
图11为本发明实施例6中的(2,6-二异丙基-n-三甲基硅基苯胺基)甲基二甲氧基硅烷的1hnmr谱图。
图12为本发明实施例6中的(2,6-二异丙基-n-三甲基硅基苯胺基)甲基二甲氧基硅烷的13cnmr谱图。
图13为本发明实施例7中的(2,6-二异丙基-n-三甲基硅基苯胺基)三乙氧基硅烷的1hnmr谱图。
图14为本发明实施例7中的(2,6-二异丙基-n-三甲基硅基苯胺基)三乙氧基硅烷的13cnmr谱图。
图15为本发明实施例8中的(2,6-二异丙基-n-三甲基硅基苯胺基)甲基二乙氧基硅烷的1hnmr谱图。
图16为本发明实施例8中的(2,6-二异丙基-n-三甲基硅基苯胺基)甲基二乙氧基硅烷的13cnmr谱图。
具体实施方式
为了更清楚地说明本发明,下面结合优选实施例对本发明做进一步的说明。本领域技术人员应当理解,下面所具体描述的内容是说明性的而非限制性的,不应以此限制本发明的保护范围。
测试方法:
1、采用核磁共振方法,测定所合成的外给电子体化合物的结构。
2、采取沸腾正庚烷抽提的方法,测定聚合产物的等规度。按照国标gb/t2412-2008进行。
3、根据国标gb/t3682-2000,测定聚合产物的熔融指数。
实施例1
(1)(n-甲基苯胺基)三甲氧基硅烷的合成
取200mlschlenk瓶,加入n-甲基苯胺8g和thf80ml,降温至0℃,缓慢滴加正丁基锂(1.6m正己烷溶液)60ml,反应2h后,滴加三甲氧基氯硅烷15g,自然升至室温反应24小时,真空除去溶剂,加入100ml正己烷过滤,然后真空除去正己烷,减压蒸馏,收集140-141℃馏分,得到黄色液体8.2g,产率42%。
1hnmr(400mhz,cdcl3,25℃,tms):δ(ppm)7.28(t,2h,3jh-h=8.0hz,ar-h),7.10(d,2h,3jh-h=8.0hz,ar-h),6.90(t,1h,3jh-h=8.0hz,ar-h),3.64(s,3h,n(och3),3.62(s,6h,n(och3),3.06(s,3h,nch3).
13cnmr(400mhz,cdcl3,25℃,tms):δ(ppm)148.50,128.90,119.43,51.30,50.92,34.06.核磁谱图见图1和图2。
(2)含钛的固体催化剂的制备
将球形mgcl2·2.85c2h5oh载体5.0g加入到装有150mltic14并事先预冷至25℃的带有搅拌的玻璃反应瓶中,逐步升温至80℃,加入2mmol内给电子体邻苯二甲酸二异丁酯,保持该温度30分钟,升温至130℃反应2小时。过滤,加入120mltic14,于130℃反应2小时,过滤;重复上述加tic14和过滤步骤1次;用正己烷洗涤6次,最后真空干燥固体物,即得到本发明的球形固体催化剂组分3.2g。
(3)丙烯聚合实验
容积为2l的不锈钢反应釜,经气体丙烯充分置换后,依次加入浓度为2.4mol/l的三乙基铝溶液5ml,所合成的外给电子体化合物n-甲基苯胺基三甲氧基硅烷0.9mmol,上述制备的含钛固体催化剂组分30mg,通入液体丙烯500g,升温至70℃,维持此温度反应0.5小时,降温,卸压,出料得聚丙烯产物。催化剂聚合实验结果如表1所示。
实施例2
(1)(n-甲基苯胺基)甲基二甲氧基硅烷的合成:
取200mlschlenk瓶,加入n-甲基苯胺10g和thf80ml,降温至0℃,缓慢滴加正丁基锂(1.6m正己烷溶液)60ml,反应2小时,然后滴加甲基二甲氧基氯硅烷16g,自然升至室温25℃反应24小时。真空除去溶剂,加入100ml正己烷过滤,然后真空除去正己烷,减压蒸馏,得到黄色液体8.8g,产率49%。
1hnmr(400mhz,cdcl3,25℃,tms):δ(ppm)7.28(t,2h,3jh-h=8.0hz,ar-h),7.10(d,2h,3jh-h=8.0hz,ar-h),6.90(t,1h,3jh-h=8.0hz,ar-h),3.64(s,3h,n(och3),3.62(s,6h,n(och3),3.06(s,3h,nch3).
13cnmr(400mhz,cdcl3,25℃,tms):δ(ppm)148.50,128.90,119.43,51.30,50.92,34.06.核磁谱图见图3和图4。
(2)含钛的固体催化剂的制备:同实施例1。
(3)丙烯聚合实验
容积为2l的不锈钢反应釜,经气体丙烯充分置换后,依次加入浓度为2.4mol/l的三乙基铝溶液5ml,所合成的外给电子体化合物n-(甲基苯胺基)甲基二甲氧基硅烷0.9mmol,上述制备的含钛固体催化剂组分30mg,通入液体丙烯500g,升温至70℃,维持此温度反应0.5小时,降温,卸压,出料得聚丙烯产物。催化剂聚合实验结果如表1所示。
实施例3
(1)(n-甲基苯胺基)三乙氧基硅烷的合成:
取200mlschlenk瓶,加入n-甲基苯胺6.5g和thf50ml,降温至0℃,缓慢滴加正丁基锂(1.6m正己烷溶液)50ml,反应2小时,然后滴加三乙氧基氯硅烷18g,自然升至室温25℃反应24小时。真空除去溶剂,加入100ml正己烷过滤,然后真空除去正己烷,减压蒸馏,得到橘黄色液体8.5g,产率51%。
1hnmr(400mhz,cdcl3,25℃,tms):δ(ppm)7.22(t,2h,3jh-h=6.8hz,ar-h),7.07(d,2h,3jh-h=8.8hz,ar-h),6.83(t,1h,3jh-h=8.0hz,ar-h),3.83(q,6h,3jh-h=7.2hz,och2ch3),3.02(s,3h,nch3),1.22(t,9h,3jh-h=6.8hz,och2ch3).
13cnmr(400mhz,cdcl3,25℃,tms):δ(ppm)148.76,128.70,119.05,116.84,58.91,34.13,18.02.核磁谱图见图5和图6。
(2)含钛的固体催化剂的制备:同实施例1。
(3)丙烯聚合实验
容积为2l的不锈钢反应釜,经气体丙烯充分置换后,依次加入浓度为2.4mol/l的三乙基铝溶液5ml,所合成的外给电子体化合物n-(甲基苯胺基)三乙氧基硅烷0.9mmol,上述制备的含钛固体催化剂组分30mg,通入液体丙烯500g,升温至70℃,维持此温度反应0.5小时,降温,卸压,出料得聚丙烯产物。催化剂聚合实验结果如表1所示。
实施例4
(1)(n-甲基苯胺基)甲基二乙氧基硅烷的合成:
取100mlschlenk瓶,加入n-甲基苯胺5.7g和thf40ml,降温至0℃,缓慢滴加正丁基锂(2.5m正己烷溶液)33.5ml,反应2小时,然后滴加甲基二乙氧基氯硅烷14g,自然升至室温反应过夜。真空除去溶剂,加入100ml正己烷过滤,然后真空除去正己烷,减压蒸馏,得到黄色液体7.4g,产率58%。
1hnmr(400mhz,cdcl3,25℃,tms):δ(ppm)7.26(t,2h,3jh-h=8.0hz,ar-h),7.09(d,2h,3jh-h=8.0hz,ar-h),6.86(t,1h,3jh-h=8.0hz,ar-h),3.84(m,4h,n(och2ch3)),3.02(s,3h,nch3),1.26(t,6h,3jh-h=8.0hz,n(och2ch3)),0.32(s,3h,sich3).
13cnmr(400mhz,cdcl3,25℃,tms):δ(ppm)149.25,128.75,118.90,117.05,58.23,33.70,18.13,-5.23.核磁谱图见图7和图8。
(2)含钛的固体催化剂的制备:同实施例1。
(3)丙烯聚合实验
容积为2l的不锈钢反应釜,经气体丙烯充分置换后,依次加入浓度为2.4mol/l的三乙基铝溶液5ml,所合成的外给电子体化合物n-(甲基苯胺基)甲基二乙氧基硅烷0.9mmol,上述制备的含钛固体催化剂组分30mg,通入液体丙烯500g,升温至70℃,维持此温度反应0.5小时,降温,卸压,出料得聚丙烯产物。催化剂聚合实验结果如表1所示。
实施例5
(1)(2,6-二异丙基-n-三甲基硅基苯胺基)三甲氧基硅烷的合成
取1000mlschlek瓶,经氮气置换后,在氮气保护下加入2,6-二异丙基苯胺75g和thf300ml,降温至0℃,然后缓慢滴加正丁基锂(1.6m正己烷溶液)350ml。待没有气泡产生后滴加三甲基氯硅烷50g在1小时滴加完,滴加完后在室温下反应2小时,然后过滤,真空下除去溶剂,剩余的油状液体减压蒸馏,得到淡黄色油状的2,6-二异丙基-n-三甲基硅基苯胺86.7g,产率85%。
取500mlschlenk瓶加入以上合成的2,6-二异丙基-n-三甲基硅基苯胺40g和thf150ml,在0℃下缓慢滴加n-buli(1.6m正己烷溶液)130ml,滴加完成后待不再产生气泡再反应2小时,然后滴加四氯化硅35g,自然升至室温搅拌反应过夜,真空除去溶剂,然后加入正己烷150ml后过滤,真空浓缩至冷冻结晶,得到白色固体状(2,6-二异丙基-n-三甲基硅基苯胺基)三氯硅烷48.6g,产率79%。
取500mlschlenk瓶加入上面合成的(2,6-二异丙基-n-三甲基硅基苯胺基)三氯硅烷10g和200ml甲苯,然后滴加无水甲醇15g和三乙胺30g的甲苯溶液,反应12h,真空下除去溶剂,加正己烷过滤,真空浓缩至刚好有固体产生,放置到冰箱结晶,得到白色固体状(2,6-二异丙基-n-三甲基硅基苯胺基)三甲氧基硅烷7.0g,产率73%,熔点:132-135℃。1hnmr(400mhz,cdcl3,25℃,tms):δ(ppm)7.10(d,1h,3jh-h=5.2hz,ar-h),7.07(t,2h,3jh-h=6.0hz,ar-h),3.57(m,2h,3jh-h=7.2hz,ch(ch3)2),3.46(s,9h,och3),1.22(q,12h,3jh-h=4.8hz,ch(ch3)2),0.11(s,9h,si(ch3)3).
13cnmr(400mhz,cdcl3,25℃,tms):δ(ppm)137.35,123.49,122.30,49.83,26.32,23.46,0.01.核磁谱图见图9和图10。
(2)含钛的固体催化剂的制备:同实施例1。
(3)丙烯聚合实验
容积为2l的不锈钢反应釜,经气体丙烯充分置换后,依次加入浓度为2.4mol/l的三乙基铝溶液5ml,所合成的外给电子体化合物2,6-二异丙基苯胺基(n-三甲基硅基)三甲氧基硅烷0.9mmol,上述制备的含钛固体催化剂组分30mg,通入液体丙烯500g,升温至70℃,维持此温度反应0.5小时,降温,卸压,出料得聚丙烯产物。催化剂聚合实验结果如表1所示。
实施例6
(1)(2,6-二异丙基-n-三甲基硅基苯胺基)甲基二甲氧基硅烷的合成
取500mlschlenk瓶加入实施例5合成的中间体2,6-二异丙基-n-三甲基硅基苯胺38g和thf150ml,在0℃下缓慢滴加n-buli(1.6m正己烷溶液)150ml,滴加完成后待不再产生气泡再反应2小时,降温至-78℃滴加甲基三氯硅烷26g,自然升至室温搅拌反应过夜,真空除去溶剂,然后加入正己烷150ml后过滤,真空浓缩至刚好有固体产生,放置到冰箱重结晶,得到白色固体状2,6-二异丙基-n-三甲基硅基苯胺基)甲基二氯硅烷40g,产率70%。
1hnmr(400mhz,cdcl3,25℃,tms):δ(ppm)7.188(t,1h,3jh-h=6.0hz,ar-h),7.188(d,2h,3jh-h=6.8hz,ar-h),3.465(m,2h,3jh-h=6.8hz,ch(ch3)2),1.24(m,12h,3jh-h=6.8hz,ch(ch3)2),0.550(s,3h,sicl2ch3),0.242(s,9h,si(ch3)3).
13cnmr(400mhz,cdcl3,25℃,tms):δ(ppm)145.238,137.336,124.077,122.353,25.969,23.291,22.937,4.653.
取500mlschlenk瓶加入(2,6-二异丙基-n-三甲基硅基苯胺基)甲基二氯硅烷10.8g和200ml甲苯,然后滴加无水甲醇35g和三乙胺13.8g的甲苯溶液,反应24小时,真空下除去溶剂,加正己烷150ml过滤,真空浓缩至刚好有固体产生,放置到冰箱结晶,得到白色固体7g,产率65%,熔点96-98℃。
1hnmr(400mhz,cdcl3,25℃,tms):δ(ppm)7.188(t,1h,3jh-h=6.0hz,ar-h),7.188(d,2h,3jh-h=6.8hz,ar-h),3.465(m,2h,3jh-h=6.8hz,ch(ch3)2),1.24(m,12h,3jh-h=6.8hz,ch(ch3)2),0.550(s,3h,sicl2ch3),0.242(s,9h,si(ch3)3).
13cnmr(400mhz,cdcl3,25℃,tms):δ(ppm)145.238,137.336,124.077,122.353,25.969,23.291,22.937,4.653.核磁谱图见图11和图12。
(2)含钛的固体催化剂的制备:同实施例1。
(3)丙烯聚合实验
容积为2l的不锈钢反应釜,经气体丙烯充分置换后,依次加入浓度为2.4mol/l的三乙基铝溶液5ml,所合成的外给电子体化合物2,6-二异丙基苯胺基(n-三甲基硅基)甲基二甲氧基硅烷0.9mmol,上述制备的含钛固体催化剂组分30mg,通入液体丙烯500g,升温至70℃,维持此温度反应0.5小时,降温,卸压,出料得聚丙烯产物。催化剂聚合实验结果如表1所示。
实施例7
(1)(2,6-二异丙基-n-三甲基硅基苯胺基)三乙氧基硅烷的合成:取200mlschlenk瓶,加入实施例5合成的中间体2,6-二异丙基-n-三甲基硅基苯胺12.5g和thf100ml,降温至0℃,缓慢滴加正丁基锂(1.6m正己烷溶液)50ml,自然升至室温反应2小时,然后滴加三乙氧基氯硅烷8.7g,反应24小时。真空除去溶剂,加入100ml正己烷后过滤,滤液真空除去溶剂,然后用柱色谱进行分离得到橘黄色固体9.5g,产率57%,熔点150-152℃。
1hnmr(400mhz,cdcl3,25℃,tms):δ(ppm)6.97(t,1h,3jh-h=5.2hz,ar-h),6.94(t,2h,3jh-h=5.6hz,ar-h),3.63(q,2h,3jh-h=7.2hz,och2ch3),3.58(t,4h,3jh-h=7.2hz,och2ch3),3.49(m,2h,3jh-h=7.2hz,ch(ch3)2),1.10(q,12h,3jh-h=6.8hz,ch(ch3)2),1.02(t,6h,3jh-h=6.8hz,och2ch3),1.01(t,3h,3jh-h=6.8hz,och2ch3),0.00(s,9h,si(ch3)3).
13cnmr(400mhz,cdcl3,25℃,tms):δ(ppm)144.99,137.36,121.85,120.83,56.25,24.91,22.26,15.51,-1.19.核磁谱图见图13和图14。
(2)含钛的固体催化剂的制备:同实施例1。
(3)丙烯聚合实验
容积为2l的不锈钢反应釜,经气体丙烯充分置换后,依次加入浓度为2.4mol/l的三乙基铝溶液5ml,所合成的外给电子体化合物2,6-二异丙基苯胺基(n-三甲基硅基)三乙氧基硅烷0.9mmol,上述制备的含钛固体催化剂组分30mg,通入液体丙烯500g,升温至70℃,维持此温度反应0.5小时,降温,卸压,出料得聚丙烯产物。催化剂聚合实验结果如表1所示。
实施例8
(1)(2,6-二异丙基-n-三甲基硅基苯胺基)甲基二乙氧基硅烷的合成:取200mlschlenk瓶加入实施例6合成的化合物2,6-二异丙基(n-三甲基硅基)苯胺基甲基二氯硅烷10.8g和15.5g无水乙醇,然后滴加三乙胺15g,反应7小时,真空下除去溶剂,加正己烷150ml过滤,真空除去溶剂得到橘黄色液体7g,产率41%。
1hnmr(400mhz,cdcl3,25℃,tms):δ(ppm)7.09(d,2h,3jh-h=5.2hz,ar-h),7.07(t,1h,3jh-h=5.2hz,ar-h),3.74(q,4h,3jh-h=6.8hz,si(och2ch3)),3.62(m,2h,3jh-h=6.8hz,ch(ch3)2),1.21(d,12h,3jh-h=6.8hz,ch(ch3)2),1.19(t,6h,3jh-h=6.8hz,si(och2ch3)),0.13(s,9h,si(ch3)3),0.01(s,3h,sich3).
13cnmr(400mhz,cdcl3,25℃,tms):δ(ppm)145.65,138.81,122.68,121.77,56.47,25.58,23.26,23.14,16.50,-6.81.核磁谱图见图15和图16。
(2)含钛的固体催化剂的制备:同实施例1。
(3)丙烯聚合实验
容积为2l的不锈钢反应釜,经气体丙烯充分置换后,依次加入浓度为2.4mol/l的三乙基铝溶液5ml,所合成的外给电子体化合物2,6-二异丙基苯胺基(n-三甲基硅基)甲基二乙氧基硅烷0.9mmol,上述制备的含钛固体催化剂组分30mg,通入液体丙烯500g,升温至70℃,维持此温度反应0.5小时,降温,卸压,出料得聚丙烯产物。催化剂聚合实验结果如表1所示。
对比例1:
采用与实施例1-8相同的含钛固体催化剂组分和丙烯聚合方法,只是将外给电子体化合物改为环己基甲基二甲氧基硅烷。
由表1催化剂聚合实验结果可以看出,使用本发明的含芳胺基硅氧烷化合物作为外给电子体,所得聚合产物的等规度与对比实施例1所使用的已知的典型的有机硅氧烷外给电子体基本相同。但是,使用本发明的含芳胺基硅氧烷化合物作为外给电子体时,丙烯聚合反应所得的聚丙烯的熔融指数明显高于对比实施例1所使用的已知的典型的有机硅氧烷外给电子体作为外给电子体时丙烯聚合反应所得的聚丙烯的熔融指数。
从而,说明了芳胺基硅氧烷化合物作为外给电子体的丙烯聚合反应催化剂具有很好的氢调敏感性;而且聚丙烯的等规度也比较高,可用来制备具有高流动、高等规度的聚丙烯材料。
表1催化剂聚合实验结果
显然,本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定,对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动,这里无法对所有的实施方式予以穷举,凡是属于本发明的技术方案所引伸出的显而易见的变化或变动仍处于本发明的保护范围之列。
- 还没有人留言评论。精彩留言会获得点赞!