光敏感通道ChR2蛋白的突变体及其应用的制作方法
本发明涉及生物技术领域,具体地涉及光敏感通道chr2蛋白的突变体及其应用。
背景技术:
脊椎动物眼睛的视网膜充当与相机中的胶片相同的功能,接收由贯穿通过眼睛的晶状体和角膜的光产生的视觉图像。接收的图像被转化成经由视神经被传送到脑的化学信号和电信号。
视网膜是个复杂的结构,包含不同细胞类型的十个清楚的层。这些层中,光感受器层负责将进入的光转化成可被脑阅读并且解释成图像的化学信号和/或电信号。光感受器层包含被称为视杆细胞和视锥细胞的两种类型的光敏细胞。这些细胞类型二者都负责与进入的光反应并且产生电信号,但它们在视网膜内的定位以及与它们反应的光的类型是不同的。具体地,视杆细胞主要在弱光中发挥功能,并且主要在周边视网膜中发现。视锥细胞对强光(即白天视觉)更有反应,负责颜色视觉,并且被发现在中央视网膜中呈最高密度。视网膜还含有第三类较少数目的光感受器细胞光敏神经节细胞,其负责测量背景光,但不负责图像处理。
光感受器丧失或变性若不完全抑制也是严重危及视网膜内视觉信息的光转导。光感受器细胞的丧失和/或光感受器细胞功能的丧失是降低的视觉敏锐度,降低的光敏感性,和盲的主要原因。
chr2最早从莱茵衣藻中发现,后经人为突变、修饰,改造成能适用于哺乳动物细胞、表达稳定对细胞无毒的工具。该蛋白在蓝光(最大激发峰在470nm波长附近)的激发下会诱导阳离子通道的打开,促使神经元的去极化,进而诱发动作电位,激活神经元。天然chr2蛋白是一个光控阳离子通道,含737个氨基酸。细胞內源视黄醛足以辅助截短至309氨基酸的chr2蛋白实现其功能,不需要添加外源色基。
因此,本领域亟需开发一种感光能力强的光敏感通道chr2蛋白及其表达体系和制备方法。
技术实现要素:
本发明的目的是提供一种感光能力强的光敏感通道chr2蛋白及其表达体系和制备方法。
本发明的第一方面,提供了一种突变的光敏感通道chr2蛋白,所述突变的光敏感通道chr2蛋白对应于野生型光敏感通道chr2蛋白的氨基酸序列中第159位苏氨酸(t)发生突变。
在另一优选例中,所述野生型光敏感通道chr2蛋白的氨基酸序列来源于莱茵衣藻。
在另一优选例中,所述野生型的光敏感通道chr2蛋白的氨基酸序列如seqidno.:1所示。
在另一优选例中,所述突变的光敏感通道chr2蛋白还包括对应于野生型光敏感通道chr2蛋白的氨基酸序列中第132位亮氨酸(l)发生突变。
在另一优选例中,所述第159位苏氨酸(t)突变为丝氨酸(s)。
在另一优选例中,所述第132位亮氨酸(l)突变为半胱氨酸(c)。
在另一优选例中,所述突变的光敏感通道chr2蛋白中的突变包括l132c和t159s。
在另一优选例中,所述突变的的光敏感通道chr2蛋白选自下组:
(1)氨基酸序列如seqidno.:2所示的多肽;或
(2)将seqidno.:2所示氨基酸序列经过一个或几个,优选1-20个、更优选1-15个、更优选1-10个、更优选1-8个、更优选1-3个、最优选1个氨基酸残基的取代、缺失或添加而形成的,具有(1)所述多肽功能的由seqidno.:2所示氨基酸序列的多肽衍生的多肽。
在另一优选例中,所述突变的的光敏感通道chr2蛋白的氨基酸序列如seqidno.:2所示。
在另一优选例中,所述突变的的光敏感通道chr2蛋白的氨基酸序列与seqidno.:2所示的序列具有至少70%,优选至少75%、80%、85%、90%,更优选至少95%、96%、97%、98%、99%以上的序列相同性。
本发明的第二方面,提供了一种分离的多核苷酸,所述多核苷酸编码本发明第一方面所述的光敏感通道chr2蛋白。
在另一优选例中,所述多核苷酸选自下组:
(a)编码如seqidno.:2所示多肽的多核苷酸;
(b)序列如seqidno.:3所示的多核苷酸;
(c)序列如seqidno.:4所示的多核苷酸;
(d)核苷酸序列与seqidno.:3或seqidno.:4所示序列的同源性≥95%(较佳地≥98%,更佳地≥99%),且编码seqidno.:2所示多肽的多核苷酸;和/或
(e)与(a)-(c)任一所述的多核苷酸互补的多核苷酸。
在另一优选例中,所述核苷酸序列包括dna序列。
本发明的第三方面,提供了一种载体,所述载体含有如本发明第二方面所述的多核苷酸。
在另一优选例中,所述载体包含一个或多个启动子,所述启动子可操作地与所述核酸序列、增强子、转录终止信号、多腺苷酸化序列、复制起点、选择性标记、核酸限制性位点、和/或同源重组位点连接。
在另一优选例中,所述载体包括质粒、病毒载体。
在另一优选例中,所述的病毒载体选自下组:腺相关病毒(aav)、腺病毒、慢病毒、逆转录病毒、疱疹病毒、sv40、痘病毒、或其组合。
在另一优选例中,所述载体用于表达光敏感通道chr2蛋白。
本发明的第四方面,提供了一种腺相关病毒载体,所述腺相关病毒载体含有如本发明第二方面所述的多核苷酸。
在另一优选例中,所述腺相关病毒的血清型选自:aav2、aav5、aav7、aav8、或其组合。
本发明的第五方面,提供了一种宿主细胞,所述宿主细胞含有本发明第三方面所述的载体或本发明第四方面所述的腺相关病毒载体,或其染色体中整合有外源的本发明第二方面所述的多核苷酸。
在另一优选例中,所述宿主细胞为哺乳动物细胞,所述哺乳动物包括人和非人哺乳动物。
在另一优选例中,所述宿主细胞包括hek细胞、感光细胞(包括锥状细胞和/或杆状细胞)、其他视觉细胞(如双节细胞)、神经细胞、或其组合。
在另一优选例中,所述宿主细胞选自下组:视杆细胞、视锥细胞、给光双极细胞、撤光双极细胞、水平细胞、神经节细胞、无长突细胞、或其组合。
本发明的第六方面,提供了如本发明第三方面所述的载体或本发明第四方面所述的腺相关病毒载体的用途,用于制备一制剂或组合物,所述制剂或组合物用于扩大或恢复视网膜的光感受器功能、恢复受试者视力或感光能力、和/或治疗视网膜退化性疾病。
在另一优选例中,所述视网膜退化性疾病选自下组:视网膜营养不良(如视杆营养不良、视杆视锥营养不良、视锥视杆营养不良、视锥营养不良或黄斑营养不良)、视网膜或黄斑退化、由光感受器能力的丧失导致的其他疾病、或其组合。
在另一优选例中,所述制剂或组合物用于治疗眼部疾病。
在另一优选例中,所述制剂或组合物用于向细胞提供光感受器功能。
本发明的第七方面,提供了一种药物制剂,所述的制剂含有(a)本发明第三方面所述的载体或本发明第四方面所述的腺相关病毒载体,以及(b)药学上可接受的载体。
在另一优选例中,所述药物制剂的剂型选自下组:冻干制剂、液体制剂、或其组合。
在另一优选例中,所述药物制剂中载体的含量为1×109-1×1016个病毒/毫升,较佳地1×1012-1×1013个病毒/毫升。
在另一优选例中,所述药物制剂用于治疗眼部疾病。
在另一优选例中,所述眼部疾病由光感受器细胞退化引起。
在另一优选例中,所述药物制剂用于扩大或恢复视网膜的光感受器功能、恢复受试者视力、和/或治疗视网膜退化性疾病。
本发明的第八方面,提供了一种治疗方法,所述方法包括将本发明第四方面所述的腺相关病毒载体施用于需要的对象。
在另一优选例中,将所述腺相关病毒载体引入到需要的对象的眼睛内。
在另一优选例中,所述需要的对象包括人和非人哺乳动物。
在另一优选例中,所述治疗方法为治疗眼部疾病的方法。
在另一优选例中,所述眼部疾病由光感受器细胞退化引起。
在另一优选例中,所述治疗方法用于扩大或恢复视网膜的光感受器功能、恢复受试者视力、和/或治疗视网膜退化性疾病。
在另一优选例中,所述视网膜退化性疾病选自下组:视网膜营养不良(如视杆营养不良、视杆视锥营养不良、视锥视杆营养不良、视锥营养不良或黄斑营养不良)、视网膜或黄斑退化、由光感受器能力的丧失导致的其他疾病、或其组合。
本发明的第九方面,提供了一种光敏感通道chr2蛋白的制备方法,包括培养本发明第五方面所述的宿主细胞,从而得到光敏感通道chr2蛋白。
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
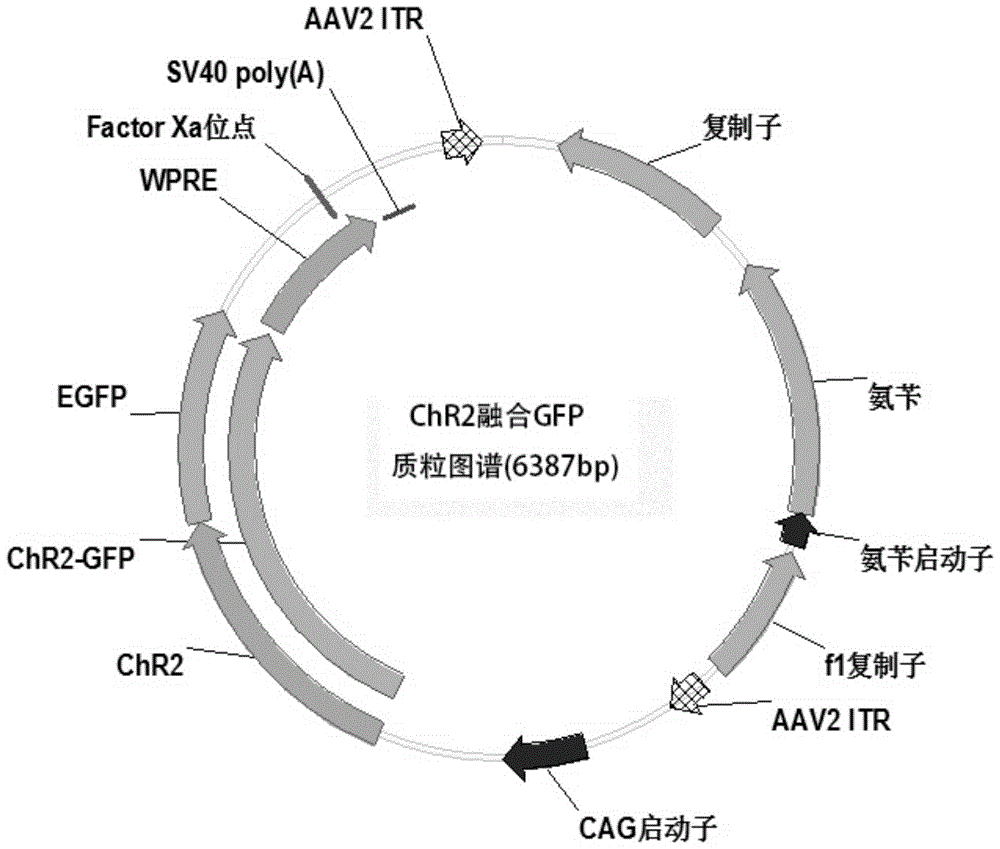
图1显示了raav2-1dna质粒的结构示意图,其中raav2-1dna质粒为携带有光敏感通道chr2蛋白的优化编码序列(seqidno.:6)的avv载体。
图2显示了优化后野生型和突变型瞬时转染hek293细胞以及粗提病毒感染hek293细胞情况。a、b(野生型)、c和d(突变型)分别为瞬时转染48小时后的荧光照片(a和c)和非荧光照片(b和d)(放大倍数100x)。e、f(野生型)、g和h(突变型)分别为病毒感染48小时后的荧光照片(e和g)和非荧光照片(f和h)(放大倍数100x)。i(野生型)和j(突变型)为病毒感染48小时后的照片(放大倍数200x)。
图3显示了优化后的野生型和突变型aav-chr2病毒感染hek293细胞后给光后全细胞膜片钳记录的电流反应。其中a、c为野生型chr2病毒感染,而b、d为突变型chr2病毒感染。a、c为同一感染细胞在不同光强度下(1.8x1014-7.2x1017photons/cm2s)电流反应,c、d为五个不同感染细胞在1.8x1014photons/cm2s光强度下的电流反应。
具体实施方式
本发明人经过广泛而深入的研究,意外地获得一种光敏感通道chr2蛋白的突变体。相比野生型chr2蛋白,本发明光敏感通道chr2蛋白的突变体具有更强的光电流,其感光能力至少提高了5倍以上。此外,本发明还对所述突变体的编码序列进行了针对性优化设计,构建了光敏感通道chr2蛋白的重组表达载体,将优化后的光敏感通道chr2蛋白编码序列(seqidno:4)转入宿主细胞,光敏感通道chr2蛋白表达量非常高、感光能力强,非常适合在哺乳动物(尤其是人)细胞内表达。在此基础上,发明人完成了本发明。
术语
为了可以更容易地理解本公开,首先定义某些术语。如本申请中所使用的,除非本文另有明确规定,否则以下术语中的每一个应具有下面给出的含义。在整个申请中阐述了其它定义。
术语“约”可以是指在本领域普通技术人员确定的特定值或组成的可接受误差范围内的值或组成,其将部分地取决于如何测量或测定值或组成。例如,如本文所用,表述“约100”包括99和101和之间的全部值(例如,99.1、99.2、99.3、99.4等)。
如本文所用,术语“含有”或“包括(包含)”可以是开放式、半封闭式和封闭式的。换言之,所述术语也包括“基本上由…构成”、或“由…构成”。
序列同一性(或同源性)通过沿着预定的比较窗(其可以是参考核苷酸序列或蛋白的长度的50%、60%、70%、80%、90%、95%或100%)比较两个对齐的序列,并且确定出现相同的残基的位置的数目来确定。通常地,这表示为百分比。核苷酸序列的序列同一性的测量是本领域技术人员熟知的方法。
如本文使用的,术语“受试者”、“需要的对象”指任何哺乳动物或非哺乳动物。哺乳动物包括但不限于人类、脊椎动物诸如啮齿类、非人类灵长类、牛、马、狗、猫、猪、绵羊、山羊、长颈鹿、鹿、骆驼、玲羊、野兔和家兔。
如本文所用,“光敏感通道”、“光敏感通道蛋白”、“chr2”、“光敏感通道chr2蛋白”、“通道视紫红质2”或“多肽”均可互换使用。
chr2
chr2最早从莱茵衣藻中发现,后经人为突变、修饰,改造成能适用于哺乳动物细胞、表达稳定对细胞无毒的工具。该蛋白在蓝光(最大激发峰在470nm波长附近)的激发下会诱导阳离子通道的打开,促使神经元的去极化,进而诱发动作电位,激活神经元。天然chr2蛋白是一个光控阳离子通道,含737个氨基酸。细胞內源视黄醛足以辅助截短至309氨基酸的chr2蛋白实现其功能,不需要添加外源色基。
通道视蛋白2(chop2)首次从绿藻莱茵衣藻(chlamydomonasreinhardtii)分离。通道视蛋白-2是一种七跨膜域蛋白质,其在与发色团全反式视黄醒结合时变为光可转换的(光敏感性)。chop2在经由schiff碱连接与视网膜分子连接时形成光门控的,非特异性,内部整流的阳离子通道,称作通道视紫红质-2(channelrhodopsin-2,缩写为chr2)。
通道视蛋白2在结合视黄醛后然后形成通道视紫红质2(chr2)。应当理解,在细胞(即视网膜神经元)中表达chop2后,内源可用的视黄醛结合chop2以形成功能性光门控通道chr2。因此,如本文中提及的chr2与chop2蛋白可以是同义的。
腺相关病毒
腺相关病毒(adeno-associatedvirus,aav),也称腺伴随病毒,属于微小病毒科依赖病毒属,是目前发现的一类结构最简单的单链dna缺陷型病毒,需要辅助病毒(通常为腺病毒)参与复制。它编码两个末端的反向重复序列(itr)中的cap和rep基因。itrs对于病毒的复制和包装具有决定性作用。cap基因编码病毒衣壳蛋白,rep基因参与病毒的复制和整合。aav能感染多种细胞。
重组腺相关病毒载体(raav)源于非致病的野生型腺相关病毒,由于其安全性好、宿主细胞范围广(分裂和非分裂细胞)、免疫源性低,在体内表达外源基因时间长等特点,被视为最有前途的基因转移载体之一,在世界范围内的基因治疗和疫苗研究中得到广泛应用。经过10余年的研究,重组腺相关病毒的生物学特性己被深入了解,尤其是其在各种细胞、组织和体内实验中的应用效果方面已经积累了许多资料。在医学研究中,raav被用于多种疾病的基因治疗的研究(包括体内、体外实验);同时作为一种有特点的基因转移载体,还广泛用于基因功能研究、构建疾病模型、制备基因敲除鼠等方面。
在本发明一个优选的实施例中,载体为重组aav载体。aav是相对较小的dna病毒,其可以稳定和位点特异性方式整合到它们所感染的细胞的基因组中。它们能够感染一大系列的细胞而不对细胞生长、形态或分化产生任何影响,并且它们似乎并不涉及人体病理学。aav基因组己被克隆、测序及表征。aav含有大约4700碱基并在每个末端包含约145个碱基的反向末端重复序列(itr)区域,其作为病毒的复制起点。该基因组的其余被分成两个带有衣壳化功能的重要区域:包含涉及病毒复制和病毒基因表达的rep基因的基因组左边部分;以及包含编码病毒衣壳蛋白的cap基因的基因组右边部分。
aav载体可采用本领域的标准方法制备。任何血清型的腺相关病毒均是合适的。用于纯化载体的方法可见于例如美国专利no.6566118、6989264和6995006,它们的公开内容整体以引用方式并入本文。杂合载体的制备在例如pct申请no.pct/us2005/027091中有所描述,该申请的公开内容整体以引用方式并入本文。用于体外和体内转运基因的衍生自aav的载体的使用己有描述(参见例如国际专利申请公布no.wo91/18088和wo93/09239;美国专利no.4,797,368、6,596,535和5,139,941,以及欧洲专利no.0488528,它们均整体以引用方式并入本文)。这些专利公布描述了其中rep和/或cap基因缺失并被所关注的基因替换的各种来源于aav的构建体,以及这些构建体在体外(进入培养的细胞中)或体内(直接进入生物体)转运所关注的基因的用途。复制缺陷重组aav可通过将以下质粒共转染进被人类辅助病毒(例如腺病毒)感染的细胞系而制备:所含的所关注核酸序列的侧翼为两个aav反向末端重复序列(itr)区域的质粒,和携带aav衣壳化基因(rep和cap基因)的质粒。然后通过标准技术纯化所产生的aav重组体。
在一些实施方案中,重组载体被衣壳化到病毒粒子(例如包括但不限于aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、aav12、aav13、aav14、aav15和aav16的aav病毒粒子)中。因此,本公开包括含有本文所述的任何载体的重组病毒粒子(因其包含重组多核苷酸而为重组的)。产生这样的粒子的方法是本领域己知的,并在美国专利no.6,596,535中有所描述。
野生型光敏感通道chr2蛋白
如本文所用,“野生型光敏感通道chr2蛋白”是指天然存在的、未经过人工改造的光敏感通道chr2蛋白,其核苷酸可以通过基因工程技术来获得,如基因组测序、聚合酶链式反应(pcr)等,其氨基酸序列可由核苷酸序列推导而得到。所述野生型光敏感通道chr2蛋白的来源为绿藻莱茵衣藻(chlamydomonasreinhardtii)。
在本发明的一个优选例中,所述野生型光敏感通道chr2蛋白的氨基酸序列如seqidno.:1所示。
mdyggalsavgrellfvtnpvvvngsvlvpedqcycagwiesrgtngaqtasnvlqwlaagfsilllmfyayqtwkstcgweeiyvcaiemvkvilefffefknpsmlylatghrvqwlryaewlltcpvilihlsnltglsndysrrtmgllvsdigtivwgatsamatgyvkviffclglcygantffhaakayiegyhtvpkgrcrqvvtgmawlffvswgmfpilfilgpegfgvlsvygstvghtiidlmskncwgllghylrvlihehilihgdirkttklniggteievetlvedeaeagav(seqidno.:1)
光敏感通道chr2蛋白的突变体
如本文所用,术语“突变蛋白”、“本发明突变蛋白”、“本发明chr2突变蛋白”、“本发明突变的光敏感通道chr2蛋白”、“光敏感通道chr2蛋白突变体”、“突变体chr2”、“突变的chr2蛋白”、“chr2的突变体”可互换使用,均指非天然存在的突变的光敏感通道chr2蛋白,且所述突变的光敏感通道chr2蛋白为基于seqidno.:1所示蛋白进行人工改造的蛋白。具体地,所述突变的光敏感通道chr2蛋白如本发明第一方面所述。
应理解,本发明突变的光敏感通道chr2蛋白中的氨基酸编号基于野生型光敏感通道chr2蛋白(优选地,seqidno.:1)作出。当某一具体突变蛋白与seqidno.:1所示序列的同源性达到80%或以上时,突变蛋白的氨基酸编号可能会有相对于seqidno.:1的氨基酸编号的错位,如向氨基酸的n末端或c末端错位1-5位,而采用本领域常规的序列比对技术,本领域技术人员通常可以理解这样的错位是在合理范围内的,且不应当由于氨基酸编号的错位而使同源性达80%(如90%、95%、98%)的、具有相同或相似chr2蛋白活性的突变蛋白不在本发明突变蛋白的范围内。
本发明突变蛋白是合成蛋白或重组蛋白,即可以是化学合成的产物,或使用重组技术从原核或真核宿主(例如,细菌、酵母、植物)中产生。根据重组生产方案所用的宿主,本发明的突变蛋白可以是糖基化的,或可以是非糖基化的。本发明的突变蛋白还可包括或不包括起始的甲硫氨酸残基。
本发明还包括所述突变蛋白的片段、衍生物和类似物。如本文所用,术语“片段”、“衍生物”和“类似物”是指基本上保持所述突变蛋白相同的生物学功能或活性的蛋白。
本发明的突变蛋白片段、衍生物或类似物可以是(i)有一个或多个保守或非保守性氨基酸残基(优选保守性氨基酸残基)被取代的突变蛋白,而这样的取代的氨基酸残基可以是也可以不是由遗传密码编码的,或(ii)在一个或多个氨基酸残基中具有取代基团的突变蛋白,或(iii)成熟突变蛋白与另一个化合物(比如延长突变蛋白半衰期的化合物,例如聚乙二醇)融合所形成的突变蛋白,或(iv)附加的氨基酸序列融合到此突变蛋白序列而形成的突变蛋白(如前导序列或分泌序列或用来纯化此突变蛋白的序列或蛋白原序列,或与抗原igg片段的形成的融合蛋白)。根据本文的教导,这些片段、衍生物和类似物属于本领域熟练技术人员公知的范围。本发明中,保守性替换的氨基酸最好根据表i进行氨基酸替换而产生。
表i
在本发明中,所述突变蛋白如本发明第一方面所述,优选地,所述的突变蛋白如seqidno.:2所示。
mdyggalsavgrellfvtnpvvvngsvlvpedqcycagwiesrgtngaqtasnvlqwlaagfsilllmfyayqtwkstcgweeiyvcaiemvkvilefffefknpsmlylatghrvqwlryaewlltcpvicihlsnltglsndysrrtmgllvsdigsivwgatsamatgyvkviffclglcygantffhaakayiegyhtvpkgrcrqvvtgmawlffvswgmfpilfilgpegfgvlsvygstvghtiidlmskncwgllghylrvlihehilihgdirkttklniggteievetlvedeaeagav(seqidno.:2)
应理解,本发明突变蛋白与seqidno.:2所示的序列相比,通常具有较高的同源性(相同性),优选地,所述的突变蛋白与seqidno.:2所示序列的同源性至少为80%,较佳地至少为85%-90%,更佳地至少为95%,最佳地至少为98%。
此外,还可以对本发明突变蛋白进行修饰。修饰(通常不改变一级结构)形式包括:体内或体外的突变蛋白的化学衍生形式如乙酰化或羧基化。修饰还包括糖基化,如那些在突变蛋白的合成和加工中或进一步加工步骤中进行糖基化修饰而产生的突变蛋白。这种修饰可以通过将突变蛋白暴露于进行糖基化的酶(如哺乳动物的糖基化酶或去糖基化酶)而完成。修饰形式还包括具有磷酸化氨基酸残基(如磷酸酪氨酸,磷酸丝氨酸,磷酸苏氨酸)的序列。还包括被修饰从而提高了其抗蛋白水解性能或优化了溶解性能的突变蛋白。
核酸编码序列
本发明还涉及编码本发明光敏感通道chr2蛋白突变体的多核苷酸。
在本发明的一个优选例中,所述多核苷酸选自下组:
(a)编码如seqidno.:2所示多肽的多核苷酸;
(b)序列如seqidno.:3所示的多核苷酸;
(c)序列如seqidno.:4所示的多核苷酸;
(d)核苷酸序列与seqidno.:3或seqidno.:4所示序列的同源性≥95%(较佳地≥98%,更佳地≥99%),且编码seqidno.:2所示多肽的多核苷酸;和/或
(e)与(a)-(c)任一所述的多核苷酸互补的多核苷酸。
本发明的多核苷酸可以是dna形式或rna形式。在另一优选例中,所述核苷酸为dna。dna形式包括cdna、基因组dna或人工合成的dna。dna可以是单链的或是双链的。dna可以是编码链或非编码链。编码成熟多肽的编码区序列可以与编码seqidno.:2所示的多肽的序列相同或者是简并的变异体。如本文所用,“简并的变异体”在本发明中是指编码具有seqidno.:2所示的多肽,但相应编码区序列有差别的核酸序列。
本发明还涉及上述多核苷酸的变异体,其编码与本发明有相同的氨基酸序列的多肽或突变蛋白的片段、类似物和衍生物。这些核苷酸变异体包括取代变异体、缺失变异体和插入变异体。如本领域所知的,等位变异体是一个多核苷酸的替换形式,它可能是一个或多个核苷酸的取代、缺失或插入,但不会从实质上改变其编码的突变蛋白的功能。本发明的突变蛋白和多核苷酸优选以分离的形式提供,更佳地,被纯化至均质。
核酸序列可以是dna、rna、cdna或pna。核酸序列可以是基因组的、重组的或合成的。核酸序列可以是分离的或纯化的。核酸序列可以是单链或双链的。优选地,核酸序列将编码如本文描述的光敏蛋白。核酸序列可以通过克隆衍生,例如使用包括限制性酶切、连接、凝胶电泳的标准的分子克隆技术,例如在sambrook等molecularcloning:alaboratorymanual,coldspringharbourlaboratorypress)中描述的。核酸序列可是分离的,例如使用pcr技术分离的。分离意指从任何杂质和从被自然地发现与其来源中的核酸序列缔合的其他核酸序列和/或蛋白中分离核酸序列。优选地,其还将不含细胞材料、培养基或来自纯化/生产过程的其他化学物质。核酸序列可以是合成的,例如通过直接的化学合成产生。核酸序列可以作为裸露的核酸被提供,或可与蛋白或脂质复合提供。
本发明的多肽的核苷酸全长序列或其片段通常可以用pcr扩增法、重组法或人工合成的方法获得。对于pcr扩增法,可根据已公开的有关核苷酸序列,尤其是开放阅读框序列来设计引物,并用市售的cdna库或按本领域技术人员已知的常规方法所制备的cdna库作为模板,扩增而得有关序列。当序列较长时,常常需要进行两次或多次pcr扩增,然后再将各次扩增出的片段按正确次序拼接在一起。目前,已经可以完全通过化学合成来得到编码本发明多肽(或其片段,或其衍生物)的dna序列。然后可将该dna序列引入本领域中已知的各种现有的dna分子(或如载体)和细胞中。
本发明也涉及包含本发明的多核苷酸的载体,以及用本发明的载体或多肽编码序列经基因工程产生的宿主细胞。上述多核苷酸、载体或宿主细胞可以是分离的。
如本文所用,“分离的”是指物质从其原始环境中分离出来(如果是天然的物质,原始环境即是天然环境)。如活体细胞内的天然状态下的多核苷酸和多肽是没有分离纯化的,但同样的多核苷酸或多肽如从天然状态中同存在的其他物质中分开,则为分离纯化的。
一旦获得了有关的序列,就可以用重组法来大批量地获得有关序列。这通常是将其克隆入载体,再转入细胞,然后通过常规方法从增殖后的宿主细胞中分离得到有关序列。
此外,还可用人工合成的方法来合成有关序列,尤其是片段长度较短时。通常,通过先合成多个小片段,然后再进行连接可获得序列很长的片段。
应用pcr技术扩增dna/rna的方法被优选用于获得本发明的基因。用于pcr的引物可根据本文所公开的本发明的序列信息适当地选择,并可用常规方法合成。可用常规方法如通过凝胶电泳分离和纯化扩增的dna/rna片段。
本发明也涉及包含本发明的多核苷酸的载体,以及用本发明的载体或蛋白编码序列经基因工程产生的宿主细胞,以及经重组技术利用所述宿主细胞表达本发明光敏感通道chr2蛋白突变体的方法。
通过常规的重组dna技术,可利用本发明的多核苷酸序列获得表达本发明光敏感通道chr2蛋白突变体的宿主细胞。一般来说包括步骤:将本发明第二方面所述的多核苷酸或本发明第三方面所述的载体转导入宿主细胞内。
本领域的技术人员熟知的方法能用于构建含本发明多肽的编码dna序列和合适的转录/翻译控制信号的表达载体。这些方法包括体外重组dna技术、dna合成技术、体内重组技术等。所述的dna序列可有效连接到表达载体中的适当启动子上,以指导mrna合成。表达载体还包括翻译起始用的核糖体结合位点和转录终止子。
此外,表达载体优选地包含一个或多个选择性标记基因,以提供用于选择转化的宿主细胞的表型性状,如真核细胞培养用的二氢叶酸还原酶、新霉素抗性以及绿色荧光蛋白(gfp),或用于大肠杆菌的四环素或氨苄青霉素抗性。
包含上述的适当dna序列以及适当启动子或者控制序列的载体,可以用于转化适当的宿主细胞,以使其能够表达多肽。
宿主细胞可以是原核细胞,或是低等真核细胞,或是高等真核细胞,如哺乳动物细胞(包括人和非人哺乳动物)。代表性例子有:cho、ns0、cos7、或293细胞的动物细胞等。在本发明的一个优选实施方式中,选择hek细胞、感光细胞(包括锥状细胞和/或杆状细胞)、其他视觉细胞(如双节细胞)、神经细胞为宿主细胞。在另一优选例中,所述宿主细胞选自下组:视杆细胞、视锥细胞、给光双极细胞、撤光双极细胞、水平细胞、神经节细胞、无长突细胞、或其组合。
用重组dna转化宿主细胞可用本领域技术人员熟知的常规技术进行。当宿主为原核生物如大肠杆菌时,能吸收dna的感受态细胞可在指数生长期后收获,用cacl2法处理,所用的步骤在本领域众所周知。另一种方法是使用mgcl2。如果需要,转化也可用电穿孔的方法进行。当宿主是真核生物,可选用如下的dna转染方法:磷酸钙共沉淀法,常规机械方法如显微注射、电穿孔、脂质体包装等。
获得的转化子可以用常规方法培养,表达本发明的基因所编码的蛋白质。根据所用的宿主细胞,培养中所用的培养基可选自各种常规培养基。在适于宿主细胞生长的条件下进行培养。当宿主细胞生长到适当的细胞密度后,用合适的方法(如温度转换或化学诱导)诱导选择的启动子,将细胞再培养一段时间。
在上面的方法中的多肽可在细胞内、或在细胞膜上表达、或分泌到细胞外。如果需要,可利用其物理的、化学的和其它特性通过各种分离方法分离和纯化蛋白。这些方法是本领域技术人员所熟知的。这些方法的例子包括但并不限于:常规的复性处理、用蛋白沉淀剂处理(盐析方法)、离心、渗透破菌、超处理、超离心、分子筛层析(凝胶过滤)、吸附层析、离子交换层析、高效液相层析(hplc)和其它各种液相层析技术及这些方法的结合。
在本发明中,所述野生型光敏感通道chr2蛋白的天然的dna编码序列(未优化的dna编码序列)如seqidno.:5所示。
atggattatggaggcgccctgagtgccgttgggcgcgagctgctatttgtaacgaacccagtagtcgtcaatggctctgtacttgtgcctgaggaccagtgttactgcgcgggctggattgagtcgcgtggcacaaacggtgcccaaacggcgtcgaacgtgctgcaatggcttgctgctggcttctccatcctactgcttatgttttacgcctaccaaacatggaagtcaacctgcggctgggaggagatctatgtgtgcgctatcgagatggtcaaggtgattctcgagttcttcttcgagtttaagaacccgtccatgctgtatctagccacaggccaccgcgtccagtggttgcgttacgccgagtggcttctcacctgcccggtcattctcattcacctgtcaaacctgacgggcttgtccaacgactacagcaggcgcaccatgggtctgcttgtgtctgatattggcacaattgtgtggggcgccacttccgccatggccaccggatacgtcaaggtcatcttcttctgcctgggtctgtgttatggtgctaacacgttctttcacgctgccaaggcctacatcgagggttaccacaccgtgccgaagggccggtgtcgccaggtggtgactggcatggcttggctcttcttcgtatcatggggtatgttccccatcctgttcatcctcggccccgagggcttcggcgtcctgagcgtgtacggctccaccgtcggccacaccatcattgacctgatgtcgaagaactgctggggtctgctcggccactacctgcgcgtgctgatccacgagcatatcctcatccacggcgacattcgcaagaccaccaaattgaacattggtggcactgagattgaggtcgagacgctggtggaggacgaggccgaggctggcgcggtc(seqidno.:5)
在本发明中,所述光敏感通道chr2蛋白突变体的dna编码序列(未优化的dna编码序列)如seqidno.:3所示。
atggattatggaggcgccctgagtgccgttgggcgcgagctgctatttgtaacgaacccagtagtcgtcaatggctctgtacttgtgcctgaggaccagtgttactgcgcgggctggattgagtcgcgtggcacaaacggtgcccaaacggcgtcgaacgtgctgcaatggcttgctgctggcttctccatcctactgcttatgttttacgcctaccaaacatggaagtcaacctgcggctgggaggagatctatgtgtgcgctatcgagatggtcaaggtgattctcgagttcttcttcgagtttaagaacccgtccatgctgtatctagccacaggccaccgcgtccagtggttgcgttacgccgagtggcttctcacctgcccggtcatttgtattcacctgtcaaacctgacgggcttgtccaacgactacagcaggcgcaccatgggtctgcttgtgtctgatattggcagtattgtgtggggcgccacttccgccatggccaccggatacgtcaaggtcatcttcttctgcctgggtctgtgttatggtgctaacacgttctttcacgctgccaaggcctacatcgagggttaccacaccgtgccgaagggccggtgtcgccaggtggtgactggcatggcttggctcttcttcgtatcatggggtatgttccccatcctgttcatcctcggccccgagggcttcggcgtcctgagcgtgtacggctccaccgtcggccacaccatcattgacctgatgtcgaagaactgctggggtctgctcggccactacctgcgcgtgctgatccacgagcatatcctcatccacggcgacattcgcaagaccaccaaattgaacattggtggcactgagattgaggtcgagacgctggtggaggacgaggccgaggctggcgcggtc(seqidno.:3)
在本发明中,提供了优化的、特别适合在哺乳动物细胞中表达的光敏感通道chr2蛋白突变体的编码序列,所述编码序列如seqidno.:4所示。
如本文所用,所述“优化的编码序列”、“优化编码基因”均指一种用于编码光敏感通道chr2蛋白突变体的核苷酸序列,所述的核苷酸序列编码seqidno.:2所示的氨基酸序列。
本发明优化了影响基因表达的序列片段,这些序列片段包括但不限于,密码子使用偏好性,消除不利于表达的二级结构(如发夹结构),改变gc含量,cpg二核苷酸含量,mrna的二级结构,隐蔽剪接位点,早期多聚腺苷化位点,内部核糖体进入位点和结合位点,负cpg岛,rna不稳定区,重复序列(直接重复、反向重复等)和可能影响克隆的限制性位点。最终得到如seqidno.:4所示的特别优化的dna编码序列。seqidno.:4所示的编码序列与seqidno.:3所示的编码序列相似度低于80%。
在本发明较佳的实施方式中,所述核苷酸序列如seqidno.:4所示。
atggactatggcggcgctttgtctgccgtcggacgcgaacttttgttcgttactaatcctgtggtggtgaacgggtccgtcctggtccctgaggatcaatgttactgtgccggatggattgaatctcgcggcacgaacggcgctcagaccgcgtcaaatgtcctgcagtggcttgcagcaggattcagcattttgctgctgatgttctatgcctaccaaacctggaaatctacatgcggctgggaggagatctatgtgtgcgccattgaaatggttaaggtgattctcgagttcttttttgagtttaagaatccctctatgctctaccttgccacaggacaccgggtgcagtggctgcgctatgcagagtggctgctcacttgtcctgtcatctgtatccacctgagcaacctcaccggcctgagcaacgactacagcaggagaaccatgggactccttgtctcagacatcgggagcatcgtgtggggggctaccagcgccatggcaaccggctatgttaaagtcatcttcttttgtcttggattgtgctatggcgcgaacacattttttcacgccgccaaagcatatatcgagggttatcatactgtgccaaagggtcggtgccgccaggtcgtgaccggcatggcatggctgtttttcgtgagctggggtatgttcccaattctcttcattttggggcccgaaggttttggcgtcctgagcgtctatggctccaccgtaggtcacacgattattgatctgatgagtaaaaattgttgggggttgttgggacactacctgcgcgtcctgatccacgagcacatattgattcacggagatatccgcaaaaccaccaaactgaacatcggcggaacggagatcgaggtcgagactctcgtcgaagacgaagccgaggccggagccgtg(seqidno.:4)
在本发明中,所述野生型光敏感通道chr2蛋白的优化后的dna编码序列如seqidno.:6所示。
atggactatggcggcgctttgtctgccgtcggacgcgaacttttgttcgttactaatcctgtggtggtgaacgggtccgtcctggtccctgaggatcaatgttactgtgccggatggattgaatctcgcggcacgaacggcgctcagaccgcgtcaaatgtcctgcagtggcttgcagcaggattcagcattttgctgctgatgttctatgcctaccaaacctggaaatctacatgcggctgggaggagatctatgtgtgcgccattgaaatggttaaggtgattctcgagttcttttttgagtttaagaatccctctatgctctaccttgccacaggacaccgggtgcagtggctgcgctatgcagagtggctgctcacttgtcctgtcatccttatccacctgagcaacctcaccggcctgagcaacgactacagcaggagaaccatgggactccttgtctcagacatcgggactatcgtgtggggggctaccagcgccatggcaaccggctatgttaaagtcatcttcttttgtcttggattgtgctatggcgcgaacacattttttcacgccgccaaagcatatatcgagggttatcatactgtgccaaagggtcggtgccgccaggtcgtgaccggcatggcatggctgtttttcgtgagctggggtatgttcccaattctcttcattttggggcccgaaggttttggcgtcctgagcgtctatggctccaccgtaggtcacacgattattgatctgatgagtaaaaattgttgggggttgttgggacactacctgcgcgtcctgatccacgagcacatattgattcacggagatatccgcaaaaccaccaaactgaacatcggcggaacggagatcgaggtcgagactctcgtcgaagacgaagccgaggccggagccgtg(seqidno.:6)
表达载体和宿主细胞
本发明还提供了一种用于光敏感通道chr2蛋白突变体的表达载体,它含有本发明突变体的编码序列。
通过提供的序列信息,熟练的技术人员可以使用可用的克隆技术以产生适于转导进入细胞的核酸序列或载体。
优选地,编码光敏感通道chr2蛋白突变体的核酸序列作为载体,优选地表达载体被提供。优选地,其可作为优选地适用于在靶视网膜细胞中转导和表达的基因治疗载体被提供。载体可以是病毒的或非病毒的(例如质粒)。病毒载体包括源自以下的那些病毒载体:腺病毒、包括突变的形式的腺相关病毒(aav)、逆转录病毒、慢病毒、疱疹病毒、牛痘病毒、脊髓灰质炎病毒、mmlv、galv、猿猴免疫缺陷病毒(siv)、hiv、痘病毒和sv40。优选地,病毒载体是复制缺陷的(replicationdefective),尽管设想其可以是复制缺乏的(replicationdeficient)、能够复制或条件性复制的。病毒载体通常可以保持染色体外状态而不整合进入靶视网膜细胞的基因组。用于向视网膜靶细胞引入编码光敏感通道chr2蛋白突变体的核酸序列的优选的病毒载体是aav载体,例如自身互补的腺相关病毒(scaav)。使用特定的aav血清型(aav血清型2到aav血清型12)或这些血清型中的任何一个的修饰的版本(包括aav4yf和aav7m8载体)可以实现选择性靶向。
病毒载体可被修饰以缺失任何非必需的序列。例如,aav中,病毒可被修饰以缺失全部或部分的ix基因、ela和/或elb基因。对于野生型aav,没有辅助病毒诸如腺病毒的存在,复制是非常低效率的。对于重组的腺相关病毒,优选地,复制基因和衣壳基因以反式被提供(在prep/cap质粒中),并且仅aav基因组的2itr被保留并且包装进入病毒体,同时需要的腺病毒基因被被腺病毒或另一个质粒提供。也可对慢病毒载体做出类似的修饰。
病毒载体具有进入细胞的能力。然而,非病毒载体诸如质粒可与剂复合以有利于病毒载体被靶细胞的摄取。此类剂包括聚阳离子剂。可选地,递送系统诸如基于脂质体的递送系统可被使用。
用于在本发明中使用的载体优选地适于在体内或体外使用,并且优选地适于在人类中使用。
载体将优选地包含一个或多个调节序列以指导核酸序列在靶视网膜细胞中的表达。调节序列可以包括与核酸序列可操作地连接的启动子、增强子、转录终止信号、多腺苷酸化序列、复制起点、核酸限制性位点、和同源重组位点。载体还可包括选择性标记,例如来确定载体在生长系统(例如细菌细胞)中或在靶视网膜细胞中的表达。
“可操作地连接”意指,核酸序列在功能上与其可操作地连接的序列相关,以使得它们以使得它们影响彼此的表达或功能的方式连接。例如,与启动子可操作地连接的核酸序列将具有被启动子影响的表达模式。
启动子介导与其连接的核酸序列的表达。启动子可以是组成型的或可以是诱导型的。启动子可以指导在内视网膜细胞中遍在的表达,或神经元特异的表达。在后一种情况中,启动子可以指导细胞类型特异的表达,例如对给光双极细胞或撤光双极细胞。合适的启动子将是本领域技术人员己知的。例如,合适的启动子可以选自由以下组成的组:l7、thy-1、恢复蛋白、钙结合蛋白、人类cmv、gad-67、鸡β肌动蛋白、hsyn、grm6、grm6增强子sv40融合蛋白。使用细胞特异的启动子可以实现靶向,例如grm6-sv40用于选择性靶向给光双极细胞。grm6启动子是grm6基因的200碱基对增强子序列和sv40真核启动予的融合体,grm6基因编码给光双极细胞特异的代谢型谷氨酸受体mglur6。grm6基因的优选的来源是小鼠和人类。使用泛-神经元的启动子可以实现遍在的表达,其实例在本领域是己知的并且可得的。一个此类实例是cag。cag启动于是cmv早期增强子和鸡β肌动蛋白启动子的融合体。
合适的启动子的一个例子为即时早期巨细胞病毒(cmv)启动子序列。该启动子序列为能够驱动可操作地连接至其上的任何多核苷酸序列高水平表达的强组成型启动子序列。合适的启动子的另一个例子为延伸生长因子-1α(ef-1α)。然而,也可使用其他组成型启动子序列,包括但不限于类人猿病毒40(sv40)早期启动子、小鼠乳癌病毒(mmtv)、人免疫缺陷病毒(hiv)长末端重复(ltr)启动子、momulv启动子、鸟类白血病病毒启动子、艾伯斯坦-巴尔(epstein-barr)病毒即时早期启动子、鲁斯氏肉瘤病毒启动子、以及人基因启动子,诸如但不限于肌动蛋白启动子、肌球蛋白启动子、血红素启动子和肌酸激酶启动子。进一步地,本发明不应被限于组成型启动子的应用。诱导型启动子也被考虑为本发明的一部分。诱导型启动子的使用提供了分子开关,其能够当这样的表达是期望的时,打开可操作地连接诱导型启动子的多核苷酸序列的表达,或当表达是不期望的时关闭表达。诱导型启动子的例子包括但不限于金属硫蛋白启动子、糖皮质激素启动子、孕酮启动子和四环素启动子。
许多表达载体可应用光敏感通道chr2蛋白突变体在哺乳动物细胞(较佳地为人,更佳地为人视觉细胞或感光细胞)表达。本发明优选用腺相关病毒作为表达载体。
本发明还提供了一种宿主细胞,用于表达光敏感通道chr2蛋白突变体。优选地,所述宿主细胞为哺乳动物细胞(较佳地为人,更佳地为人视觉细胞或感光细胞)。
制剂和组合物
本发明提供一种制剂或组合物,所述制剂或组合物含有(a)本发明第三方面所述的载体或本发明第四方面所述的腺相关病毒载体,以及(b)药学上可接受的载体。
在另一优选例中,所述药物制剂用于治疗眼部疾病。
在另一优选例中,所述眼部疾病由光感受器细胞退化引起。
在另一优选例中,所述药物制剂用于扩大或恢复视网膜的光感受器功能、恢复受试者视力、和/或治疗视网膜退化性疾病。
本发明所述药物组合物中的“活性成分”是指本发明所述的载体(vector),例如病毒载体(包括腺相关病毒载体)。
本发明所述的“活性成分”、制剂和/或组合物可用于治疗眼部疾病。
“安全有效量”指的是:活性成分的量足以明显改善病情或症状,而不至于产生严重的副作用。
“药学上可接受的载体或赋形剂(excipient)”指的是:一种或多种相容性固体或液体填料或凝胶物质,它们适合于人使用,而且必须有足够的纯度和足够低的毒性。
“相容性”在此指的是组合物中各组份能和本发明的活性成分以及它们之间相互掺和,而不明显降低活性成分的药效。
组合物可以是液体或固体,例如粉末、凝胶或糊剂。优选地,组合物是液体,优选地可注射液体。合适的赋形剂将是本领域技术人员己知的。
在本发明中,所述载体可通过视网膜下或玻璃体内施用向眼睛施用。在任一种施用模式中,优选地,载体作为可注射液体被提供。优选地,可注射液体作为胶囊或注射器被提供。
药学上可以接受的载体部分例子有纤维素及其衍生物(如羧甲基纤维素钠、乙基纤维素钠、纤维素乙酸酯等)、明胶、滑石、固体润滑剂(如硬脂酸、硬脂酸镁)、硫酸钙、植物油(如豆油、芝麻油、花生油、橄榄油等)、多元醇(如丙二醇、甘油、甘露醇、山梨醇等)、乳化剂(如
组合物可包含生理上可接受的无菌含水或无水溶液、分散液、悬浮液或乳液,和用于重新溶解成无菌的可注射溶液或分散液的无菌粉末。适宜的含水和非水载体、稀释剂、溶剂或赋形剂包括水、乙醇、多元醇及其适宜的混合物。
本发明的组合物可被提供用于在向细胞提供光感受器功能的方法中使用。在一个实施方案中,本发明的组合物可被提供用于在对视网膜恢复光感受器功能的方法中使用。在一个实施方案中,本发明的组合物可被提供用于在对受试者恢复视力的方法中使用。在一个实施方案中,本发明的组合物可被提供用于在治疗视网膜退化的状况的方法中使用,所述视网膜退化的状况例如视网膜营养不良,包括视杆营养不良、视杆视锥营养不良、视锥视杆营养不良、视锥营养不良和黄斑营养不良;其他形式的视网膜或黄斑退化、缺血性状况、葡萄膜炎和由光感受器能力的丧失导致的任何其他疾病,例如视网膜色素变性。
治疗方法
本发明提供了向细胞提供光感受器功能的方法,所述方法包括将包含编码光敏感通道chr2蛋白突变体的核酸的载体引入到眼睛内。所述方法可包括向眼睛的内视网膜细胞视网膜下或玻璃体内施用核酸载体。本发明提供了用于通过向细胞提供光感受器功能在治疗视网膜退化的方法中使用的核酸载体,所述核酸载体包含编码光敏感通道chr2蛋白突变体的核酸序列。本发明组合物可以单独给药,或者与其他治疗药物联合给药(如配制在同一药物组合物中)。
本发明还提供了扩大视网膜中的光感受器功能的方法,特别是在视杆和/或视锥细胞退化之后扩大视网膜中的光感受器功能的方法,所述方法包括将核酸载体引入到眼睛的玻璃体腔内,所述核酸载体包含编码光敏感通道chr2蛋白突变体的核酸序列。所述方法可包括向眼睛的内视网膜细胞,视网膜下或玻璃体内施用核酸载体。本发明提供了用于通过扩大视网膜中的光感受器功能在治疗视网膜退化中使用的核酸载体,所述核酸载体包含编码光敏感通道chr2蛋白突变体的核酸序列。
本发明还提供了对受试者恢复视力的方法,所述方法包括将包含编码光敏感通道chr2蛋白突变体的核酸序列的载体引入到眼睛内。方法可包括视网膜下或玻璃体内施用核酸载体到眼睛的内视网膜细胞。本发明提供了用于在对受试者恢复视力中使用的核酸载体,所述核酸载体包含编码光敏感通道chr2蛋白突变体的核酸序列。
本发明还提供了治疗受试者中的视网膜疾病的方法,所述方法包括将包含编码光敏感通道chr2蛋白突变体的核酸序列的载体引入到眼睛内。方法可包括视网膜下或玻璃体内施用核酸载体到眼睛的内视网膜细胞。疾病可以是视网膜营养不良,包括视杆营养不良、视杆视锥营养不良、视锥视杆营养不良、视锥营养不良和黄斑营养不良;其他形式的视网膜或黄斑退化、缺血性状况、葡萄膜炎和由光感受器能力的丧失导致的任何其他疾病。
如本文所用,向细胞提供光感受器功能意指,之前不具有光感受器能力或其光感受器能力已经完全地或部分地退化的细胞,在其中表达编码光敏感通道chr2蛋白突变体的外来核酸序列后,变成感光的。此类细胞在本文中可被称作转化的细胞,因为其在其中包含非天然的核酸。优选地,转化的视网膜细胞展现天然的感光细胞的一些或全部的光感受器能力。优选地,转化的细胞展现天然的视网膜光感受器细胞的至少相同或大体上相同的感光能力。优选地,转化的细胞展现比患病的或正在退化的天然的视网膜光感受器细胞高的感光能力。因此,转化的细胞相比于来自同一来源、保持在同一条件下、未经处理的退化的或患病的细胞,将优选地具有增加的光感受器。转化的细胞通过其中的外源核酸的存在可与天然的细胞区分。
如本文所用,扩大光感受器功能意指通过增加光感受器细胞诸如视杆或视锥细胞中的功能和/或通过向细胞提供光感受器功能,增加视网膜的光感受器功能。因此,视网膜相比于未用如本文描述的方法处理的视网膜,将具有增加的接收光信号并且传送此类信号的能力,增加可以是任何量。
如本文所用,恢复受试者中的视力意指,受试者相比于治疗之前,例如使用如本文描述的视力测试,显示改进的视力。恢复包括任何程度的改进,包括视力的完全恢复到完美的或接近完美的视力。
如本文所用,治疗疾病意指施用如本文描述的核酸或载体以改善或减轻疾病的一种或多种症状,所述疾病选自由以下组成的组:视网膜营养不良,包括视杆营养不良、视杆视锥营养不良、视锥视杆营养不良、视锥营养不良和黄斑营养不良;另一种形式的视网膜或黄斑退化、缺血性状况、葡萄膜炎和由光感受器能力的丧失导致的任何其他疾病。改善或减轻可导致外周或中央视力、和/或白天或夜间视力的改善。
本发明的方法包括将编码光敏感通道chr2蛋白突变体的核酸序列引入到眼睛的玻璃体腔内。优选地,方法包括使细胞与包含编码光敏感通道chr2蛋白突变体的核酸序列的载体(较佳地为病毒,更佳地为腺相关病毒)接触。优选地,细胞是视网膜细胞,优选地给光双极细胞、撤光双极细胞、水平细胞、神经节细胞和/或无长突细胞。
当核酸序列和一种或多种酶以多个(两个或多个)剂量被提供时,这些剂量可分隔合适的时间间隔,例如30秒到若干小时或1天或多天。
每个剂量可包含有效量的核酸序列或病毒载体。核酸序列或病毒载体的有效剂量可以在每治疗方案1×109-1×1016病毒的范围。
本发明是基于靶向编码光敏感通道chr2蛋白突变体的核酸序列到视网膜细胞,以补偿视网膜中光感受器细胞的退化。核酸序列被靶向至的细胞是视网膜的细胞,其是活的并且能够表达外来核酸序列。视网膜细胞是视网膜的细胞,其是神经或神经元细胞并且能够变兴奋并传送电信号。优选地,靶视网膜细胞将能够产生电信号并且起始信号级联,导致信号向视神经的传送。优选地,靶视网膜细胞是内视网膜的细胞。靶细胞可以是视杆或视锥细胞,和/或可以是非光感受器细胞(即呈其天然形式的对光不响应的视网膜细胞)。靶视网膜细胞可以包括一种或多种细胞类型,所述细胞类型选自由以下组成的组:视杆细胞、视锥细胞、给光双极细胞、撤光双极细胞、水平细胞、神经节细胞、米勒细胞和/或无长突细胞。
因此,当靶视网膜细胞是靶向视网膜的给光双极细胞、撤光双极细胞、水平细胞、神经节细胞和/或无长突细胞时,编码光敏感通道chr2蛋白突变体的核酸的表达可以被称作异位表达。因此,本发明在其范围内包括在非光感受器细胞中异位表达编码光敏感通道chr2蛋白突变体的核酸序列的方法。此类异位表达通过其中的异源光敏蛋白的表达,具有向细胞提供光感受器功能的作用。这用于增加观察到退化的视网膜的感光能力。
水平细胞是内视网膜细胞,参与信号加工和反馈到光感受器细胞;双极细胞是内视网膜细胞并且在视杆/视锥细胞和无长突和/或神经节细胞间通信;无长突细胞发现于内视网膜并且允许在光感受器途径和神经节细胞间的通信;神经节细胞是最内部的视网膜细胞,其将信号从光感受器细胞传递到视神经。
本文对细胞的提及包括细胞的后代。优选地,根据本发明的对细胞的修饰还发生在转化的宿主细胞以后的代中。后代细胞可以不与最初的靶向细胞一致,但优选地将也展现非天然的光敏感通道chr2蛋白突变体的表达。
本发明主要具有以下优点:
1.本发明提供了一种感光能力得到显著提高的chr2蛋白突变体,具有更强的光电流,光电效应显著提升,其感光能力相比野生型chr2蛋白至少提高了5倍以上。
2.本发明对chr2基因序列进行了优化。与光敏感通道chr2蛋白突变体的未优化的dna编码序列seqidno.3相比,优化后的序列(seqidno.:4)的光敏感通道chr2蛋白突变体表达量和感光能力显著提高。
3.本发明chr2蛋白突变体的编码序列非常适合在哺乳动物体内表达。在本发明中,表达的chr2蛋白突变体既保持了天然chr2蛋白的活性,且chr2蛋白表达量高,感光能力强,可用于扩大或恢复视网膜的光感受器功能、恢复受试者视力、和/或治疗视网膜退化性疾病。
下面结合具体实施,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数按重量计算。
实施例1序列优化
在本实施例中,基于野生型chr2蛋白的氨基酸序列(seqidno.:1)和天然的编码序列(seqidno.:5),本发明人对氨基酸序列和核酸编码序列进行了突变和优化。
具体地,本发明人先将野生型chr2蛋白的氨基酸序列的第132位亮氨酸(l)突变为半胱氨酸(c),第159位苏氨酸(t)突变为丝氨酸(s),得到chr2蛋白突变体的氨基酸序列seqidno.:2。相应地,所述突变蛋白的核酸编码序列如seqidno.:3所示。
本发明人还进一步优化了影响基因表达的序列片段,这些序列片段包括但不限于:密码子使用偏好性,消除不利于表达的二级结构(如发夹结构),改变gc含量,cpg二核苷酸含量,mrna的二级结构,隐蔽剪接位点,早期多聚腺苷化位点,内部核糖体进入位点和结合位点,负cpg岛,rna不稳定区,重复序列(直接重复、反向重复等)和可能影响克隆的限制性位点。通过分析和试验筛选,最终得到如seqidno.:4所示的特别优化的dna编码序列。此外,对野生型chr2蛋白的编码序列也进行了优化,所述野生型光敏感通道chr2蛋白的优化后的dna编码序列如seqidno.:6所示,其中除突变位点外其他序列完全相同。
实施例2raav-chr2病毒的包装、纯化和感染
全基因合成raav2-1dna质粒,其中raav2-1dna质粒为携带有野生型光敏感通道chr2蛋白的优化序列(seqidno.:6)和gfp的avv载体(如图1所示),raav2-2dna质粒为携带有突变型光敏感通道chr2蛋白的优化序列(seqidno.:4)和gfp的avv载体。raav2-2dna质粒中除chr2蛋白的编码序列不同(即,将seqidno.:6替换为seqidno.:4),其它与和raav2-1dna质粒完全相同。将raav2-1dna质粒和raav2-2dna质粒分别联同paav-rc和phelper共同转染到hek293细胞中,转染步骤如下(北京博奥龙免疫技术有限公司quickshuttle转染试剂):
将hek-293细胞维持在改良dmem培养基(advanceddulbecco’sminimumessentialmedium,购自lifetechnologies公司),改良dmem培养基中添加有5%胎牛血清,在37℃、潮湿的5%co2条件下培养。
在准备dna转染时,将细胞接种在100-mm培养皿中,然后使用quickshuttle转染试剂(北京博奥龙免疫技术有限公司)用raav2-1dna质粒和raav2-2dna质粒分别联同paav-rc和phelper质粒共同转染。在dna转染的同时将全反式视黄醛(1μm)加入到培养基中。具体方法如下:
1.转染前18-24小时接种细胞到100-mm细胞板中,每孔6×106细胞,10ml完全培养基。
2.将20μg质粒dna(三种质粒分子数比例为1:1:1)和60μl转染试剂分别稀释到500μl生理盐水中。
3.合并上述两溶液并混匀。
4.将上述复合物直接加入到细胞培养基中,轻摇细胞板或用加样器吸打混匀。
5.转染后将细胞板移至37℃/5%co2孵箱中进行培养48小时,以进行荧光检测。
6.收集感染后的细胞,每50盘用10mlpbs悬浮,经过3次干冰/乙醇-37℃冻融后,10000g离心,收集上清。经过millipore100kd超滤管浓缩至200μl左右,得到病毒粗体液。
7.通过荧光定量pcr测定粗提病毒的滴度(gc/ml)。
8.将10μl1013gc/ml的粗提病毒与2ml5x104hek293细胞混合,并接种到3.5cm细胞板中,培养72小时,用于单细胞膜片钳记录。
结果表明,成功将raav2-1dna质粒和raav2-2dna质粒分别转染到hek293细胞中并包装出raav-chr2重组病毒。转导有raav2-1dna质粒或raav2-2dna质粒的hek293细胞均表现出强荧光,可较强地瞬时表达chr2突变蛋白(图2)。其粗提病毒滴度可达1013gc/ml,并可很好感染hek293细胞并表达chr2-gfp融合蛋白(图2)。
实施例3单细胞膜片钳记录
对于荧光检测,将hek细胞用0.1m磷酸盐缓冲液(pb)中的4%多聚甲醛固定10分钟,然后用0.1mpb洗涤3次,每次10分钟。在固定条件下(光照强度和曝光时间),使用zeissaxioplan2显微镜(carlzeiss)和apotome振荡光栅(以减少离焦杂散光)拍照。使用imagej软件通过将单个光学切片的质膜区域的总荧光值除以相同区域的像素总数,计算每个hek细胞的荧光强度。
使用axopatch200b膜片钳放大器和clampex10软件(美国axon公司)在室温(20-25℃)下使用标准程序获取具有贴片电极的全细胞构型的记录。电极(bf150-86-10,sutter)经电极拉制仪(pc-100,narishige)制备后电阻是4-7mω。电极与目标细胞形成高阻封接后补偿电容。破细胞形成全细胞记录模式时再次补偿电容和电阻。在hank’s平衡盐溶液中进行记录,hank’s平衡盐溶液含有(以mm计):138nacl,1nahco3,0.3na2hpo4,5kcl,0.3kh2po4,1.25cacl2,0.5mgso4,0.5mgcl2,5hepes,22.2葡萄糖和0.001%(vv)酚红,并用0.3nnaoh将ph调节至7.2。将全反式视黄醛(1μm)加入到记录溶液中。电极溶液含有(以mm计):110cs-甲磺酸盐,30tea-cl,2mgcl2,0.1cacl2,10egta和10hepes,使用csoh将ph调节至7.25。全细胞记录在钳制电压-60mv下进行电流记录。
优化后的野生型和突变型aav-chr2病毒感染hek293细胞后并在给光后全细胞膜片钳记录的电流反应通过单细胞膜片钳分析,结果表明:
相比野生型chr2蛋白,chr2突变蛋白具有更强的光电流和光电效应,可以看出突变型(图3-b)无论在电流峰值以及稳定平台期,都比野生型的高(图3-a)。虽然不同细胞存在细胞大小和融合蛋白表达量的差别(表现在荧光强度的差别),但所有的野生型在光强度低于1015photons/cm2s后就难以检测到电流变化(图3-c),而突变型在1.8x1014photons/cm2s光强度下仍然可以检测到明显的电流变化(图3-d),感光能力显著提高,至少提高了5倍以上。
此外,本发明还构建并表达了对应于野生型chr2蛋白(seqidno.:1)仅在第159位苏氨酸(t)突变为丝氨酸(s)的chr2蛋白突变体。结果发现,该chr2蛋白突变体相对于野生型chr2蛋白,也具有更强的光电流和光电效应,感光能力显著提高(至少提高了5倍以上)。
讨论
光遗传通常是指结合光学与遗传学手段,精确控制特定神经元活动的技术。该技术利用分子生物学、病毒生物学等手段,将外源光敏感蛋白基因导入活细胞中,在细胞膜结构上表达了光敏感通道蛋白;然后通过特定波长光的照射,控制细胞膜结构上的光敏感通道蛋白的激活与关闭;光敏感蛋白的激活和关闭可控制细胞膜上离子通道的打开与关闭,进而改变细胞膜电压的变化,如膜的去极化与超极化。当膜电压去极化超过一定阈值时就会诱发神经元产生可传导的电信号,即神经元的激活;相反,当膜电压超极化到一定水平时,就会抑制神经元动作电位的产生,即神经元的抑制。神经元生物学家经常运用这种技术,通过光学方法无损伤或低损伤地控制特异神经元的活动,来研究该神经网络功能,特别适用于在体、甚至清醒动物行为学实验。同时,利用类似的光学与遗传学手段,可控制脑细胞外其它细胞中的蛋白表达,从而实现光诱导蛋白质表达,启动细胞内生物学过程,进而控制生物行为。因此光遗传技术在生命活动与疾病研究中应用广泛。
光感基因包括chr2,ebr,nahr3.0,arch或optoxr等,其中chr2应用最为广泛。天然chr2蛋白是一个光控阳离子通道,含737个氨基酸。细胞內源视黄醛足以辅助截短至309氨基酸的chr2蛋白实现其功能,不需要添加外源色基。毕安定等在2006年首创应用包裹chr2编码序列的重组腺相关病毒(raav)感染视神经节细胞,建立人工视网膜。应用盲小鼠品系rd1(亦称c3h)实验证明,一次注射上述raav-chr2载体可以成功感染20%左右的视神经节细胞,比照人类视网膜,可以恢复近20万视神经节细胞的感光能力,相当于重新架设了一台20万像素的感光片。毕安定等首次利用光遗传技术,通过导入chr2光感基因,成功恢复了完全失明小鼠的感光能力。盲小鼠rd1品系模拟人类视网膜色素变性(rp),类似应用也可以治疗干性老年型视黄斑变性(dry-amd)最终导致失明的患者。目前中国有统计的盲人人口约700万,保守估计符合基因治疗条条件的盲人患者不低于20万人。随着人口老龄化加重,人均寿命的增长,amd患者数量必然会进一步增加。基于chr2的光遗传技术的基因治疗,是恢复盲人感光能力的一个最有希望的治疗手段。
chr2作为光遗传学工具的代表,光遗传学工具的应用不仅仅局限于盲人的视觉恢复。光遗传学工具本质上是一个蛋白质光电开关,进一步改造可以构建光化学开关,乃至于任何光控细胞生理效应开关。即理论上可以由光控制细胞内的一切生理生化过程,而且由于光的特性,这种控制既可以精密到分子水平,也可以做组织器官甚至个体水平的宏观操控。
举例而言:
1)大脑γ震荡频率在25赫兹至80赫兹,阿尔茨海默症(ad)患者往往伴随γ波损伤。本发明人在2011年国家自然科学基金课题申请书中提及可以用chr2调控大脑皮层基底神经节β频率震荡,从而改善帕金森症(pd)的设想。2016年edboyden与蔡立慧教授应用光遗传学工具成功控制大脑γ震荡,有效缓解实验小鼠的ad症状,大幅降低ad小鼠视皮层β淀粉样蛋白沉积斑块。相关论文发表于自然(nature)杂志。
2)大脑杏仁核是控制人体动作、情感和恐惧的区域,在小鼠中分别用光控制负责追捕和负责撕咬的神经,单独抑制追捕时老鼠仍然会撕咬,单独抑制撕咬则只追捕不撕咬。而光激活两个通路时,老鼠则不加选择地攻击遇到的任何障碍。相关论文2016年发表于细胞(cell)杂志。
3)脑机界面。由于电极植入是损伤性且不可持续,哈佛医学院最近考虑用磁场刺激替代,事实上,光遗传学工具才是最佳的选择。理论上说弱磁场刺激产生的弱电场对细胞是无损的,较强磁场刺激对人体的危害仍然在评估中,而强磁场刺激毫无疑问是对人体有害的。光作为一种特殊的电磁波,本身具有磁场的优点,在光遗传学工具的配合下,可以简单类比为共振效应,必然以几何级数提高目的细胞的响应。因此,只需要使用较弱的光源就能够达到较强磁场才能获得的效果,而脑神经细胞内所需定向导入的光遗传学工具只需事先注射表达,在封闭无光刺激的大脑中不会产生任何副作用。
4)非接触式给药,例如脉冲释放生长激素、神经递质、光控胰岛素合成等。华东师大叶海峰团队用红外led激活外源移植细胞表达胰岛素,成功缓解糖尿病模型小鼠的临床症状,该研究最近发表于科学杂志转化医学子刊(sciencetranslationalmedicine)。
5)光起搏器。根据心脏节律控制的研究成果,将光遗传学工具导入心肌细胞,即可建立光控心脏搏动节律。早期实验显示光控斑马鱼心动过速、心动过缓、房室传导阻滞和心脏骤停都是可行的;在哺乳动物中则往往表现为干扰导致心律失常。最近研究显示心房、心室浦肯野细胞或许是最佳的刺激对象,极微弱的光辐射即可诱导心肌细胞兴奋。联合使用兴奋型和抑制型光遗传学工具有望开发出可供临床应用的光起搏器。
6)非显性阈值下细胞膜去极化(或极化)调控。有文献证明这种不诱发细胞膜电位的细胞膜电位变化对神经突触的可塑性具有调控作用,其可能的机理是通过调控神经突触向细胞核传递的化学信号实现。这种应用不像神经电位开关那么明显,也缺乏合适的内参照系,在研究和应用中面临实际挑战。
7)独立光谱和独立遗传表达调控原件组合可以简单便捷地实现对生物体的复杂调控。本发明人尝试过联合应用兴奋型工具chr2和抑制型工具(halorhodopsin,halor)模拟视网膜对光的“亮”/“暗”反应。本发明人也尝试过应用mglur6启动子元件调控chr2的视双极细胞特异表达,本发明人还尝试过应用neuroligin-1(nlg-1)亚细胞定位信号定位表达chr2于神经细胞外周,从而在特定意义上实现视神经“外周”/“中心”视觉效应(surroundoroff-center)。另一方面,目前已经报道的光遗传学工具激发光谱覆盖从紫外到红外全波段,例如人眼敏感光谱为437、498、533和564nm,cochr最大吸收光谱约440nm,chr2最大吸收光谱约470nm,reachr最大吸收光谱约530nm,chrimson最大吸收光谱约580nm,可以同时恢复人眼全光谱;精确的突变子筛选甚至可以获得与人眼感光谱完全一致的chr突变子。
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
序列表
<110>上海视霁生物工程有限公司
<120>光敏感通道chr2蛋白的突变体及其应用
<130>p2018-0160
<160>6
<170>siposequencelisting1.0
<210>1
<211>309
<212>prt
<213>莱茵衣藻(chlamydomonasreinhardtii)
<400>1
metasptyrglyglyalaleuseralavalglyarggluleuleuphe
151015
valthrasnprovalvalvalasnglyservalleuvalprogluasp
202530
glncystyrcysalaglytrpilegluserargglythrasnglyala
354045
glnthralaserasnvalleuglntrpleualaalaglypheserile
505560
leuleuleumetphetyralatyrglnthrtrplysserthrcysgly
65707580
trpglugluiletyrvalcysalaileglumetvallysvalileleu
859095
gluphephephegluphelysasnprosermetleutyrleualathr
100105110
glyhisargvalglntrpleuargtyralaglutrpleuleuthrcys
115120125
provalileleuilehisleuserasnleuthrglyleuserasnasp
130135140
tyrserargargthrmetglyleuleuvalseraspileglythrile
145150155160
valtrpglyalathrseralametalathrglytyrvallysvalile
165170175
phephecysleuglyleucystyrglyalaasnthrphephehisala
180185190
alalysalatyrilegluglytyrhisthrvalprolysglyargcys
195200205
argglnvalvalthrglymetalatrpleuphephevalsertrpgly
210215220
metpheproileleupheileleuglyprogluglypheglyvalleu
225230235240
servaltyrglyserthrvalglyhisthrileileaspleumetser
245250255
lysasncystrpglyleuleuglyhistyrleuargvalleuilehis
260265270
gluhisileleuilehisglyaspilearglysthrthrlysleuasn
275280285
ileglyglythrgluilegluvalgluthrleuvalgluaspgluala
290295300
glualaglyalaval
305
<210>2
<211>309
<212>prt
<213>人工序列(artificialsequence)
<400>2
metasptyrglyglyalaleuseralavalglyarggluleuleuphe
151015
valthrasnprovalvalvalasnglyservalleuvalprogluasp
202530
glncystyrcysalaglytrpilegluserargglythrasnglyala
354045
glnthralaserasnvalleuglntrpleualaalaglypheserile
505560
leuleuleumetphetyralatyrglnthrtrplysserthrcysgly
65707580
trpglugluiletyrvalcysalaileglumetvallysvalileleu
859095
gluphephephegluphelysasnprosermetleutyrleualathr
100105110
glyhisargvalglntrpleuargtyralaglutrpleuleuthrcys
115120125
provalilecysilehisleuserasnleuthrglyleuserasnasp
130135140
tyrserargargthrmetglyleuleuvalseraspileglyserile
145150155160
valtrpglyalathrseralametalathrglytyrvallysvalile
165170175
phephecysleuglyleucystyrglyalaasnthrphephehisala
180185190
alalysalatyrilegluglytyrhisthrvalprolysglyargcys
195200205
argglnvalvalthrglymetalatrpleuphephevalsertrpgly
210215220
metpheproileleupheileleuglyprogluglypheglyvalleu
225230235240
servaltyrglyserthrvalglyhisthrileileaspleumetser
245250255
lysasncystrpglyleuleuglyhistyrleuargvalleuilehis
260265270
gluhisileleuilehisglyaspilearglysthrthrlysleuasn
275280285
ileglyglythrgluilegluvalgluthrleuvalgluaspgluala
290295300
glualaglyalaval
305
<210>3
<211>927
<212>dna
<213>人工序列(artificialsequence)
<400>3
atggattatggaggcgccctgagtgccgttgggcgcgagctgctatttgtaacgaaccca60
gtagtcgtcaatggctctgtacttgtgcctgaggaccagtgttactgcgcgggctggatt120
gagtcgcgtggcacaaacggtgcccaaacggcgtcgaacgtgctgcaatggcttgctgct180
ggcttctccatcctactgcttatgttttacgcctaccaaacatggaagtcaacctgcggc240
tgggaggagatctatgtgtgcgctatcgagatggtcaaggtgattctcgagttcttcttc300
gagtttaagaacccgtccatgctgtatctagccacaggccaccgcgtccagtggttgcgt360
tacgccgagtggcttctcacctgcccggtcatttgtattcacctgtcaaacctgacgggc420
ttgtccaacgactacagcaggcgcaccatgggtctgcttgtgtctgatattggcagtatt480
gtgtggggcgccacttccgccatggccaccggatacgtcaaggtcatcttcttctgcctg540
ggtctgtgttatggtgctaacacgttctttcacgctgccaaggcctacatcgagggttac600
cacaccgtgccgaagggccggtgtcgccaggtggtgactggcatggcttggctcttcttc660
gtatcatggggtatgttccccatcctgttcatcctcggccccgagggcttcggcgtcctg720
agcgtgtacggctccaccgtcggccacaccatcattgacctgatgtcgaagaactgctgg780
ggtctgctcggccactacctgcgcgtgctgatccacgagcatatcctcatccacggcgac840
attcgcaagaccaccaaattgaacattggtggcactgagattgaggtcgagacgctggtg900
gaggacgaggccgaggctggcgcggtc927
<210>4
<211>927
<212>dna
<213>人工序列(artificialsequence)
<400>4
atggactatggcggcgctttgtctgccgtcggacgcgaacttttgttcgttactaatcct60
gtggtggtgaacgggtccgtcctggtccctgaggatcaatgttactgtgccggatggatt120
gaatctcgcggcacgaacggcgctcagaccgcgtcaaatgtcctgcagtggcttgcagca180
ggattcagcattttgctgctgatgttctatgcctaccaaacctggaaatctacatgcggc240
tgggaggagatctatgtgtgcgccattgaaatggttaaggtgattctcgagttctttttt300
gagtttaagaatccctctatgctctaccttgccacaggacaccgggtgcagtggctgcgc360
tatgcagagtggctgctcacttgtcctgtcatctgtatccacctgagcaacctcaccggc420
ctgagcaacgactacagcaggagaaccatgggactccttgtctcagacatcgggagcatc480
gtgtggggggctaccagcgccatggcaaccggctatgttaaagtcatcttcttttgtctt540
ggattgtgctatggcgcgaacacattttttcacgccgccaaagcatatatcgagggttat600
catactgtgccaaagggtcggtgccgccaggtcgtgaccggcatggcatggctgtttttc660
gtgagctggggtatgttcccaattctcttcattttggggcccgaaggttttggcgtcctg720
agcgtctatggctccaccgtaggtcacacgattattgatctgatgagtaaaaattgttgg780
gggttgttgggacactacctgcgcgtcctgatccacgagcacatattgattcacggagat840
atccgcaaaaccaccaaactgaacatcggcggaacggagatcgaggtcgagactctcgtc900
gaagacgaagccgaggccggagccgtg927
<210>5
<211>927
<212>dna
<213>莱茵衣藻(chlamydomonasreinhardtii)
<400>5
atggattatggaggcgccctgagtgccgttgggcgcgagctgctatttgtaacgaaccca60
gtagtcgtcaatggctctgtacttgtgcctgaggaccagtgttactgcgcgggctggatt120
gagtcgcgtggcacaaacggtgcccaaacggcgtcgaacgtgctgcaatggcttgctgct180
ggcttctccatcctactgcttatgttttacgcctaccaaacatggaagtcaacctgcggc240
tgggaggagatctatgtgtgcgctatcgagatggtcaaggtgattctcgagttcttcttc300
gagtttaagaacccgtccatgctgtatctagccacaggccaccgcgtccagtggttgcgt360
tacgccgagtggcttctcacctgcccggtcattctcattcacctgtcaaacctgacgggc420
ttgtccaacgactacagcaggcgcaccatgggtctgcttgtgtctgatattggcacaatt480
gtgtggggcgccacttccgccatggccaccggatacgtcaaggtcatcttcttctgcctg540
ggtctgtgttatggtgctaacacgttctttcacgctgccaaggcctacatcgagggttac600
cacaccgtgccgaagggccggtgtcgccaggtggtgactggcatggcttggctcttcttc660
gtatcatggggtatgttccccatcctgttcatcctcggccccgagggcttcggcgtcctg720
agcgtgtacggctccaccgtcggccacaccatcattgacctgatgtcgaagaactgctgg780
ggtctgctcggccactacctgcgcgtgctgatccacgagcatatcctcatccacggcgac840
attcgcaagaccaccaaattgaacattggtggcactgagattgaggtcgagacgctggtg900
gaggacgaggccgaggctggcgcggtc927
<210>6
<211>927
<212>dna
<213>人工序列(artificialsequence)
<400>6
atggactatggcggcgctttgtctgccgtcggacgcgaacttttgttcgttactaatcct60
gtggtggtgaacgggtccgtcctggtccctgaggatcaatgttactgtgccggatggatt120
gaatctcgcggcacgaacggcgctcagaccgcgtcaaatgtcctgcagtggcttgcagca180
ggattcagcattttgctgctgatgttctatgcctaccaaacctggaaatctacatgcggc240
tgggaggagatctatgtgtgcgccattgaaatggttaaggtgattctcgagttctttttt300
gagtttaagaatccctctatgctctaccttgccacaggacaccgggtgcagtggctgcgc360
tatgcagagtggctgctcacttgtcctgtcatccttatccacctgagcaacctcaccggc420
ctgagcaacgactacagcaggagaaccatgggactccttgtctcagacatcgggactatc480
gtgtggggggctaccagcgccatggcaaccggctatgttaaagtcatcttcttttgtctt540
ggattgtgctatggcgcgaacacattttttcacgccgccaaagcatatatcgagggttat600
catactgtgccaaagggtcggtgccgccaggtcgtgaccggcatggcatggctgtttttc660
gtgagctggggtatgttcccaattctcttcattttggggcccgaaggttttggcgtcctg720
agcgtctatggctccaccgtaggtcacacgattattgatctgatgagtaaaaattgttgg780
gggttgttgggacactacctgcgcgtcctgatccacgagcacatattgattcacggagat840
atccgcaaaaccaccaaactgaacatcggcggaacggagatcgaggtcgagactctcgtc900
gaagacgaagccgaggccggagccgtg927
- 还没有人留言评论。精彩留言会获得点赞!