一种2-甲基四氢呋喃的制备方法与流程
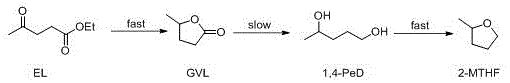
本发明涉及2-甲基四氢呋喃,尤其是涉及一种双金属催化剂催化乙酰丙酸乙酯深度加氢制备2-甲基四氢呋喃的方法。
背景技术:
如今,由于化石资源的不断消耗,可再生能源得到了广泛关注。目前,来自可再生生物质资源的生物柴油和生物乙醇已经广泛用作液体燃料,但是当它们用作运输燃料时仍然存在部分局限性。这些燃料需要以粮食为原料,成本高且存在与人争地的情况。同时,生物柴油氧化稳定性低,低温下流动性较差,而生物乙醇燃烧热值低,只能作为汽油的添加剂使用。这些局限性促使了对新型燃料的发展的需求。
2-甲基四氢呋喃是一种低极性的环醚,具有较高的辛烷值,能够以任意比例和石油燃料混合,是一种相对理想的燃料和燃料添加剂。它还是一些药物合成的重要中间体,例如磷酸氯喹、磷酸伯安喹。2-甲基四氢呋喃具有适宜的沸点(80.2oc),具有和四氢呋喃类似的碱性,被认为是四氢呋喃最适宜的替代品,可应用于一些有机合成和高分子聚合的溶剂。
乙酰丙酸及其酯类衍生物是一类重要的生物质基平台化合物,制备方式简单。目前,乙酰丙酸及其酯类衍生物加氢合成2-甲基四氢呋喃主要有均相和非均两类体系。均相体系以ru基催化剂为主,反应体系中需加入添加剂,如nh4pf6[journaloftheamericanchemicalsociety,2014,136(38):13217-13225.]。贵金属催化剂成本高,添加剂的使用也增加了一定成本,此外均相催化剂的使用也增加了分离纯化的难度,极大限制了该技术的广泛使用。目前开发出负载型cu基非均相催化剂催化乙酰丙酸/乙酰丙酸酯加氢制备2-甲基四氢呋喃,这些催化剂的催化活性低,选择性差。向cu催化剂中加入另一种金属ni以形成双金属cu-ni催化剂被发现在乙酰丙酸/γ-戊内酯加氢合成的2-甲基四氢呋喃中表现出更好的催化性能。例如,使用23ni-12cu/al2o3进行乙酰丙酸的转化,在250oc和5mpah2压力,在溶剂异丙醇体系中获得56%的2-甲基四氢呋喃产率[chemsuschem,2015,8:3483-3488.]。在250oc和7mpah2压力下,使用35cu-4ni/sio2催化剂作固定床反应器,在260℃下得到67%的2-甲基四氢呋喃,1/1的乙酰丙酸乙酯/乙醇的体积比(乙酰丙酸乙酯的whsv为0.6h-1),2-甲基四氢呋喃产率为64%[rscadvances,2016,6(90):87294-87298]。上述反应反应条件苛刻且反应产率偏低。专利(201610962296.4)提供了使用cu系催化剂用于固定床反应器中乙酰丙酸酯在无溶剂加氢获得98%高产率2-甲基四氢呋喃。然而该技术仅适用于固定床类反应器,且对更普遍的乙酰丙酸等酸性底物的转化和催化剂寿命等问题并未涉及。
综上来看,尽管乙酰丙酸及其酯类转化获得2-甲基四氢呋喃虽然已经取得了显著的进步,但是非贵金属的催化剂体系仍然面临催化活性低、反应温度高、产率低和底物适用性有限等问题。因此,探索一种新的催化体系从乙酰丙酸及其酯类化合物合成2-甲基四氢呋喃的方法,具有十分重要的现实意义。
技术实现要素:
本发明的目的在于提供一种2-甲基四氢呋喃的制备方法;
将乙酰丙酸或其酯类化合物、溶剂和铜镍双金属催化剂混合均匀后,加入到反应器中,在反应器中充入h2,加热反应器催化所述乙酰丙酸或其酯类化合物加氢制备2-甲基四氢呋喃;所述溶剂为烷烃类化合物。
进一步的,反应温度160-220℃。
进一步的,所述的乙酰丙酸或其酯类化合物与溶剂的质量比为(0.01-0.1):1,氢气压力1-5mpa,搅拌转速400-800rpm,反应时间1-5h。
进一步的,所述烷烃类溶剂为c5-c10长链烷烃和环烷烃。
进一步的,所述溶剂为正己烷。
进一步的,所述催化剂铜镍双金属非均相催化剂,载体为zro2、al2o3或tio2。
所述双金属催化剂采用浸渍法获得。
所述双金属催化剂的制备方法如下:将1.7g载体(al2o3)和0.495g六水合硝酸镍和0.760g三水合硝酸铜置于50ml圆底烧瓶中加入20ml水,700rpm搅拌12h,45°c下旋蒸至糊状,置于105°c烘箱中干燥12h。充分研磨成粉末状,置于马弗炉中400°c煅烧4h。初温25°c,7°c/min升至400°c,保持4h。最后放置于管式炉中进行还原处理,10%h2/n2,10°c/min升温至500°c,保持3h,自然降温。得到反应活性最大的10cu-5ni/al2o3催化剂。
本发明的优点在于:本发明采用浸渍法制备出的双金属催化剂10cu-5ni/al2o3,能够一步加氢乙酰丙酸乙酯到2-甲基四氢呋喃,选择性高,没有中间体γ-戊内酯,也几乎无副产物(戊酸乙酯)产生。更重要的是,本发明第一次报道了使用烷烃类溶剂的铜镍双金属催化体系可以高选择性、高效率的将乙酰丙酸及其酯类化合物一步加氢还原至2-甲基四氢呋喃,在该催化体系中,该溶剂能够极大地促进反应原料和中间体在催化剂表面的吸附作用,有效地降低了反应关键步骤转化的反应活化能,从而降低整个反应的反应温度,体现了溶剂在该催化体系中的重要作用。另一方面,烷烃类溶剂的沸点较低,使得反应后的产物分离步骤可以在低温下进行,大大节省了后续的分离能耗,为生物质平台化合物乙酰丙酸及其酯类化合物的工业化应用奠定了极为重要的基础。
附图说明
图1为本发明产品2-甲基四氢呋喃的合成示意图。
图2为本发明实施例1所得产物的气相谱图。
图3为本发明合成的10cu-5ni双金属催化剂的tem图。
图4为不同溶剂的溶氢能力。
图5为催化剂对不同底物和中间体的吸附。
具体实施方式
下面结合实施例对本发明作进一步的描述。
催化剂载体
实施例1
将120mg10cu-5ni/al2o3(cu含量10%wt,ni含量5%wt),1mmol乙酰丙酸乙酯,12ml正己烷置于25ml高压反应釜中,充入4mpah2,180oc下以800rmp的搅拌速度反应4h,反应产物为2-甲基四氢呋喃,通过气相色谱分析,产率接近98%。
实施例2
与实施例1相同,所不同的是:用10cu-5ni/tio2代替实施例1中的10cu-5ni/al2o3检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为14%。
实施例3
与实施例1相同,所不同的是:用10cu-5ni/sio2代替实施例1中的10cu-5ni/al2o3检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为3%。
实施例4
与实施例1相同,所不同的是:用10cu-5ni/zro2代替实施例1中的10cu-5ni/al2o3检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为82%。
不同cu-ni比例
实施例5
与实施例1相同,所不同的是:cu含量为5%wt的5cu-10ni/al2o3代替实施例1中的10cu-5ni/al2o3检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为93%。
实施例6
与实施例1相同,所不同的是:cu含量为15%wt的15cu/al2o3代替实施例1中的10cu-5ni/al2o3检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为70%。
实施例7
与实施例1相同,所不同的是:ni含量为15%wt的15ni/al2o3代替实施例1中的10cu-5ni/al2o3,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为35%。
实施例8
与实施例1相同,所不同的是:cu含量为12%wt的12cu-3ni/al2o3代替实施例1中的10cu-5ni/al2o3检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为90%。
实施例9
与实施例1相同,所不同的是:cu含量为3%wt的3cu-12ni/al2o3代替实施例1中的10cu-5ni/al2o3检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为64%。
不同溶剂:
实施例10
与实施例1相同,所不同的是:用异丙醇代替实施例1中的正己烷,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为40%。
实施例11
与实施例1相同,所不同的是:用正丙醇代替实施例1中的正己烷,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为17%。
实施例12
与实施例1相同,所不同的是:用1,4-二氧六环代替实施例1中的正己烷,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为1%。
实施例13
与实施例1相同,所不同的是:用四氢呋喃代替实施例1中的正己烷,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为0%。
实施例14
与实施例1相同,所不同的是:用环戊烷代替实施例1中的正己烷,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为95%。
实施例15
与实施例1相同,所不同的是:用正庚烷代替实施例1中的正己烷,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为94%。
实施例16
与实施例1相同,所不同的是:用正辛烷代替实施例1中的正己烷,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为92%。
实施例17
与实施例1相同,所不同的是:用正癸烷代替实施例1中的正己烷,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为90%。
从实施例1和10-17可以看出,低极性烷烃溶剂的使用可以促进反应产率的大幅提升(产率从常规溶剂1%产率提升烷烃溶剂>90%)。深入研究表明,烷烃溶剂促进效应有两方面原因:1)如附图4所示,烷烃溶剂相比于其他常规加氢反应所需溶剂,具有更高的氢气溶解能力,这有助于提高氢气在溶剂中的浓度,从而提高反应速率;2)低极性烷烃溶剂和具有较高极性的催化剂表面相比,前者与反应的原/中间体的相互作用弱,与底物在催化剂表面几乎无竞争吸附,催化剂极性表面对原料/中间体的吸附能力则越强,则可以促进了固体催化剂和原料、中间体的相互作用。如附图5所示,在低极性的烷烃溶剂中,催化剂对原料和中间体的吸附效应远远大于在其他类型的溶剂中。通过计算可知,在实施例1中,在正己烷溶剂中,催化剂可将反应的决速步—gvl的开环的活化能降低至48.9kj/mol。这些因素也解释了在前人工作中同样使用cu基催化剂却难以降低反应温度和取得较高反应产率的原因。
催化剂用量
实施例18
与实施例1相同,所不同的是:用80mg12cu-3ni/al2o3代替实施例1中的120mg10cu-5ni/al2o3检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为76%。
实施例19
与实施例1相同,所不同的是:140mg12cu-3ni/al2o3代替实施例1中的120mg10cu-5ni/al2o3检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为95%。
反应温度
实施例20
与实施例1相同,所不同的是:采用140℃代替实施例1中的180℃,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为7%。
实施例21
与实施例1相同,所不同的是:采用160℃代替实施例1中的180℃,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为71%。
实施例22
与实施例1相同,所不同的是:采用200℃代替实施例1中的180℃,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为96%。
实施例23
与实施例1相同,所不同的是:采用220℃代替实施例1中的180℃,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为91%。
氢气压力
实施例24
与实施例1相同,所不同的是:采用1mpa代替实施例1中的4mpa,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为56%。
实施例25
与实施例1相同,所不同的是:采用5mpa代替实施例1中的4mpa,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为97%。
反应时间
实施例26
与实施例1相同,所不同的是:采用1h代替实施例1中的4h,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为89%。
实施例27
与实施例1相同,所不同的是:采用5h代替实施例1中的4h,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为95%。
底物拓展
实施例28
与实施例1相同,所不同的是:采用乙酰丙酸代替实施例1中的乙酰丙酸乙酯,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为98%。
实施例29
与实施例1相同,所不同的是:采用乙酰丙酸甲酯代替实施例1中的乙酰丙酸乙酯,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为99%。
实施例30
与实施例1相同,所不同的是:采用乙酰丙酸丙酯代替实施例1中的乙酰丙酸甲酯,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为97%。
实施例31
与实施例1相同,所不同的是:采用乙酰丙酸异丙酯代替实施例1中的乙酰丙酸甲酯,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为96%。
实施例32
与实施例1相同,所不同的是:采用乙酰丙酸丁酯代替实施例1中的乙酰丙酸甲酯,检测结果为,本发明实施例得到2-甲基四氢呋喃的产率为96%。
- 还没有人留言评论。精彩留言会获得点赞!