单核细胞增生李斯特菌血清型4h多重PCR检测试剂盒的制作方法
本发明涉及一种生物检测试剂盒,特别是涉及一种单核细胞增生李斯特菌血清型4h的多重pcr检测试剂盒。
背景技术:
单核细胞增生李斯特菌(listeriamonocytogenes,lm)是一种重要的食源性人兽共患病原菌,其对食品安全及人类健康的危害已经引起很多国家的高度重视。单核细胞增生李斯特菌引起的人和动物的李斯特菌病具有低发病率、高致死率的特点。据统计,人李斯特菌病发病率约每百万人0.1~11.3例,死亡率为20%~30%。
单核细胞增生李斯特菌包括4个进化谱系,14种血清型。其中1/2a、1/2b和4b是引起李斯特菌病的主要血清型,而4h是我国发现的一种新的李斯特菌血清型。血清型4h的单核细胞增生李斯特菌通常具有超强毒力,李斯特菌病的爆发多与超强毒力菌株的出现有关,因此,建立单核细胞增生李斯特菌尤其是针对血清型4h的快速、有效的检测方法对于李斯特菌的监测与控制是非常必要的。
目前食品中单核细胞增生李斯特菌的检测方法通常参照食品安全国家标准gb4789.30-2016,在样品增菌培养及选择性培养后进行传统的生化鉴定实验。该方法能够较为准确地检出单核细胞增生李斯特菌,但同时也存在着耗时耗力,且不能快速区分超强毒力单核细胞增生李斯特菌的不足。
因此,提供一种新的快速便捷的检测方法十分必要。
技术实现要素:
鉴于以上所述现有技术的缺点,本发明的目的在于提供一种单核细胞增生李斯特菌血清型4h的多重pcr检测试剂盒,用于解决现有技术中无法直接检测单核细胞增生李斯特菌血清型4h的问题,该方法操作简单,准确度高,耗时短,满足现在食品安全检测的需要。
为实现上述目的及其他相关目的,本发明的第一方面提供了基因lmo1210以及基因xysn_1693在制备检测单核细胞增生李斯特菌血清型4h检测试剂盒中的用途。
将基因lmo1210以及基因xysn_1693用于制备单核细胞增生李斯特菌血清型4h检测试剂,是指将基因lmo1210以及基因xysn_1693作为检测靶标应用于单核细胞增生李斯特菌血清型4h的检测。
本发明的一些实施方式中,基于所述基因lmo1210以及基因xysn_1693的序列,筛选特异性针对基因lmo1210以及基因xysn_1693扩增引物对从而作为增生李斯特菌血清型4h检测试剂。
上述用途应当是基因lmo1210以及基因xysn_1693共同作用的结果,并非是单个基因分别发挥作用。
本发明提供一种单核细胞增生李斯特菌血清型4h的多重pcr检测试剂盒,所述试剂盒中包括基因lmo1210检测引物以及基因xysn_1693检测引物。
优选地,所述基因lmo1210检测引物包括核苷酸序列如seqidno.3所示的正向引物和核苷酸序列如seqidno.4所示的反向引物。
进一步地,基因lmo1210检测引物扩增区域核苷酸序列如seqidno:5所示。检测片段长度为211bp。
优选地,所述基因xysn_1693检测引物包括核苷酸序列如seqidno.6所示的正向引物和核苷酸序列如seqidno.7所示的反向引物。
进一步地,基因xysn_1693检测引物扩增区域核苷酸序列如seqidno:8所示。检测片段长度为429bp。
本发明采用pcr技术对基因lmo1210以及基因xysn_1693进行检测,根据其扩增情况可判断检测对象是否属于单核细胞增生李斯特菌血清型4h。因此,引物的设计是本发明的试剂盒的关键。
基于本发明所述试剂盒是采用pcr技术来进行检测的,所以试剂盒中还可以包括其他一些pcr所需要的常规试剂,如:ddh2o、dntp、pcrbuffer、rtaq酶、样品基因组dna提取试剂等常用pcr反应试剂中的一种或多种。由于此类pcr常用试剂均可经市场途径单独购得或者自行配置,因此具体需要将哪些试剂装配入试剂盒,可以根据客户实际需要配置,为方便起见,也可全部装配入试剂盒。
本发明的试剂盒,可以是含有独立包装的引物对,也可以是含有配置好的含有引物对的pcr检测液。
所述pcr检测液可自行配置,也可直接以市售的不含引物的通用pcr反应液加入引物获得。例如,所述试剂盒中还可以含有ddh2o、dntp、pcrbuffer、rtaq酶。加入本发明的引物、待检样本dna提取物或者样本菌液即可获得pcr反应体系。
优选地,所述试剂盒中还可含有阳性对照。所述阳性对照为含有基因lmo1210和/或基因xysn_1693表达的dna样本。
优选地,所述试剂盒中还可含有阴性对照。阴性对照可为无基因lmo1210和基因xysn_1693表达的dna样本。
本发明的第二方面提供了上述多重pcr检测试剂盒的检测方法,所述方法包括以下步骤:
(1)提取样品基因组dna;
(2)加样:将样品基因组dna、阳性对照和/或阴性对照分别加入装有pcr反应体系的pcr管中,获得对应的样品反应管、阳性反应管和/或阴性反应管,所述pcr反应体系中含有前述基因lmo1210以及基因xysn_1693检测引物;
(3)pcr反应:反应管置于pcr仪上,设置循环参数,进行pcr反应;
(4)pcr反应结束后,分析结果。
上述方法为非疾病诊断目的方法。
进一步地,所述步骤(1)中,提取样品基因组dna为现有技术,本领域技术人员可以根据现有操作方法制备。
进一步地,所述步骤(3)中pcr反应条件为:95℃预变性5min;95℃变性30s、55℃退火30s、72℃延伸30s,35个循环;72℃终止10min。
进一步地,所述步骤(4)中结果分析判定方法如下:同时扩增出211bp和429bp条带时,判定为血清型4h的单核细胞增生李斯特菌阳性;仅扩增出211bp条带时,判定为其他血清型单核细胞增生李斯特菌阳性;无条带则为单核细胞增生李斯特菌阴性。
本发明的第三方面提供了上述试剂盒在制备基因lmo1210以及基因xysn_1693检测产品中的用途。
所述检测产品用于检测单核细胞增生李斯特菌血清型4h。
如上所述,本发明的单核细胞增生李斯特菌血清型4h的多重pcr检测试剂盒,具有以下有益效果:
本发明利用了pcr扩增技术,建立了利用两对引物快速检测单核细胞增生李斯特菌血清型4h的多重pcr方法,该方法具有特异性好,灵敏度高,检测速度快,易与操作和判定结果的优点。经李斯特菌属和非李斯特菌属菌株的实际样本检测,未出现假阳性结果,具有良好的特异性。
附图说明
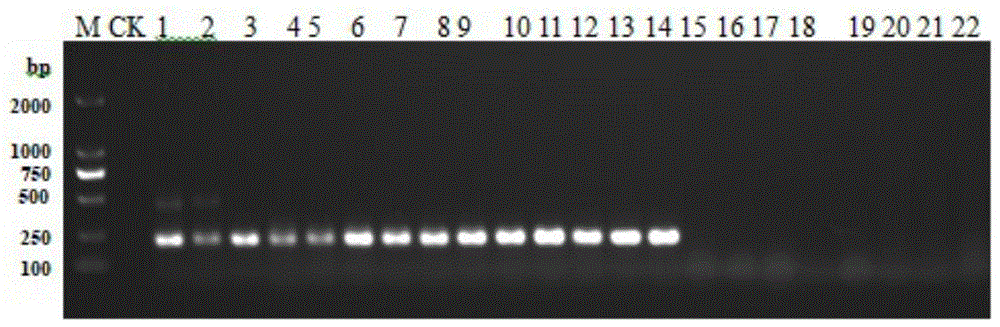
图1a和1b为本发明实施例1中的多重pcr方法特异性评价实验结果。其中m.dl2000;ck.阴性对照;1-2.单核细胞增生李斯特菌血清型4h菌株;3-14.依次为血清型1/2a、1/2b、1/2c、3a、3b、3c、4a、4ab、4b、4c、4d和7的单核细胞增生李斯特菌;15.伊氏李斯特菌;16.无害李斯特菌;17.塞氏李斯特菌;18.格氏李斯特菌;19.威氏李斯特菌;20.肠炎沙门菌;21.鸡白痢沙门菌;22.鼠伤寒沙门菌,23.副溶血弧菌;24.大肠杆菌;25.金黄色葡萄球菌;26.空肠弯曲菌;27.结肠弯曲菌。
图2为本发明实施例1中的多重pcr方法灵敏度评价的实验结果。其中m.dl2000;ck.阴性对照;1-9.单核细胞增生李斯特菌血清型4h菌株xysn基因组dna浓度分别为100ng/μl、10ng/μl、1ng/μl、100pg/μl、10pg/μl、1pg/μl、100fg/μl、10fg/μl和1fg/μl。
图3a和3b为本发明实施例2中的不同来源样品中单核细胞增生李斯特菌多重pcr检测结果。其中m.dl2000;ck.阴性对照;1.单核细胞增生李斯特菌xysn(血清型4h);2.单核细胞增生李斯特菌egd-e(血清型1/2a);3-37.不同来源样品中分离的单核细胞增生李斯特菌。
具体实施方式
以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所公布的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
在进一步描述本发明具体实施方式之前,应理解,本发明的保护范围不局限于下述特定的具体实施方案;还应当理解,本发明实施例中使用的术语是为了描述特定的具体实施方案,而不是为了限制本发明的保护范围;在本发明说明书和权利要求书中,除非文中另外明确指出,单数形式“一个”、“一”和“这个”包括复数形式。
当实施例给出数值范围时,应理解,除非本发明另有说明,每个数值范围的两个端点以及两个端点之间任何一个数值均可选用。除非另外定义,本发明中使用的所有技术和科学术语与本技术领域技术人员通常理解的意义相同。除实施例中使用的具体方法、设备、材料外,根据本技术领域的技术人员对现有技术的掌握及本发明的记载,还可以使用与本发明实施例中所述的方法、设备、材料相似或等同的现有技术的任何方法、设备和材料来实现本发明。
除非另外说明,本发明中所公开的实验方法、检测方法、制备方法均采用本技术领域常规的分子生物学、生物化学、染色质结构和分析、分析化学、细胞培养、重组dna技术及相关领域的常规技术。这些技术在现有文献中已有完善说明,具体可参见sambrook等molecularcloning:alaboratorymanual,secondedition,coldspringharborlaboratorypress,1989andthirdedition,2001;ausubel等,currentprotocolsinmolecularbiology,johnwiley&sons,newyork,1987andperiodicupdates;theseriesmethodsinenzymology,academicpress,sandiego;wolffe,chromatinstructureandfunction,thirdedition,academicpress,sandiego,1998;methodsinenzymology,vol.304,chromatin(p.m.wassarmananda.p.wolffe,eds.),academicpress,sandiego,1999;和methodsinmolecularbiology,vol.119,chromatinprotocols(p.b.becker,ed.)humanapress,totowa,1999等。
以下实例中,所有引物均由南京金斯瑞生物科技有限公司合成;细菌dna提取试剂盒购自天根生化科技(北京)有限公司;dna分子量markerdl2000、2×taqmastermix购自南京诺唯赞生物科技有限公司;单核细胞增生李斯特菌血清型诊断试剂盒购自日本生研。
实施例1:单核细胞增生李斯特菌血清型4h的多重pcr检测方法的建立
1)引物
从genebank中下载单核细胞增生李斯特菌全基因组序列进行比对,最终确定两个特异性靶基因lmo1210和xysn_1693。分析并确定引物从中选择最佳检测引物对,两对检测用引物序列及相应扩增产物长度如表1所示。
seqidno:1lmo1210核苷酸序列
atgacaaaaagatcatccaaatcattattactatttatggcaatgggacttgtttctggactactttccccgattcaaacgtcgattaatagccaacttcggctaactgtcggttctccttttgtggcatcatttatttcctttttagttgggacgactttgcttacactggtttgtttaatcgttgagcgtcgtttgacttttcaactgaaaggtgtcggccgaattccttggtgggttttcactggcggtgcgcttggagtgctcttcgtaacttctaacattttacttttaccattactcggctcagcaatgacggttgttttagcgctttgtgggcaaatgattattgcacttattattgatcattttggttttttcggggttattcctcatccaattaaccgttatcgtatgattggtgttttattaatgcttattggtgtatttttaattcaacgtttttaa
seqidno:2xysn_1693核苷酸序列
atgaagaaagacataaaaaagagatacattagtttaatagtaattggggcattgatggtgggtatgacctttccttatggtactaccgtacatgcagacagtgttcaaagtgataacttatatccaagtgatcaagtgaatactgataatcagtttattgtcttggatgattacactataacggatgaggaaggtaatatagttaatgaggagcagaataaaaattcacatcttcttaagtcagctacagggttccactacaaaacattgtctcagtcaatgaaaaaaggtagcagaacttatttgggaaaaaagaaatataaaaaaggctttgattttagtgtgaaagtaatcgtaaaaggtgtatatgttaacttgggaggatatgcatcaaaaactggatattataaagagtataaacaaaatgtaaagataactgttaaagttaaaaaatatgaaaatggatcaggaaagtatgttggaacctacacctatacatctaatacttcatatgtagatagaattccagtataa
表1单核细胞增生李斯特菌血清型4h的多重pcr检测引物
2)基因组dna模板制备
取菌液2ml,按照常规细菌基因组dna提取方法制备细菌基因组dna。基因组dna提取为分子生物学领域常用方法,常规市售各种细菌dna提取试剂盒均可实现基因组dna模板的提取。
3)反应体系及条件
pcr反应体系为:2×taqmastermix12.5μl;10μm引物lmo1210f、lmo1210r、xysn_1693f和xysn_1693r各1μl;基因组dna模板1μl;ddh2o补齐至25μl。pcr扩增反应条件为95℃预变性5min;95℃变性30s、55℃退火30s、72℃延伸30s,35个循环;72℃终止10min;4℃保存。
4)结果判定
基因lmo1210正反向引物扩增区域核苷酸序列如seqidno:5所示,检测片段长度为211bp;
seqidno:5lmo1210正反向引物扩增区域核苷酸序列
gtcgtttgacttttcaactgaaaggtgtcggccgaattccttggtgggttttcactggcggtgcgcttggagtgctcttcgtaacttctaacattttacttttaccattactcggctcagcaatgacggttgttttagcgctttgtgggcaaatgattattgcacttattattgatcattttggttttttcggggttattcctcatccaat
基因xysn_1693正反向引物扩增区域核苷酸序列如seqidno:8所示。检测片段长度为429bp。
seqidno:8xysn_1693正反向引物扩增区域核苷酸序列
tccaacatactttcctgatccattttcatattttttaactttaacagttatctttacattttgtttatactctttataatatccagtttttgatgcatatcctcccaagttaacatatacaccttttacgattactttcacactaaaatcaaagccttttttatatttcttttttcccaaataagttctgctaccttttttcattgactgagacaatgttttgtagtggaaccctgtagctgacttaagaagatgtgaatttttattctgctcctcattaactatattaccttcctcatccgttatagtgtaatcatccaagacaataaactgattatcagtattcacttgatcacttggatataagttatcactttgaacactgtctgcatgtacggtagtaccataaggaaaggtcatacccaccat
判定方法为:同时扩增出211bp和429bp条带时,判定为血清型4h的单核细胞增生李斯特菌阳性;仅扩增出211bp条带时,判定为其他血清型单核细胞增生李斯特菌阳性;无条带则为单核细胞增生李斯特菌阴性。
5)多重pcr方法特异性评价实验
表2共涉及细菌27株。其中李斯特菌属细菌19株,包括单核细胞增生李斯特菌血清型4h菌株2株,其他血清型的单核细胞增生李斯特菌12株,伊氏李斯特菌、无害李斯特菌、塞氏李斯特菌、格氏李斯特菌和威氏李斯特菌各1株;非李斯特菌属细菌8株,其中肠炎沙门菌、鸡白痢沙门菌、鼠伤寒沙门菌、副溶血弧菌、大肠杆菌、金黄色葡萄球菌、空肠弯菌和结肠弯曲菌各1株。
表2单核细胞增生李斯特菌血清型4h的多重pcr检测方法特异性评价实验参考菌株
以表2中的27株细菌的基因组dna作为模板。在pcr小管中分别加入12.5μl2×taqmastermix,基因组dna模板1μl,10μm引物lmo1210f、lmo1210r、xysn_1693f和xysn_1693r各1μl,用ddh2o补齐到25μl并混匀,同时设置一个阴性对照。多重pcr反应结束后进行琼脂糖凝胶电泳,分析结果。
图1a和图1b所示为多重pcr方法特异性评价实验结果。其中m.dl2000;ck.阴性对照;1-2.单核细胞增生李斯特菌血清型4h菌株;3-14.依次为血清型1/2a、1/2b、1/2c、3a、3b、3c、4a、4ab、4b、4c、4d和7的单核细胞增生李斯特菌;15.伊氏李斯特菌;16.无害李斯特菌;17.塞氏李斯特菌;18.格氏李斯特菌;19.威氏李斯特菌;20.肠炎沙门菌;21.鸡白痢沙门菌;22.鼠伤寒沙门菌;23.副溶血弧菌;24.大肠杆菌;25.金黄色葡萄球菌;26.空肠弯曲菌;27.结肠弯曲菌。
可见,2株血清型4h的单核细胞增生李斯特菌均扩增出429bp和211bp特异性条带;12株其他血清型的单核细胞增生李斯特菌均仅扩增出221bp特异性条带;而13株阴性菌株均无特异性扩增条带。以上结果表明本发明多重pcr方法易于操作和结果判定且具有良好的特异性。
6)多重pcr方法灵敏度评价实验
提取单核细胞增生李斯特菌血清型4h菌株xysn的基因组dna并测出初始浓度,以ddh2o调整浓度为100ng/μl,随后进行10倍连续梯度稀释至1fg/μl置于冰上备用。在pcr小管中分别分别加入12.5μl2×taqmastermix,取各稀释度的基因组dna1μl作为模板,10μm引物lmo1210f、lmo1210r、xysn_1693f和xysn_1693r各1μl,用ddh2o补齐到25μl并混匀,同时设置一个阴性对照。多重pcr反应结束后进行琼脂糖凝胶电泳,分析结果。
结果如图2所示,其中m.dl2000;ck.阴性对照;1-9.单核细胞增生李斯特菌血清型4h菌株xysn基因组dna浓度分别为100ng/μl、10ng/μl、1ng/μl、100pg/μl、10pg/μl、1pg/μl、100fg/μl、10fg/μl和1fg/μl。可见,多重pcr方法对于单核细胞增生李斯特菌血清型4h菌株的基因组dna检测灵敏度为100fg/μl,说明该方法具有较高的灵敏度。
实施例2试剂盒的制备
分别合成基因lmo1210检测引物以及基因xysn_1693检测引物,具体见表1。
上述引物可以独立包装也可以分别单独包装,其用量采用本领域技术人员所知悉的常规用量即可。
也就是说,本发明的试剂盒,可以是含有上述独立包装的各组引物对,也可以是含有配置好的含有各组引物pcr检测混合液。
进一步地,上述试剂盒中还可以包括其他一些pcr所需要的常规试剂,如:ddh2o、dntp、pcrbuffer、rtaq酶、样品基因组dna提取试剂等常用pcr反应试剂中的一种或多种。
实施例3:不同来源样品中单核细胞增生李斯特菌多重pcr鉴定
利用本发明所建立的多重pcr方法,对前期从零售猪肉(包括冷鲜肉、熟肉制品)、羊场及污水等样品中分离的35株单核细胞增生李斯特菌进行鉴定。通过玻片凝集实验对这35株细菌的血清型进行鉴定。菌株编号及血清型等信息如表3所示。
表3不同来源样品中单核细胞增生李斯特菌分离株
菌株基因组dna模板提取方法按照常规细菌dna提取试剂盒方法进行。利用实施例2制备的试剂盒对dna进行扩增:在pcr小管中分别加入12.5μl2×taqmastermix,基因组dna模板1μl,10μm引物lmo1210f、lmo1210r、xysn_1693f和xysn_1693r各1μl,用ddh2o补齐到25μl并混匀,同时设置一个阴性对照。多重pcr反应结束后进行琼脂糖凝胶电泳,分析结果。
多重pcr鉴定结果如图3a和3b所示,这35株细菌均为单核细胞增生李斯特菌,与前期分菌鉴定结果一致,说明了多重pcr检测方法的准确度较高。同时,通过多重pcr方法可知35株细菌中血清型4h的单核细胞增生李斯特菌有两株,分别为16e和ha-p161020-d14。通过商品化诊断血清可以对包括1/2a、1/2b、1/2c等在内的13种单核细胞增生李斯特菌血清型进行鉴定,但不包含近期报道的血清型4h,多重pcr方法是对其的补充且未出现误诊。
本发明相较于传统方法的优势在于,样品经增菌和选择性培养后可直接进行多重pcr鉴定,3h内即可判定结果,无需糖发酵试验初筛以及后续的生化实验鉴定,节省时间,且成本更低、操作简单,适合应用到样品的检测中。
以上的实施例是为了说明本发明公开的实施方案,并不能理解为对本发明的限制。此外,本文所列出的各种修改以及发明中方法、组合物的变化,在不脱离本发明的范围和精神的前提下对本领域内的技术人员来说是显而易见的。虽然已结合本发明的多种具体优选实施例对本发明进行了具体的描述,但应当理解,本发明不应仅限于这些具体实施例。事实上,各种如上所述的对本领域内的技术人员来说显而易见的修改来获取发明都应包括在本发明的范围内。
序列表
<110>扬州大学
<120>单核细胞增生李斯特菌血清型4h多重pcr检测试剂盒
<160>8
<170>siposequencelisting1.0
<210>1
<211>468
<212>dna
<213>人工序列(artificialsequence)
<400>1
atgacaaaaagatcatccaaatcattattactatttatggcaatgggacttgtttctgga60
ctactttccccgattcaaacgtcgattaatagccaacttcggctaactgtcggttctcct120
tttgtggcatcatttatttcctttttagttgggacgactttgcttacactggtttgttta180
atcgttgagcgtcgtttgacttttcaactgaaaggtgtcggccgaattccttggtgggtt240
ttcactggcggtgcgcttggagtgctcttcgtaacttctaacattttacttttaccatta300
ctcggctcagcaatgacggttgttttagcgctttgtgggcaaatgattattgcacttatt360
attgatcattttggttttttcggggttattcctcatccaattaaccgttatcgtatgatt420
ggtgttttattaatgcttattggtgtatttttaattcaacgtttttaa468
<210>2
<211>534
<212>dna
<213>人工序列(artificialsequence)
<400>2
atgaagaaagacataaaaaagagatacattagtttaatagtaattggggcattgatggtg60
ggtatgacctttccttatggtactaccgtacatgcagacagtgttcaaagtgataactta120
tatccaagtgatcaagtgaatactgataatcagtttattgtcttggatgattacactata180
acggatgaggaaggtaatatagttaatgaggagcagaataaaaattcacatcttcttaag240
tcagctacagggttccactacaaaacattgtctcagtcaatgaaaaaaggtagcagaact300
tatttgggaaaaaagaaatataaaaaaggctttgattttagtgtgaaagtaatcgtaaaa360
ggtgtatatgttaacttgggaggatatgcatcaaaaactggatattataaagagtataaa420
caaaatgtaaagataactgttaaagttaaaaaatatgaaaatggatcaggaaagtatgtt480
ggaacctacacctatacatctaatacttcatatgtagatagaattccagtataa534
<210>3
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>3
gtcgtttgacttttcaactga21
<210>4
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>4
attggatgaggaataaccccg21
<210>5
<211>211
<212>dna
<213>人工序列(artificialsequence)
<400>5
gtcgtttgacttttcaactgaaaggtgtcggccgaattccttggtgggttttcactggcg60
gtgcgcttggagtgctcttcgtaacttctaacattttacttttaccattactcggctcag120
caatgacggttgttttagcgctttgtgggcaaatgattattgcacttattattgatcatt180
ttggttttttcggggttattcctcatccaat211
<210>6
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>6
tccaacatactttcctgatcca22
<210>7
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>7
atggtgggtatgacctttcctt22
<210>8
<211>429
<212>dna
<213>人工序列(artificialsequence)
<400>8
tccaacatactttcctgatccattttcatattttttaactttaacagttatctttacatt60
ttgtttatactctttataatatccagtttttgatgcatatcctcccaagttaacatatac120
accttttacgattactttcacactaaaatcaaagccttttttatatttcttttttcccaa180
ataagttctgctaccttttttcattgactgagacaatgttttgtagtggaaccctgtagc240
tgacttaagaagatgtgaatttttattctgctcctcattaactatattaccttcctcatc300
cgttatagtgtaatcatccaagacaataaactgattatcagtattcacttgatcacttgg360
atataagttatcactttgaacactgtctgcatgtacggtagtaccataaggaaaggtcat420
acccaccat429
- 还没有人留言评论。精彩留言会获得点赞!