一种中分子量段黄芪多糖、制备方法及其应用与流程
本发明涉及生物医药制造技术领域,具体涉及一种中分子量段黄芪多糖的制备方法及其应用。
背景技术:
黄芪是中医临床应用最为广泛的大宗中药材之一,由于黄芪疗效确切,适用范围广,为历代医家所推崇。黄芪性味甘温,具有补气升阳、益卫固表、利水消肿和托疮生肌等作用;临床上对循环系统、神经系统、消化系统、呼吸系统、内分泌和血液系统疾病均有较好疗效。药理学研究显示,黄芪提取物或者单体化合物在抗炎、免疫调节、抗肿瘤、心肌缺血保护、糖尿病、抗氧化,抗衰老等方面均有明确的作用。从现代研究的角度看,黄芪的主要功效是调节免疫功能,黄芪对免疫功能的调节作用与其传统应用中的“益气固表”作用密切相关,《黄帝内经·灵枢》中曾说:“卫气不营,邪气居之”,明确指出“卫气”是机体内与邪气相抗衡的一种防御机制,现代研究认为卫气虚弱主要表现为免疫功能低下,因此,黄芪的核心功效是对免疫功能的影响。现有技术中有大量研究均证实黄芪多糖是黄芪的主要活性组分之一。天然黄芪多糖分子量较高,平均分子量在10万以上,不能被人体正常消化吸收,因此本申请提出一种中分子量段黄芪多糖、制备方法及其应用。
技术实现要素:
本发明的目的是为了克服现有技术中的问题,提供一种中分子量段黄芪多糖、制备方法及其应用。
本发明的目的之一是提供一种中分子量段黄芪多糖,由黄芪粗多糖水解获得,该中分子量段黄芪多糖的分子量范围在103-104道尔顿。
本发明的目的之二提供一种中分子量段黄芪多糖的制备方法,具体如下:先将黄芪粗多糖热水溶解,加酸并水浴加热,然后加入碱液调节ph至中性,待水解液浓缩干燥后,粉碎过筛,得黄芪多糖水解物,所述黄芪多糖水解物中中分子量段黄芪多糖的含量不小于50%。
较佳地,待水解液浓缩后干燥前还进行了透析处理,获得纯化后的中分子量段黄芪多糖。
较佳地,酸为能够水解糖苷键的有机酸和无机酸。
较佳地,酸为盐酸,调至黄芪粗多糖溶液中盐酸浓度为0.03~0.30mol/l,水浴加热温度为10~100℃,时间为1~8h。
较佳地,酸为三氟乙酸,调至黄芪粗多糖溶液中三氟乙酸浓度为0.05~0.30mol/l的,水浴加热温度为10~100℃,时间为1~8h。
较佳地,所述黄芪粗多糖的提取方法如下:将黄芪药材粉碎后水温浸提取,浓缩提取液,除蛋白,离心,上清液浓缩后,经80%乙醇洗涤沉淀,得到黄芪粗多糖。
本发明的目的之三在于上述中分子量段黄芪多糖在制备用于改善肠黏膜免疫及肠道微生态系统功能的药物或食品中的应用。
与现有技术相比,本发明的有益效果是:本发明中中分子量段黄芪多糖的分子量范围在103~104道尔顿之间,分子扩散速度较快,易于被肠道菌利用,也更易于和肠粘膜细胞相互作用,能更好的实现调节肠粘膜免疫及肠道微生态系统的功能;
本发明将天然黄芪多糖水解以获得中分子量段的黄芪多糖,且采用酸水解的方法能将黄芪多糖水解为中分子量段的黄芪多糖,又不至于将黄芪多糖彻底降解为单糖或者寡糖,经本发明的酸水解方法获得的黄芪多糖水解产物中中分子量段黄芪多糖含量不低于50%;
本发明还通过实验证明了本发明的黄芪多糖水解后产生的中分子量段黄芪多糖在调节肠黏膜免疫和肠道微生态系统方面比天然黄芪多糖效应更好,增强了黄芪多糖的保健效果。本发明中的黄芪多糖酸水解工艺简单,易于实现工业化生产。
附图说明
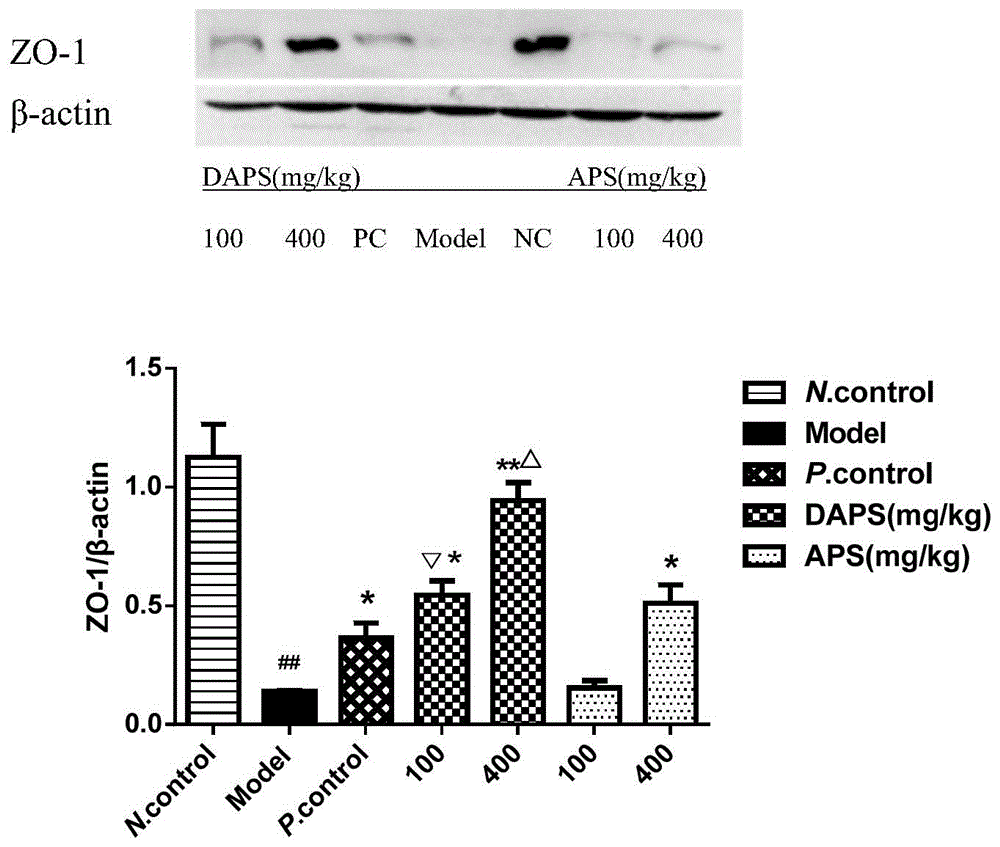
图1为本发明aps和daps处理对免疫抑制小鼠小肠组织小肠组织zo-1的影响(
图2为本发明小鼠肠道菌群微生态系统多样性指数和丰富度指数(n=3);
图2a为本发明aps、daps处理后小鼠肠道菌群的chao指数;
图2b为本发明aps、daps处理后小鼠肠道菌群的ace指数;
图2c为本发明aps、daps处理后小鼠肠道菌群的shannon指数;
图2d为本发明aps、daps处理后小鼠肠道菌群的simpson指数;
图3为本发明aps、daps处理后小鼠肠道菌群的pcoa分析图(n=3);
图4为本发明aps、daps处理后对小鼠肠道菌群代谢产物scfa的影响(
图4a为aps、daps处理后对小鼠肠道菌群代谢产物乙酸的影响。
图4b为aps、daps处理后对小鼠肠道菌群代谢产物丙酸的影响。
图4c为aps、daps处理后对小鼠肠道菌群代谢产物丁酸的影响。
具体实施方式
下面结合附图以及实施例对本发明的具体实施方式进行详细描述,但应当理解本发明的保护范围并不受具体实施方式的限制。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
以制备含活性成分为中分子量段黄芪多糖片剂1000片为例所用原料和辅料及其质量配比如下:
1、黄芪多糖的提取:将黄芪药材粉碎后水温浸提取,浓缩提取液,通过sevag法除蛋白,离心,上清液浓缩后,80%乙醇沉淀,沉淀洗涤得到黄芪粗多糖;
2、黄芪粗多糖的酸水解:黄芪粗多糖热水溶解后,加入盐酸至浓度为0.16mol/l(质量百分比浓度为0.05%w/w),在80℃水浴3h,然后加入等当量naoh溶液调节ph至中性,水解液浓缩至浸膏状,干燥后粉碎、过筛得到富含分子量介于103~104道尔顿之间的中分子量段黄芪多糖产物。
以制备含活性成分为中分子量段黄芪多糖的片剂1000片为例所用原料和辅料及其质量配比如下:富含中分子量段黄芪多糖产物150g,玉米淀粉1450g,硬脂酸镁5g按制剂学片剂的常规工艺进行,每片重0.3g,每片含中分子量段黄芪多糖150mg。用法用量:口服,每次3片,一日三次,小儿酌减。
实施例2
以制备含活性成分为中分子量段黄芪多糖颗粒剂1000包为例所用原料和辅料及其质量配比如下:
1、黄芪多糖的提取:将黄芪药材粉碎后水温浸提取,浓缩提取液,通过sevag法除蛋白,离心,上清液浓缩后,80%乙醇沉淀,沉淀洗涤得到黄芪粗多糖;
2、黄芪粗多糖的酸水解:黄芪粗多糖热水溶解后,加入三氟乙酸调至浓度为0.1mol/l(0.8%w/w)在80℃水浴3h;在80℃水浴3h,然后加入等当量naoh溶液调节ph至中性,水解液浓缩后,分别用截留分子量为1kd和10kd的透析袋透析处理,干燥后粉碎、过筛获得纯化的分子量介于103~104道尔顿之间的中分子量段黄芪多糖产物。
以制备含活性成分为中分子量段黄芪多糖的颗粒剂1000包为例所用原料和辅料及其质量配比如下:中分子量段黄芪多糖产物450g,蔗糖粉2000g,糊精650g。按制剂学颗粒剂的常规工艺进行,每包重3g,含中分子量段黄芪多糖450mg。用法用量:口服,每次一袋,一天三次。
实施例3
以制备含活性成分为中分子量段黄芪多糖胶囊剂1000粒为例所用原料和辅料及其质量配比如下:
1、黄芪多糖的提取:将黄芪药材粉碎后水温浸提取,浓缩提取液,通过sevag法除蛋白,离心,上清液浓缩后,80%乙醇沉淀,沉淀洗涤得到黄芪粗多糖;
2、黄芪粗多糖的酸水解:黄芪粗多糖热水溶解后,加入盐酸调至浓度为0.16mol/l(0.5%)、80℃水浴6h,然后加入等当量naoh溶液调节ph至中性,水解液浓缩至浸膏状,干燥后粉碎、过筛得到富含分子量介于103~104道尔顿之间的中分子量段黄芪多糖产物。
以制备含活性成分为中分子量段黄芪多糖的颗粒剂1000包为例所用原料和辅料及其质量配比如下:中分子量段黄芪多糖产物150g,玉米淀粉150g。按制剂学胶囊剂的常规工艺进行,每粒重3g,含中分子量段黄芪多糖150mg。用法用量:口服,每次2粒,一天三次。
实施例4
以制备含活性成分为中分子量段黄芪多糖口服液1000粒为例所用原料和辅料及其质量配比如下:
1、黄芪多糖的提取:将黄芪药材粉碎后水温浸提取,浓缩提取液,通过sevag法除蛋白,离心,上清液浓缩后,80%乙醇沉淀,沉淀洗涤得到黄芪粗多糖;2、黄芪粗多糖的酸水解:黄芪粗多糖热水溶解后,加入三氟乙酸调至浓度为0.10mol/l(0.5%)、60℃水浴6h,然后加入等当量naoh溶液调节ph至中性,水解液浓缩后,分别用截留分子量为1kd和10kd的透析袋透析处理,干燥后粉碎、过筛获得纯化的分子量介于103~104道尔顿之间的中分子量段黄芪多糖产物。
以制备含活性成分为中分子量段黄芪多糖的口服液1000支为例所用原料和辅料及其质量配比如下:中分子量段黄芪多糖450g,蔗糖粉6000g,苯甲酸10g,蒸馏水10000ml。按制剂学口服液的常规工艺进行,每支10ml,含中分子量段黄芪多糖450mg。用法用量:口服,每次1支,一天三次。
实施例5
以制备含活性成分为中分子量段黄芪多糖的面包为例其流程如下:
1、黄芪多糖的提取:将黄芪药材粉碎后水温浸提取,浓缩提取液,通过sevag法除蛋白,离心,上清液浓缩后,80%乙醇沉淀,沉淀洗涤得到黄芪粗多糖;
2、黄芪粗多糖的酸水解:黄芪粗多糖热水溶解后,加入盐酸至浓度为0.16mol/l(质量百分比浓度为0.05%w/w),在80℃水浴3h,然后加入等当量naoh溶液调节ph至中性,水解液浓缩后,分别用截留分子量为1kd和10kd的透析袋透析处理,干燥后粉碎、过筛获得纯化的分子量介于103~104道尔顿之间的中分子量段黄芪多糖产物。
以制备含活性成分为中分子量段黄芪多糖的面包为例所用原料和辅料及其质量配比如下:中分子量段黄芪多糖产物5.4g,蔗糖粉930g面粉,植物油50g,活性酵母20g。按照常规面包制作工艺制作面包。每人每天食用面包250g,含中分子量段黄芪多糖1.35g。
在如饼干、蛋糕等食品中,也可以加入中分子量段黄芪多糖,按每人每天中分子量段黄芪多糖食用量1~2g为宜。
我们验证了不同水解条件下黄芪多糖的水解效应及水解工艺的稳定性问题;为了验证中分子量段黄芪多糖在调节肠黏膜免疫功能和肠道微生态系统方面的有益性,申请人还做了各种工艺参数的对比及药效试验,相关实验如下:
一、黄芪多糖的酸水解工艺研究:
1.1黄芪多糖的制备
取黄芪干粉100g,按料液比1∶10加水回流提取,过滤,收集滤液,重复3次,合并滤液,离心取上清,上清液减压浓缩至400ml,然后加入乙醇使醇浓度为80%,静置24h,过滤,得沉淀,干燥即的粗黄芪多糖,粗黄芪多糖用sevage法脱蛋白处理后,干燥,即得黄芪多糖。经考马斯亮蓝法检测,制备的黄芪多糖中蛋白含量<1%,经苯酚-硫酸法检测,制备的黄芪多糖中糖含量为57.40%(0.5740±0.0174,n=5)。
1.2多糖分子量的检测---高效凝胶渗透色谱法:
1.2.1色谱条件:reprosil125sec色谱柱,5μm,300×7.8mm,柱温30℃,流动相为去离子水,流速0.5ml/min,检测器为elsd3300蒸发光散射检测器(alltech),温度100℃。葡聚糖分子量标准品(mw4320、mw12600、mw70800、mw126000,北京索莱宝科技有限公司)。
需要说明的是,reprosil125sec色谱柱的有效分离范围为3000~500000,所以计算出来的分子量与实际分子量会有出入,考虑到本实验的研究目的,该分离柱分离范围已足以判断黄芪多糖的水解情况及中分子量段黄芪多糖产率问题。
1.2.2分子量标准曲线的制作
在上述色谱条件下,分别以葡聚糖分子量标准品(mw4320、12600、70800、126000,北京索莱宝科技有限公司)和葡萄糖进样检测。以保留时间(min)为横坐标,相对分子量对数(lgmw)为纵坐标作标准曲线图。
1.2.3样品分子量检测
在上述色谱条件下,样品溶于去离子水进样检测。将样品保留时间带入标准曲线的方程中,计算样品相对分子质量(mw)。
1.3黄芪多糖酸水解工艺研究
1.3.1黄芪多糖盐酸水解工艺
称取10mg黄芪多糖,放入具塞试管中,分别考察时间及酸浓度的影响。
根据预实验结果,盐酸浓度分别设置为:0.08、0.160、0.320mol/l;水解温度为80℃,水解时间为5h,水解后将溶液用naoh溶液调ph至中性,冷冻干燥后,用去离子水溶解,hplc-elsd分析其分子量信息。
1.3.2黄芪多糖三氟乙酸水解工艺
称取10mg黄芪多糖,放入具塞试管中,分别考察时间及酸浓度的影响。
根据预实验结果,三氟乙酸浓度分别设置为:0.05、0.10、0.20mol/l;水解温度为80℃,水解时间为5h,水解后将溶液用naoh溶液调ph至中性,冷冻干燥后,用去离子水溶解,hplc-elsd分析其分子量信息。
1.4黄芪多糖酸水解工艺研究结果
1.4.1多糖分子量标准曲线
利用不同相对分子质量的葡聚糖标品和葡萄糖,依据1.2方法。通过hpsec-elsd方法测定其在色谱柱保留时间,以各标品的保留时间(t)为x轴,lgmw为y轴,绘制标准曲线的回归方程为:y=-0.281x+8.279,r2=0.9839。
表1不同标准葡聚糖分子的保留时间
1.4.2黄芪多糖盐酸水解工艺结果
在不同的盐酸浓度水解之后,测定水解产物中多糖的分子量组成,结果如下:
表2不同盐酸浓度条件下黄芪多糖的水解效果
根据实验结果可以看出,水解后黄芪多糖主要由高、中、低三部分不同分子量段的物质组成,其中高分子量段的主要是未水解的黄芪多糖,平均相对分子量1.5×105道尔顿左右,中分子量段的主要由部分水解的黄芪多糖组成,分子量位于103~104道尔顿之间,而低分子量段主要为水解比较彻底的单糖或者寡糖组成,分子量小于103道尔顿。从结果可以看出,随着盐酸浓度的逐渐上升,高分子量段所占比例逐渐下降,中低分子量段所占比例逐渐上升,在盐酸浓度为0.16mol/l时,高分子量段的黄芪多糖含量降低至10%左右,而中分子量段的多糖相对比例达到70%以上,说明绝大多数黄芪多糖都已发生水解,产物中主要为中等分子量大小的黄芪多糖。在盐酸浓度为0.32mol/l时,低分子量段的物质相对比例达到90%以上,分子量在400-500道尔顿之间,说明黄芪多糖水解已经比较彻底。
所以选择盐酸浓度为0.16mol/l时,水解温度为80℃,水解时间为5h作为制备中分子量段黄芪多糖的较合适的水解条件。
1.4.3黄芪多糖三氟乙酸水解工艺结果
在不同的三氟乙酸浓度水解之后,测定水解产物中多糖的分子量组成,结果如下:
表3不同三氟乙酸浓度条件下黄芪多糖的水解效果
与盐酸水解的实验结果类似,水解后黄芪多糖主要由高、中、低三部分不同分子量段的物质组成,其中高分子量段的主要是未水解的黄芪多糖,平均相对分子量1.5×105道尔顿左右,中分子量段的主要由部分水解的黄芪多糖组成,分子量位于103~104道尔顿之间,而低分子量段主要为水解比较彻底的单糖或者寡糖组成,分子量低于1000道尔顿。从结果可以看出,随着三氟乙酸浓度的逐渐上升,高分子量段所占比例逐渐下降,中低分子量段的所占比例逐渐上升,根据实验结果可以看出,在三氟乙酸浓度为0.10mol/l时,高分子量段的黄芪多糖含量降低至25%左右,而中分子量段的相对比例达到60%以上,说明绝大多数黄芪多糖都已发生水解,相对分子量分别在4000道尔顿左右。在三氟乙酸浓度为0.20mol/l时,产物中低分子量段分子量低于1000的相对比例已经很高,说明水解已经比较彻底。
所以选择三氟乙酸浓度为0.10mol/l时,水解温度为80℃,水解时间为5h作为制备中分子量段黄芪多糖的较合适的水解条件。
1.4.4结论:
黄芪多糖的盐酸水解较适合的浓度为0.16mol/l;三氟乙酸较合适的酸浓度为0.10mol/l在以上条件下,不同酸水解时,温度可以采用80℃,水解时间可以采用5h。
1.4.6讨论
黄芪多糖水解比较彻底时,产物主要为寡糖和单糖,分子量一般低于1000道尔顿,而寡糖和单糖类物质对粘膜免疫功能影响较小;水解产物分子量位于103~104道尔顿之间的多糖类物质可能既有良好的粘膜免疫调节功能,也有肠道微生态系统调节功能,所以黄芪多糖水解工艺的主要评价指标就是尽可能提高水解产物中分子量位于103~104道尔顿之间的多糖类物质相对含量。在以上实验中较优条件下,分子量位于103~104道尔顿的中分子量段黄芪多糖在总水解产物中的相对含量不低于50%。
影响黄芪多糖水解的最主要因素是酸浓度,酸浓度过高,会导致水解过度,乃至全部水解为单糖,而酸浓度过低,水解程度过低,位于103~104道尔顿之间的多糖类物质产物过少。水解时间、水解温度等条件对水解程度影响相对较小,可以根据生产的实际需要调整。另外,黄芪多糖的水解可以选择的酸的种类很多,如硫酸、磷酸、硝酸等等,但从理论上分析,硫酸、硝酸有氧化性,水解产物的种类会比较多,产物的结构也可能发生变化,同时产物中掺入了硫酸根、硝酸根等其他粒子,影响产品的后续功能,环境污染也较高。而盐酸水解工艺引入的是氯离子,三氟乙酸的沸点为72.4℃,在干燥过程中可以挥发除去,在产品中的残留对未来产品的功能影响较小,所以在工厂化生产中,选择盐酸、三氟乙酸有一定的优势。
二黄芪多糖的酸水解工艺的稳定性研究
与酶水解法相比,利用酸水解法水解多糖由于水解位点随机性高,产物成分相对复杂,所以酸水解工艺条件下,产物组成是否稳定是关系到产品功效的重要因素,所以我们探索了优化的工艺条件下酸水解产物的组成稳定性情况。对于本发明来说,酸水解产物的核心要求是黄芪多糖经水解后,产物为分子量较小的聚合度较小的黄芪多糖,又不至于将黄芪多糖过度水解为单糖或者寡糖而降低其免疫调节功能。通过检测黄芪多糖酸水解产物的分子量组成反应水解工艺的稳定性情况。
2.1黄芪多糖的制备:同1.1
2.2多糖分子量的检测---高效凝胶渗透色谱法:同1.2
2.3黄芪多糖酸水解工艺稳定性研究
2.3.1黄芪多糖盐酸水解工艺稳定性研究
称取10mg黄芪多糖,放入具塞试管中,加入盐酸浓度为0.160mol/l;水解温度为80℃,水解时间为5h,水解后将溶液用naoh溶液调ph至中性,冷冻干燥后,用去离子水溶解,hplc-elsd分析其分子量信息。实验重复三次,计算不同批次间水解产物分子量分布相对比例的相对标准偏差(rsd)变化。
2.3.2黄芪多糖三氟乙酸水解工艺稳定性研究
称取10mg黄芪多糖,放入具塞试管中,加入三氟乙酸酸浓度为0.10mol/l;水解温度为80℃,水解时间为5h,水解后将溶液用naoh溶液调ph至中性,冷冻干燥后,用去离子水溶解,hplc-elsd分析其分子量信息。实验重复三次,计算不同批次间水解产物分子量分布的相对标准偏差(rsd)变化。
2.4结果
2.4.1同1.4.1通过hpsec-elsd方法测定其在色谱柱保留时间,以各标品的保留时间(t)为x轴,lgmw为y轴,绘制标准曲线的回归方程为:y=-0.281x+8.279,r2=0.9839。
2.4.2黄芪多糖盐酸水解工艺稳定性研究
如表5示,从黄芪多糖水解产物的分子量变化及各个分子量段的相对含量来看,rsd值均比较小,其中峰2在是我们期望的产物,其分子量范围变异都相对较大,但仍然在我们期望的范围内,峰2的相对含量变化较小,说明该工艺稳定性较好,可以满足黄芪多糖水解产物制备的需求。
表5黄芪多糖盐酸水解工艺稳定性研究
2.4.3黄芪多糖三氟乙酸水解工艺稳定性研究
如表6示,与黄芪盐酸水解工艺结果相似,峰2的相对含量及分子量变化的rsd值较小,平均分子量位于3000道尔顿左右,相对含量在总产物中约占60%以上,说明该工艺稳定性较好,可以满足黄芪多糖水解产物制备的需求。
表6黄芪多糖三氟乙酸水解工艺稳定性研究
2.4.3结论
以上重复性实验证实黄芪多糖的盐酸水解工艺,三氟乙酸水解工艺均有较好的重复性,适合工业生产及中分子量段黄芪多糖制备。
三黄芪多糖的酸水解产物对免疫抑制小鼠粘膜免疫功能的影响的实验研究
3.1实验材料:黄芪多糖的制备同1.1方法。黄芪多糖酸水解物的制备同2.3.1,黄芪多糖酸水解物分别用截留分子量为1kd和10kd的透析袋透析处理,获得纯化的分子量介于103~104道尔顿之间的中分子量段黄芪多糖,经检测,其中分子量介于103~104的多糖相对含量90%。
主要实验试剂:trisbase(sigma)、甘氨酸(sigma)、蛋白marker(thermo)、zo-1antibody(affinitybiosciences)、抗-β-actin兔多克隆抗体(affinitybiosciences)、hrpgoatanti-rabbitiggantibody(abcam)、pvdf膜(millipore)、乙醇(天津科密欧)、二甲苯(天津科密欧)、乙醚(天津富宇化工)、苏木精(北京索莱宝)、伊红(北京索莱宝)、bca蛋白定量试剂盒(碧云天)、sigaelisa试剂盒(上海酶远生物)、ifn-γelisa试剂盒(上海酶远生物)、il-4elisa试剂盒(上海酶远生物)、il-2elisa试剂盒(酶远生物)、et试剂盒(酶远生物)、凝胶配制试剂盒(西安博士德)、ripa蛋白裂解试剂盒(西安博士德)、吐温-20(国药集团)、环磷酰胺(上海源叶生物)、粪便dna提取试剂盒(天根生化科技)、核酸染料genegreen(天根生化科技)、2000bpdnamarker(天根生化科技)、loadingbuffer(天根生化科技)、乙酸标品(天津科密欧)、丙酸标品(天津科密欧)、丁酸标品(天津科密欧)。
3.2实验动物
雌性昆明小鼠,18g±2g,购自第四军医大学实验动物中心,动物生产许可证号syxk(陕)2014-001。
3.3实验动物分组及处理
雌性昆明小鼠,体重18g±2g,适应饲养一周后,进行随机分层分组、编号,每组12只。分为正常对照组,模型组,阳性药组,黄芪多糖(aps)高、低剂量组,中分子量段黄芪多糖(daps)高、低剂量组,腹腔注射环磷酰胺诱导免疫抑制动物模型,各组动物处理方法如表8。每两天记录一次小鼠体重。连续给药30天,药物治疗结束后,无菌收集小鼠粪便。然后对小鼠禁食不禁水12小时,记录每只小鼠的体重,小鼠进行眼球取血后脱颈椎处死,分离血清,取小鼠的胸腺及脾脏并进行称重;截取动物小肠空肠段20cm左右,用pbs冲洗该段组织,回收肠黏液;空肠段组织冻存待用;截取动物完整空肠段约2cm,浸泡于4%多聚甲醛中,固定处理,用于后续切片制作观察。
表8实验动物分组及给药方案
注:n.control:正常对照组;model:模型组;p.control:阳性对照组;aps(100):黄芪多糖低剂量组;aps(400):黄芪多糖高剂量组;daps(100):中分子量段黄芪多糖低剂量组;daps(400):中分子量段黄芪多糖高剂量组
3.4实验测试指标及方法
3.4.1小鼠肠粘膜形态学观察
取固定好的小鼠空肠按照常规石蜡切片制作方法经脱水、透明、浸蜡、包埋、切片,he染色后封片,显微镜下观察,测量记录小肠的绒毛长度(v)、隐窝深度(c)。
3.4.2elisa法检测黄芪多糖、中分子量段黄芪多糖对小鼠肠黏液siga、ifn-γ、il-4含量的影响
按照相应的试剂盒说明操作,分别检测小鼠肠粘液siga、ifn-γ、il-4含量,利用bca蛋白定量试剂盒测定肠粘液中蛋白质含量后,计算单位蛋白质中siga、ifn-γ、il-4。
3.4.3小鼠小肠组织紧密连接蛋白zo-1的检测-westernblot法
提取小肠组织蛋白:用液氮将100mg小鼠肠组织冷冻研碎至细粉状,加入750μlripa裂解液(750μl裂解液、7.5μlpmsf(苯甲基磺酰氟,蛋白酶抑制剂)在使用前数分钟内加入。继续研磨至肠组织呈液态,吸入ep管中,4℃离心机14000r/min,离心5min。吸取上清液,从中取10μl用于蛋白定量,剩余的上清液以30μl为单位分装入多个ep管,-80℃冰箱冻存待用。
提取的肠组织蛋白经聚丙烯酰胺凝胶电泳分离后,经转膜、封闭、一抗反应、二抗反应、发光反应、显影、定影后拍照,凝胶图象处理系统分析目标带的分子量和净光密度值。
3.4.4黄芪多糖、中分子量段黄芪多糖对小鼠肠道菌群的影响--16srrnamiseqillumina测序法
利用粪便dna提取试剂盒提取小鼠粪便基因组dna,以细菌16sdnav3-v4区域序列设计引物,引物序列如下:上游:actcctacgggaggcagca,下游:ggactachvgggtwtctaat。进行pcr扩增。扩增条件为:95℃,3min(变性);95℃,30s(变性)--55℃,30s(退火)---72℃,45s(延伸);30个循环后,72℃,10min。pcr扩增体系及扩增条件如下:
表9pcr扩增体系组成
扩增完成后,对pcr产物进行纯化、定量、均一化分析;然后进行miseqillimina测序(由上海美吉生物医药科技有限公司完成)并进行肠道菌鉴定及相关信息学分析,检测肠道菌群多样性及群落结构的变化。
3.4.5小鼠粪便中scfa(短链脂肪酸)的测定
将200mg小鼠粪便充分溶于1.5ml色谱乙醇中,离心(10000r/min、5min),在4℃环境下静置30min,用1ml注射器吸取上清液,用0.22μm的滤器过滤至气相小瓶中备用。色谱条件:色谱柱at-wax(30m×0.25mm×0.25μm);色谱柱升温程序:初始温度40℃,保持1min;以8℃/min的速率升至180℃,保持1min;以20℃/min的速率升温200℃,保持5min。载气:he;载气流速:1.2ml/min;进样口温度:200℃;进样方式:无分流;进样量:1μl;检测器温度(fid):230℃。以乙酸、丙酸、丁酸为标准品进样后定量分析。
3.5实验结果
3.5.1黄芪多糖、中分子量段黄芪多糖对小鼠肠粘膜形态学的影响
自然状态下生长的动物(n.control)肠绒毛紧密、整齐、完整;cy处理的小鼠(model)肠绒毛变短、加粗、肿胀、萎缩、断裂;经过丽珠肠乐(p.control)、黄芪多糖、中分子量段黄芪多糖治疗后,小肠绒毛长度有明显恢复趋势,肿胀、萎缩、断裂现象也不同程度减轻甚至消失,绒毛排列结构也恢复整齐。
黄芪多糖、中分子量段黄芪多糖对小鼠小肠绒毛长度(v)、隐窝深度(c)、v/c的影响如表10所示。结果显示,模型组的v值降低,与正常组相比差异有显著意义。各药物处理组均可以提高v值,数据差异有显著意义。模型组c与正常组相比增高,各药物处理组c值较模型组有所降低,除黄芪多糖(100mg/kg)组之外,差异均有显著意义。与正常组相比,模型组的v/c值下降,各药物组处理均可以提高v/c值,数据差异均有显著意义。
表10aps和daps对免疫抑制小鼠小肠v、c、v/c的影响
n.control:正常对照组;model:模型组;p.control:阳性对照组;daps(mg/kg):中分子量段黄芪多糖组;aps(mg/kg):黄芪多糖组
注:与正常组比,#p<0.05,##p<0.01;与模型组比,*p<0.05,**p<0.01。note:comparedwithnormalcontrol,#p<0.05,##p<0.01;comparedwithmodelcontrol,*p<0.05,**p<0.01。
3.5.2黄芪多糖、daps对小鼠肠黏液siga、ifn-γ、il-4含量的影响
如表11所示,模型组肠粘液中siga分泌量显著下降,其余各组的siga分泌量高于模型组,数据差异有显著意义,与aps(400)相比较,daps(400)肠黏液中siga含量较高,差异有显著意义。图2中,与正常组比,#p<0.05;与模型组比,**p<0.01;与黄芪多糖(400)组比,△p<0.05。
表11aps和daps对免疫抑制小鼠肠粘液中siga含量的影响
如
表12所示,模型组小鼠的ifn-γ/il-4值显著下降,其余各组的ifn-γ/il-4均有所恢复,数据差异有显著意义,与aps(400)相比较,daps(400)肠黏液中ifn-γ/il-4较高,差异有显著意义。
表12aps和daps对免疫抑制小鼠肠粘液中ifn-γ/il-4的影响
如图1所示,免疫抑制小鼠肠粘膜机械屏障受损,小肠组织紧密连接蛋白zo-1表达下降明显,经药物处理后,紧密连接蛋白的表达有所恢复,其中中分子量段黄芪多糖的恢复效果优于aps。图1中,n.control:正常对照组;model:模型组;p.control:阳性对照组;daps:中分子量段黄芪多糖组;aps:黄芪多糖组
注:与正常组比,##p<0.01;与模型组比,*p<0.05、**p<0.01;与aps(400)组比,△p<0.05;与aps(100)相比,▽p<0.05。n=3)。
3.5.4黄芪多糖、中分子量段黄芪多糖对小鼠肠道菌群的影响
对小鼠肠道菌群16srrna测序时的样品稀释曲线数据分析得知,随着测序序列数量的的提高,out水平数不再增多,稀释曲线趋向平坦,表示测序数据合理,后续的数据分析是有意义的。描述肠道菌群结构多样性的指数有多个,其中ace、chao指数代表了群落的丰富度,shannon、simpson指数代表了群落的多样性。ace、chao指数越大,代表丰富度越高;shannon指数越大,表示群落多样性越高;simpson指数越小,代表群落的多样性越高。从图2可以得出:与ncontrol相比,model的丰富度(ace、chao)有降低趋势(p<0.05),而pcontrol、中分子量段黄芪多糖、黄芪多糖的chao指数显著性增高(p<0.05);pcontrol、中分子量段黄芪多糖的ace指数显著性增高(p<0.05);黄芪多糖的ace指数有恢复趋势,但无显著性差异。各组间群落多样性指数shannon指数变化差异较小,simpson指数可以看出,模型组的多样性有下降趋势,仅中分子量段黄芪多糖组显示对simpson有一定的恢复作用。
pcoa分析(principalco-ordinatesanalysis)用于研究各组肠道菌群组成的相似性与差异性。pcoa图中横、纵坐标轴的数字各样本间的相对距离,距离越近,表示两组的相似性越高,反之则说明差异性较大。横纵坐标的百分比代表了造成不同组之间差异性的不同因素所占比例。图3是各组间的肠道菌结构pcoa分析图,由图可以看出,model与ncontrol距离较远,pcontrol、中分子量段黄芪多糖与ncontrol距离比较接近,恢复趋势较明显,而黄芪多糖则恢复趋势较弱。
通过miseqillumina测序对所有组样品粪便dnav3-v4区进行检测,共检测到8个主要的菌门,将小于1%的菌门归于others。这八个菌门分别是deferribacteres(脱铁杆菌门)、spirochaetae(螺旋菌门)、fusobacteria(梭杆菌门)、proteobacteria(变形菌门)、actinobacteria(放线菌门)、firmicutes(厚壁菌门)、bacteroidetes(拟杆菌门)、unclassified_k__norank。对各组中firmicutes/bacteroidetes的变化进行统计,如表13示。与ncontrol相比,model中的firmicutes/bacteroidetes比例呈极显著增加(p<0.01);与model相比,pcontrol、daps中firmicutes/bacteroidetes比例显著或极显著下降(p<0.05、p<0.01),有明显的恢复趋势,aps该比例没有下降;与aps相比,daps显著性下降(p<0.05)。
表13aps和daps对firmicutes/bacteroidetes的影响
aps:黄芪多糖组;daps:中分子量段黄芪多糖组;ncontrol:正常对照组;model:模型组;pcontrol:阳性对照组
注:与正常组比,##p<0.01;与模型组比,*p<0.05、**p<0.01;与aps比,△p<0.05。
在属水平上的分析显示,对相对含量小于1%的菌属归入others,大于1%的共检测到35种菌属。表14对在各组中变化含量显著的菌属进行了统计。与ncontrol相比,model中相对含量变化较大的主要有:bacteroides、lactobacillus、prevotellaceae_ugg-001、norank_f_bacteroidales_s24-7_group、odoribacter、lachnospiraceae_nk4a136_group、alloprevolella等的相对丰度下降(p<0.05或p<0.01),rhodococcus相对丰度增加(p<0.05)。与model相比,pcontrol、daps菌属变化有明显的恢复趋势(p<0.05或p<0.01),aps组中lactobacillus恢复效果明显(p<0.05),对其他几类菌属的恢复趋势并不明显。与aps相比,daps中bacteroides、prevotellaceae_ugg-001、norank_f_bacteroidales_s24-7_group、odoribacter、lachnospiraceae_nk4a136_group、alloprevolella显著或极显著增加(p<0.05或p<0.01),rhodococcus显著性下降(p<0.05)。综上所述,daps对肠道菌群属水平紊乱具有明显的恢复作用,效果优于aps。
表14aps和daps对属水平的影响
aps:黄芪多糖组;daps:中分子量段黄芪多糖组;ncontrol:正常对照组;model:模型组;pcontrol:阳性对照组;与正常组比,#p<0.05、##p<0.01;与模型组比,*p<0.05、**p<0.01;与aps比,△p<0.05、△△p<0.01。
3.5.5小鼠粪便中scfa(短链脂肪酸)的测定
利用标准乙酸、丙酸和丁酸分别进样,其标准曲线分别为:y=0.00000418x+0.52159094,r2=0.999(乙酸);y=0.00000013x+0.02089694,r2=0.999(丙酸);y=0.00000011x+0.01671176,r2=0.999(丁酸)。
短链脂肪酸(scfa)是肠道菌群以碳水化合物为底物的发酵产物,主要包含乙酸、丙酸、丁酸、戊酸等。根据标曲求得scfa在各组中的相对含量。如图4所示,与n.control相比,cy诱导的免疫抑制小鼠粪便中乙酸(aceticacid)、丙酸(propionicacid)、丁酸(butyrate)含量均呈明显下降趋势(p<0.05)。图4中aps:黄芪多糖组;daps:中分子量段黄芪多糖组;n.control:正常对照组;model:模型组;p.control:阳性对照组;
注:与正常组比,#p<0.05、##p<0.01;与模型组比,*p<0.05、**p<0.01;与aps(400)比,△p<0.05。
黄芪多糖及中分子量段黄芪多糖处理后,粪便中短链脂肪酸含量均有所上升,与model相比较,数据差异有显著意义(p<0.05)。因此黄芪多糖、中分子量段黄芪多糖均能恢复由cy导致的免疫抑制小鼠肠道菌群代谢产物scfa降低,结果显示,中分子量段黄芪多糖的恢复效果要优于黄芪多糖。
3.6结论
黄芪多糖有免疫促进功能;黄芪多糖对环磷酰胺诱导的免疫制小鼠的肠道菌群紊乱也有一定的影响,可以促进肠道菌代谢物短链脂肪酸的产生;因此,黄芪多糖对粘膜免疫功能的影响与黄芪多糖对肠道菌群微生态的影响相关;离体肠培养实验证实,黄芪多糖可以促进siga的分泌,增强肠黏膜免疫功能。在所检测的多项指标中,如siga分泌,ifn-γ/il-4、小肠组织紧密连接蛋白zo-1表达,肠道微生态变化、scfa含量脾脏指数等多项指标中,均显示中分子量段黄芪多糖对免疫抑制小鼠的恢复效应优于黄芪多糖,说明黄芪多糖水解产物有更好的促进黏膜免疫功能的效应。
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
- 还没有人留言评论。精彩留言会获得点赞!