用于一次性HIV基因型耐药检测的简并引物组及其应用的制作方法
本发明涉及病毒基因型检测
技术领域:
,尤其涉及用于一次性hiv基因型耐药检测的简并引物组及其应用。
背景技术:
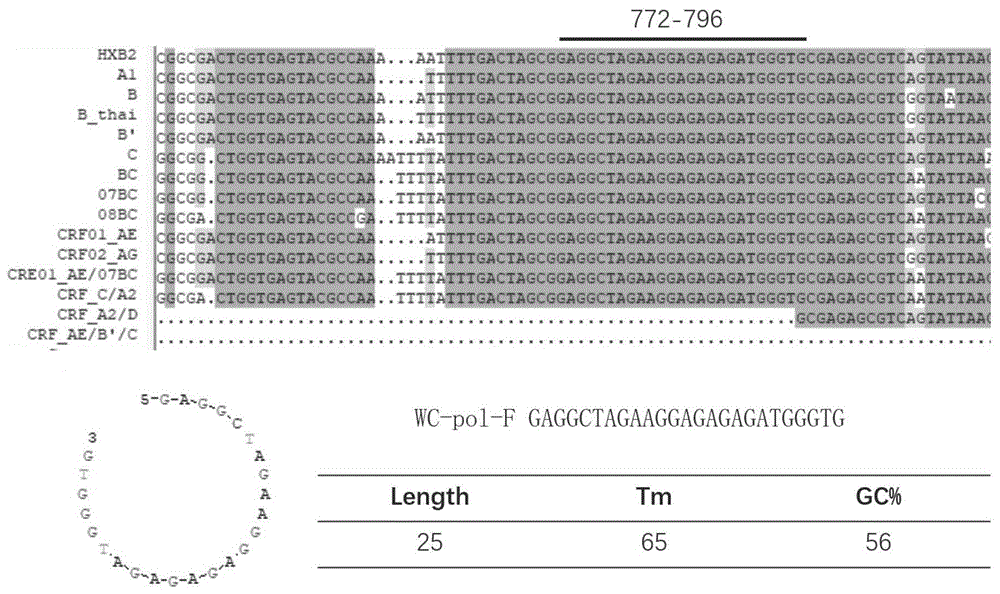
:人类免疫缺陷病毒(humanimmunodeficiencyvirus,hiv)攻击人类免疫系统,严重威胁人类生命健康。hiv耐药突变株的出现,不仅使得患者抗病毒治疗的效果下降,死亡病例增加;更重要的是,耐药毒株的流行将带来严重的公共卫生问题。为此,检测hiv基因型耐药突变是非常必要的。hiv-1基因组全长约9kb,为单链反义rna病毒,其中pol区编码蛋白酶、逆转录酶和整合酶,从2357nt到5095nt,是引起耐药突变的主要区域。当前,几家公司有成熟的商品化检测试剂盒,比如viroseq,truegene,geneship等,但都仅仅检测蛋白酶和部分逆转录酶区,而且价格昂贵,预计单次检测在人民币2000元以上。在临床上,为了节省成本,主要采用“in-house”的方法:提取待检者血浆中游离的病毒rna,然后逆转录pcr成cdna,以cdna为模板进行pcr扩增和巢氏pcr扩增,纯化回收pcr产物,目的片段经sanger测序,将序列在stanforduniversitydrugresistancedatabase里比对,得到相应的耐药突变位点。随着整合酶抑制剂的使用,整合酶耐药突变毒株也开始出现。因此,临床上又需要开展整合酶编码基因的突变检测。但是,至今为止,蛋白酶-逆转录酶区和整合酶区的检测都是单独进行的,要分别至少进行一次逆转录pcr反应和普通pcr扩增。这意味着hiv基因型耐药检测需要两次逆转录pcr反应和两次pcr扩增,费钱费时。这样的缺点在临床检验部门处理大量样本时尤其突出。hivrna在复制过程中,由于没有校正(proofreading)功能,会产生大量序列变异。这样就导致单一的引物在遇到不同亚型(subtype)的hiv毒株时,无法与模板结合,导致逆转录pcr或者巢氏pcr扩增失败。而且,由于整个过程步骤多,中间产物无法检测,在失败时,只能从头开始重复实验,甚至重新提取rna,大大增加成本。另外,在常规sanger测序时,由于单一引物不能结合模板,而导致测序失败。检测结果不能及时报告,使得临床医生没有耐药数据,在更换抗病毒治疗方案时非常困惑。因此,非常有必要重新设计和优化针对不同亚型的pcr引物和测序引物。技术实现要素:本发明为了克服现有的hiv基因型耐药检测失败率高、检测成本高、检测时间长的缺陷,提供了一种新的用于hiv基因型耐药检测的简并引物组和试剂盒以及检测方法,利用本发明提供的简并引物组可一次性扩增hiv的蛋白酶-逆转录pcr酶-整合酶的编码基因,降低了临床检测成本、节约时间,增加了检测成功率。为了实现上述发明目的,本发明提供以下技术方案:本发明提供了用于一次性hiv基因型耐药检测的简并引物组,包括逆转录pcr引物、巢氏pcr扩增引物和测序通用引物;所述逆转录pcr引物包括wc-pol-f和wc-pol-r;所述wc-pol-f的核苷酸序列如seqidno.1所示;所述wc-pol-r的核苷酸序列如seqidno.2所示;所述巢氏pcr扩增引物包括wc-nest-f和wc-nest-r;所述wc-nest-f的核苷酸序列如seqidno.3所示;所述wc-nest-r的核苷酸序列如seqidno.4所示;所述测序通用引物包括hbx2-3017r、hbx2-3785r和hbx2-4561r;所述hbx2-3017r的核苷酸序列如seqidno.5所示;所述hbx2-3785r的核苷酸序列如seqidno.6所示;所述hbx2-4561r的核苷酸序列如seqidno.7所示;seqidno.2~4所示的核苷酸序列中的r为a或g。优选的,所述简并引物组能够检测的hiv亚型包括但不限于:a、b、b’、c、crf01_ae、crf02_ag、crf_07bc、crf_08bc、crf_bc、crf_07bc/08bc、crf01_ae/b、crf01_ae/07bc和crf01_ae/b’/c。优选的,所述wc-pol-r、wc-nest-f或wc-nest-r中,r为a的特定引物与r为g的特定引物的数量比为1:1。本发明还提供了上述技术方案所述简并引物组在hiv基因型耐药检测中的应用。本发明还提供了一次性hiv基因型耐药检测试剂盒,包括前述技术方案所述的简并引物组。本发明还提供了利用前述技术方案所述简并引物组制备一次性hiv基因型耐药检测所需dna样品的方法,包括以下步骤:(1)从待测样品中提取hivrna,得到待测rna;(2)以所述简并引物组中的逆转录pcr引物对所述待测rna进行一步法逆转录pcr,得到待测dna;(3)以所述待测dna为模板,利用所述简并引物组中的巢氏pcr引物对进行巢氏pcr扩增,得到待测的dna样品。(4)对所述待测的dna样本,利用所述简并引物组中的测序通用引物、wc-nest-f以及wc-nest-r进行sanger测序,得到待分析的dna序列。优选的,步骤(2)中,所述逆转录pcr的反应条件包括:50℃30min,94℃2min,94℃30s、62℃30s、72℃2min,30个循环,72℃10min。优选的,步骤(2)中,所述逆转录pcr过程中,逆转录pcr引物在反应体系中的浓度为0.4μm。优选的,步骤(3)中,所述巢氏pcr扩增的反应条件包括:94℃3min,94℃30s、58℃30s、72℃1min,30个循环,72℃10min。优选的,步骤(3)中,所述巢氏pcr扩增过程中,巢氏pcr扩增引物在反应体系中的浓度为0.4μm。与现有技术相比,本发明的有益效果:1、在全球的hiv-1流行亚型中,a亚型、b亚型、c亚型、crf02_ag和crf01_ae重组型占到所有流行亚型的84%。中国hiv-1流行最广泛的毒株为crf01_ae、crf07_bc重组型,以及b’亚型。本发明将上述hiv病毒亚型的序列进行多序列比对寻找到不同亚型的保守区域。在保守区域设计引物,可以实现对不同hiv亚型进行扩增以及对扩增产物进行sanger测序。2、随着整合酶抑制剂的应用,对hiv亚型关于整合酶区域耐药性的检测也至关重要。本发明提供的简并引物可一次性扩增得到含有“蛋白酶-逆转录酶-整合酶”编码基因的dna片段,可实现更为全面的对hiv基因型耐药检测的需求。3、本发明通过优化逆转录pcr引物和巢氏扩增引物,在关键位置引入了混合碱基(r),以确保变异时,引物总能与模板退火进行逆转录pcr。更重要的是,通过本发明设计的简并引物组,可直接一次性扩增蛋白酶-逆转录酶-整合酶编码区。这样的片段可以进行sanger测序从而拿到hiv基因型耐药突变信息。4、相对于常规“in-house”技术分别检测hiv的蛋白酶-逆转录酶区与整合酶区的两次hiv基因型耐药检测,本发明提供的一次性hiv基因型耐药检测的简并引物组、试剂盒、测序通用引物以及检测方法的成本更低、检测速度更快,同时检测成功率高于现有“in-house”技术。附图说明图1为wc-pol-f的引物序列和对应的多序列比对结果;图2为wc-pol-r的引物序列和对应的多序列比对结果;图3为wc-nest-f的引物序列和对应的多序列比对结果;图4为wc-nest-r的引物序列和对应的多序列比对结果;图5为hbx2-3017r的引物序列和对应的多序列比对结果;图6为hbx2-3785r的引物序列和对应的多序列比对结果;图7为hbx2-4561r的引物序列和对应的多序列比对结果;图8为琼脂糖凝胶电泳检测巢氏pcr产物;其中,m为分子量标准,泳道1为阳性对照,以pnl4-3.luc.r–e为模板;泳道2-6分别是样本1-5号的巢氏pcr产物;图9为1号样本的耐药测序报告截图;1号样本为crf_01ae亚型;图10为2号样本的耐药测序报告截图;2号样本为crf_01ae亚型;图11为3号样本的耐药测序报告;3号样本为a亚型;图12为4号样本的耐药测序报告;4号样本为crf68_01b亚型;图13为5号样本的耐药测序报告;5号样本为b+c亚型。具体实施方式本发明提供了用于hiv基因型耐药检测的简并引物组,包括逆转录pcr引物、巢氏pcr扩增引物和测序通用引物。利用本申请所述简并引物组扩增的目的产物为hiv的“蛋白酶-逆转录酶-整合酶”的编码基因,目的产物的全长为2955bp。本发明所述逆转录pcr引物包括wc-pol-f和wc-pol-r;所述wc-pol-f的核苷酸序列如seqidno.1所示:seqidno.1:5’-gaggctagaaggagagagatgggtg-3’;所述wc-pol-r的核苷酸序列如seqidno.2所示;seqidno.2:5’-cttcctgccatagraratgcctaag-3’。本发明所述巢氏pcr扩增引物包括wc-nest-f和wc-nest-r;所述wc-nest-f的核苷酸序列如seqidno.3所示;seqidno.3:5’-tcactctttggcarcgacc-3’;所述wc-nest-r的核苷酸序列如seqidno.4所示;seqidno.4:5’-tgggatrtgtacttctgaactta-3’。本发明所述测序通用引物包括hbx2-3017r、hbx2-3785r和hbx2-4561r;所述hbx2-3017r的核苷酸序列如seqidno.5所示;seqidno.5:5’-tgatcctttccatccctgtg-3’。所述hbx2-3785r的核苷酸序列如seqidno.6所示;seqidno.6:5’-aggaatccaggtggcttgc-3’。所述hbx2-4561r的核苷酸序列如seqidno.7所示;seqidno.7:5’-ttgactggccatcttcctgc-3’。在本发明中,seqidno.2~4所示的核苷酸序列中的r为a或g。本发明优选的,所述wc-pol-r、wc-nest-f或wc-nest-r中,r为a的特定引物与r为g的特定引物的数量比为1:1。本发明所述的简并引物组是根据hiv各基因型亚型的保守序列设计得到,所述简并引物组能够用于检测的hiv基因型的亚型包括但不限于a、b、b’、c、crf01_ae、crf02_ag、crf_07bc、crf_08bc、crf_bc、crf_07bc/08bc、crf01_ae/b、crf01_ae/07bc和crf01_ae/b’/c。具体的,本发明在ncbi数据库上获得hiv不同亚型毒株的全长或者近全长序列,包括a、b、b’、c、crf01_ae、crf02_ag、crf_07bc、crf_08bc、crf_bc、crf_07bc/08bc、crf01_ae/b、crf01_ae/07bc、crf01_ae/b’/c。经过多序列比对(dnaman软件),我们发现在pol区前后有相对保守区域(如图1~7所示)。在这些相对保守的区域设计引物,使得引物可以结合不同hiv亚型的rna。以参考毒株hxb2全长(9719bp)为基础,wc-pol-f设计在从772nt到796nt的保守区;wc-pol-r设计在从5957nt到5981nt的保守区。wc-nest-f设计在从2260nt到2278nt的保守区;wc-nest-r设计在从5192nt到5214nt的保守区;hbx2-3017r设计在从2998nt到3017nt的保守区;hbx2-3785r设计在从3767nt到3785nt的保守区;hbx2-4561r设计在从4542nt到4561nt的保守区;wc-pol-f:gaggctagaaggagagagatgggtg(seqidno.1);wc-pol-r:cttcctgccatagraratgcctaag(seqidno.2);wc-nest-f:tcactctttggcarcgacc(seqidno.3);wc-nest-r:tgggatrtgtacttctgaactta(seqidno.4);hbx2-3017r:tgatcctttccatccctgtg(seqidno.5);hbx2-3785r:aggaatccaggtggcttgc(seqidno.6);hbx2-4561r:ttgactggccatcttcctgc(seqidno.7)其中r代表a或者g,在合成时,a:g=1:1。本发明还提供了一种一次性hiv基因型耐药检测的试剂盒,包括上述技术方案所述的简并引物组。本发明优选的,所述试剂盒还包括hivrna的提取试剂、一步法逆转录pcr试剂、巢氏pcr扩增试剂。本发明还提供了上述技术方案所述简并引物组在hiv基因型耐药检测中的应用。具体的,利用本发明提供的简并引物组可一次性扩增得到hiv基因型耐药性检测所需的dna片段,后续再进行sanger测序、突变位点比对等步骤即可。将本发明所述简并引物应用到hiv基因型耐药检测中,可有效缩短检测时间和检测成本,并提高检测的成功率。本发明还提供了一次性hiv基因型耐药检测试剂盒,包括前述技术方案所述的简并引物组。本发明优选的,所述试剂盒还包括hivrna的提取试剂、逆转录pcr试剂、巢氏pcr扩增试剂。在本发明中,所述hivrna的提取试剂用于提取待测样品中游离的hivrna。本发明所述hivrna的提取试剂可选用市售的提取试剂盒,也可自行配制试剂。在本发明中,所述逆转录pcr试剂包括除了逆转录pcr引物以外的反应试剂,包括但不限于反应缓冲液、逆转录酶、taq酶和纯化水。本发明所述逆转录pcr试剂可购买市售试剂也可以自行制备。如本发明的实施例所示,选用市售的takaraonestep试剂盒进行一步法逆转录pcr。在本发明中,所述巢氏pcr扩增试剂包括除了巢氏pcr扩增引物以外的反应试剂,包括但不限于巢氏pcr扩增反应缓冲液、taq酶和纯化水。本发明所述巢氏pcr扩增试剂可购买市售试剂也可以自行制备。在本发明中,所述测序通用引物也是在不同hiv亚型序列的保守区域,可以保证在测序时,引物能结合上去,保证测序成功。本发明还提供了利用前述技术方案所述简并引物组制备一次性hiv基因型耐药检测所需dna样品的方法,包括以下步骤:(1)从待测样品中提取hivrna,得到待测rna;在本发明中,所述待测样品为待测患者的血液。在本发明中,所述提取hiv的rna优选的利用hivrna的提取试剂进行,本发明对此无特殊限定。(2)以所述简并引物组中的逆转录pcr引物对所述待测rna进行一步法逆转录pcr,得到待测dna。本发明中的逆转录pcr引物对能够实现对多种hiv亚型进行互补扩增,可提高逆转录的成功率。在本发明中,所述一步法逆转录pcr的反应条件优选的包括:50℃30min,94℃2min,94℃30s、62℃30s、72℃2min,30个循环,72℃10min。在本发明中,所述一步法逆转录pcr过程中,逆转录pcr引物在反应体系中的浓度优选的独立为0.4μm,即wc-pol-f的浓度为0.4μm,wc-pol-r中的每个特定引物浓度为0.4μm。在本发明中,所述一步法逆转录pcr的反应体系,每50μl反应体系中优选的包括:primescript1stepenzymemix2μl、2×1stepbuffer25μl、20μm的wc-pol-f1μl、100μm的wc-pol-r0.8μl、待测rna5μl和余量的水。(3)以所述待测dna为模板,利用所述简并引物组中的巢氏pcr引物对进行巢氏pcr扩增,得到待测的dna样品。经由逆转录得到的待测dna较长,且特异性不够高,本发明利用所述巢氏pcr引物对进行巢氏pcr扩增,能够有效增加所得dna片段的特异性。在本发明中,所述巢氏pcr扩增的反应条件优选的包括:94℃3min,94℃30s、58℃30s、72℃1min,30个循环,72℃10min。在本发明中,所述巢氏pcr扩增过程中,巢氏pcr扩增引物在反应体系中的浓度优选的独立为0.4μm;即wc-nest-f和wc-nest-r中的每一个特定引物浓度独立的为0.4μm。在本发明中,所述巢氏pcr扩增的反应体系,每50μl反应体系优选的包括:2×buffermix25μl、40μm的wc-nest-f1μl、40μm的wc-nest-r1μl、待测dna5μl和余量的水。若本发明得到的待测扩增产物全长为2955bp,则对待测扩增产物进行进一步的sanger测序。在本发明中,所述sanger测序可委托测序公司进行。(4)对所述待测的dna样本,利用所述简并引物组中的测序通用引物、wc-nest-f以及wc-nest-r进行sanger测序,得到待分析的dna序列。下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。实施例1、用viralrnamini(货号52906)试剂盒分别从5个hiv感染病人血浆中提取游离的hivrna,5份血浆中病毒载量都大于1000个拷贝。2、利用takara公司的一步法逆转录试剂盒(primescripttmonesteprt-pcrkitver.2,货号,rr055a),加入本发明所述简并引物组中逆转录pcr引物对中的上游引物(wc-pol-f)和下游引物(wc-pol-r)进行逆转录成cdna。具体如下:wc-pol-f:gaggctagaaggagagagatgggtg(seqidno.1);wc-pol-r:cttcctgccatagraratgcctaag(seqidno.2);表1逆转录pcr的反应体系试剂用量终浓度primescript1stepenzymemix2μl2×1stepbuffer25μl1xwc-pol-f(20μm)1μl0.4μmwc-pol-r(100μm)0.8μl0.4μm*rnatemplate5μlh2o16.2μl*由于是简并引物组,每一条特定的引物在混合引物中占的比例是1/4,也就是25μm,当在50μl体系中加入0.8μl时,每一条有效引物的终浓度为0.4μm。一步法逆转录pcr条件:50℃30min;94℃2min,94℃30s,62℃30s,72℃2min,30个循环,72℃10min,12℃待机。3、取5μl第一步pcr产物作为模板,加入primestarmaxdnapolymerase酶(货号r045a)。另外,单独加入pnl4-3.luc.r–e作为阳性对照(pnl4-3.luc.r–e中包含hiv-1全长的dna序列)。采用本发明所述简并引物组中的巢氏pcr引物对中的上游引物(wc-nest-f)和下游引物(wc-nest-r)进行巢氏pcr扩增,得到待测的dna样品。所述待测扩增产物为2955bp的dna片段,包括蛋白酶-逆转录酶-整合酶编码基因。wc-nest-f:tcactctttggcarcgacc(seqidno.3);wc-nest-r:tgggatrtgtacttctgaactta(seqidno.4);表2巢氏pcr扩增的反应体系*由于是简并引物组,每一条特定的引物在混合引物中占的比例是1/2,也就是20μm,当在50μl体系中加入1μl时,每一条有效引物的终浓度为0.4μm。pcr条件:94℃3min,94℃30s,58℃30s,72℃1min,30个循环,72℃10min。4、对待测扩增产物进行纯化回收后,纯化回收都是按照试剂盒标准流程做。5、将纯化的pcr产物外送测序公司进行sanger测序。测序所用引物为wc-nest-f、wc-nest-r、hbx2-3017r、hbx2-3785r和hbx2-4561r。6、将测序序列进行拼接,然后将全长输入美国斯坦福大学的hiv耐药数据库进行分析(https://hivdb.stanford.edu/hivdb/by-sequences/),得出耐药突变。结果检测:琼脂糖凝胶电泳的结果如图8所示,可以看出,5份待测样本与对照质粒均得到了2955bp的产物。如图9~13所示,5份报告截图显示了本发明扩增的pcr产物包含了hiv蛋白酶-逆转录酶-整合酶的编码基因全长。并且,5份hiv样本中,包含了crf01_ae、crf68_01b、a和b+c等4种不同的亚型。成功率为100%。以上所述仅是本发明的优选实施方式,应当指出,对于本
技术领域:
的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。序列表<110>南京市第二医院<120>用于一次性hiv基因型耐药检测的简并引物组及其应用<160>7<170>siposequencelisting1.0<210>1<211>25<212>dna<213>人工序列(artificialsequence)<400>1gaggctagaaggagagagatgggtg25<210>2<211>25<212>dna<213>人工序列(artificialsequence)<400>2cttcctgccatagraratgcctaag25<210>3<211>19<212>dna<213>人工序列(artificialsequence)<400>3tcactctttggcarcgacc19<210>4<211>23<212>dna<213>人工序列(artificialsequence)<400>4tgggatrtgtacttctgaactta23<210>5<211>20<212>dna<213>人工序列(artificialsequence)<400>5tgatcctttccatccctgtg20<210>6<211>19<212>dna<213>人工序列(artificialsequence)<400>6aggaatccaggtggcttgc19<210>7<211>20<212>dna<213>人工序列(artificialsequence)<400>7ttgactggccatcttcctgc20当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1