与青光眼发生发展相关的生物标志物及其应用的制作方法
本发明涉及生物医学领域,涉及一种与青光眼发生发展相关的生物标志物及其应用,所述生物标志物为spata33或wdr61。
背景技术:
青光眼是一组以特征性视神经萎缩和视野缺损为共同特征的疾病,病理性眼压升高是其主要危险因素。是现今世界第二大的致盲性眼病,位居不可逆盲目的第一位。据统计,2013年全球有6.43亿人患有青光眼,到2020年大约有7.60亿人将患有青光眼,2040年青光眼患病人数将上升至11.18亿人(thamyc,lix,wongty,quigleyha,aungt,chengcy.globalprevalenceofglaucomaandprojectionsofglaucomaburdenthrough2040:asystematicreviewandmeta-analysis[j].ophthalmology2014;121:2081-2090.)。青光眼以高发病率及高致盲率,严重威胁人类的生活质量。
临床上通常将青光眼分为原发性青光眼、继发性青光眼、儿童(发育)性青光眼三种类型。各类型青光眼的发病机制目前不完全清楚。目前大多数学者认为青光眼眼底视神经损害很大程度上与病理性眼压升高相关,眼压升高后可机械性压迫视神经纤维,或使视网膜血管缺血缺氧,最终导致视网膜神经节细胞的凋亡。青光眼的发病和遗传方式很复杂,可能是多种基因之间的相互作用及基因与环境的相互作用共同引起。青光眼可能与家族史、特征性结构、年龄、种族、环境、遗传等危险因素有关,其中遗传因素在其中占据重要地位。目前临床明确诊断青光眼,青光眼的病程已不在早期,青光眼是不可逆的致盲病,所以早期诊断、早期治疗具有重大意义。
随着基因研究技术的发展,发现越来越多的青光眼相关致病基因、位点及相关基因突变,对于进一步明确青光眼的分子发病机制,对人群实行早期基因干预,高危人群筛查,临床前诊断及基因治疗,提高青光眼患者生活质量,甚至根治青光眼具有重要的意义。
技术实现要素:
为了弥补现有技术的不足,本发明基于遗传因素在青光眼的发生发展中的作用,研究与青光眼发生发展相关的生物标志物,从而为青光眼的诊断和治疗提供新的手段。
本发明提供了检测生物标志物的试剂在制备诊断青光眼的产品中的应用,所述生物标志物选自spata33或wdr61。
进一步,与正常人相比,当spata33或wdr61在受试者样本中的表达水平上调时,则受试者患有青光眼或者存在患有青光眼的风险。其中样本包括但不限于组织或流体,如组织、血液、血浆、血清、淋巴液、尿液、浆膜腔液、脊髓液、滑液、房水、泪液、唾液、或其组分或经过处理的材料。
进一步,所述样本为组织,更进一步地,所述组织为小梁网组织。
进一步,所述试剂包括:
特异性识别spata33或wdr61基因的探针;
特异性扩增spata33或wdr61基因的引物;或
特异性结合spata33或wdr61编码的蛋白的结合剂。
进一步,所述特异性扩增spata33或wdr61基因的引物序列对分别如seqidno.1~2和seqidno.3~4所示。
本发明提供了一种诊断青光眼的产品,所述产品包括检测spata33或wdr61水平的试剂。
进一步,所述产品包括核酸膜条、芯片或试剂盒。
进一步,核酸膜条包括基底和固定于所述基底上的特异性识别spata33或wdr61的寡核苷酸探针;所述基底可以是任何适于固定寡核苷酸探针的基底,例如尼龙膜、硝酸纤维素膜、聚丙烯膜、玻璃片、硅胶晶片、微缩磁珠等。
进一步,所述芯片包括基因芯片、蛋白质芯片,其中基因芯片包括针对spata33或wdr61的引物或寡核苷酸探针,蛋白质芯片包括特异性结合spata33或wdr61蛋白的结合剂。其中,特异性结合剂是例如蛋白质spata33或wdr61的受体、结合蛋白质spata33或wdr61的凝集素、针对蛋白质spata33或wdr61的抗体、针对蛋白质spata33或wdr61的肽抗体(peptidebody)、双特异性双重结合剂或双特异性抗体形式。
特异性结合剂的例子是肽、肽模拟物、aptamer、spiegelmer、darpin、锚蛋白重复蛋白、kunitz型域、抗体、单域抗体和单价抗体片段。在本发明的具体实施例中,所述特异性结合剂为spata33或wdr61特异性抗体。
进一步,所述试剂盒包括基因检测试剂盒和蛋白检测试剂盒,所述基因检测试剂盒包括特异性针对spata33或wdr61的引物、寡核苷酸探针或芯片;所述蛋白检测试剂盒包括特异性结合spata33或wdr61蛋白的结合剂。试剂盒包括一种或多种无菌容器,这样的容器可以是盒、安瓿、瓶子、管形瓶、管、袋、小袋、泡罩包装、或本领域已知的其它合适的容器形式。这样的容器可以由塑料、玻璃、层压纸、金属箔、或适于容器药物的其它材料。
进一步,特异性针对spata33或wdr61的引物序列如seqidno.1~4所示。
本发明提供了一种诊断青光眼的方法,包括步骤:
1)获取样本;
2)提取样本中的rna;
3)检测rna中的spata33或wdr61的表达水平;
4)比较判断,与正常人相比,当spata33或wdr61的表达水平显著升高时,则受试者患有青光眼。
本发明提供了spata33或wdr61在制备治疗青光眼的药物组合物中的应用。
进一步,所述药物组合物包括spata33或wdr61的抑制剂。其中,所述抑制剂可以在转录或翻译水平降低spata33或wdr61的表达。
在本发明中,spata33(基因id:124045)包括人spata33基因及其所编码的蛋白。作为非限制性的实例,spata33的基因序列如nm_001271907.1、nm_001271908.1、nm_001271909.1、nm_001271910.1、nm_153025.2任一转录本所示,相应的氨基酸序列如np_001258836.1、np_001258837.1、np_001258838.1、np_001258839.1、np_694570.1所示。其中,一种代表性的spata33的基因序列如nm_001271907.1所示,相对应的氨基酸序列如np_001258836.1所示。
wdr61(基因id:80349)包括人wdr61基因及其所编码的蛋白。作为非限制性的实例,wdr61的基因序列如nm_001303247.2、nm_001303248.2、nm_025234.3任一转录本所示,其相应的氨基酸序列如np_001290176.1、np_001290177.1、np_079510.1所示。在本申请中,一种代表性的wdr61的基因序列如nm_001134870.2所示,氨基酸序列如np_001290176.1所示。
本领域技术人员应当理解,测定基因表达的手段不是本发明的重要方面。本发明可以利用本领域内已知的任何方法测定基因的表达水平。
本发明的spata33或wdr61使用本领域普通技术人员已知的多种核酸以及蛋白技术进行检测,这些技术包括但不限于:核酸测序、核酸杂交、核酸扩增技术、蛋白免疫技术。
本发明中诊断青光眼的产品可用于检测包括spata33或wdr61基因在内的多个基因(例如,与青光眼相关的多个基因)的表达水平,将青光眼的多个标志物同时进行检测,可大大提高青光眼诊断的准确率。
本发明的优点和有益效果:
本发明首次发现了spata33或wdr61基因在青光眼患者中表达水平上调,通过检测spata33或wdr61基因的表达水平可以辅助诊断受试者是否患有青光眼或患青光眼病病的风险,从而指导医生提供预防或治疗方案。
附图说明
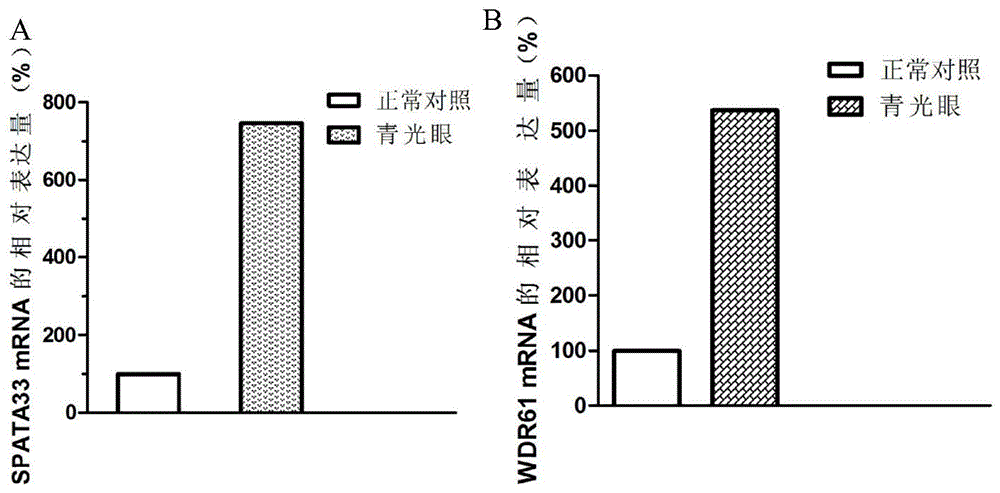
图1是利用qpcr检测spata33在青光眼患者中的表达水平图,其中图a是spata33的表达水平图,图b是wdr61的表达水平图。
具体的实施方式
下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。
实施例qpcr检测spata33和wdr61在青光眼中的表达
1、样品收集
青光眼手术过程中的小梁组织31例以及正常外伤的小梁组织19例,排除角膜病、葡萄膜炎、眼内炎和眼底病及全身系统疾病的患者。
2、rna样品的制备及质量分析
使用trizol法提取组织中的总rna
取组织加加液氮研磨,加入trizol裂解液(美国invitrogen公司)和氯仿(trizo1裂解液:氯仿=5:1),振荡混匀15s,37℃孵育2min,4℃下12000r/min。离心15min,吸取上层无色液体至干净的无菌离心管中,加入等体积异丙醇混匀,37℃孵育10min,4℃下12000r/min离心10min,弃上清,用体积分数75%乙醇清洗rna沉淀,室温下干燥5~10min,用无rna酶的无菌水溶解rna。紫外吸收法检测rna纯度,a260/a280比值1.8~2.1。
3、逆转录:
使用takara公司的反转录试剂盒(takaracode:drr047a)进行操作。
1)去除基因组dna
在试管中加入5×gdnaeraserbμffer2.0μl,gdnaeraser1.0μl,总rna1μg,加rnasefreeddh2o使总体积至10μl,水浴锅中42℃加热2min。
2)反转录反应
将
4、实时荧光定量pcr
1)引物设计
根据spata33、wdr61和gadph的基因序列设计引物,具体引物序列如表1所示:
表1引物序列
2)实时荧光定量pcr扩增检验
用
表2实时荧光定量pcr扩增体系和反应条件
5、结果
qpcr结果如图1所示,与正常组织相比,spata33和wdr61在青光眼患者中表达显著上调,spata33上调约7.46倍,wdr61上调约5.37倍,差异具有统计学意义(p<0.05),其中31例青光眼患者中有26例spata33显著上调,有29例wdr61显著上调,提示spata33和wdr61可应用于青光眼的诊断。
同时,根据spata33和wdr61在青光眼中显著上调,可以设计针对spata33和wdr61基因的sirna、shrna或者特异性结合spata33和wdr61蛋白的抗体应用于青光眼的治疗。
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
序列表
<110>汶上县中医院
<120>与青光眼发生发展相关的生物标志物及其应用
<160>6
<170>siposequencelisting1.0
<210>1
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>1
aaagagaaacccaggaaag19
<210>2
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>2
gaatgcttctccatcaact19
<210>3
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>3
cagataaagtccatagat18
<210>4
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>4
gcaatactaagaatgaat18
<210>5
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>5
aatcccatcaccatcttccag21
<210>6
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>6
gagccccagccttctccat19
- 还没有人留言评论。精彩留言会获得点赞!