一种7-O-酰胺基取代的橙皮素类衍生物及其制备方法和应用与流程
本发明属于医药工业技术领域,尤其涉及一种7-o-酰胺基取代的橙皮素类衍生物及其制备方法和应用。
背景技术:
炎症是许多病理条件的一个中心特征,是对有害刺激的一种生物学反应,如病原体引起组织和细胞损伤。但持续性炎症可引起机体的严重损伤,对人体健康有害。许多常见的疾病(如自身免疫疾病、动脉粥样硬化、创伤修复等)都属于炎症范畴。随着医学技术的不断研究和发展,一些对炎症有抑制作用的药物逐渐被发现。1929年,美国病理学家亨齐最先研究发现甾类抗炎药“可的松”,这是人类在抗炎药领域的一大重要突破。但是随着抗炎药的广泛应用,一些问题逐渐被暴露,例如现有的抗炎药物的副作用,并且抗炎药物长期使用会有产生耐药性。比如,cox-2选择性抑制剂增加心肌梗塞和中风的发生率,阿司匹林等对胃有一定程度的伤害。克服这些副作用成为了研究抗炎药的一个重要的难题,所以抗炎药的发展研究一直是医药领域所瞩目。
当机体受到有害刺激侵犯时,机体自身通过炎症反应消除致炎因子,这是一个损伤和抗损伤的过程。因此炎症是由一些促炎的细胞因子和炎症分子介导的一个复杂的过程。研究发现,血管内皮细胞经大肠杆菌脂多糖刺激后no分泌增加,目前针对no的分泌抑制的新药研究逐步展开。当机体受到感染时,腹腔巨噬细胞受到大量脂多糖刺激,产生大量的tnf-α和il-6等,它们相互诱生,相互协同。由于这些细胞因子的过量存在,加速了花生四烯酸代谢,释放血栓素a2、前列腺素、白三烯等炎症介质,导致过度炎症反应。在新药设计和研发过程中,可以根据药物活性是否可以抑制炎症因子no,tnf-α和il-6等的释放为标准,筛选出一些新的可能成为抗炎的化合物,然后再根据其化合物的特性研究它可能成为抗炎药的机制,这些都是初步筛选的主要依据。抗炎类药物能够抑制或阻断炎症介质的产生和释放,抑制炎性反应。近年来,随着人们对炎症机制认识和不断研究深入以及分子生物技术的广泛应用,抗炎药物的研究已从器官组织水平逐渐发展到细胞、分子水平,并且取得了长足进步,已经逐渐制备出更多品种,范围更广的抗炎药物。
技术实现要素:
本发明目的就是为了弥补已有技术的缺陷,提供一种7-o-酰胺基取代的橙皮素类衍生物及其制备方法和应用。
为了实现上述的目的,本发明提供以下技术方案:
一种7-o-酰胺基取代的橙皮素类衍生物,其结构式如式(ⅰ)所示:
式(ⅰ)中,r1为甲胺基,乙胺基,二甲胺基,正丙胺基,异丙胺基,正丁胺基,异丁胺基,叔丁胺基,二乙胺基,环丙胺基,环戊胺基,吡咯烷基,噻唑烷基,哌啶基,3-羟甲基哌啶基,2-羟甲基哌啶基,n-甲基哌嗪基,n-乙基哌嗪基,n-乙基哌嗪基,吗啉基,2-羟基乙胺基,2-二甲胺基乙胺基,2-(4-吗啉基)乙胺基中的一种。
一种如上所述的7-o-酰胺基取代的橙皮素类衍生物的制备方法,包括以下步骤:
(1)将如式(ⅱ)所示的橙皮苷用10-20倍量的10%浓硫酸乙醇溶液分散溶解,回流条件发生水解反应,得到如式(ⅲ)所示的产物橙皮素;
(2)将步骤(1)所得产物橙皮素与2-3倍量的溴乙酸乙酯在弱碱作用下搅拌后得到如式(ⅳ)所示的产物;
(3)将步骤(2)所得产物用强碱水解后,在edc·hcl催化下与hobt发生缩合反应生成活性酯后,加入各种胺类进行胺解得到如式(ⅰ)所示的终产物酰胺基取代的橙皮素类衍生物。
所述步骤(1)苷水解反应中,浓硫酸为催化剂,乙醇为溶剂,加热回流,反应时间为8-10h。
所述步骤(2)中弱碱为1.5倍量k2co3和3倍量的khco3混合物,室温下进行反应,反应时间为30-60min,反应溶剂为dmf。
所述步骤(3)中水解反应条件为naoh催化,溶剂为10%乙醇水溶液,冰浴条件,反应时间为20-30min;酰胺取代反应中在edc·hcl的催化下与hobt发生缩合,反应溶剂为无水无醇氯仿,三乙胺作为缚酸剂,室温条件下进行,反应1-2h;再与各种胺进行胺解,反应3-6h。
一种如上所述的7-o-酰胺基取代的橙皮素类衍生物在制备抗炎药物中的应用。
所述应用中的药物为注射剂、片剂、丸剂、胶囊剂、悬浮剂或乳剂。
本发明7-o-酰胺基取代的橙皮素类衍生物的制备方法,主要合成路线如下:
其具体步骤为:
(1)将如式(ⅱ)所示的橙皮苷用10-20倍量的10%浓硫酸乙醇溶液分散溶解,回流条件反应8-10h,反应结束后,倒入冰水中,析出固体,抽滤,用乙醇加热溶解后,活性炭脱色,用乙醇和二氯甲烷重结晶,析出土白色固体,抽滤得到如式(ⅲ)所示的产物橙皮素;
(2)将橙皮素用10倍量的dmf溶解,依次加入3倍量的khco3和1.5倍量的k2co3,搅拌15min后,加入2-3倍量的溴乙酸乙酯,常温反应30-60min,用乙酸乙酯和饱和食盐水反复萃取洗去dmf,先用二氯甲烷和甲醇重结晶,析出白色固体,再用二氯甲烷和乙醚重结晶,析出针状晶体,得到如式(ⅳ)所示的产物;
(3)将上述产物分散溶解在10%乙醇水溶液中,将反应装置放于冰浴条件下,搅拌30min,加入适量10%naoh溶液调ph到12-13左右,反应20-30min,终止反应,滴加冰浴过的1mol/l稀盐酸,滴加过程中有白色固体析出,调节ph至3-4,抽滤得到水解产物,晒干后,真空干燥;用无水无醇氯仿溶解,加入3倍量的hobt和1.5-2倍量的edc·hcl,搅拌均匀后,加入1.5-2倍量的三乙胺作为缚酸剂,常温反应1-2h后;加入3-5倍量的脂肪胺,常温反应3-6h;停止反应,加入乙酸乙酯萃取,加入适量无水naso4干燥,过滤,减压回收乙酸乙酯,用二氯甲烷、乙醇重结晶,得到白色固体或晶体,即为如式(ⅰ)所示的最终产物酰胺基取代的橙皮素衍生物。
本发明的优点是:
本发明所涉及的酰胺基取代的橙皮素类衍生物能够成浓度依赖性抑制no的释放,减少炎症介质il-6和tnf-α的产生,相较于吲哚美辛和塞来昔布,显示出更好的抑制炎症活性,并且明显抑制一氧化氮合酶(inos)和cox-2的表达。表明该类化合物具有发展成为抗炎的药物的潜力和价值,有望成为抗炎活性候选药物。
附图说明
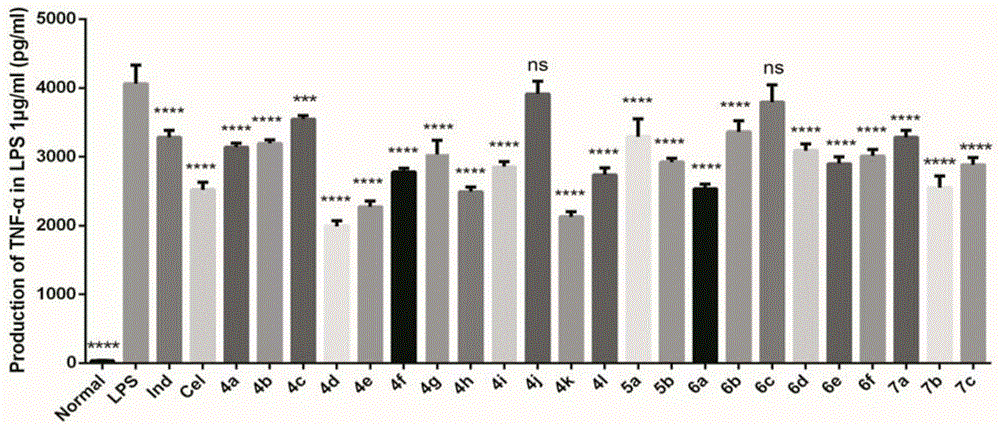
图1所示为化合物在10μm浓度下对lps刺激raw264.7细胞tnf-α分泌的抑制作用,10μm的吲哚美辛(ind)和塞来昔布(cel)作为阳性对照药物。
图2所示为化合物在10μm浓度下对lps刺激raw264.7细胞il-6分泌的抑制作用,10μm的吲哚美辛(ind)和塞来昔布(cel)作为阳性对照药物。
图3所示为化合物4d在(20,10,5,2.5,1.25)μm浓度下对lps刺激raw264.7细胞tnf-α产生的抑制作用,10μm的吲哚美辛(ind)和塞来昔布(cel)作为阳性对照药物。
图4所示为化合物4d在(20,10,5,2.5,1.25)μm浓度下对lps刺激raw264.7细胞il-6分泌的抑制作用,10μm的吲哚美辛(ind)和塞来昔布(cel)作为阳性对照药物
图5所示为化合物4d在(20,10,5)μm浓度下对lps刺激raw264.7细胞产生的抑cox-2和inos具有抑制作用,并且成浓度依赖性,bay作为阳性对照药物。
具体实施方式
以下结合具体的实例对本发明的技术方案做进一步说明,除非特别说明,本发明采用的试剂、设备和方法为本技术领域常规市购的试剂、设备和常规使用的方法。
本发明7-o-酰胺基取代的橙皮素类衍生物的制备方法,主要合成路线如下:
实施例1
化合物1的合成:
称取橙皮苷(72g,约0.12mol)倒入1000ml圆底烧瓶中,加入720ml10%浓硫酸乙醇溶液,置于油浴锅中搅拌均匀后,加热回流,反应8h后,冷却后,倒入冰水中,有固体析出,静置,抽滤,干燥。将粗品用乙醇加热溶解后,活性炭脱色,过滤。滤液减压回收乙醇,固体用乙醇和二氯甲烷重结晶,析出土白色固体,抽滤,干燥,得到橙皮素粉末(31.5g),产率87%。1hnmr(400mhz,dmso)δ12.14(s,1h,5-oh),6.94–6.92(m,j=5.1,3.2hz,2h,2’-h,5’-h),6.87(dd,j=8.3,1.9hz,1h,6’-h),5.90(d,j=2.1hz,1h,8-h),5.89(d,j=2.1hz,1h,6-h),5.42(dd,j=12.3,3.0hz,1h,2-h),3.77(s,3h,och3),3.19(dd,j=17.1,12.3hz,1h,3-h),2.71(dd,j=17.1,3.1hz,1h,3-h).13cnmr(101mhz,dmso)δ196.61,167.22,163.92,163.24,148.34,146.85,131.54,118.20,114.45,112.34,102.21,96.31,95.49,78.68,56.07,42.46.hr-ms(esi):calcd.c16h14o6,[m+h]+m/z:303.0875,found:303.0881.
化合物1的化学式如下:
实施例2
化合物2的合成:
称取化合物1,即橙皮素(30.2g,约0.1mol)倒入500ml圆底烧瓶中,加入300mldmf溶液,搅拌溶解后,加入30gkhco3,搅拌均匀后;再加入20.8gkco3,搅拌均匀后;加入2.5倍量约41.8g溴乙酸乙酯,室温反应30min,倒入分液漏斗,用乙酸乙酯和饱和食盐水反复萃取,洗去dmf。加入适量无水naso4干燥,过滤,减压回收乙酸乙酯,得到油状液体,用少量二氯甲烷加热溶解后,加热状态下加入大量乙醇,静置冷却,有白色固体析出。抽滤,干燥,得白色固体。将白色固体用二氯甲烷和乙醚重结晶,静置冷却,析出白色针状晶体,抽滤,干燥,得到化合物2(约19.8g),产率50%。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),6.98–6.91(m,2h,2’-h,5’-h),6.89(dd,j=8.4,1.5hz,1h,6’-h),6.11(d,j=2.1hz,1h,8-h),6.09(d,j=2.1hz,1h,6-h),5.49(dd,j=12.5,2.7hz,1h,2-h),4.87(s,2h,aroch2c=o),4.17(q,j=7.1hz,2h,cch2oc=o),3.78(s,3h,och3),3.28(dd,j=17.1,12.6hz,1h,3-h),2.75(dd,j=17.1,2.9hz,1h,3-h),1.21(t,j=7.1hz,3h,ch3coc=o).13cnmr(101mhz,dmso)δ197.43,168.50,166.08,163.54,163.18,148.43,146.94,131.35,118.24,114.59,112.37,103.46,95.65,94.74,78.98,65.22,61.32,56.10,42.60,14.48.hr-ms(esi):calcd.c20h20o8,[m+h]+m/z:389.1252,found:389.1257.
化合物2的化学式如下:
实施例3
化合物3的合成:
称取化合物2(19.4g,50mmol),倒入1000ml烧杯中,加入100ml10%乙醇水溶液分散溶解,置于冰浴中,搅拌30min后,滴加冰浴过的10%naoh水溶液,调节ph至12-13,搅拌反应30min后,慢慢滴加冰浴过的1mol/l稀盐酸,滴加过程中,有白色固体析出,调节ph至3-4,静置;抽滤,烘干,减压干燥。得淡黄色粉末,即为化合物3(约16.5g),产率92%。1hnmr(400mhz,dmso)δ12.07(s,1h,5-oh),9.21(s,1h,3’-oh),6.97–6.92(m,2h,2’-h,5’-h),6.89(dd,j=8.4,1.8hz,1h,6’-h),6.07(d,j=2.2hz,1h,8-h),6.06(d,j=2.2hz,1h,6-h),5.48(dd,j=12.5,2.9hz,1h,2-h),4.76(s,2h,aroch2c=o),3.77(s,3h,och3),3.26(dd,j=17.1,12.5hz,1h,3-h),2.75(dd,j=17.1,3.0hz,1h,3-h).13cnmr(101mhz,dmso)δ197.33,169.97,166.25,163.49,163.11,148.41,146.86,131.30,118.29,114.49,112.34,103.34,95.59,94.69,78.93,65.11,56.08,42.53.hr-ms(esi):calcd.c18h16o8,[m+h]+m/z:361.0919,found:361.0933.
化合物3的化学结构如下:
实施例4
化合物4a的合成:
称取化合物3(720mg,2mmol)于100ml圆底烧瓶中,加入40ml无水无醇氯仿分散溶解,搅拌均匀后,加入hobt(6mmol,811mg)和edc·hcl(4mmol,780mg),搅拌均匀后,加入400μl三乙胺,室温反应1h。加入750g25-30%甲胺水溶液(约6mmol),室温反应3h。用乙酸乙酯萃取,先用ph为3-4的饱和食盐水萃取,再用饱和碳酸氢钠溶液萃取,分别萃取两次。加入适量的无水naso4干燥,过滤,减压回收有机溶剂,固体用二氯甲烷和乙醇重结晶,静置冷却,有白色晶体析出,抽滤,干燥。得白色晶体,即为化合物4a(约573mg),产率72%。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),8.07(d,j=4.5hz,1h,nh),6.97–6.92(m,2h,2’-h,5’-h),6.88(dd,j=8.4,1.8hz,1h,6’-h),6.11(d,j=2.2hz,1h,8-h),6.10(d,j=2.2hz,1h,6-h),5.49(dd,j=12.5,2.9hz,1h,2-h),4.54(s,2h,aroch2c=o),3.78(s,3h,och3),3.27(dd,j=17.1,12.5hz,1h,3-h),2.75(dd,j=17.1,3.0hz,1h,3-h),2.65(d,j=4.6hz,3h,nch3).13cnmr(101mhz,dmso)δ197.41,167.61,166.09,163.48,163.13,148.41,146.93,131.36,118.21,114.56,112.38,103.42,95.84,94.85,78.94,67.49,56.11,42.59,25.82.hrms(esi):calcd.c19h19no7,[m+h]+m/z:374.1234,found:374.1241.
化合物4a的化学式如下:
实施例5
化合物4b的合成:
方法同实施例四,所不同的是用乙胺水溶液代替甲胺水溶液,得白色固体4b。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),8.14(t,j=5.5hz,1h,nh),6.95–6.93(m,2h,2’-h,5’-h),6.88(dd,j=8.4,1.8hz,1h,6’-h),6.12(d,j=2.2hz,1h,8-h),6.10(d,j=2.2hz,1h,6-h),5.49(dd,j=12.4,2.9hz,1h,2-h),4.53(s,2h,aroch2c=o),3.78(s,3h,och3),3.27(dd,j=17.2,12.5hz,1h,3-h),3.19–3.10(m,2h,nch2),2.76(dd,j=17.1,3.0hz,1h,3-h),1.04(t,j=7.2hz,3h,ncch3).13cnmr(101mhz,dmso)δ197.39,166.86,166.16,163.48,163.11,148.41,146.93,131.37,118.19,114.55,112.38,103.41,95.82,94.88,78.93,67.48,56.10,42.58,33.71,15.18.hrms(esi):calcd.c20h21no7,[m+h]+m/z:388.1391,found:388.1403.
化合物4b的化学式如下:
实施例6
化合物4c的合成:
方法同实施例四,所不同的是用二甲胺水溶液代替甲胺水溶液,得白色固体4c。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),6.95–6.93(m,2h,2’-h,5’-h),6.91–6.86(m,1h,6’-h),6.09(d,j=2.1hz,1h,8-h),6.07(d,j=2.1hz,1h,6-h),5.47(dd,j=12.6,2.7hz,1h,2-h),4.91(s,2h,aroch2c=o),3.78(s,3h,och3),3.26(dd,j=17.1,12.7hz,1h,3-h),2.95(s,3h,nch3),2.83(s,3h,nch3),2.73(dd,j=17.1,2.9hz,1h,3-h).13cnmr(101mhz,dmso)δ197.29,166.87,166.71,163.42,163.07,148.41,146.93,131.41,118.24,114.59,112.37,103.16,95.86,94.83,78.96,66.18,56.11,42.62,35.80,35.41.hrms(esi):calcd.c20h21no7,[m+h]+m/z:388.1391,found:388.1401.
化合物4c的化学式如下:
实施例7
化合物4d的合成:
方法同实施例四,所不同的是用正丙胺代替甲胺,得白色固体4d。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),8.12(t,j=5.6hz,1h,nh),6.95–6.93(m,2h,2’-h,5’-h),6.88(dd,j=8.4,1.7hz,1h,6’-h),6.11(d,j=2.2hz,1h,8-h),6.09(d,j=2.2hz,1h,6-h),5.49(dd,j=12.4,2.8hz,1h,2-h),4.54(s,2h,aroch2c=o),3.78(s,3h,och3),3.27(dd,j=17.1,12.5hz,1h,3-h),3.08(dd,j=13.2,6.6hz,2h,nch2),2.76(dd,j=17.1,3.0hz,1h,3-h),1.52–1.36(m,2h,ncch2),0.83(t,j=7.4hz,3h,nccch3).13cnmr(101mhz,dmso)δ197.38,167.06,166.21,163.48,163.10,148.40,146.93,131.37,118.18,114.55,112.37,103.39,95.80,94.89,78.92,67.46,56.10,42.58,40.57,22.79,11.78.hrms(esi):calcd.c21h23no7,[m+h]+m/z:402.1557,found:402.1562.
化合物4d的化学式如下:
实施例8
化合物4e的合成:
方法同实施例四,所不同的是用异丙胺代替吡咯烷,得白色固体4e。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),7.96(d,j=7.8hz,1h,nh),6.95–6.93(m,2h,2’-h,5’-h),6.88(dd,j=8.3,1.8hz,1h,6’-h),6.11(d,j=2.2hz,1h,8-h),6.09(d,j=2.2hz,1h,6-h),5.49(dd,j=12.3,2.9hz,1h,2-h),4.51(s,2h,aroch2c=o),3.92(dq,j=13.4,6.6hz,1h,chnc=o),3.78(s,3h,och3),3.27(dd,j=17.1,12.4hz,1h,3-h),2.76(dd,j=17.1,3.0hz,1h,3-h),1.09(d,j=6.6hz,6h,(ch3)2cn).13cnmr(101mhz,dmso)δ197.36,166.31,166.11,163.49,163.08,148.39,146.93,131.39,118.17,114.54,112.37,103.37,95.77,94.89,78.90,67.44,56.09,42.58,40.85,22.68,22.68.hrms(esi):calcd.c21h23no7,[m+h]+m/z:402.1557,found:402.1562.
化合物4e的化学式如下:
实施例9
化合物4f的合成:
方法同实施例四,所不同的是用正丁胺基代替甲胺,得白色固体4f。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),8.10(t,j=5.7hz,1h,nh),6.94(dd,j=5.1,3.2hz,2h,2’-h,5’-h),6.88(dd,j=8.4,1.8hz,1h,6’-h),6.11(d,j=2.2hz,1h,8-h),6.09(d,j=2.2hz,1h,6-h),5.49(dd,j=12.4,2.9hz,1h,2-h),4.54(s,2h,aroch2c=o),3.78(s,3h,och3),3.26(dd,j=17.1,12.5hz,1h,3-h),3.11(dd,j=13.0,6.7hz,2h,nch2),2.76(dd,j=17.1,3.0hz,1h,3-h),1.46–1.34(m,2h,ncch2),1.33–1.18(m,2h,nccch2),0.86(t,j=7.3hz,3h,ncccch3).13cnmr(101mhz,dmso)δ197.37,167.01,166.21,163.49,163.11,148.40,146.93,131.38,118.17,114.54,112.37,103.38,95.82,94.87,78.94,67.47,56.10,42.60,38.46,31.62,19.97,14.11.hrms(esi):calcd.c22h25no7,[m+h]+m/z:416.1704,found:416.1717.
化合物4f的化学式如下:
实施例10
化合物4g的合成:
方法同实施例四,所不同的是用异丁胺基代替甲胺,得白色固体4g。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.12(s,1h,3’-oh),8.12(t,j=5.9hz,1h,nh),6.97–6.91(m,2h,2’-h,5’-h),6.88(dd,j=8.4,1.7hz,1h,6’-h),6.11(d,j=2.2hz,1h,8-h),6.09(d,j=2.2hz,1h,6-h),5.49(dd,j=12.4,2.9hz,1h,2-h),4.57(s,2h,aroch2c=o),3.78(s,3h,och3),3.26(dd,j=17.1,12.5hz,1h,3-h),2.94(t,j=6.4hz,2h,nch2),2.76(dd,j=17.1,3.0hz,1h,3-h),1.72(dp,j=13.4,6.7hz,1h,ncchc2),0.83(d,j=6.7hz,6h,ncc(ch3)2).13cnmr(101mhz,dmso)δ197.37,167.15,166.26,163.49,163.09,148.39,146.93,131.38,118.16,114.54,112.37,103.37,95.78,94.90,78.92,67.45,56.10,46.26,42.59,28.51,20.50,20.50.hrms(esi):calcd.c22h25no7,[m+h]+m/z:416.1704,found:416.1716.
化合物4g的化学式如下:
实施例11
化合物4h的合成:
方法同实施例四,所不同的是用叔丁胺代甲胺,得白色固体4h。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),7.61(br,1h,nh),6.97–6.91(m,2h,2’-h,5’-h),6.88(dd,j=8.4,1.7hz,1h,6’-h),6.08(d,j=2.2hz,1h,8-h),6.06(d,j=2.2hz,1h,6-h),5.49(dd,j=12.3,2.9hz,1h,2-h),4.48(s,2h,aroch2c=o),3.78(s,3h,och3),3.26(dd,j=17.1,12.4hz,1h,3-h),2.76(dd,j=17.1,3.0hz,1h,3-h),1.28(s,9h,nc(ch3)3).13cnmr(101mhz,dmso)δ197.33,166.48,166.41,163.51,163.07,148.39,146.93,131.39,118.18,114.54,112.38,103.31,95.61,94.84,78.89,67.51,56.09,50.89,42.57,28.87,28.87,28.87.hrms(esi):calcd.c22h25no7,[m+h]+m/z:416.1704,found:416.1717.
化合物4h的化学式如下:
实施例12
化合物4i的合成:
方法同实施例四,所不同的是用二乙胺代替甲胺,得白色固体4i。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),6.97–6.91(m,2h,2’-h,5’-h),6.89(d,j=8.2hz,1h,6’-h),6.08(d,j=1.9hz,1h,8-h),6.05(d,j=1.9hz,1h,6-h),5.48(dd,j=12.5,2.4hz,1h,2-h),4.88(s,2h,aroch2c=o),3.78(s,3h,och3),3.34–3.20(m,5h,n(ch2c)2,3-h),2.73(dd,j=17.1,2.7hz,1h,3-h),1.13(t,j=7.0hz,3h,ncch3),1.02(t,j=7.0hz,3h,ncch3).13cnmr(101mhz,dmso)δ197.29,166.83,165.82,163.45,163.08,148.41,146.93,131.40,118.23,114.58,112.37,103.19,95.78,94.85,79.65,78.96,66.38,56.10,42.62,40.86,14.53,13.33.hrms(esi):calcd.c22h25no7,[m+h]+m/z:416.1704,found:416.1714.
化合物4i的化学式如下:
实施例13
化合物4j的合成:
方法同实施例四,所不同的是用环丙胺代替甲胺,得白色固体4j。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),8.17(d,j=4.0hz,1h,nh),6.95–6.93(m,2h,2’-h,5’-h),6.88(dd,j=8.4,1.7hz,1h,6’-h),6.10(d,j=2.2hz,1h,8-h),6.08(d,j=2.2hz,1h,6-h),5.49(dd,j=12.4,2.8hz,1h,2-h),4.51(s,2h,aroch2c=o),3.78(s,3h,och3),3.27(dd,j=17.1,12.5hz,1h,3-h),2.76(dd,j=17.1,3.0hz,1h,3-h),2.72–2.64(m,1h,nch),0.68–0.60(m,2h,ncch2),0.51–0.43(m,2h,ncch2).13cnmr(101mhz,dmso)δ197.38,168.33,166.24,163.46,163.09,148.40,146.93,131.37,118.19,114.55,112.37,103.38,95.78,94.84,78.92,67.37,56.09,42.58,22.64,6.05,6.05.hrms(esi):calcd.c21h21no7,[m+h]+m/z:400.1401,found:400.1407.
化合物4j的化学式如下:
实施例14
化合物4k的合成:
方法同实施例四,所不同的是用环戊胺代替甲胺,得白色固体4k。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),8.04(d,j=7.4hz,1h,nh),6.95–6.93(m,2h,2’-h,5’-h),6.88(dd,j=8.4,1.7hz,1h,6’-h),6.10(d,j=2.2hz,1h,8-h),6.08(d,j=2.2hz,1h,6-h),5.49(dd,j=12.3,2.8hz,1h,2-h),4.52(s,2h,aroch2c=o),4.12–3.99(m,1h,nch),3.78(s,3h,och3),3.26(dd,j=17.1,12.4hz,1h,3-h),2.76(dd,j=17.1,3.0hz,1h,3-h),1.80(dt,j=12.6,6.1hz,2h,ncch2),1.72–1.58(m,2h,ncch2),1.56–1.46(m,2h,nccch2),1.46–1.34(m,2h,nccch2).13cnmr(101mhz,dmso)δ197.35,166.54,166.37,163.49,163.08,148.39,146.93,131.39,118.17,114.54,112.36,103.34,95.73,94.87,78.90,67.42,56.09,50.63,42.58,32.54,32.54,23.92,23.92.hrms(esi):calcd.c23h25no7,[m+h]+m/z:428.1714,found:428.1723.
化合物4k的化学式如下:
实施例15
化合物4l的合成:
方法同实施例四,所不同的是用环己胺代替甲胺,得白色固体4l。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),7.95(d,j=8.0hz,1h,nh),6.95–6.93(m,2h,2’-h,5’-h),6.88(dd,j=8.4,1.7hz,1h,6’-h),6.11(d,j=2.1hz,1h,8-h),6.09(d,j=2.2hz,1h,6-h),5.49(dd,j=12.3,2.8hz,1h,2-h),4.53(s,2h,aroch2c=o),3.78(s,3h,och3),3.60(m,1h,nch),3.26(dd,j=17.1,12.4hz,1h,3-h),2.76(dd,j=17.1,3.0hz,1h,3-h),1.78–1.62(m,4h,nc(ch2)2),1.57–1.54(m,1h,ncccch),1.34–1.18(m,4h,ncc(ch2)2),1.15–1.09(m,1h,ncccch).13cnmr(101mhz,dmso)δ197.35,166.33,166.07,163.49,163.07,148.39,146.93,131.39,118.16,114.54,112.36,103.35,95.74,94.89,78.90,67.42,56.09,47.96,42.58,32.71,32.71,25.61,25.07,25.07.hrms(esi):calcd.c24h27no7,[m+h]+m/z:442.1860,found:442.1870.
化合物4l的化学式如下:
实施例16
化合物5a的合成:
方法同实施例四,所不同的是用吡咯烷代替甲胺,得白色固体5a。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),6.95–6.93(m,2h,2’-h,5’-h),6.89(dd,j=8.4,1.8hz,1h,6’-h),6.09(d,j=2.3hz,1h,8-h),6.07(d,j=2.3hz,1h,6-h),5.47(dd,j=12.7,2.8hz,1h,2-h),4.81(s,2h,aroch2c=o),3.78(s,3h,och3),3.42(t,j=6.8hz,2h,ch2nc=o),3.30(t,j=6.8hz,2h,ch2nc=o),3.26((dd,j=17.1,12.4hz,1h,3-h),2.72(dd,j=17.1,3.0hz,1h,3-h),1.88(p,j=6.7hz,2h,ch2cnc=o),1.81–1.71(p,j=6.7hz,2h,ch2cnc=o).13cnmr(101mhz,dmso)δ197.30,166.85,165.17,163.42,163.08,148.42,146.92,131.40,118.26,114.59,112.36,103.18,95.85,94.79,78.98,66.59,56.11,46.03,44.93,42.63,26.07,23.97.hrms(esi):calcd.c22h23no7,[m+h]+m/z:414.1557,found:414.1563.
化合物5a的化学式如下:
实施例17
化合物5b的合成:
方法同实施例四,所不同的是用四氢噻唑代替甲胺,得白色固体5b。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),6.95–6.93(m,2h,2’-h,5’-h),6.89(dd,j=8.3,1h,6’-h),6.13(d,j=2.2hz,1h,8-h),6.10(d,j=2.2hz,1h,6-h),5.48(dd,j=12.6,2.8hz,1h,2-h),4.94(s,2h,aroch2c=o),4.52(br,2h,sch2n),3.78(s,3h,och3),3.72(t,j=6.2hz,1h,nchcs),3.67(t,j=6.3hz,1h,nchcs)),3.27(dd,j=17.1,12.7hz,1h,3-h),3.11(t,j=6.2hz,1h,ncchs),2.98(t,j=6.3hz,1h,ncchs),2.73(dd,j=17.1,3.0hz,1h,3-h).13cnmr(101mhz,dmso)δ197.34,166.67,165.39,163.43,163.11,148.42,146.92,131.38,118.26,114.59,112.36,103.25,95.87,94.83,78.98,66.61,56.11,48.59,47.54,42.62,31.25.hrms(esi):calcd.c21h21no7s,[m+h]+m/z:432.1111,found:432.1126.
化合物5b的化学式如下:
实施例18
化合物6a的合成:
方法同实施例四,所不同的是用哌啶代替甲胺,得白色固体6a。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),6.94(d,j=7.1hz,2h,2’-h,5’-h),6.89(d,j=8.2hz,1h,6’-h),6.08(d,j=2.1hz,1h,8-h),6.06(d,j=2.1hz,1h,6-h),5.48(dd,j=12.3,2.1hz,1h,2-h),4.90(s,2h,aroch2c=o),3.78(s,3h,och3),3.41(m,2h,nch2),3.34(m,2h,nch2),3.26(dd,j=17.0,12.8hz,1h,3-h),2.73(dd,j=17.0,2.4hz,1h,3-h),1.70–1.34(m,6h,nc(ch2)2ch2).13cnmr(101mhz,dmso)δ197.30,166.83,165.01,163.44,163.08,148.41,146.93,131.41,118.23,114.58,112.36,103.18,95.81,94.83,78.96,66.47,56.10,45.42,42.62,42.62,26.34,25.72,24.37.hrms(esi):calcd.c23h25no7,[m+h]+m/z:428.1704,found:428.1718.
化合物6a的化学式如下:
实施例19
化合物6b的合成:
方法同实施例四,所不同的是用3-羟甲基哌啶代替甲胺,得白色固体6b。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),6.97–6.91(m,2h,2’-h,5’-h),6.89(dd,j=8.3,1.6hz,1h,6’-h),6.08(d,j=2.3hz,1h,8-h),6.06(d,j=2.3hz,1h,6-h),5.48(dd,j=12.5,2.5hz,1h,2-h),4.91(s,2h,aroch2c=o),4.61–4.55(m,1h,oh),3.78(s,3h,och3),3.66(d,j=13.0hz,1h,ch2oh),3.36(m,1h,ch2oh),3.29–3.12(m,3h,3-h,nch2),3.01–2.77(m,2h,nch2),2.73(dd,j=17.1,2.8hz,1h,3-h),1.79–1.50(m,3h,chch2ch2),1.44–1.38(m,1h,chch2ch2),1.34–1.19(m,1h,chch2ch2).13cnmr(101mhz,dmso)δ197.29,166.82,165.09,163.44,163.07,148.41,146.93,131.41,118.24,114.58,112.37,103.19,95.80,94.84,78.96,66.54,64.11,56.10,47.60,45.40,42.63,39.08,27.23,25.40.hr-ms(esi):calcd.c24h27no8,[m+h]+m/z:458.1819,found:458.1828.
化合物6b的化学式如下:
实施例20
化合物6c的合成:
方法同实施例四,所不同的是用2-羟甲基哌啶代替甲胺,得白色固体6c。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),6.97–6.92(m,2h,2’-h,5’-h),6.89(dd,j=8.4,1.7hz,1h,6’-h),6.07(d,j=15.6hz,2h,8-h,6-h),5.48(dd,j=12.6,2.7hz,1h,2-h),4.92(s,2h,aroch2c=o),4.24(d,j=12.9hz,1h,oh),3.91–3.71(m,4h,och3,ch2oh),3.55–3.48(m,2h,nch,ch2oh),3.45–3.37(m,2h,nch2),3.26(dd,j=17.1,12.7hz,1h,3-h),2.72(dd,j=17.0hz,2.7hz,1h,3-h),1.70–1.34(m,5h,ch2ch2ch2),1.31–1.18(m,1h,ch2ch2ch2).13cnmr(101mhz,dmso)δ197.25,167.12,166.26,163.44,163.05,148.42,146.93,131.45,118.26,114.60,112.38,103.07,95.82,94.82,78.96,66.42,59.45,56.11,53.35,42.65,36.56,25.92,25.43,21.22.hr-ms(esi):calcd.c24h27no8,[m+h]+m/z:458.1819,found:458.1827.
化合物6c的化学式如下:
实施例21
化合物6d的合成:
方法同实施例四,所不同的是用n-甲基哌嗪代替甲胺,反应后处理,用乙酸乙酯萃取,不用酸性饱和食盐水萃取,只用饱和碳酸氢钠萃取,无水naso4干燥,过滤,旋干,用硅胶柱层析纯化,洗脱溶剂为氯仿,得白色固体6d。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.14(s,1h,3’-oh),6.97–6.91(m,2h,2’-h,5’-h),6.89(dd,j=8.3,1.8hz,1h,6’-h),6.10(d,j=2.2hz,1h,8-h),6.07(d,j=2.2hz,1h,6-h),5.48(dd,j=12.6,2.8hz,1h,2-h),4.92(s,2h,aroch2c=o),3.78(s,3h,och3),3.43(m,2h,ncch2nc=o),3.39(m,2h,ncch2nc=o),3.26(dd,j=17.1,12.7hz,1h,3-h),2.73(dd,j=17.1,3.0hz,1h,3-h),2.32(m,2h,nch2cnc=o),2.26(m,2h,nch2cnc=o),2.17(s,3h,nch3).13cnmr(101mhz,dmso)δ197.30,166.76,165.37,163.44,163.08,148.41,146.93,131.40,118.23,114.58,112.36,103.20,95.83,94.84,78.96,66.30,56.10,54.99,54.67,46.12,44.28,42.62,41.61.hrms(esi):calcd.c23h26n2o7,[m+h]+m/z:443.1823,found:443.1833.
化合物6d的化学式如下:
实施例22
化合物6e的合成:
方法同实施例二十一,所不同的是用n-乙基哌嗪代n-甲基哌嗪,得白色固体6e。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.14(s,1h,3’-oh),6.96–6.91(m,2h,2’-h,5’-h),6.89(d,j=8.2hz,1h,6’-h),6.10(d,j=1.7hz,1h,8-h),6.07(d,j=1.9hz,1h,6-h),5.47(dd,j=12.6,2.6hz,1h,2-h),4.92(s,2h,aroch2c=o),3.78(s,3h,och3),3.43(m,2h,ncch2nc=o),3.39(m,2h,ncch2nc=o),3.26(dd,j=17.1,12.7hz,1h,3-h),2.73(dd,j=17.1,2.7hz,1h,3-h),2.42–2.26(m,6h,n(ch2c)2nc=o,nch2c),0.99(t,j=7.1hz,3h,ncch3).13cnmr(101mhz,dmso)δ197.30,166.77,165.32,163.44,163.08,148.41,146.93,131.40,118.23,114.58,112.36,103.20,95.83,94.85,78.96,66.31,56.10,52.85,52.40,51.97,44.41,42.63,41.73,12.33.hrms(esi):calcd.c24h28n2o7,[m+h]+m/z:457.1979,found:457.1985.
化合物6e的化学式如下:
实施例23
化合物6f的合成:
方法同实施例四,所不同的是用吗啉代替甲胺,得白色固体6f。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),6.96–6.92(m,2h,2’-h,5’-h),6.89(dd,j=8.4,1.7hz,1h,6’-h),6.11(d,j=2.2hz,1h,8-h)),6.09(d,j=2.2hz,1h,6-h)),5.48(dd,j=12.6,2.7hz,1h,2-h)),4.94(s,2h,aroch2c=o),3.78(s,3h,och3),3.63–3.52(m,4h,o(ch2c)2n),3.42(m,4h,o(cch2)2n),3.27(dd,j=17.1,12.7hz,1h,3-h),2.73(dd,j=17.1,2.9hz,1h,3-h).13cnmr(101mhz,dmso)δ197.32,166.75,165.65,163.44,163.10,148.42,146.92,131.40,118.25,114.59,112.36,103.22,95.86,94.85,78.98,66.49,66.37,66.21,56.10,44.92,42.62,42.01.hr-ms(esi):calcd.c22h23no8,[m+h]+m/z:430.1506,found:430.1511.
化合6f的化学式如下:
实施例24
化合物7a的合成:
方法同实施例四,所不同的是用乙醇胺代替甲胺,得白色固体7a。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),8.09(t,j=5.6hz,1h,nh),6.95–6.93(m,2h,2’-h,5’-h),6.89(dd,j=8.4,1.8hz,1h,6’-h),6.12(d,j=2.2hz,1h,8-h),6.10(d,j=2.2hz,1h,6-h),5.49(dd,j=12.4,2.9hz,1h,2-h),4.74(t,j=5.5hz,1h,oh),4.55(s,2h,aroch2c=o),3.78(s,3h,och3),3.43(q,j=5.9hz,2h,ncch2o),3.27(dd,j=17.2,12.5hz,1h,3-h),3.20(q,j=6.0hz,2h,nch2co),2.76(dd,j=17.1,3.0hz,1h,3-h).13cnmr(101mhz,dmso)δ197.38,167.29,166.16,163.49,163.12,148.41,146.93,131.37,118.21,114.56,112.40,103.42,95.82,94.87,78.93,67.40,60.06,56.11,42.58,41.71.hr-ms(esi):calcd.c20h21no8,[m+h]+m/z:404.1360,found:404.1369.
化合物7a的化学式如下:
实施例25
化合物7b的合成:
方法同实施例二十一,所不同的是用n,n-二甲基乙二胺代替n-甲基哌嗪,得白色固体7b。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.15(s,1h,3’-oh),8.04(t,j=5.6hz,1h,nh),6.95–6.93(m,2h,2’-h,5’-h),6.88(dd,j=8.4,1.7hz,1h,6’-h),6.11(d,j=2.2hz,1h,8-h),6.09(d,j=2.2hz,1h,6-h),5.49(dd,j=12.4,2.8hz,1h,2-h),4.55(s,2h,aroch2c=o),3.78(s,3h,och3),3.32–3.16(m,3h,3-h,ncch2nc=o),2.76(dd,j=17.1,3.0hz,1h,3-h),2.30(t,j=6.6hz,2h,nch2cnc=o),2.13(s,6h,(ch3)2n).13cnmr(101mhz,dmso)δ197.25,167.12,166.27,163.44,163.05,148.42,146.93,131.45,118.26,114.60,112.38,103.07,95.82,94.80,78.96,66.42,60.24,59.45,56.11,53.35,42.65,36.56.hrms(esi):calcd.c22h26n2o7,[m+h]+m/z:431.1823,found:431.1830.
化合物7b的化学式如下:
实施例26
化合物7c的合成:
方法同实施例二十一,所不同的是用2-(4-吗啉基)乙胺代替n-甲基哌嗪,得白色固体7c。1hnmr(400mhz,dmso)δ12.08(s,1h,5-oh),9.13(s,1h,3’-oh),8.02(t,j=5.6hz,1h,nh),6.95–6.93(m,2h,2’-h,5’-h),6.88(dd,j=8.3,1.8hz,1h,6’-h),6.11(d,j=2.1hz,1h,8-h),6.10(d,j=2.1hz,1h,6-h),5.48(dd,j=12.4,2.8hz,1h,2-h),4.56(s,2h,aroch2c=o),3.78(s,3h,och3),3.58–3.46(m,4h,(och2cn)2),3.33–3.18(m,3h,ncch2nc=o,3-h),2.76(dd,j=17.1,3.0hz,1h,3-h),2.37–2.34(m,j=6.5hz,6h,(occh2n)2,nch2cnc=o).13cnmr(101mhz,dmso)δ197.39,167.16,166.13,163.50,163.14,148.42,146.93,131.35,118.20,114.56,112.37,103.43,95.86,94.87,78.98,67.45,66.61,66.61,57.62,56.10,53.65,42.60,35.98.hrms(esi):calcd.c24h28n2o8,[m+h]+m/z:473.1928,found:473.1932.
化合物7c的化学式如下:
实施例27
测试化合物对no释放和炎症因子tnf-α和il-6分泌的抑制作用:
结果用ic50值表示,以吲哚美辛(ind)和塞来昔布(cel)作为阳性对照药物。所有的测试均在powerwavexs2型全波长酶标仪上进行,在37℃的条件下测定。数据分析利用软件origin进行处理。
实验步骤和结果:
(1)化合物溶液的配制
将测试化合物配成100μm浓度(溶剂:dmso),-20℃低温保存,使用时用所需的细胞培养基稀释到所需浓度。
(2)细胞的培养
本实验所用的raw264.7巨噬细胞为贴壁生长细胞株,采用含10%胎牛血清的dmem培养液进行培养。培养环境为37℃,5%的co2培养箱,每天更换一次培养液,取对数生长期的细胞进行实验。
(3)no释放含量的测定
采用吲哚美辛及塞来昔布,经典抗炎药物作为本系列药物对照。具体实验步骤如下:取对数增殖期的raw264.7细胞,以每孔接种7万个细胞于24孔板种,培养箱中培养一天,弃去培养基后,每孔中加入现配的不同浓度的药物(1.25,2.5,5,10,20μm)继续培养1小时后,每孔加入1μg/ml的lps刺激24小时,用空白对照加入等量的培养基。共培养24小时后,吸取各孔的上清液,离心4℃,12000rpm/min的转速离心5分钟,收集上清液。一氧化氮的测定用griessreagent反应。依次加入griessreagentⅰ和griessreagentⅱ各50μl。反应1分钟,用酶标仪540nm测定吸光度值。
表1
表1所示为化合物在10μm浓度下对lps刺激raw264.7细胞no释放的抑制作用,10μm的吲哚美辛(ind)和塞来昔布(cel)作为阳性对照药物,以及抑制no的ic50值。
实验结果为三次独立实验的平均值,数据表示为平均±sd(n=3)值,p(*)<0.05,p(**)<0.01,p(***)<0.001,p(****)<0.0001时,认为差异具有统计学意义。
结果讨论:所合成的化合物都有一定的no抑制效果,在给药浓度为10μm时,化合物4b-4g,4i,4k-4l,5b,6a-6b,6d-6f,7a,均显示出比吲哚美辛更好的抑制率以及ic50;其中化合物4d,4e,4g,4k,6a对no的抑制率以及ic50优于塞来昔布。证明这些药物明显抑制no的释放。
(4)化合物对tnf-α和il-6分泌的抑制作用
同样取对数增殖期的raw264.7细胞。以每孔7×104个/孔的细胞密度接种细胞于24孔板中。加不同浓度药物培养1小时(药物浓度:5,10,20,30,40μm),空白对照不做任何处理只加等量的培养基,再加入1μg/mllps溶液刺激,继续培养24小时。吸取各孔上清液,离心机4℃,10000rpm/min的转速离心5分钟,取上清液。按照elisa试剂盒说明操作。然后450nm波长处测定各孔值。
实验结果为三次独立实验的平均值,数据表示为平均±sd(n=3)值,p(*)<0.05,p(**)<0.01,p(***)<0.001,p(****)<0.0001时,认为差异具有统计学意义。
结果讨论:如图1和图2所示,结果证明化合物对炎症因子的分泌有抑制作用,其中4d抑制炎症因子il-6和tnf-α的释放效果最明显。并且明显优于吲哚美辛与塞来昔布。这些化合物中4d最有可能发展成为抗炎药物。
我们进一步对4d抑制炎症因子的表达与该化合物浓度关系进行探究。
实验结果为三次独立实验的平均值,数据表示为平均±sd(n=3)值,p(*)<0.05,p(**)<0.01,p(***)<0.001,p(****)<0.0001时,认为差异具有统计学意义。
结果表明:如图3和图4所示,化合物4d能成浓度依赖性抑制炎症因子表达。其抑制率明显优于10μm下的吲哚美辛以及塞来昔布。
(5)分子水平上探究4d对炎症因子cox-2和inos表达的影响
不同浓度梯度化合物的处理raw264.7细胞1h后,用lps(1mg/ml)处理后,收集培养上清液,收集细胞并用ripa裂解缓冲液(beyotime,中国)和磷酸酶抑制剂(beibokitchina)裂解。离心(4℃,30分钟,12,000rpm),使用bca蛋白质测定试剂盒(beyotime,china)测定总蛋白质浓度。将含有总蛋白质的裂解物在sds聚丙烯酰胺凝胶上分级分离并转移至聚偏二氟乙烯膜(pvdf)(millipore,usa)。用tbst中的5%脱脂乳或3%bsa封闭膜,并在4℃下与它们各自的一抗孵育过夜:β-肌动蛋白(1:1000稀释;abcam,usa),inos(1:1000稀释;abcam,usa),cox-2(1:1000稀释;abcam,usa);用tbst洗涤三次后,将膜与二抗在室温下在振荡器上孵育1小时。在用tbst洗涤三次后,通过超灵敏增强化学发光(ecl)底物(ecl-plus,thermosscientific)显现蛋白质条带。westernblot结果表明化合物4d成浓度依赖性明显抑制cox-2和inos的表达,bay11-7082是产生cox-2和inos主要通路的抑制剂,作为试验阳性对照药物。
实验结果为三次独立实验的平均值,数据表示为平均±sd(n=3)值,p(*)<0.05,p(**)<0.01,p(***)<0.001,p(****)<0.0001时,认为差异具有统计学意义。
结果表明:如图5所示,化合物4d能成浓度依赖性在蛋白水平抑制炎症因子cox-2和inos的表达。
- 还没有人留言评论。精彩留言会获得点赞!