本发明属于生物医学领域,涉及一种检测j亚群禽白血病病毒的cpa引物组、cpa核酸试纸条试剂盒及其应用。
背景技术:
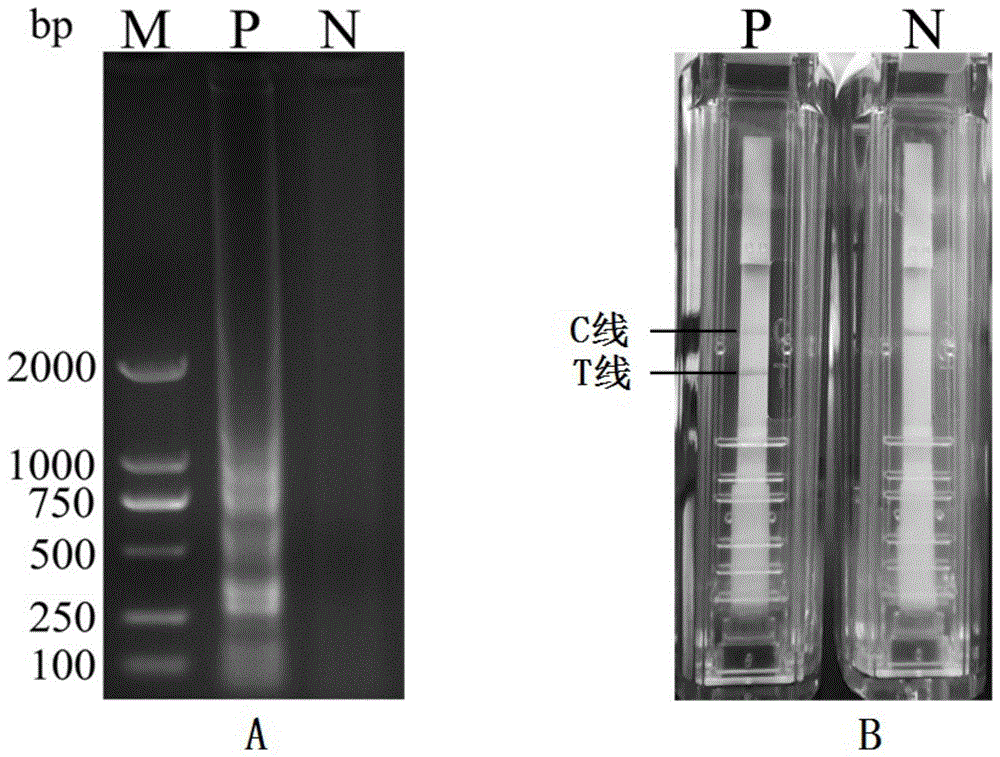
:j亚群禽白血病病毒(subgroupjavianleukosisvirus,alv-j)是20世纪80年代从肉用型鸡中分离鉴定的禽白血病病毒新亚群,主要引起肉用型鸡的髓细胞瘤。之后,j亚群禽白血病在我国呈现出不断发展的态势,宿主范围已由肉用型鸡向蛋鸡和地方鸡种蔓延。j亚群禽白血病往往导致病鸡生产性能降低,死亡率明显升高,给我国养禽业造成严重的经济损失,因此建立alv-j的快速检测方法意义重大。传统的病毒分离和鉴定所需时间过长,不能满足快速诊断的要求;pcr、荧光定量pcr等分子生物学检测方法对仪器设备要求较高,不利于基层单位使用;现有alv-j的lamp检测方法虽对仪器设备要求不高,但却存在假阳率高、弱阳性结果判别不够准确,且容易受气溶胶污染的问题。交叉引物恒温扩增(crossprimingamplification,cpa)技术是由杭州优思达生物公司研发,近年来发展比较迅速的一种快速检测方法,是中国首个具有自主知识产权的体外核酸扩增技术。根据体系中交叉引物数量的不同,这种技术可以分为单交叉扩增(singlecrossingcpa)和双交叉扩增(doublecrossingcpa)两种。cpa技术具有特异性高、敏感性强的特性,同时不需昂贵仪器,操作过程更加简便快速,在55~65℃恒温对核酸进行指数级扩增,整个反应只需30~60min,扩增产物用一次性核酸检测试纸条检测,且闭管操作,使结果判定直观、客观,且可有效避免气溶胶污染,已被推广用于感染性疾病的诊断和病原体的检测。目前,国内外针对alv-j的cpa检测方法还未见报道。技术实现要素:本发明的首要目的在于弥补现有技术的缺点与不足,提供一种检测j亚群禽白血病病毒的cpa引物组。本发明的另一目的在于提供一种检测j亚群禽白血病病毒(alv-j)的cpa核酸试纸条试剂盒。本发明的再一目的在于提供上述cpa引物组或cpa核酸试纸条试剂盒的应用。本发明的目的通过下列技术方案实现:一种用于检测alv-j的cpa引物组,包含如下引物:引物引物序列(5’-3’)f3ggatgacgtgagtaagaaagb3cgtaccataggtaacagacgf2gggaaggtgagcaagaaggf1cgtcagcaacaagcaagagacprgggaaggtgagcaagaaggcaagcaggtgcggaatgg其中,引物f1的5'端标记fam,引物f2的5'端标记biotin。上述检测alv-j的cpa引物组在制备用于cpa检测alv-j试剂盒、扩增反应试剂中的应用。一种用于检测alv-j的cpa核酸试纸条试剂盒,包括上述cpa引物组和核酸检测试纸条。一种用于检测alv-j的cpa核酸试纸条试剂盒,包含上述cpa引物组和全封闭式靶核酸扩增物快速检测装置。所述的全封闭式靶核酸扩增物快速检测装置为杭州优思达生物技术有限公司产品,该检测装置将核酸检测试纸条置入一个掌上塑料检测装置内得到。所述的核酸检测试纸条为通用型一次性核酸检测试纸条。所述的用于检测alv-j的cpa核酸试纸条试剂盒,还包括:betaine溶液、mg2+溶液、dntps混合物溶液、bstdna聚合酶(bstdnapolymerase)、反应缓冲液。更优选的,所述的试剂盒包含10×反应缓冲液(10×thermopolbuffer)、浓度为5mol·l-1的betaine溶液、浓度为10mmol·l-1的dntps混合物溶液、浓度为100mmol·l-1的mgso4溶液、浓度为8u·μl-1的bstdnapolymerase、浓度为10μmol·l-1的引物cpr、浓度为10μmol·l-1的引物b3、浓度为10μmol·l-1的引物f1、浓度为10μmol·l-1的引物f2、浓度为10μmol·l-1的引物f3。上述用于检测alv-j的cpa核酸试纸条试剂盒在鉴定和/或检测alv-j中的应用。一种鉴定和/或非诊断性检测alv-j的方法,包括如下步骤:(1)配置反应体系,见下表:组分用量(ul)终浓度10×thermopolbuffer2.51×/μl5mol·l-1betaine2.00.4mol·l-110mmol·l-1dntps1.750.7mmol·l-1100mmol·l-1mg2+1.04.0mmol·l-18u·μl-1bstdnapolymerase1.00.32u·μl-110μmol·l-1cpr2.51.0μmol·l-110μmol·l-1f12.00.8μmol·l-110μmol·l-1f22.00.8μmol·l-110μmol·l-1b31.50.6μmol·l-110μmol·l-1f31.50.6μmol·l-1模板1.0/ddh20补足至25μl/所述的模板为待检测样品dna;(2)反应:将步骤(1)中的cpa反应体系60℃恒温反应30~60min(优选为60min),得到的产物用核酸检测试纸条检测,5~10min后观察结果;(3)结果判读,直接肉眼观察1)阳性(+):试纸条出现两条红色条带,一条位于质控区(c线control-line),一条位于检测区(t线test-line);2)阴性(-):试纸条的质控区出现一条红色条带(c线control-line),检测区没有条带(t线test-line);3)无效:试纸条的质控区(c线control-line)和检测区(t线test-line)均未出现条带。本发明相对于现有技术具有如下的优点及效果:(1)本发明以5条精确设计的引物及探针严格识别靶核苷酸序列上的5个独立区域,从而避免反应混合物中存在非靶序列的影响,特异性高。(2)本发明的扩增模板最低为18.6拷贝,比常规pcr灵敏10倍。(3)本发明的cpa引物组不需要通过温度循环变化来扩增,在60℃的单一温度扩增30~60min就能将靶基因大量扩增,操作简单,反应时间短。(4)本发明所需的设备简单,不需要pcr仪,也不需要凝胶成像系统,只需一台普通水浴锅或金属浴,即使在基层实验室和医疗机构也可使用。(5)本发明的扩增产物通过一次性核酸检测试纸条检测,使结果判定直观、客观,且可有效避免气溶胶污染。(6)本发明的恒温反应所得产物用一次性核酸检测试纸条检测后直接判读结果;出现检测线和质控线两条红色条带判读为阳性结果;试剂盒操作简单、成本低廉、反应结果易于观察、特异性好,尤其适用于户外以及基层医疗单位的检验分析,易于推广应用。附图说明图1是实施例1中引物组合2的cpa产物通过琼脂糖凝胶电泳和一次性核酸检测装置检测的结果图;其中,a为琼脂糖凝胶电泳检测结果图,b为一次性核酸检测装置检测结果图;m为dnamarkerds2000;p为实施例1中提取的质粒dna;n为阴性对照。图2是实施例1中不同浓度引物及比例对cpa效果的影响结果图;其中,m为dnamarkerds2000;1、3、5、7、9、11、13、15、17、19、21泳道分别为引物浓度组合1~11;2、4、6、8、10、12、14、16、18、20、22泳道分别为引物浓度组合1~11的阴性对照。图3是实施例1中不同betaine浓度对cpa效果的影响结果图;其中,泳道m为dnamarkerds2000;1为0mol·l-1的betaine;2为0.2mol·l-1的betaine;3为0.4mol·l-1的betaine;4为0.6mol·l-1的betaine;5为0.8mol·l-1的betaine;6为1.0mol·l-1的betaine;7为1.2mol·l-1的betaine;8为1.4mol·l-1的betaine;9为阴性对照。图4是实施例1中不同mgso4浓度对cpa效果的影响结果图;其中,m为dnamarkerds2000;1为0mmol·l-1的mgso4;2为1mmol·l-1的mgso4;3为2mmol·l-1的mgso4;4为3mmol·l-1的mgso4;5为4mmol·l-1的mgso4;6为5mmol·l-1的mgso4;7为阴性对照。图5是实施例1中不同dntps浓度对cpa效果的影响结果图;其中,m为dnamarkerds2000;1为0mmol·l-1的dntps混合液;2为0.2mmol·l-1的dntps混合液;3为0.4mmol·l-1的dntps混合液;4为0.6mmol·l-1的dntps混合液;5为0.8mmol·l-1的dntps混合液;6为1mmol·l-1的dntps混合液;7为1.2mmol·l-1的dntps混合液;8为1.4mmol·l-1的dntps混合液;9为阴性对照。图6是实施例1中不同用量bstdna聚合酶对cpa效果的影响结果图;其中,m为dnamarkerds2000;1为0μl的bstdna聚合酶;2为0.2μl的bstdna聚合酶;3为0.4μl的bstdna聚合酶;4为0.6μl的bstdna聚合酶;5为0.8μl的bstdna聚合酶;6为1.0μl的bstdna聚合酶;7为1.5μl的bstdna聚合酶;8为2.0μl的bstdna聚合酶;9为阴性对照。图7是实施例1中不同温度对cpa效果的影响结果图;其中,m为dnamarkerds2000;1为54℃;3为55℃;5为56℃;7为57℃;9为58℃;11为59℃;13为60℃;15为61℃;17为62℃;19为63℃;21为64℃;23为65℃;2、4、6、8、10、12、14、16、18、20、22、24分别为1、3、5、7、9、11、13、15、17、19、21、23的阴性对照。图8是实施例1中不同反应时间对cpa效果的影响结果图;其中,m为dnamarkerds2000;1为15min的反应时间;2为30min的反应时间;3为45min的反应时间;4为60min的反应时间;5为75min的反应时间;6为90min的反应时间;7为105min的反应时间;8为120min的反应时间;9为扩增90min时的阴性对照。图9是实施例2中alv-j的cpa引物的特异性检测通过琼脂糖凝胶电泳的结果图;其中,m为dnamarkerds2000;1为alv-j的cpa引物对alv-jcdna反应后通过琼脂糖凝胶电泳的结果;2为alv-j的cpa引物对alv-acdna反应后通过琼脂糖凝胶电泳的结果;3为alv-j的cpa引物对alv-bcdna反应后通过琼脂糖凝胶电泳的结果;4为alv-j的cpa引物对alv-kcdna反应后通过琼脂糖凝胶电泳的结果;5为alv-j的cpa引物对alv-ecdna反应后通过琼脂糖凝胶电泳的结果;6为alv-j的cpa引物对e.coli菌株反应后通过琼脂糖凝胶电泳的结果;7为alv-j的cpa引物对pa菌株反应后通过琼脂糖凝胶电泳的结果;8为alv-j的cpa引物对mg反应后通过琼脂糖凝胶电泳的结果;9为alv-j的cpa引物对se反应后通过琼脂糖凝胶电泳的结果为阴性对照;10为阴性对照。图10是实施例2中alv-j的cpa引物的特异性检测用一次性核酸检测试纸条检测的结果图;其中,m为dnamarkerds2000;1为alv-j的cpa引物对alv-jcdna反应后用一次性核酸检测试纸条检测的结果;2为alv-j的cpa引物对alv-acdna反应后用一次性核酸检测试纸条检测的结果;3为alv-j的cpa引物对alv-bcdna反应后用一次性核酸检测试纸条检测的结果;4为alv-j的cpa引物对alv-kcdna反应后用一次性核酸检测试纸条检测的结果;5为alv-j的cpa引物对alv-ecdna反应后用一次性核酸检测试纸条检测的结果;6为alv-j的cpa引物对e.coli菌株反应后用一次性核酸检测试纸条检测的结果;7为alv-j的cpa引物对pa菌株反应后用一次性核酸检测试纸条检测的结果;8为alv-j的cpa引物对mg反应后用一次性核酸检测试纸条检测的结果;9为alv-j的cpa引物对se反应后用一次性核酸检测试纸条检测的结果;10为阴性对照。图11是实施例2中不同浓度alv-j质粒dna模板的cpa产物通过琼脂糖凝胶电泳的结果图;其中,1~12分别为1.86×1010~1.86×10-1拷贝/管的质粒dna的cpa产物通过琼脂糖凝胶电泳的结果;13为阴性对照;m为dnamarkerds2000。图12是实施例2中不同浓度alv-j的质粒dna模板的cpa产物通过一次性核酸检测试纸条检测的结果图;其中,1~12分别为1.86×1010~1.86×10-1拷贝/管的质粒dna的cpa产物通过一次性核酸检测试纸条检测的结果;13为阴性对照;m为dnamarkerds2000。图13是实施例2中不同浓度alv-j的质粒dna模板的常规pcr产物通过琼脂糖凝胶电泳的结果图;其中,1~12分别为1.86×1010~1.86×10-1拷贝/管的质粒dna的cpa产物通过琼脂糖凝胶电泳的结果;13为阴性对照;m为dnamarkerds2000。具体实施方式下面将结合实施方式和附图对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施方式和实施例仅用于说明本发明,而不应视为限制本发明的范围。未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。实施例中所涉及的材料、试剂和仪器:(1)j亚群禽白血病病毒(alv-j)为hn06株(zhangetal.,analv-jisolateisresponsibleforspontaneoushaemangiomasinlayerchickensinchina.avianpathol,2011,40(3):p.261-7.)、a亚群禽白血病病毒(alv-a)为gd-13株(zhaoetal.,phylogeneticanalysisandpathogenicityassessmentoftheemergingrecombinantsubgroupkofavianleukosisvirusinsouthchina.viruses,2018,10(4):p.194.)、b亚群禽白血病病毒(alv-b)为cd08株(fengetal.,thepi3k/aktpathwayisinvolvedinearlyinfectionofsomeexogenousavianleukosisviruses.j.genvirol,2011,92:p.1688-1697.)、k亚群禽白血病病毒(alv-k)为gdfx0601株(zhaoetal.,phylogeneticanalysisandpathogenicityassessmentoftheemergingrecombinantsubgroupkofavianleukosisvirusinsouthchina.viruses,2018,10(4):p.194.)、e亚群禽白血病病毒(alv-e)为hn1301株(chenetal.,developmentandapplicationofasybrgreenreal-timepcrfordetectionoftheemergingavianleukosisvirussubgroupk.poult.sci.2018,97(7):p.2568-2574.),均由农业部兽用疫苗创制重点实验室保存;鸡毒支原体(mycoplasmagallisepticum,mg)为鸡毒支原体cvcc353,购自中国兽医药品监察所;铜绿假单胞菌(pseudomonasaeruginosa,pa)为铜绿假单胞菌atcc27853、大肠杆菌(escherichiacoli,e.coli)为大肠杆菌atcc27853、沙门氏菌(salmonellaenteritidis,se)为沙门氏菌cmcc50335,均为环凯微生物科技有限公司产品bstdnapolymerase、reactionbuffer、dntp混合液及mgso4为neb公司产品;betaine为sigma产品;一次性核酸检测试纸条为杭州优思达生物技术有限公司产品;sqtissue组织dna提取试剂盒、胶回收试剂盒dnagelextractionkit为omega公司产品。(2)仪器:zhjh-c1214c超净工作台苏州净化设备有限公司dk-8d型电热恒温水槽上海一恒科技有限公司gds8000pc凝胶成像及分析系统uvp公司nd-1000分光光度计nanodrop公司t3000thermocyclerpcr仪whatmanbiometra公司微量可调移液器德国eppendorf公司powerpactm基础电泳仪bio-rad公司普通离心机德国eppendorf公司实施例1一、cpa引物设计根据ncbi数据库中已发表的alv-j序列(genebankid:hq900844.1,hm776937.1,jq935966.1,z46390.1),利用在线软件primerexpolrer(http://primerexplorer.jp/e/)、primerpremier5.0及oligo7软件在alv-j的env基因区域设计了5组cpa反应的引物及探针,其中每组引物包括两条外引物f3(正向外引物)和b3(反向外引物),一条交叉扩增引物cpr由两条短引物b2和f2组成(b2不单独参与反应),还有两条检测探针f1(5'端标记fam)和f2(5'端标记biotin)。引物探针名称及序列见表1。f3与b3同时也作为克隆引物和普通pcr引物使用。所有引物均由生工生物工程(上海)股份有限公司合成,稀释为10μmol·l-1备用。表1cpa引物和探针序列二、cpa反应1、阳性质粒dna的提取及定量采用omega公司的dna提取试盒提取alv-j的cdna,使用引物f3、b3扩增目的基因片段,扩增产物经1%琼脂糖凝胶电泳,采用凝胶回收试剂盒(omega)对pcr产物纯化回收,连接至pmd-18t载体,16℃连接过夜,连接产物转化至dh5α感受态细胞,涂布在含有氨苄抗性的lb平板上,倒置37℃培养12-16h,形成单菌落。挑取单克隆扩大培养,经菌液pcr鉴定的阳性单菌落按质粒抽提试剂盒(omega)提取质粒dna并送生工生物工程(上海)股份有限公司测序,进一步鉴定。利用分光光度计检测dna质量及纯度,计算拷贝数,-20℃保存备用。2、cpa反应体系的建立及条件优化反应体系参考xu等建立的cpa体系(xu,g.,etal.,crossprimingamplification:mechanismandoptimizationforisothermaldnaamplification.scirep,2012.2:p.246.),用无菌ddh2o作为阴性对照,以步骤1中提取的质粒dna为阳性模板,60℃恒温扩增60min。扩增产物用分别通过2%琼脂糖凝胶电泳及一次性核酸检测装置进行检测。一次性核酸检测装置结果判读如下:1)阳性(+):试纸条出现两条红色条带,一条位于质控区(c线control-line),一条位于检测区(t线test-line);2)阴性(-):试纸条的质控区(c线control-line)出现一条红色条带,检测区(t线test-line)没有条带;3)无效:试纸条的质控区(c线control-line)和检测区(t线test-line)均未出现条带。若阴、阳性结果成立,则该基础反应体系可用于后续优化:按照表2对不同浓度引物组合进行优化,其他试剂工作浓度不变,每个组合均设阴性对照引物组合,采用控制变量法,对扩增体系中的betaine浓度、mg2+浓度、dntps浓度、bstdna聚合酶浓度、扩增温度和扩增时间进行优化,确定最佳反应体系和条件。各体系中模板用无菌ddh2o代替,即为阴性对照。根据实验结果发现引物组1、3、4、5的阴、阳性反应结果不成立,其阴、阳性均能扩增出梯形条带,说明引物本身能发生非特异性扩增;或者阴阳性均不能扩增出梯形条带,表面引物无法对目的基因进行扩增,无法实现检测,被淘汰掉。而只有引物组2能满足cpa反应体系阴、阳性结果成立的基本条件(图1),因此下文中所进行的优化和一系列研究都以引物组2为基础,其扩增目的基因片段为548bp。反应体系优化实验结果表明,引物浓度组合7所得到的条带最清晰(图2),为最佳引物浓度;最优betaine浓度为0.2mol·l-1见(图3);最优mg2+浓度为4mmol·l-1(图4);最优dntps浓度为0.8mmol·l-1(图5);最优bstdna聚合酶为1μl/体系(图6);最佳反应温度为60℃(图7);最佳反应时间60min(图8)。最终确定的优化的检测体系如表3所示。表2不同引物浓度组合表3交叉引物恒温扩增的最佳反应体系及条件实施例21、cpa反应特异性分析根据dna提取试剂盒(omega)提取alv-a、alv-b、alv-k、alv-e、pa、e.coli、se、mg的cdna或dna作为模板,用于alv-jcpa检测方法的特异性试验。阴性对照为模板用无菌ddh2o代替。以最佳反应体系和条件进行特异性试验,分别以琼脂糖凝胶电泳和一次性核酸检测装置进行检测,结果显示(图9、图10),仅以实施例1得到的质粒dna、alv-j的cdna为模板时,能出现梯形条带或同时出现c线和t线;而以alv-a、alv-b、alv-k、alv-e、pa、e.coli、se、mg的核酸为模板时,无任何条带或仅出现c线,表明建立的cpa检测方法特异性良好。2、cpa反应灵敏度分析将实施例1步骤1制备的质粒dna用无菌ddh2o进行10倍倍比稀释,以不同浓度的质粒dna为模板,用alv-jcpa的最佳反应体系及条件进行扩增,同时以f3、b3为引物进行常规pcr检测,比较两者的灵敏度。以最佳反应体系和条件进行特异性试验,对于cpa扩增,分别以琼脂糖凝胶电泳和一次性核酸检测装置进行检测。阴性对照为模板用无菌ddh2o代替。结果显示,cpa方法的检测限为1.86×101拷贝·μl-1(图11、图12)。常规pcr的检测限为1.86×102拷贝·μl-1(图13),因此,本研究建立的alv-jcpa检测方法的灵敏度是常规pcr的10倍。实施例3临床血浆样品的检测对alvp27抗原elisa检测判为阳性(s/p值>0.2)的血浆样品,用alv-jcpa方法进行检测,同时进行常规pcr检测,并参考文献(daimm,etal.,developmentandapplicationofsybrgreenireal-timepcrassayfortheseparatedetectionofsubgroupjavianleukosisvirusandmultiplexdetectionofavianleukosisvirussubgroupsaandb.virologyjournal,2015,12:p.52-61.)进行荧光定量pcr检测,分析三种方法的符合率。对alvp27elisa检测判为非阳性的血浆样品(0.1≤s/p值≤0.2)的,用上述三种方法检测alv-j,分析比较三者的灵敏度。结果共收集到alvp27抗原elisa检测判为阳性(s/p值>0.2)的血浆样品共48份,0.1≤s/p值≤0.2的非阳性血浆样品共75份。用alv-jcpa方法、常规pcr及荧光定量pcr对上述样本进行比较检测。结果显示:(1)在48份s/p值>0.2的阳性血浆样品中,cpa、荧光定量pcr、pcr检测的阳性率分别为54.2%(26/48)、54.2%(26/48)、52.1%(25/48),cpa与荧光定量pcr的检测结果一致,与pcr方法的符合率为96.2%(25/26),详细数据见表4;(2)在75份0.1≤s/p值≤0.2的非阳性血浆样品中,cpa、荧光定量pcr、pcr检测的阳性率分别为60.0%(45/75)、62.6%(47/75)、38.7%(29/75),详细数据见表5。说明alv-jcpa检测方法的灵敏度高于常规pcr,与荧光定量pcr处于同一水平,在所有的123份血浆样品中,cpa与荧光定量pcr的符合率为97.3%(71/73)。表4s/p值>0.2的血浆样品检测结果表50.1≤s/p值≤0.2的血浆样品检测结果上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。序列表<110>华南农业大学<120>一种检测j亚群禽白血病病毒的cpa引物组、cpa核酸试纸条试剂盒及其应用<160>30<170>siposequencelisting1.0<210>1<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合1-f3<400>1ggaaggtgagcaagaaggac20<210>2<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合1-b3<400>2cgtcttatttgcccaggtga20<210>3<211>19<212>dna<213>人工序列(artificialsequence)<220><223>组合1-b2<400>3cccacacgtttcctggttg19<210>4<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合1-f2<400>4ctaagaagaagccgtcagca20<210>5<211>22<212>dna<213>人工序列(artificialsequence)<220><223>组合1-f1<400>5gaagacacccttgctgccatcg22<210>6<211>39<212>dna<213>人工序列(artificialsequence)<220><223>组合1-cpr<400>6cccacacgtttcctggttgctaagaagaagccgtcagca39<210>7<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合2-f3<400>7ggatgacgtgagtaagaaag20<210>8<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合2-b3<400>8cgtaccataggtaacagacg20<210>9<211>18<212>dna<213>人工序列(artificialsequence)<220><223>组合2-b2<400>9caagcaggtgcggaatgg18<210>10<211>19<212>dna<213>人工序列(artificialsequence)<220><223>组合2-f2<400>10gggaaggtgagcaagaagg19<210>11<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合2-f1<400>11cgtcagcaacaagcaagaga20<210>12<211>37<212>dna<213>人工序列(artificialsequence)<220><223>组合2-cpr<400>12gggaaggtgagcaagaaggcaagcaggtgcggaatgg37<210>13<211>18<212>dna<213>人工序列(artificialsequence)<220><223>组合3-f3<400>13agacccggagaagacacc18<210>14<211>18<212>dna<213>人工序列(artificialsequence)<220><223>组合3-b3<400>14tgcctatcaagcaggtgc18<210>15<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合3-b2<400>15tgaggtcgctgactgtagac20<210>16<211>19<212>dna<213>人工序列(artificialsequence)<220><223>组合3-f2<400>16ctgccatcgagaggtcact19<210>17<211>22<212>dna<213>人工序列(artificialsequence)<220><223>组合3-f1<400>17tatttcggtcgttccaggggtg22<210>18<211>39<212>dna<213>人工序列(artificialsequence)<220><223>组合3-cpr<400>18tgaggtcgctgactgtagacctgccatcgagaggtcact39<210>19<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合4-f3<400>19aggtgagcaagaaggactct20<210>20<211>18<212>dna<213>人工序列(artificialsequence)<220><223>组合4-b3<400>20atctgtctggcccgtctt18<210>21<211>18<212>dna<213>人工序列(artificialsequence)<220><223>组合4-b2<400>21ggtgacccacacgtttcc18<210>22<211>18<212>dna<213>人工序列(artificialsequence)<220><223>组合4-f2<400>22gccgtcagcaacaagcaa18<210>23<211>22<212>dna<213>人工序列(artificialsequence)<220><223>组合4-f1<400>23ttgctgccatcgagaggtcact22<210>24<211>36<212>dna<213>人工序列(artificialsequence)<220><223>组合4-cpr<400>24ggtgacccacacgtttccgccgtcagcaacaagcaa36<210>25<211>19<212>dna<213>人工序列(artificialsequence)<220><223>组合5-f3<400>25ggraaggtgagcaagaagg19<210>26<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合5-b3<400>26ygtcttatttgcccaggtga20<210>27<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合5-b2<400>27cgtaccataggtaacagacg20<210>28<211>20<212>dna<213>人工序列(artificialsequence)<220><223>组合5-f2<400>28actctaagaagaagccgcca20<210>29<211>19<212>dna<213>人工序列(artificialsequence)<220><223>组合5-f1<400>29gctgccrtcgagaggttac19<210>30<211>39<212>dna<213>人工序列(artificialsequence)<220><223>组合5-cpr<400>30cccacacgtttcctggttgactctaagaagaagccgcca39当前第1页12
